ОСТ НКММП 36
Методы лабораторного исследования мяса
Купить ОСТ НКММП 36 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
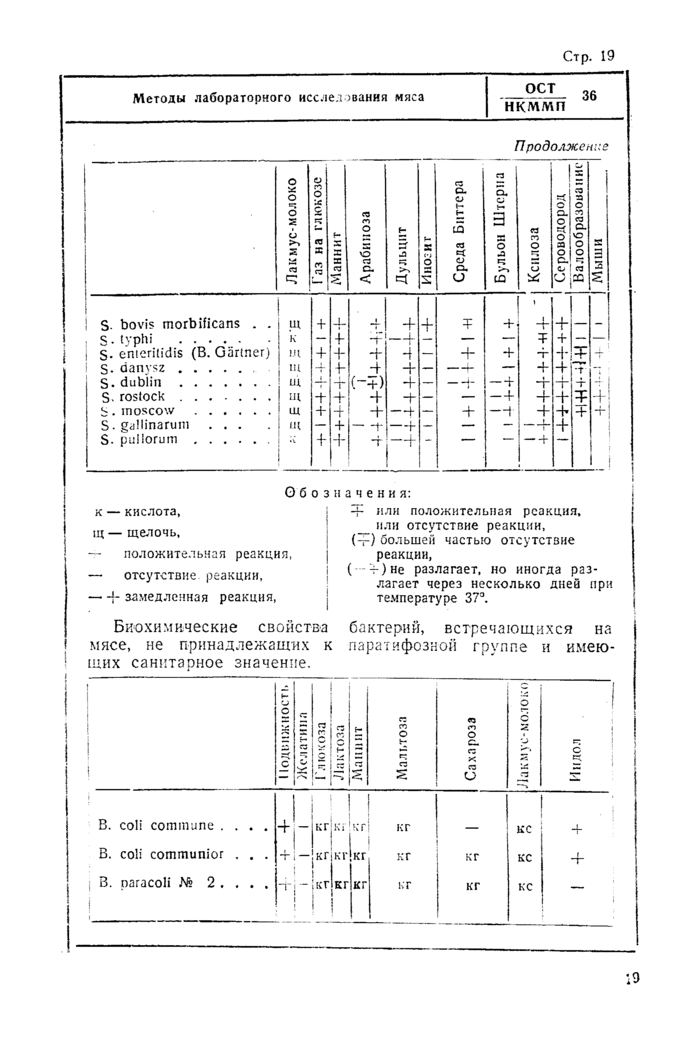
Распространяется на правила отбора образцов и методы органолептического и химико-бактериологического исследования мяса.
Оглавление
Раздел I Определение свежести мяса
А. Правила отбора образцов и подготовка их к исследованию
Б. Органолептические методы определения свежести
В. Лабораторные методы определения свежести
Г. Химические исследования
Раздел II Бактериологическое исследование мяса
А. Исследование на присутствие аэробов
Б. Исследование на присутствие анаэробов
В. Окраска препаратов
Г. Приготовление питательных сред
| Дата введения | 01.01.1940 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Организации:
| 03.12.1939 | Утвержден | Народный комиссариат мясной и молочной промышленности | |
|---|---|---|---|
| Разработан | Главмясо | ||
| Разработан | Главконсервмясо | ||
| Издан | СТАНДАРТГИЗ | 1947 г. |
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3
стр. 4
стр. 5
стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18
стр. 19
стр. 20
стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
ВСЕСОЮЗНЫЙ КОМИТЕТ СТАНДАРТОВ при СОВЕТЕ МИНИСТРОВ СССР
МЯСО И МЯСОПРОДУКТЫ
СБОРНИК СТАНДАРТОВ
Цена 14 руС. €0 коп.
ИЗДАНИЕ ОФИЦИАЛЬНОЕ
СТАНДАРТГИЗ- 1947
J логического исследования мяса.
| ||||||||||||
|
I Настоящий стандарт распространяется на правила отбора j образцов и методы органолептического и химико-бактерио- |
I
РАЗДЕЛ I ОПРЕДЕЛЕНИЕ СВЕЖЕСТИ МЯСА
Санитарное качество мяса определяется путем органолептического и химико-бактериологического исследования туши ( или ее части.
Химико-бактериологическому исследованию на свежесть | подвергаются туши или ее части в случаях получения сомнительных данных при органолептическом исследовании.
А. ПРАВИЛА ОТБОРА ОБРАЗЦОВ И ПОДГОТОВКА ИХ I К ИССЛЕДОВАНИЮ
1. Правила отбора образцов
От каждой туши или части ее, подлежащих химико-бактериологическому исследованию на свежесть, отбираются образцы весом около 200 г, каждый цельным куском.
Образцы берутся из следующих частей туши:
а) у зареза против 4-го и 5-го шейных позвонков,
б) из мышц в области лопатки,
в) из толстых частей мышц бедра.
Примечания:
1. Исследованию подлежит каждый образец в отдельности.
2. Правила отбора образцов для бактериологического исследования — см. при исследовании на соответствующие заболевания.
2. Упаковка образцов для отсылки
а) В производственную лабораторию
1. Отобранные образцы обертываются в пергаментную бумагу, каждый в отдельности. На пергаменте карандашом
| ||||||
|
1 |
|
0СТ 36 |
Методы лабораторного исследования мяса |
|
н к м м п | |
|
РАЗДЕЛ И | |
|
БАКТЕРИОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ МЯСА | |
Во всех случаях, где можно предположить наличие в мясе мясных отравителей или других «возбудителен инфекций, переходящих с животных на человека и животных, производится бактериологическое исследование мяса, а именно:
а) При подозрении на повально-заразные болезни и ос- j тро инфекционные заболевания.
б) При подозрении на септико-тшэмические процессы и j отравления.
в) При вынужденном убое.
г) При желудочно-кишечных заболеваниях. jf
д) При заболеваниях родовых путей, осложнениях, свя- [ занных с тяжелыми родами, остром воспалении вымени, г суставов, сухожилий, влагалища, копыт.
е) При гнойных и гангренозных ранах, когда имеется повышение температуры тела.
ж) При вынужденном убое без установления прижизненного диагноза.
з) При всех заболеваниях и условиях, вызывающих резкое нарушение общего состояния животного (истощение, понижение температуры ниже нормы и др.).
и) При выемке кишечника позднее 2 час. после убоя.
к) При осмотре туш в отсутствии органов . и невозможности дать заключение о пригодности мяса в пищу.
л) При осмотре животных, кажущихся здоровыми, но у которых при жизни было установлено выделение микробов группы мясных отравителей.
м) При убое животных-продуцентов:
1) Обработанных микробами (кроме туберкулезных) живыми или ослабленными, если убой животного производится по истечении трех недель после обработки (до этого срока туша непригодна в пищу).
2) Обработанных убитыми микробами, вытяжками или продуктами жизнедеятельности микробов, если убой животного производится по истечении 7 дней после обработки (до этого срока туши в пищу людям не пригодны).
н) При недостаточном обескровливании туши.
ОСТ
НКММП
о) По требоуаншо санитарной и ветсакитарной инспекции.
Примечание. Не требуется бактериологического исследования: г» при ящуре, оспе, бруцеллезе, протекающих без секуидарных явлений;
б) при переломах костей или других внешних повреждениях, когда убой произведен непосредственно после повреждения и когда еще нет* последствий повреждения.
Взятие образцов. Образцы берутся ветврачом или лаборантом лаборатории стерильным ножом из различных органов и частей туши в зависимости от заболевания.
Упаковка образцоз и отправка в свою лабораторию — см. разд. I А.
В случае пересылки материала за пределы предприятия упаковка образцов производится согласно инструкции Наркомзема от 2/1 193G г. «Наставление с порядке упаковки и пересылки патологического инфицированного материала для исследования в ветеринарно-бактериологических лабораториях».
А. ИССЛЕДОВАНИЕ НА ПРИСУТСТВИЕ АЭРОНОВ
I. Исследование на присутствие возбудителя сибирской язвы
(Bacillus Anthracis)
Взятие материала производится обязательно самим бактериологом немедленно после извещения. При этом соблюдаются все необходимые меры предосторожности, а пробы помещаются в металлический, непроницаемый и закрывающийся ящик.
При отсутствии своей лаборатории образцы берет врач убойно-разделочного цеха и пересылает в лабораторию с соблюдением всех правил, предусмотренных инструкцией Наркомзема.
а) Исследование туш крупного рогатого скота.
При исследовании туш или частей туш рогатого скота и лошадей берут отечные ткани, а также внутренние органы: часть селезенки, печени и лимфоузлы, собирающие лимфу с места локализации процесса. У привозных туш, при отсутствии внутренних органов, для исследования берут имеющиеся лимфоузлы и трубчатую кость и отечные места туши. Ст павших я невскрытых животных берут ухо, разрез которого прижигается.
ОСТ
нкммп
Методы лабораторного исследования мяса
Бактериоскопическое исследование. Из пораженных участков приготовляют 5—10 мазков на предметных стеклах. Мазки- высушиваются, фиксируются и окрашиваются по Граму и по Гимза. Присутствие грам-положи-тельных, с обрубленными концами палочек, заключенных в капсулы, дает основание подозревать наличие сибиреязвенных бацилл. В мазках из органов лошадей капсулы могут отсутствовать. При наличии в мазках характерных микробов дается предварительный ответ на производство, которое принимает все меры, предусмотренные для случаев сибирской язвы.
Бактериологическое исследование. Для бактериологического исследования производится посев из подозрительного материала на чашки с МП агаром и средой Эндо и в пробирки с МП бульоном после измельчения проб. Если материал сильно загрязнен посторонней микрофлорой, то посев производится в две пробирки с бульоном, одна из которых прогревается на водяной бане при 80° в течение 20 мин. Из подозрительного материала производится также реакция термопреципитации по Асколн. Для этого 1—2 г материала мелко нарезают и кипятят в пробирке «а огне с 10 мл карболизированного (0,5%) физиологического раствора. Затем экстракт выдерживают в кипящей водяной бане 30—40 мин. и фильтруют через бумагу или асбестовую вату до полной прозрачности.
Полученный прозрачный экстракт вносится в количестве 1 мл в уленгутовекую пробирку и под него подслаивается такое же количество преципитирующей сибиреязвенной сыворотки, профильтрованной через бумажный фильтр. В положительных случаях на границе жидкостей не позже чем через 15 мин. появляется белое кольцо.
Контролем служит: 1) заведомо сибиреязвенный анти
ген + сибиреязвенная преципитируюшая сыворотка, 2) нормальная сыворотка + исследуемый экстракт и 3) преципити-руюшая сыворотка + физиологический раствор. В первом' контроле должно получиться белое кольцо, во втором и третьем отсутствие кольца.
При отрицательном результате исследования реакцией термопреципитации проб, взятых от туш или частей туш, после убоя которых прошло менее 24 час., исследование повторяется через 24 часа с содержанием пробы при комнатной температуре.
Заражение животных. Для заражения животных часть материала растирается в ступке с стерильным пес-
12
_ОСТ ^
нкммп
кой и небольшим количеством физиологического раствора; жидкость з количестве 0,25 мл впрыскивается мышам под кожу в область спины.
На второй день исследования просматриваются посевы на чашках. Подозрительные колонии компактные, полупрозрачные, серовато-белые с шероховатой поверхностью, имеющие при слабом увеличении микроскопа вид завитков, отсеиваются на косой агар, бульон, лакмусовое молоко, на желатину (уколом) и на чашки с кровяным агаром.
Из колонии приготовляют препарат для окраски по Гра-му и исследования на подвижность. Если на чашках нет подозрительных колоний, то делается высев из флакона с бульоном на простой агар в чашках и на среду Эндо.
В случае гибели мышей, что случается большей частью через 24—48 час., павшее животное вскрывают, из крови сердца, печени, селезенки и места заражения приготовляют мазки, а из органов делают посевы, а также реакцию преципитации, причем экстракты разводят 1:10 и 1 :50. Ложно-сибиреязвенные палочки могут давать положительную -реакцию при разведении не выше чем 1 :20.
При наличии характерных колоний, характерного роста на средах, грам-положительных неподвижных бацилл, наличии капсул у микробов из органов мышеи и положительной реакции Асколи из органов мышей в разведении не ниже 1 : 50 дается положительный ответ. Если зараженная мышь еще не погибла, то заражается новая мышь из посева в бульоне.
Сибиреязвенный бацилл дает на средах следующий рост: на бульоне осадок в виде клочка ваты и прозрачный бульон; на агаре с кровью отсутствие гемолиза, молоко краснеет через 24 часа, но свертывание молока и разжижение желатины наступают в следующие дни. Рост по уколу в желатине напоминает опрокинутую елку.
б) Исследование свиных туш У подозрительных по заболеванию свиных туш, кроме перечисленных частей, обязательно берутся миндалины, шейные и подчелюстные лимфоузлы, а при обнаружении подозрительной картины в кишечнике — желчный пузырь мезентериальные лимфоузлы, имеющие геморрагические воспалительные фокусы, и трубчатая кость.
Из каждого пораженного участка приготовляется не менее 10 мазков. Мазки фиксируются и окрашиваются по Г раму и по Гимзг или Ольгу, У свиней при хронических за-
13
ОСТ
нкммп
болеваниях в мазках могут встретиться сильно измененные формы, раздутые или слабо окрашивающиеся.
При обнаружении таких форм в мазках и при соответствующей патолого-анатомической картине туша признается сибиреязвенной.
При исследовании материала от свиней заражение животных производится только выделенной чистой культурой, ввиду возможности смешанной инфекции. Посев материала производится таким же образом, как и в предыдущем случае: колонии на агаре могут быть атипичными, с ровными краями, иногда слизистой консистенции.
Реакция преципитации производится таким же образом, как и при исследовании туш рогатого скота.
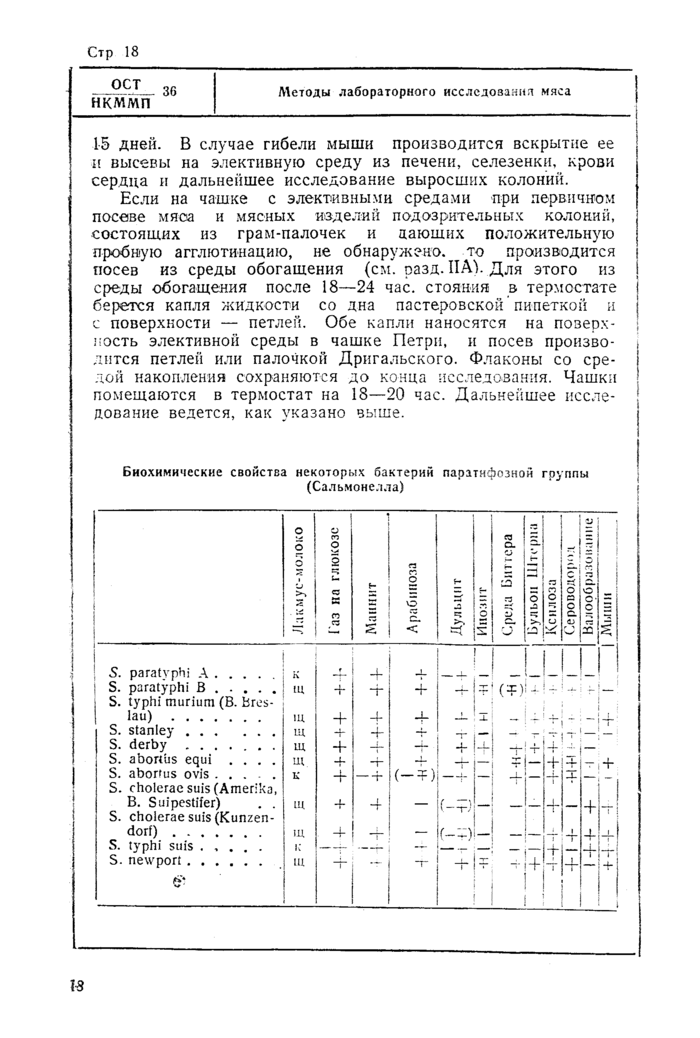
2. Исследование на присутствие бактерий паратифозной группы (Salmonellae)
Для исследования на присутствие указанных микробов берутся: 1) лимфоузлы шейные поверхностные и коленной складки, 2) паренхиматозные органы — почка, часть селезенки, часть печени (ближайшую к воротам печени с лимфоузлом), 3) желчный пузырь, освобожденный от желчи, 4) по куску сгибателя или разгибателя пута передней и задней конечностей, покрытого фасцией длиной от 6 до 10 см.
При исследовании полутуши и четвертей, при отсутствии паренхиматозных органов, берутся пробы из мышц, трубчатая кость и имеющиеся лимфоузлы.
Бактериологическое исследование начинается с бактериоскопии двух проб: мышцы и лимфатического узла печени,
а при отсутствии органов — из взятого для исследования лимфоузла туши. Исследование производится аналогично исследованию на свежесть.
Для бактериологического исследования взятые стерильно из глубины кусочки и соскоб с внутренней поверхности желчного пузыря засеиваются путем размазывания на поверхности чашек Петри с какой-либо из элективных сред (Эндо, Дригальскнй, Климмер и др.). Для каждой пробы следует брать отдельную чашку.
Для посева из костного мозга распил кости прижигается, и посев производится петлей или пипеткой.
Примечая и е. При наличии в посеве протея для подавления его роста применяют среды с добавлением карболовой кислоты (2—2.5 у.л 5%-когэ раствора карболовой кислоты на 100 мл твердой среды).
остнкммп
Кроме того взятые кусочки после тщательного измельчения ножницами засеваются на одну из сред обогащения (среду Мюллера, Кауфмана, в крайнем случае простой бульон). В колбу или флакон с 100 мл среды засевают примерно 8—10 г материала. Все паренхиматозные органы могут быть засеяны вместе. Пробы из мышц и их лимфоузлов засеваются в другой флакон Чашки и флаконы помещаются в термостат на 18—24 часа. Через 18—24 часа чашки просматриваются микроскопически и с лупой или малым увеличением микроскопа. Подозрительные колонии отмечаются. Если их много, то для исследования берется не менее 5 шт.
Подозрительными считаются колонии небольшие, круглой формы, прозрачные или полупрозрачные, бесцветные на среде Эндо, синие на среде Дригальского и зеленые на среде Климмера.
Каждая подозрительная колония платиновой иглой ‘отвивается на следующие среды: 1) косой агар, 2) среду Гисса с лактозой -р сахароза, 3) среду Гисса с маннитом и 4) бульон Готтингера (для индола). Пробирки помещают в термостате на 12—15 час.
Для засева сред пользуются следующим приемом: часть колонии снимается петлей и размешивается в конденсационной воде косого агара. Этой взвесью посредством петли и засевают пробирки со средами. Для получения конденсационной -воды разлитый по пробиркам МП агар растапливается и скашивается обычным образом, после чего пробирки ставятся вертикально. Через некоторое время на дне скапливается j конденсационная вода.
С остатком колонии производится пробная агглютинация I на стекле. Для этого сыворотки: 1) В. parat. В. (или В. typhi murium); 2) В. enteritidis (Gartner) и 3) В. cholerae suis I (b. suipestifer). каждая в разведении 1 : 10, смешиваются в » равных частях.
Реакция производится следующим образом: на предмет-гое стекло наносят капли физиологического раствора и дом каплю смеси сывороток. Остаток колонии растирается платиновой петлей сначала в капле физиологического раствора, а затем в капле сывороток до получения рав-омерной мути. В случае положительной реакции через l. i—1 мин. в капле сыворотки образуются хлопья, а сама жидкость просветляется. Это хорошо видно при наклонении стекла. В контроле (физиологический раствор) муть остается равномерной.
ОСТ
нкммп
обозначается номер туши и название ткани или органа, взятых для образца.
2. Образцы, взятые от одной туши, связываются вместе в бумажный пакет, укладываются в металлический закрывающийся ящик и отправляются в лабораторию.
3. Образцы сопровождаются документом с обозначением даты, времени и места взятия образца, вида животного, номера туши, фамилии владельца мяса, причины и цели исследования и подписи отправителя.
б) В лабораторию, находящуюся вне места осмотра
1. При отправке образцов для исследования на свежесть каждый образец обертывается отдельно в пергаментную и простую бумагу. На бумаге обозначается наименование тканей или органа, а при нескольких однородных образцах наносится соответствующая нумерация. Образцы, взятые от одной туши, связываются вместе в бумажный пакет, которой опечатывается или пломбируется.
2. Посылка сопровождается актом изъятия образцов с обозначением места и времени взятия образцов, вида животного, номера туши, фамилии владельца мяса, причины и цели исследования.
|
Б. ОРГАНОЛЕПТИЧЕСКИЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ СВЕЖЕСТИ МЯСА Признаки охлажденного мяса (говяжьего, свиного, бараньего) | ||||||||
|
ОСТ
нкммп
|
Продолжение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
ост |
Методы лабораториого исследования мяса |
|
нкммп |
|
Продолжение | ||||||||||||||||||||
|
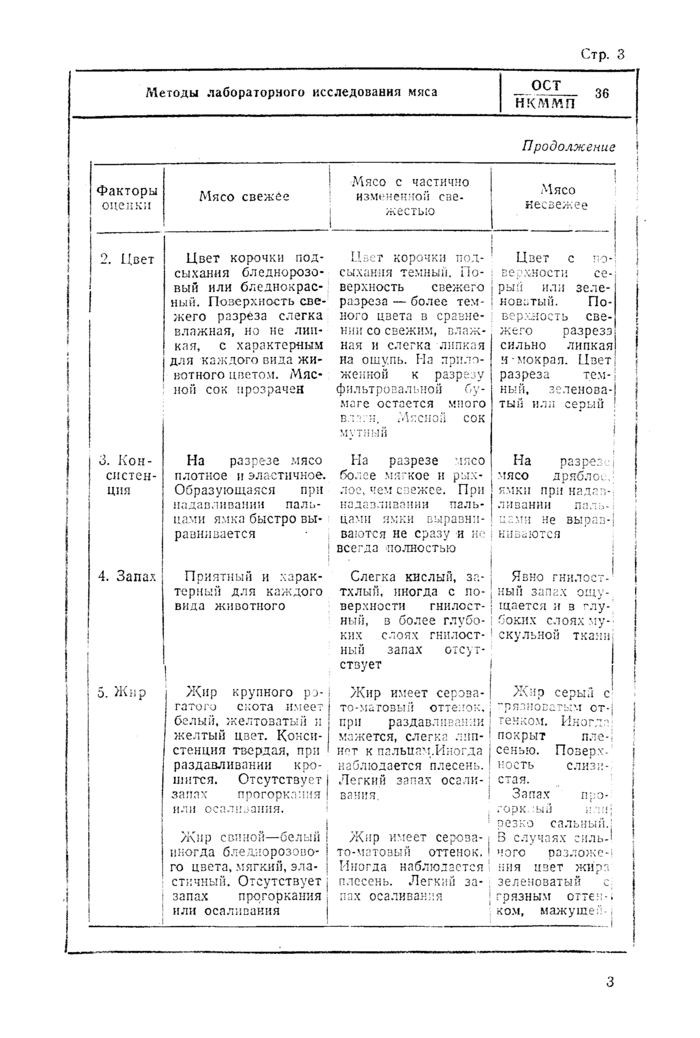
Примечания:
1. При определении запаха мяса, кроме непосредственного определения запаха на разрезе, посторонний запах определяется путем варки, для чего кусочек исследуемого мяса помешают в небольшой химический стакан, заливают водой, закрывают стакан часовым стеклом п нагревают до появления первых паров.
Посторонний запах определяется при открывании стакана.
2. Консистенция мяса, жира, костного мозга и наличие на испорченном мясе липкости определяются ощупыванием.
|
Стр. 5 | ||||
|
|
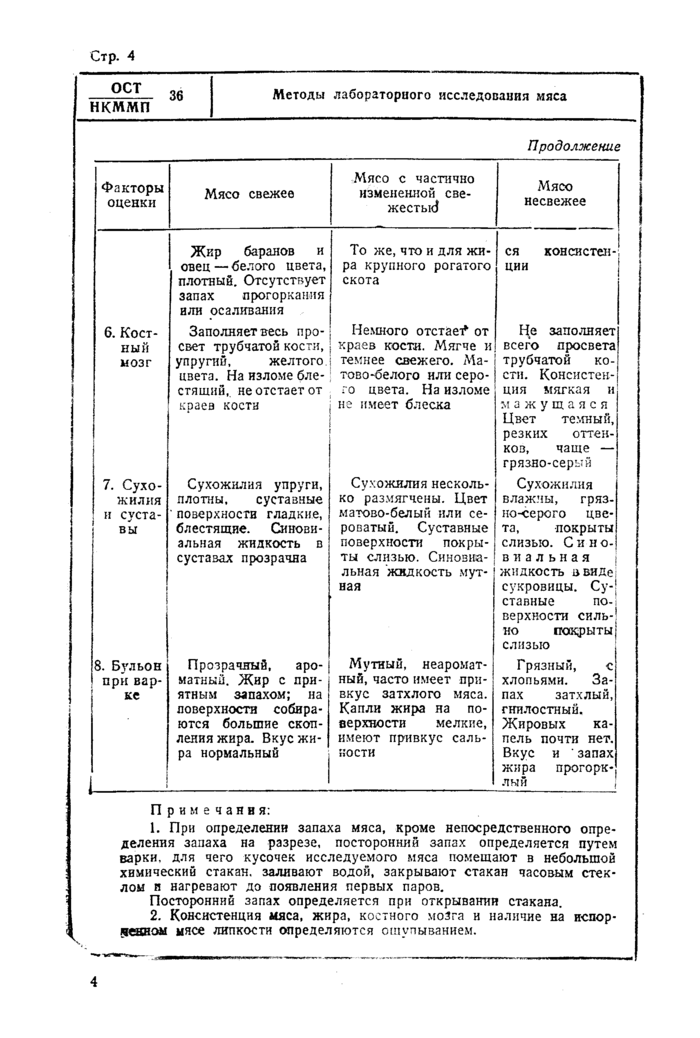
Признаки свежего мороженого и оттаянного мяса (говяжьего, свиного и бараньего) | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
|
Примечание. Признаки мороженого, дефростирозанного и повторно замороженного мяса с частичными изменениями свежести а несвежего те же, что и для охлажденного мяса. | ||||||||||||||||||||||||||||||||||||||||||||||||
о
|
Г.тр. 6 | ||||
| ||||
|
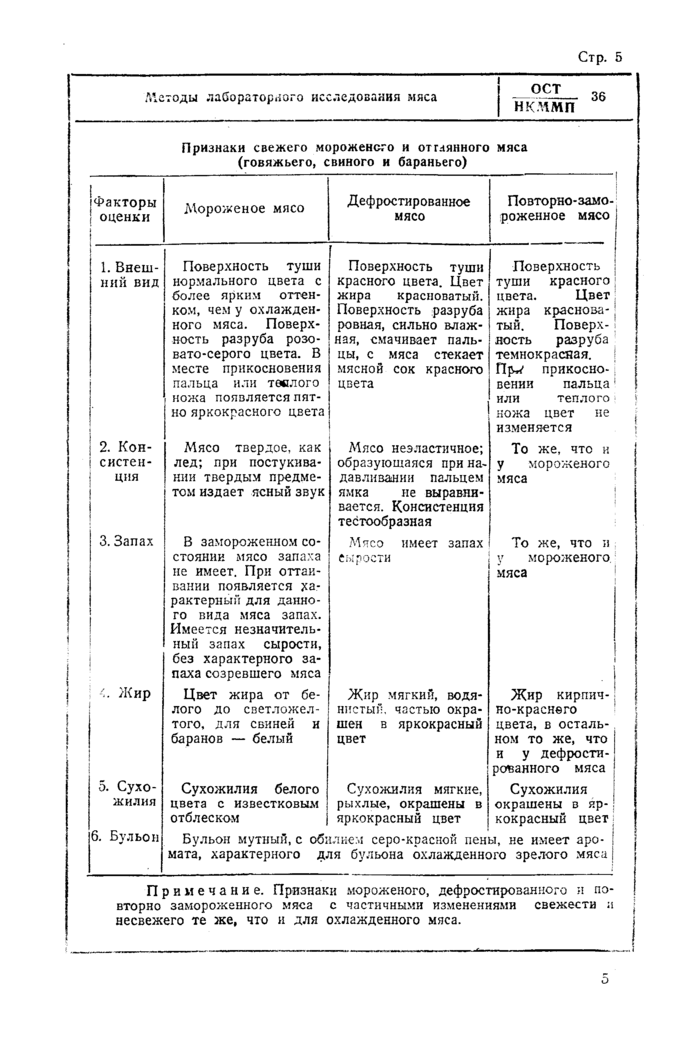
В. ЛАБОРАТОРНЫЕ МЕТОДЫ ОПРЕДЕЛЕНИЯ СВЕЖЕСТИ МЯСА |
В лаборатории образцы осматривают, записывают время поступления и отмечают все дефекты упаковки.
Для определения свежести мяса производят:
а) органолептическую оценку,
б) бактериоскопическое исследование,
в) определение pH среды .электрометрическим путем или по Михаэлису,
г) реакцию на аммиак с реактивом Несслера,
д; реакцию на сероводород и
е) реакцию с бензидином.
Эти исследования производятся следующим образом:
1. Органолептическая оценка производится согласно вышеприведенным таблицам.
2. Бактериоскопическое исследование:
а) из образца мяса стерильно вырезаются небольшие кусочки и срезанными сторонами прикладываются к предметному стеклу,
б) отпечатки высушиваются на воздухе, фиксируются на пламени и окрашиваются по Граму,
в) отпечатки необходимо сделать из слоев мяса различной глубины.
|
Признаки свежести мяса | ||||||||
|
I
в.
Г. ХИМИЧЕСКИЕ ИССЛЕДОВАНИЯ
:
Для проведения реакции: а) на аммиак с реактивом Нес* елера, б) на пероксидазу с бензидином, в) определения pH— приготовляется водная вытяжка из мяса.
Приготовление вытяжки
|
Для приготовления вытяжки пробы берутся из поверхностного и более глубокого слоя мышц. Вытяжки делаются из каждой пробы отдельно. Для этого взятые пробы осво бождаются механически от.жира и соединительной ткани. Из разных мест этих проб отбирается навеска в 10 г, которая затем грубо измельчается на 40—50 кусочков.
Кусочки мяса настаиваются в эрленмейеровской колбе в 100 мл прокипяченной дестиллированной воды в течение 15 мин. с троекратным встряхиванием в течение этого времени. Полученный водный «экстракт фильтруется через бумажный фильтр.
Определение реакции среды (pH)
Определение реакции среды можно сделать двумя методами: а) электрометрическим и б) колориметрическим по
Михаэлису.
а) Электрометрическое определение производится с помощью потенциометра с хингидроном, согласно инструкции для каждой системы потенциометра.
б) При колортпметрнчооком определении пользуются одноцветной шкалой Михаэлиса. При этом методе определение pH мяса производится с применением шестигнездового компаратора Вальподя.
© © ©
ост_
нкммп
!
I
I
© © ©
В пробирку 5 (см. рис.) наливают 2 мл исследуемо!! вытяжки из мяса-, 1 мл индикатора и 4 мл дестиллированной воды; пробирки 3 и 1 содержат раствор Михаэлиса для сравнения; в пробирки 4 и 6 наливают 2 мл исследуемой жидкости, 5 мл дестиллированной воды без индикатора и, наконец, в пробирку 2 наливают воду.
ост
НКММГ1
При определении необходимо получить одинаковые цвета в пробирках 5 и 6 или 5 и 4У что достигается подбором пробирок из шкалы Михаэли с а. Цифра на пробирке с -раствором Михаэлиса, одинаковая по цвету с испытуемым раствором, указывает концентрацию водородных ионов в экстракте мяса, причем:
pH свежего охлажденного мяса 5,8—6,4 pH свежего дефростированного мяса 6,0—6,5.
Примечание. В случае изменения pH против указанного предела вопрос о степени пригодности мяса решается в соответствии » с правилами браковки НКЗема и НКЗдрава. |
Реакция на аммиак с реактивом Несслсра
К 1 мл мясного экстракта добавляется реактив Несслера по каплям от 1 до 10 капель; пробирка взбалтывается после добавления каждой капли, причем наблюдаются изменения цвета и степени прозрачности экстракта.
Мясо свежее: при прибавлении в указанном выше
количестве реактива Несслера к вытяжке из свежего мяса не наблюдается помутнение и пожелтение экстракта. Если в редких случаях появляется после 10 капель пожелтение, то прозрачность ие уменьшается и помутнение не наступает.
Мясо подозрительной свежести: пожелтение экстракта и слабое помутнение его появляются после прибавления нескольких капель (от 6 и более). После отстаивания помутневшего экстракта в течение 20 мин. появляется !" на дне пробирки слабый осадок.
Мясо несвежее: помутнение и резкое пожелтение
экстракта наблюдается после прибавления первых капель, после 10-й наблюдается сильно желтое или красноватое помутнение с обильным осадком после отстоя.
Приготовление реактива Несслера
10 г йодистого калия растворяется в *10 мл горячей де-стиллированной воды и прибавляют к этому раствору горячий насыщенный раствор сулемы (HgCb) до появления красного осадка.
Затем фильтруют и в фильтрат добавляют 30 г едкого | калия, растворенного в 80 мл воды, и 1—5 мл такого же, j как и раньше, раствора сулемы. После охлаждения рас- ! твора объем его доводят до 200 мл разбавлением дестил- j лнрованной водой.
ОСТ
нкммп
Полученный раствор хранят в темной банке с притертой пробкой и в холодном месте. Для реакции берется только прозрачный слой.
Реакция на сероводород
В баночку с притертой пробкой емкостью около 80—100 мл помещают кусочки исследуемого мяса до Уз его объема и туда же опускают полоску фильтровальной бумаги, с.моченной щелочным раствбром уксуснокислого свинца, зажимая бумажку между поверхностью горла и пробкой банки. Исследование прекращают через 15 мим. при комнатной температуре. При наличии сероводорода бумажка окрашивается в светлобурый или черный цвет.
Мясо подозрительной свежести дает слабололожитель-ную реакцию. Мясо несвежее—ярко выраженную реакцию.
Реакция с бензидином
В пробирку наливают 2 мл испытуемой вытяжки, прибавляют 5 капель 0,2%-ного спиртового раствора бензиди-на, встряхивают содержимое пробирки, после чего добавляют 2 капли 1 % -ного раствора перекиси водорода (одна часть продажной 3%-ной перекиси водорода и две части воды). Положительной реакцией считается появление в течение Уг—2 мин. сине-зеленого цвета, постепенно переходящего в темнскоричневый.
Примечания:
1. Отрицательная реакция с бензидином при отсутствии других признаков разложения мяса указывает на необходимость сделать бактериологическое исследование (на сальмонеллы и сибирскую язву).
2. 0,2%-нын спиртовый раствор бензидина хранить не более недели в темной банке.
3. Оценка мяса. Вопрос об оценке мяса решается на основании всего комплекса реакций с учетом органолептических данных.