Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1.
МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
пестицидов в пищевых продуктах,
сельскохозяйственном сырье и объектах
окружающей среды
Сборник
МУК 4.1.2859 - 4.1.2866-11
Москва
2011
1. Разработаны Российским государственным аграрным
университетом - МСХА им. К.А. Тимирязева, Учебно-научный консультационный центр
«Агроэкология пестицидов и агрохимикатов» Минсельхоза России (В.А. Калинин,
профессор, канд. с-х. наук., Е.В. Довгилевич, ст.н.сотр., канд. биол. наук,
А.В. Довгилевич, ст.н.сотр., канд. хим. наук, Н.В. Устименко, ст.н.сотр., канд.
биол. наук, Е.Н. Щербинкина, инженер).
2. Рекомендованы к утверждению Комиссией по
санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в
сфере защиты прав потребителей и благополучия человека (протокол от 28 12.2010
№ 3).
3. Утверждены руководителем Федеральной службы по надзору в
сфере защиты прав потребителей и благополучия человека, Главным государственным
санитарным врачом Российской Федерации Г.Г. Онищенко 31 марта 2011 г.
4. Введены в действие с момента утверждения.
5. Введены впервые.
СОДЕРЖАНИЕ
|
Общие положения и область применения. 2
1. Краткая характеристика препарата. 2
2. Методика определения Тиабендазола в семенах и масле
рапса методом ВЭЖХ.. 2
3. Проверка приемлемости результатов параллельных
определений. 7
4. Оформление результатов. 7
5. Контроль качества результатов измерений. 8
6. Требования безопасности. 9
7. Требования к квалификации оператора. 9
8. Разработчики. 9
|
|
|
УТВЕРЖДАЮ
Руководитель
Федеральной службы
по надзору в сфере защиты прав
потребителей и благополучия человека,
Главный государственный санитарный
врач Российской Федерации
Г.Г. Онищенко
31
марта 2011 г.
Дата введения: с момента утверждения
|
4.1.
МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Методика
измерений остаточных количеств
Тиабендазола в семенах и масле рапса методом
высокоэффективной жидкостной хроматографии
Методические указания
Общие положения и область применения
Свидетельство об аттестации методики от 23.11.2010 №
01.5.04.693.
Настоящие методические указания устанавливают метод
измерения массовой концентрации Тиабендазола в семенах и масле рапса в
диапазоне концентраций 0,01 - 0,1 мг/кг.
1. Краткая характеристика препарата
Действующее вещество: Тиабендазол.
Структурная формула:
Название действующего вещества по ИЮПАК: 2-(1,3-тиазол-4-ил)
бензимидазол.
2-(4-тиазолил)-1Н-бензимидазол (С.А.).
Эмпирическая формула: C10H7N3S.
Молекулярная масса: 201,3.
Белое кристаллическое вещество. Температура плавления: 297 -
298 °С. Давление паров при 25 °С: 4,6×10-4 мПа. Коэффициент
распределения н-октанол-вода: Kow logР = 2,39 (рН 7).
Растворимость (г/л) при 20 °С: н-гептан - < 0,01, ксилол
- 0,13, ацетон - 2,43, 1,2-дихлорэтан - 0,81, метанол - 8,28, этилацетат -
1,49, н-октанол - 3,91, вода - 10,0 (рН 2), 0,16 (рН 4), 0,03 (рН 7 - 10). Устойчив
к гидролизу. Водный фотолиз (20 °С, рН 5, DT50 29 ч); pКa1
= 4,73; рКа2 = 12,00.
Краткая токсикологическая характеристика: Острая
пероральная токсичность (LD50) для мышей - 3600 мг/кг, крыс - 3100
мг/кг, кроликов - 3800 мг/кг, птиц - более 2250 мг/кг; острая дермальная
токсичность (LD50) для кроликов - более 2000 мг/кг, не ирритант;
ингаляционная токсичность (LС50) для крыс - более 0,5 мг/кг. Не
токсичен для пчел. СК50 для рыб 0,55 мг/л при экспозиции 96 ч. Класс
токсичности по ВОЗ-III.
Область применения: Тиабендазол - системный фунгицид
защитного и лечебного действия. Тиабендазол образует защитный слой на
обработанной поверхности, используется на овощных, плодовых и зерновых
культурах. Не совместим с купратами и окисляющими агентами, такими как хлораты
и нитраты.
Гигиенические нормативы для Тиабендазола в семенах и масле
рапса в России не установлены.
2. Методика определения Тиабендазола в семенах и масле
рапса методом ВЭЖХ
2.1.
Основные положения
2.1.1.
Принцип метода
Методика основана на определении Тиабендазола методом ВЭЖХ с
использованием УФ-детектора после его извлечения из образцов органическим
растворителем с последующей очисткой на колонке с силикагелем.
2.1.2.
Метрологическая характеристика метода
При соблюдении всех регламентированных условий проведения
анализа в точном соответствии с данной методикой погрешность (и ее
составляющие) результатов измерений при доверительной вероятности Р =
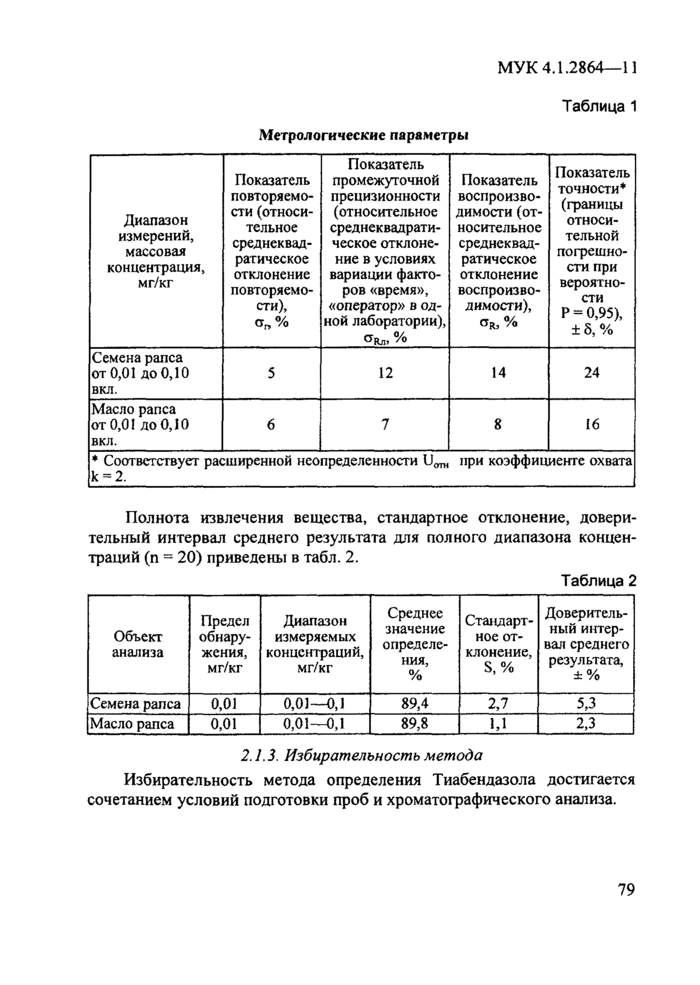
0,95 не превышает значений, приведенных в табл. 1 для соответствующих диапазонов концентраций.
Таблица 1
Метрологические параметры
|
Диапазон
измерений, массовая концентрация, мг/кг
|
Показатель
повторяемости (относительное среднеквадратическое отклонение повторяемости), σr %
|
Показатель
промежуточной прецизионности (относительное среднеквадратическое отклонение в
условиях вариации факторов «время», «оператор» в одной лаборатории), σRл, %
|
Показатель
воспроизводимости (относительное среднеквадратическое отклонение
воспроизводимости), σR, %
|
Показатель
точности* (границы относительной погрешности при вероятности Р =
0,95), ±δ, %
|
|
Семена рапса от 0,01 до
0,10 вкл.
|
5
|
12
|
14
|
24
|
|
Масло рапса от 0,01 до
0,10 вкл.
|
6
|
7
|
8
|
16
|
|
* Соответствует расширенной неопределенности Uотн при коэффициенте
охвата k = 2.
|
Полнота извлечения вещества,
стандартное отклонение, доверительный интервал среднего результата для полного
диапазона концентраций (n = 20) приведены в
табл. 2.
Таблица 2
|
Объект
анализа
|
Предел
обнаружения, мг/кг
|
Диапазон
измеряемых концентраций, мг/кг
|
Среднее
значение определения, %
|
Стандартное
отклонение, S, %
|
Доверительный
интервал среднего
результата,
±%
|
|
Семена рапса
|
0,01
|
0,01
- 0,1
|
89,4
|
2,7
|
5,3
|
|
Масло рапса
|
0,01
|
0,01
- 0,1
|
89,8
|
1,1
|
2,3
|
2.1.3.
Избирательность метода
Избирательность метода определения Тиабендазола достигается сочетанием
условий подготовки проб и хроматографического анализа.
2.2.
Реактивы и материалы
|
Ацетон, осч
|
ТУ 6-09-3513-86
|
|
Ацетонитрил для ВЭЖХ, сорт 1 или
хч
|
ТУ 6-09-3534-87
|
|
Бумажные фильтры «красная лента»
|
ТУ
2642-001-42624157-98
|
|
Вода бидистиллированная,
деионизированная
|
ГОСТ 6709-79
|
|
н-Гексан, хч, свежеперегнанный
|
ТУ
2631-003-05807999-98
|
|
Изопропиловый спирт
|
ТУ 2632-015-11291058-95
|
|
Калий углекислый, хч
|
ГОСТ 4221-76
|
|
Калия перманганат
|
ГОСТ
20490-75
|
|
Кальция хлорид, хч
|
ГОСТ 4161-77
|
|
Кислота ортофосфорная, хч, 0,005 М
водный раствор
|
ГОСТ
6552-80
|
|
Кислота серная, хч
|
ГОСТ
4204-77
|
|
Натрий двууглекислый
|
ГОСТ
83-79
|
|
Натрий сернокислый безводный, ч,
свежепрокаленный
|
ГОСТ
4166-76
|
|
Натрий хлористый, чда
|
ГОСТ
4233-77
|
|
Натрия гидроксид, хч
|
ГОСТ 4328-77
|
|
Подвижная фаза для ВЭЖХ:
ацетонитрил: 0,005 М раствор Н3РО4 (40:60, по объему)
|
|
|
Силикагель для колоночной
хроматографии 60 (0,040 - 0,063 mm) («Merck», Германия)
|
|
|
Стекловата
|
|
|
Тиабендазол, аналитический
стандарт с содержанием д.в. 99,8 % (Cheminova)
|
|
|
Элюент № 1 для колоночной хроматографии:
смесь гексан - ацетон (80:20, по объему)
|
|
|
Элюент № 2 для колоночной
хроматографии: смесь гексан - ацетон (15:85, по объему)
|
|
Допускается использование реактивов квалификацией не ниже
указанных.
2.3.
Приборы и посуда
|
Жидкостный хроматограф «Альянс»
фирмы «Waters» с УФ-детектором (Waters 2487) с дегазатором и автоматическим
пробоотборником или аналогичный
|
|
|
Колонка Spherisorb Phenyl (150×4,6)
мм, 3 мкм (Waters, USA) или аналогичная
|
|
|
Ванна ультразвуковая УЭВ-1,3, или
аналогичная
|
ГОСТ
Р МЭК 60335-2-15-98
|
|
Весы аналитические BЛA-200 или
аналогичные
|
ГОСТ
24104-2001
|
|
Мельница лабораторная зерновая ЛMЗ
|
ТУ 1-01-0593-79
|
|
Гомогенизатор
|
МРТУ 42-1505-63
|
|
Ротационный испаритель вакуумный
Buchi R-205 или аналогичный
|
|
|
Бидистиллятор рН-метр
универсальный ЭВ-74
|
ГОСТ
22261-76
|
|
Насос водоструйный
|
МРТУ 42 861-64
|
|
Колбы плоскодонные на шлифах КШ500
29/32 ТС
|
ГОСТ 10384-72
|
|
Колбы круглодонные на шлифах КШ10
и КШ250 29-32 ТС
|
ГОСТ 10384-72
|
|
Воронки лабораторные В-75-110
|
ГОСТ
25336-82
|
|
Воронки делительные ВД-3-250 и 500
|
ГОСТ 8613-75
|
|
Цилиндры мерные на 50, 100, 500 и
1000 см3
|
ГОСТ 1774-74
|
|
Колбы мерные на 25, 50, 100 и 1000
см3
|
ГОСТ
1770-74
|
|
Пипетки на 1, 2, 5, 10 см3
|
ГОСТ
22292-74
|
|
Колонки стеклянные (25×1) см
|
|
Допускается использование приборов и посуды с метрологическими
характеристиками не ниже указанных.
2.4.
Отбор проб
Отбор проб семян рапса производится в соответствии с ГОСТ
10852-86 «Семена масличные. Правила приемки и методы отбора проб». Семена
хранят при комнатной температуре в полотняных мешочках, перед анализом доводят
до стандартной влажности и измельчают. Растительное масло хранят в холодильнике
при температуре 0 - 4 °С в герметично закрытой стеклянной таре в течение 2
месяцев.
2.5.
Подготовка к определению
2.5.1.
Подготовка и очистка реактивов и растворителей
Перед началом работы проверяют чистоту применяемых
органических растворителей. Для этого 100 см3 растворителя упаривают
в ротационном вакуумном испарителе при температуре 40 °С до объема 1,0 см3
и хроматографируют. При обнаружении мешающих определению примесей очистку
растворителей производят в соответствии с общепринятыми методиками.
2.5.2.
Кондиционирование колонки
Перед началом анализа колонку (Spherisorb Phenyl)
кондиционируют в потоке подвижной фазы (1 см3/мин) до стабилизации
нулевой линии в течение 1 - 2 ч.
2.5.3. Приготовление растворов
Для приготовления 0,005 М раствора ортофосфорной кислоты 0,5
г 98 % ортофосфорной кислоты помещают в мерную колбу объемом 1 дм3,
растворяют в бидистиллированной воде и доводят объем до метки.
Для приготовления подвижной фазы смешивают ацетонитрил с
0,005 М раствором ортофосфорной кислоты в соотношении 50:50 по объему,
используя мерные цилиндры.
Для приготовления элюента № 1 в колбе на 1000 мл смешивают
800 мл н-гексана и 200 мл ацетона. Для приготовления элюента № 2 в колбе на
1000 мл смешивают 150 мл н-гексана и 850 мл ацетона.
Приготовление стандартного и градуировочных растворов:
Берут точную навеску Тиабендазола (50 мг), переносят в
мерную колбу на 50 мл, растворяют навеску в ацетонитриле и доводят до метки
(стандартный раствор с концентрацией 1,0 мг/см3).
Градуировочные растворы с концентрациями 0,1, 0,2, 0,5, 1,0
и 2,0 мгк/cм3 готовят методом последовательного разбавления по
объему, используя раствор подвижной фазы [смесь ацетонитрил - 0,005 М Н3РО4
(40:60, по объему)]. Стандартный и градуировочные растворы можно хранить в
холодильнике при температуре 0 - 4 °С в течение 1 месяца.
Для внесения в контрольный образец при определении полноты
извлечения используют стандартный раствор, разбавленный ацетонитрилом до
нужного уровня концентраций методом последовательного разбавления. Растворы для
внесения в масло готовят из стандартного раствора с концентрацией 0,5 мг/см3
методом последовательного разбавления по объему изопропиловым спиртом.
2.5.4.
Построение градуировочного графика
Для построения градуировочного графика (площадь пика -
концентрация Тиабендазола в растворе) в хроматограф вводят по 20 мм3
градуировочных растворов (не менее 3 параллельных измерений для каждой
концентрации, не менее 4 точек по диапазону измеряемых концентраций), измеряют
площади пиков и строят график зависимости среднего значения площади пика от
концентрации Тиабендазола в градуировочном растворе (мкг/см3).
Градуировочную характеристику
необходимо проверять при замене реактивов, хроматографической колонки или
элементов хроматографической системы, а также при отрицательном результате
контроля градуировочного коэффициента:
λконтр. - норматив
контроля градуировочного коэффициента, %. (λконтр. = 10 % при Р
= 0,95).
2.5.5. Подготовка колонки с силикагелем для очистки экстракта
В нижнюю часть стеклянной колонки длиной 25 см и внутренним диаметром
1 см помещают тампон из стекловаты, закрывают кран и вносят суспензию 5 г
силикагеля в 30 см3 смеси гексан-ацетон (80:20, по объему). Дают
растворителю стечь до верхнего края сорбента. Колонку последовательно промывают
30 см3 элюента № 2 и 30 см3 элюента № 1 со скоростью 1 -
2 капли в секунду, после чего она готова к работе.
2.5.6.
Проверка хроматографического поведения Тиабендазола на колонке с силикагелем
В круглодонную колбу емкостью 10 см3 отбирают 0,1
см3 стандартного раствора Тиабендазола с концентрацией 10 мкг/см3.
Отдувают растворитель током теплого воздуха (температура не выше 40 °С),
остаток растворяют в 5 см3 элюента № 1 и наносят на колонку. Колбу
обмывают еще 5 см3 элюента № 1 и также вносят на колонку. Промывают
колонку 50 см3 элюента № 1, которые отбрасывают, затем 100 см3
элюента № 2 со скоростью 1 - 2 капли в секунду. Отбирают фракции по 10 см3
каждая, упаривают, остаток растворяют в 2 см3 подвижной фазы для
ВЭЖХ (п. 2.5.3) и анализируют на
содержание Тиабендазола (п. 2.6.3).
Фракции, содержащие Тиабендазол, объединяют, упаривают
досуха, остаток растворяют в 2 см3 подвижной фазы для ВЭЖХ и вновь
анализируют (п. 2.6.3). Рассчитывают
содержание Тиабендазола в элюате, определяя полноту вымывания вещества из
колонки и необходимый для этого объем элюента.
Примечание: параметры удерживания Тиабендазола и сопутствующих
экстрактивных веществ могут меняться при использовании новой партии сорбента и
растворителей.
2.5.7.
Подготовка приборов и средств измерения
Установка и подготовка всех приборов и средств измерения
проводится в соответствии с требованиями технической документации.
2.6.
Проведение определения
2.6.1. Извлечение Тиабендазола из проб семян и масла рапса
Навеску измельченных семян массой 20 г помещают в коническую
колбу емкостью 100 мл и экстрагируют Тиабендазол 40 см3 ацетонитрила
на ультразвуковой установке в течение 15 мин. Суспензию фильтруют через бумажный
фильтр «красная лента». Экстракцию повторяют дважды порциями по 30 см3.
Навеску масла массой 20 г помещают в делительную воронку
емкостью 250 см3 и экстрагируют Тиабендазол трижды ацетонитрилом
порциями по 30 см3, встряхивая смесь каждый раз в течение 2 - 3 мин
и собирая нижний органический слой.
Объединенные экстракты семян или масла промывают гексаном в
делительных воронках дважды по 25 см3, встряхивая смесь каждый раз в
течение 1 - 2 мин и собирая нижний органический слой.
После этого экстракты выпаривают досуха на ротационном
испарителе при температуре не выше 40 °С. Дальнейшую очистку экстрактов
проводят на колонке с силикагелем по п. 2.6.2.
Внимание! Отделение ацетонитрильного слоя следует
производить только после полного расслоения жидкостей в делительной воронке.
2.6.2. Очистка на колонке с силикагелем
Сухой остаток в колбе, полученный при упаривании очищенных
по п. 2.6.1 экстрактов растительных
материалов, количественно переносят двумя порциями смеси гексан-ацетон (80:20,
по объему) по 5 см3 каждая в кондиционированную хроматографическую
колонку (п. 2.5.5). Промывают колонку
50 см3 элюента № 1, который отбрасывают. Тиабендазол элюируют 80 см3
элюента № 2, собирая элюат в грушевидную колбу емкостью 250 см3.
Раствор упаривают досуха на вакуумном ротационном испарителе при температуре не
выше 40 °С. Сухой остаток растворяют в 2 см3 подвижной фазы для ВЭЖХ
и 20 мм3 раствора вводят в жидкостный хроматограф.
2.6.3. Условия хроматографирования
Жидкостный хроматограф «Альянс» фирмы «Waters» с
УФ-детектором (Waters 2 487), снабженный дегазатором, автоматическим
пробоотборником и термостатом колонки.
Колонка Spherisorb Phenyl (150×4,6) мм, 3 мкм (Waters, USA).
Температура колонки 30 ± 1 °С.
Подвижная фаза для ВЭЖХ: ацетонитрил: 0,005 М раствор Н3РО4
(40:60, по объему).
Скорость потока элюента: 1 мл/мин.
Рабочая длина волны 300 нм.
Объем вводимой пробы 20 мм3.
Линейный диапазон детектирования 0,1 - 2,00 мкг/мл.
2.6.4.
Обработка результатов анализа
Количественное определение проводят методом абсолютной
калибровки, содержание Тиабендазола в образцах семян или масла (X,
мг/кг) вычисляют по формуле:
S1 - площадь пика Тиабендазола в
стандартном растворе, мм2 (мв∙сек);
S2 - площадь пика Тиабендазола в
анализируемой пробе, мм2 (мв∙сек);
V - объем пробы, подготовленной для
хроматографического анализа, см3;
Р - навеска анализируемого образца, г;
С - концентрация стандартного раствора Тиабендазола,
мкг/см3;
Содержание остаточных количеств Тиабендазола в анализируемом
образце вычисляют как среднее из 2 параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор
Тиабендазола 2 мкг/см3, разбавляют подвижной фазой для ВЭЖХ.
3. Проверка приемлемости результатов параллельных
определений
За результат анализа принимают
среднее арифметическое результатов двух параллельных определений, расхождение
между которыми не превышает придела повторяемости (1):
X1, Х2
- результаты параллельных определений, мг/кг;
r - значение предела
повторяемости (r = 2,8σr).
При невыполнении условия (1)
выясняют причины превышения предела повторяемости, устраняют их и вновь
выполняют анализ.
4. Оформление результатов
Результат анализа представляют в виде:
(X ± Δ)
мг/кг при вероятности Р = 0,95, где
X - среднее арифметическое результатов определений,
признанных приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг;
Δ =
δ∙X/100, где
δ - граница относительной погрешности методики
(показатель точности в соответствии с диапазоном концентраций), %.
В случае если содержание компонента менее нижней границы
диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе менее нижней границы
определения» (например: менее 0,01 мг/кг*, где * - 0,01 мг/кг - предел
обнаружения Тиабендазола в рапсе).
5. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости
измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность
(правильность и прецизионность) методов и результатов измерений».
5.1. Стабильность результатов измерений контролируют перед
проведением измерений, анализируя один из градуировочных растворов.
5.2. Плановый внутрилабораторный оперативный контроль
процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Cд должна удовлетворять
условию:
Cд
= Δл,Х + Δл,Х', где
±Δл,Х (±Δл,Х') -
характеристика погрешности (абсолютная погрешность) результатов анализа,
соответствующая содержанию компонента в испытуемом образце (расчетному значению
содержания компонента в образце с добавкой, соответственно), мг/кг; при этом:
Δл
= ±0,84Δ, где
Δ - граница абсолютной погрешности, мг/кг: где
Δ =
δ∙X/100, где
δ - граница относительной погрешности методики
(показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк
рассчитывают по формуле:
Кк
= X' - X - Cд, где
X', X, Cд - среднее
арифметическое результатов параллельных определений (признанных приемлемыми по
п. 4) содержания компонента в образце с
добавкой, испытуемом образце, концентрация добавки соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
Проводят сопоставление результата контроля процедуры (Кк)
с нормативом контроля (К).
Если результат контроля
процедуры удовлетворяет условию:
процедуру анализа признают
удовлетворительной.
При невыполнении условия (2)
процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным
результатам, и принимают меры к их устранению.
5.3. Проверка приемлемости результатов измерений, полученных
в условиях воспроизводимости:
Расхождение между результатами измерений,
выполненных в двух разных лабораториях, не должно превышать предела
воспроизводимости (R):
Х1, Х2
- результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с
диапазоном концентраций), %.
6. Требования безопасности
6.1. При работе необходимо соблюдать требования техники
безопасности, установленные для работ с токсичными, едкими,
легковоспламеняющимися веществами (ГОСТ
12.1.005, ГОСТ
12.1.007). Организация обучения работников безопасности труда по ГОСТ
12.0.004.
При выполнении измерений с использованием жидкостного
хроматографа и работе с электроустановками соблюдать правила
электробезопасности в соответствии с ГОСТ
12.1.019-79 и инструкциями по эксплуатации приборов.
6.2. Помещение лаборатории должно быть оборудовано
приточно-вытяжной вентиляцией, соответствовать требованиям пожарной
безопасности по ГОСТ
12.1.004-91 и иметь средства пожаротушения по ГОСТ
12.4.009. Содержание вредных веществ в воздухе не должно превышать норм,
установленных ГН 1.2.2701-10 и ГН
2.2.5.1313-03 «Предельно допустимые концентрации (ПДК) вредных веществ в
воздухе рабочей зоны».
7. Требования к квалификации оператора
Измерения в соответствии с настоящей методикой может
выполнять специалист-химик, имеющий опыт работы методом высокоэффективной
жидкостной хроматографии, ознакомленный с руководством по эксплуатации
жидкостного хроматографа, освоивший данную методику и подтвердивший
экспериментально соответствие получаемых результатов нормативам контроля погрешности
измерений по п. 5.
8. Разработчики
Цибульская И.А., Черменская Т.Д., Ковров Н.Г. (ГНУ
Всероссийский научно-исследовательский институт защиты растений
Россельхозакадемии, г. Санкт-Петербург).
Методика прошла метрологическую экспертизу (Свидетельство об
аттестации № 01.5.04.686) и внесена в Федеральный реестр (ФР. 1.31.2011.09107).