МУК 4.1.2549-09
Определение остаточных количеств тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографии
Купить МУК 4.1.2549-09 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методические указания устанавливают метод газожидкостной хроматографии для определения в зерне сои, соевом и кукурузном масле массовой концентрации тебуконазола в диапазоне концентраций 0,05 - 1,0 мг/кг.
Оглавление
1. Вводная часть
2. Методика определения тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографии
2.1. Основные положения
2.2. Реактивы и материалы
2.3. Приборы и посуда
2.4. Отбор и хранение проб
2.5. Подготовка к определению
2.6. Проведение определения
3. Проверка приемлемости результатов параллельных определений
4. Оформление результатов
5. Контроль качества результатов измерений
6. Требования техники безопасности
7. Требования к квалификации оператора
8. Разработчики
| Дата введения | 01.12.2009 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
- Раздел Автомобильные дороги
Организации:
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 10852-86 Семена масличные. Правила приемки и методы отбора проб
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 22300-76 Реактивы. Эфиры этиловый и бутиловый уксусной кислоты. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ 4221-76 Реактивы. Калий углекислый. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4
стр. 5

стр. 6
стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
Государственное санитарно-эпидемиологическое нормирование _Российской Федерации_
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографии
Методические указания МУК 4.1.2549—09
Издание официальное
Москва * 2009
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
4.2. МЕТОДЫ КОНТРОЛЯ, БИОЛОГИЧЕСКИЕ И МИКРОБИОЛОГИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографии
Методические указания МУК 4.1.2549—09
МУК 4.1.2549—09
жды порциями по 30 см3. Для ускорения расслоения можно добавить небольшое количество (5 см3) насыщенного раствора хлорида натрия. Объединенные дихлорметановые экстракты фильтруют через слой безводного сернокислого натрия. Полученный раствор выпаривают на ротационном испарителе при температуре бани 50 °С до полного удаления дихлорметана. Далее проводят очистку экстрактов по п. 2.6.3.
2.6.2. Экстракция тебуконазола из соевого и кукурузного масла. Навеску масла 10 г растворяют в 50 см3 гексана и экстрагируют тебуко-назол 50 см3 ацетонитрила в УЗ-ванне в течение 15 мин. Полученную смесь помещают в делительную воронку объемом 250 см3. После расслоения* нижний ацетонитрильный слой сливают, из верхнего гексанового слоя экстрагируют тебуконазол ацетонитрилом еще дважды порциями по 25 см3. К объединенному ацетонитрильному экстракту добавляют воду в соотношении ацетонитрил : вода - 1 :4 и переэкстрагируют тебуконазол дихлорметаном трижды порциями по 30 см3. Объединенные дихлорметановые экстракты сушат над безводным сернокислым натрием и выпаривают досуха на ротационном испарителе при температуре 50 °С. Сухой остаток растворяют в 5 см3 ацетона и помещают в морозильную камеру с температурой - 18 °С на 2 ч. Охлажденный ацетоновый раствор декантируют в круглодонную колбу на 10 см3 через фильтр «красная лента», после чего фильтр промывают 2 см3 охлажденного ацетона. Полученный раствор упаривают на ротационном испарителе при температуре бани не выше 40ооС до полного удаления ацетона. Далее очистку проводят по п. 2.6.3.
*В случае образования сравнительно стойких эмульсий можно добавить несколько мл насыщенного раствора хлорида натрия.
2.6.3. Очистка экстрактов на колонке с флористом. Остаток в колбе, полученный при упаривании очищенных по п.п. 2.6.1 и 2.6.2 экстрактов зерна сои или масла, количественно переносят двумя порциями по 2 см3 смеси i ексан-этилацегат (1 : 1, по объему) в кондиционированную хроматографическую колонку (п. 2,5.5). Промывают колонку 20 см3 гексана, которые отбрасывают, затем 10 см3 элюента № 2, которые тоже отбрасывают. Тебуконазол элюируют 40 см3 элюента № 3 (гексан-этилацетат = 3:7). Весь элюат собирают в грушевидную колбу емкостью 100 см3. Раствор выпаривают досуха на ротационном испарителе при температуре не выше 50ооС. Сухой остаток растворяют в 1—2 см3 гексана и 1 мм3 раствора вводят в хроматограф.
2.6.4. Условия хроматографирования. Газовый хроматограф «Цвет-550М» с ТИД или аналогичный.
МУК 4.1.2549—09
Колонка стеклянная 1 м * 3 мм, заполненная хроматоном N-Super (0,125—0,160 мм) с 5 % SE-30. Температура колонки 235 °С, испарителя
- 250 °С, детектора - 390 °С.
Скорость газа-носителя (азот) через колонку 32,2 см3/мин, водорода
- 16,9 см3/мин, воздуха-200 см3/мин. Объем вводимой пробы 1—2 мкл.
Линейный диапазон детектирования 0,5—10 нг.
2.6.6. Обработка результатов анализа. Количественное определение проводят методом абсолютной градуировки, содержание тебукона-зола в образце зерна сои или масла (X, мг/кг) вычисляют по формуле:
, где
Н2хСхУ
Н{хР
Н\ - высота (площадь) пика тебуконазола в стандартном растворе, мм (мв*сек);
Н2 - высота (площадь) пика тебуконазола в анализируемой пробе, мм (мв-сек);
К- объём экстракта, подготовленного для хроматшрафирования, см3;
Р - навеска анализируемого образца, г;
С - концентрация тебуконазола в стандартном растворе, мкг/см3.
Содержание остаточных количеств тебуконазола в анализируемом образце вычисляют как среднее из 2 параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор тебуконазола 10 мкг/мл разбавляют.
3. Проверка приемлемости результатов параллельных определений
2х|ЛГ,-ЛГ2|х100
(1)
^ г, где
2х|ЛГ,-ЛГ2|х100
(1)
^ г, где
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости (1):
Х\, X) - результаты параллельных определений, мг/кг; г - значение предела повторяемости (г = 2,8аг).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
4. Оформление результатов
Результат анализа представляют в виде:
11
МУК 4.1.2549—09
X ± А мг/кг при вероятности Р = 0,95, где
X - среднее арифметическое результатов определений, признанных приемлемыми, мг/кг;
А - граница абсолютной погрешности, мг/кг;
где
д*Х
100
S - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Б случае, если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде: «содержание вещества в пробе «менее нижней границы определения» (например: менее 0,01 мг/кг* где *- 0,05мг/кг - предел обнаружения в растительном масле).
5, Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ ? ИСО 5725-1-6—2002 «Точность (правильность и прецизионность) методов и результатов измерений».
5.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
5.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Сд должна удовлетворять условию:
+ > где
± Д^ ^(± Ад. х.) - характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой, соответственно), мг/кг; при этом:
Д* = ±0,84Д, где
А - граница абсолютной погрешности, мг/кг;
л 8*Х
где
Д = — 100
12
МУК 4.1.2549—09
S - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по формуле:
^=Г-Х-С„где
Xf, X, Сд - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п. 4) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки, соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле
^ = + •
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
\Kk\zK (2)
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
5.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (R):
5 R, где
2х\Х, -Л^хЮО
(*,+**)
Х\, Хг - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций), %.
13
МУК 4.1.2549—09
6. Требования техники безопасности
При проведении работы необходимо соблюдать требования безопасности, установленные для работ с токсичными, едкими, легковоспламеняющимися веществами (ГОСТ 12.1005-88).
При выполнении измерений с использованием газового хроматографа и работе с электроустановками соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019-79 и инструкциями по эксплуатации приборов.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91.
7. Требования к квалификации оператора
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом газожидкостной хроматографии, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 5.
8. Разработчики
Долженко В. И., Цибульская И. А., Блинова Т. Ф.
ГНУ Всероссийский научно-исследовательский институт защиты растений (Санкт-Петербург, г. Пушкин).
Определение остаточных количеств тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографииМетодические указания МУК 4.1.2549—09
Технический редактор А. В. Терентьева
Подписано в печать 18.12.09 Формат 60x88/16 Г1еч. л. 1,0
Тираж 200 экз.
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., д. 18, стр. 5, 7
Оригинал-макет подготовлен к печати и тиражирован отделом издательского обеспечения Федерального центра гигиены и эпидемиологии Роспотребнадзора 117105, Москва, Варшавское ш., 19а Отделение реализации, тел./факс 952-50-89
ББК 51.21 060
060 Определение остаточных количеств тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографии: Методические указания.—М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009.— 14 с.
1. Разработаны ГНУ Всероссийский научно-исследовательский институт защиты растений (авторы Долженко В. И., Цибульская И. А., Блинова Т. Ф.).
2. Рекомендованы к утверждению Комиссией по санитарно-эпидемиологическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 25 июня 2009 г. № 2).
3. Утверждены Руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главным государственным санитарным врачом Российской Федерации Г. Г. Онищенко 9 сентября 2009 г.
4. Введены в действие с 1 декабря 2009 г.
5. Введены впервые.
ББК 51.21
© Роспотребнадзор, 2009 © Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009
МУК 4.1.2549—09
Содержание
1. Вводная часть..........................................................................................................4
2. Методика определения тебуконазола в зерне сои, соевом и кукурузном
масле методом газожидкостной хроматографии.................................................5
2.L Основные положения......................................................................................5
2.2. Реактивы и материалы.....................................................................................6
2.3. Приборы и посуда............................................................................................7
2.4. Отбор и хранение проб....................................................................................8
2.5. Подготовка к определению.............................................................................8
2.6. Проведение определения................................................................................9
3. Проверка приемлемости результатов параллельных определений..................11
4. Оформление результатов......................................................................................11
5. Контроль качества результатов измерений.........................................................12
6. Требования техники безопасности......................................................................14
7. Требования к квалификации оператора..............................................................14
8. Разработчики.........................................................................................................14
3
МУК 4.1.2549—09
УТВЕРЖДАЮ
Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главный государственный санитарный врач Российской Федерации
9 сентября 2009 г.
Дата введения: 1 декабря 2009 г
Г. Г. Онищенко
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографии
Методические указания МУК 4.1.2549—09
Настоящие методические указания устанавливают метод газожидкостной хроматографии для определения в зерне сои, соевом и кукурузном масле массовой концентрации тебуконазола в диапазоне концентраций 0,05—1,0 мг/кг.
1. Вводная часть
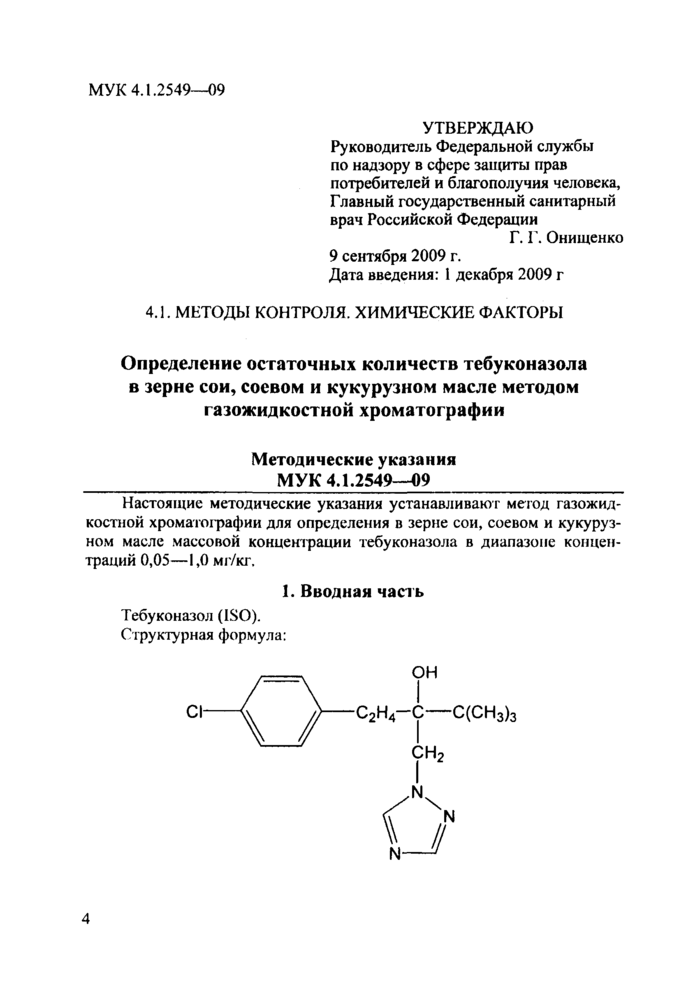
Тебуконазол (ISO). Структурная формула:
|
ОН |
|
сн2 |
4
МУК 4.1.2549-4)9
(RS)-1 р-хлорфенил-4,4-диметил-3-( 1Н-1,2,4-триазол-1 -ил ме-
тил)пентан-3-ил (ШРАС).
Брутто формула: C16H22CIN3 О.
Мол. масса: 307,8.
Химически чистый препарат - бесцветное кристаллическое вещество.
Температура плавления: 105 °С.
Давление паров при 20 °С -1,7 * 10'3 шРа.
Коэффициент распределения н-октанол/вода: Kow log Р = 3,7 (20 °С).
Растворимость в воде при 20 °С - 36 мг/дм3 (pH 5—9); гексане <0,1; изопропаноле, толуоле - 5—100, дихлорметане > 200 (в г/дм3 при 20 °С).
Вещество стабильно на свету, при повышенной температуре и гидролизу в чистой воде.
Класс токсичности по ВОЗ - III, ЕПА - II.
Острая оральная токсичность (LD50) для крыс 4 000 мг/кг, дермальная > 5 000 мг/кг.
Гигиенические нормативы для рапса: МДУ в кукурузе (зерно) -0,1 мг/кг, в сое (зерно, масло) - 0,1 мг/кг.
Область применения: системный фунгицид широкого спектра действия для борьбы с болезнями листьев и колосьев зерновых (фузариоз, септориоз, ржавчина, мучнистая роса и др.), серой гнилью виноградной лозы, некоторыми заболеваниями сои, рапса, подсолнечника. Используется как протравитель семян на зерновых.
2, Методика определения тебуконазола в зерне сои, соевом и кукурузном масле методом газожидкостной хроматографии
2.1. Основные положения
2.1.1. Область применения и принцип метода. Настоящий документ устанавливает методику определения остаточных количеств тебуконазола в зерне сои, соевом и кукурузном масле в диапазоне концентраций 0,05—1,0 мг/кг.
Методика основана на извлечении тебуконазола из зерна сои и растительного масла водно-ацетоновым раствором или ацетонитрилом с последующей очисткой перераспределением между двумя несмеши-вающимися жидкостями и на колонке с флорисилом. Количественное определение проводят методом газожидкостной хроматографии с использованием термоионного детектора.
5
МУК 4.1.2549—09
2.1.2. Избирательность метода. Избирательность метода обеспечивается очисткой экстрактов анализируемых проб и сочетанием условий хроматографирования.
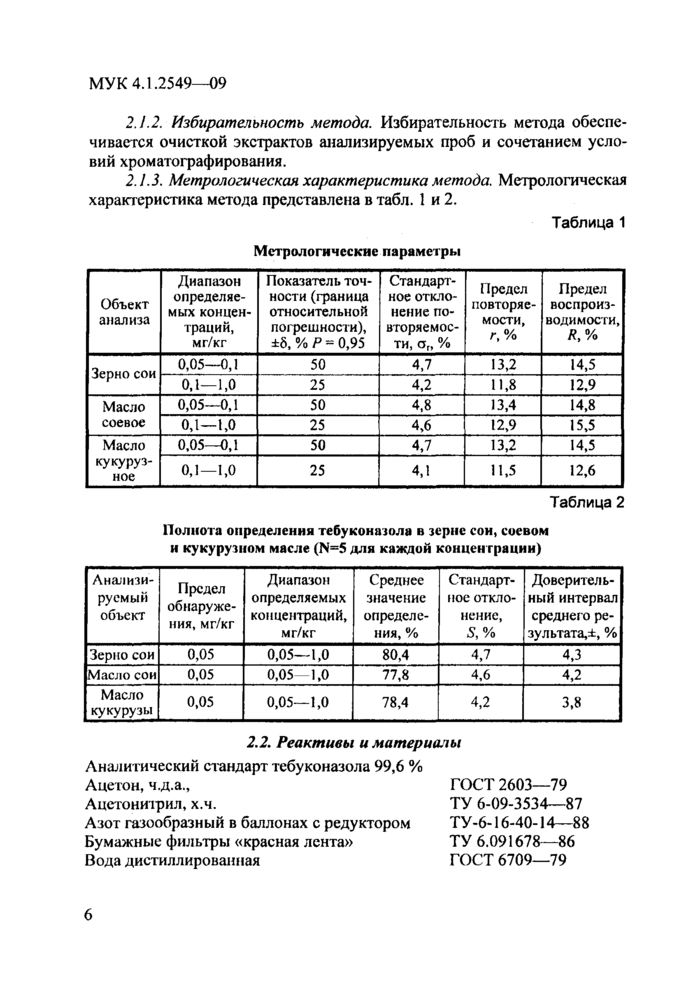
2.1.3. Метрологическая характеристика метода. Метрологическая характеристика метода представлена в табл. 1 и 2.
Таблица 1
|
Метрологические параметры | |||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||
|
Таблица 2 |
|
Полнота определения тебуконазола в зерне сои, соевом н кукурузном масле (N==5 для каждой концентрации) | ||||||||||||||||||||||||
| ||||||||||||||||||||||||
|
2.2. Реактивы и материалы |
ГОСТ 2603-79 ТУ 6-09-3534—87 ТУ-6-16-40-14—88 ТУ 6.091678—86 ГОСТ 6709-79
Аналитический стандарт тебуконазола 99,6 % Ацетон, ч,д.а..
Ацетонитрил, х.ч.
Азот газообразный в баллонах с редуктором Бумажные фильтры «красная лента»
Вода дистиллированная
МУК 4 Л .2549—09
Гексан, х.ч.
Дихлорметан х.ч.
Калий углекислый, х.ч.
Кальция хлорид, х.ч.
Насадка для колонки: хроматон N-Super (0,125—0,160 мм) с 5 % SE-30 (Чехия) Натрий сернокислый безводный, ч., свежепрокаленный Натрия хлорид, х.ч.
Стекловата
Флорисил 150—250 pm (Merck, Германия), содержание воды < 2,5 %
Этиловый эфир уксусной кислоты, ч.д.а. Элюент для колоночной хроматографии № 1: гексан-этилацетат (50 : 50 по объему) Элюент для колоночной хроматографии № 2: гексан-этилацетат (70 : 30 по объему) Элюент для колоночной хроматографии № 3: гексан-этилацетат (30 : 70 по объему)
ТУ 2631-003-05807999—98 ТУ 2631-019-44493179—98 ГОСТ 4221-76 ГОСТ 4161-77
23. Приборы и посуда.
Газовый хроматограф Цвет-550 М
с термоионным детектором и стеклянной
насадочной колонкой, длиной 1 м; внутренним
диаметром 3 мм, или аналогичный по своим
техническим характеристикам
Весы аналитические ВЛА-200 или аналогичные
Весы технические ВЛКТ-500
Мельница лабораторная зерновая ЛМЗ
Установка ультразвуковая «Серьга»
Ротационный вакуумный испаритель Biichi R-
200/205 (Швейцария) или аналогичный
Микрошприц МШ-10, МШ- ЮМ
Насос водоструйный
Колбы плоскодонные на шлифах
КШ500 29/32 ТС
Колбы круглодонные на шлифах
КШ50 29-32 ТС
Воронки лабораторные В-75-110 Воронки делительные ВД-3-500
ГОСТ 24104-2001 ГОСТ 24104-80 ТУ 1-01-0593—79 ТУ 3.836.008
7
МУК 4.1.2549—09
ГОСТ 1774-74Е ГОСТ 1770-74Е ГОСТ 29227-91 ГОСТ 25336-82Е
Цилиндры мерные на 100 см3
Колбы мерные на 25, 50,100 см3
Пипетки на 1, 2, 5, 10 см3
Стаканы химические
Колонка стеклянная хроматографическая
длиной 25 см, диаметром 10 мм
2.4. Отбор и хранение проб Отбор проб производится в соответствии с ГОСТ 10852-86. «Семена масличные. Правила приемки и методы отбора проб».
Для длительного хранения зерно сои подсушивают при комнатной температуре в отсутствие света. Сухие образцы могут храниться в течение года. Перед анализом пробы зерна доводят до стандартной влажности и измельчают. Пробы масла хранят в холодильнике при 0—4 °С в закрытой стеклянной таре не более 2 мес.
2.5. Подготовка к определению
2.5.1. Подготовка и очистка реактивов и растворителей. Перед началом работы рекомендуется проверить чистоту применяемых органических растворителей. Для этого 100 мл растворителя упаривают в ротационном вакуумном испарителе при температуре + 40 °С до объема 1,0 см3 и хроматографируют. При обнаружении мешающих определению примесей очистку растворителей производят в соответствии с общепринятыми методиками.
2.5.2. Кондиционирование колонки. Перед началом анализа колонку, заполненную хроматоном N-Super (0,125—0,160 мм) с 5% SE-30, не присоединяя к детектору, кондиционируют в токе инертного газа (азот) при температуре 250 °С до получения стабильной нулевой линии.
2.5.3. Приготовление стандартного и градуировочных растворов. Берут точную навеску тебуконазола (50 мг), переносят в мерную колбу на 50 см3, растворяют навеску в ацетоне и доводят до метки (Стандартный раствор с концентрацией 1,0мг/см3). Градуировочные растворы с концентрациями 0,5; 1,0; 2,0; 5,0 и 10 мкг/см5 готовят методом последовательного разбавления по объему, используя для разбавления гексан. Стандартный раствор можно хранить в холодильнике при температуре 0—4о0С в течение 6 мес., градуировочные растворы - в течение недели.
Для внесения в образец при определении полноты извлечения используют градуировочные растворы.
2.5.4. Построение градуировочного графика. Для построения градуировочного графика (высота или площадь пика - концентрация тебу-коназола в растворе) в хроматограф вводят по 1 мм3 градуировочных
МУК 4 Л .2549—09
растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций), измеряют высоты или площади пиков и строят график зависимости среднего значения высоты (площади) пика от концентрации тебуконазола в градуировочном растворе (мкг/см3).
2.5.5. Подготовка колонки с флористом для очистки экстракта. В нижнюю часть стеклянной колонки длиной 25 см и внутренним диаметром 1 см помещают тампон из стекловаты и вносят суспензию 4 г флори-сила в 20 см3 смеси гексан:этилацетат (1 : ], по объему), дают растворителю стечь до верхнего края сорбента. Колонку промывают 20 мл этой же смеси со скоростью 1—2 кап./сек, после чего она готова к работе.
2.5.6. Проверка хроматографического поведения тебуконазола на колонке с флористом. В круглодонную колбу емкостью 10 см3отбирают
1 см3 стандартного раствора тебуконазола с концентрацией 2 мкг/см3. Отдувают растворитель током теплого воздуха, остаток растворяют в
2 см3 элюента № 1 и вносят в колонку. Колбу обмывают еще 2 см3 элю-ента № 1 и также вносят в колонку. Затем последовательно промывают колонку 20 см3 гексана и 10 см3 элюента № 2. Далее элюируют тебуко-назол 40 см3 элюента № 3 со скоростью 1—2 кап./сек. Отбирают фракции по 10 см3 каждая, упаривают досуха, остаток растворяют в 1 см3 гексана и анализируют на содержание тебуконазола по п. 2.6.4. Фракции, содержащие тебуконазол, объединяют, упаривают досуха, остаток растворяют в 1 см3 гексана и анализируют по п. 2.6.4. Рассчитывают содержание тебуконазола в элюате, определяя полноту вымывания вещества из колонки и необходимый для этого объем элюента.
Примечание: профиль вымывания тебуконазола может меняться при использовании новой партии сорбента.
2.5.7. Подготовка приборов и средств измерения. Установка и подготовка всех приборов и средств измерения проводится в соответствии с требованиями технической документации.
2.6. Проведение определения
2.6.1. Экстракция тебуконазола из зерна сои. Навеску измельченного на лабораторной мелышце зерна сои, массой 10 г помещают в коническую колбу на 250 см3, заливают 50—100 см3 смеси растворителей ацетон - вода (в соотношении 1 : 1) и экстрагируют тебуконазол в ультразвуковой ванне в течение 10 мин. Экстракт фильтруют через бумажный фильтр («красная лента»). Экстракцию повторяют дважды порциями по 30 см3 той же смеси. Объединенный фильтрат помещают в делительную воронку и переэкстрагируют тебуконазол дихлорметаном три-
9