Государственное санитарно-эпидемиологическое нормирование Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств хизалофоп-П-Этила в зеленой массе рапса, семенах и масле рапса и сои по основному метаболиту хизалофоп-П кислоте методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.2336—08
Издание официальное
Москва * 2009
Федеральная служба по надзору в сфере зашиты прав потребителей и благополучия человека
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств хизалофоп-П-Этила в зеленой массе рапса, семенах и масле рапса и сои по основному метаболиту хизалофоп-П кислоте методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.2336-08
МУК 4.1.2336-08
2.6.2. Очистка экстрактов.
2.6.2.1. Очистка переэкстракцией Отобранные аликвоты экстрактов, полученных по п. 2.6.1, упаривают на роторном испарителе до объема 7-10 см3 при температуре 40°С Водный остаток переносят в делительную воронку емкостью 100 см3, приливают 15 см3 бидистиллированной воды, 20 см3 гексана и смесь встряхивают в течение 1 мин. Верхний органический слой отбрасывают. Водную фазу подкисляют 1 н соляной кислотой до pH 2, переносят в делительную воронку, прибавляют 20 см3диэтилового эфира и смесь встряхивают 1мин. Собирают органический слой, а экстракцию водной фазы повторяют дважды по 10 см3 диэтилового эфира. Объединенную органическую фазу пропускают через слой безводного сульфата натрия и выпаривают досуха на роторном испарителе при температуре 30°С
2.6.2.2. Очистка на патронах с силикагелем Остаток в колбе, полученный после упаривания очищенных по п.
2.6.2.1. экстрактов, растворяют в 2 см3 этилацетата и раствор переносят на предварительно промытый 3 см3 этилацетата концентрирующий патрон Bond Elut . Затем патрон промывают двумя порциями по 2 см2 этилацетата и двумя порциями по 2 см3 элюента №1 (смеси этилацетат-метанол = 80:20). Элюаты отбрасывают. Хизалофоп-П элюируют 4 см3 элюента №2 (смеси этилацетат-метанол = 60:40). Элюат собирают в грушевидную колбу-концентратор и выпаривают досуха на роторном испарителе при температуре 30°С
Сухой остаток растворяют в 1.25 см3 подвижной фазы для ВЭЖХ и 10 мм5 вводят в жидкостный хроматограф.
2.6.3. Условия хроматографирования Жидкостный хроматограф с УФ-детектором Acuity (Waters, USA). Колонка стальная длиной 10 см, внутренним диаметром 2.1 мм, заполненная октадецилсиликагелем зернением 1.7 мкм (ВЕН С18). Температура колонки 30±1°С
Подвижная фаза: ацетонитрил - 0.005М ортофосфорная кислота (50:50). Скорость потока элюента 0.25 см3/мин.
Рабочая длина волны 235 нм.
Дозируемый объем 10 мм3.
Линейный диапазон детектирования 1-10 нг.
Время удерживания хизалофоп-П кислоты 4,05±0,05мин.
Ю
МУК 4.1.2336-08
2.7. Обработка результатов анализа Количественное определение проводят методом абсолютной калибровки, содержание хизалофоп-П кислоты в пробе (X, мг/кг) вычисляют по формуле:
S2 С • V • п
S.-P
где Sp высота (площадь) пика хизалофоп-П в стандартном растворе, мм (мвсек);
S2 - высота (площадь) пика хизалофоп-П в анализируемой пробе, мм (мв сек);
V - объём пробы, подготовленной для хроматографического анализа, см3;
Р - навеска анализируемого образца, г;
С - концентрация стандартного раствора хизалофоп-П, мкг/см3.
п - коэффициент, учитывающий отбор аликваты экстракта (п=2 для зерна сои, зеленой массы и семян рапса; п=1 для масла сои и рапса).
Содержание остаточных количеств хизалофоп-П в анализируемом образце вычисляют как среднее из 2-х параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор хиза-лофоп-П 1 мкг/см3, разбавляют подвижной фазой для ВЭЖХ
Пересчет на содержание хизалофоп-П-этила (Х|) проводят по формуле: Х|= 1,08Х
3. Проверка приемлемости результатов параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости(1):
2- |Х,-Х2|100
------------<г (I)
(Х, + Х2)
где Х|, Х2 - результаты параллельных определений, мг/кг; г - значение предела повторяемости (г = 2.8аг).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
11
МУК 4.1.2336-08
4. Оформление результатов
Результат анализа представляют в виде:
(X ± Л) мг/кг при вероятности Р=0.95,
где X - среднее арифметическое результатов определений, признанных приемлемыми, мг/кг;
А - граница абсолютной погрешности, мг/кг;
Д = 6*Х/Ю0,
6 - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае, если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
"содержание вещества в пробе «менее нижней границы определения» (например: менее 0.005 мг/кг*, где *-0.005 мг/кг - предел обнаружения).
5. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-2002 «Точность (правильность и прецизионность) методов и результатов измерений».
5.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
5.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки С^должна удовлетворять условию:
C# = А я,х + Ая Х ,
где ± А я.х (± Дя.х ) - характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой, соответственно), мг/кг; при этом:
Дя = ± 0.84 Д . где Д - граница абсолютной погрешности, мг/кг:
МУК 4.1.2336-08
Д = 5*Х/100,
6 - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры К* рассчитывают по формуле:
К« = Х'-Х-Са,
где X', X, Сг - среднее арифметическое результатов параллельных определений (признанных приемлемыми по п.4) содержания компонента в образце с добавкой, испытуемом образце, концентрация добавки, соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
К = V Д2л^с + Д2д.х Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
|Кк|<К, (2)
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
5.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости:
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости
(R):
2* | X, -Хг| * 100
--------------<R, (3)
(Х, + Х2)
где Хь Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций).
13
6. Требования техники безопасности
При проведении работы необходимо соблюдать требования безопасности» установленные для работ с токсичными, едкими, легковоспламеняющимися веществами (ГОСТ 12.1005-88).
При выполнении измерений с использованием жидкостного хроматографа и работе с электроустановками необходимо соблюдать правила электробезопасности в соответствии с ГОСТ 12.1.019-79 и требования инструкций по эксплуатации приборов.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91.
7. Требования к квалификации оператора
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы методом высокоэффективной жидкостной хроматографии, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п.5.
14
ББК 51.21 0-60
0-60 Определение остаточных количеств хизапофоп-П-
этила в зеленой массе рапса, семенах и масле рапса и сои по основному метаболиту хизалофоп-П кислоте методом высокоэффективной жидкостной хроматографии. Методические указания. - М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009. - 14 с.
1. Разработаны Всероссийским НИИ зашиты растений (В.И. Довженко, И.А. Цибульская, И.К. Журкович, Н.В. Луговкина, Н.Г. Ковров).
2. Рекомендованы к утверждению Комиссией по санитарно-эпидемиологическому нормированию при Федеральной службе по защите прав потребителей и благополучия человека (протокол от 6 декабря 2007 г. № 3).
3. Утверждены Руководителем Федеральной службы по надзору в сфере зашиты прав потребителей и благополучия человека. Главным государственным санитарным врачом Российской Федерации Г.Г. Онишенко 15 февраля 2008 г.
4. Введены в действие с 10 апреля 2008 г.
5. Введены впервые.
ББК 51.21
Формат 60x88/16 Печ. л. 1,0.
Тираж 200 эю.
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994, Москва, Вадковский пер., д. 18/20
Тиражировано отделом издательского обеспечения Федерального центра гигиены и эпидемиологам Роспотребнадзора 117105, Москва, Варшавское ш., 19а Отделение реализации, тел ./факс 952-50-89
€> Роспотребнадзор, 2009 © Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009
МУК 4.1.2336-08
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главный Государственный санитарный врач Российской Федерации
Г.Г. Онищенко
15 февраля 2008 г.
Дата введения: 10 апреля 2008 г.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств хизалофоп-П-Этила в зеленой массе рапса, семенах и масле рапса и сои по основному метаболиту хизалофоп-П кислоте методом высокоэффективной жидкостной хроматографии
Методические указания МУК 4.1.2336-08
1. Вводная часть
Краткая характеристика препарата:
Действующее вещество (д.в.): хизалофол-П-этил.
Название д.в. по номенклатуре ИЮПАК: (Л)-2-[4-[(6-хлор-хиноксалин-2-илокси)-фенокси] пропионовой кислоты этиловый эфир. Структурная формула д.в.:
Эмпирическая формула д.в.: C19H17CIN2O4.
Молекулярная масса д.в.: 372,8.
Химически чистое вещество: светло-коричневые кристаллы.
3
Температура плавления д.в.: 76-77°С
Давление пара д.в. при 20°С: 1.1-КГ1 мПа.
Растворимость д.в. (г/л) при 20°С: в воде - 0,0004, в гексане - 5,0, этаноле - 22, ксилоле - 360, ацетоне - 650.
Стабильность д.в.: устойчив к действию света и при нагревании, разлагается до хизалофоп-П кислоты в щелочной среде. В почве разлагается до хизалофоп -П кислоты, To.s< 1 дня.
Острая пероральная токсичность препаратов (LDso) для крыс -1180-1210 мг/кг, для мышей - 1750-1800 мг/кг. Не оказывает раздражающего действия на кожу.
Гигиенические нормативы: ВМДУ в сое (семена, масло) -0,05 мг/кг.
Область применения: гербицид системного действия, применяется для борьбы с однолетними и многолетними злаковыми сорняками на различных культурах, в том числе на посевах сои и рапса.
Краткая характеристика хизалофоп-П кислоты.
Название по номенклатуре ИЮПАК: (Я)-2-[4-[(6-хлорхиноксалин-2-илокси)фен-окси) пропионовая кислота.
Структурная формула:
Эмпирическая формула д.в.: С17Н,зС1Ы204.
Молекулярная масса д.в.: 344,8.
2. Метод определения хизалофоп-П-этила в зеленой массе рапса, семенах и масле рапса и сои по основному метаболиту хизалофоп-П кислоте методом высокоэффективной жидкостной хроматографии
2.1. Основные положения
2.1.1. Область применения и принцип метода Настоящий документ устанавливает метод определения остаточных количеств хизалофоп-П-этила в зеленой массе рапса, семенах и масле
МУК 4.1.2336-08
рапса и сои в диапазоне концетраций 0,025-0,25 мг/кг. Метод основан на количественном определении хизалофоп-П кислоты, основного метаболита хизалофоп-П-этила, и включает извлечение остаточных количеств хизалофоп-П кислоты из анализируемого объекта органическими растворителями, очистку экстракта перераспределением в системе несме-шивающихся растворителей и на патронах с силикагелем (Bond Elut). Количественное определение проводят методом высокоэффективной жидкостной хроматографии с УФ-детектором.
2.1.2. Избирательность метода Избирательность метода обеспечивается сочетанием условий подготовки проб и хроматографического анализа.
2.1.3. Метрологические характеристики При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р=0.95 не превышает значений, приведенных в таблице 1, для соответствующих диапазонов концентраций.
Таблица 1
|
Метрологические параметры |
|
Объект
анализа |
Диапазон определяемых концентраций, мг/кг |
Показатель точности (граница относительной погрешности),
±6. % |
Стандартное отклонение повторяемости, о„ % |
Предел повторяемости,
г.% |
Предел
воспроиз
водимо
сти,
R, % |
|
Зеленая
масса
рапса |
0.025-0.1 |
50 |
4.6 |
12.9 |
15.5 |
|
-«- |
0.1-0.25 |
25 |
3.6 |
10.1 |
12.1 |
|
Семена
рапса |
0.025-0.1 |
50 |
4.8 |
13.4 |
16.0 |
|
-«- |
0.1-0.25 |
25 |
3.8 |
10.6 |
12.7 |
|
Масло
рапса |
0.025-0.1 |
50 |
5.0 |
14.0 |
16.8 |
|
-«- |
0.1-0.25 |
25 |
4.2 |
11.8 |
12.9 |
|
Зерно сои |
0.025-0.1 |
50 |
4.6 |
12.9 |
14.2 |
|
|
0.1-0.25 |
25 |
5.2 |
14.6 |
17.5 |
|
Масло сои |
0.025-0.1 |
50 |
4.6 |
12.9 |
15.5 |
|
|
0.1-0.25 |
25 |
5.3 |
14.8 |
17.7 |
|
|
5 |
МУК 4.1.2336-08
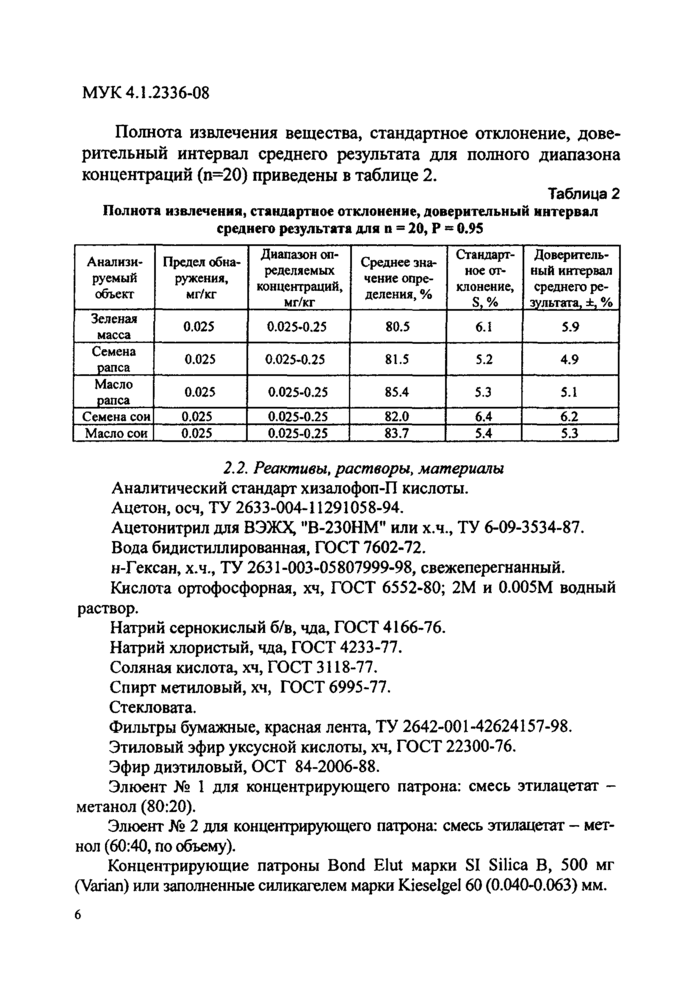
Полнота извлечения вещества, стандартное отклонение, доверительный интервал среднего результата для полного диапазона концентраций (п=20) приведены в таблице 2.
Таблица 2
Полнота извлечения, стандартное отклонение, доверительный интервал среднего результата для о = 20, Р « 0.95
|
Анализи
руемый
объект |
Предел обнаружения, мг/кг |
Диапазон определяемых концентраций, мг/кг |
Среднее значение определения, % |
Стандартное отклонение, S,% |
Доверительный интервал среднего результата, ±, % |
|
Зеленая
масса |
0.025 |
0.025-0.25 |
80.5 |
6.1 |
5.9 |
|
Семена
рапса |
0.025 |
0.025-0.25 |
81.5 |
5.2 |
4.9 |
|
Масло
рапса |
0.025 |
0.025-0.25 |
85.4 |
5.3 |
5.1 |
|
Семена сои |
0.025 |
0.025-0.25 |
82.0 |
6.4 |
6.2 |
|
Масло сои |
0.025 |
0.025-0.25 |
83.7 |
5.4 |
5.3 |
2.2. Реактивы, растворы, материалы Аналитический стандарт хизалофоп-П кислоты.
Ацетон, осч, ТУ 2633-004-11291058-94.
Ацетонитрил для ВЭЖХ, "В-230НМ" или х.ч., ТУ 6-09-3534-87. Вода бидистиллированная, ГОСТ 7602-72. н-Гексан, х.ч., ТУ 2631-003-05807999-98, свежеперегнанный. Кислота ортофосфорная, хч, ГОСТ 6552-80; 2М и 0.005М водный раствор.
Натрий сернокислый б/в, чда, ГОСТ 4166-76.
Натрий хлористый, чда, ГОСТ 4233-77.
Соляная кислота, хч, ГОСТ 3118-77.
Спирт метиловый, хч, ГОСТ 6995-77.
Стекловата.
Фильтры бумажные, красная лента, ТУ 2642-001-42624157-98. Этиловый эфир уксусной кислоты, хч, ГОСТ 22300-76.
Эфир диэтиловый, ОСТ 84-2006-88.
Элюент № 1 для концентрирующего патрона: смесь этилацетат -метанол (80:20).
Элюент Jfe 2 для концентрирующего патрона: смесь этилацетат - мет-нол (60:40, по объему).
Концентрирующие патроны Bond Elut марки SI Silica В, 500 мг (Varian) или заполненные силикагелем марки Kieselgel 60 (0.040-0.063) мм.
6
МУК 4.1.2336-08
Подвижная фаза для ВЭЖХ: ацетонитрил - 0.005М ортофосфорная кислота (50:50).
2.3. Приборы, аппаратура, посуда Жидкостный хроматограф "ACQUITY" фирмы «Waters» с быстро-сканирующим УФ детектором, снабженный дегазатором, автоматическим пробоотборником и термостатом колонки или хроматограф «Breeze» с УФ-детектором или аналогичный.
Колонка ACQUITY UPLC ВЕН С-18, (100x2.1) мм, 1,7 мкм (Waters).
Аппарат для встряхивания, ТУ 64-1-1081-73 или аналогичный.
Баня ультразвуковая нСерьгаи УЗМ002 или аналогичная.
Весы аналитические типа ВЛА-200, ГОСТ 24104-2001.
Воронки делительные емкостью 250 и 500 см3, ГОСТ 25336-82. Воронки химические конусные, ГОСТ 25336-82.
Индикаторная бумага универсальная, ТУ 6-09-1181-76. Колбы-концентраторы емкостью 100 и 250 см3, ГОСТ 25336-82. Колбы плоскодонные емкостью 100 и 300 см3, ГОСТ 25336-82. Колбы мерные со шлифом емкостью 25, 50, 100 см3, ГОСТ 1770-74. Насос водоструйный, ГОСТ 10696-75.
Ротационный вакуумный испаритель типа ИР-1 или аналогичный. Пипетки мерные емкостью 1,2, 5 и 10 см3, ГОСТ 20292-74. Пробирки мерные со шлифом емкостью 5,0 см3, ГОСТ 1770-74. Стаканы химические на 100, 200 и 500 см3, ГОСТ 25336-82. Установка для упаривания растворителей в токе азота.
Шприц для ввода образцов в концентрирующий патрон.
2.4. Подготовка к определению
2.4.1. Подготовка растворителей и приготовление растворов Перед началом работы рекомендуется проверить чистоту применяемых органических растворителей. Для этого 100 мл растворителя упаривают в ротационном вакуумном испарителе при температуре +40°С до объема 1,0 см3 и хроматографируют. При обнаружении мешающих определению примесей очистку растворителей производят в соответствии с общепринятыми методиками.
Для приготовления 2М раствора ортофосфорной кислоты 200 г 98% (или 225 г 87%) кристаллической Н3Р04 помещают в мерную колбу объемом 1 дм3, растворяют в 600 см3 дистиллированной воды и доводят объем до метки дистиллированной водой.
7
МУК 4.1.2336-08
Для приготовления 0.005М раствора ортофосфорной кислоты 2.5 см3 2М раствора Н3РО4 вносят в мерную колбу на 1 дм3 и доводят до метки деионизированной бидистиллированной водой.
Для приготовления подвижной фазы в колбе емкостью 1 дм3 смешивают 500 см3 ацетонитрила с 500 см3 0.005М раствора ортофосфорной кислоты.
2.4.2. Кондиционирование колонки Перед началом анализа колонку (ВЕН С-18) кондиционируют в потоке подвижной фазы (0.25 см3/мин) до стабилизации нулевой линии в течение 1-2 часов.
2.4.3. Приготовление стандартных растворов Основной раствор хизалофоп-П кислоты с содержанием 100 мкг/см3 готовят растворением в ацетонитриле 0,01 г аналитического стандарта в мерной колбе емкостью 100 см3. Раствор хранят в холодильнике при температурю +4-6°С не более двух недель.
Градуировочные растворы с концентрациями 0.1 , 0.2, 0.5, 0.75 и 1.0 мкг/см3 готовят из основного стандартного раствора хизалофоп-П кислоты последовательным разбавлением подвижной фазой для ВЭЖХ непосредственно в день проведения анализа.
При определении полноты извлечения хизалофоп-П-этила из модельных матриц используют растворы, приготовленные из основного стандартного раствора последовательным разбавлением ацетонитрилом.
2.4.4. Построение калибровочного графика Для построения калибровочного графика в инжектор хроматографа вводят по 10 мкл приготовленных по п.2.4.2, растворов, содержащих хизалофоп-П кислоту. Осуществляют не менее трех параллельных измерений и находят среднее значение высоты (площади) хроматографического пика для каждой концентрации. Строят калибровочный график зависимости высоты (площади) хроматографического пика в мм (мв сек) от концентрации хизалофоп-П кислоты в рабочем растворе в мкг/см3.
2.4.5. Подготовка концентрирующего патрона для очистки экстракта
Концентрирующий патрон промывают последовательно с помощью шприца 5 см5 бидистиллированной воды и 5 см3ацетонитрила со скоро-
8
МУК 4.1.2336-08
стью 5 см3/мин. Затем промывают патрон 3 см3 этил ацетата. Элюаты отбрасывают.
2.5. Отбор и хранение проб Отбор проб семян рапса и сои производится в соответствии с ГОСТ 10852-86. «Семена масличные. Правила приемки и методы отбора проб». Семена хранят при комнатной температуре в полотняных мешочках, перед анализом доводят до стандартной влажности и измельчают. Масло рапса и сои хранят в холодильнике при температуре 0-4°С в герметично закрытой стеклянной таре в течение 6 месяцев.
2.6. Проведение определения
2.6.1. Экстракция хизалофоп-П
2.6.1.1. Зерно сои и зеленая масса и семена рапса Навеску измельченных семян или зеленой массы рапса (10 г) помещают в плоскодонную колбу емкостью 250 см3 и добавляют 100 см3 смеси ацетонитрил-бидистиллированная вода (80:20, по объему) и помещают в УЗ-баню на 10 мин. Суспензию фильтруют под вакуумом на воронке Бюхнера через бумажный фильтр. Растительный материал повторно экстрагируют 50 см3 той же смеси на УЗ-бане в течение 5 мин.
Из объединенного экстракта отбирают аликвоту (около 70 см3), соответствующую 5 г зерна сои, семян или зеленой массы рапса. Дальнейшую очистку проводят по п.2.6.2.
2.6.1.2. Масло сои и рапса Навеску масла (5 г) растворяют в 20 см3 гексана в конической колбе на 150 см3, затем приливают 50 см3 80%-ного ацетонитрила и эмульсию энергично перемешивают в течение 30 мин на аппарате для встряхивания. Ацетонитрильный слой осторожно декантируют в делительную воронку емкостью 200 см3, а к оставшемуся маслу добавляют 50 см3 80%-ного ацетонитрила и эмульсию перемешивают на аппарате для встряхивания 30 мин. Эмульсию количественно переносят в ту же делительную воронку, которую помещают в холодильник на 30 мин для четкого разделения слоев. Отделяют ацетонитрильную фазу и пропускают ее через слой ваты в грушевидную колбу емкостью 200 см3. Дальнейшую очистку проводят по п. 2.6.2.
9
1