МУ 42-51-18-93
Испытание стерилизующей способности мембранных фильтров патронного типа
Купить МУ 42-51-18-93 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методические указания устанавливают порядок подготовки и проведения испытания стерилизующей способности мембранных фильтров патронного типа, предназначенных для стерилизующей фильтрации водных и органических растворов лекарственных веществ, воды, спиртов и органических растворителей, используемых в производстве инъекционных лекарственных средств
Оглавление
1. Общие положения
2. Подготовка к проведению испытания
3. Проведение испытания
4. Учет результатов
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
- Раздел Экология
- Раздел 19 ИСПЫТАНИЯ
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2
стр. 3

стр. 4

стр. 5
министерство ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
ОРГАНИЗАЦИЯ И КОНТРОЛЬ ПРОИЗВОДСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ
СТЕРИЛЬНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА МУ 42-51-1-93 -v МУ 42-61-26-93
М<х««а
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Испытание стерилизующей способности МУ 42-51-18-93
мембранных фильтров патронного типа
1. ОБЩИЕ ПОЛОЖЕНИЯ
1.1. Методические указания устанавливают порядок подготовки и проведения испытания стерилизующей способности мембранных фильтров патронного типа, предназначенных для стерилизующей фильтрации водных и органических растворов лекарственных веществ, воды, спиртов и органических растворителей. используемых в производстве инъекционных лекарственных средств.
1.2. Под мембранными фильтрами патронного типа (фильтрэлементами) подразумевается конструкция цилиндрической формы, состоящая из мембраны складчатой конфигурации с порами размером 0.22 мкм и опорных подложек по обе стороны мембраны, помещенных между двумя перфорированными корпусами. Оба конца фильтрэлемента герметизируются торцевыми колпачками путем термосварки. Фильтрэлемеиты используются при фильтрации больших объемов жидкостей (400 л и более).
1.3. Под стерилизующей способностью подразумевается абсолютная способность фильтрэлементов задерживать микроорганизмы и частицы другой природы с размерами равными или более 0.22 мкм.
1.4. Основанием для оценки стерилизующей способности фильтрэлементов является способность тест-культуры Pseudomonas dlmlnuta АТСС 19146 частично проходить через мембрану с порами размером 0,45 мкм и полностью задерживаться на мембране с порами размером 0.22 мкм.
1.5. Испытание должно проводиться в 'чистом* помещении на рабочем месте, оборудованном установкой подачи ламинарного потока стерильного воздуха (1 класс чистоты).
1.6. Персонал, проводящий испытание, должен работать в стерильной технологической одежде из безворсовой ткани и в перчатках.
2. ПОДГОТОВКА К ПРОВЕДЕНИЮ ИСПЫТАНИЯ
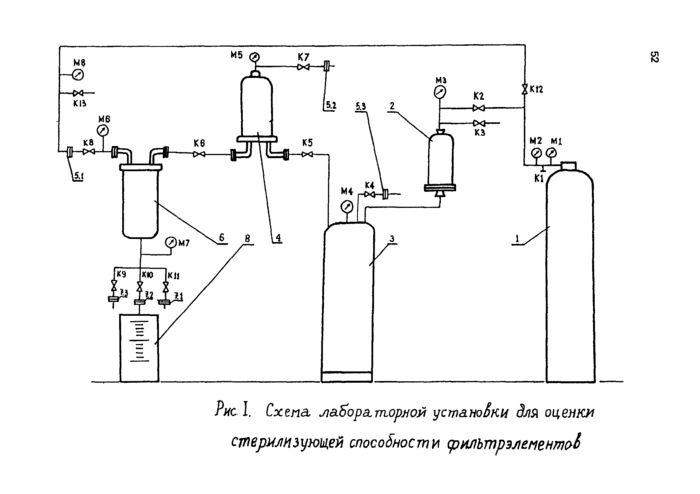
2.1. Испытания стерилизующей способности фильтрэлементов следует проводить с использованием лабораторной установки, схема которой представлена на рис.1, где:
1 - источник давления (баллон с азотом или компрессор);
2 - патронный фильтр для стерилизации воздуха (азота):
3 - сосуд для суспензии;
4 - фильтр с испытуемым фильтрэлементом:
5.1 - 5.3 - вентиляционный мембранный фильтр с гидрофобной мембраной диаметром 47 мм и порами размером 0.22 мкм;
6 - сборник фильтрата;
7.1 - 7.3 - контрольный мембранный фильтр с гидрофильной мембраной диаметром 90 мм и порами размером 0.22 мкм;
8 - приемник фильтрата;
М I ■ 8 ■ манометры:
К 1 - 13 - клапаны.
2.2. Перед началом испытаний собрать установку в соответствии со схемой (рис.1), начиная с поз.2 до поз.7 включительно.
2.3. Фильтры 7.1 - 7.3 экипировать гидрофильными, фильтры 5.1 - 5.3 гидрофобными мембранами.
2.4. Установить испытуемый фильтрэлемент в посадочное гнездо фильтра 4.
Рис I. Cxtna. siafiopa. торной установки для оценки стерилизующей способности (рнпътрэлементоб
53
2.5. Открыть клапаны К 2 - К 11.
2.6. Собранную установку простерилизовать острым паром в “линии* или насыщенным паром в автоклаве при избыточном давлении 0.11 МПа (1.1 кгс/см j и температуре (120+1 )®С в течение 45 минут. При стерилизации в автоклаве колокол фильтра 4 стерилизуется не в сборе с установкой.
2.7. После стерилизации установку охладить до комнатной температуры, закрепить колокол на корпусе фильтра 4 и присоединить установку к источнику давления 1.
2.8. Проверить герметичность установки и целостность фильтрэлементэ методом “точки пузырька’. Для этого в емкость залить 5 литров стерильной воды очищенной, закрыть кл^ланы КЗ. К 4. К 8 - К 10. К 12. К 13 и при давлении 0.05 МПа (0.5 кгс/см2) пропустить воду через фильтр 4.
2.9. По окончании истечения воды через фильтр 7.1 закрыть клапаны К 7. К 11. на выходной конец фильтра 5.1 надеть шланг и поместить в сосуд 8 с водой, открыть клапан К 8 и при постепенном повышении давления наблюдать за появлением пузырьков воздуха в сосуде 8.
2.10. В том случае, если значение 'точки пузырька* ниже установленного изготовителем фильтрэлементэ. следует смочить его повторно и провести пузырьковый тест в соответствии с п.п.2.8 - 2.9.
2.11. При повторном несоответствии требованиям, предъявляемым к фильтр-элементам по показателю “точки пузырька*, данный фильтрэлемент испытанию стерилизующей способности не подвергается.
2.12. Убедившись в целостности фильтрэлемеита и герметичности системы в целом, снять давление, для чего следует закрыть клапан К 1.
2.13. При наличии приборов типа ’Сарточек*. "Паллтроник* или аналогичных можно проводить проверку герметичности установки и целостности фильтр-элементов с использованием этих приборов по соответствующей методике.
2.14. Для проведения испытания стерилизующей способности фильтрэлемен-та используют тест-культуру Pseudomonas dimlnuta АТСС 19146. представляющую собой мелкие кокковидные палочки размером (0.3-0.4) к (0.8-1.0) мкм преимущественно в виде одиночных клеток; грамотрицательна. не образует спор, характеризуется одиночными полярными жгутиками. На агаризованной питательной среде культура образует колонии светло-бежевого цвета, выпуклые, блестящие, с ровными краями. При росте в жидкой питательной среде часто образует пленку на поверхности среды.
2.15. Тест-культуру Pseudomonas dimlnuta АТСС 19146 выращивают при температуре 32°С в течение 22-24 часов в солевом лактозном бульоне с целью получения суспензии культуры с концентрацией, равной 107 микроорганизмов в 1 мл среды.
2.16. Для проведения испытания от каждой партии фильтрэлементов отбирать не менее 1% от их общего количества.
3. ПРОВЕДЕНИЕ ИСПЫТАНИЯ
3.1. Залить в емкость 3 60Q0 мл суспензии культуры Pseudomonas dimlnuta АТСС 19146 с концентрацией 10' микроорганизмов в 1 мл.
3.2. Закрыть клапан К 8. а клапаны К 1. К 2. К 5 - К 7. К 10 открыть и проводить фильтрацию при давлении, не превышающем 0.1 МПа (1.0 кгс/см2).
3.3. По окончании фильтрации суспензии через фильтр 4 закрыть клапаны К 2. К 5 - К 7. К 13. присоединить источник давления 1 с помощью быстрось-емного фланцевого соединения к фильтру 5.1. открыть клапаны К 12. К 8 и отфильтровать фильтрат из сборника 6 через фильтр 7.2.
54
3.4. Закрыть клапан К 1. снять остаточное давление в системе, для чего открыть клапан К 13. и отсоединить источник давления 1 от фильтра 5.1.
3.5. Залить в емкость 3 не менее 5000 мл стерильной воды очищенной.
3.6. Закрыть клапаны К 8, К 10. К 12, К 13, а клапаны К 1. К 2. К 5 -К 7. К 9 открыть и проводить фильтрацию промывной воды при давлении 0.1 МПа (1.0 кгс/см2).
3.7. По окончании фильтрации промывной воды через фильтр 4 проводить фильтрацию через фильтр 7.3. аналогично п.п.3.3 - 3.4.
3.8. Контрольные мембраны из фильтров 7.1 - 7.3 поместить в чашки Петри с питательным агаром.
3.9. Посевы инкубировать при температуре 32°С в течение 2-3 суток.
3.10. По окончании испытания провести обеззараживание установки и передать ее в помещение мойки.
3.11. Установку разобрать, все узлы установки тщательно промыть и подготовить к следующему испытанию.
4. УЧЕТ РЕЗУЛЬТАТОВ
4.1. Оценку результатов испытания стерилизующей способности филырэле-мента проводят по наличию или отсутствию роста колоний тест-культуры Pseudomonas diminuta АТСС 19146 на контрольных мембранных фильтрах.
4.2. При появлении колоний тест-культура на контрольных мембранных фильтрах следует сосчитать их количество и провести идентификацию.
4.3. Наличие роста колоний тест-культуры и (или) посторонней микрофлоры на контрольном мембранном фильтре 7.1 свидетельствует о неудовлетворительной отмывке и стерилизации установки перед проведением испытания.
4.4. Фильтрэлемент обладает абсолютной стерилизующей способностью при условии отсутствия роста колоний тест-культуры Pseudomonas diminuta АТСС 19146 на контрольных мембранных фильтрах 7.2 и 7 3.
4.5. При наличии роста колоний тест-культуры хотя бы на одном из контрольных фильтров 7.2 или 7.3 и отсутствии роста на фильтре 7.1 испытуемый фильтрэлемент считают неудовлетворяющим требованиям по абсолютной стерилизующей способности. Испытание следует повторить.
4.6. При повторном обнаружении роста колоний тест-культуры на контрольных фильтрах партия фильтрэлементов бракуется.