МУ 28-6/5
Методические указания по стерилизации некоторых гемосорбентов
Купить МУ 28-6/5 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методические указания предназначены для разработчиков и изготовителей гемосорбентов, а также для специалистов лечебно-профилактических учреждений, применяющих новый метод детоксикационной терапии - метод гемосорбции при лечении некоторых заболеваний и отравлений, а также для работников санитарно-эпидемиологических и дезинфекционных станций, осуществляющих контроль за соблюдением асептики и стерилизации.
Оглавление
1. Общие положения
2. Стерилизация гемосорбентов
3. Контроль стерильности гемосорбентов
4. Требования, предъявляемые к помещению для подготовки гемосорбентов к гемосорбции
5. Меры предосторожности при работе с растворами перекиси водорода
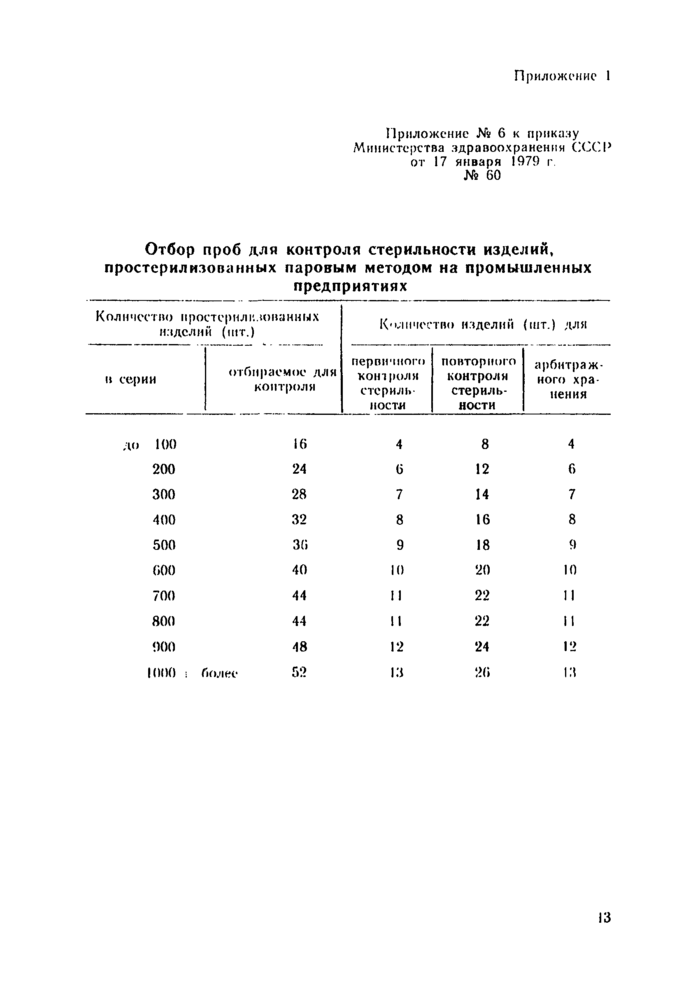
Приложение 1 Отбор проб контроля стерильности изделий, простерилизованных паровым методом на промышленных предприятиях
Приложение 2 Приготовление рабочих растворов комплекса перекиси водорода с моющими средствами
Приложение 3 Средства и способы обработки рук персонала, проводящего подготовку гемосорбентов к гемосорбции
Приложение 4 Журнал инструктажа на рабочем месте (первичный, повторный, внеплановый, текущий)
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
- Раздел Экология
Организации:
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18
МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО СТЕРИЛИЗАЦИИ НЕКОТОРЫХ ГЕМОСОРБЕНТОВ
Москва, 1984 год
Заинтересованным министерствам и ведомствам представляется право размножения настоящих «Методических указаний» в необходимом количестве экземпляров.
2
допускаются лица не моложе 18 лет, прошедшие соответствующий инструктаж по технике безопасности, мерам предосторожности и профилактике случайных отравлений, а также по оказанию первой медицинской помощи при случайных отравлениях и несчастных случаях1. Инструктаж проводят 2 раза в год ответственные специалисты, назначенные администрацией предприятия. Время проведения инструктажа (число, месяц, год) регистрируются в специальном журнале (Приложение 4).
5-2. Медицинский персонал проходит предварительный и периодический (раз в год) медицинский осмотр. Лица с повышенной чувствительностью к перекиси водорода и другим применяемым химическим средствам от работы с ними отстраняются.
5.3. Расфасовку и приготовление рабочих растворов перекиси водорода проводят в вытяжном шкафу или в отдельном проветриваемом помещении, хранение — в плотно закрывающихся емкостях, в темной посуде. Рабочие растворы можно хранить при указанных условиях не более недели, пергидроль — до 2-х месяцев (в дальнейшем его использование проводить после химического анализа).
5.4. Работу по обработке помещения перекисью водорода проводят в защитных герметических очках ПО-2, ПО-3, в универсальных респираторах, и резиновых перчатках и фартуке.
5.5- Во вспомогательных помещениях в аптечках необходимо иметь средства для оказания первой медицинской помощи, применяемые при отравлениях и поражениях кожи и слизистых дезрастворами.
5.6. В случае попадания на кожу или в глаза растворов перекиси водорода необходимо немедленно обильно промыть их струей водопроводной воды.
В случае возникновения сухости кожи рук их промывают и смазывают любым увлажняющим кремом или глицериновой смесью для рук.
5.7. После работы перчатки обмыть водой с мылом и затем высушить. Руки вымыть и смазать смягчающим кремом.
5.8. В помещениях необходимо иметь средства противопожарной защиты.
5.9. Перед проведением обработки помещения необходимо обесточить электрооборудование.
5.10. Не допускать попадания перекиси водорода на электропровода и коррозирующие поверхности.
12
Приложение 1
Приложение № б к приказу Министерства здравоохранения СССР от 17 января 1979 г № 60
|
Отбор проб для контроля стерильности изделий* простерилизованных паровым методом на промышленных предприятиях | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
13
Приложение 2
Приготовление рабочих растворов комплекса перекиси водорода с моющими средствами
|
Приготовление растворов комплекса перекиси водорода с моющими средствами Астра, Лотос, Прогресс проводят в соответствии с расчетами, приведенными в таблице. | |||||||||||
| |||||||||||
|
30.0 31.0 32.0 33.0 |
100 97 94 90 |
895 898 901 905 |
5 |
3,0 |
0,5 |
|
30,0 |
200 |
795 | |||
|
31,0 |
194 |
801 |
5 |
6,0 |
0,5 |
|
32,0 |
188 |
807 | |||
|
33,0 |
180 |
815 |
При приготовлении рабочего раствора перекись водорода приливают к раствору моющего средства. Для приготовления комплекса перекиси водорода с моющими средствами можно использовать как медицинскую перекись водорода, так и техническую марок А и Б по ГОСТ 177-77.
14
Приложение
Средства и способы обработки рук персонала, проводящего подготовку гемосорбентов к гемосорбции
1. Рецептуру С-4 (первомур) готовят из перекиси водорода и муравьиной кислоты, которые смешивают в стеклянной посуде, помещают в воду (Т° 15—20° С) на 1—1,5 часа, периодически встряхивают. Полученный раствор хранят не более суток в герметично закрытом стеклянном сосуде в прохладном месте. Раствор готовят только в день использования. Для обработки рук применяют 2,4% раствор рецептуры С-4 (первомур). Обработку проводят в течение 1 минуты, полностью погружая руки в эмалированный таз с раствором рецептуры С-4, после чего вытирают стерильной салфеткой и надевают стерильные перчатки.
|
Количество ингредиентов для приготовления раствора рецептуры С-4 | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
2. Хлоргексидин биглюконат (гибитан) выпускается в виде 20"/« водного раствора в стеклянных емкостях по 500 мл.
Для обработки рук используют 0,5% водно-спиртовой раствор препарата, для получения которого 20%> раствор разводят в спирте (70%) в соотношении 1:40. Обработку рук производят ватным тампоном, смоченным этим раствором, в течение 3 минут.
3. Церигель прозрачная, бесцветная несколько вязкая жидкость. В состав препарата введен пленкообразователь, за счет которого при обработке рук образуется тонкая пленка церигеля. Обработку рук проводят путем тщательного растирания 3—4 г препарата в течение 8—10 секунд. При этом следят за тем, чтобы препарат покрыл ладонные поверхности, межпальцевые промежутки и нижнюю треть пред-
15
плечья- После окончания работы пленку церигеля снимают спиртом.
4. Дегмин — твердое воскоподобное вещество, хорошо растворимое в воде. Растворы дегмина слегка опалесцируют и устойчивы при хранении.
Дегмицид — жидкость, содержит 30% дегмина.
Дегмин и дегмицид рекомендованы в Г'/<» концентрации для обработки рук, которую проводят путем последовательного протирания двумя тампонами, обильно смоченными раствором препарата, по 3 минуты. При повторной обработке руки протирают одним тампоном 2—3 минуты.
5. йодогшрон — смесь комплекса поливинилпирролидона-йода с йодидом калия (йодофор), желто-коричневый аморфный порошок без запаха или со слабым специфическим запахом, содержащий 6—8% активного йода.
Для обработки рук применяют 0,1% водный раствор препарата (по активному йоду), получаемый из 1% раствора, который готовят в аптечных условиях.
При обработке рук их моют в проточной воде с мылом в течение 1 минуты и вытирают стерильной салфеткой. Затем кисти рук полностью погружают в 0,1% раствор йодопирона (по активному йоду) и моют в течение 4-х минут стерильной марлевой салфеткой. Особенно тщательно обрабатывают ногти. Руки сушат стерильной марлевой салфеткой.
16
; x зс^> ~ - к;
55-^
■ to*
o\
о
£
СЛ
7;
н
£ 00 2 fo"
£
3
-5 3:
_; -! й н
2 = ~ *3
= 0: > H
-5 = о
5? X X
~ S^-a
c _X ^ £}
~* - nS
* o
П
П
■3
£tf
ТЭ r
V sa
О
X
О
*тз
*
|
X n н "О << 3! Н &> * X ю а о оз н о ■о X tr х« | ||||||||||||||||||||||||||||||||||||||
“а
ГС
>
Ьа
*
Приложение 4
Л 70862 от 26.03.1984 г. Зак. 840 Тир. 1000
Типография Министерства здравоохранения СССР
МЕТОДИЧЕСКИЕ УКАЗАНИЯ ПО СТЕРИЛИЗАЦИИ НЕКОТОРЫХ ГЕМОСОРБЕНТОВ21. Общие положения
1.1. Настоящие методические указания предназначены для разработчиков и изготовителей гемосорбентов, а также для специалистов лечебно-профилактических учреждений, применяющих новый метод детоксикационной терапии — метод гемосорбции при лечении некоторых заболеваний и отравлений, а также для работников санитарно-эпидемиологических и дезинфекционных станций, осуществляющих контроль за соблюдением асептики и стерилизации.
1.2. Гемосорбенты — инертные поглотители с большой удельной поверхностью (активированые угли, ионообменные смолы и др.), используемые для удаления из крови токсических веществ эндогенной и экзогенной природы при непосредственном контакте с кровью больного в процессе гемосорбции.
1.3. Гемосорбенты относятся к изделиям медицинского назначения, которые подлежат обязательной стерилизации перед применением-
УТВЕРЖДАЮ Начальник Управления по внедрению новых лекарственных средств и медицинской техники Минздрава СССР
УТВЕРЖДАЮ Зам. начальника Главного управления
карантинных инфекций Минздрава СССР
О. Г. Имамалисв 28 декабря 1983 г.
Hi 28-6/5
Э. А. Бабаян 26 января 1984 г.
СССР.
1.4. На эффективность стерилизации изделий значительное влияние оказывает массивность их инициальной (исходной) контаминации, поэтому в процессе подготоки гемосорбентов к гемосорбции до стерилизации следует предохранять их от обсеменения микроорганизмами, что достигается созданием соответствующих санитарно-гигиенических условий.
1.5. Поскольку инициальная контаминация изделий формируется не только микроорганизмами, содержащимися в сырьевых материалах, но также и микроорганизмами, обсеменяющими руки, технологическую одежду персонала, воздух, поверхности производственных помещений и оборудования, для ограничения инициальной контаминации гемосорбентов на предприятиях — изготовителях необходимо проведение комплекса мероприятий, включающего достаточный набор, рациональную планировку и оснащение производственных и вспомогательных помещений, правильный режим работы персонала, эффективную деконтаминацию помещений, оборудования, технологической одежды.
1.6. Комплекс мероприятий по обеспечению требуемых санитарно-гигиенических условий на предприятиях, в цехах и на участках, выпускающих стерильные гсмосорбенты, должен быть разработан с учетом требований и особенностей технологического процесса изготовления конкретного гемосорбента.
1.7- Контроль обсемененности микроорганизмами объектов. перечисленных в п. 1,5., обязано обеспечить предприятие — изготовитель гемосорбентов первоначально не реже j раза в неделю, а в дальнейшем после достижения стабильного уровня микробной обсемененности соответствующего установленным нормам для каждого объекта (п. 1.8.), не реже 1 раза в месяц.
1.8. Допустимый уровень микробной обсемененности для каждого из объектов, перечисленных в п- 1.5., соответствует следующему количеству микробных клеток:
- для кожи рук персонала — 200 микробных клеток (м.к.) па одну кисть руки (метод смыва);
- для одежды персонала — не более 10 м.к./см2;
- для воздуха помещении — пс более 200 м.к./мл (аспирационный метод с помощью аппарата Кротова);
— для поверхностей оборудования помещений — не более 5 м.к./см2;
— для поверхности пола — 25 м.к./см2.
1.9. Контроль микробной обссмеипостн объектов, перечисленных в п. 1.5., проводят в соответствии с «Методикой оценки санитарно-гигиенического состояния на предприятиях, выпускающих радиационно стерилизуемую продукцию медицинского назначения» № 2534-82 от 11.02.82 г., утвержденной Минздравом СССР*
2. Стерилизация гемосорбентов
2.1. Стерилизацию гсмосорбситоп, применяемых для целей гемосорбции, проводят в условиях промышленного пред-
приятия. В отдельных случаях (по решению Минздрава СССР в установленном порядке) допускается стерилизация гемосорбентов в лечебно-профилактических учреждениях.
2.2. Стерилизация должна быть заключительным этапом в процессе подготовки гемосорбентов к гемосорбции.
2.3- Для стерилизации гемосорбентов в промышленных условиях может быть использован радиационный метод (с применением гамма-излучения), а также паровой метод с применением водяного насыщенного пара при избыточном давлении.
2.4. В лечебно-профилактических учреждениях стерилизацию гемосорбентов в упаковке осуществляют водяным насыщенным 11 а ром при избыточном давлении в паровом стерилизаторе.
2.5. Гемосорбенты подвергают стерилизации в колонке, флаконе, массообменнпке и защитных упаковках, предохраняющих поверхность колонки, флакона от повторного обсеменения микроорганизмами в процессе хранения и транспортировки.
2.6. Гемосорбенты марок СКТ-7а, КАУ-1, КАУ-2, ГСУ, СКН, ГС-01 стерилизуют паровым и радиационным ( методами;
— паровым методом при температуре 120° С в течение 45 минут (для колонок объемом до 200 мл) и температуре 126° С в течение 30 минут (для колонок объемом 200—500 мл);
— радиационным методом — при использовании гамма-излучения в дозе 25 к Гр.
2.7. Приведенные в п. 2.6. режимы стерилизации эффективны при инициальной контаминации гемосорбентов, не превышающей I06 микробных клеток на I г сорбента.
Определение инициальной контаминации гемосорбентов до стерилизации проводит бактериологическая лаборатория предприятия или лечебно-профилактического учреждения, где осуществляется стерилизация гемосорбентов в соответствии с методикой, изложенной в и. 2.9.
2.8. Гемосорбенты, перечисленные в п. 2.6., стерилизованные указанными методами, нетоксичны.
2.9. Методика и техника определения инициальной контаминации гемосорбентов.
2.9.1. Инициальную контаминацию определяют в микробиологическом боксе или в настольном боксе, находящемся в обычном лабораторном помещении.
Подготовка бокса, инструментов и персонала к работе проводится в соответствии с н. 2-2. Приложения № 6 к приказу Минздрава СССР № 60 от 17 января 1979 г.
2.9.2. Поверхность стола, чашки весов обрабатывают 6^«
5
раствором перекиси водорода, выдерживают в течение 30 минут, готовят стерильный лоток и инструмент для вскрытия упаковки (колонки, флакона) гемосорбента.
2.9.3. Вскрывают защитную упаковку, протирают поверхность колонки, флакона б°/« раствором перекиси водорода, оставляют ее на стерильном лотке на 30 минут.
2-9.4. Колонку, флакон вскрывают стерильным инструментом и с помощью стерильной ложки берут навеску гемосорбента около 1 г (не менее 3-х проб, отобранных, по возможности, на разном уровне в колонке, флаконе). Навеску помещают в К) мл стерильного физиологического раствора, налитого в стерильную широкогорлую пробирку с бусами, и встряхивают в течение 10 минут.
2.9.5. Посев смывной жидкости производят в количестве 0,5—1,0 мл в глубь казеинового или мясопептонного агара (для определения общего количества микрофлоры) и 0,1 мл — на поверхность агара (для определения видового состава микрофлоры).
После инкубации посевов в термостате в течение 48 часов производят подсчет выросших колоний и пересчет количества микроорганизмов на 1 г сорбента.
3. Контроль стерильности гемосорбентон
3.1. Контроль стерильности гемосорбептов, стерилизуемых на предприятии, должна осуществлять бактериологическая лаборатория данного предприятия, а гемосорбептов, стерилизуемых в условиях лечебно-профилактических учреждений; — бактериологическая лаборатория учреждения, в котором осуществляется их стерилизация, не реже 1 раза в месяц, а также бактериологическая лаборатория санитарно-эпидемиологической станции, не реже 2 раз в год* Стерильность материалов и инструментов, используемых при подготовке гемосорбентов к гемосорбции, а также обсемеиенность микроорганизмами воздуха боксированного помещения, предназначенного для подготовки гемосробентов к гемосорбции, контролируют бактериологические лаборатории лечебно-профилактических учреждений и санитарно-эпидемиологических станций с указанной выше кратностью.
Контроль стерильности гемосорбентов проводят при условиях, исключающих возможность вторичной контаминации, в специально оборудованных помещениях с соблюдением правил асептики.
Мероприятия, обеспечивающие асептические условия при посевах, проводятся в соответствии с п. 2 Приложения № б к приказу Министерства здравоохранения СССР № 60 от 17.01.1979 г.
о
3.2. Отбор проб гемосорбентов, стерилизуемых радиационным методом, проводят согласно п. 2 Приложения к приказу Минздрава СССР и Минмедпрома № 964/410 от 17.09-1979 г.
Отбор проб гемосорбентов, стерилизуемых паровым методом в условиях предприятия-изготовителя, производят из каждой серии изделий, подвергнутых обработке за один цикл в одном стерилизаторе, из разных точек стерилизатора. Максимальное количество проб, отбираемых для первичного посева при паровом методе стерилизации —13. Общее количество проб расчитывают по формуле 0,4 Vn, где п — количество изделий в серии. Кроме изделий, направленных непосредственно па анализ, отбирают также дубликаты в тройном количестве: две части из них используют в случае необходимости для повторного контроля, одну часть оставляют для арбитражного хранения. При отсутствии роста в первичных посевах дубликаты, предназначенные для повторного контроля, подлежат реализации. При отборе проб следует руководствоваться таблицей, указанной в приложении I.
Отбор проб гемосорбентов, стерилизуемых паровым методом в условиях лечебно-профилактического учреждения, имеющего централизованное стерилизационное отделение, проводят в количестве не менее 1"/о от числа одновременно про-стерилизованных изделий.
В лечебно-профилактических учреждениях, не имеющих централизованных стерилизационных отделений и осуществляющих стерилизацию в хирургических отделениях, контролю стерильности подлежат не менее 3 упаковок гемосорбентов (колонок, флаконов), подготовленных для гемосорбции.
33. Методика и техника посева гемосорбентов.
3.3.1. Посев гемосорбснта осуществляют два специалиста (бактериолог и лаборант).
3.3.2. В предбокснике с колонки, флакона удаляют защитную упаковку и поверхность колонки протирают с помощью пинцета стерильной салфеткой, смоченной 6% раствором переписи водорода, оставляют на стерильном лотке в течение 30 минут, затем колонку, флакон вместе с лотком вносят в бокс ,где ее вскрывают стерильным инструментом.
3.3.3. Отбор проб содержимого колонки, флакона производят с помощью специально для этих целей изготовленного мерного пробоотборника (в виде ложки или небольшого цилиндра с держателем), позволяющего отобрать пробу (взвесь гемосорбента в изотоническом растворе хлорида натрия) объемом около 2 мл.
7
Отобранные пробы помещают в пробирки с питательными средами.
3.4. Для контроля стерильности применяют следующие питательные среды: тиогликолевую среду, среду Сабуро, сахарный бульон Хоттингера с содержанием 1°/о глюкозы — при контроле стерильности гемосорбентов* стерилизованных ра-диационным методом, и с содержанием глюкозы — при
контроле стерильности изделий, стерилизованных паровым методом. Посев производят не менее, чем в две пробирки с каждой из названных питательных сред. Посевы в бульон Хоттингера и тиогликолевую среду выдерживают в термостате при температуре 32°С, в среду Сабуро — при температуре 22° С. Срок инкубации посевов после стерилизации радиационным методом — 14 суток, паровым — 8 суток.
3-5. Учет результатов посева гемосорбентов на стерильность после стерилизации радиационным методом проводят согласно п. 2 приложения к приказу Минздрава СССР • Мннмедпрома № 964/410 от 17.09.1979 г.
Учет результатов посева гемосорбсптов, стерилизованных паровым методом, проводят после 8 суток их культивирования в термостате.
При отсутствии роста микроорганизмов во всех средах выдают заключение о стерильности серии гсмосорбентов.
При прорастании питательной среды хотя бы в одной пробирке проводят повторный контроль стерильности удвоенного количества образцов данной серии. Если при повторном посеве новых образцов прорастание не наблюдается, то исследуемую серию считают стерильной.
В случае прорастания посевов (помутнение питательной среды, образование пленки, осадка) готовят мазки для бак-териоскопического подтверждения роста микробов. При паровом методе стерилизации рост в единичных пробирках вегетативной микрофлоры не учитывают, его относят за счет mieceniия этой микрофлоры в процессе посева, материал подлежит повторному исследованию.
Результаты бактериологического контроля гсмосорбентов па стерильность отмечают и журнале: «стерильно* или «не
стерильно».
3.(3. В процесс посева в боксе регулярно проверяют обсе-мененность воздуха. Для этого на рабочий стол ставят 2 чашки с питательным агаром, открывая их на 15 минут, затем чашки помещают в термостат при температуре 37° С на 48 часов.
Допускается рост не более трех колоний неспорообразующих сапрофитов, рост спорообразующих микроорганизмов не допускается.
В случае нарушении указанных требований проведение дальнейших работ в данном боксе запрещается, в нем до-8
полнитсльно проводят тщательную обработку 6°^ раствором перекиси водорода с 0,5% моющих средств: Астра, Лотос,
Прогресс.
4. Требования, предъявляемые к помещению для подготовки гемосорбентов к гемосорбции
4.1. В тех случаях, когда после стерилизации гемосорбенты подвергают последующей обработке при подготовке к гемосорбции с целью отмывки их от разрушенных гранул, эту работу проводят в асептических условиях в специально оборудованном боксированном помещении или в чистой операционной.
4.2. В боксированном помещении предусматривают:
— приточно-вытяжную вентиляцию с подачей стерильного воздуха (с преобладанием на 15°/» притока над вытяжкой), прошедшего через бактериальные фильтры с материалом Петрянова;
— отделку стен керамической плиткой или окраску их масляной краской на всю высоту, потолка — масляной краской, покрытие пола мозаичное, а также керамической плиткой или антистатическим линолеумом, покрытие рабочих столов стеклом или пластиком;
— размещение на высоте 2—2,5 м от пола настенных и потолочных ультрафиолетовых облучателей (БОН, ОБП) из расчета 2 вт удельной мощности ламп, создающих прямое излучение на 1 м3 помещения.
4.3. Подготовку гсмосорбентов к гемосорбции в чистой операционной проводят вне операций специально выделенным для этой работы персоналом в отсутствии посторонних лиц.
4.4. Перед проведением работы в помещении бокса илй операционной обрабатывают все поверхности (стены, пол, оборудование) 3% раствором перекиси водорода с 0,5"/*. моющих средств, перечисленных в п. 3.6. В случае обнаружения в воздухе бокса грибов или спорообразующих бактерий проводят влажную уборку (>'%• раствором перекиси водорода с 0,5% одного из названных моющих средств. Способ приготовления рабочих растворов перекиси водорода с моющим сред-ством указан в приложении 2. За 1,5—2 часа до начала работы включают бактерицидные облучатели на 1,5—2 часа.
4.5. В помещении, где проводят подготовку гем «сорбентов к гемосорбции, регламентируют микробную обссменен-ность воздуха:
— до начала работы в I м:1 воздуха допускается не более 200 микробных клеток общей микрофлоры; золотистого
<)
стафилококка, спорообразующих бактерии и грибов до работы быть ие должно.
4.6. Отбор проб воздуха аспирационным методом с помощью аппарата Кротова, их обработку и учет осуществляют в соответствии с п. 1.9.
4.7. Перед входом в бокс (операционную) персонал, проводящий подготовку гемосорбентов к гемосорбции, осуществляет мероприятия, обеспечивающие асептические условия работы: моет и обрабатывает руки антисептиками, надевает стерильную одежду: пижаму, тапочки, шапочку, халат, стерильные резиновые перчатки, которые каждые 30 минут ополаскивает в антисептике и вытирает стерильной салфеткой-
4.8. Для обработки рук используют различные антисептики, разрешенные Фармакологическим комитетом Министерс! ва здравоохранения СССР: рецептуру С-4, хлоргексидин биглюконат (гибитаи), дегмин, дегмицид, йодогжрон, церигель.
Перед обработкой рекомендуемыми препаратами руки моют проточной водой, щеткой и мылом в течении 1 минуты (при использовании рецептуры С-4 — без щетки) после чего насухо вытирают стерильной салфеткой. Способ применения перечисленных антисептиков указан в приложении 3.
4.9. Инструменты, посуду, спецодежду, используемые в ра
боте, предварительно стерилизуют: металлические, стеклянные, текстильные изделия водяным насыщенным паром при избыточном давлении при температуре 132° С в течение 20 минут; изделия из резины (перчатки и т. д.) при температуре 120° С в течение 45 минут; изделия из нетермостойких, но коррозионностойких материалов и пластмасс — погружением в 6% раствор перекиси водорода иа 360 минут при температуре не ниже 18° С и на 180 минут при температуре не ниже 50° С, в 1% раствор дезоксона=1 (по надуксусной кислоте) — на 45 минут (температура не ниже
18° С). После стерилизации перекисью водорода и дезоксо-ном= 1 изделия промывают стерильной водой (после дезоксоиа-1 — трижды).
4.10. Применяемые для промывки гемосорбентов жидкости (физиологический раствор, дистиллированная вода, водопроводная вода) в емкостях, имеющих объем нс более 1000 mjk, стерилизуют в паровом стерилизаторе при температуре 120° С в течение 45 минут.
5. Меры предсторожности при работе с растворами перекиси водорода
5.1. К работе с растворами перекиси водорода при создании асептических условий в боксированном помещении
10
1
Инструктаж и» рабочем месте (первичный, повторны», («неплановый, текущий) регистрируется в журнале инструктажа в соответствии с Приложением № 5 к приказу Министра здравоохранения СССР от 30 августа 1982 г. № 862 «О мерах по дальнейшему улучшению охраны труда и техники безопасности п органах, учреждениях, организациях и на предприятиях системы Министерства здравоохранения СССР».
11
2
Методические указания разработаны: Всесоюзным научно-исследовательским институтом дезинфекции и стерилизации Минздрава СССР, Вторым Московским ордена Ленина Государственным медиицнеким институтом им. Н. И. Пирогова Минздрава РСФСР, Всесоюзным научно-исследовательским и испытательным институтом медицинской техники Минздрава СССР, Московским химико технологическим институтом нм. Д. И. Менделеева Министерства высшего и среднего специального образования
3