Методика зарегистрирована в Федеральном реестре методик выполнения измерений, применяемых в сферах распространения государственного метрологического контроля и надзора (регистр, код ФР. 1.31.2008.04296)
МУ 08-47/215
(по реестру аккредитованной метрологической службы Томского политехнического университета)
ВИНА ВИНОГРАДНЫЕ, ПЛОДОВЫЕ И ВИНОМАТЕРИАЛЫ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ ЛИМОННОЙ КИСЛОТЫ МЕТОДОМ ПОТЕНЦИОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
Редакция. №2 (с изменениями)
ТОМСК5.2 Требования к квалификации операторов
Измерения может проводить химик-аналитик, владеющий техникой потенциометрического анализа и изучивший инструкции по эксплуатации используемой аппаратуры.
5.3 Условия выполнения измерений
Измерения проводят в нормальных лабораторных условиях:
• Температура окружающего воздуха (25 ± 10) °С;
• Атмосферное давление (97 ± 10) кПа;
• Относительная влажность не более 80 %;
• Частота переменного тока (50 ± 5) Гц;
• Напряжение в сети (220 ± 22) В.
6 ОТБОР И ХРАНЕНИЕ ПРОБ
Отбор, консервацию и хранение проб вина и виноматериала проводят в соответствии с ГОСТ или другим конкретным нормативным документом, регламентирующим отбор проб конкретных видов и типов: например, по ГОСТ Р 51144. При отборе проб составляется сопроводительный документ по утвержденной форме.
Пробы вина и виноматериала хранят в темных бутылках или под темным колпаком в холодильнике.
7 СРЕДСТВА ИЗМЕРЕНИЙ, ВСПОМОГАТЕЛЬНОЕ ОБОРУДОВАНИЕ, ПОСУДА, РЕАКТИВЫ И МАТЕРИАЛЫ
При проведении количественного химического анализа применяют следующие средства измерений, вспомогательное оборудование, посуду, материалы и реактивы:
7.1 Средства измерений и вспомогательное оборудование
7.1.1 Мономер ИК-1 илидр.по ГОСТ 27987.
Допускается использовать другое оборудование и приборы, позволяющие воспроизводить технические и метрологические характеристики, указанные в данной методике анализа.
7.1.2 В состав иономера ИК-1 входят:
- электроды:
• индикаторный электрод - медный электрод, состоящий из медного стержня диаметром 1,5-2,0 мм и длиной рабочей части 8-12 мм;
• электрод сравнения - хпоридсеребряный электрод, заполненный насыщенным раствором хлорида калия, с сопротивлением не более 3,0 кОм по ГОСТ 17792;
- сменная ячейка (стаканчики из стекла вместимостью 20 - 50 см3);
11
-магнитная мешалка и вращающийся железный стержень в изоляции.
7.1.3 Весы лабораторные по ГОСТ 24104, с наибольшим пределом взвешивания 210 г и ценой деления 0,1 мг.
7.1.4 Набор гирь Г-2-200 по ГОСТ 7328.
7.1.5 Дозаторы типа ДП-1-5-40 или ДП-1-20-200 или ДП-1-200-1000 с дискретностью установки доз 1,0 - 3,0 мкл и погрешностью не более 5 % отн.
7.2 Посуда
7.2.1 Пипетки мерные лабораторные стеклянные 2-го класса точности вместимостью 0,5; 1,0; 2,0; 5,0 см3 по ГОСТ 29227 и ГОСТ 29169.
7.2.2 Посуда мерная лабораторная стеклянная 2-го класса точности по ГОСТ 1770: колбы вместимостью 25,0; 50,0; 100,0; 250,0 см3, цилиндры вместимостью 25,0 см3.
7.2.3 Палочки стеклянные по ГОСТ 21400.
7.2.4 Воронки лабораторные стеклянные по ГОСТ 25336.
7.2.5 Колонки стеклянные ионообменные диаметром 15 мм, высотой 250 - 300 мм (в качестве колонок можно использовать бюретки вместимостью 50 см3 диаметром 12-15 мм).
7.3 Реактивы и материалы
7.3.1 Калий хлористый по ГОСТ 4234.
7.3.2 Натрия гидроокись по ГОСТ 4328.
7.3.3 Кислота соляная по ГОСТ 30553 или по [1].
7.3.4 Медь сернокислая 5-водная по ГОСТ 4236.
7.3.5 Вода бидистиллированная по [2] или дистиллированная по ГОСТ 6709, перегнанная в присутствии серной кислоты по ГОСТ 4204 и калия марганцовокислого по ГОСТ 20490 (0,5 см3 концентрированной серной кислоты и 3,0 см3 3%-ного раствора перманганата калия на 1,0 дм3 дистиллированной воды).
7.3.6 Фенолфталеин по [3] приготовленный по ГОСТ 4919.1.
7.3.7 Бура по ГОСТ 8429.
7.3.8 Кислота лимонная моногидрат и безводная по ГОСТ 3652.
7.3.9 Бумага индикаторная универсальная [4].
7.3.10 Бумага фильтровальная по ГОСТ 12026.
7.3.11 Натрий двууглекислый (пищевая сода) по ГОСТ 2156.
7.3.12 Калий марганцовокислый по ГОСТ 20490.
7.3.13 Шприц медицинский, вместимостью 2 см3 по ГОСТ 24861
7.3.14 Анионит АВ -17-8 или другой анионит данной группы по ГОСТ 20301.
7.3.15 Калий роданистый по ГОСТ 4139.
Все реактивы должны быть квалификации ОСЧ, ХЧ или ЧДА.
8 ПОДГОТОВКА К ВЫПОЛНЕНИЮ ИЗМЕРЕНИЙ
При подготовке к выполнению измерений проводят следующие этапы работы:
- подготовка приборов к работе по 8.1,
- проверка и подготовка лабораторной посуды по 8.2,
- подготовка индикаторного электрода и электрода сравнения по 8.3,
- приготовление основных и вспомогательных растворов по 8.4,
- подготовка анионообменной колонки по 8.5,
- подготовка проб по 8.6.
8.1 Подготовка приборов к работе
Подготовку и проверку иономера ИК-1 или другого средства измерения проводят в соответствии с инструкцией по эксплуатации, «Руководством пользователя» и техническим описанием соответствующего прибора.
8.2 Проверка и подготовка лабораторной посуды
Лабораторную стеклянную посуду, сменные наконечники дозаторов, пипетки протирают фильтром с питьевой содой, промывают многократно дистиллированной водой и высушивают.
8.3 Подготовка электродов
8.3.1 Подготовка индикаторного (рабочего) медного электрода
Медный электрод представляет собой медный стержень диаметром 1,5-2,0 мм, запрессованный во фторопластовую трубку диаметром 5-6 мм так, чтобы длина выступающей части медного стержня (рабочей поверхности меди) составляла 8-12 мм (поставляется потребителю в готовом виде).
Для подготовки электрода к работе рабочую поверхность медного электрода выдерживают 5-10 с в растворе соляной кислоты концентрации 0,1 моль/дм3, промывают бидистиллированной водой и зачищают фильтровальной бумагой.
По мере необходимости (при снижении чувствительности и повторяемости, после долгого перерыва между анализами) медный электрод подвергают механической обработке. Для этого электрод промывают в растворе соляной кислоты концентрации 0,1 моль/дм3 с последующей зачисткой поверхности электрода фильтровальной бумагой.
Между анализами электрод хранят в сухом виде на воздухе.
13
8.3.2 Подготовка к работе электрода сравнения
В качестве электрода сравнения используют хлоридсеребряный электрод (ХСЭ).
ХСЭ представляет собой спираль из серебряной проволоки, покрытой хлоридом серебра, помещенную в корпус с полупроницаемой пробкой. Корпус заполнен насыщенным раствором хлорида калия. Конец серебряной проволоки имеет токовыводящий контакт для подключения к прибору (поставляется потребителю в готовом виде).
Перед работой корпус электрода заполняют с помощью дозатора или шприца насыщенным раствором калия хлорида, закрывают и выдерживают не менее 12 час (при первом заполнении) в насыщенном растворе хлорида калия для установления равновесного значения потенциала электрода. Сопротивление ХСЭ не должно быть более 3,0 кОм
Заполнение электрода производят не реже одного раза в 2 недели.
Хранят электроды в насыщенном растворе хлорида калия.
8.4 Приготовление растворов
8.4.1 Раствор буры концентрации 0,05 моль/дм3
Для приготовления 100,0 см3 раствора буры концентрации 0,05 моль/дм3 берут навеску буры (Na2B4O7-10 Н20) массой 1,907 г с точностью до 0,001 г, вносят в мерную колбу объемом 100,0 см3. Добавляют 30-40 см3 бидистиллированной воды и тщательно перемешивают для растворения. Объем раствора доводят бидистиллированной водой до метки и перемешивают.
8.4.2 Боратный буферный раствор с pH 8,5
Для приготовления по ГОСТ 4919.2 боратного буферного раствора с pH 8,5 в мерную колбу вместимостью 200 см3 пипеткой вносят 130,5 см3 раствора буры концентрации 0,05 моль/дм3, добавляют 30-40 см3 соляной кислоты концентрации 0,1 моль/дм3 и тщательно перемешивают. Объем раствора доводят до метки соляной кислотой концентрации 0,1 моль/дм3 и перемешивают.
8.4.3 Раствор лимонной кислоты концентрации 100,0 г/дм3
Для приготовления исходного раствора лимонной кислоты концентрации 100,0 г/дм3 навеску лимонной кислоты 10,000 г, взятую с точностью до 0,002 г, помещают в мерную колбу вместимостью 100 см3, добавляют 25 - 30 см3 бидистиллированной воды и тщательно перемешивают до полного растворения. Объем раствора доводят бидистиллированной водой до метки и перемешивают.
8.4.4 Раствор лимонной кислоты концентрации 10,0 г/дм3
Для приготовления разбавленного (1:10) раствора лимонной кислоты (10,0 г/дм3) 10,0 см3 исходного раствора лимонной кислоты концентра-
14
ции 100,0 г/дм3 помещают в мерную колбу вместимостью 100,0 см3, добавляют 30-40 см3 бидистиллированной воды и тщательно перемешивают. Объем раствора доводят бидистиллированной водой до метки и перемешивают.
8.4.5 Раствор сульфата меди концентрации 0,1 моль/дм3
Для приготовления 100,0 см3 раствора сульфата меди концентрации 0,1 моль/дм3 берут навеску CuS04-5H20 массой 2,495 г с точностью до 0,001 г, вносят в мерную колбу объемом 100,0 см3. Добавляют 30 -40 см3 бидистиллированной воды и тщательно перемешивают до полного растворения. Объем раствора доводят бидистиллированной водой до метки и перемешивают.
8.4.6 Раствор сульфата меди концентрации 0,05 моль/дм3
Для приготовления раствора сульфата меди концентрации 0,05 моль/дм3 исходный раствор сульфата меди по 8.4.5 разбавляют в 2 раза. Для этого в колбу объемом 100,0 см3 вносят 50,0 см3 раствора сульфата меди концентрации 0,1 моль/дм3 добавляют 30-40 см3 бидистиллированной воды и тщательно перемешивают. Объем раствора доводят бидистиллированной водой до метки и перемешивают.
8.4.7. Насыщенный раствор хлорида калия (для заполнения электрода сравнения)
Для приготовления насыщенного раствора хлорида калия хлористый калий растворяют в бидистиллированной воде до насыщения.
8.4.8 Соляную кислоту перегоняют при температуре 120 °С. Перегнанная соляная кислота должна быть концентрации не менее 6 моль/дм3.
8.4.9 Раствор соляной кислоты концентрации 2,0 моль/дм3
Для приготовления раствора соляной кислоты концентрации 2,0 моль/дм3 в мерную колбу вместимостью 100 см3, наполовину заполненную бидистиллированной водой, вносят 33,3 см3 раствора соляной кислоты концентрации 6 моль/дм3, затем доводят объем раствора бидистиллированной водой до метки.
8.4.10 Раствор соляной кислоты концентрации 0,1 моль/дм3
Для приготовления раствора соляной кислоты концентрации 0,1 моль/дм3 в мерную колбу вместимостью 100 см3 вносят 5,0 см3 раствора соляной кислоты концентрации 2,0 моль/дм3, добавляют 30-40 см3 бидистиллированной воды и тщательно перемешивают. Затем доводят объем раствора до метки бидистиллированной водой.
15
8.4.11 Раствор гидроксида натрия концентрации 3,5 моль/дм3
Для приготовления раствора гидроксида натрия концентрации 3,5 моль/дм3 берут навеску гидроксида натрия 14,00 г с точностью до 0,02 г и помещают в мерную колбу вместимостью 100 см3, добавляют 30 - 40 см3 дистиллированной воды и тщательно перемешивают до полного растворения. Объем раствора доводят дистиллированной водой до метки и перемешивают.
8.4.12 Насыщенный раствор хлорида натрия (для подготовки к работе ионообменной колонки)
Для приготовления насыщенного раствора хлорида натрия хлористый натрий растворяют дистиллированной водой до насыщения.
8.4.13 Раствор калия роданистого концентрации 10,0 г/дм3 (для подготовки к работе ионообменной колонки)
Для приготовления раствора калия роданистого концентрации
10.0 г/дм3 навеску роданистого калия 1,0 г, взятую с точностью до 0,002 г, помещают в мерную колбу вместимостью 100 см3, добавляют 25,0 -
30.0 см3 дистиллированной воды и тщательно перемешивают до полного растворения. Объем раствора доводят дистиллированной водой до метки и перемешивают.
8.4.14 Раствор натрия гидроокиси концентрации 0,2 моль/дм3 (для подготовки к работе ионообменной колонки)
Для приготовления раствора натрия гидроокиси концентрации 0,2 моль/дм3 навеску натрия гидроокиси 0,8 г, взятую с точностью до 0,002 г, помещают в мерную колбу вместимостью 100 см3, добавляют 25 -30 см3 дистиллированной воды и тщательно перемешивают до полного растворения. Объем раствора доводят дистиллированной водой до метки и перемешивают.
8.5 Подготовка анионообменной колонки
8.5.1 Подготовка анионообменной колонки
Подготовка анионообменной колонки проводится с целью отмывания анионита от неорганических низкомолекулярных примесей и зарядки анионита в нужную хпоридную форму.
Навеску анионита АВ-17-8 (мелкая фракция) массой 5,0 г, взятой с точностью до 0,2 г, помещают в стакан вместимостью 50 - 100 см3, заливают 40 см3 насыщенного раствора хлористого натрия и выдерживают 24 час при комнатной температуре. Раствор сливают и помещают часть набухшей смолы в колонку слоем высотой 100 - 150 мм. При полностью открытом кране колонки анионит промывают раствором соляной кислоты 16
концентрации 2,0 моль/дм3 до полного удаления железа, следя, чтобы пузырьки воздуха не задерживались между зернами смолы. Наличие ионов железа контролируется с помощью реакции с калием роданистым: при добавлении к раствору, содержащему ионы Fe3+, раствора калия роданистого концентрации 10 г/дм3 появляется интенсивная кроваво-красная окраска роданида железа(Ш).
Затем через колонку с анионитом пропускают дистиллированную воду до нейтральной среды, контролируя значения pH с помощью индикаторной бумаги.
Затем анионит в колонке промывают (примерно 50,0 см3) раствором натрия гидроокиси концентрации 0,2 моль/дм3 для удаления из смолы мономеров. После этого анионит вновь промывают дистиллированной водой до нейтральной реакции элюата (по индикаторной бумаге должно быть значение pH 6,0).
Для перевода анионита в активную хлоридную форму через колонку пропускают раствор соляной кислоты концентрации 2,0 моль/дм3 объемом 30-40 см^ со скоростью 1 -2 капли в секунду. Затем отмывают би-дистиллированной водой (100- 150 см3) от избытка кислоты до нейтральной реакции элюата (по индикаторной бумаге значение pH 6,0). После этого анионит готов к работе.
8.5.2 Регенерация анионообменной колонки
Регенерацию анионообменной колонки проводят после подготовки пробы к измерению, т.е. по окончании отделения лимонной кислоты от сопутствующих кислот пробы, а также в случае получения неудовлетворительных результатов анализа (завышенных или заниженных результатов по контрольной пробе методом «введено-найдено»).
Анионит регенерируют промыванием дистиллированной водой до слабокислой реакции промывной жидкости (по индикаторной бумаге значение pH 5,0), затем пропусканием 100,0 см3 раствора соляной кислоты концентрации 0,1 моль/дм3.
После чего колонку отмывают бидистиллированной водой (100-150 см3) от избытка кислоты до нейтральной реакции элюата (по индикаторной бумаге значение pH 6,0). После этого анионит вновь готов к работе.
Хранят колонку с анионитом, залив смолу бидистиллированной водой.
17
8.6 Подготовка проб
Для анализа используют две параллельные пробы.
Для подготовки проб берут анализируемую пробу вина или винома-териала объемом 10,0 см3 (Vnp) с помощью пипетки с точностью до 0,01 см3, подщелачивают 0,02-0,05 см3 раствора натрия гидроокиси концентрации 3,5 моль/дм3 до pH 4 - 5 (значение pH контролируют с помощью индикаторной бумаги). После этого пробу вносят в колонку с подготовленным по разделу 8.5 к работе анионитом и пропускают со скоростью 1 капля в секунду. Элюат собирают в отдельную емкость и выливают. Затем промывают колонку с такой же скоростью бидистиллированной водой объемом 100 см3. Затем связанную с анионитом лимонную кислоту элюируют со скоростью 1 капля в секунду раствором соляной кислоты концентрации 0,1 моль/дм3 объемом 20,0 см3. Элюат подготовленной пробы собирают в мерную колбу вместимостью 25,0 см3 и доводят бидистиллированной водой до метки (Х/эл). Из отобранного элюата подготовленной пробы для потенциометрического титрования с помощью пипетки отбирают аликвоту объемом 5,0 - 10,0 см3 (Vaj1) с точностью до 0,01 см3.
Аналогично готовят вторую параллельную пробу.
9 ВЫПОЛНЕНИЕ ИЗМЕРЕНИЙ
Мономер ИК-1 или другое средство измерения должно быть предварительно подготовлено к работе в соответствии с «Руководством пользователя».
При выполнении потенциометрических измерений с использованием иономера или другого средства измерения по 7.1 для определения массовых концентраций лимонной кислоты выполняют следующие операции:
- устанавливают параметры измерений по 9.1;
- проводят проверку работы электрохимической ячейки по 9.2;
-проводят измерения при анализе подготовленной пробы по 9.3.
9.1 Установка параметров измерения
Режимы выполнения измерений выбирают в соответствии с требованиями руководства по эксплуатации прибора или паспорта.
9.2 Проверка работы электрохимической ячейки при определении массовой концентрации лимонной кислоты
Проверка работы электрохимической ячейки заключается в проверке работы рабочего медного электрода.
Проверку медного электрода проводят:
• после обработки электрода раствором соляной кислотой концентрации 0,1 моль/дм3 по 8.3.1;
• при неудовлетворительной повторяемости результатов анализа;
• после длительного перерыва в работе.
В чистый стаканчик объемом 50 см3 вносят пипеткой или дозатором 0,20 см3 раствора лимонной кислоты концентрации 10 г/дм3, добавляют 1 каплю фенолфталеина и нейтрализуют раствором натрия гидроокиси концентрации 3,5 моль/дм3 до появления малиновой окраски, после этого добавляют 2,0 см3 боратного буфера pH 8,5 и добавляют 10-15 см3 биди-стиллированной воды (чтобы раствор закрывал рабочую поверхность медного электрода). Поскольку при дальнейшем потенциометрическом титровании определяется не концентрация, а содержание (количество) лимонной кислоты, то объем раствора в стаканчике для титрования не имеет значения. Таким образом, получена контрольная проба с содержанием лимонной кислоты в аликвоте, равным 10 г/дм3.
Затем помещают стаканчик с контрольной пробой на магнитную мешалку, опускают в стаканчик рабочий медный электрод, электрод сравнения и стержень магнитной мешалки. Включают мешалку и титруют раствор контрольной пробы добавлением по 0,01...0,02 см3 раствора сульфата меди концентрации 0,1 моль/дм3. Записывают объемы раствора сульфата меди, пошедшего на титрование (VCu2+, см3), и замеренные по потенциометру значения потенциалов (Е, мВ), установившиеся во времени.
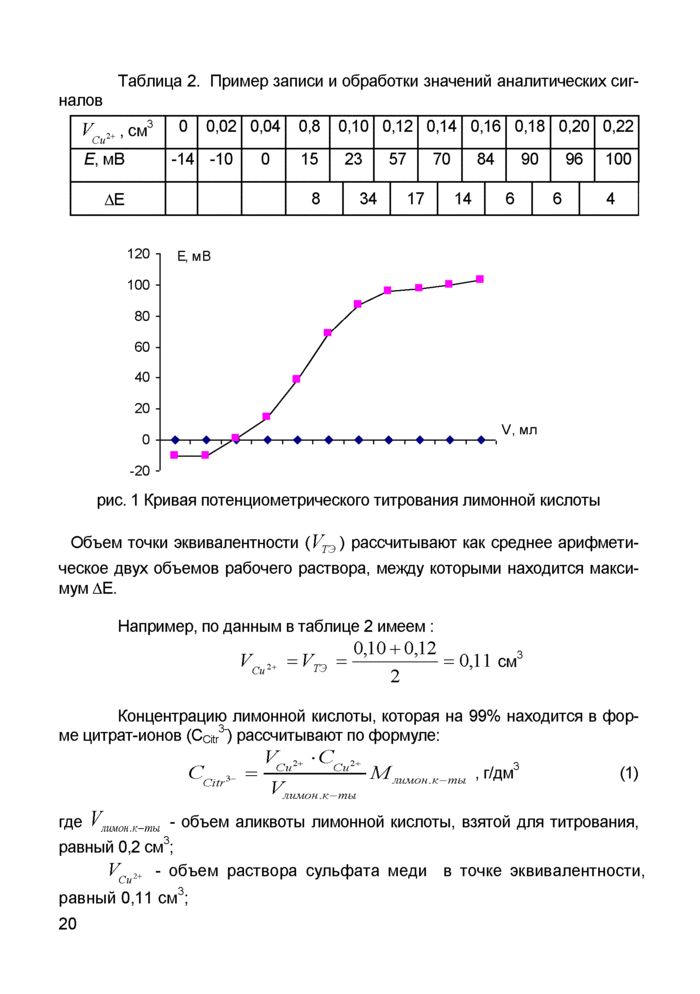
Данные вносят в таблицу 2 (приведен пример титрования). Титруют до получения 3 - 4 значений после резкого возрастания потенциала (см. рис.1). Если вместо увеличения происходит резкое уменьшение потенциала, то необходимо заменить электрод сравнения или индикаторный электрод.
Далее рассчитывают или АЕ и находят область максимума этих
значений. При равных объемах добавляемого реагента, AV, можно упростить расчет, используя вместо разность потенциалов АЕ.
19
налов
|
Таблица 2. Пример записи и обработки значений аналитических сиг |
|
VCu- ’ СМЗ |
0 |
0,02 |
0,04 |
0,8 |
0,10 |
0,12 |
0,14 |
0,16 |
0,18 |
0,20 |
0,22 |
|
Е, мВ |
-14 |
-10 |
0 |
15 |
23 |
57 |
70 |
84 |
90 |
96 |
100 |
|
АЕ |
|
|
|
8 |
34 |
17 |
14 |
6 |
6 |
4 |
|
рис. 1 Кривая потенциометрического титрования лимонной кислоты
Например, по данным в таблице 2 имеем :
0,10 + 0,12
Объем точки эквивалентности (VT3) рассчитывают как среднее арифметическое двух объемов рабочего раствора, между которыми находится максимум АЕ.
Концентрацию лимонной кислоты, которая на 99% находится в форме цитрат-ионов (Cat3") рассчитывают по формуле:
Ссир- = °CU" Млим0п.к- Г/ДМ3 (1)
у лимон.к—ты
где Кшон.к-ты" объем аликвоты лимонной кислоты, взятой для титрования,
равный 0,2 см3;
VCu2+ - объем раствора сульфата меди в точке эквивалентности, равный 0,11 см3;
20
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ЛО ОБРАЗОВАНИЮ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
АККРЕДИТОВАННАЯ МЕТРОЛОГИЧЕСКАЯ СЛУЖБА ТПУ
(аттестат об аккредитации № РОСС RU 01.00143-03 от 24.12.01)^
ООО «ВНЕДРЕНЧЕСКАЯ НАУЧНО-ПРОИЗВОДСТВЕННАЯ ФИРМА «ЮМХ»
СВИДЕТЕЛЬСТВО ОБ АТТЕСТАЦИИ МВИ № 08-47/215
Методика выполнения измерений массовой концентрации лимонной кислоты методом! потенциометрического титрования, разработанная в Томском политехническом университете И1 ООО «ВНПФ «ЮМХ» и регламентированная в МУ 08-47/215 (по реестру аккредитованной метрологической службы Томского политехнического университета)
ВИНА ВИНОГРАДНЫЕ, ПЛОДОВЫЕ И ВИНОМАТЕРИАЛЫ.МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ ЛИМОННОЙ КИСЛОТЫ МЕТОДОМ ПОТЕНЦИОМЕТРИЧЕСКОГО ТИТРОВАНИЯ,
аттестована в соответствии с ГОСТ Р 8,563 (ГОСТ 8,010).
Аттестация осуществлена по результатам теоретического и экспериментального исследования МВИ.
В результате аттестации МВИ установлено, что данная МВИ соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
|
1 Диапазон измерений, относительные значения показателей точности, повторяемости и воспроизводимости методики при доверительной вероятности Р=0,95 |
|
Наименование определяемого компонента |
Диапазон измеряемых концентраций, г/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости),
<7, , % |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости),
°v% |
Показатель точности (границы, в которых находится погрешность методики), 5,% |
|
Лимонная
кислота |
От 0,1 до 5,0 включ. |
5 |
10 |
20 |
|
3
CCu2+ - концентрация сульфата меди, используемого для титрования, равная 0,1 моль/дм3;
МШМОн.к-ты ~ молярная масса лимонной кислоты, равная 192,13 г/моль для реактива безводной лимонной кислоты.
В данном примере получена концентрация лимонной кислоты Cat3' равная:
С = °’11'0’1.192,13 = 10,54, г/дм3
сиг 0,2
Контрольный образец содержит количество лимонной кислоты в аликвоте, равное
Ccitr3' =10,00 г/дм3.
Работа медных электродов и электрохимической ячейки считается удовлетворительной при соответствии полученных результатов массовой концентрации лимонной кислоты с концентрацией введенной в пробу. При этом расхождение между результатом измерения и введенной концентрацией лимонной кислоты должно отличаться не более чем на 8%.
9.3 Измерения при анализе подготовленной пробы
В чистый стаканчик вносят пипеткой аликвоту подготовленной по 8.6 пробы объемом 5,0 - 10,0 см3 с точностью до 0,01см3. Добавляют 1 каплю фенолфталеина и нейтрализуют раствором натрия гидроокиси концентрации 3,5 моль/дм3 до появления малиновой окраски, после чего добавляют 2,0 см3 боратного буфера pH 8,5, и добавляют 10-15 см3 бидистиллиро-ванной воды (чтобы раствор закрывал рабочую поверхность медного электрода). Стаканчик с раствором помещают на магнитную мешалку, опускают в стаканчик рабочий медный электрод, электрод сравнения и стержень магнитной мешалки. Включают мешалку и титруют раствор пробы неизвестной концентрации лимонной кислоты раствором сульфата меди концентрации 0,05 моль/дм3, проводя операции аналогично 9.2.1.
Титрование в области скачка титрования раствором сульфата меди проводят малыми объемами с постоянным значением VCu2+ (по 0,01 или 0,02 см3), каждый раз записывают установившееся во времени значение потенциала (Е) в таблицу аналогично таблице 2 раздела 9.2.1. Титруют до получения 3 - 4 значений после резкого возрастания потенциала.
Рассчитывают точку эквивалентности (УТЭ) - объем раствора сульфата
меди, пошедшего на титрование цитрат-ионов, как указано в 9.2.1 для каждой из двух параллельных анализируемых проб; получают соответственно значения X? и Х2.
21
Продолжение свидетельства Ns 08-47/ 215
2 Диапазон измерений, значения предела повторяемости и воспроизводимости при доверительной вероятности Р=0,95
|
Определяемый
компонент |
Диапазон измеряемых концентраций, г/дмэ |
Предел повторяемости (для двух результатов параллельных определений), г |
Предел воспроизводимости (для двух результатов измерений),
R |
|
Лимонная кислота |
От 0,1 до 5,0 вкпюч. |
0,14 X |
0,28* X |
|
X - среднее арифметическое значение результатов параллельных определений массовой концентрации компонента. |
|
X - среднее арифметическое значение результатов измерений, полученных в двух разных лабораториях |
|
|
3 Дата выдачи свидетельства 1 декабря 2006 г |
Метролог метрологической службы ТПУ
Н.П.Пикула декабря 200 г.
«СОГЛАСОВАНО»
Главный метролог ТПУ
|
«СОГЛАСОВАНО» |
|
М.МЧухланцева 200 г. |
|
«УТВЕРЖДАЮ»
Директор ООО «ВНПФ «ЮМХ» |
|
«УТВЕРЖДАЮ»
Проректор по HP и И ТПУ |
|
ФЕДЕРАЛЬНОЕ АГЕНСТВО ПО ОБРАЗОВАНИЮ ГОСУДАРСТВЕННОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
«ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»АККРЕДИТОВАННАЯ МЕТРОЛОГИЧЕСКАЯ СЛУЖБА ТПУ
(аттестат аккредитации № РОСС RU 01.00143-03 от 22.02.08)
"УТВЕРЖДАЮ"
Проректор по HP и И
ООО «ВНЕДРЕНЧЕСКАЯ НАУЧНО-ПРОИЗВОДСТВЕННАЯ ФИРМА «ЮМХ»
"УТВЕРЖДАЮ"
Директор ООО «ВНПФ «ЮМХ»
Методика зарегистрирована в Федеральном реестре л применяемых в сферах распросп государственного метрологического контроля и надзора (регистр, код ФР. 1.31.2008.04296)
МУ 08-47/215
(по реестру аккредитованной метрологической службы Томского политехнического университета)
ВИНА ВИНОГРАДНЫЕ,ПЛОДОВЫЕ И ВИНОМАТЕРИАЛЫ.
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ ЛИМОННОЙ КИСЛОТЫ МЕТОДОМ ПОТЕНЦИОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
Редакция №2 (с изменениями)
«СОГЛАСОВАНО»
Метролог аккредитованной метрологической службы ТПУ
Н.П. Пикула сентября 2008 г.
Томск
6
1 НАЗНАЧЕНИЕ И ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий документ (МУ 08-47/215) устанавливает методику выполнения измерений массовой концентрации лимонной кислоты при анализе проб вин (плодовых и виноградных) и виноматериалов методом потенциометрического титрования.
Диапазон определяемых концентраций лимонной кислоты составляет от 0,1 до 5,0 г/дм3 включ.
Если содержание компонента в пробе выходит за верхнюю границу диапазона определяемых концентраций, допускается разбавление подготовленной к измерению пробы или уменьшение объема аликвоты анализируемой пробы.
Лимонная кислота С6Н807 (H3Citr) представляет собой трёхосновную органическую оксикислоту, имеющую универсальное распространение в живой природе. Она входит в состав вин и виноматериалов наряду с другими органическими кислотами и является одним из показателей при проведении экспертизы на предмет выявления фальсификации винной продукции (например, по ГОСТ Р 52523 «Вина столовые и виномате-риалы столовые. Общие технические условия»).
2 НОРМАТИВНЫЕ ССЫЛКИ
В настоящей методике использованы ссылки на следующие стандарты:
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Технические условия
ГОСТ 2156-76 Натрий двууглекислый. Технические условия ГОСТ 3652-69 Кислота лимонная моногидрат и безводная. Технические условия.
ГОСТ 4139-75 Калий роданистый. Технические условия
ГОСТ 4165-78 Медь (II) сернокислая 5-водная. Технические условия
ГОСТ 4234-77 Калий хлористый. Технические условия ГОСТ 4919.1-77 Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов
7
ГОСТ 4919.2-77 Реактивы и особо чистые вещества. Методы приготовления буферных растворов
ГОСТ 4328-77 Натрия гидроокись. Технические условия ГОСТ 6709-72 Вода дистиллированная. Технические условия ГОСТ 7328-2001 Гири. Общие технические условия ГОСТ 8429-77 Бура. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 14262-78 Кислота серная особой чистоты. Технические условия
ГОСТ 17792-72 Электрод сравнения хпорсеребряный насыщенный образцовый 2-го разряда
ГОСТ 20301-74 Смолы ионообменные. Аниониты. Технические условия
ГОСТ 20490-75 Калий марганцовокислый. Технические условия ГОСТ 21400-75 Стекло химико-лабораторное. Технические требования. Методы испытаний
ГОСТ 24104-2001 Весы лабораторные. Общие технические требования ГОСТ 24861-91 (ИСО 7886-84) Шприц инъекционный однократного применения
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 27869-88 Вещества особо чистые. Метод концентрирования микропримесей ионным обменом
ГОСТ 27987-88 Анализаторы жидкости потенциометрические ГСП. Общие технические условия.
ГОСТ 29169-91 (ИСО 648-77) Посуда лабораторная стеклянная. Пипетки с одной отметкой
ГОСТ 29227-91 (ИСО 835-1-81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 30553-98 (ИСО 904-76) Кислота соляная. Технические условия ГОСТ Р 8.563-96 Государственная система обеспечения единства измерений. Методики выполнения измерений
ГОСТ Р 51144-98 Продукты винодельческой промышленности. Правила приемки и методы отбора проб
ГОСТ Р 52523-2006 Вина столовые и виноматериалы столовые. Общие технические условия
ГОСТ Р ИСО 5725-1-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике.
3 СУЩНОСТЬ МЕТОДИКИ
Сущность методики состоит в предварительной подготовке проб вин и виноматериалов путем отделения мешающих компонентов органических кислот (щавелевой, уксусной, винной, яблочной, молочной и янтарной) с помощью ионного обмена на анионите АВ-17-8 с последующим определением массовой концентрации лимонной кислоты методом потенциометрического титрования.
Суть предварительной подготовки проб заключается в выделении лимонной кислоты (рК = 3,07) из матрицы пробы вина или виноматериала. Для этого применяют сильноосновный анионит в хпоридной форме при pH = 3,5 -4. При значении pH около 4 99 % лимонной кислоты находится в форме аниона цитрат-иона (Citr3~), а остальные компоненты вина остаются в незаряженной форме. Незаряженные компоненты вина, аминокислоты и более слабые карбоновые кислоты проходят через колонку с анионитом, не задерживаясь, а анионы лимонной кислоты адсорбируются на анионите в колонке. Для элюирования лимонной кислоты из анионита используют раствор соляной кислоты концентрации 0,1 моль/дм3.
Метод потенциометрического титрования заключается в измерении потенциала индикаторного медного электрода (относительно электрода сравнения) в процессе титрования подготовленной пробы на фоне боратного буфера pH 8,5 реагентом, вступающим в реакцию с определяемым веществом, с образованием прочного комплекса. В качестве комплексообразующего реагента используют ионы меди (2+). В растворе боратного буфера pH 8,5 цитрат-ионы (Citr3) образуют с ионами меди (2+) прочный комплекс состава 1:1.
Массовую концентрацию цитрат-ионов определяют по массовой концентрации ионов меди (2+) в точке эквивалентности на кривой титрования. Точку эквивалентности - эквивалентный объем меди - определяют по резкому изменению потенциала в процессе титрования.
Массовая концентрация цитрат-ионов соответствует массовой концентрации лимонной кислоты в анализируемой пробе.
4 ПРИПИСАННЫЕ ХАРАКТЕРИСТИКИ ПОГРЕШНОСТИ ИЗМЕРЕНИЙ
4.1 Методика выполнения измерений массовых концентраций лимонной кислоты в пробах вин и виноматериалов методом потенциометрического титрования обеспечивает получение результатов измерений с погрешностью, не превышающей значений, приведенных в таблице 1.
9
|
Таблица 1 - Диапазон измерений, относительные значения показателей точности, повторяемости и воспроизводимости методики при доверительной вероятности Р=0,95 |
|
Наименование определяемого компонента |
Диапазон измеряемых концентраций, г/дм3 |
Показатель повторяемости (среднеквадратическое отклонение повторяемости),
<?г, % |
Показатель
воспроиз
водимости
(среднеквад
ратическое
отклонение
воспроизво
димости),
°R ’ % |
Показатель точности (границы, в которых находится погрешность методики), 6,% |
|
Лимонная
кислота |
От 0,1 до 5,0 включ. |
5 |
10 |
20 |
|
4.2 Значения показателя точности методики используют при:
- оценке деятельности лабораторий на качество проведения испытаний;
- оценке возможности использования результатов измерений при реализации методики выполнения измерений в конкретной лаборатории.
5 ТРЕБОВАНИЯ БЕЗОПАСНОСТИ, ОХРАНЫ ОКРУЖАЮЩЕЙ СРЕДЫ ПРИ ВЫПОЛНЕНИИ ИЗМЕРЕНИЙ5.1 Условия безопасного проведения работ
К работе с иономером (потенциометром), нагревательными приборами и химическими реактивами допускается персонал, изучивший инструкцию по эксплуатации прибора, правила работы с химическими реактивами и химической посудой.
При работе с реактивами соблюдают требования безопасности, установленные для работы с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
При работе с электроустройствами соблюдают правила электробезопасности в соответствии с ГОСТ 12.1.019 и инструкцией по эксплуатации приборов.
Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.