МР 3.1.2.0135-18
Генетический мониторинг циркуляции вирусов кори и краснухи
Купить МР 3.1.2.0135-18 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
МР предназначены для специалистов органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, а также научных и медицинских организаций
Оглавление
I. Область применения
II. Общие положения
III. Генотипирование вируса кори, методология, номенклатура генотипов, географическое распространение
IV. Генотипирование вируса краснухи, методология, номенклатура генотипов, географическое распространение
V. Организация работ по генотипированию вирусов
VI. Использование результатов генотипирования вирусов кори и краснухи в эпидемиологическом расследовании
Приложение 1. Рекомендуемый порядок сбора, подготовки, транспортирования и хранения клинических образцов
Приложение 2. Термины и определения
Библиографические данные
| Дата введения | 08.11.2018 |
|---|---|
| Добавлен в базу | 01.02.2020 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
Организации:
- Федеральный закон 52-ФЗ О санитарно-эпидемиологическом благополучии населения
- СП 3.1.2952-11 Профилактика кори, краснухи и эпидемического паротита
- СП 3.1/3.2.3146-13 Общие требования по профилактике инфекционных и паразитарных болезней
- МУ 3.1.2.1177-02 Эпидемиологический надзор за корью, краснухой и эпидемическим паротитом
- МУ 3.1.2.2356-08 Эпидемиологический надзор за врожденной краснухой
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8
стр. 9
стр. 10

стр. 11
стр. 12

стр. 13

стр. 14
стр. 15
стр. 16

стр. 17
стр. 18

стр. 19

стр. 20

стр. 21
стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
Государственное санитарно-эпидемиологическое нормирование _Российской Федерации___
3.1.2. ЭПИДЕМИОЛОГИЯ. ПРОФИЛАКТИКА ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ. ИНФЕКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Генетический мониторинг циркуляции вирусов кори и краснухи
Методические рекомендации МР 3.1.2.0135—18
Издание официальное
Москва • 2019
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека
3.1.2. ЭПИДЕМИОЛОГИЯ. ПРОФИЛАКТИКА ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ. ИНФЕКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Генетический мониторинг циркуляции вирусов кори и краснухи
Методические рекомендации МР 3.1.2.0135—18
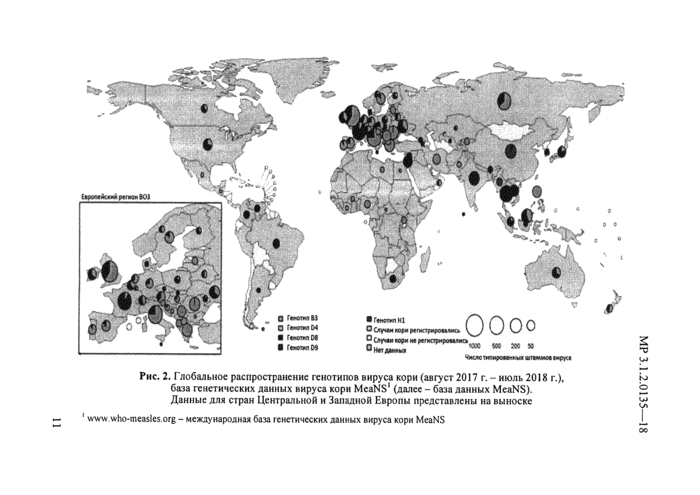
га, в период с августа 2017 г. по июль 2018 г. в мире циркулировали генотипы D8, ВЗ, HI, D9, D4 (рис. 2).
В последние годы наблюдается глобализация циркуляции некоторых генотипов вируса кори (ВЗ, D8), что обусловлено миграцией населения в мировом масштабе, ростом пассажиропотока международных перевозок, в первую очередь авиационных, расширением географии туризма и международной торговли, участием граждан разных стран в спортивных, культурных и политических мероприятиях.
В этой связи для описания разнообразия генетических вариантов вируса в пределах генотипа в номенклатуру было включено понятие «наименованный штамм» («named strain») [12, 13].
Наименованный штамм представляет собой репрезентативный вариант вируса кори для группы штаммов с идентичными нуклеотидными последовательностями 450 нт N-гена (допускается наличие не более одной нуклеотидной замены), характеризующихся продолжительной (не менее 2 лет) циркуляцией и относительно широкой географией распространения (как минимум несколько стран). Такая группа штаммов определяется как уникальная генетическая линия, отличающаяся от других линий в пределах генотипа. Описанный подход позволяет осуществлять мониторинг не только генотипов вируса, но и генетических вариантов в пределах одного генотипа.
3.5. Все вакцинные штаммы вируса кори принадлежат к генотипу А. [14—16). Прототипные «дикие» штаммы соответствующих вакцинных штаммов были независимо изолированы в середине прошлого века в нескольких странах (США, Советский Союз, Китай, Япония), что позволило ряду исследователей предположить широкое географическое распространение генотипа А в довакцинальную эру. Однако после широкого внедрения программ вакцинации штаммы генотипа А очень редко изолировались в мире, не описано ни одной вспышки кори, связанной с их циркуляцией. Эпизодическое обнаружение штаммов генотипа А связано с выделением вируса из клинических образцов недавно привитых коревой вакциной пациентов либо обусловлено лабораторной контаминацией. «Дикие» штаммы генотипа А в мире в настоящее время не циркулируют.
3.6. Антигенные различия между штаммами вируса кори - представителями разных генотипов минимальны, все известные генотипы вируса принадлежат к одному серотипу [14, 16]. Коревые вакцины, производящиеся с использованием вакцинных штаммов генотипа А, эффективны в отношении всех известных генотипов (генетических вариантов) вируса, их применение в вакцинопрофилактике позволяет добиваться устойчивого контроля кори и ее элиминации.
|
Рис. 2. Глобальное распространение генотипов вируса кори (август 2017 г. - июль 2018 г.), база генетических данных вируса кори McaNS1 (далее - база данных MeaNS). Данные для стран Центральной и Западной Европы представлены на выноске |
1 www who-measles.org- международная база генетических данных вируса кори McaNS
МР 3.1.2.0135—18
3.7. ВОЗ в сотрудничестве со специалистами Агентства защиты здоровья (Лондон, Великобритания) была создана специализированная международная база генетических данных вируса кори MeaNS [13, 17]. База данных предоставляет пользователям наиболее полную информацию по генотипам вируса кори, циркулировавшим в мире с момента изоляции первых штаммов, возможность типирования, филогенетического анализа, поиска идентичных/родственных штаммов, анализа (в том числе ретроспективного) данных генетического мониторинга по странам и регионам ВОЗ, а также эпидемиологические данные, демонстрирующие импортирование/экспортирование генетических вариантов вируса в глобальном масштабе.
IV. Генотипирование вируса краснухи, методология, номенклатура генотипов, географическое распространение
4.1. Вирус краснухи является членом семейства Togaviridae и единственным представителем рода Rubivirus. Вирион содержит РНК, окруженную капсидом и липопротеидной оболочкой. Капсид образован капсидным белком (С), липопротеидная оболочка содержит два гликопротеина - Е1 и Е2. Геном вируса представлен одноцепочечной РНК позитивной полярности протяженностью 9 700 нт и помимо структурных белков (С, Е1 и Е2) кодирует два неструктурных белка Р150 и Р90. Как и вирус кори, вирус краснухи серологически монотипичен, однако его генетическое разнообразие позволяет выделять генетические генотипы и варианты.
С 2004 года действует утвержденный ВОЗ протокол генотипирова-ния диких штаммов вируса краснухи [18]. Для рутинного молекулярногенетического анализа используется «окно секвенирования», включающее 739 нуклеотидов (8 731—9 469 нт) гена, кодирующего белок Е1 (рис. 3).
4.2. Номенклатура генотипов вируса краснухи предусматривает единый подход в наименовании штаммов как описано ниже [18, 19]:
- RVi - изолят вируса, полученный на культуре клеток, RVs - нуклеотидная последовательность 739 нуклеотидов гена вируса Е1, полученная из клинического материала;
- город/регион, в котором выделен штамм;
- страна, обозначенная трехбуквенным кодом, принятым в ВОЗ;
- порядковый номер эпидемиологической недели, в которую выделен штамм (от 1 до 53), календарный год;
- порядковый номер штамма в том случае, если в течение недели выделено более 1 штамма;
- генотип, к которому относится штамм;
- в случае выделения вируса от пациентов с синдромом врожденной краснухи (далее - СВК) в название штамма добавляется обозначение «CRS».
|
•4 |
|
5'
ААА 3'
9 469
8 731
739 нт
Рис. 3. Схема структурной организации генома вируса краснухи и положение «окна секвснирования» гена Е1
Например, изолят RVi/Ryazan.RUS/09.08[lH] выделен на 9-й эпидемиологической неделе 2008 г. в Российской Федерации, г. Рязани, принадлежит к генотипу 1Н.
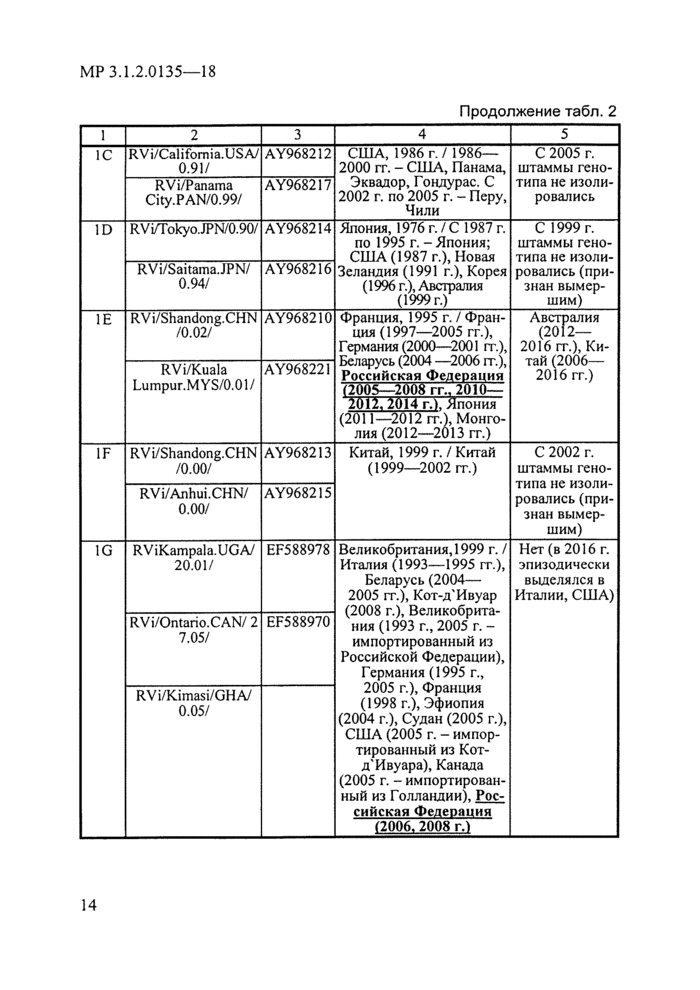
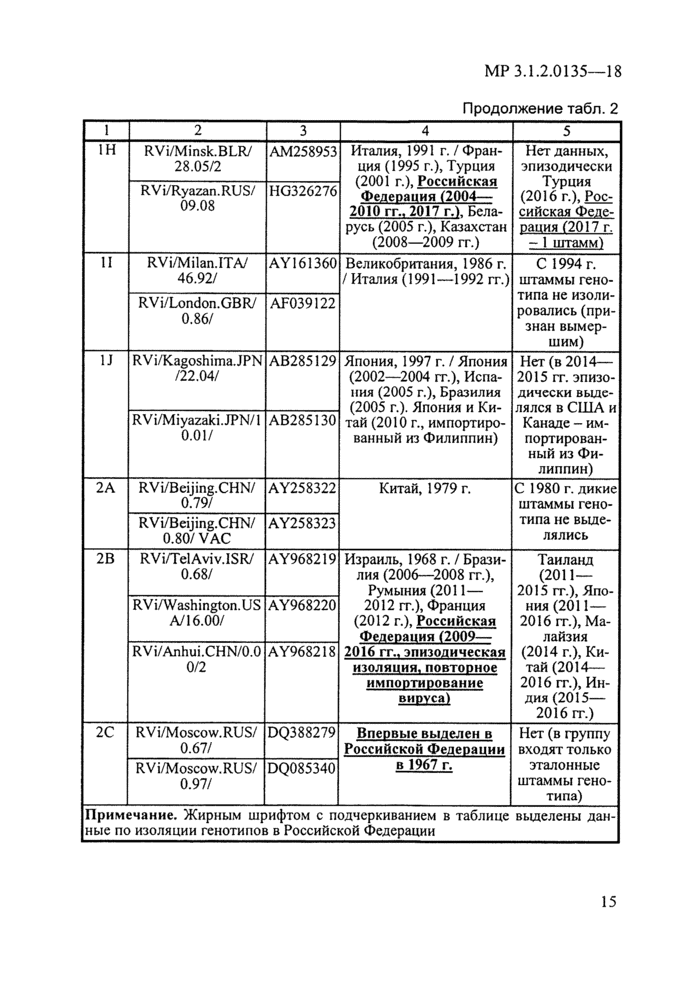
4.3. Номенклатура генотипов вируса краснухи включает 2 группы (1-го и 2-го, 10-го и 3-го генотипа соответственно), всего описано 13 генотипов вируса [18, 19]. Для всех генотипов описаны эталонные штаммы, как правило, исторически изолированные первыми. Краткая характеристика генотипов вируса краснухи представлена в табл. 2. Некоторые генотипы не изолировались достаточно давно и считаются вымершими.
Таблица 2
|
Характеристика генотипов вируса краснухи | ||||||||||||||||||||||||||||
|
|
Продолжение табл. 2 | |||||||||||||||||||||||||||||||||||||||||||
|
|
Продолжение табл. 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Примечание. Жирным шрифтом с подчеркиванием в таблице выделены дан-ные по изоляции генотипов в Российской Федерации | |||||||||||||||||||||||||||||||||||||||||||||||||||||
4.4. Почти все вакцинные штаммы относятся к генотипу 1А. Так как данный генотип включает также ряд диких штаммов и является гетерогенным, он имеет статус «предварительного», в будущем возможен пересмотр его статуса по мере накопления данных.
4.5. Особенности биологии вируса, трудности его изоляции на культуре клеток и типирования, небольшое число стран, в которых осуществляется генетический мониторинг циркуляции вируса, обусловливают ограниченность данных по генотипам вируса краснухи, циркулирующим в мире. Так, в 2015 г. из 106 стран - членов ВОЗ, регистрировавших случаи краснухи, только 11 предоставили информацию о генотипах циркулирующих вирусов [20]. Таким образом, доступные данные не отражают в полной мере генетическое разнообразие и географию циркуляции вируса краснухи.
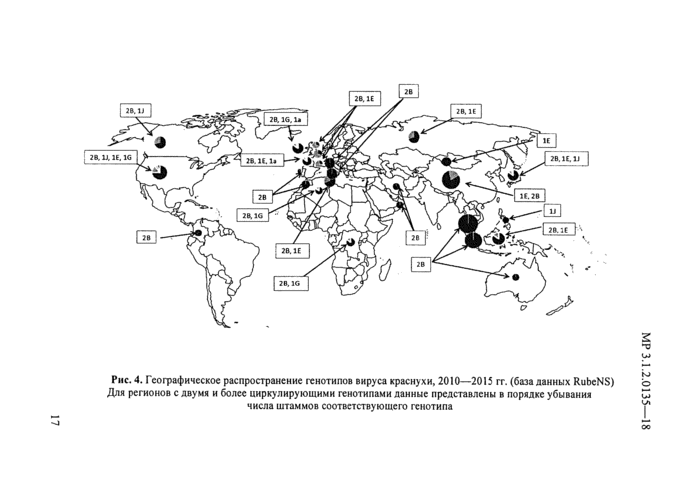
Данные мониторинга глобальной циркуляции вируса в период 2010—2015 гг. демонстрируют активную циркуляцию 5 генотипов (рис. 4). Наиболее часто изолировались штаммы генотипа 2В, представленные двумя основными группами вируса африканского либо азиатского происхождения. Генотип 2В в настоящее время характеризуется глобальным распространением. Вторым по частоте изоляции является генотип 1Е, эндемичный для Китая.
4.6. Вирус краснухи представлен единственным серотипом, крас-нушные вакцины вне зависимости от генотипа вакцинного штамма эффективны в отношении всех описанных на сегодняшний день генетических вариантов вируса краснухи «дикого» типа.
4.7. ВОЗ в сотрудничестве со специалистами Агентства защиты здоровья (Лондон, Великобритания) была создана специализированная международная база генетических данных вируса краснухи RubcNS1 (далее - база данных RubeNS) [12, 13, 19]. База данных предоставляет пользователям наиболее полную информацию по генотипам вируса краснухи, возможность типирования, филогенетического анализа, поиска идентичных/родственных штаммов, анализа (в том числе ретроспективного) данных генетического мониторинга по странам и регионам ВОЗ, а также эпидемиологические данные, демонстрирующие импорти-рование/экспортирование генетических вариантов вируса в глобальном масштабе.
|
Рис. 4. Географическое распространение генотипов вируса краснухи. 2010—2015 гг. (база данных RubeNS) Для регионов с двумя и более циркулирующими генотипами данные представлены в порядке убывания числа штаммов соответствующего генотипа |
МР 3.1.2.0135—18
V. Организация работ но генотипированию вирусов
5.1. Сбор клинических образцов для генотипирования осуществляется специалистами медицинских организаций, выявившими случай ко-ри/краснухи. Образцы собираются в максимально ранние сроки от начала заболевания.
5.2. Порядок сбора, подготовки, хранения и транспортирования клинических образцов изложен в прилож. 1 к МР.
5.3. Полнота и достоверность исследования обеспечивается сбором клинических образцов от достаточного количества случаев инфекции. Выбор случаев заболевания, подлежащих генотипированию, проводится таким образом, чтобы обеспечить возможность генотипирования не менее 80 % вспышек (цепочек передачи) инфекции, а также всех импортированных и завозных случаев.
При вспышечной заболеваемости нецелесообразно осуществлять сбор клинических образцов для исследования от всех случаев инфекции, ассоциированных с конкретной вспышкой. Необходимо организовать сбор клинических образцов от первых 5—10 случаев при каждой вспышке, всего не более 10 случаев от вспышки на протяжении 1 месяца.
При продолжительности вспышки более 1 месяца рекомендуется осуществлять сбор образцов не чаще 1 раза в месяц от 2—3 последних зарегистрированных случаев.
Генотипированию подлежат 100% импортированных случаев (при невозможности сбора клинических образцов в регламентируемые сроки от импортированного случая образцы должны быть собраны от нескольких случаев, связанных с импортированным).
Генотипированию подлежат 100% завозных (из других субъектов Российской Федерации) случаев (при невозможности сбора клинических образцов в регламентируемые сроки от завозного случая образцы должны быть собраны от нескольких случаев, связанных с завозным).
При регистрации единичных случаев заболевания («спорадическая» заболеваемость, менее 1 случая/млн населения) генетическому ти-пированию подлежат 100 % зарегистрированных случаев.
5.4. При импортировании коревой/краснушной инфекции может наблюдаться социркуляция нескольких генетических вариантов вируса. Для дифференцирования вспышек, регистрируемых в одно и то же время на одной территории, но вызванных разными генетическими вариантами вирусов, целесообразно генотипировать дополнительно случаи инфекции (группы связанных случаев), для которых не установлена эпидемиологическая связь с ранее генотипированными.
VI. Использование результатов генотипирования вирусов
кори и краснухи в эпидемиологическом расследовании
6.1. Использование данных генотипирования вирусов кори и краснухи на практике позволяет ретроспективно уточнить результаты эпидемиологического расследования случая кори/краснухи и откорректировать эпидемиологические связи в цепочках вторичного распространения инфекции.
6.2. На основании эпидемиологического расследования осуществляется окончательная классификация случая: «местный», «завозной» с другой территории Российской Федерации, «импортированный» (завозной с территории другого государства), «связанный с завозным/импор-тированным» случаем.
6.3. На первом этапе эпидемиологического расследования необходимо определить степень распространения инфекции и классифицировать случай кори/краснухи. Вспышкой считается 5 и более случаев, во время вспышки могут формироваться разные по интенсивности очаги (например, по месту работы, учебы, месту жительства), цепочки и единичные с неустановленными эпидемиологическими связями случаи.
При анализе принято выделять случаи, связанные цепочкой передачи инфекции от импортированного/завозного случая. Нередко цепочка ограничивается первым поколением воспроизводства инфекции (случаи заболевания в результате контакта с больным, прибывшим с территории другого государства или другого субъекта Российской Федерации). Эти случаи классифицируются как «связанные с импортирован-ным/завозным». Все последующие вторичные случаи заражения от случая, связанного с завозным, расцениваются как «местные».
Необходимо учитывать, что географическое происхождение генотипов вирусов кори/краснухи не всегда совпадает со страной импортирования и не дает основания классифицировать случай как импортированный. В случаях выявления генотипа/подтипа, ранее на территории страны не встречавшегося, необходимо изменить классификацию «местный» на «связанный с импортированным». При этом следует помнить, что результаты генотипирования вирусов кори/краснухи не влияют на тактику лечения пациентов, сроки и объём проводимых противоэпидемических мероприятий.
Нередко при импортировании коревой/краснушной инфекции может наблюдаться социркуляция нескольких генетических вариантов вирусов. Для дифференцирования эпидемиологических связей между случаями, регистрируемыми в одно и то же время на одной территории, но вызванными разными генетическими вариантами вируса, целесообразно генотипировать дополнительно случаи инфекции (группы связанных
ББК51.9
Г34
Г34 Генетический мониторинг циркуляции вирусов кори и краснухи: Методические рекомендации.—М.: Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека, 2019.—31 с.
ISBN 978-5-7508-1678-1
1. Разработаны ФБУН «Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г. Н. Габричевского»
(С. В. Шульга, О. В. Цвиркун, Н. Т. Тихонова, Т. С. Чехляева, А. Г. Герасимова, Т. А. Мамаева, М. А. Наумова).
2. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А. Ю. Поповой 8 ноября 2018 г.
3. Введены впервые.
ББК51.9
ISBN 978-5-7508-1678-1
© Роспотребнадзор, 2019
случаев), для которых не установлена эпидемиологическая связь с ранее генотипированными случаями.
Напротив, выявление одного и того же генотипа и подтипа вируса у единичных случаев кори/краснухи при условии, что цепочка передачи инфекции ограничена одним инкубационным периодом, позволяет объединить эти случаи в одну вспышку (цепочку).
Примеры:
1) на территории первого административного уровня зарегистрированы случаи кори: в городе - 5 случаев (вспышка), в селе Б - 4 случая (групповая заболеваемость), а также б единичных, не связанных между собой, случаев кори в селе А. Интервал регистрации даты сыпи у заболевших в городе, в селе Айв селе Б составил 7—18 дней, т. е. не превышал инкубационный период (21 день). Источник инфекции и предполагаемое место заражения первого заболевшего установить не удаюсь.
До получения результатов генотипирования при эпидемиологическом расследовании установлено формирование двух очагов кори - в городе и селе Б, а также 6 очагов в селе А. Выделение одного и того же генотипа и подтипа (например, D4 Manchester) вируса на разных этапах регистрации случаев кори при учете возможного наличия пропущенных случаев позволили объединить все случаи в одну вспышку с 15 заболевшими.
Выявление разных генотипов или подтипов вируса кори/краснухи в пределах одной территории любого административного уровня позволяет откорректировать установленные эпидемиологические связи и количество сформированных очагов.
2) на основании оперативного эпидемиологического расследования были установлены эпидемиологические связи с предполагаемым источником или местом заражения, что давало основание предположить о наличии вспышки кори с 8 заболевшими. Источник инфицирования у первого заболевшего установить не удалось. Во время вспышки были зарегистрированы: семейный очаг с 2 случаями, очаг с вторичным распространением по месту учебы и по месту работы. Ретроспективный анализ с учетом данных молекулярно-генетического типирования (выявление на разных сроках распространения инфекции у двух пациентов генотипа D4 и у двух - генотипа D8) дал основание разделить вспышку на два очага по 4 заболевших (групповая заболеваемость), обусловленных социркуляцией двух генотипов (D4 и D8) на одной территории.
6.4. Генотипирование штаммов вируса кори/краснухи необходимо в случае, когда при вакцинации по эпидемическим показаниям контактных в очагах инфекции выявляются среди привитых лица с клинической симптоматикой кори/краснухи, что требует дифференцирования инфекции и поствакцинальной реакции. Указанные случаи должны регистрироваться
Содержание
I. Область применения...............................................................................................4
II. Общие положения .................................................................................................4
III. Гснотипирование вируса кори, методология, номенклатура
генотипов, географическое распространение..........................................................5
IV. Генотипирование вируса краснухи, методология, номенклатура
генотипов, географическое распространение........................................................12
V. Организация работ по генотипированию вирусов...........................................18
VI. Использование результатов генотипирования вирусов кори и
краснухи в эпидемиологическом расследовании..................................................19
Приложение 1. Рекомендуемый порядок сбора, подготовки,
транспортирования и хранения клинических образцов.............22
Приложение 2. Термины и определения...............................................................28
Нормативные и методические документы............................................................29
Библиографические данные...................................................................................30
УТВЕРЖДАЮ
Руководитель Федеральной службы по надзору в сфере зашиты прав потребителей и благополучия человека, Главный государственный санитарный врач Российской Федерации
А. Ю. Попова
8 ноября 2018 г.
Дата введения: с момента утверждения
3.1.2. ЭПИДЕМИОЛОГИЯ. ПРОФИЛАКТИКА ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ. ИНФЕКЦИИ ДЫХАТЕЛЬНЫХ ПУТЕЙ
Генетический мониторинг циркуляции вирусов кори и краснухи
Методические рекомендации _MP 3.1.2.0135—18_
I. Область применения
1.1. Настоящие методические рекомендации (далее - МР) содержат теоретические принципы и практические рекомендации по мониторингу циркуляции вирусов кори и краснухи, анализу и интерпретации полученных данных, их использованию в качестве доказательства элиминации кори и краснухи.
1.2. МР предназначены для специалистов органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, а также научных и медицинских организаций.
II. Общие положения
2.1. Глобальный стратегический план Всемирной организации здравоохранения (далее - ВОЗ) по кори и краснухе на 2012—2020 гг. предполагает достижение элиминации кори в 5 из 6 регионов ВОЗ и краснухи - в 2 регионах (Панамериканский, Европейский) [1]. В Российской Федерации реализуется программа «Элиминация кори и краснухи в Российской Федерации (2016—2020 гг.)», в соответствии с которой планируется достижение элиминации кори и краснухи к 2020 г. с последующей ее верификацией (подтверждением).
Усиление системы эпидемиологического надзора - одна из ключевых стратегий достижения элиминации кори/краснухи [2—4]. Организо-
ванный в масштабе страны индивидуальный учет больных с проведением эпидемиологического расследования, лабораторной верификацией и генетическим типированием случаев заболевания, подозрительных на корь/краснуху, позволяет обеспечить высокую достоверность данных эпидемиологического надзора.
2.2. Генетическое типирование вирусов позволяет определять эндемичные для конкретной страны генотипы, осуществлять мониторинг циркуляции вирусов на региональном и глобальном уровнях, идентифицировать импортированные случаи инфекции (генотипы вируса), определять их географическое происхождение, документировать прекращение циркуляции ранее эндемичных генотипов, демонстрируя прогресс в контроле инфекции и достижении ее элиминации, подтверждать (верифицировать) достижение и поддержание фазы элиминации [4, 5].
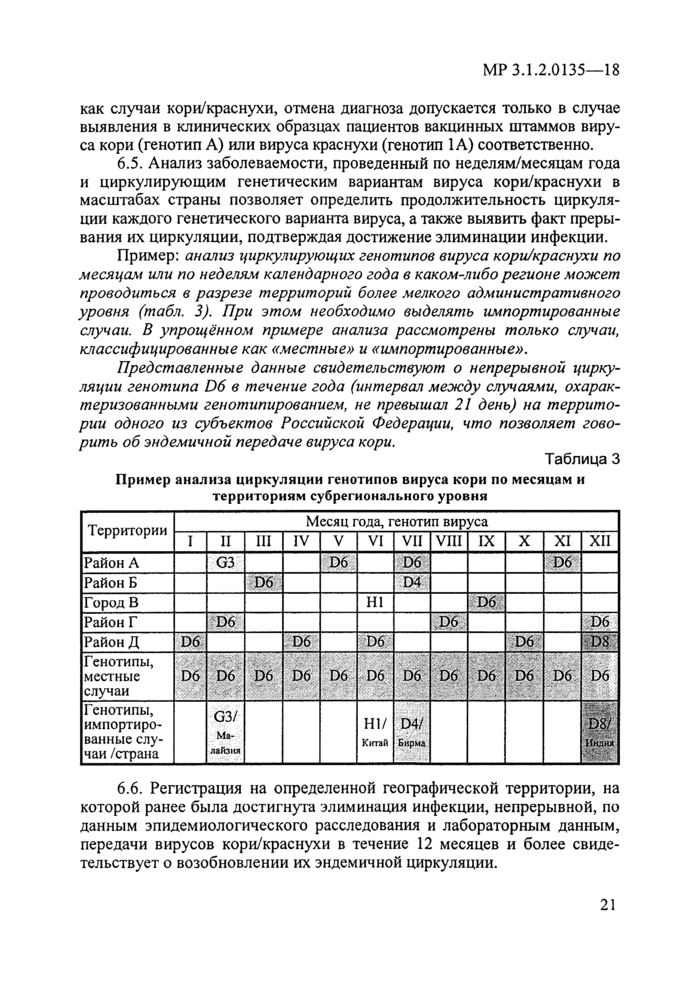
По критериям ВОЗ, демонстрация отсутствия циркуляции какого-либо из генетических вариантов вируса на протяжении не менее 12 месяцев при условии генотипирования нс менее 80 % вспышек (цепочек циркуляции) на определенной территории является необходимым для подтверждения достижения элиминации инфекции [2, 4]. Отсутствие эндемичной циркуляции вируса на протяжении не менее 36 месяцев рассматривается в качестве одного из ключевых показателей, используемых в верификации элиминации.
Генотип вирусов кори и краснухи не имеет значения с точки зрения диагностики заболеваний и лечения пациентов, не требует изменения тактики противоэпидемических мероприятий и мероприятий в очагах, по необходимости генотипирование может быть проведено ретроспективно при наличии соответствующих клинических образцов.
2.3. Верификация элиминации требует совершенствования подходов к генетическому мониторингу циркуляции вирусов кори/краснухи, интеграции эпидемиологических и лабораторных (генетических) данных.
III. Генотипирование вируса кори, методология, номенклатура генотипов, географическое распространение
3.1. Вирус кори является представителем семейства Paramyxoviri-dae, рода Morbillivirus. Вирусные частицы сферической формы имеют размер 120—250 нм. Вирион состоит из свернутого во вторичную шарообразную структуру нуклеокапсида, построенного по спиральному типу симметрии и внешней липидной оболочки, имеющей происхождение из клетки хозяина.
Геном вируса представлен одноцепочечной несегментированной РНК негативной полярности длиной около 16 000 нт. Шесть неперекры-вающихся структурных генов расположены линейно и кодируют 6
структурных белков: нуклеопротеин (N), фосфопротеин (Р), матриксный белок (М), фузионный белок (F), гемагглютинин (Н), полимераза («большой» белок L) и два неструктурных белка - С и V. Геномная РНК служит матрицей для синтеза антигеномной РНК позитивной полярности, которая, в свою очередь, является матрицей для транскрипции вирусных белков и синтеза геномной РНК в процессе репликации. Несмотря на то, что вирус кори представлен единственным серотипом, его генетическое разнообразие позволяет выделять различные генетические варианты и группировать их по происхождению и истории циркуляции, что находит свое практическое применение в мониторинге циркуляции вируса.
Для генетического типирования вируса кори используются данные сравнительного анализа нуклеотидных последовательностей (рис. 1) СООН - концевого фрагмента N-гена (450 нт, 1 126—1 575 нт) и полноразмерной последовательности Н-гена (1 854 нт) [6—12]. Указанные гены являются наиболее вариабельными структурными генами вируса.
| ||||||||||||||||
|
Рис. 1. Схема структурной организации генома вируса кори и положение «окон секвенирования», используемых для типирования вируса (гены N, Н) | ||||||||||||||||
Для типирования вируса достаточно анализа СООН - концевого фрагмента N-гена, для эталонных штаммов новых генотипов необходим дополнительно анализ нуклеотидной последовательности гена Н.
3.2. Генотип - оперативная таксономическая единица, определяемая на основании различий нуклеотидных последовательностей у разных штаммов вируса. Генотип включает родственные штаммы, отличающиеся на нуклеотидном уровне от ближайшего штамма другого генотипа не менее чем на 2,5 % для СООН - концевого фрагмента N-гена и 2 % - для Н-гена. Некоторые генотипы характеризуются гетерогенностью, превышающей 2,5 % для 450 нт N-гена [9], для других отличие последовательностей Н-гена составляет менее 2 %. Отказ от выделения новых генотипов в первом случае и отнесение родственных вирусов к разным генотипам во втором обусловлены необходимостью адаптации номенклатуры генотипов к задачам мониторинга географического рас-
пространения и циркуляции вирусов кори. Современный подход в разработке номенклатуры генотипов вируса кори предполагает таким образом учет как филогенетических взаимоотношений, так и географии циркуляции разных штаммов вируса, что позволяет использовать данные типирования в эпидемиологическом надзоре за коревой инфекцией.
3.3. Номенклатура генотипов вируса кори предусматривает единый подход в наименовании штаммов как описано ниже:
- MVi - изолят вируса, полученный на культуре клеток, MVs - нуклеотидная последовательность СООН - концевого фрагмента N-гена вируса, полученная из клинического материала;
- город/регион, в котором выделен штамм;
- страна, обозначенная трехбуквенным кодом, принятым в ВОЗ;
- порядковый номер эпидемиологической недели, в которую выделен штамм (от 1 до 53), календарный год;
- порядковый номер штамма в том случае, если в течение недели выделено более 1 штамма;
- генотип, к которому относится штамм;
- в случае выделения вируса от пациентов с энцефалитом телец включения или подострым склерозирующим панэнцефалитом в наименование штамма может быть добавлено необходимое обозначение («М1ВЕ» или «SSPE» соответственно).
Например, изолят MVi/Moscow.RUS/51.12[D8] выделен на 51-й эпидемиологической неделе 2012 г. в Российской Федерации, г. Москве и принадлежит к генотипу D8.
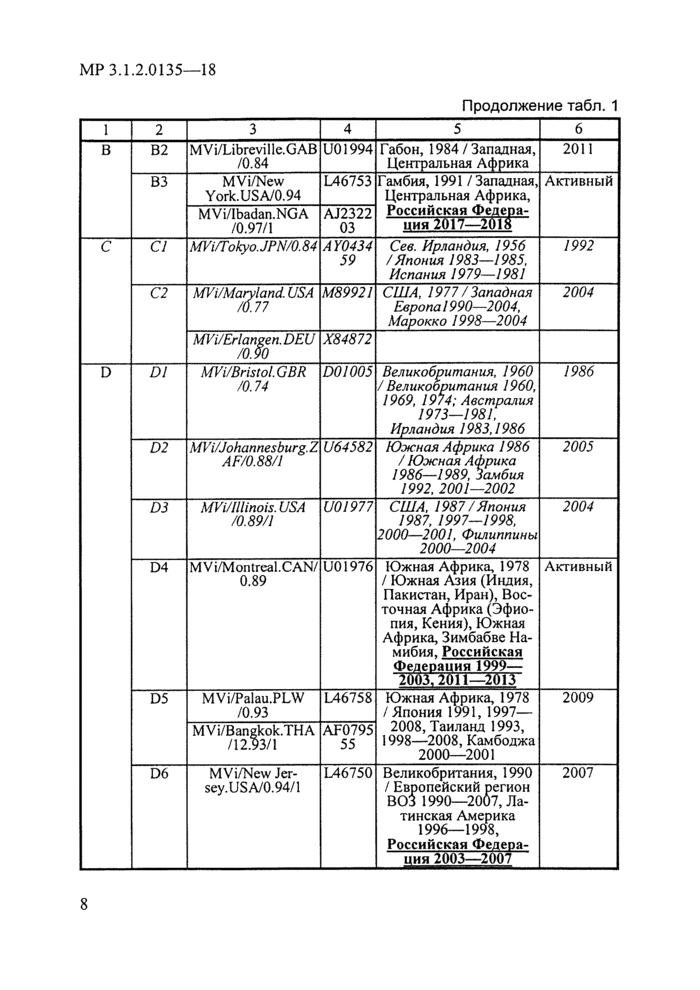
3.4. Номенклатура генотипов вируса кори включает 24 генотипа, представляющих 8 филогенетических клад (групп). Для всех генотипов описаны эталонные штаммы вируса, как правило, исторически изолированные первыми либо отражающие гетерогенность штаммов генотипа, циркулирующих в последнее время. Краткая характеристика генотипов вируса кори представлена в табл. 1.
Таблица 1
|
Характеристика генотипов вируса кори | ||||||||||||||||||||||||
|
|
Продолжение табл. 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Продолжение табл. 1
|
1 |
2 |
3 |
4 |
5 |
6 |
|
D7 |
MVi/Victoria.AUS /16.85 |
AF2434 50 |
Великобритания, 1980 /Австралия 1985— 1988,2000, Великобритания 1980, 1982, 2002—2003, Германия 2000—2001. Франция, Испания 2001—2003, Ирландия 2002—2003 |
2007 | |
|
MVi/IUinois.USA 50.99 |
AY0370 20 | ||||
|
D8 |
М V i/M anchester. G В R/30.94 |
AF2808 03 |
Великобритания 1994 / Индия, Непал, Рос-сийская Федерация 2013—2018 |
Активный | |
|
D9 |
MVi/Victoria.AUS /12.99 |
AF4814 85 |
Австралия 1999 / Индонезия, Малайзия, Таиланд 2008—2013 |
Активный | |
|
D10 |
MVi/Kampala.UGA/ 51.00/1 |
AY9231 85 |
Уганда, 2000/ Уганда |
2005 | |
|
D11 |
MVi/Menglian.Yunn an.CHN/47.09 |
GU4405 71 |
Австралия 2001 / Мьянма (предположительно) |
2010 | |
|
£ |
£ |
MVi/Goettingen. DE U/0.71 |
X84879 |
США. 1970/Нет данных |
1987 |
|
F |
F |
MVs/Madrid. ESP /0.94 [SSPEJ |
X84865 |
Испания, 1970/ Нет данных |
1994 |
|
G |
GJ |
MVi/Berkeley. USA /0.83 |
U01974 |
США, 1983/Нет данных |
1983 |
|
G2 |
MVi/Amsterdam. NL D/49.97 |
AF1712 32 |
Нидерланды 1997 / Индонезия, Малайзия |
2004 | |
|
G3 |
MVi/Gresik.IDN /18.02 |
AY 1842 17 |
Австралия, 1999 / Восточный Тимор, Индонезия |
Активный | |
|
Н |
Н1 |
MVi/Hunan.CHN /0.93/7 |
AF0452 12 |
Тайвань, 1992/Китай |
Активный |
|
Н2 |
MVi/Beijing.CHN /0.94/1 |
AF0452 17 |
Китай 1994 /Вьетнам |
2003 |
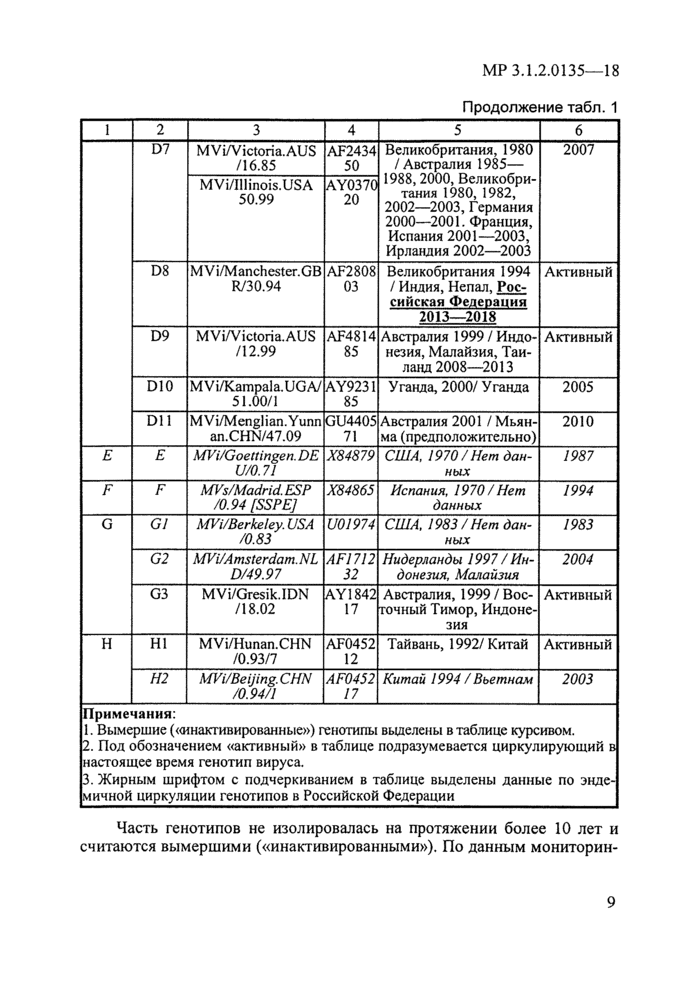
Примечания:
1. Вымершие («инактивированные») генотипы выделены в таблице курсивом.
2. Под обозначением «активный» в таблице подразумевается циркулирующий в настоящее время генотип вируса.
3. Жирным шрифтом с подчеркиванием в таблице выделены данные по энде-
мичной циркуляции генотипов в Российской Федерации_
Часть генотипов не изолировалась на протяжении более 10 лет и считаются вымершими («инактивированными»). По данным мониторин-
1
www.who-rubella.org - международная база генетических данных вируса краснухи RubeNS.