МВИ.МН 3239-2009
Определение бета-каротина в специализированных продуктах питания. Методика выполнения измерений
Купить МВИ.МН 3239-2009 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методика предназначена для определения содержания бета-каротина (мг/100 г) в специализированных продуктах питания (пищевые продукты, обогащенные витаминными премиксами, продукты для питания детей, беременных женщин и кормящих матерей, спортсменов, биологически активные добавки к пище, витаминные премиксы, предназначенные для обогащения продуктов питания), а также может быть использована для определения содержания бета-каротина в необогащенных продуктах питания.
Документ аттестован РУП "Белорусский государственный институт метрологии", свидетельство об аттестации № 538/2009 от 19.10.2009 года
Оглавление
1 Область применения
2 Показатели прецизионности методики
3 Средства измерений, вспомогательные устройства, реактивы, материалы
4 Метод измерения
5 Требования безопасности
6 Требования к квалификации оператора
7 Условия выполнения измерений
8 Подготовка к выполнению измерений
9 Выполнение измерений
10 Обработка результатов измерений
11 Оформление результатов измерений
12 Проверка приемлемости результатов измерений, полученных в условиях повторяемости
13 Проверка приемлемости результатов измерений, полученных в условиях внутрилабораторной воспроизводимости
14 Проверка стабильности результатов испытаний
Приложение А. Нормативные ссылки
Приложение Б. Пример методики расчета неопределенности измерений
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Организации:
| 16.10.2009 | Принят | БелГИМ |
|---|---|---|
| 02.11.2009 | Утвержден | Главный Государственный санитарный врач Республики Беларусь |
| Разработан | ГУ РНПЦ гигиены МЗ РБ |
- ГОСТ 15150-69 Машины, приборы и другие технические изделия. Исполнения для различных климатических районов. Категории, условия эксплуатации, хранения и транспортирования в части воздействия климатических факторов внешней среды
- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.2.003-91 Система стандартов безопасности труда. Оборудование производственное. Общие требования безопасности
- ГОСТ 23932-90 Посуда и оборудование лабораторные стеклянные. Общие технические условия
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
- ГОСТ 20015-88 Хлороформ. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 2603-79 Реактивы. Ацетон. Технические условия
- ГОСТ 29169-91 Посуда лабораторная стеклянная. Пипетки с одной отметкой
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 3145-84 Часы механические с сигнальным устройством. Общие технические условия
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
стр. 17
СОГЛАСОВАНО
УТВЕРЖДАЮ
Заместитель директора БелГИМ
Заместитель Министра Главный государственный санитарный врач Республики Беларусь адароС:
В.И. Качан 2009 г.
ОПРЕДЕЛЕНИЕ р-КАРОТИНА В СПЕЦИАЛИЗИРОВАННЫХ ПРОДУКТАХ ПИТАНИЯ
МЕТОДИКА ВЫПОЛНЕНИЯ ИЗМЕРЕНИЙ МВИ.МН -Ш9-2009
МВИ аттестована РУН ’’Белорусский государственный институт метрологии”
Свидетельство- об аттестации
№ gr - >1 -
Минск 2009
СОДЕРЖАНИЕ
3
3
4
5
5
6 6 6 9
9
10
11
12
12
14
15
Область применения
Показатели прецизионности методики
Средства измерений, вспомогательные устройства, реактивы, материалы
Метод измерения
Требования безопасности
Требования к квалификации оператора
Условия выполнения измерений
Подготовка к выполнению измерений
Выполнение измерений
Обработка результатов измерений
Оформление результатов измерений
Проверка приемлемости результатов измерений, полученных в условиях повторяемости
Проверка приемлемости результатов измерений, полученных в условиях внутрилабораторной воспроизводимости Проверка стабильности результатов испытаний Приложение А Нормативные ссылки
Приложение Б Пример методики расчета неопределенности измерений
|
2 |
- Наименование (шифр) пробы;
- Дату проведения измерений;
- Результаты измерений, включая все необходимые данные и промежуточные расчеты;
- Результаты параллельных определений;
- Окончательный результат измерений;
- Фамилию оператора.
12 Проверка приемлемости результатов измерений, полученных в условиях повторяемости
Проверку приемлемости результатов измерений, полученных в условиях повторяемости осуществляют согласно п. 5.2.2.1 СТБ ИСО 5725-6. Два результата испытаний должны быть получены в условиях повторяемости.
Рассчитывают абсолютное расхождение между результатами единичных наблюдений \Х] - Х21,
значение которого сравнивают с абсолютным значением предела повторяемости габС. Абсолютное значение предела повторяемости габс., мг/100 г, рассчитывают по формуле
габс=0,01-г-Х (6)
где 0,01 - коэффициент для пересчета процентов;
X - среднее арифметическое значение двух результатов единичных наблюдений, мг/100 г; г - относительное значение предела повторяемости, %, указанное в таблице 2.
Если для значения абсолютного расхождения между двумя результатами единичных наблюдений выполняется условие
\х,-ху.глс (7)
то оба результата считают приемлемыми и в качестве результата измерений указывают среднее арифметическое значение X, рассчитанное по формуле (2).
Если абсолютное значение разности превышает значение г, то следует получить еще два результата. Если размах четырех результатов испытаний равен или меньше критического размаха (формула 7), то среднее арифметическое четырех результатов (9) должно указываться как конечный заявляемый результат.
I^max ~ ^min | ^R0.95, (8)
где Crow = 3,6хоу (9)
Значения аг представлены в таблице 1.
Если данное условие не выполняется, то следует отказаться от полученных данных, выяснить и устранить причины, приводящие к неудовлетворительным результатам.
13 Проверка приемлемости результатов измерений, полученных в условиях внутрила-бораторной воспроизводимости
Проверку приемлемости результатов измерений, полученных в условиях внутрилаборатор-ной воспроизводимости, осуществляют согласно п. 5.3.2.2 СТБ ИСО 5725-6.
После проверки полученных результатов параллельных определений по критерию повторяемости по п.12 рассчитывают среднее арифметическое X двух результатов измерений Xi и X2 соответственно, мг/100 г:
X = Xl +Хг , (И)
2
где X1 и Хг - средние значения, рассчитанные на основании двух параллельных измерений, вычисленные по формуле (2) в условиях внутрилабораторной воспроизводимости.
Рассчитывают абсолютную разность результатов Х\ и Хг, и сравнивают со значением предела внутрилабораторной воспроизводимости CRaec-
CRaSc = 0,01 ■ CR0 95 • ^Х (11)
где 0,01 - коэффициент для пересчета процентов;
СЯод5=^2---, (12)
где R и г - относительные значения пределов повторяемости и внутрилабораторной воспроизводимости, указанные в таблице 2.
Если для значения абсолютного расхождения между результатами выполняется условие
-Хг\£Кл, (13)
то оба конечных результата, полученные в условиях внутрилабораторной воспроизводимости,
считаются приемлемыми и среднее значение X, рассчитанное по формуле (11), может быть использовано в качестве заявляемого результата.
При превышении указанного норматива должны быть выяснены и устранены причины, приводящие к неудовлетворительным результатам контроля внутрилабораторной воспроизводимости.
14 Проверка стабильности результатов измерений
Стабильность результатов измерений может быть проверена с использованием контрольной карты Шухарта (R-карта размахов по ИСО 8258) в соответствии с СТБ ИС0557^3М-''&бГ2^ч
При построении контрольной карты-используют рабочие пробы стабильные во времени. Содержание p-каротина в рабочей пробе должно соответствовать диапазону измерений. Рассчитывают:
- центральную линию: d2xar,
где d2 = 1,128 (коэффициент для расчета центральной линии для п=2);
- границы регулирования: UCL=D2xcr,
где D2 = 3,686 (коэффициент для расчета границы регулирования для п=2);
- предупреждающие границы: UCL=D2(2)xar,
где D2(2) = 2,834 (коэффициент для расчета предупреждающих границ для п=2); стг - стандартное отклонение повторяемости, % (таблица 1).
Оценку стандартного отклонения повторяемости Sr за отчетный период (20 - 30 измерений) получают по формуле:
Yuwi
( L \
(14)
ld2=w/d2 ,
v у
где w(. =\Хи - X2i | - размах;
Хц и X2j - результаты первого и второго определения для i-ой пары, мг/100г;
L - количество пар проведенных измерений за отчетный период (20 - 30 измерений).
|
Полученные значения заносят в лист данных контрольной карты: | ||||||||||||||||||||||
| ||||||||||||||||||||||
Графически по оси X откладывают дату проведения анализа, по оси Y - размах w. Также отмечают центральную линию и линии предупреждающей и регулирующей границ.
Интерпретацию результатов проводят в соответствии с требованиями СТБ ИСО 5725-6-2002 п.6.
Методика разработана лабораторией химии пищевых продуктов отдела физико-химических
исследований ГУ «РНПЦ гигиены» М3 РБ.
Разработчики:
Зав. лабораторией ХПП, к.х.н.
Ст.н.с. лаборатории XI111 Мл.н.с. лаборатории ХПП
ПРИЛОЖЕНИЕ А (обязательное)
Нормативные ссылки
1 ГОСТ 15150-69 Машины, приборы и другие технические изделия. Исполнения для различных климатических районов. Категории, условия эксплуатации, хранения и транспортирования в части воздействия климатических факторов внешней среды.
2 ППБ 1.04 - 2002 Общие правила пожарной безопасности Республики Беларусь для общественных зданий и сооружений.
3 Основные правила безопасности работы в химических лабораториях/ - М.: Химия,
1979 г.
4 ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования.
5 ГОСТ 12.2.003-91 Система стандартов безопасности труда. Оборудование производственное. Общие требования безопасности.
6 СТБ 1036-97 Продукты пищевые и продовольственное сырье. Методы отбора проб для определения показателей безопасности.
7 СТБ ИСО 5725-6 -2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике (ISO 5725-6:1994/Соч.1 : 2001, ШТ).
8 Р.Досон, Д.Эллиот, У.Эллиот, К.Джонс Справочник биохимика. М: «Мир», 1991. -
С.196.
9 Скурихин В.Н., Шабаев С.В. Методы анализа витаминов А, Е, Д и каротина в кормах, биологических объектах и продуктах животноводства. М.:Химия, 1996. - С. 14.
10 Carotenoids as colorants vitamin A precursors. Technological and nutritional applications // Edited by J.C Bauemfeind. - New York: Academic Press, 1981. - P.883 - 918.
11 Гороновский, И.Т. Краткий справочник по химии / И.Т. Гороновский, Ю.П. Назаренко, Е.Ф. Некряч. - Киев, 1987. - 829 с.
ПРИЛОЖЕНИЕ Б (обязательное)
Пример методики расчета неопределенности измерений.
1 Описание измеряемой величины
Измерение содержания p-каротина согласно МВИ включает следующие операции:
- Отбор навески анализируемой пробы;
- Проведение щелочного гидролиза;
- Экстракция органическим растворителем;
- Измерение точного объема разведения экстракта Р-каротина в органическом растворите-
ле;
|
10 х 100x2) х V |
- Измерение оптической плотности полученного экстракта на спектрофотометре. Математическая модель измерений выражается соотношением:
(1)
где D — оптическая плотность измеряемого раствора;
V— объем гексанового (хлороформенного) экстракта, см3;
т - масса навески, г;
Е1* - удельный показатель поглощения для Р-каротина в органическом растворителе:
для гексана Ef* =2550у для хлороформа=2592;
10 - коэффициент пересчета в мг;
100 - пересчет на 100 г продукта;
Rec - степень извлечения;
Еяер - фактор сходимости
Исходя из полученной модели, неопределенность измеренной массовой концентрации Р~ каротина включает следующие основные составляющие:
а) неопределенность, обусловленную случайными факторами (фактор сходимости);
б) неопределенность, обусловленную смещением метода;
в) другие составляющие неопределенности, не учтенные при исследовании прецизионности и смещения.
2 Оценивание относительной стандартной неопределенности, обусловленной случайными факторами
|
?/,о" |
Учитывая, что результат измерения получают усреднением результатов двух параллельных определений, оценку относительной стандартной неопределенности (ОСН) ддя у&^щгощйайазбна
рассчитывают по формуле:
°~г
(2)
л/2 ’
где сгг - показатель повторяемости (таблица 1 МВ И).
3 Оценивание относительной стандартной неопределенности, обусловленной смещением метода
При метрологической аттестации методики установлено, что максимальное значение неопределенности, обусловленной смещением следующее: и (Re с) % = 0,02
4 Оценивание других составляющих неопределенности
К другим составляющим неопределенности выполнения измерений относятся: а) неопределенность, связанная с неопределенностью удельного поглощения p-каротина; б) неопределенность, связанная с обработкой пробы; в) неопределенность связанная с погрешностью измерения оптической плотности спектрофотометром.
1) Для оценки неопределенности связанной, с неопределенностью удельного поглощения p-каротина, можно воспользоваться данными, полученными в результате проведения метрологи-чекой аттестации методики (таблица 1 Приложения Б). Представленные значения оценены на основании исследования зависимости D=f(C).
Таблица 1 - Результаты исследований относительной стандартной неопределенности удельного поглощения р-каротина, оцененной на основании исследования зависимости D=f(C)
|
XL 3 мкг/см |
Щх, % |
U-xi, % |
5 ^ &\СМ |
|
0,25 |
5,5 |
4,1 |
7,0 |
|
0,50 |
2,7 |
2,0 |
3,4 |
|
2,00 |
0,7 |
0,5 |
0,9 |
|
4,00 |
0,4 |
0,3 |
0,5 |
|
7,60 |
0,2 |
0,13 |
0,3 |
Как видно из таблицы 1 приложения Б, неопределенность удельного поглощения вносит большой вклад в бюджет неопределенности измерений. Это значение существенно зависит от концентрации р-каротина в спектрофотометрируемом объеме. Данный факт необходимо учитывать при вычислении неопределенности отдельного измерения и стремиться к проведению измерений в середине диапазона измеряемых концентраций 0,25 - 7,00 мкг/см3.
2) Математическая модель измерения включает составляющие неопределенности, связанные с взвешиванием пробы, взятой для анализа и измерением объема органического растворителя для растворения экстракта Р-каротина (и,).
Значение ип составляет:
U-n = т + UV ’ , *, ■ ......
где ит - ОСН, связанная с взвешиванием пробы и учетом тарирования/весов-при взвешйва-нии навески: J1 \'!'1
н'и,. jsj$
«я(вив)= —*100%.
т
(4)
(5)
где т — масса навески, мг;
А - погрешность весов, мг
иу — ОСН, связанная с измерением объема органического растворителя для растворения
экстракта р-каротина.
и(Г) = ^г(¥,) + и\Г,) (6)
где u(V0) и u(Vj - стандартная неопределенность, возникающая из-за отклонения объема мерной колбы от номинальной вместимости при ее изготовлении;
где Ау— погрешность колбы (пипетки) 0,001445х5хК
(8)
и(К) = -
(7)
где 0,001445 - коэффициент объемного расширения для гексана (для хлороформа -0,001273);
5 - пределы колебания температуры в лаборатории во время проведения исследований;
V - объем мерной колбы (пипетки).
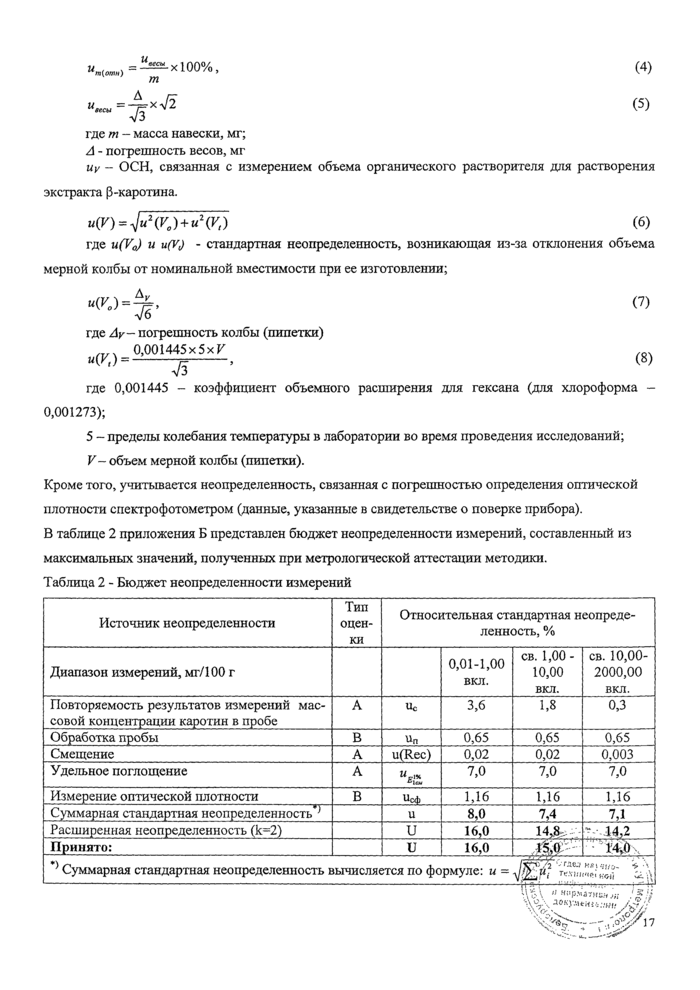
Кроме того, учитывается неопределенность, связанная с погрешностью определения оптической плотности спектрофотометром (данные, указанные в свидетельстве о поверке прибора).
В таблице 2 приложения Б представлен бюджет неопределенности измерений, составленный из
максимальных значений, полученных при метрологической аттестации методики.
|
Таблица 2 - Бюджет неопределенности измерений | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1 Область применения
Методика предназначена для определения содержания p-каротина (мг/100 г) в специализированных продуктах питания (пищевые продукты, обогащенные витаминными премиксами, продукты для питания детей, беременных женщин и кормящих матерей, спортсменов, биологически активные добавки к пище, витаминные премиксы, предназначенные для обогащения продуктов питания), а также может быть использована для определения содержания Р-каротина в необога-щенных продуктах питания.
P-Каротин относится к группе каротиноидов, в которую входит большое количество соединений с различной биологической активностью. Наиболее активным является p-каротин - его активность принята за 100 %. Молекула Р-каротина состоит из сорока атомов углерода, включает сопряженную полиеновую систему, которая располагается между двумя циклогексеновыми кольцами. Химическая формула С40Н56. М.в. 536,9, tnn. 183 °С. Оптически неактивен. Растворим в гексане, сероуглероде, дихлорэтане, хлороформе, изопропаноле, бензоле и кипящем петролейном эфире. Легко расщепляется под действием ультрафиолетового света, кислорода, устойчив к сильным щелочам.
Метод определения основан на экстрагировании Р-каротина из продуктов органическим растворителем с последующим анализом экстракта спектрофотометрическим методом.
Диапазоны измерений:
для продуктов питания!),01 - 10,00 мг/100 г;
для БАД и витаминных премиксов св. 10,00 - 2000,00 мг/100 г.
Нижний предел измерения методики (LOQ) составляет 0,01 мг/100 г.
Диапазон определяемых концентраций в спектрофотометрируемом объеме 0,25 - 7,00 мкг/см3.
2 Показатели прецизионности методики
Относительные значения показателей прецизионности (повторяемости и внутрилаборатор-ной воспроизводимости) при доверительной вероятности Р=0,95 МВИ представлены в таблице 1. Таблица 1 - Относительные значения показателей повторяемости, внутрилабораторной воспроизводимости МВИ при доверительной вероятности Р=0,95
|
Диапазон измерений (мг/100 г) |
Показатель повторяемости, % |
Показатель внутрилабораторной воспроизводимости,% |
|
0,01 - 1,00 вкл. |
5,3 |
7,3 |
|
св. 1,00 - 10,00 вкл. |
2,7 |
4Д |
|
св. 10,00 - 2000,00 вкл. |
0,4 |
1,6 |
. г.Т0%> - < -■ *.
Относительные значения пределов повторяемости и внутрилабораторной воспроизводимости при доверительной вероятности Р=0,95 указаны в таблице 2 .
|
Таблица 2 - Относительные значения пределов повторяемости и внутрилабораторной воспроизво димости при доверительной вероятности Р=0,95 | ||||||||||||
|
3 Средства измерений, вспомогательные устройства, реактивы и материалы
3.1 Средства измерений
Спектрофотометр, обеспечивающий измерения в диапазоне длин волн 220-800 нм;
Пределы измерений (0,0 -ь 2,0) Б;
Класс точности (погрешность) ± 0,015Б Дискретность шкалы 0,0001 Б
Весы лабораторные электронные, (диапазон взвешивания 0,0100-210,0000 г, погрешность взвешивания 0,3 мг)
| ||||||||||||||||||||||||||||||||||||||||||||||||
|
4 |
|
3.2 Вспомогательные устройства и оборудование | ||||||||||||||||||||||||||||||||||
|
Могут быть использованы другие средства измерения и вспомогательные устройства по метрологическим и техническим характеристикам, не уступающие рекомендуемым, а также реактивы не ниже указанной чистоты 4 Метод измерения
Метод основан на экстракции (3-каротина органическим растворителем (гексаном или хлороформом) и измерении оптической плотности полученного раствора на спектрофотометре при длине волны 450 нм (растворитель - гексан), при длине волны 465 нм (растворитель - хлороформ). Для расчета используются табличные значения коэффициентов оптической плотности 1 % раствора (3-каротина в 1 см3 (ед. оптич. плотности х см3мг'1см'1) в гексане Ех°^ - 2550 или в хлороформе ££=2592 [8,9, 10].
5 Требования безопасности
При выполнении работ персонал должен знать и строго соблюдать на рабочем месте требования:
- электробезопасности (ГОСТ 12.2.003);
- пожарной безопасности (ГОСТ 12.1.004);
- техники безопасности при работе в химической лаборатории;
//$/ л\\
- техники безопасности, изложенные в эксплуатационных документах на средства измерений и оборудование, применяемые при проведении измерений.
6 Требования к квалификации оператора
К выполнению измерений могут быть допущены лица, имеющие высшее или среднее специальное образование, изучившие настоящую методику, прошедшие подготовку для работы на спектрофотометре.
7 Условия выполнения измерений
При выполнении измерений в лаборатории согласно ГОСТ 15150 должны быть соблюдены следующие условия.
- температура воздуха при приготовлении растворов (20 ± 2)°С;
- температура воздуха при выполнении измерений (20 ± 5)°С;
- атмосферное давление 84,0-106,7 кПа (630 - 800 мм рт. ст.);
- влажность воздуха (65 ±15)% при температуре 25°С;
- напряжение питающей сети (220 ± 10) В;
- частота переменного тока (50 ± 0,5) Гц.
Помещения для проведения измерений должны быть оснащены приточно-вытяжной вентиляцией и подводкой воды.
8 Подготовка к выполнению измерений
Перед выполнением измерений должны быть проведены следующие работы: подготовка измерительной аппаратуры, приготовление растворов, отбор и подготовка проб к анализу.
8.1 Подготовка измерительной аппаратуры
Включают спектрофотометр согласно инструкции по эксплуатации. Устанавливают рабочий режим измерения длины волны 450 нм (или 465 нм). Измерения проводят не раньше, чем через 30 минут после включения прибора.
8.2 Приготовление растворов
8.2.1 Приготовление смеси ацетон:гексан (1:1)
В колбе вместимостью 250 см3 с пришлифованной пробкой смешивают 100 см3 ацетона и 100 см3 гексана при (20±2) °С. Готовится непосредственно перед анализом.
8.2.2 Приготовление водного раствора 50 % NaOH
К 50 г NaOH добавляют 50 см3 дистиллированной воды, осторожно перемешивают и охлаждают до комнатной температуры. Годен 6 мес. Хранить в стеклянной посуде с притертой полимерной пробкой при комнатной температуре в затемненном месте.
8.2.3 Приготовление спиртового раствора 10 % NaOH
К 10 г NaOH добавляют 112,3 см3 этилового спирта (р=0,8014), осторо^койеремешивают и
„ ?!■•- [ ГУ?
охлаждают до комнатной температуры. Готовится непосредственно перед анализом. '’тианои / ?
8.3 Подготовка анализируемых образцов
Отбор проб осуществляется согласно ТИПА на продукцию.
Анализируемый продукт 400 - 500 г термостатируют при температуре (20 ± 2) °С в течение 30 минут. Твердые образцы предварительно измельчают с помощью ножа, терки, ступки и т.п., гомогенизируют в блендере, тщательно перемешивают.
8.3.1 Молочные продукты, детское питание на молочной основе, мясопродукты, яйца, рыбопродукты, кондитерские изделия, продукты переработки растительных масел, пищевые добавки
В том случае, если исследуемый продукт обогащен Р-каротином, навеска образца должна составлять 1 - 7 г, если объект исследования содержит натуральное количество Р-каротина, навеска может быть увеличена до 20 г. Таким образом, навеску образца 1 - 20 г, взвешивают с точностью ± 0,01 г, помещают в круглодонную колбу вместимостью 100 - 250 см3. Если исследуемый образец представляет собой сухой порошок - добавляют небольшое количество дистиллированной воды, достаточное для того, чтобы полностью покрыть анализируемую навеску (10 - 20 см3) и вращательными движениями колбы по часовой стрелке перемешивают содержимое. Затем прибавляют 3-7 см3 раствора 50 % гидроксида натрия для проведения реакции щелочного омыления пробы, 40 см3 этилового спирта для растворения выделяющегося в результате щелочного омыления Р-каротина, а для предотвращения его от разрушения добавляют 0,1 - 0,2 г аскорбиновой кислоты. Смесь кипятят в течение 30 мин на водяной бане 90°С с обратным холодильником. Содержимое колбы охлаждают под струей холодной воды до комнатной температуры и количественно переносят в делительную воронку. Колбу ополаскивают 50 см3 дистиллированной воды и переносят в ту же делительную воронку. Признаком полного омыления служит то, что после добавления воды смесь остается прозрачной. При образовании мути необходимо повторить омыление с новой навеской, увеличив количество щелочи для омыления (но не более 7 см3). После омыления выделившийся Р-каротин экстрагируют из смеси диэтиловым эфиром трижды. В первый раз для экстракции используют 50 см3 диэтилового эфира, в двух последующих - по 30 см3. Объединенные экстракты переносят в делительную воронку и отмывают дистиллированной водой от щелочи, контролируя pH промывной воды до нейтральной реакции по фенолфталеину. К экстракту добавляют 8 - 10 г безводного сульфата натрия (Na2S04), выдерживают 20-30 мин в темном месте и фильтруют в круглодонную колбу, промывая Na2SC>4 небольшими порциями эфира. Эфир отгоняют под вакуумом на ротационном испарителе. Сухой остаток растворяют в точном объеме гексана (но не менее 5 см3).
8.3.2 Концентраты пищевые, хлеб, мука, макаронные изделия, детское п^ЩпамШЗШ зерновой ОСНОве //£';/Оглы нглчно- \-v"
Навеску образца 3 - 5 г взвешивают с точностью ± 0,01 г, помещают в Химический' стакан S
вместимостью 100 см3, добавляют 20 см3 дистиллированной воды, перемешивают стеклянной палочкой и оставляют на 20 мин. Затем экстрагируют (3-каротин смесью ацетон:гексан (1:1), приливая по 25 см3 экстрагирующего раствора в стакан с подготовленной пробой, перемешивают стеклянной палочкой в течение 1-2 мин и дают смеси отстояться 3-5 мин. Образовавшийся верхний слой, содержащий p-каротин, аккуратно сливают в делительную воронку. Экстракцию повторяют 3-5 раз до тех пор, пока экстрагирующий раствор не перестанет окрашиваться извлекаемым p-каротином (свидетельствует о том, что p-каротин полностью извлечен). Объединенные гексановые экстракты отмывают от ацетона дистиллированной водой порциями по 60- 70 см3 пять раз. Гексановый экстракт переносят в коническую колбу, добавляют 8 - 10 г безводного сульфата натрия, выдерживают 20-30 мин в темном месте и фильтруют в мерную колбу вместимостью 100 -200 см3, промывая Na2SC>4 небольшими порциями гексана. Объем доводят гексаном до метки.
8.3.3 Плодоовощная продукция, напитки, чай, БАД на растительной основе
а) Навеску пастообразного или сухого образца 1 - 3 г взвешивают с точностью ± 0,01 г, помещают в химический стакан вместимостью 50 см3, добавляют 10 см3 дистиллированной воды, перемешивают. Затем экстрагируют Р-каротин 15 см3 ацетона, перемешивают стеклянной палочкой 1-2 мин и дают смеси отстояться 3-5 мин. Образовавшийся верхний слой, содержащий Р-каротин, аккуратно сливают в делительную воронку. Экстракцию повторяют до тех пор, пока последняя порция ацетона не перестанет окрашиваться извлекаемым p-каротином. Затем объединенные ацетоновые экстракты встряхивают в делительной воронке с 15 см3 гексана.
б) Жидкие продукты в количестве 10 -20 г взвешивают с точностью ± 0,01 г, помещают в делительную воронку, добавляют 20 см3 ацетона, встряхивают в течение 1-2 мин, затем добавляют 15 см3 гексана.
P-Каротин переходит из нижнего ацетонового слоя в верхний гексановый слой, который собирают в отдельную колбу. Если после встряхивания слои полностью не разделились, добавляют 2-3 см3 дистиллированной воды. Экстракцию гексаном повторяют еще 2 раза по 15 см3. Объединенные гексановые экстракты помещают в делительную воронку и отмывают от ацетона дистиллированной водой порциями по 60 - 70 см3 4-5 раз. Г ексановый экстракт переносят в коническую колбу, добавляют 8 - 10 г безводного сульфата натрия, выдерживают 20-30 мин в темном месте и фильтруют в мерную колбу вместимостью 100 - 200 см3, промывая Na2S04 небольшими порциями гексана. Объем доводят гексаном до метки.
При визуально обнаруживаемом содержании хлорофилла в гексановом экстракте (экстракт зеленого цвета) проводят его очистку. Гексановый экстракт помещают в делительную воронку, прибавляют равный объем 10 % спиртового раствора NaOH. Смесь встряхиваюъДб' тбх пор,- пока
при визуальном наблюдении хлорофиллы не перейдут в нижний слой спирт^вбй щелочи (зеленая
П'1 ! ;sj|
окраска), который затем сливают. Верхний слой многократно промывают водой' до ЦёйтрдтглЦ >й
реакции по фенолфталеину. Гексановый экстракт переносят в коническую колбу, добавляют 8 - 10 г безводного сульфата натрия, выдерживают 20-30 мин в темном месте и фильтруют в мерную колбу вместимостью 100 - 200 см3, промывая Na2SC>4 небольшими порциями гексана. Объем доводят гексаном до метки.
При анализе продуктов из моркови и моркови в смеси с компонентами, не содержащими 13-каротин, очистку экстракта не производят.
8.3.4 Премиксы, БАД
а) Навеску образца 0,1 - 1,5 г, взвешенную с точностью ± 0,001 г, помещают в мерную колбу вместимостью 250 см3, добавляют 80 -100 см3 дистиллированной воды, перемешивают до растворения навески и доводят объем до метки дистиллированной водой. Отбирают 5 см3 полученного раствора, помещают в делительную воронку, добавляют 40 см3 ацетона. Из полученной смеси экстрагируют Р-каротин гексаном трижды порциями по 30 см3. Объединенные гексановые экстракты, содержащие Р-каротин, помещают в делительную воронку и отмывают гексановый слой от ацетона Дистиллированной водой порциями по 60- 70 см3 пять раз. Гексановый экстракт Р-каротина переносят в коническую колбу, добавляют 8 - 10 г безводного сульфата натрия, выдерживают 20-30 мин в темном месте и фильтруют в мерную колбу вместимостью 100 - 200 см3, промывая Na2SC>4 небольшими порциями гексана. Объем доводят гексаном до метки.
б) При определении Р-каротина в маслах, обогащенных p-каротином, навеску образца 1,0 - 10 г, взвешенную с точностью ± 0,01 г, помещают в мерную колбу, вместимостью 100 - 200 см3, добавляют 40 - 60 см3 хлороформа, перемешивают, доводят объем до метки хлороформом.
9 Выполнение измерений
Анализ проводится на спектрофотометре. Полученные по п. 8.3 экстракты помещают в кювету для спектрофотометрирования с толщиной поглощающего свет слоя 1 см3. Оптическую плотность гексановых экстрактов измеряют при длине волны 450 нм, раствором сравнения служит гексан. Оптическую плотность хлороформенных экстрактов измеряют при длине волны 465 нм, раствором сравнения служит хлороформ. Проводят анализ двух параллельных проб.
10 Обработка результатов измерений
Расчет концентрации Р-каротина X (мг/100 г) проводится по формуле:
10 х 100 х £) х Г
Е]% х т
1 СМ
хК,
X
О)
где D — оптическая плотность измеряемого раствора, (ед. оптич. плотности); V- конечный объем гексанового (хлороформенного) экстракта, см3;
т - масса навески, г;
Е\м ~ удельный показатель поглощения для 1% раствора р-каротина в 1 см3 органического растворителя, (ед. оптич. плотности х см3мг'1см"1): для гексана Е\°'°м = 2550; для хлороформа^ =2592;
10 - коэффициент пересчета в мг;
100 - пересчет на 100 г продукта;
К - коэффициент разбавления (К=1 для п.8.3.1. - 8.3.3. и п. 8.3.4. б); К=5 для п. 8.3.4. а)).
За окончательный результат измерения принимают среднее арифметическое значение результатов двух параллельных определений. Вычисления проводят до третьего знака после запятой и округляют до второго.
После проверки полученных результатов параллельных определений по критерию повторяемости по п.12 рассчитывают X.
Результат анализа X, рассчитывают по формуле (2):
'X=bllxj (2)
2
где Xj - результат первого параллельного определения;
Х2 - результат второго параллельного определения;
Гарантированный результат измерений, выдаваемый лабораторией, может быть представлен в виде
(X ± U(X)), мг/100 г, (3)
где X - среднее арифметическое из результатов измерений 2-х параллельных проб, полученное в соответствии с п.9 и рассчитанное согласно п.10;
U(X) — абсолютное значение расширенной неопределенности результата измерений X,
мг/100 г. Рассчитывается по формуле:
U(X) = U х0,01хХ, (4)
где U - относительное значение расширенной стандартной неопределенности, вычисленное в соответствии с Приложением Б
Если величина X оказывается меньше предела измерения методики (Cloq), то вычисления по п.10 не производятся, а дается односторонняя оценка массовой концентрации Р-каротина в пробе в виде Х< (Cloq), где Cloq - нижний предел измерения методики для группы продуктов:
(5)
г 10 х 100 х £)min х V
^ LOO т-,1%
где Dmin =0,6375Б
11 Оформление результатов измерений
Результаты измерений оформляют по форме, установленной действующей в лаборатории системой регистрации данных.
Результаты должны включать следующую информацию: $ ".’Г: - -