Инструкция 1.1.11-12-35-2004
Требования к постановке экспериментальных исследований для первичной токсикологической оценки и гигиенической регламентации веществ
Купить Инструкция 1.1.11-12-35-2004 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Инструкция предназначена для учреждений Министерства здравоохранения Республики Беларусь и других ведомств, уполномоченных на проведение исследований по токсикологической оценке и гигиенической регламентации химических веществ, материалов, изделий и продуктов, независимо от области их производства и применения.
Оглавление
Глава 1 Область применения
Глава 2 Термины и определения
Глава 3 Объем исследований
Глава 4 Исследования по установлению параметров токсичности и оценке потенциальной опасности острого отравления
Глава 5 Исследования раздражающего действия на слизистые глаз
Глава 6 Оценка местно-раздражающих и кожно-резорбтивных свойств
Глава 7 Исследования кумуляционных свойств
Глава 8 Оценка сенсибилизирующих свойств
Глава 9 Токсиколого-гигиеническая интерпретация результатов экспериментальных исследований
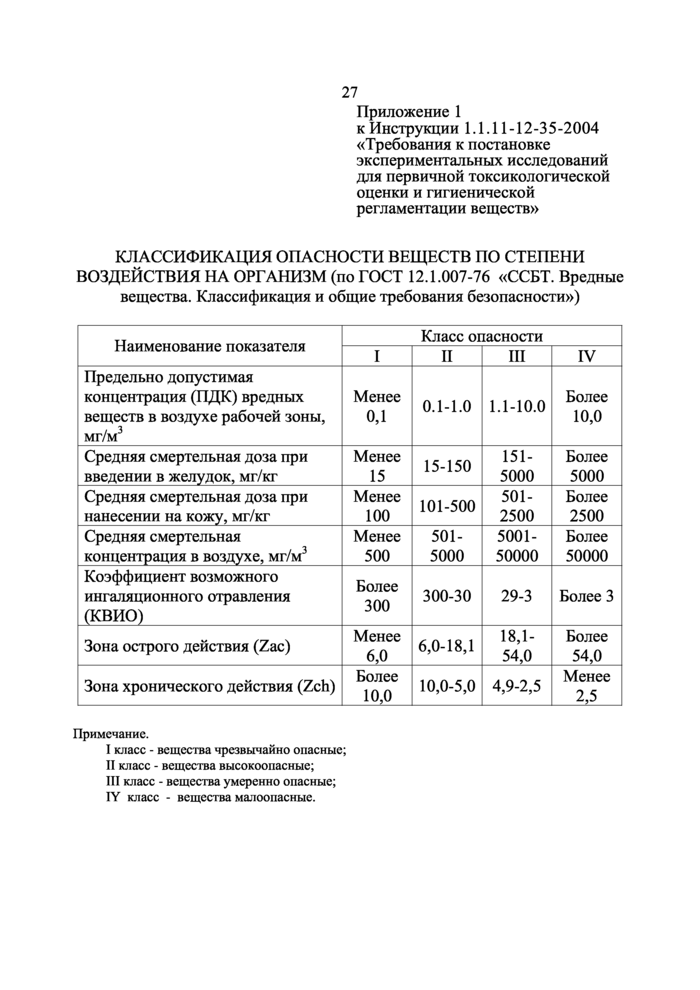
Приложение 1 Классификация опасности веществ по степени воздействия на организм
Приложение 2 Зависимость характера видовой чувствительности животных от величины коэффициента видовой чувствительности
Приложение 3 Оценка раздражающего действия химических соединений на слизистые оболочки глаз кроликов
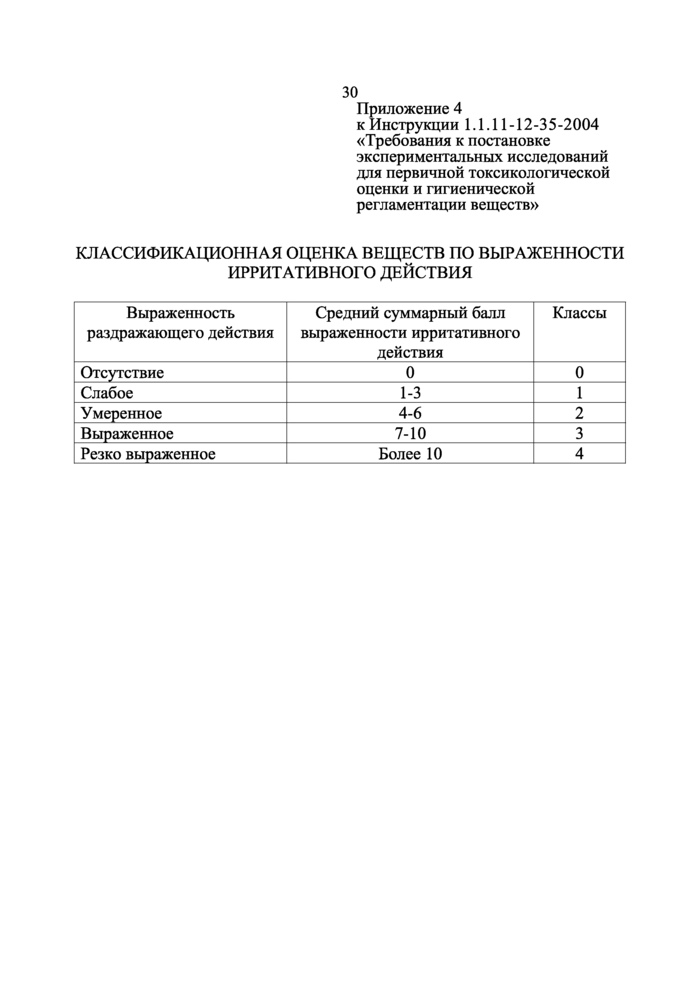
Приложение 4 Классификационная оценка веществ по выраженности ирритативного действия
Приложение 5 Оценка состояния кожи при изучении местного действия веществ
Приложение 6 Классификация выраженности кожно-раздражающих свойств веществ при их однократном местном воздействии
Приложение 7 Рекомендуемые сроки изучения морфофункциональных показателей организма животных при проведении подострого эксперимента
Приложение 8 Ориентировочный перечень морфофункциональных показателей организма животных, рекомендуемый к изучению в подостром эксперименте
Приложение 9 Методические приемы выявления сенсибилизирующей способности вещества
Приложение 10 Рекомендуемая форма представления результатов первичной токсикологической оценки химических веществ
Информационные данные
| Дата введения | 03.01.2005 |
|---|---|
| Добавлен в базу | 01.01.2018 |
| Актуализация | 01.01.2021 |
Организации:
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26
стр. 27

стр. 28

стр. 29
стр. 30
Министерство здравоохранения Республики Беларусь
Инструкция 1.1.11-12-35-2004 ТРЕБОВАНИЯ К ПОСТАНОВКЕ ЭКСПЕРИМЕНТАЛЬНЫХ ИССЛЕДОВАНИЙ ДЛЯ ПЕРВИЧНОЙ ТОКСИКОЛОГИЧЕСКОЙ ОЦЕНКИ И ГИГИЕНИЧЕСКОЙ РЕГЛАМЕНТАЦИИ ВЕЩЕСТВ
Минск - 2004
|
2 |
РЕСПУБЛИКА БЕЛАРУСЬ
РЭСПУБЛ1КА БЕЛАРУСЬ
Министерство здравоохранения
ГЛАВНЫЙ ГОСУДАРСТВЕННЫЙ САНИТАРНЫЙ ВРАЧ РЕСПУБЛИКИ БЕЛАРУСЬ
Телефон 212-49-9" 22MM8.I. Минск. >л Мкишеом. 39
факс 220-64-59 E-mua:Vklucheno\xltdbdrmi.b>'
М|И1Стэрства аховы здарофя
ГАЛОУНЫ ДЗЯРЖАУНЫ САШТАРНЫ РРАЧ РЭСПУБЛ1К1 БЕЛАРУСЬ
220ОД8.1.Микк.в>.1. Мжшком. 39 факс 220-64-59 E-mail:Vlli>chcno\xh:u.bekmi Ы
pe&rfytl__20о£г..**
На2*_
ПОСТАНОВЛЕНИЕ No 131
Об утверждении Инструкции 1.1.11-12-35-2004 «Требования к постановке экспериментальных исследований для первичной токсикологической оценки и гигиенической регламентации веществ»
В целях исполнения Закона Республики Беларусь «О санитарноэпидемическом благополучии населения» в редакции от 23 мая 2000 года (Национальный реестр правовых актов Республики Беларусь, 2000 г., № 52, 2/172) постановляю:
1. Утвердить прилагаемую Инструкцию 1.1.11-12-35-2004 «Требования к постановке экспериментальных исследований для первичной токсикологической оценки и гигиенической регламентации веществ» и ввести ее в действие на территории Республики Беларусь с 03 января 2005 г.
2. С момента введения в действие Инструкции 1.1.11-12-35-2004 «Требования к постановке экспериментальных исследований для первичной токсикологической оценки и гигиенической регламентации веществ» считать утратившими силу на территории Республики Беларусь Методические указания «Постановка исследований в объеме первичной токсикологической оценки веществ», утвержденные Главным государственным санитарным врачом Республики Беларусь 30 июня 1994 г., № 48-9405.
3. Главному врачу ГУ «Республиканский центр гигиены, эпидемиологии и общественного здоровья» Филонову В.П., главным государственным санитарным врачам областей и г.Минска довести
11
Регистрируются наличие рвоты, видимые кровоизлияния, частота дыхания, мышечные подергивания, тремор, судороги, парезы, параличи, температура тела, окраска ушей, конечностей, глаз, развитие наркотического или коматозного состояния и других симптомов интоксикации. Особое внимание обращают на сроки гибели животных. Погибших и выживших животных следует подвергать макроскопическому и/или патоморфологическому исследованию. При этом для вскрытия отбираются только те особи, гибель которых наступила не позже чем за 3-5 часов до патоморфологического исследования.
22. Классификацию веществ по степени их опасности в условиях однократного внутрижелудочного воздействия проводят согласно приложению 1 настоящей Инструкции. При отнесении изучаемого вещества к I-II классам опасности (чрезвычайно- или высокоопасные химические соединения) дальнейшие исследования проводят не в объеме первичной токсикологической оценки, а по программе гигиенического нормирования соединения в окружающей среде (воздух рабочей зоны, атмосферный воздух, вода водоемов и т.д.).
23. Оценку особенностей проявления видовой резистентности животных к токсическому действию вещества осуществляют с использованием показателя КВЧ. Интерпретацию результатов исследования видовой чувствительности проводят согласно приложению 2 настоящей Инструкции.
При определении величины КВЧ от 3,1-9,0 необходимо установить среднесмертельную дозу вещества на третьем виде животных (целесообразно методом «одной точки»), а все дальнейшие исследования, в первую очередь подострые эксперименты, проводить на наиболее чувствительном к данному веществу виду лабораторных животных.
24. Для оценки потенциальной опасности развития острого отравления веществ (строительные и отделочные материалы, лакокрасочные изделия, изделия хозяйственно-бытового назначения, одорирующие вещества, косметические отдушки, посуда, изделия детского обихода, изделия медицинского назначения и др.) для целей их гигиенической регистрации или сертификации рекомендуются следующие методы исследований:
статическая ингаляционная затравка;
метод свободного выпаивания и/или однократного введения в желудок белых крыс водных вытяжек из изделий;
метод оценки однократной внутрибрюшинной токсичности;
25. Определение вероятности развития острого отравления возможно с использованием экспресс-методик на клеточных тест-объектах (бычья сперма и др.). При положительных результатах таких экспериментов обяза-
12
тельным условием является использование теплокровных животных (белые крысы, белые мыши и др.).
26. Задачей статической ингаляционной затравки является установление способности веществ (химических соединений, мигрирующих из них) вызывать гибель или клинические симптомы интоксикации лабораторных животных, что позволит судить о степени их потенциальной опасности в плане возможности развития острого отравления. Статическая ингаляционная затравка проводится однократно с использованием половозрелых белых мышей или крыс. Количество животных в опыте не менее 6 штук. Продолжительность статической затравки - 2 часа (для мышей) и 4 часа (для крыс).
Основные требования к устройствам для затравки: инертность конструктивного материала (предпочтительно стекло или неокрашенная нержавеющая сталь);
отсутствие прямого контакта испытуемого вещества с кожными покровами экспериментальных животных (оборудование специальной подставки и домиков для размещения животных);
возможность визуального наблюдения во время затравки (оборудование смотровых окон в конструкциях из нержавеющей стали);
доступность тщательной уборки устройства после проведения эксперимента;
достаточность воздухообмена (наличие воздушно-отводного патрубка, температура внутри устройства не должна превышать 25-27°С); герметичность основных конструктивных узлов устройств; наличие приспособления для отбора проб воздуха (при необходимости) из затравочных устройств при проведении эксперимента.
Наиболее приемлемыми и доступными устройствами для статической ингаляционной затравки являются эксикаторы, стеклянные бутыли (емкостью от 20 л). Возможны другие конструкции устройств, отвечающие вышеуказанным требованиям.
Вещество (изделия) помещают в затравочное устройство с животными из расчета:
1 м2/м3 (обои, панели, пластики и пр.; лакокрасочные материалы, после их высыхания на стеклянной или металлической пластине);
косметические отдушки, деодоранты, дезинфектанты, антисептики и прочие изделия бытовой химии (при наличии сведений о летучести) наливаются в чашки Петри для свободного испарения (максимально насыщающие концентрации), а вещества в аэрозольной упаковке распыляются в течение времени, соответствующему инструкции по применению для конкретной продукции.
13
27. Для оценки потенциальной опасности развития острого внутри-желудочного и внутрибрюшинного отравления (общетоксическое действие) используются водные вытяжки из изделий. Условия приготовления вытяжек аналогичны таковым при проведении санитарно-химических исследований, зависят от вида изделий, их назначения.
Эксперименты проводятся на здоровых половозрелых белых крысах обоего пола (в группе должно быть не менее 3-5 животных).
Метод свободного выпаивания заключается в том, что животным, лишенным корма в течение суток, дают пить вытяжки из изделий, которые заливают в поилки вместо питьевой вода. Отмечается количество выпитой вытяжки. Отказ животного от приема вытяжки является неблагоприятным прогностическим признаком.
28. Вместо свободного выпаивания можно применять метод однократного введения вытяжек в желудок белых крыс (натощак) с помощью иглы-зонда в объеме 3 мл/200 грамм массы животного или брюшную полость белых мышей (натощак) в объеме 1 мл/ 20 грамм массы животного. Кормление животных необходимо осуществлять через сутки после манипуляций.
Визуально оценивается общее состояние животных, клинические симптомы интоксикации, регистрируется возможная гибель в период затравок и в течение суток после них. При отсутствии сведений о химическом составе изделий в затравочных устройствах можно проводить замеры концентраций веществ, потенциально способных мигрировать из изделий. Дополнительно (при необходимости) осуществляются лабораторные исследования животных после затравок.
ГЛАВА 5
ИССЛЕДОВАНИЯ РАЗДРАЖАЮЩЕГО ДЕЙСТВИЯ НА СЛИЗИСТЫЕ ГЛАЗ
29. Для проведения испытаний берут не менее 3-х кроликов или морских свинок, в нижний конъюнктивальный свод правый глаз которых однократно вносится исследуемое вещество в нативном виде в количестве 50-100 мкл (для жидких, в т.ч. вытяжек) и 50-100 мкг (порошок), левый глаз при этом служит в качестве контрольного (закапывается 1-2 капли дистиллированной воды).
30. В случаях невозможности использования веществ в нативном виде допускается их применение в разбавленном виде. В качестве раство-рителей/разбавителей следует применять индифферентные вещества,
14
перечень которых указан в главе 4 настоящей Инструкции. При этом растворитель вносится в контрольный глаз кроликов в эквивалентных количествах.
31. Вещества, обладающие выраженными кислотными (pH < 2,5 ед.) и щелочными (pH > 12,5 ед.) свойствами, а также вызывающие раздражение кожных покровов (1 балл) исследованию раздражающих эффектов на слизистую глаз не подвергаются.
Визуальное наблюдение за состоянием слизистой и конъюнктивы глаз подопытных животных проводится на протяжении 24 часов - при отсутствии раздражения и инстиляции вытяжек (через 1 и 24 часа после воздействия) и в течение двух недель (для веществ, обладающих выраженным раздражающим действием). Регистрируются признаки раздражения слизистой оболочки (слезотечение, птоз, блефароспазм, инъецирование сосудов, набухание век и т.д.), их выраженность и длительность.
32. Оценку степени выраженности раздражающего действия веществ (вытяжек) на слизистые оболочки глаз и их классификационную оценку по данному признаку проводят согласно приложениям 3 и 4 настоящей Инструкции.
ГЛАВА 6
ОЦЕНКА МЕСТНО-РАЗДРАЖАЮЩИХ И КОЖНО-РЕЗОРБТИВНЫХ
свойств
33. Задачей исследований по изучению особенностей эпикутанного воздействия веществ является оценка степени проявления их кожно-раздражающих и кожно-резорбтивных свойств при однократных и повторных аппликациях экспериментальным животным.
В результате проведения опытов представляется возможным:
получить данные по оценке реальной опасности возникновения острых и подострых проявлений воздействия веществ на кожные покровы;
обосновать необходимость технологических и специальных защитных мероприятий, направленных на полное или максимальное исключение контакта кожных покровов работающих с вредными веществами.
34. Изучение местно-раздражающих и кожно-резорбтивных свойств веществ проводят путем их однократных и повторных аппликаций на кожу спины или хвосты экспериментальных животных. Количество животных в группе не менее 6 особей.
Участок аппликации должен составлять 5% общей поверхности кожи животных, что соответствует поверхности 2/3 хвоста у крыс или участку
15
кожи на спине крыс 4x4 см, морских свинок 5x5 см, кроликов 7x8 см. За сутки до эксперимента тщательно выстригают ножницами или электромашинкой шерсть на боковой поверхности или спине. Применение депиляторов недопустимо. В опыт пригодны животные с чистой здоровой кожей без механических повреждений. Для изучения местного действия шерсть выстригают на симметричных участках спины по обе стороны от позвоночника, оставляя шерстяной покров между ними в 1-2 см. Правый бок служит для аппликации изучаемого вещества, левый - для контроля.
На время экспозиции, для исключения слизывания вещества с кожи и поступления его через органы дыхания, животных фиксируют в специальных индивидуальных домиках.
Вещество наносят на кожные покровы лабораторных животных, как правило, в нативном виде. В случае невозможности нанесения вещества per se, а также при наличии выраженного раздражающего либо токсического эффекта при проведении подострого эксперимента применяют разведение вещества. При этом в опыте используют недействующую концентрацию. В качестве растворителей и разбавителей следует использовать дистиллированную воду, допускается применение растительного и вазелинового масел, разбавленных растворов этилового спирта и ацетона. Нанесение вещества осуществляется открытым способом при температуре окружающей среды 18-24°С. Для летучих веществ (температура кипения до 160°С) следует использовать закрытый способ: компрессный метод, метод наклейки капсул и часовых стекол. Контрольные животные должны находиться в одинаковых условиях. На соответствующие участки кожи им наносится раство-ритель/разбавитель, используемый в опыте. При изучении местного действия контролем служит противоположный участок кожи того же животного.
По окончании аппликаций необходимо остатки вещества удалить теплой водой с мылом или растворителем, избегая грубых приемов и манипуляций, способных вызывать повреждение кожи. Жидкость, применяемая для смыва, должна обладать способностью растворять исследуемое вещество и быть безвредной как для кожи, так и для целостного организма. Ватным тампоном, смоченным в жидкости, проводится смыв с участка кожи, на котором проводили аппликацию вещества. Манипуляцию повторяют не менее 2-х раз, последним сухим - промокают участок кожи.
35. Исследования по оценке местно-раздражающих свойств вещества проводят в однократных и повторных (20-кратные аппликации по 5 раз в неделю) опытах. На кожные покровы лабораторных животных равномерно наносится вещество в дозе 20 мг/см2. Ежедневная экспозиция составляет 4 часа. Период наблюдений за клиническими проявлениями интоксикации и
16
состоянием кожных покровов, включая инструментальные исследования, проводят через 1 и 16 часов после аппликации и смыва остатков вещества. Расчет ведется по каждому животному и затем вычисляется среднегрупповой показатель.
Функциональные нарушения кожи характеризуются появлением различной степени выраженности эритемы, отека, трещин, изъязвлений, изменением ее температуры и уменьшением нейтрализующей способности. Оценка в баллах функционального состояния кожи по выраженности эритемы и величины отека и классификация выраженности раздражающих свойств веществ, приведены в приложениях 5, 6 настоящей Инструкции.
Вещества, относящиеся к 5 классу, дальнейшему изучению кожно-резорбтивного действия не подлежат. Для веществ, относящихся к 4-5 классам раздражающего действия на кожу, ставится пометка «опасно при контакте с кожными покровами».
36. Определение степени опасности острого отравления при чрез-кожном поступлении веществ (DL50 он)-
Для определения DL50 аа на выстриженный участок спины опытных лабораторных животных (4x5 см для белых крыс, 5x6 см для морских свинок, 7x9 см для кроликов) наносят исследуемое вещество из расчета 100-2500 мг/кг веса животного и втирают его в кожу стеклянной или деревянной палочкой легкими массирующими движениями. Для предотвращения слизыва-ния животных фиксируют в специальных домиках до высыхания вещества, но не менее чем на 4 часа. Сухие вещества целесообразно растворять либо увлажнять индифферентными жидкостями (дистиллированная вода, глицерин, растительное масло, полиэтиленгликоль и др.), расчет дозы при этом рассчитывают по действующему (исследуемому) веществу.
В качестве контроля выступает группа животных, которым апплици-руется растворитель.
Наблюдение за состоянием животных в первые 8 часов после нанесения проводится ежечасно, в последующие 2 недели - ежесуточно с регистрацией поведения, особенностей клинической картины отравления, сроков гибели животных. Возможно сокращение сроков наблюдения в зависимости от наличия симптомов интоксикации.
Классификацию веществ по степени опасности острого отравления ими проводят согласно приложению 1 настоящей Инструкции.
37. Задачей этапа исследований по оценке кожно-резорбтивного действия является получение альтернативного ответа о возможности вещества проникать через неповрежденную кожу и вызывать интоксикацию организма при многократном воздействии.
3
данное постановление до сведения всех заинтересованных и установить контроль за его исполнением.
4
УТВЕРЖДЕНО Постановление Главного государственного санитарного врача Республики Беларусь «14» декабря 2004 № 131
Инструкция 1.1.11-12-35-2004 «ТРЕБОВАНИЯ К ПОСТАНОВКЕ ЭКСПЕРИМЕНТАЛЬНЫХ ИССЛЕДОВАНИЙ ДЛЯ ПЕРВИЧНОЙ ТОКСИКОЛОГИЧЕСКОЙ ОЦЕНКИ И ГИГИЕНИЧЕСКОЙ РЕГЛАМЕНТАЦИИ ВЕЩЕСТВ»
ГЛАВА 1 ОБЛАСТЬ ПРИМЕНЕНИЯ
1. Настоящая Инструкция предназначена для учреждений Министерства здравоохранения Республики Беларусь (далее - Минздрав) и других ведомств, уполномоченных на проведение исследований по токсикологической оценке и гигиенической регламентации химических веществ, материалов, изделий и продуктов (далее - веществ), независимо от области их производства и применения.
2. Первичная токсикологическая оценка, паспортизация и гигиеническая регламентация веществ осуществляется учреждениями и подразделениями токсиколого-гигиенического профиля, аккредитованными на право проведения такого рода исследований Минздравом и Госстандартом Республики Беларусь.
3. Требования положений Инструкции применяются для токсикологогигиенического изучения безопасности веществ.
4. Инструкция устанавливает порядок проведения, единые методические подходы, схемы, принципы и методы изучения веществ с целью обеспечения предприятий, учреждений и организаций исходными данными для составления нормативной документации, проектирования производств, разработки оздоровительных и профилактических мероприятий, выдачи гигиенического заключения для осуществления предупредительного и текущего государственного санитарного надзора (далее - госсаннадзора), а также для проведения государственной гигиенической регистрации, регламентации, сертификации веществ.
5
5. Токсикологические исследования в объеме первичной оценки новых веществ, которые являются или содержат в своем составе чрезвычайно опасные и высокоопасные компоненты, не имеющие токсиколого-гигиенических характеристик и гигиенических регламентов их содержания в окружающей среде, проводятся на стадии научного исследования и составления лабораторного технологического регламента производства. Результаты первичной токсикологической оценки, устанавливающие, что изучаемое вещество относится к умеренно- и малоопасным, или содержит таковые в своем составе, могут быть использованы для последующего обоснования гигиенических нормативов, разработки временных технологических регламентов и технических условий на опытную партию на стадии опытного производства с их согласованием с органами и учреждениями госсаннадзора.
6. Представление веществ для первичной токсикологической оценки и государственной гигиенической регистрации осуществляется заказчиком с соблюдением требований, изложенных в постановлении Совета Министров Республики Беларусь от 14 декабря 2001 г. №1807 «О совершенствовании системы государственной гигиенической регламентации и регистрации химических и биологических веществ, материалов, и изделий из них, продукции производственно-технического назначения, товаров для личных (бытовых) нужд, продуктов питания на территории Республики Беларусь» (Национальный Реестр правовых актов Республики Беларусь, 2002 г., №1, 5/9611), постановлении Главного государственного санитарного врача Республики Беларусь от 13 ноября 2000 г. №54 «Об утверждении Положения о порядке осуществления государственной гигиенической регламентации и регистрации химических и биологических веществ, материалов и изделий из них, продукции производственно-технического назначения, товаров для личных (бытовых) нужд, продуктов питания на территории Республики Беларусь и перечня продукции, подлежащей государственной гигиенической регистрации» и постановлении Министерства здравоохранения Республики Беларусь от 08 октября 2003 г. №44 «Об утверждении перечня химических и биологических веществ, материалов и изделий из них, продукции производственно-технического назначения, товаров для личных (бытовых) нужд, продовольственного сырья и пищевых продуктов, а также материалов и изделий, применяемых для производства, упаковки, хранения, транспортировки, продажи, иных способов отчуждения продовольственного сырья и пищевых продуктов и их использования, подлежащих государственной гигиенической регламентации и регистрации».
7. Отбор образцов на исследования для целей государственной гигиенической регламентации и регистрации производится в соответствии с
6
нормативной документацией (СанПиН, ГОСТ, СТБ, ОСТ, ТУ, ВМУ и другие) на конкретную продукцию организациями, уполномоченными на данный вид деятельности. Организации, разрабатывающие или представляющие вещества для исследований, несут ответственность за достоверность представленной информации о веществе (-ах) в соответствии с действующим законодательством Республики Беларусь.
ГЛАВА 2 ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
8. Вещество - предмет государственной гигиенической регламентации и регистрации, которым могут быть химические и биологические вещества, материалы и изделия из них, продукция производственно-технического назначения, товары для личных (бытовых) нужд, продукты питания, производимые в Республике Беларусь или ввозимые из-за ее пределов и применяемые в народном хозяйстве и быту, а также соединения, возникающие в ходе технологических процессов производства и поступающие в окружающую среду в виде отходов производства и побочных продуктов.
Среднесмертельная концентрация (CL50) вещества (мг/м3) - концентрация, вызывающая гибель 50% мышей или крыс при соответственно 2 и 4 часовом воздействии и последующим 14-суточном периоде наблюдения.
Смертельная доза (DL50) вещества (мг/кг) - доза, вызывающая гибель 50% мышей или крыс при однократном введении вещества и последующим 14-суточном периоде наблюдения.
Коэффициент видовой чувствительности (далее - КВЧ) - представляющий собой показатель соотношения среднесмертельных доз более устойчивого вида животных к менее резистентному (например, DLsoKpucbi / DL50 мыши).
Местно-раздражающие свойства вещества - способность вещества в условиях однократного или повторного воздействия оказывать раздражающее действие на кожные покровы или слизистые.
Кожно-резорбтивные свойства вещества - способность вещества при однократном или повторном воздействии проникать через неповрежденные кожные покровы и вызывать интоксикацию организма.
Кумулятивные свойства вещества - способность вещества при повторном поступлении накапливаться в организме и оказывать неблагоприятное действие на уровне проявления смертельных эффектов или на функциональное состояние ряда органов и систем подопытных животных (функциональная и материальная кумуляция).
7
Коэффициент кумуляции (КошО - рассчитывается отношением суммарной дозы вещества при многократном введении, вызвавшей гибель 50% животных, взятых в эксперимент, к DL5o. установленной при однократном введении.
Потенциальная аллергенная опасность - способность вещества в условиях однократной внутрикожной сенсибилизации проявлять аллергизи-рующую активность.
Токсичность - мера несовместимости вещества с жизнью; величина обратная абсолютному значению среднесмертельной дозы (I/DL50) или (I/CL50).
ГЛАВА 3 ОБЪЕМ ИССЛЕДОВАНИЙ
9. Исследования предусматривают оценку токсичности и опасности веществ при воздействии на организм лабораторных животных путями, адекватными реальным условиям трудовой деятельности и обитания человека.
10. Объем исследований при первичной токсикологической оценке и гигиенической регламентации вещества включает:
проведение литературно-информационного поиска сведений, отражающих биологические свойства и токсиколого-гигиеническую характеристику изучаемого вещества и его аналогов;
установление параметров острой токсичности и потенциальной опасности острого отравления при различных путях поступления (в желудок, внутрибрюшинно, накожно, ингаляционно) в организм животных с учетом половой и видовой чувствительности;
определение способности оказывать местное раздражающее действие на слизистые оболочки глаз;
оценку местно-раздражающих и кожно-резорбтивных свойств при однократном и повторном воздействии;
выявление возможных кумулятивных свойств и получение сведений о преимущественно поражаемых органах и системах организма подопытных животных;
изучение сенсибилизирующей способности при однократном внутри-кожном введении.
11. Объем исследований при наличии достаточных сведений о токсикологической характеристике вещества, его содержания в рецептурах в незначительных количествах может быть сокращен в части, касающейся
8
трудоемких и длительных экспериментов по оценке кумулятивной и сенсибилизирующей активности.
12. Для веществ, в процессе первичной токсикологической оценки которых установлены параметры токсикометрии, классифицирующие их как чрезвычайно- или высокоопасные (1, 2 классы опасности согласно ГОСТ 12.1.007-76 «ССБТ. Вредные вещества. Классификация и общие требования безопасности»), а также обладающих аллергенной активностью или имеющих обоснованные литературные сведения о существовании аналогов, проявляющих канцерогенные или мутагенные свойства, результаты исследований являются недостаточными для выдачи гигиенического заключения о возможности их безопасного применения и служат основанием для продолжения экспериментов по токсиколого-гигиенической регламентации.
13. Исследования проводят на следующих видах половозрелых лабораторных животных: белые мыши (масса 18-22 г); белые крысы (масса 180-220 г); морские свинки (масса 250-400 г); кролики (масса 2000-4000 г). Подбор животных и формирование из них однородных опытных и контрольных групп осуществляют с учетом одинаковой массы тела (среди животных одной группы максимальная разница в массе не должна превышать 10%), отсутствия различий в поведении и общем состоянии.
Содержание животных должно соответствовать требованиям «Санитарных правил по устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)» №1045-73, утвержденных Главным государственным врачом СССР 06 апреля 1973 года.
14. К выполнению токсикологических экспериментов допускаются лица, имеющие среднее или высшее медицинское (биологическое) образование, изучившие требования безопасности и прошедшие подготовку для работы с лабораторными животными согласно «Правилам проведения работ с использованием лабораторных животных», утвержденным Приказом М3 СССР от 12 августа 1977 г. №755.
ГЛАВА 4
ИССЛЕДОВАНИЯ ПО УСТАНОВЛЕНИЮ ПАРАМЕТРОВ ТОКСИЧНОСТИ И ОЦЕНКЕ ПОТЕНЦИАЛЬНОЙ ОПАСНОСТИ ОСТРОГО ОТРАВЛЕНИЯ
15. Задачей данного этапа исследований является определение токсичности и потенциальной опасности веществ и, в первую очередь, установление величины среднесмертельной дозы (DL50), которая выражается отношением миллиграммов вещества, введенного в желудок экспери-
9
ментальных животных с помощью иглы-зонда (DL50 р» о*) или нанесением на неповрежденные кожные покровы (DL50 Cut), к их массе тела в килограммах (мг/кг).
16. В условиях острого опыта представляется возможным:
определить степень токсичности и опасности, диапазон токсического
действия и получить первичную информацию о токсикодинамике вещества;
оценить видовую и половую чувствительность лабораторных животных к действию вещества.
Если неизвестна степень токсичности изучаемого вещества, острые опыты рекомендуется начинать с предварительных экспериментов, в ходе которых устанавливаются ориентировочные уровни смертельных доз. С этой целью на 2-3 белых мышах или крысах испытываются дозы, отличающиеся на порядок (например: 10, 100, 1000 мг/кг и т.д.). Наименьшая доза, после введения которой животное погибло, может рассматриваться как ориентировочная среднесмертельная.
17. После нахождения ориентировочной среднесмертельной дозы ставится развернутый опыт на белых крысах и белых мышах. Учитывая возможную индивидуальную чувствительность животных к действию токсического вещества, нужно подобрать шкалу испытуемых доз с таким расчетом, чтобы предварительно найденная ориентировочная среднесмертельная доза занимала в ней по возможности среднее положение. Каждая выбранная доза испытывается на 6-10 животных. Число животных в группе, а также интервал между дозами в значительной степени зависит от используемого в дальнейшем метода статистического расчета.
18. При обработке результатов острого опыта предпочтение нужно отдавать менее трудоемким методам, в первую очередь, методу Беренса и Беренса-Шлоссера (М.Л.Беленький, 1963), методу Б.В.Прозоровского (1978), компьютерной программе RTGIC «Toxi» производства Copyright (1995). В случаях необходимости проведения сравнительной оценки токсичности нескольких близких по механизму своего действия веществ, более рационально применение метода пробит-анализа Литчфильда и Уилкоксона (М.Л.Беленький, 1963). Этот метод позволяет математически оценивать сравнительную токсичность веществ при параллельности прямых «доза-эффект».
19. Для определения сравнительной видовой чувствительности лабораторных животных к действию вещества в целях экономии количества животных (особенно таких, как морские свинки, кролики) рекомендуется пользоваться методами Deichman a. Le Blanc (1943), а также методом «одной точки» Wan der Warden (1940), сущность которых и техника проведения
10
расчета описана в литературе (В.Б.Прозоровский с соавт., 1978).
20. Выяснение возможных различий в половой резистентности животных к изучаемому веществу достигается путем формирования в процессе экспериментов (предварительного и развернутого) равновеликих по содержанию в них самцов и самок экспериментальных групп. Если в процессе опыта выявлена тенденция к увеличению смертности особей одного пола суммарно во всех группах более чем на 20%, то различия считают сущее-ственными. В таком случае проводят дополнительные исследования по установлению параметров острой токсичности вещества отдельно для самок и самцов. Для получения сопоставимых результатов и нивелирования возрастной чувствительности в опыт следует брать половозрелых животных.
21. Исследуемые вещества вводятся в желудок лабораторных животных натощак в нативном виде, в водном растворе, растительном масле, индифферентных растворителях и эмульгаторах (полиэтиленгликоле, Твин, диметилсульфоксид и т.д.), а также в виде водных вытяжек, масляных эмульсий или крахмальных суспензий. При этом разные дозы вещества следует вводить животным в растворах одинаковой концентрации и оптимальных объемах, составляющих 1-1,5% от массы тела, т.е. 0,2-0,3 мл для мышей (допустимый - 1,0 мл); 2,0-3,0 мл для крыс (допустимый - 5,0 мл) и 4,0-6,0 мл для морских свинок. Кормление животных производится не ранее чем через 3 часа после введения вещества. В опытах следует избегать введения веществ или их растворов, обладающих выраженными раздражающими свойствами, в том числе, кислотными или щелочными. Это может привести к ошибкам в трактовке результатов. Такого рода вещества целесообразно вводить в виде масляных растворов или на 1,0-2,0% крахмальном клейстере.
При отсутствии летальных исходов от воздействия максимально возможных объемов вещества допускается применение теста «накопления».
Вещество вводится в максимально возможной концентрации в объеме, составляющем до 5% массы тела (масляных растворов - до 2%), с интервалом между введениями 1,5-2,0 часа в течение 6-12 часов. При таком дробном введении можно в течение одного дня ввести вещество в количестве нескольких десятков грамм на килограмм массы животного.
Срок наблюдения за животными в остром опыте при наличии единичной гибели должен составлять не менее 14 суток. Однако период наблюю-дений зависит от степени проявления токсических реакций, начала и длительности периода восстановления и может быть укорочен или продлен.
При наблюдении за подопытными животными необходимо регистрировать их поведение, состояние, внешний вид, наличие аппетита, уровень водопотребления, степень проявления реакции на внешние раздражители.