ГОСТ EN 15851-2013
Продукты пищевые. Определение афлатоксина B1 в продуктах на зерновой основе для питания грудных детей и детей раннего возраста. Метод ВЭЖХ с применением иммуноаффинной колоночной очистки экстракта и флуориметрическим детектированием
Купить ГОСТ EN 15851-2013 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает метод определения афлатоксина В1 в продуктах на зерновой основе для питания грудных детей и детей раннего возраста с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) с применением очистки экстракта на колонке с иммуноаффинным сорбентом и флуориметрическим детектированием. Метод прошел валидацию путем межлабораторных испытаний проб, загрязненных афлатоксином В1 естественным и искусственным образом в диапазоне содержания от 0,07 до 0,18 мкг/кг.
Идентичен EN 15851:2010
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Реактивы
5 Аппаратура
6 Процедура проведения испытания
7 Анализ с помощью ВЭЖХ
8 Обработка результатов
9 Прецизионность
10 Протокол испытаний
Приложение А (справочное) Пример типичной хроматограммы
Приложение В (справочное) Данные по прецизионности метода
Библиография
| Дата введения | 01.07.2014 |
|---|---|
| Добавлен в базу | 01.11.2014 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
Организации:
| 28.08.2013 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 58-П |
|---|---|---|---|
| 17.10.2013 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1170-ст |
| Разработан | ГНУ ВНИИКОП | ||
| Разработан | ОАО ВНИИС | ||
| Издан | Стандартинформ | 2014 г. |
Foodstuffs. Determination of aflatoxin B1 in cereal based foods for infants and young children. HPLC method with immunoaffinity column cleanup and fluorescence detection
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11
стр. 12
стр. 13

стр. 14

стр. 15
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
Продукты пищевые
ОПРЕДЕЛЕНИЕ АФЛАТОКСИНА Вт В ПРОДУКТАХ НА ЗЕРНОВОЙ ОСНОВЕ ДЛЯ ПИТАНИЯ ГРУДНЫХ ДЕТЕЙ И ДЕТЕЙ РАННЕГО ВОЗРАСТА
Метод ВЭЖХ с применением иммуноаффинной колоночной очистки экстракта и флуориметрическим детектированием
(EN 15851:2010, ЮТ)
Издание официальное
ГОСТ EN
15851—
2013
|
Москва Стандартинформ 2014 |
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 - 92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Открытым акционерным обществом «Всероссийский научно-исследовательский институт сертификации» (ОАО «ВНИИС») при участии специалистов Государственного научного учреждения Всероссийского научно-исследовательского института консервной и овощесушильной промышленности Российской академии сельскохозяйственных наук (ГНУ ВНИИКОП Россельхозакадемии) на основе собственного аутентичного перевода на русский язык европейского регионального стандарта, указанного в пункте 4
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (ТК 335)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 28 августа 2013 г. № 58-П)
|
За принятие проголосовали: | |||||||||||||||||||||
|
4 Настоящий стандарт идентичен европейскому региональному стандарту EN 15851:2010 «Foodstuffs. Determination of aflatoxin B1 in cereal based foods for infants and young children. HPLC method with immunoaffinity column cleanup and fluorescence detection» (Продукты пищевые. Определение афлатоксина В1 в продуктах на зерновой основе для питания грудных детей и детей раннего возраста. Метод ВЭЖХ с применением иммуноаффинной колоночной очистки экстракта и флуориметрическим детектированием).
Перевод с немецкого языка (de)
Официальный экземпляр европейского регионального стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, имеется в Федеральном агентстве по техническому регулированию и метрологии Российской Федерации.
Степень соответствия - идентичная (IDT)
5 Приказом Федерального агентства по техническому регулированию и метрологии от 17 октября 2013 г. № 1170-ст межгосударственный стандарт ГОСТ EN 15851-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2014 г.
6 ВВЕДЕН ВПЕРВЫЕ
X =0,18 мкг/кг, r= 0,067 мкг/кг (проба с искусственным внесением афлатоксина В^;
X = 0,07 мкг/кг, г= 0,028 мкг/кг;
X = 0,09 мкг/кг, г= 0,020 мкг/кг;
X =0,17 мкг/кг, г= 0,059 мкг/кг.
9.3 Воспроизводимость
Абсолютное расхождение между результатами двух единичных испытаний, полученными одним методом на идентичном объекте испытаний в разных лабораториях разными операторами с использованием разного оборудования не должно превышать предел воспроизводимости R более чем в 5 % случаев.
Значения предела воспроизводимости для продуктов для питания грудных детей и детей раннего возраста равны:
X =0,10 мкг/кг, R = 0,034 мкг/кг (проба с искусственным внесением афлатоксина В^;
X =0,18 мкг/кг, R = 0,118 мкг/кг (проба с искусственным внесением афлатоксина ВО;
X = 0,07 мкг/кг, R = 0,048 мкг/кг;
X = 0,09 мкг/кг, R = 0,022 мкг/кг;
X =0,17 мкг/кг, R = 0,109 мкг/кг.
10 Протокол испытаний
Протокол испытаний должен содержать как минимум следующие сведения:
a) всю информацию, необходимую для идентификации пробы;
b) ссылку на настоящий стандарт;
c) дату и время отбора пробы (если известны);
d) дату поступления пробы в лабораторию;
e) дату проведения испытания;
f) результаты испытания с указанием единиц измерения;
д) все особенности, наблюдавшиеся при проведении испытания;
h) все операции, не оговоренные в методе или рассматриваемые как необязательные, которые могли повлиять на результат испытания.
8
rOCTEN 15851-2013
Приложение А
(справочное)
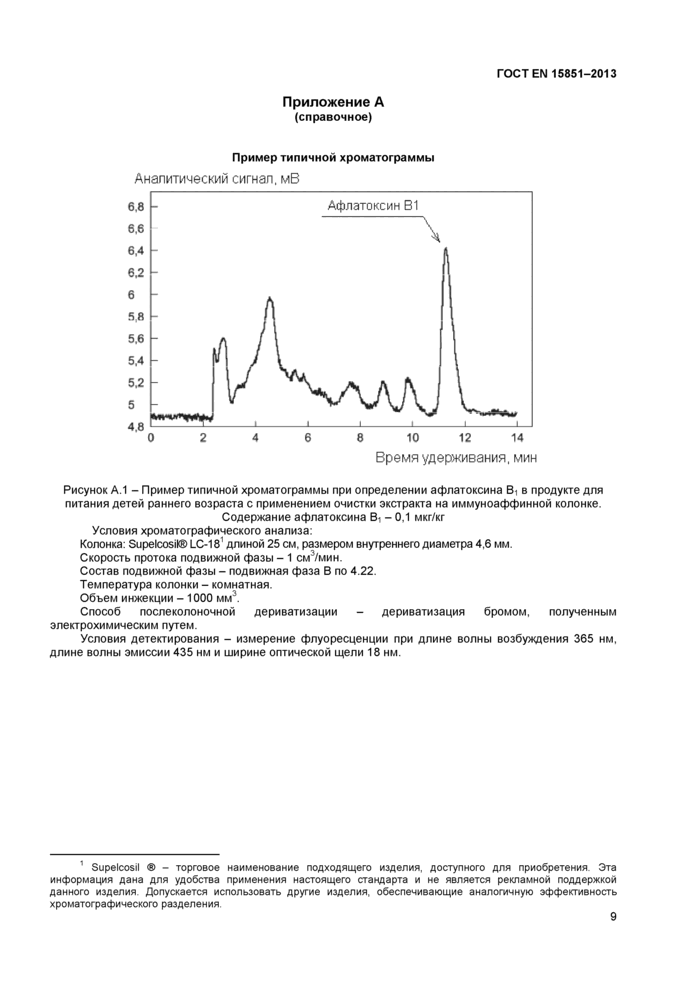
Пример типичной хроматограммы
Аналитический сигнал, мВ
Рисунок А.1 - Пример типичной хроматограммы при определении афлатоксина В1 в продукте для питания детей раннего возраста с применением очистки экстракта на иммуноаффинной колонке.
Содержание афлатоксина В1 - 0,1 мкг/кг Условия хроматографического анализа:
Колонка: Supelcosil® LC-181 2 длиной 25 см, размером внутреннего диаметра 4,6 мм.
Скорость протока подвижной фазы - 1 см3/мин.
Состав подвижной фазы - подвижная фаза В по 4.22.
Температура колонки - комнатная.
Объем инжекции - 1000 мм3.
Способ послеколоночной дериватизации - дериватизация бромом, полученным электрохимическим путем.
Условия детектирования - измерение флуоресценции при длине волны возбуждения 365 нм, длине волны эмиссии 435 нм и ширине оптической щели 18 нм.
9
Приложение В(справочное)Данные по прецизионности метода
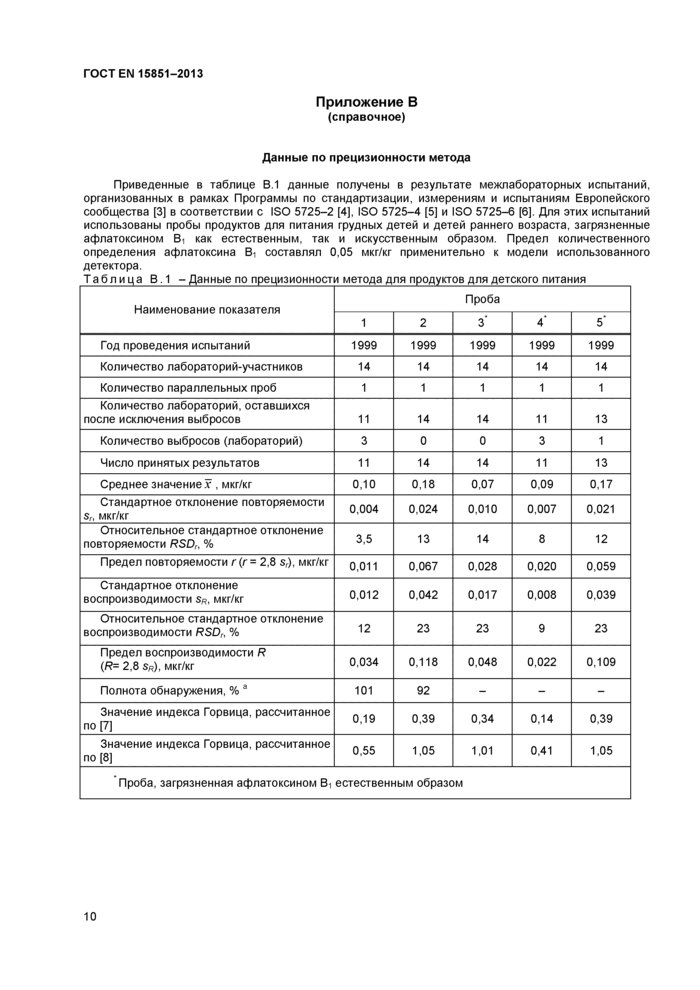
Данные по прецизионности метода
Приведенные в таблице В.1 данные получены в результате межлабораторных испытаний, организованных в рамках Программы по стандартизации, измерениям и испытаниям Европейского сообщества [3] в соответствии с ISO 5725-2 [4], ISO 5725-4 [5] и ISO 5725-6 [6]. Для этих испытаний использованы пробы продуктов для питания грудных детей и детей раннего возраста, загрязненные афлатоксином В1 как естественным, так и искусственным образом. Предел количественного определения афлатоксина В1 составлял 0,05 мкг/кг применительно к модели использованного детектора.
|
Таблица В.1 - Данные по прецизионности метода для продуктов для детского питания | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Проба, загрязненная афлатоксином В1 естественным образом | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
rOCTEN 15851-2013Библиография
[1] Castegnaro M., Barek J., Fremy J. M.., Lafontaine M., Sansone E. B. and Telling G. M. Laboratory decontamination and destruction of carcinogens in laboratory wastes: some mycotoxins. IARC Scientific Publication No. 113, International Agency for Research on Cancer, Lyon (France), 1991, p. 63
[2] Nesheim, S.; Trucksess, M. W.; Page, S. W., Molar absorptivities of aflatoxins B-1, B-2, G(1), and G(2) in acetonitrile, methanol, and toluene-acetonitrile (9+1) (modification of AOAC official method 971.22): Collaborative study. Journal of AOAC International, 1999, 82 (2), p. 251-258.
[3] Stroka, J.; Anklam, E.; Joerissen, U.; Gilbert, J., Immunoaffinity column clean-up with liquid chromatography using post-column bromination for the determination of aflatoxin B1 in baby food: Collaborative study. Journal of AOAC International, 2001,84, p. 1116
[4] ISO 5725-2:1994. Accuracy (trueness and precision) of measurement methods and results - Part 2 : Basic method for the determination of repeatability and reproducibility of a standard measurement method
[Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерения]
[5] ISO 5725-4:1994. Accuracy (trueness and precision) of measurement methods and results - Part 4: Basic methods for the determination of the trueness of a standard measurement method [Точность (правильность и прецизионность) методов и результатов измерений. Часть 4. Основные методы определения правильности стандартного метода измерения]
[6] ISO 5725-6:1994. Accuracy (trueness and precision) of measurement methods and results - Part 6: Use in practice of accuracy values
[Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике]
[7] Horwitz, W. and Albert, R., (2006), The Horwitz Ratio (HorRat): A Useful Index of Method Performance with Respect to Precision, Journal of AOAC International, 89,1095-1109
[8] Thompson, M., 2000, Recent trends in inter-laboratory precision at ppb and sub-ppb concentrations in relation to fitness for purpose criteria in proficiency testing, Analyst, 125, 385-386
11
УДК 637:543.6:006.354 МКС 67.050 ЮТ
67.060
Ключевые слова: продукты пищевые, определение афлатоксина В-ь продукты на зерновой основе для питания детей грудного и раннего возраста, метод высокоэффективной жидкостной хроматографии, очистка экстракта на иммуноаффинной колонке, флуориметрическое детектирование
Подписано в печать 01.08.2014. Формат 60x84V8.
Уел. печ. л. 1,86. Тираж 60 экз. Зак. 2945.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
ФГУП «СТАНДАРТИНФОРМ»
123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
ГОСТ EN 15851-2013
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2014
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
TOCTEN 15851-2013 СТАНДАРТ
МЕЖГОСУДАРСТВЕННЫЙ
Продукты пищевыеОПРЕДЕЛЕНИЕ АФЛАТОКСИНА Вл В ПРОДУКТАХ НА ЗЕРНОВОЙ ОСНОВЕ ДЛЯ ПИТАНИЯ ГРУДНЫХ ДЕТЕЙ И ДЕТЕЙ РАННЕГО ВОЗРАСТАМетод ВЭЖХ с применением иммуноаффинной колоночной очистки экстракта и флуориметрическим детектированием
МЕЖГОСУДАРСТВЕННЫЙ
ОПРЕДЕЛЕНИЕ АФЛАТОКСИНА Вл В ПРОДУКТАХ НА ЗЕРНОВОЙ ОСНОВЕ ДЛЯ ПИТАНИЯ ГРУДНЫХ ДЕТЕЙ И ДЕТЕЙ РАННЕГО ВОЗРАСТАМетод ВЭЖХ с применением иммуноаффинной колоночной очистки экстракта и флуориметрическим детектированием
Foodstuffs.
Determination of aflatoxin Bi in cereal based foods for infants and young children. HPLC method with immunoaffinity
column cleanup and fluorescence detection
Дата введения - 2014—07—01
1 Область применения
Настоящий стандарт устанавливает метод определения афлатоксина В1 в продуктах на зерновой основе для питания грудных детей и детей раннего возраста с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) с применением очистки экстракта на колонке с иммуноаффинным сорбентом и флуориметрическим детектированием. Метод прошел валидацию путем межлабораторных испытаний проб, загрязненных афлатоксином В1 естественным и искусственным образом в диапазоне содержания от 0,07 до 0,18 мкг/кг. Подробная информация о валидации метода приведена в разделе 9 и в приложении В.
2 Нормативные ссылки
Приведенные ниже ссылочные нормативные документы являются обязательными для применения настоящего стандарта. Датированные ссылки предполагают возможность использования только указанного издания документа. В случае недатированных ссылок используют последнее издание документа, включая все дополнения.
EN ISO 3696:1995 Water for analytical laboratory use - Specification and test methods (ISO 3696:1987) (Вода для лабораторного анализа. Технические требования и методы испытаний)
3 Сущность метода
Анализируемую пробу экстрагируют смесью метанола и воды. Экстракт фильтруют, разбавляют фосфатно-хпоридным буферным раствором и пропускают через колонку с иммуноаффинным сорбентом, содержащим антитела, специфичные к афлатоксину В-ь при этом происходит очистка экстракта и концентрирование афлатоксина В1. Афлатоксин В1 элюируют с колонки метанолом и определяют с помощью обращенно-фазовой ВЭЖХ с применением послеколоночной дериватизации методом бромирования и детектированием по флуоресценции.
Послеколоночную дериватизацию осуществляют с использованием брома, полученного электрохимическим путем или с помощью бромида-пербромида пиридиния.
4 Реактивы4.1 Общие положения
Для проведения анализа при отсутствии особо оговоренных условий используют только реактивы гарантированной аналитической чистоты и воду не ниже первой степени чистоты по EN ISO 3696:1995. Используемые растворители по степени чистоты должны быть пригодны для применения в анализе с помощью ВЭЖХ. Допускается использование готовых растворов, доступных для приобретения, при условии, что их характеристики не отличаются от приведенных ниже.
ПРЕДУПРЕЖДЕНИЕ - Утилизацию отработанных растворителей проводят в соответствии с требованиями законодательства по охране окружающей среды. Способы обезвреживания отработанных реактивов приведены в материалах Международного агентства по исследованию рака (IARC) [1].
4.2 Гелий газообразный очищенный сжатый.
4.3 Азот.
4.4 Натрий фосфорнокислый двухзамещенный безводный (Na2HP04) или гидратированный (Na2HP04- 12Н20).
4.5 Калий бромистый.
4.6 Калий хлористый.
4.7 Калий фосфорнокислый однозамещенный.
4.8 Натрий хлористый.
4.9 Натрия гидроксид.
4.10 Кислота соляная, водный раствор массовой долей w(HCI) = 37 %.
4.11 Кислота соляная, раствор молярной концентрации с (HCI) = 0,1 моль/дм3
Раствор готовят разбавлением 8,28 см3 раствора соляной кислоты по 4.10 водой до 1 дм3.
4.12 Натрия гидроксид, раствор молярной концентрации с (NaOH) = 0,1 моль/дм3
Растворяют 4 г гидроксида натрия по 4.9 в 1 дм3 воды.
4.13 Раствор фосфатно-хлоридный буферный молярной концентрации натрия хлористого c(NaCI) = 120 ммоль/дм3, хлористого калия с(КС1)= 2,7 ммоль/дм3, суммы натрия фосфорнокислого и калия фосфорнокислого с (Na2HP04 + КН2Р04) = 10 ммоль/дм3, pH = 7,4
Растворяют 8,0 г натрия хлористого по 4.8, 1,2 г безводного двухзамещенного фосфорнокислого натрия [или 2,9 г гидратированного двухзамещенного фосфорнокислого натрия (Na2HP04-12H20)] по 4.4, 0,2 г однозамещенного фосфорнокислого калия по 4.7 и 0,2 г хлористого калия по 4.6 в 900 см3 воды.
Значение pH приготовленного раствора доводят до 7,4 ед. pH путем добавления раствора соляной кислоты по 4.11, либо раствора гидроксида натрия по 4.12, после чего объем раствора доводят водой до 1 дм3. В качестве альтернативы допускается использовать доступный для приобретения таблетированный препарат или готовый раствор с аналогичными характеристиками.
4.14 Пиридиния бромид-пербромид (CAS 39416-48-3).
4.15 Ацетонитрил.
ПРЕДУПРЕЖДЕНИЕ - Ацетонитрил является токсичным веществом, поэтому все операции по приготовлению растворов, содержащих ацетонитрил, следует проводить в вытяжном шкафу с использованием взрывобезопасного перемешивающего устройства. Фильтрование растворов, содержащих ацетонитрил, следует проводить также в вытяжном шкафу.
4.16 Метанол для ВЭЖХ.
4.17 Метанол технический.
4.18 Толуол.
4.19 Экстрагент
Смешивают 8 объемных частей метанола по 4.17 с двумя объемными частями воды.
4.20 Кислота азотная, раствор молярной концентрации c(HN03) = 4 моль/дм3.
4.21 Подвижная фаза А для использования при послеколоночной дериватизации бромидом-пербромидом пиридиния
Смешивают шесть объемных частей воды с двумя объемными частями ацетонитрила по 4.15 и тремя объемными частями метанола по 4.16. Перед использованием подвижную фазу дегазируют, например, с помощью гелия по 4.2.
4.22 Подвижная фаза В для использования при послеколоночной дериватизации бромом, полученным электрохимическим путем
Смешивают шесть объемных частей воды с двумя объемными частями ацетонитрила по 4.15 и тремя объемными частями метанола по 4.16. Добавляют из расчета на 1 дм3 подвижной фазы по 120 мг бромистого калия по 4.5 и по 350 мм3 азотной кислоты по 4.20. Перед использованием подвижную фазу дегазируют, например, с помощью гелия по 4.2.
4.23 Реактив для послеколоночной дериватизации
Растворяют 50 мг бромида-пербромида пиридиния по 4.14 в 1 дм3 воды. Реактив используют в сочетании с подвижной фазой А по 4.21. Срок годности раствора - четыре дня при хранении в темном месте при комнатной температуре.
4.24 Смесь толуола и ацетонитрила
Смешивают девять объемных частей толуола по 4.18 с одной объемной частью ацетонитрила по 4.15.
4.25 Колонка с иммуноаффинным сорбентом
Для проведения испытания пригодна колонка с иммуноаффинным сорбентом с иммобилизованными антителами, специфичными в отношении афлатоксина Bi, имеющая сорбционную емкость по отношению к афлатоксину Bi не менее 100 нг и обеспечивающая полноту обнаружения не менее 80 % при внесении в нее 5 нг афлатоксина Bi в растворе, состоящем из 10 объемных частей метанола и 90 объемных частей воды.
2
ГОСТ EN 15851-2013
4.26 Афлатоксин В1 кристаллический или в виде ампульного препарата в пленочной форме, либо в виде раствора, доступного для приобретения.
ПРЕДУПРЕЖДЕНИЕ - Афлатоксины подвержены фотохимическому разложению. Лабораторное помещение, в котором проводятся испытания, должно быть в достаточной мере защищено от доступа дневного света. Это достигается путем аппликации на окна пленки, поглощающей ультрафиолетовый свет, в сочетании с обеспечением отсутствия доступа прямого солнечного света, либо путем применения занавесей или жалюзи при искусственном освещении, при этом в качестве источников света допустимо использовать люминесцентные лампы.
Растворы афлатоксинов следует всеми возможными мерами защищать от доступа света путем хранения в темном месте в сосудах из темного стекла или обернутых алюминиевой фольгой.
4.27 Афлатоксин Bi, основной раствор массовой концентрации с = 10 мкг/см4
Готовят основной раствор афлатоксина В! массовой концентрации около 10 мкг/см4 в смеси толуола с ацетонитрилом по 4.24.
М 100
Для определения точной массовой концентрации афлатоксина В1 в основном растворе регистрируют его оптическую плотность в диапазоне длин волн от 330 до 370 нм в кварцевой кювете длиной оптического пути 1 см с использованием спектрофотометра по 5.14. В качестве раствора сравнения используют смесь толуола с ацетонитрилом по 4.24. По полученному спектру определяют длину волны, соответствующую максимальной оптической плотности. Массовую концентрацию афлатоксина Bi, рап, мкг/см , рассчитывают по формуле
(1)
где Amax - максимальное значение оптической плотности в данном диапазоне
длин волн (между 330 и 370 нм);
М- молярная масса афлатоксина Bi, г/моль (М= 312 г/моль);
s - молярный коэффициент поглощения афлатоксина Bi в смеси толуола с ацетонитрилом по 4.24, м2/моль, (е = 1930 м2/моль) [2];
b - длина оптического пути кюветы, см.
Основной раствор хранят при температуре около минус 18 °С. Перед использованием раствор выдерживают до достижения комнатной температуры. При указанных условиях хранения срок годности раствора составляет как правило 12 мес. При хранении основного раствора более 12 мес перед его использованием проверяют соответствие фактической массовой концентрации афлатоксина Bi ранее установленному значению.
4.28 Афлатоксин Bi, стандартный раствор массовой концентрации р = 5,00 нг/см4
Пипеткой отбирают порцию основного раствора по 4.27, содержащую точно 1,00 мкг
афлатоксина Bi, и помещают ее в мерную колбу вместимостью 200 см4, объем содержимого в колбе доводят до метки смесью толуола с ацетонитрилом по 4.24. Массовая концентрация афлатоксина Bi в полученном стандартном растворе составляет 5,00 нг/см4.
Раствор хранят при температуре не выше минус 4 °С в колбе, плотно обернутой алюминиевой фольгой. Перед использованием алюминиевую фольгу удаляют после достижения раствором комнатной температуры с целью предотвращения попадания конденсата внутрь колбы. При указанных условиях хранения срок годности раствора составляет не менее четырех недель.
4.29 Афлатоксин Bi, раствор массовой концентрации р = 2 мкг/см4 для внесения в пробу при контроле полноты обнаружения
Пипеткой отбирают порцию основного раствора по 4.27, содержащую точно 20 мкг афлатоксина Bi, и помещают ее в мерную колбу вместимостью 10 см4. Растворитель (смесь толуола с ацетонитрилом) удаляют досуха в токе азота при комнатной температуре, после чего объем содержимого в колбе доводят до метки метанолом по 4.16, содержимое колбы тщательно перемешивают. Массовая концентрация афлатоксина Bi в полученном растворе составляет 2 мкг/см4.
Раствор хранят при температуре не выше минус 4 °С в колбе, плотно обернутой алюминиевой фольгой. Перед использованием алюминиевую фольгу удаляют после достижения раствором комнатной температуры с целью предотвращения попадания конденсата внутрь колбы. При указанных условиях хранения срок годности раствора составляет не менее 3 мес.
5 Аппаратура
ПРЕДУПРЕЖДЕНИЕ - Всю стеклянную лабораторную посуду, контактирующую при проведении испытания с водными растворами афлатоксинов, перед использованием ополаскивают раствором кислоты. Данная процедура является составной частью программы работы многих машин для мойки лабораторной посуды. В качестве альтернативы стеклянную посуду, контактирующую с водными растворами афлатоксинов, помещают на длительный срок (например, на 15 ч на ночь) в раствор серной кислоты концентрации 2 моль/дм3, после чего тщательно (не менее трех раз) ополаскивают водой для полного удаления кислоты. Полноту удаления кислоты контролируют с помощью индикаторной бумаги.
Необходимость данной процедуры обусловлена потерями афлатоксинов при контакте их растворов со стеклянной посудой, не обработанной кислотой. Обработка кислотой необходима в отношении круглодонных колб, мерных колб и цилиндров, стеклянных колб и сосудов для градуировочных растворов и раствора пробы для хроматографического анализа, в особенности, для флаконов к автосамплеру, а также для пастеровских пипеток, используемых при отборе градуировочных растворов и экстрактов.
При проведении испытания используют общеупотребительные лабораторные приборы и оборудование, в частности, перечисленные ниже.
5.1 Весы аналитические, пригодные для взвешивания с точностью до 0,0001 г.
5.2 Весы лабораторные, пригодные для взвешивания с точностью до 0,01 г.
5.3 Встряхиватель лабораторный вертикального или горизонтального типа с возможностью регулировки скорости встряхивания.
5.4 Фильтры складчатые диаметром, например, 24 см.
5.5 Колбы конические с винтовой крышкой или стеклянной пробкой вместимостью 500 см3.
5.6 Фильтры из стеклянного микроволокна, задерживающие частицы размером не менее 1,6 мкм, или аналогичные.
5.7 Резервуары вместимостью 75 см3 с адаптером типа люер-лок в комплекте с приспособлениями для подсоединения иммуноаффинных колонок.
5.8 Насос ручной объемом цилиндра 20 см3, снабженный адаптером типа люер-лок или резиновой втулкой для соединения с иммуноаффинной колонкой.
5.9 Колбы мерные вместимостью 5, 10, 20, 150 и 200 см3 точностью не ниже 0,5 %.
5.10 Фильтры мембранные шприцевые размером диаметра пор 0,45 мкм
Перед использованием следует убедиться в отсутствии потерь афлатоксина В1 при фильтрации путем установления полноты его обнаружения.
Примечание - Некоторые фильтрующие материалы могут задерживать афлатоксин Bi.
5.11 Пипетки вместимостью 2 и 10 см .
5.12 Микрошприцы или микропипетки градуированные вместимостью от 25 до 500 мм3.
5.13 Система для ВЭЖХ в указанной ниже комплектации:
5.13.1 Инжектор, обеспечивающий объем ввода 1000 мм3 (рекомендуется полное заполнение петли).
Объем инжекции может быть меньше указанного при условии обеспечения предела обнаружения афлатоксина Bi не более 0,05 мкг/кг (при отношении уровня аналитического сигнала к уровню шума, равном 3) и предела количественного определения не более 0,1 мкг/кг. Предел количественного определения устанавливают путем многократных анализов стандартного раствора афлатоксина Bi массовой концентрации, соответствующей содержанию афлатоксина Bi в пробе 0,1 мкг/кг. При этом относительное стандартное отклонение аналитического сигнала не должно превышать 10 %. Полученные результаты документируют.
5.13.2 Насос для подачи подвижной фазы, обеспечивающий скорость подачи подвижной фазы 1 см3/мин.
5.13.3 Детектор флуориметрический, снабженный оптическим фильтром для выделения длины волны возбуждения 360 нм и отсекающим оптическим фильтром для выделения диапазона длин волн эмиссии выше 420 нм, или аналогичный детектор, например, снабженный монохроматорами.
5.13.4 Самописец, интегратор или компьютерная система обработки данных.
5.13.5 Колонка для ВЭЖХ аналитическая, заполненная обращенно-фазовым сорбентом, например, с привитыми октадецильными группами (Ci8 или ODS-2), снабженная соответствующей обращенно-фазовой защитной колонкой.
Для проведения испытания пригодна колонка, обеспечивающая отделение пика афлатоксина Bi от сопутствующих пиков матрицы пробы. Перекрывание пика афлатоксина Bi другими пиками не должно превышать 10 % его высоты. При необходимости для достижения требуемой степени разделения пиков проводят корректировку состава подвижной фазы.
4
ГОСТ EN 15851-2013
5.13.6 Система для послеколоночной дериватизации с использованием бромида-пербромида пиридиния (применяется только с подвижной фазой А по 4.21), состоящая из насоса, обеспечивающего отсутствие пульсаций скорости потока, соединительного элемента для трех капилляров, имеющего нулевой мертвый объем, и реактора в виде капилляра из политетрафторэтилена длиной 45 см и внутренним диаметром 0,5 мм.
5.13.7 Система для послеколоночной дериватизации с использованием брома, полученного электрохимическим путем (применяется только с подвижной фазой В по 4.22), например, ячейка KOBRA®5 6.
5.13.8 Дегазатор подвижной фазы (применяется по выбору пользователя).
5.14 Спектрофотометр, пригодный для измерений оптической плотности в ультрафиолетовой области спектра, в комплекте с кварцевыми кюветами.
6 Процедура проведения испытания6.1 Экстракция
Перед отбором пробы для анализа лабораторную пробу тщательно перемешивают.
50 г пробы для анализа, измеренной с точностью до 0,1 г, помещают коническую колбу вместимостью 500 см7. В колбу добавляют 5 г хлористого натрия по 4.8 и 250 см7 экстрагента по 4.19. Содержимое колбы встряхивают сначала вручную в течение 15-30 с, затем с использованием встряхивателя по 5.3 в течение 30 мин. Полученный экстракт фильтруют через складчатый фильтр по 5.4. Пипеткой по 5.11 отбирают аликвоту фильтрата объемом 10 см7 и переносят ее в мерную колбу вместимостью 100 см7 по 5.9. Объем содержимого в колбе доводят до метки фосфатно-хпоридным буферным раствором по 4.13. Содержимое колбы снова фильтруют через фильтр из стеклянного микроволокна по 5.6. Аликвоту фильтрата объемом от 50 до 100 см7 переносят в резервуар по 5.7, присоединенный к предварительно кондиционированной иммуноаффинной колонке по 4.25. Дальнейшую очистку экстракта на иммуноаффинной колонке проводят в соответствии с 6.2.
6.2 Очистка экстракта на колонке с иммуноаффинным сорбентом
Очистку экстракта проводят с применением разрежения либо избыточного давления, либо жидкость протекает через колонку под действием собственной силы тяжести. При этом скорость протока не должна превышать предельно допустимой величины для данной колонки. Соблюдение данного требования требует особого внимания при применении разрежения.
Иммуноаффинную колонку по 4.25 подготавливают к использованию в соответствии с инструкцией изготовителя. Если в этой инструкции предписано избегать попадания воздуха в колонку, на соблюдение этого требования обращают особое внимание. Перед кондиционированием колонку выдерживают до достижения ею комнатной температуры.
Аликвоту фильтрованного экстракта пропускают через колонку со скоростью около 3 см7/мин (примерно одна капля в секунду), но не более 5 см7/мин. Далее колонку промывают фосфатно-хпоридным буферным раствором по 4.13 объемом около 15 см7 порциями по 5 см7 при скорости протока не более 5 см7/мин. По окончании промывания колонку высушивают, для чего на выходе из нее создают небольшое разрежение в течение 5 - 10 с или пропускают через нее воздух с помощью шприца в течение 10 с.
6.3 Приготовление раствора пробы для хроматографического анализа
Афлатоксин Bi элюируют с колонки, для чего через нее пропускают 0,50 см7 метанола по 4.16 под действием силы тяжести. Элюат собирают в мерную колбу по 5.9 вместимостью 5 см7. Колонку оставляют в покое на 1 мин, после чего через нее пропускают вторую порцию метанола по 4.16 объемом 0,75 см7. Элюирование заканчивают продуванием колонки воздухом с целью сбора максимально возможного количества элюата. Объем содержимого колбы с элюатом доводят до метки водой, содержимое колбы тщательно перемешивают. Если полученный раствор прозрачен, его непосредственно используют для хроматографического анализа. Если раствор непрозрачен, перед хроматографическим анализом его фильтруют через мембранный шприцевой фильтр по 5.10.
Примечание - Для иммуноаффинных колонок различных изготовителей операции пропускания экстракта через колонку, промывки колонки и элюирования несколько различаются, поэтому при их проведении следует руководствоваться прилагаемой к колонке инструкцией по ее использованию.
6.4 Процедура проведения испытания пробы с добавкой афлатоксина Bi
Для контроля полноты обнаружения афлатоксина Bi проводят испытание пробы с добавкой
5
метанольного раствора афлатоксина Bi по 4.29. Содержание афлатоксина В1 в пробе должно находиться в пределах диапазона градуировки, желательно, в середине этого диапазона. В пробу пипеткой по 5.11 добавляют не более 2 см5 раствора афлатоксина В^ после чего пробу выдерживают в темноте в течение 0,5 - 2 ч для удаления растворителя.
7 Анализ с помощью ВЭЖХ7.1 Условия хроматографического анализа
Хроматографический анализ афлатоксина В1 проводят при комнатной температуре с использованием обращенно-фазовой колонки по 5.13.5 и подвижной фазы подходящего состава по 4.21 или 4.22 в изократическом режиме при объеме инжекции 1000 мм3. Для обеспечения максимальной прецизионности рекомендуется полностью заполнять петлю инжектора анализируемым раствором (см. 5.13.1). При использовании колонки внутренним диаметром 4,6 мм рекомендуется устанавливать скорость подачи подвижной фазы 1 см3/мин. Допускается использовать колонки других размеров при условии обеспечения требуемого предела количественного определения, что должно быть подтверждено экспериментально. В этом случае подбирают оптимальную скорость подачи подвижной фазы применительно к размерам колонки.
Время удерживания пика афлатоксина Bi составляет около 11 мин. Необходимым условием является достижение отделения пика афлатоксина В1 от пиков других компонентов матрицы пробы на уровне базовой линии. Для достижения максимальной эффективности и степени разделения пиков состав подвижной фазы корректируют добавлением воды, метанола по 4.16 или ацетонитрила по 4.15. Типичная хроматограмма приведена в приложении А.
7.2 Условия послеколоночной дериватизации
При дериватизации бромидом-пербромидом пиридиния используют систему для
послеколоночной дериватизации. Дериватизацию проводят при скорости подачи подвижной фазы 1,0 см3/мин и скорости подачи дериватизирующего реактива 0,30 см3/мин (значение этого параметра корректируют в зависимости от скорости протока подвижной фазы).
При дериватизации бромом, полученным электрохимическим путем (например, с использованием ячейки KOBRA®) электрохимическую ячейку устанавливают в соответствии с инструкциями изготовителя и проводят дериватизацию при скорости протока подвижной фазы 1,0 см3/мин и силе тока электролиза 100 мА.
7.3 Приготовление градуировочных растворов
В мерные колбы вместимостью 10 см3 пипеткой вносят стандартный раствор афлатоксина В1 по 4.28 в объемах, указанных в таблице 1. Растворитель удаляют досуха в токе азота при комнатной температуре. Далее в колбы вносят по 3,5 см3 метанола по 4.16 для перерастворения афлатоксина Bi. Объем содержимого в колбах доводят до метки водой, содержимое колб тщательно перемешивают. При соблюдении указанных параметров диапазон массовых концентраций афлатоксина Bi в градуировочных растворах соответствует диапазону его содержания в пробе от 0,05 мкг/кг до 0,35 мкг/кг.
|
Примечание - При смешивании метанола с водой имеет место уменьшение объема смеси по отношению к суммарному объему компонентов Таблица 1 - Приготовление градуировочных растворов | ||||||||||||||||||||||||
|
ГОСТ EN 15851-2013
Для приготовления градуировочных растворов используют пипетки либо другие доступные градуированные стеклянные средства измерения объема.
7.4 Построение градуировочного графика
Градуировку осуществляют в день проведения испытания перед хроматографическим анализом растворов проб, для чего проводят хроматографический анализ градуировочных растворов, приготовленных в соответствии с таблицей 1, при объеме инжекции 1000 мм3. При построении градуировочного графика в системе координат откладывают значения массовой концентрации афлатоксина В1 против соответствующих значений площади пика. Полученный график проверяют на соответствие требованиям линейности.
Если содержание афлатоксина В1 в пробе превышает верхнюю границу диапазона градуировки, проводят новую градуировку, соответствующим образом изменив ее диапазон. В качестве альтернативы анализируемый раствор пробы разбавляют до получения в нем массовой концентрации афлатоксина В1 в пределах диапазона градуировки.
7.5 Определение афлатоксина В.| в растворе пробы
Проводят хроматографический анализ растворов проб по 6.3 при тех же условиях что были использованы при анализе градуировочных растворов.
7.6 Подтверждение правильности идентификации пика афлатоксина Bi
Для подтверждения правильности идентификации пика афлатоксина Bi выходной конец колонки отсоединяют от системы послеколоночной дериватизации, подсоединяют его непосредственно к флуориметрическому детектору. При отключенной системе послеколоночной дериватизации аналитический сигнал, относящийся к пику афлатоксина Bi, существенно меньше (в десять раз или более). При использовании электрохимической ячейки данный способ не следует реализовывать, отключив ток электролиза и оставив ячейку подсоединенной к хроматографу, поскольку мембрана ячейки может содержать остаточный бром.
Альтернативным способом идентификации пика афлатоксина Bi является хроматографический анализ с применением масс-спектрометрического или тандемного масс-спектрометрического детекторов.
8 Обработка результатов
По градуировочному графику определяют массовую концентрацию афлатоксина Bi, нг/см3, в растворе пробы для анализа.
Содержание афлатоксина Bi в пробе, wafia, мкг/кг, рассчитывают по формуле
(2)
w
afla
PaflgVl Уз v2 m s
где рада- массовая концентрация афлатоксина Bi в растворе пробы для
хроматографического анализа, определенная по градуировочному графику, нг/см3;
Vi - объем экстрагента, использованный для экстракции, см3 (\/| = 250 см3);
V2 -объем аликвоты неразбавленного экстракта, отобранной для очистки на
иммуноаффинной колонке, см3 [V2 = (5 - 10) см3];
V3 - объем приготовленного раствора пробы для хроматографического анализа, см3 (1/3 = 5 см3); ms - масса анализируемой пробы, г (ms = 50 г).
9 Презиционность9.1 Общие положения
Подробности межлабораторных испытаний по определению прецизионности метода приведены в таблице В.1 (приложение В). Значения метрологических характеристик, полученные в результате межлабораторных испытаний, могут быть не применимы к другим содержаниям аналита и другим типам матриц, чем те, что указаны в приложении В.
9.2 Повторяемость
Абсолютное расхождение между результатами двух независимых единичных испытаний, полученными одним методом на идентичном объекте испытаний в одной лаборатории одним оператором с использованием одного оборудования в течение короткого промежутка времени, не должно превышать предел повторяемости г более чем в 5 % случаев.
Значения предела повторяемости для продуктов для питания грудных детей и детей раннего возраста равны:
X =0,10 мкг/кг, г = 0,011 мкг/кг (проба с искусственным внесением афлатоксина Bi);
7
1
Supelcosil ® - торговое наименование подходящего изделия, доступного для приобретения. Эта
2
информация дана для удобства применения настоящего стандарта и не является рекламной поддержкой
3
данного изделия. Допускается использовать другие изделия, обеспечивающие аналогичную эффективность хроматографического разделения.
4
5
Ячейка KOBRA - торговое наименование подходящего изделия, доступного для приобретения. Эта
6
информация дана для удобства применения настоящего стандарта и не является рекламной поддержкой
7
данного изделия. Допускается использовать другие изделия с аналогичными техническими характеристиками