ГОСТ EN 14663-2014
Продукция пищевая. Определение витамина В6 (включая гликозилированные формы) методом высокоэффективной жидкостной хроматографии
Купить ГОСТ EN 14663-2014 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает метод определения витамина В6 в пищевой продукции с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
Витамин В6 определяется как сумма пиридоксина, пиридоксаля, пиридоксамина, включая их фосфорилированные производные, а также бета-гликозилированные формы, в пересчете на пиридоксин.
Настоящий метод был успешно проверен на манной крупе с молоком (детское питание), картофельном пюре, овощах с ветчиной (типичная пищевая продукция) и мультивитаминном напитке в диапазоне концентраций от 0,034 мг/100 г до 1,210 мг/100 г.
Идентичен EN 14663:2005
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Реактивы
5 Оборудование
6 Методика проведения испытания
7 Вычисление результата
8 Прецизионность
9 Протокол испытания
Приложение А (справочное) данные по прецизионности
Приложение В (справочное) Примеры подходящих условий проведения ВЭЖХ для определения соединений витамина В6
Приложение С (справочное) Примеры молярных коэффициентов поглощения
Приложение D (справочное) Примеры хроматограмм
Приложение ДА (справочное) Сведения о соответствии ссылочных европейских стандартов межгосударственным стандартам
Библиография
| Дата введения | 01.06.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 25.06.2014 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 45 |
|---|---|---|---|
| 29.06.2016 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 733-ст |
| Разработан | БелГИСС | ||
| Издан | Стандартинформ | 2016 г. |
Foodstuffs. Determination of vitamin B6 (including its glycosylated forms) by high performance liquid chromatography method
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15
стр. 16
стр. 17
стр. 18
стр. 19
стр. 20
стр. 21

стр. 22

стр. 23

стр. 24

стр. 25
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ПРОДУКЦИЯ ПИЩЕВАЯ
Определение витамина В6 (включая гликозилированные формы) методом высокоэффективной жидкостной хроматографии
(EN 14663:2005, ЮТ)
Издание официальное
ГОСТ
EN 14663— 2014
|
Москва Стандартинформ 2016 |
Предисловие
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Научно-производственным республиканским унитарным предприятием «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) на основе собственного перевода на русский язык англоязычной версии стандарта, указанного в пункте 5
2 ВНЕСЕН Государственным комитетом по стандартизации Республики Беларусь
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 25 июня 2014 г. № 45)
|
За принятие проголосовали: | |||||||||||||||||||||
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 29 июня 2016 г. № 733-ст межгосударственный стандарт ГОСТ EN 14663—2014 введен в действие в качестве национального стандарта Российской Федерации с 1 июня 2017 г.
5 Настоящий стандарт идентичен европейскому стандарту EN 14663:2005 «Продукты пищевые. Определение витамина В6 (включая гликозилированные формы) с помощью высокоэффективной жидкостной хроматографии» [(«Foodstuffs — Determination of vitamin B6 (including its glycosylated forms) by HPLC», IDT],
Европейский стандарт разработан Техническим комитетом по стандартизации CEN/TC 275 «Анализ пищевых продуктов. Горизонтальные методы» Европейского комитета по стандартизации (CEN).
При применении настоящего стандарта рекомендуется вместо ссылочного европейского стандарта использовать межгосударственный стандарт, сведения о котором приведены в дополнительном приложении ДА
6 ВВЕДЕН ВПЕРВЫЕ
rOCTEN 14663—2014
Установлено, что разделение и количественное определение является удовлетворительным при следующих условиях:
Колонка ВЭЖХ - в соответствии с 5.5;
Подвижная фаза - в соответствии с 4.16;
Расход жидкости - 1,5 см3/мин;
Вводимый объем - от 1 до 50 мм3;
Детектор - флуоресцентный: длина волны возбуждения (Ех) - 290 нм;
длина волны эмиссии (Ет) - 390 нм.
6.5 Идентификация
Вводят одинаковые подходящие объемы раствора анализируемой пробы (см. 6.2.2), «холостой» пробы (см. 6.3) и смешанных градуировочных растворов (см. 4.21) в систему ВЭЖХ в условиях по 6.4.
Идентифицируют пики PM, PL и PN путем сравнения времени удерживания пиков на хроматограммах раствора анализируемой пробы и стандартного раствора. Идентификацию пика допускается также проводить с помощью сдвига значения pH в сторону увеличения, например при установлении pH = 6,6 ед. pH при использовании устройства постколоночной дериватизации (см. 5.4) при скорости потока послеколоночного реагента 0,1 см3/мин (см. 4.6). Обнаружение осуществляется при возбуждении при 330 нм и регистрации при 390 нм (см. [2], [4], [5]).
Примечание — Увеличение значения pH путем использования послеколоночного реагента (см. 4.6) приводит к сдвигу длины волны возбуждения до 330 нм. Кроме того, избирательность матриц улучшается в связи с уменьшением матрицы пиков ([2], [4], [5]).
6.6 Определение
Вводят одинаковые подходящие объемы стандартного раствора, а также раствора анализируемой пробы в систему ВЭЖХ согласно условиям по 6.4. Для определения содержания методом внешней градуировки определяют среднее значение площади пиков или высоты пиков и сравнивают результаты с соответствующими значениями образца сравнения.
7 Вычисление результата
7.1 Вычисление проводят с использованием градуировочной зависимости либо соответствующих программ интегратора, либо в соответствии с нижеприведенными формулами (3) - (6).
Массовую долю пиридоксамина (РМ), пиридоксаля (PL) или пиридоксина (PN), w, мг/100 г пробы вычисляют по формуле
(3)
у. F 100
W = —---,
т 1000 ’
где yj — содержание PM, PL и PN, определенное по площади пика или высоте пика с использованием линейной регрессии или градуировочной зависимости, мкг/20 см3 раствора анализируемой пробы (см. 6.2.2); т — масса пробы, г;
F — коэффициент разбавления из формулы (6).
Значение у, вычисляют по формуле
yi = bixi + ai, (4)
где bj, аi — коэффициенты регрессии для PM, PL или PN, вычисленные методом линейной регрессии на основе концентрации и площади пика в градуировочных растворах;
Xj — откорректированная площадь пика раствора анализируемой пробы PM, PL или PN. Значение х( вычисляют по формуле
xi=Pi-Bh (5)
где Pi — площади пика PM, PL или PN для раствора анализируемой пробы;
Bj — площади пика PM, PL или PN для «холостой» пробы.
7
Коэффициент разбавления F вычисляют по формуле
где V — общий объем раствора кислой вытяжки пробы (см. 6.2.1.2), (см. 6.2.1.3), см3;
V1 — общий объем раствора кислой вытяжки пробы, подвергнутый ферментативной обработке (см. 6.2.2), см3.
7.2 Массовую долю витамина В6 в пересчете на пиридоксин w, мг/100 г пробы вычисляют по формуле
где 1,006 —
WPM 1 012 —
WpL — WPN —
W = 1,006WpM +1,012wP|_ + Wpng , (7)
коэффициент для пересчета РМ на PN; содержание пиридоксамина, мг/100 г пробы; коэффициент для пересчета PL на PN; содержание пиридоксаля, мг/100 г пробы; содержание пиридоксина, мг/100 г пробы.
пробы.
7.3 Массовую долю витамина В6 в пересчете на пиридоксин выражают в миллиграммах на 100
Примечание — Если необходимо представить результат в пересчете на гидрохлорид пиридоксина, используют коэффициент пересчета 1,216. Сведения о проведении пересчета должны быть четко указаны в протоколе испытания.
8 Прецизионность8.1 Общие положения
Данные по прецизионности для определения витамина В6 были установлены в ходе межлабораторных испытаний в соответствии с [8], проведенных бывшим BgVV (Bundesinstitut furgesundheitlichen Verbraucherschutz und Veterinarmedizin (Немецкий федеральный институт по защите прав потребителей и ветеринарной медицине).
Подробная информация о совместном испытании точности метода приведена в приложении А. Значения, полученные в ходе межлабораторных испытаний, могут быть не применимы к диапазонам концентраций и пробам, не приведенным в приложении А.
Применимость и надежность настоящего метода были подтверждены в ходе испытаний различной пищевой продукции, например мяса, рыбы, молока, овощей, фруктов и злаков (см. [2], [3]). Полученные результаты были в достаточной степени воспроизводимы, и только иногда наблюдались относительно небольшие мешающие влияния матричных пиков проб, которые могут быть легко устранены. Для градуировочных растворов наблюдается сильно выраженная корреляция и линейная регрессия между площадью пика и концентрацией PM, PL и PN соответственно. Относительные стандартные отклонения от общего содержания витамина В6 в последовательности, включающей от трех до пяти определений в различных продуктах, варьируются от 2 % до 6 %.
Полнота извлечения PM, PL и PN варьируется от 85 % до 105 % (см. [2], [3]). Определение общего содержания витамина В6 настоящим методом дает в результате значительно более высокие значения в пищевой продукции растительного происхождения (содержащих гликозилированный пиридоксин), чем другие методы, в которых не используется обработка (5-глюкозидазой (см. [2], [3], [7]).
8.2 Повторяемость
Абсолютное расхождение между двумя отдельными результатами испытания, которые были получены при использовании одного и того же метода на идентичном испытательном материале одним и тем же оператором на одном и том же оборудовании в течение короткого промежутка времени, не должно превышать предел повторяемости г более чем в 5 % случаев.
Значения для порошковой манной крупы с молоком:
Пиридоксамин х = 0,065 мг/100 г г = 0,008
Пиридоксаль х = 0,080 мг/100 г г = 0,022
Пиридоксин х = 0,523 мг/100 г г = 0,067
rOCTEN 14663—2014
|
Витамин В6 |
х = 0,667 мг/100 г |
г = 0,084 |
|
Значения для порошкового картофельного пюре: | ||
|
Пиридоксамин |
х = 0,163 мг/100 г |
г = 0,016 |
|
Пиридоксаль |
х = 0,032 мг/100 г |
г = 0,012 |
|
Пиридоксин |
х= 1,008 мг/100 г |
г = 0,080 |
|
Витамин В6 |
х= 1,204 мг/100 г |
г = 0,089 |
|
Значения для овощей с ветчиной (детское питание) | ||
|
Пиридоксамин |
х = 0,043 мг/100 г |
г = 0,005 |
|
Пиридоксаль |
х = 0,009 мг/100 г |
г = 0,004 |
|
Пиридоксин |
х = 0,047 мг/100 г |
г= 0,010 |
|
Витамин В6 |
х= 0,107 мг/100 г |
г = 0,011 |
|
Значения для мультивитаминного напитка: | ||
|
Пиридоксамин |
х = 0,004 мг/100 г |
г = 0,003 |
|
Пиридоксаль |
х = 0,004 мг/100 г |
г = 0,003 |
|
Пиридоксин |
х = 0,374 мг/100 г |
г = 0,056 |
|
Витамин В6 |
х = 0,380 мг/100 г |
г = 0,056 |
8.3 Воспроизводимость
Абсолютное расхождение между результатами двух единичных испытаний, полученными на идентичном объекте испытаний двумя лабораториями, должно превышать предел воспроизводимости R не более чем в 5 % случаев.
|
Пиридоксамин |
х = 0,065 мг/100 г |
R = 0,035 |
|
Пиридоксаль |
х = 0,080 мг/100 г |
Я? = 0,071 |
|
Пиридоксин |
х = 0,523 мг/100 г |
Я? = 0,151 |
|
Витамин В6 |
х = 0,667 мг/100 г |
R = 0,193 |
|
Значения для порошкового картофельного пюре: | ||
|
Пиридоксамин |
х = 0,163 мг/100 г |
R = 0,089 |
|
Пиридоксаль |
х = 0,032 мг/100 г |
R = 0,022 |
|
Пиридоксин |
х = 1,008 мг/100 г |
Я? = 0,314 |
|
Витамин BR |
х = 1,204 мг/100 г |
R = 0,369 |
|
Значения для овощей с ветчиной (детское питание | ||
|
Пиридоксамин |
х = 0,043 мг/100 г |
Я? = 0,013 |
|
Пиридоксаль |
х = 0,009 мг/100 г |
Я? = 0,013 |
|
Пиридоксин |
х = 0,047 мг/100 г |
Я? = 0,021 |
|
Витамин В6 |
х = 0,107 мг/100 г |
Я? = 0,039 |
|
Значения для мультивитаминного напитка: | ||
|
Пиридоксамин |
х= 0,004 мг/100 г |
Я? = 0,005 |
|
Пиридоксаль |
х = 0,004 мг/100 г |
Я? = 0,005 |
|
Пиридоксин |
х= 0,374 мг/100 г |
Я? = 0,086 |
|
Витамин В6 |
х = 0,380 мг/100 г |
Я? = 0,095 |
|
9 Протокол |
испытания | |
Значения для порошковой манной крупы с молоком:
Протокол испытания должен содержать по меньшей мере следующие сведения:
a) всю информацию, необходимую для полной идентификации пробы;
b) ссылку на настоящий стандарт или используемый метод;
c) дату и метод отбора пробы (если они известны);
d) дату поступления пробы в лабораторию;
e) дату проведения испытания;
f) результаты и единицы, в которых выражены результаты испытания;
д) информацию о других специфичных особенностях, которые наблюдались в ходе проведения испытания;
h) информацию о других особенностях, не установленных в настоящем методе или рассматриваемых как дополнительные, которые могут повлиять на результаты испытания.
9
Приложение A (справочное)
Данные по прецизионности
Имеющиеся данные были получены с использованием методов ВЭЖХ, установленных в приложении С. Данные результатов испытаний для определения витамина В6 были установлены в ходе межлабораторных испытаний в соответствии с [8], проведенных бывшим BgVV [Bundesinstitut fQr gesundheitlichen Verbraucherschutz und Veterinarmedizin (Немецкий федеральный институт по защите прав потребителей и ветеринарной медицине)].
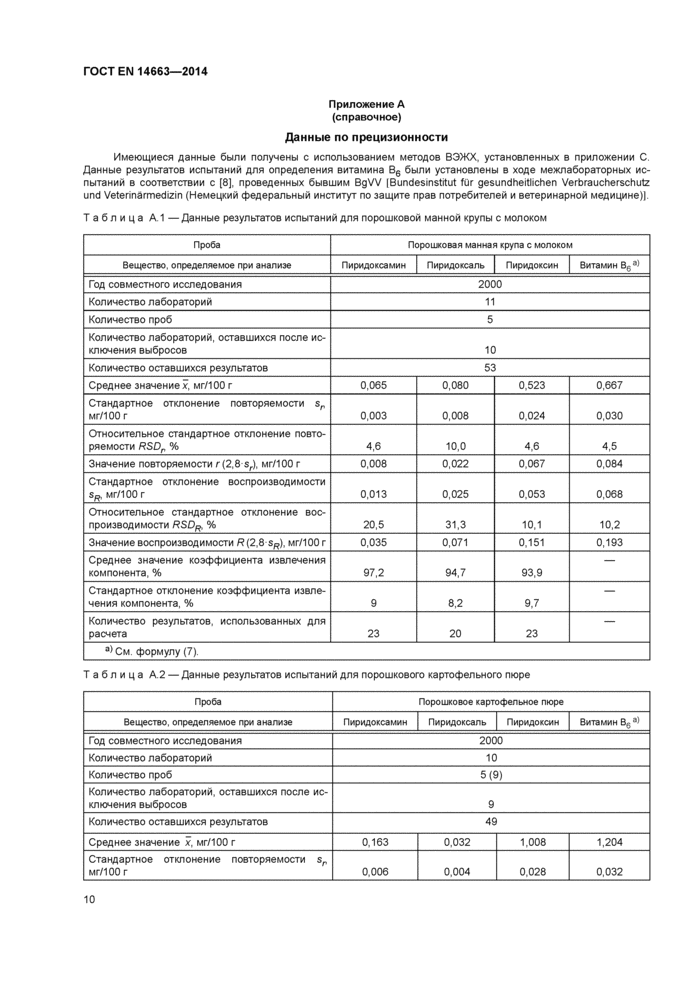
Таблица А.1 —Данные результатов испытаний для порошковой манной крупы с молоком
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Т а б л и ц а А.2 — Данные результатов испытаний для порошкового картофельного пюре | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Проба |
Порошковое картофельное пюре | |||
|
Вещество, определяемое при анализе |
Пиридоксамин |
Пиридоксаль |
Пиридоксин |
Витамин В6а> |
|
Год совместного исследования |
2000 | |||
|
Количество лабораторий |
10 | |||
|
Количество проб |
5(9) | |||
|
Количество лабораторий, оставшихся после исключения выбросов |
9 | |||
|
Количество оставшихся результатов |
49 | |||
|
Среднее значение х, мг/100 г |
0,163 |
0,032 |
1,008 |
1,204 |
|
Стандартное отклонение повторяемости sp мг/100 г |
0,006 |
0,004 |
0,028 |
0,032 |
|
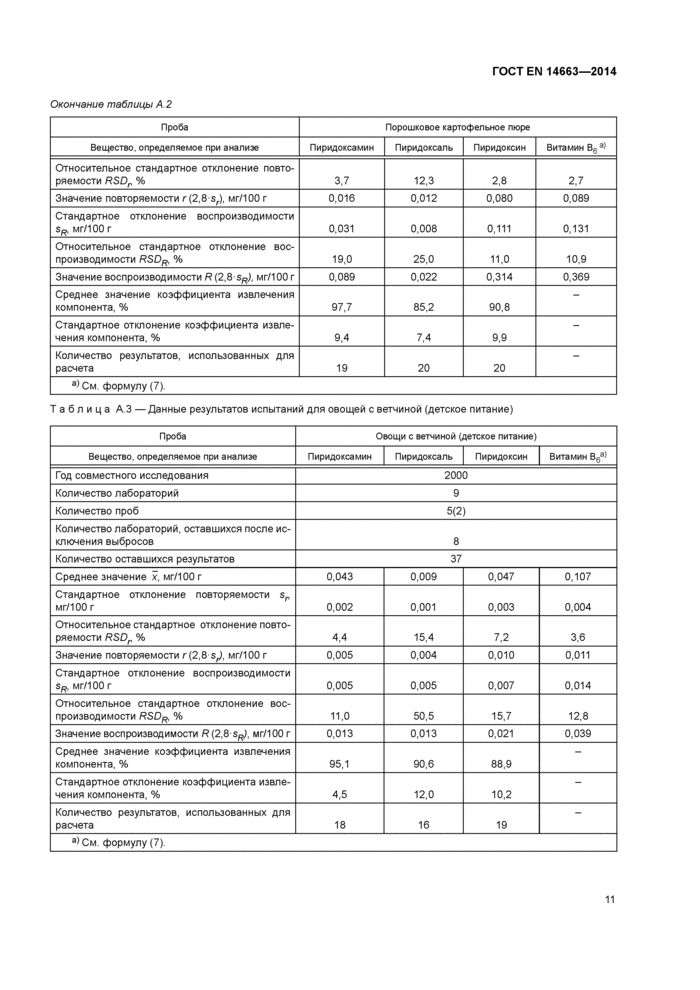
Окончание таблицы А 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица А.З —Данные результатов испытаний для овощей с ветчиной (детское питание) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
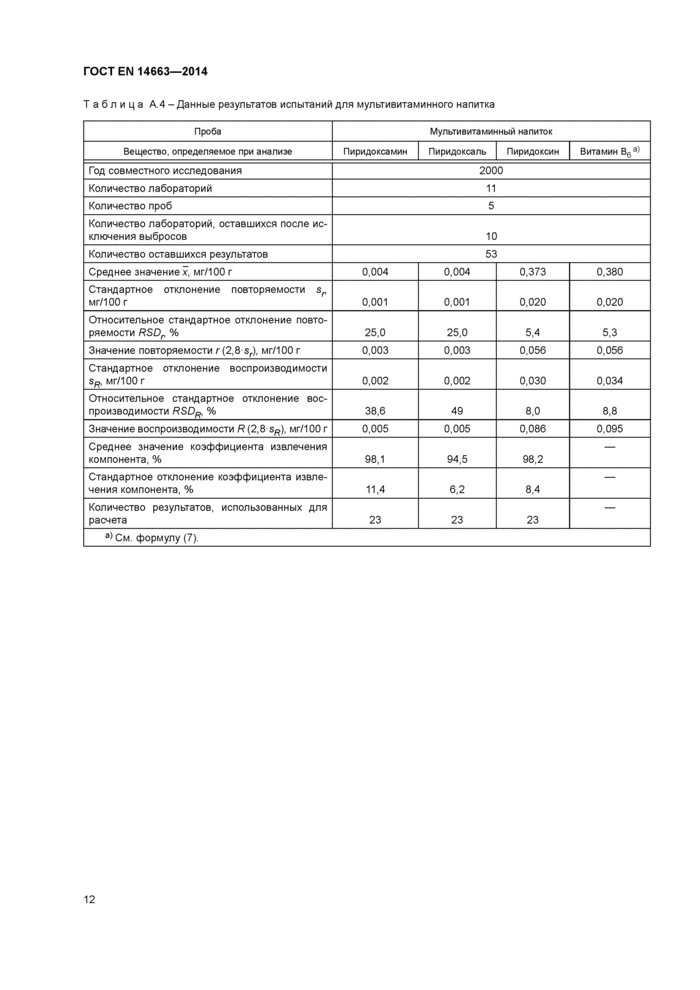
T а б л и ц a А.4 - Данные результатов испытаний для мультивитаминного напитка | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
12
Приложение В (справочное)
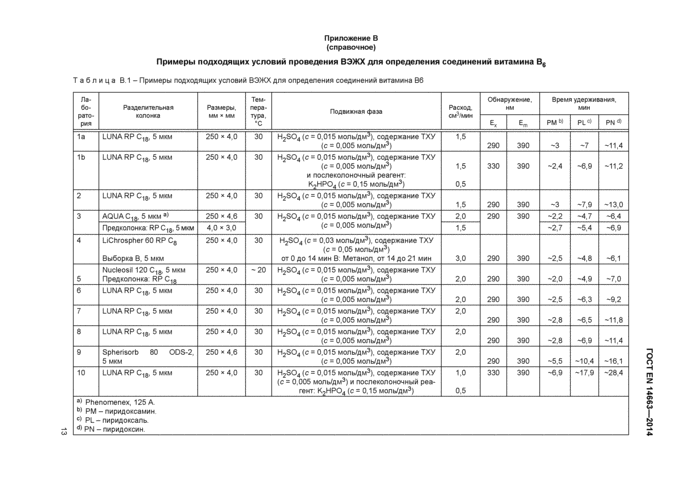
Примеры подходящих условий проведения ВЭЖХ для определения соединений витамина В6
Таблица В.1- Примеры подходящих условий ВЭЖХ для определения соединений витамина В6
|
Ла- бо- рато- рия |
Разделительная колонка |
Размеры, мм х мм |
Тем пера тура, °С |
Подвижная фаза |
Расход, см3/мин |
Обнаружение, нм |
Время удерживания, мин | |||
|
Ех |
Ет |
РМ ь> |
PL с> |
PN d> | ||||||
|
1а |
LUNA RP С18, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
1,5 |
290 |
390 |
~3 |
~7 |
-11,4 |
|
1 b |
LUNA RP С18, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) и послеколоночный реагент: К2НР04 (с = 0,15 моль/дм3) |
1,5 0,5 |
330 |
390 |
—2,4 |
-6,9 |
-11,2 |
|
2 |
LUNA RP С18, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
1,5 |
290 |
390 |
~3 |
-7,9 |
-13,0 |
|
3 |
AQUAC18, 5 мкм а) |
250 х 4,6 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
2,0 |
290 |
390 |
—2,2 |
-4,7 |
-6,4 |
|
Предколонка: RP С18, 5 мкм |
4,0 х 3,0 |
1,5 |
-2,7 |
-5,4 |
-6,9 | |||||
|
4 |
LiChrospher 60 RP С8 Выборка В, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,03 моль/дм3), содержание ТХУ (с = 0,05 моль/дм3) от 0 до 14 мин В: Метанол, от 14 до 21 мин |
3,0 |
290 |
390 |
-2,5 |
-4,8 |
-6,1 |
|
5 |
Nucleosil 120 С18, 5 мкм Предколонка: RP С18 |
250 х 4,0 |
~ 20 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
2,0 |
290 |
390 |
-2,0 |
-4,9 |
-7,0 |
|
6 |
LUNA RP С18, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
2,0 |
290 |
390 |
-2,5 |
-6,3 |
-9,2 |
|
7 |
LUNA RP С18, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
2,0 |
290 |
390 |
-2,8 |
-6,5 |
-11,8 |
|
8 |
LUNA RP С18, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
2,0 |
290 |
390 |
-2,8 |
-6,9 |
-11,4 |
|
9 |
Spherisorb 80 ODS-2, 5 мкм |
250 х 4,6 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) |
2,0 |
290 |
390 |
-5,5 |
-10,4 |
-16,1 |
|
10 |
LUNA RP С18, 5 мкм |
250 х 4,0 |
30 |
H2S04 (с = 0,015 моль/дм3), содержание ТХУ (с = 0,005 моль/дм3) и послеколоночный реагент: К2НР04 (с = 0,15 моль/дм3) |
1,0 0,5 |
330 |
390 |
-6,9 |
-17,9 |
-28,4 |
|
a) Phenomenex, 125 А. b) РМ - пиридоксамин. c) PL-пиридоксаль. d) PN - пиридоксин. | ||||||||||
rOCTEN 14663—2014
Приложение С (справочное)
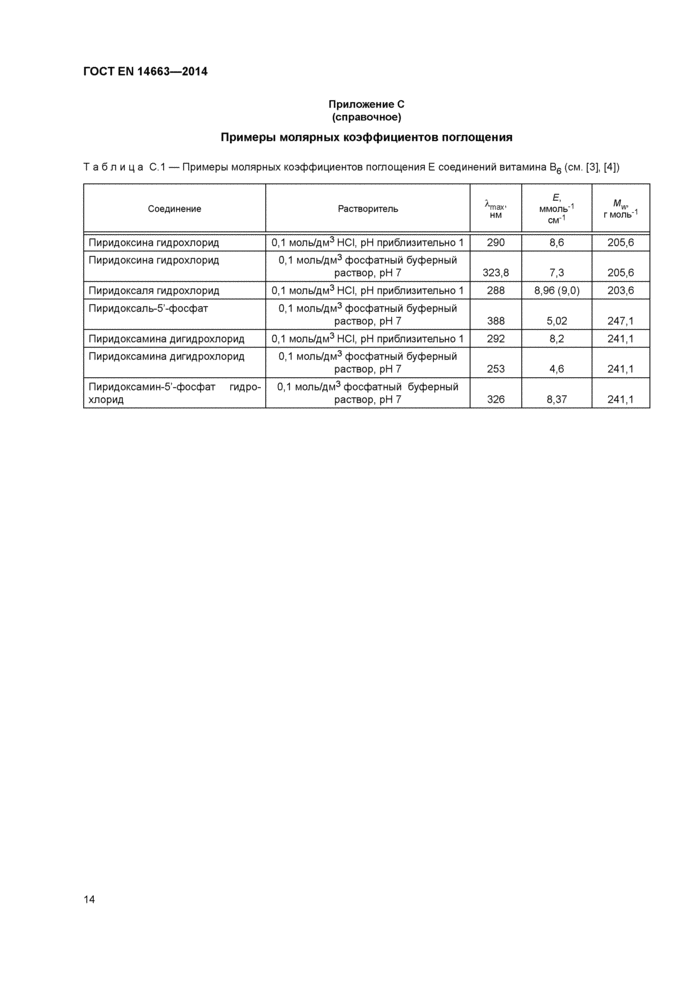
Примеры молярных коэффициентов поглощения
|
Таблица С.1 — Примеры молярных коэффициентов поглощения Е соединений витамина В6 (см. [3], [4]) | ||||||||||||||||||||||||||||||||||||||||
|
14
ГОСТ EN 14663—2014
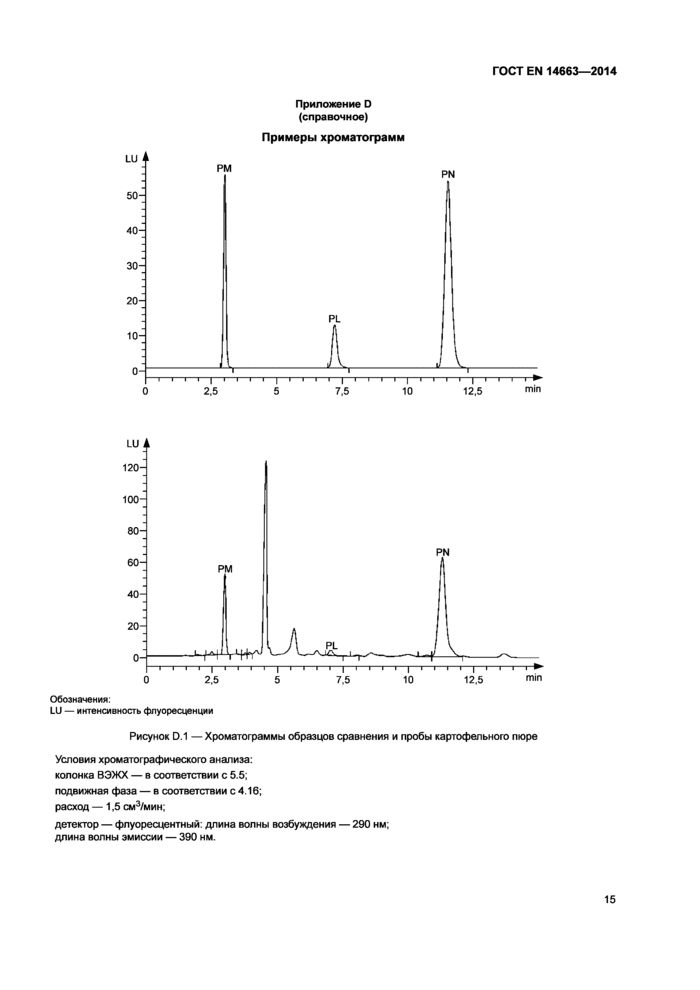
Приложение D (справочное)
Примеры хроматограмм
Обозначения:
LU — интенсивность флуоресценции
Рисунок D.1 —Хроматограммы образцов сравнения и пробы картофельного пюре
Условия хроматографического анализа: колонка ВЭЖХ — в соответствии с 5.5; подвижная фаза — в соответствии с 4.16; расход —1,5 см3/мин;
детектор — флуоресцентный: длина волны возбуждения — 290 нм; длина волны эмиссии — 390 нм.
15
Приложение ДА (справочное)
Сведения о соответствии ссылочных европейских стандартов межгосударственным
стандартам
|
Т а б л и ц а ДА. 1 | |||||||||
| |||||||||
^ В Российской Федерации действует ГОСТ Р 52501-2005 «Вода для лабораторного анализа. Технические условия».
rOCTEN 14663—2014
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ, 2016
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
rOCTEN 14663—2014Библиография
[1] Bognar, A.: Bestimmung von Vitamin B6 in Lebensmitteln mit Hilfe der Hochdruckflussig-Chromatographie (HPLC) Z Lebensm Unters Forsch A, 1985, 181: 200—205 (Определение содержания витамина B6 в продуктах питания с использованием ВЭЖХ)
[2] Bognar, A., Ollilainen, V: Influence of Extraction on the Determination of Vitamin B6 in Food by FIPLC Z Lebensm Unters Forsch A, 1997, 204: 327—335 (Влияние экстракции на определение витамина В6 в пищевых продуктах методом ВЭЖХ)
[3] Metzler, D. Е., and Snell, Е. Е.: Spectra and Ionisation Constants of the Vitamin B6 — Group and Related 3-Plydroxy-pyridine Derivates Journal ofthe American Chemical Society. 1955, 77:2431—2437 (Константы спектра и ионизации группы витамина В6 — группа и связанные производные 3-гидроксипиридина)
[4] Bitsch, R., Moller, J., J Chromatogr 1989, 463: 207—211 (Журнал хроматографии)
[5] Ollilainen, V: FIPLC Analysis of Vitamin B6 in Agricultural and Food Science in Finland Department of Applied Chemistry and Microbiology University of FHelsinki 1999. Vol. 8:No. 6: 515—619 (Анализ ВЭЖХ витамина B6 в науках о сельском хозяйстве и продуктах питания в Финляндии)
[6] Bergaentzle, М., Arella, F., Bourguignon, J.B., Plasselmann, С.: Determination of vitamin B6 in foods by FIPLC A collaborative study. Food Chemistry, 1995, 52: 81—86 (Определение витамина B6 в пищевых продуктах методом ВЭЖХ)
[7] Ndaw, S., Bergaentzle, М., Aoude-Werner, D., Plasselmann, C.: Extraction procedures for the liquid chromatographic determination of thiamin Riboflavin and vitamin B6 in foodstuffs Food Chemistry 2000, 71, 129—138 (Процедуры экстракции для определения тиамина, рибофлавина и витамина В6 в пищевых продуктах методом жидкостной хроматографии)
[8] ISO 5725:19861) Precision of test methods — Determination of repeatability and reproducibility for a standard test
method by inter-laboratory tests (Точность (правильность и прецизионность) методов и результатов измерений. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений)
!> ISO 5725:1986 отменен и заменен на ISO 5725-1:1994, ISO 5725-2:1994, ISO 5725-3:1994, ISO 5725-4:1994, ISO 5725-5:1998, ISO 5725-6:1994.
17
Содержание
1 Область применения....................................................................................................................................1
2 Нормативные ссылки....................................................................................................................................1
3 Сущность метода..........................................................................................................................................1
4 Реактивы........................................................................................................................................................1
5 Оборудование...............................................................................................................................................5
6 Методика проведения испытания................................................................................................................5
7 Вычисление результата................................................................................................................................7
8 Прецизионность............................................................................................................................................8
9 Протокол испытания.....................................................................................................................................9
Приложение А (справочное) Данные по прецизионности..........................................................................10
Приложение В (справочное) Примеры подходящих условий проведения ВЭЖХ
для определения соединений витамина В6......................................................................13
Приложение С (справочное) Примеры молярных коэффициентов поглощения.....................................14
Приложение D (справочное) Примеры хроматограмм...............................................................................15
Приложение ДА (справочное) Сведения о соответствии ссылочных европейских
стандартов межгосударственным стандартам...............................................................16
Библиография................................................................................................................................................17
IV
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТПРОДУКЦИЯ ПИЩЕВАЯОпределение витамина В6 (включая гликозилированные формы) методом высокоэффективной жидкостной хроматографии
Определение витамина В6 (включая гликозилированные формы) методом высокоэффективной жидкостной хроматографии
Foodstuffs.
Determination of vitamin B6 (including its glycosylated forms) by high performance liquid chromatography method
Дата введения — 2017—06—01
1 Область применения
Настоящий стандарт устанавливает метод определения витамина В6 в пищевой продукции с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
Витамин В6 определяется как сумма пиридоксина, пиридоксаля, пиридоксамина, включая ихфос-форилированные производные, а также p-гликозилированные формы, в пересчете на пиридоксин.
Настоящий метод был успешно проверен на манной крупе с молоком (детское питание), картофельном пюре, овощах с ветчиной (типичная пищевая продукция) и мультивитаминном напитке в диапазоне концентраций от 0,034 мг/100 г до 1,210 мг/100 г.
2 Нормативные ссылки
Для применения настоящего стандарта необходим следующий ссылочный стандарт. Для недатированных ссылок применяют последнее издание ссылочного стандарта (включая все его изменения).
EN ISO 3696 Water for analytical laboratory use — Specification and test methods (Вода для лабораторного анализа. Технические требования и методы испытаний)
3 Сущность метода
Производные витамина В6 (пиридоксаль, пиридоксамин и пиридоксин) извлекают из пищевой продукции путем кислотного гидролиза, затем подвергают ферментативному воздействию: дефосфорили-руют, используя кислую фосфатазу, и дегликозилируют, используя (5-глюкозидазу.
Полученные производные витамина В6 разделяют и количественно определяют методом ВЭЖХ с флуоресцентным детектированием ([1], [2]).
4 Реактивы4.1 Общие положения
В ходе анализа используют только реактивы признанной аналитической чистоты и воду не ниже первой степени чистоты в соответствии с EN ISO 3696 или бидистиллированную воду.
4.2 Фосфат калия двузамещенный, массовая доля w(K2HP04-3H20) > 99,9 %.
4.3 Ацетат натрия безводный, w(CH3COONa) > 99,0 %.
4.4 Трихлоруксусная кислота (ТХУ), w(CI3CCOOOH) > 99,0 %.
4.5 Раствор ацетата натрия молярной концентрацией с (CH3COONa) = 2,5 моль/дм3
205 г ацетата натрия (см. 4.3) растворяют в 1 дм3 воды.
4.6 Реагент послеколоночный (дополнительно), К2НР04 раствор с концентрацией с (К2НР04) = = 0,15 моль/дм3.
Издание официальное
Растворяют 34,2 г фосфата калия двузамещенного (см. 4.2) в воде, доводят до 1000 см3, перемешивают и дегазируют.
4.7 Соляная кислота, c(HCI) = 1 моль/дм3.
4.8 Соляная кислота, с(НС1) = 0,1 моль/дм3.
4.9 Соляная кислота, с(НС1) = 0,2 моль/дм3.
4.10 Серная кислота, c^SO^ = 1 моль/дм3.
4.11 Эфир петролейный, диапазон кипения от 40 °С до 60 °С.
4.12 Фосфатаза кислая из картофеля. Ферментативная активность составляет около 5,3 U/мг1).
Необходимо, чтобы используемый фермент с положительным результатом проходил проверку
ферментативной активности согласно 4.13.2 (более подробная информация приведена в [2], [7]).
4.13 Раствор кислой фосфатазы
4.13.1 Общие положения
Растворяют 60 мг кислой фосфатазы (см. 4.12) в 10 см3 воды в конической колбе, перемешивая в течение 2 мин.
Раствор готовят в день проведения анализа.
4.13.2 Проверка ферментативной активности кислой фосфатазы
Взвешивают 10 г свинины, 5 г картофельного пюре или 5 г муки из цельного зерна в конической колбе и экстрагируют кислотой, как описано в 6.2.1. Добавляют к 12,5 см3 раствора экстрагированной пробы 1 см3 раствора кислой фосфатазы (см. 4.13.1) и опционально 1 см3 раствора р-глюкозидазы (см. 4.15) и перемешивают. Инкубируют раствор в течение не менее 12 ч или в течение ночи при температуре 37 °С при постоянном перемешивании. Повторяют эту операцию с двойным количеством раствора кислой фосфатазы.
Определяют массовую концентрацию витаминов в соответствии с 6.6. Ферментативная активность используемого фермента считается достаточной, если значения массовой концентрации соединений витамина В6 в обоих растворах пробы эквивалентны. На хроматограмме должен отсутствовать пик фосфата пиридоксамина.
Примечание — Для межлабораторного испытания использовали кислую фосфатазу производства Sigma Nr Р 37522).
4.14 р-глюкозидаза из миндаля с ферментативной активностью приблизительно 3,2 U/мг
Необходимо, чтобы используемый фермент с положительным результатом проходил проверку ферментативной активности согласно 4.15.2 (более подробная информация приведена в [2], [7]).
4.15 Раствор р-глюкозидазы
4.15.1 Общие положения
Растворяют 100 мг р-глюкозидазы (см. 4.14) в 10 см3 воды в конической колбе, перемешивая в течение 2 мин.
Раствор готовят в день проведения анализа.
4.15.2 Проверка ферментативной активности р-глюкозидазы
Взвешивают 10 г свинины, 5 г картофельного пюре или 5 г муки из цельного зерна в конической колбе и экстрагируют кислотой, как описано в 6.2.1. Добавляют к 12,5 см3 раствора экстрагированной пробы 1 см3 раствора кислой фосфатазы (см. 4.13.1) и 1 см3 раствора р-глюкозидазы (см. 4.15.1) и перемешивают. Инкубируют раствор в течение не менее 12 ч или в течение ночи при температуре 37 °С при постоянном перемешивании. Данную операцию повторяют с двойным количеством раствора Р-глюкозидазы.
Определяют массовую концентрацию витаминов в соответствии с 6.6. Ферментативная активность используемого фермента считается достаточной, если значения массовой концентрации соединений витамина В6 в обоих растворах пробы эквивалентны. На хроматограмме должен отсутствовать пик фосфата пиридоксамина.
Примечание — Для межлабораторного испытания использовали кислую фосфатазу Sigma Nr G-03952).
rOCTEN 14663—2014
4.16 Подвижная фаза для ВЭЖХ (серная кислота, c(H2S04) = 0,015 моль/дм3, содержащая0,005 моль/дм3 трихлоруксусной кислоты)
(817 ± 5) мг трихлоруксусной кислоты (см. 4.4) растворяют в 15 см3 серной кислоты молярной концентрацией 1 моль/дм3 (см. 4.10), переливают в мерную колбу вместимостью 1000 см3, объем содержимого в колбе доводят до метки водой, перемешивают и дегазируют.
4.17 Силиконовое масло для удаления пены.
4.18 Образцы сравнения4.18.1 Общие положения
Пиридоксамин (РМ), пиридоксаль (PL) и пиридоксин (PN) могут быть получены у различных поставщиков. Чистота образцов сравнения может варьироваться, поэтому необходимо определить их концентрацию и чистоту (см. 4.19.4 и 4.20.7).
4.18.2 Пиридоксамина (РМ) дигидрохпорид, w(C8H12N202-2HCI) > 98 %.
4.18.3 Пиридоксаля (PL) гидрохлорид, w (C8H9N03-HCI) > 98 %.
4.18.4 Пиридоксина (PN) гидрохлорид, w (CgH^NOg-HCI) > 98 %.
4.19 Исходные растворы4.19.1 Исходный раствор пиридоксамина (РМ), массовой концентрацией р(РМ) приблизительно 500 мкг/см3
71.7 мг пиридоксамина дигидрохпорида (см. 4.18.2) растворяют в соляной кислоте молярной концентрацией 0,1 моль/дм3 (см. 4.8) в мерной колбе вместимостью 100 см3, объем содержимого в колбе доводят до метки этим же раствором соляной кислоты.
Срок хранения раствора — 1 неделя при температуре 4 °С или 2 мес при температуре минус 18 °С.
4.19.2 Исходный раствор пиридоксаля (PL) массовой концентрацией p(PL) приблизительно 500 мкг/см3
60,9 мг пиридоксаля гидрохлорида (см. 4.18.3) растворяют в соляной кислоте молярной концентрацией 0,1 моль/дм3 (см. 4.8) в мерной колбе вместимостью 100 см3, объем содержимого в колбе доводят до метки этим же раствором соляной кислоты.
Срок хранения раствора — 1 неделя при температуре 4 °С или 2 мес при температуре минус 18 °С.
4.19.3 Исходный раствор пиридоксина (PN), массовой концентрацией p(PN) приблизительно 500 мкг/см3
60.8 мг пиридоксина гидрохлорида (см. 4.18.4) растворяют в соляной кислоте молярной концентрацией 0,1 моль/дм3 (см. 4.8) в мерной колбе вместимостью 100 см3, объем содержимого в колбе доводят до метки этим же раствором соляной кислоты.
Срок хранения раствора — 1 неделя при температуре 4 °С или 2 мес при температуре минус 18 °С.
4.19.4 Определение концентраций растворов
Отбирают пипеткой 1 см3 исходного раствора пиридоксамина (см. 4.19.1), пиридоксаля (см. 4.19.2) и пиридоксина (см. 4.19.3) соответственно в мерные колбы вместимостью 50 см3 и содержимое колб доводят до метки 0,1 моль/дм3 HCI (см. 4.8). Измеряют оптическую плотность растворов в кювете из кварцевого стекла с толщиной поглощающего слоя 1 см при длинах волн, соответствующих максимумам поглощения относительно 0,1 моль/дм3 HCI (см. таблицу 1).
|
Таблица 1 — Примеры молярных коэффициентов поглощения соединений витамина В6 | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
|
Массовую концентрацию пиридоксамина, пиридоксаля и пиридоксина в исходных растворах р,, мкг/см3, вычисляют, используя молярный коэффициент поглощения, по формуле | ||||||||||||||||||||||||||||||
где A — значение оптической плотности растворов пиридоксамина, пиридоксаля и пиридоксина при длинах волн, соответствующих максимумам поглощения ^тах (см. таблицу 1);
М(- — молярная масса образцов сравнения PM, PL или PN соответственно согласно таблице 1, г/моль;
V — коэффициент разбавления, см3 (в данном случае V = 50 см3);
F — коэффициент для вычисления доли свободных форм соединений витамина В6;
еI — молярный коэффициент поглощения PM, PL или PN при соответствующем pH согласно таблице 1, ммоль-1 см-1.
Данные значения массовой концентрации используют для вычисления точных концентраций веществ, приведенных в пунктах 4.19.1—4.19.3 и 4.20.1—4.20.6.
4.20 Стандартные растворы4.20.1 Стандартный раствор пиридоксамина (PM) I, массовой концентрацией р(РМ) приблизительно 10 мкг/см3
Разбавляют 2 см3 исходного раствора пиридоксамина (см. 4.19.1) 0,1 моль/дм3 HCI (см. 4.8) и доводят до 100 см3. Полученный раствор хранению не подлежит.
4.20.2 Стандартный раствор пиридоксаля (PL) I, р(Р1_) приблизительно 10 мкг/см3 Разбавляют 2 см3 исходного раствора пиридоксаля (см. 4.19.2) 0,1 моль/дм3 HCI (см. 4.8) и доводят до 100 см3. Полученный раствор хранению не подлежит.
4.20.3 Стандартный раствор пиридоксина (PN) I, р(Р1_) приблизительно 10 мкг/см3 Разбавляют 2 см3 исходного раствора пиридоксаля (см. 4.19.3) 0,1 моль/дм3 HCI (см. 4.8) и доводят до 100 см3. Полученный раствор хранению не подлежит.
4.20.4 Стандартный раствор пиридоксамина (PM) II, р(РМ) приблизительно 1 мкг/см3 Разбавляют 10 см3 исходного раствора пиридоксамина (см. 4.20.1) 0,1 моль/дм3 HCI (см. 4.8) и
доводят до 100 см3. Полученный раствор хранению не подлежит.
4.20.5 Стандартный раствор пиридоксаля (PL) II, p(PL) приблизительно 1 мкг/см3 Разбавляют 10 см3 стандартного раствора пиридоксаля (см. 4.20.2) 0,1 моль/дм3 HCI (см. 4.8) до
100 см3. Полученный раствор хранению не подлежит.
4.20.6 Стандартный раствор пиридоксина (PN) II, p(PL) приблизительно 1 мкг/см3 Разбавляют 10 см3 стандартного раствора пиридоксина (см. 4.20.3) 0,1 моль/дм3 HCI (см. 4.8) и
доводят до 100 см3. Полученный раствор хранению не подлежит.
4.20.7 Проверка хроматографической чистоты методом ВЭЖХ
Чистота образцов сравнения может быть проверена методом ВЭЖХ, как описано ниже: вводят соответствующие объемы PM, PL и PN стандартных растворов I (см. 4.20.1, 4.20.2, 4.20.3) в систему ВЭЖХ и анализируют, как установлено в 6.4.
Степень чистоты образцов сравнения Rh %, вычисляют по формуле
(2)
X. 100
X/ + В ’
где х( — площадь пика образца сравнения /;
В — сумма площадей пиков загрязняющих веществ (без пика растворителя).
Хроматографическая чистота образцов сравнения должна быть не менее 98 %, в ином случае используют новые образцы сравнения или готовят новые стандартные растворы.
4.21 Смешанный градуировочный раствор (например р(РМ, PL, PN) = 0,1 мкг/см3 до 10 мкг/см3)
Отбирают пипеткой подходящие объемы исходных растворов PM, PL и PN (см. 4.19.1—4.19.3) или стандартных растворов (см. 4.20.1—4.20.6) в мерную колбу вместимостью 20 см3 и при необходимости доводят 0,1 моль/дм3 HCI (см. 4.8) до объема 6,5 см3. Доводят pH до значения 4,8 ед. pH, используя раствор ацетата натрия молярной концентрацией 2,5 моль/дм3 (см. 4.5), а затем доводят pH до значения 3,0 ед. pH, используя серную кислоту (см. 4.10), объем содержимого в колбе доводят водой до метки и перемешивают (градуировочные растворы). Рекомендуется использовать не менее трех градуировочных точек. При необходимости допускается разбавление смешанных градуировочных растворов подвижной фазой до ввода в хроматограф.
ГОСТ EN 14663—20145 Оборудование
5.1 Общие положения
Используют общепринятое лабораторное оборудование, стеклянную посуду, вспомогательное оборудование и следующие средства измерений.
5.2 УФ-спектрофотометр, пригодный для измерения оптической плотности при определенных длинах волн.
5.3 Нагревательные приборы
Используют лабораторный автоклав и печь или водяную баню, оборудованные мешалками и позволяющие устанавливать температуру на уровне 37 °С.
5.4 Система для ВЭЖХ
Система для ВЭЖХ состоит из насоса, устройства для ввода проб, флуоресцентного детектора, обеспечивающего длину волны возбуждения 290 нм и длину волны регистрации 390 нм, интегратора или устройства для обработки данных, устройства для постколоночной дериватизации.
5.5 Колонки для ВЭЖХ
Используют обращенно-фазовую колонку со следующими характеристиками:
Luna™ RP С18, 5 мкм3), размер частицы 5 мкм, диаметр 4,0 мм, длина 250 мм4). Другие примеры подходящих колонок для ВЭЖХ приведены в приложении В.
5.6 Устройства фильтровальные
Фильтрация подвижной фазы, а также раствора анализируемой пробы через мембранный фильтр с размером пор 0,45 мкм перед использованием или вводом проб увеличит срок службы колонок.
6 Методика проведения испытания6.1 Подготовка анализируемой пробы
Отбирают и гомогенизируют анализируемую пробу. Измельчают материал в соответствующем смесителе-мельнице и снова перемешивают. Чтобы не подвергать пробу воздействию высокой температуры в течение длительного периода времени, необходимо предварительно ее охладить. После гомогенизации пробу сразу анализируют.
6.2 Подготовка раствора анализируемой пробы6.2.1 Экстракция
6.2.1.1 Общие положения
Из проб с высоким содержанием жира (более 25 %) следует удалить жир, например, путем обработки петролейным эфиром перед кислотным гидролизом.
Для обработки пенящихся материалов рекомендуется использование нескольких капель силиконового масла (см. 4.17).
Значение pH экстрагированного раствора должно быть приблизительно 1 ед. pH. В ином случае рекомендуется уменьшить массу пробы или использовать соляную кислоту с более высокой концентрацией [(например, 0,2 моль/дм5 6 7 (см. 4.9) или 1 моль/дм5 (см. 4.7)].
6.2.1.2 Экстракция из сухих продуктов (содержание воды менее 20 %; например, в крупах, сухом молоке, сушеных овощах)
Взвешивают от 1 до 10 г гомогенизированной анализируемой пробы (см. 6.1) с точностью до миллиграмма в конической колбе вместимостью 150 см5, добавляют 50 см5 0,1 моль/дм5 соляной кислоты (см. 4.8), перемешивают и проверяют, чтобы значение pH составляло приблизительно 1 ед. pH.
Нагревают в автоклаве (см. 5.3) в течение 30 мин при температуре 120 °С, затем охлаждают до комнатной температуры, переносят в мерную колбу вместимостью 100 см3, объем содержимого в колбе доводят водой до 100 см3 (с возможным силиконовым слоем выше метки) и перемешивают.
Фильтруют или центрифугируют при 3000 об/мин аликвотную часть (приблизительно 50 см3) пробы, обработанной кислотой, и отбирают верхний слой в герметичные стеклянные емкости (данный раствор является экстрактом пробы).
6.2.1.3 Экстракция из продуктов с высоким содержанием влаги (более 20 %) и жидких продуктов (например, в мясе, овощах, соках)
Взвешивают от 2 до 40 г гомогенизированной пробы (см. 6.1) с точностью до миллиграмма в конической колбе вместимостью 150 см3, добавляют 10 см3 1 моль/дм3 соляной кислоты (см. 4.7), доводят водой до приблизительно 50 см3, перемешивают и проверяют, чтобы значение pH составляло приблизительно 1 ед. pH.
Нагревают в автоклаве (см. 5.3) втечение 30 мин притемпературе 120 °С, затем охпаждаютдо комнатной температуры, переносят в мерную колбу вместимостью 100 см3 и объем содержимого в кобле доводят водой до 100 см3 (с возможным силиконовым слоем выше метки) и перемешивают.
Фильтруют или центрифугируют при 3000 об/мин аликвотную часть (приблизительно 50 см3) пробы, обработанной кислотой, и отбирают верхний слой в герметичные стеклянные емкости (данный раствор является экстрактом пробы).
Примечание — Во время автоклавирования может произойти взаимное превращение различных форм витамина, например, путем трансаминирования. Это часто наблюдается в приготовленном мясе или в пробах с высоким содержанием свободных аминогрупп (см. [2], [7]).
6.2.2 Ферментативная обработка и этапы подготовки проб трансформации
Для проб пищевой продукции животного происхождения (свинина, молоко, рыба и т. д.), которые не содержат р-глюкозилированного связанного пиридоксина, ферментативная обработка р-глюкозидазой не является необходимой. Лабораторные эксперименты показывают, что результаты определения общего содержания витамина В6 в пищевой продукции, полученные с применением и без применения р-глюкозидазы для ферментативной обработки, были приблизительно одинаковыми (см. [2], [7]).
Отбирают пипеткой 12,5 см3 экстракта пробы по 6.2.1.2, 6.2.1.3 в коническую колбу вместимостью 20 см3 и доводят pH до значения (4,8 ± 0,1) ед. pH, используя раствор ацетата натрия (см. 4.5). Добавляют 1 см3 раствора кислой фосфатазы (см. 4.13) и 1 см3 раствора р-глюкозидазы (см. 4.15) и перемешивают. Накрывают коническую колбу и инкубируют раствор в течение не менее 12 ч или в течение ночи при температуре 37 °С, постоянно перемешивая.
После охлаждения до комнатной температуры доводят pH до значения приблизительно 3 ед. pH, используя серную кислоту (см. 4.10), переливают отрегулированный раствор количественно в мерную колбу вместимостью 20 см3 и объем содержимого в колбе доводят до метки водой. Встряхивают и фильтруют через сухой складчатый бумажный фильтр, удаляют первые 5 см3 фильтрата.
Подготовленный раствор пробы хранят до 3 сут в холодильнике при температуре около 4 °С.
Перед хроматографическим анализом фильтруют аликвоту (приблизительно 2 см3) через мембранный фильтр (см. 5.6) и разбавляют подвижной фазой, если необходимо.
6.3 Подготовка «холостой» пробы
Отбирают пипеткой 12,5 см3 раствора соляной кислоты (см. 4.8) в коническую колбу вместимостью 20 см3 и доводят pH до значения (4,8 ± 0,1) ед. pH, используя раствор ацетата натрия молярной концентрацией 2,5 моль/дм3 (см. 4.5). Добавляют 1 см3 раствора кислой фосфатазы (см. 4.13) и 1 см3 раствора р-глюкозидазы (см. 4.15) и перемешивают. Инкубируют раствор в течение не менее 12 ч или в течение ночи при температуре 37 °С при постоянном перемешивании.
После охлаждения до комнатной температуры доводят pH до значения приблизительно 3 ед. pH, используя серную кислоту (см. 4.10), переливают количественно в мерную колбу вместимостью 20 см3, объем содержимого в колбе доводят водой до метки, встряхивают и фильтруют через сухой складчатый бумажный фильтр, удаляя первые 5 см3 фильтрата.
Перед хроматографическим анализом фильтруют аликвоту (приблизительно 2 см3) через мембранный фильтр (см. 5.6) и разбавляют подвижной фазой, если необходимо.
6.4 Условия хроматографического анализа
Эффективность системы ВЭЖХ должна обеспечивать разделение пиков PM, PL и PN друг от друга, а также от пиков всех других веществ пробы до базовой линии.
6
1
1) U — данная единица измерения (международная или стандартная единица) определяется количеством фермента, который катализирует трансформацию 1 мкмоль субстрата в минуту при стандартных условиях.
2) Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламой указанного продукта со стороны CEN. Допускается использовать аналогичную продукцию, если она позволяет получать сопоставимые результаты.
2
3
^ Luna™ — это пример продукта, доступного на рынке, поставляемого фирмой Phenomenex. Данная информация приведена для удобства пользователей настоящего стандарта и не является рекламой указанного продукта со стороны CEN. Допускается использовать аналогичную продукцию, если она позволяет получать сопоставимые результаты.
4
) Допускается использовать размеры частиц или колонок, которые отличаются от установленных в настоя
5
щем стандарте. Параметры разделения должны адаптироваться к таким материалам, чтобы гарантировать эквивалентные результаты. Критерий эффективности функционирования подходящих аналитических колонок является
6
базовым разрешением рассматриваемых веществ, определяемых при анализе.
7