ГОСТ 15848.1-90
Руды хромовые и концентраты. Метод определения оксида хрома (III)
Купить ГОСТ 15848.1-90 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на хромовые руды и концентраты и устанавливает титриметрический серебряно-персульфатный метод определения массовой доли оксида хрома (III) (от 10 до 65%).
Ограничение срока действия снято: Протокол № 7-95 МГС от 01.03.95 (ИУС 11-95)
Оглавление
1 Общие требования
2 Аппаратура, реактивы и растворы
3 Проведение анализа
4 Обработка результатов
Приложение Руды хромовые и концентраты
| Дата введения | 01.01.1992 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 29.12.1990 | Утвержден | Госстандарт СССР | 3671 |
|---|---|---|---|
| Разработан | Министерство черной металлургии СССР |
Chromium ores and concentrates. Method for determination of chromium oxide (III)
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 11125-84 Кислота азотная особой чистоты. Технические условия
- ГОСТ 1277-75 Реактивы. Серебро азотнокислое. Технические условия
- ГОСТ 14262-78 Кислота серная особой чистоты. Технические условия
- ГОСТ 15848.0-90 Руды хромовые и концентраты. Общие требования к методам химического анализа
- ГОСТ 20478-75 Реактивы. Аммоний надсернокислый. Технические условия
- ГОСТ 20490-75 Реактивы. Калий марганцовокислый. Технические условия
- ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
- ГОСТ 4208-72 Реактивы. Соль закиси железа и аммония двойная сернокислая (соль Мора). Технические условия
- ГОСТ 4220-75 Реактивы. Калий двухромовокислый. Технические условия
- ГОСТ 435-77 Реактивы. Марганец (II) сернокислый 5-водный. Технические условия
- ГОСТ 4461-77 Реактивы. Кислота азотная. Технические условия
- ГОСТ 4462-78 Реактивы. Кобальт (II) серно-кислый 7-водный. Технические условия
ГОСТ 4465-74Реактивы. Никель (II) сернокислый 7-водный. Технические условия. Заменен на ГОСТ 4465-2016.- ГОСТ 5839-77 Реактивы. Натрий щавелево-кислый. Технические условия
- ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
- ГОСТ 83-79 Реактивы. Натрий углекислый. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6
стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13
УДК 622.346.1 —15 : 546.722—31.06 Группа А39
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
РУДЫ ХРОМОВЫЕ И КОНЦЕНТРАТЫ
Метод определения оксида хрома (III)
Chromium oks and contenhaks Me*hod for dekrmmatton of chiommm oxide (III)
ГОСТ 15848.1-90 (ИСО 6331—83)
ОКСТУ 0741
Срок действия с 01.01.92
до 01.01.2002
Настоящий стандарт распространяется на хромовые руды и концентраты и устанавливает титриметрический серебряно-пср-сульфатный метод определения массовой доли оксида хрома (III) (от 10 до 65 %).
Метод определения оксида хрома по международному стандарту ИСО 6331—84 указан в приложении.
Метод основан на окислении трехвалентного хрома в сернокислой среде надсернокислым аммонием в присутствии катализатора—азотнокислого серебра или смеси сернокислого кобальта и сернокислого никеля.
Шестивалентный хром восстанавливают раствором соли Мора и избыток его огтитровывают раствором марганцовокислого калия. При массовой доле ванадия в анализируемом образце до 0,05 % допускается шестивалентный хром титровать непосредственно раствором соли Мора в присутствии индикатора фенилан-траниловой кислоты. Конечную точку титрования можно устанавливать потенциометрически.
Навеску руды или концентрата сплавляют с пероксидом натрия или разлагают в смеси серной и фосфорной кислот.
1. ОБЩИЕ ТРЕБОВАНИЯ
Общие требования к методу определения оксида хрома — по
Издание официальное
ГОСТ 15848.1-90 С. 2
2. АППАРАТУРА, РЕАКТИВЫ И РАСТВОРЫ
Печь муфельная с терморегулятором, обеспечивающая температуру нагрева не ниже 800 °С.
Установка потенциометрическая с парами электродов: плати-на-хлорид-серебряный, платина-вольфрам или другими электродами, обеспечивающими четкое фиксирование конечной точки титрования (к. т. т.).
Тигли железные.
Кислота азотная по ГОСТ 4461 или ГОСТ 11125.
Кислота ортофосфорная по ГОСТ 6552.
Кислота серная по ГОСТ 4204 или ГОСТ 14262 и разбавленная 1:1, 1:4, 1 : 100.
Марганец (II) сернокислый 5-водный по ГОСТ 435 (сульфат марганца (II), раствор с массовой концентрацией 1 г/дм3.
Серебро азотнокислое по ГОСТ 1277 (нитрат серебра (I), раствор с массовой концентрацией 1 г/дм3. Для большей устойчивости раствора азотнокислого серебра приливают 0,5 см3 азотной кислоты на каждый 1 дм3 раствора. Раствор хранят в склянке из темного стекла.
Кобальт (II) сернокислый 7-водный по ГОСТ 4462 (сульфат кобальта (II).,
Никель (II) сернокислый 7-водный по ГОСТ 4465 (сульфат
никеля пи).
Кобальто-никелевый катализатор, раствор: 15 г сернокислого кобальта и 15 г сернокислого никеля помещают в стакан вместимостью 700—800 см3, приливают 500 см3 воды и перемешивают до растворения солей.
Аммоний надсернокислый по ГОСТ 20478 (пероксодисульфат аммони,Я|), раствор с массовой концентрацией 250 г/дм3. Раствор юден к применению в течение 7—10 сут.
Натрий углекислый по ГОСТ 83 (карбонат натрия), раствор с массовой концентрацией 2 г/дм3.
Натрий хлористый по ГОСТ 4233 (хлорид натрия), раствор с массовой концентрацией 50 г/дм3.
Кислота фенилантраниловая, раствор, содержащий 2 г кислоты в 100 см3 раствора углекислого натрия.
Натрия перекись (натрия пероксид).
Калий двухромовокислый по ГОСТ 4220 (дихромат калия), раствор с молярной концентрацией эквивалента ^(УбКгСггОт) = = 0 1 моль/дм3; 4,903? г дв\voqmobo^cпот k-vhh. дважды пере-кристаллизованного и высушенного в течение 2—3 ч при 150—> 170°С, растворяют в 500 —G00 см3 воды в мерной колбе вместимостью 1000 см3, доливают водой до метки и перемешивают, 1 см3 раствора соответствует 0,002533 г оксида хрома (III).
Соль закиси железа и аммония двойная сернокислая (соль
9
0 3 2 Потенциометрическое титрование
Добавляют к испытуемому раствору 63 ом3 раствора серной кислоты (п 4 4), в стакан помещают два электрода (п 5 3 1), включают магнитную мешалку [п 5 1 2) и титруют раствором сульфата железа (II) аммония до максимального о!к гонении стреаки милливольтамперметра к концу титрования — медленно Примечание Объем израсходованного на титрование раствора соответ ствует общему содержанию храма и ванадия
Добавляют по каплям раствор перманганата калия (п 4 11) до появления розовой окраски не исчезающей в течение 2 мин для окисления ванадия Восстанавливают избыток раствора перманганата калия, добавляя по каплям раствор нитрата калия (п 4 13) до исчезновения розовой окраски Немедленно добавляют 1 — 1 5 г мочевины (п 4 14) для удаления избытка нитрата калия Титруют ванадий раствором сульфата железа (II) аммсния до максимального отклонения стрелки милливольтметра
Разница в объемах раствора сульфата железа (II) аммония, израсходованных на титрование соответствует содержанию хрома
7. Обработка результатов
71 Расчет содержания хрома при титровании с визуальной фиксацией точки эквивалентности
Содержание хрома (Сг) в процентах (т/т) вычисляют по формуле
^ [(У> I-Vi)-(V4 f-V,) 1 Т ь
где V0 — объем раствора сульфата железа (II) аммония, изр а сх оде ванный на проведение анализа, см3,
V!—-объем раствора перманганата калия, израсходованный на титрование избытка раствора сульфата железа (II) аммония* ом3,
V2-“ объем раствора сульфата железа (II) аммония, добавленный к раствору контрольного опыта, ом3,
V3 —объем раствора перманганата калия, израсходованный на титрование избытка раствора сульфата железа (II) аммония в контрольном опыте, см3,
/ — соотношение между растворами сульфата железа (II) аммония и перманганата калия,
Т — титр раствора перманганата калия, выраженный в г/см3 хрома; m — масса навески материала г
К — фактор пересчета содержания хрома на cvxoe вещество 72 Расчет содержания хрома при потенциометрическом титровании
Т\ по
m
Сг=
К,
Содержание хрома (Сг) в процентах (m/m) вычисляют по формуле
где Vj —объем раствора сульфата железа (II) аммония, израсходованный на тит~ рование хрома и ванадия, см3,
V2 — объем раствора сульфата железа (II) аммония израсходованный на титрование ванадия, см3 Л — титр раствора сульфата железа (II) аммония, выраженный в г/см3 хрома
тп — масса навески материала* г;
К — фактор пересчета содержания хрома на сухое вещество,
7Э Пересчет содержания хрома на окись хрома
Сг203 [% (m/m)] = 1,4615 Cr[% (m/m)]
ИНФОРМАЦИОННЫЕ ДАННЫЕ
1. РАЗРАБОТАН Министерством металлургии СССР
РАЗРАБОТЧИКИ
Н. И. Стенина (руководитель темы), Г. В. Шибалко, Н. И. Забугорная
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета СССР по управлению качеством продукции и стандартам от 29.12.90 № 3671
Приложение «Руды хромовые и концентраты. Определение содержания хрома. Титриметрический метод» настоящего стандарта подготовлено на основе прямого применения международного стандарта И СО 6331—81
3. ВЗАМЕН ГОСТ 15848.1-70
4. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка
ГОСТ 83-79 ГОСТ 435-77 ГОСТ 1277-75 ГОСТ 4204-77 ГОСТ 4208-72 ГОСТ 4220-75 ГОСТ 4233-77 ГОСТ 4461-77 ГОСТ 4462-78 ГОСТ 4465-74 ГОСТ 5839-77 ГОСТ 6552-80 ГОСТ 11125-84 ГОСТ 14262-78
ГОСТ 15848 0—90
ГОСТ 20478-75 ГОСТ 20490-75 ИСО 6629-81
2
2
2
2
2
2
2
2
2
2
2
2
2
2
2 приложение
2
2
Приложение
С. 3 ГОСТ 15848.1-90
Мора) по ГОСТ 4208, раствор с молярной концентрацией эквивалента c(NH4)2S04* FeS04-6H20) =0,1 моль/дм3: 39,5 г соли Мора растворяют в 250 см3 серной кислоты (1:4), раствор фильтруют в мерную колбу вместимостью 1000 см3, доливают водой до метки и перемешивают.
Для установления массовой концентрации раствора соли Мора 25 см3 раствора двухромовокислого калия с молярной концентрацией эквивалента с(1/бК2Сг207) = 0,1 моль/дм3 помещают в коническую колбу вместимостью 500 см3, приливают 200 см3 воды, 40 см3 серной кислоты (1:1), раствор перемешивают и охлаждают. Затем приливают 5—6 капель раствора фенилантраниловой кислоты, снова перемешивают и медленно титруют раствором соли Мора до перехода вишневой окраски раствора в зеленую.
Массовую концентрацию раствора соли Мора (С) по оксиду хрома (III) в граммах на кубический сантиметр вычисляют по формуле
0,002533 25 с у1
где 0,002533 — масса оксида хрома (III), соответствующая 1 см3 раствора двухромовокислого калия, г;
25 — объем раствора двухромовокислого калия, взятый для титрования, см3;
Vi—объем раствора соли Мора, израсходованный на титрование с учетом значения контрольного опыта, см3.
Массовую концентрацию раствора соли Мора допускается устанавливать по стандартному образцу, близкому по составу к анализируемым пробам. Стандартный образец проводят через ход анализа, как указано в пп. 3.1 и 3.2.
Массовую концентрацию (С) раствора соли Мора по оксиду хрома (III) в граммах на кубический сантиметр вычисляют по формуле
А т1
1— V% 100 1
где А — аттестованное значение массовой доли оксида хрома ап) в стандартном образце, %;
Ш\ — масса навески высушенного стандартного образца, г;
V2 — объем раствора соли Мора, израсходованный на титрование, с учетом значения контрольного опыта, см3.
Натрий щавелевокислый по ГОСТ 5839, перекристаллизован-ный и высушенный при 105—110°С до постоянной массы
Калий марганцовокислый по ГОСТ 20490, раствор с молярной концентрацией эквивалента с(У5КМп04) = 0J моль/дм3: 32 г марганцовокислого калия растворяют в 1000 см3 воды, перелива-
10
ГОСТ 15848.1-90 С. 4
ют в бутыль из темного стекла вместимостью 10 дм3, приливают 9 дм3 воды, перемешивают и оставляют на 7—10 сут. Раствор переливают, пользуясь сифоном, не доходящим до дна бутыли на 15 мм, в другую бутыль из темного стекла. Вместо сифонирования можно применять фильтрование через прокаленный асбест.
Для установления массовой концентрации марганцовокислого калия 0,2 г щавелевокислого натрия помещают в коническую колбу вместимостью 250 см3 и растворяют при слабом нагревании в 75 см3 воды, затем приливают 15 см3 серной кислоты (1:1), нагревают до 70—80 °С и титруют раствором марганцовокислого калия до появления розовой окраски, устойчивой в течение 1—2 мин.
Массовую концентрацию раствора марганцовокислого калия (С) по оксиду хрома (III) в граммах на кубический сантиметр вычисляют по формуле
п_ /»а 0,3781 V» ’
где т2>—масса навески щавелевокислого натрия, г;
0,3781—коэффициент пересчета щавелевокислого натрия на оксид хрома (III);
Уз — объем раствора марганцовокислого калия, израсходованный на титрование, с учетом значения контрольного опыта, см3.
Для установления соотношения между растворами марганцовокислого калия и соли Мора в коническую колбу вместимостью 250 см3 приливают 20 см3 раствора соли Мора с молярной концентрацией эквивалента 0,1 моль/дм3, 50—60 см3 воды и титруют раствором марганцовокислого калия с молярной концентрацией эквивалента 0,1 моль/дм3 до появления слабо-розовой окраски, устойчивой в течение 1—2 мин.
Коэффициент, определяющий соотношение между объемом раствора марганцовокислого калия, израсходованного на титрование, и объемом раствора соли Мора, взятого на титрование (К), вычисляют по формуле
где У4— объем раствора марганцовокислого калия с молярной концентрацией эквивалента 0,1 моль/дм3 израсходованный на титрование, с учетом значения контрольного опыта,
см3;
V$ — объем раствора соли Мора, взятый для титрования, см3.
11
3. ПРОВЕДЕНИЕ АНАЛИЗА
3 1 Обратное титрование избытка соли Мора раствором марганцовокислого калия
311 Разложение навески в смеси серной и фосфорной кислот
0,2 г хромовой р>ды или концентрата помещают в колбу вместимостью 500 см , смачивают водой, приливают 10 см* фосфорной кислоты, перемешивают, приливают 20 см3 серной кислоты, вновь перемешивают и нагревают до разложения навески, периодически перемешивая содержимое колбы Затем раствор охлаждают, приливают 300—500 см3 воды и перемешивают. К полученному раствору приливают 5 см3 раствора сернокислого марганца, 10 см5 раствора азотнокислого серебра или 10 см3 раствора кобальто-никелевого катализатора, 50 см* раствора надсернокислого аммония и нагревают до появления малиновой окраски, что указывает на полное окисление хрома. Раствор кипятят до прекращения выделения пузырьков кислорода, приливают 10 см3 раствора хлористого натрия и снова кипятят до исчезновения малиновой окраски.
Раствор охлаждают, приливают раствор соли Мора до перехода окраски из желтой в зеленую и в избыток 5—6 см3. Избыток соли Мора оттитровывают раствором марганцовокислого калия до появления розовой окраски устойчивой в течение 1—2 мин.
3.1.2. Разложение навески сплавлением с пероксидом натрия
0,2 г хромовой руды или концентрата помещают в железный тигель и насыпают 3—4 г пероксида натрия Содержимое тигля перемешивают, насыпают еще 1—2 г пероксида натрия и сплавляют при 700—750°С до получения однородного плава Тигель охлаждают, помещают в стакан вместимостью 600 см3 и выщелачивают плав 100—150 см" воды; тигель вынимают и обмывают водой К содержимому стакана приливают серную кислоту (1:1) до растворения осадка гидроксидов. При наличии на дне стакана окалины раствор фильтруют через вату в колбу вместимостью 500 см3. Вату промывают 5—6 раз серной кислотой (1 • 100). К раствору приливают 30 см3 серной кислоты (1:1), 5 см3 фосфорной кислоты и кипятят 20—25 мин для разрушения основной массы пероксида водорода. Раствор охлаждают, приливают 5 см3 раствора сернокислого марганца и анализ ведут, как указано в п. 3.1 1.
3 2 Прямое титрование шестивалентного хрома раствором соли Мора (для руд и концентратов, содержащих менее 0,05 % ванадия)
12
ГОСТ 15848.1-90 С. 6
3.2.1. При разложении навески пробы в смеси серной и фосфорной кислот анализ проводят, как указано в п. 3.1.1. После этого раствор охлаждают, приливают 25 см3 серной кислоты (1 : 1), перемешивают и вновь охлаждают, приливают 5—6 капель фенилантраниловой кислоты и титруют раствором соли Мора до перехода вишневой окраски раствора в зеленую.
При потенциометрической индикации конечной точки титрования (к. т. т.) после приливания 25 см3 серной кислоты (1:1) раствор перемешивают и охлаждают. В колбу опускают соответствующую пару электродов и титруют раствором соли Мора до максимального скачка потенциалов при перемешивании анализируемого раствора на магнитной мешалке,
3.2.2. При сплавлении навески с пероксидом натрия анализ проводят, как указано в п. 3.1.2. После чего раствор охлаждают, приливают 25 см3 серной кислоты (1:1), перемешивают и вновь охлаждают, приливают 5—6 капель фенилантраниловой кислоты и титруют раствором соли Мора до перехода вишневой окраски раствора в зеленую.
Допускается потенциометрическая индикация конечной точки титрования (к. т. т.), как указано в п. 3. 2. L
4. ОБРАБОТКА РЕЗУЛЬТАТОВ
в процен-
4.1. Массовую долю оксида хрома (III) (ХСг2о, тах в рудах и концентратах вычисляют по формуле
(У-К—Ve)'G-100
т
тде V — объем раствора соли Мора, взятый для анализа, см3;
К — соотношение между объемами растворов марганцовокислого калия и соли Мора;
V& — объем раствора марганцовокислого калия, израсходованный на титрование избытка раствора соли Мора, см3; С — массовая концентрация раствора марганцовокислого калия по оксиду хрома (Ш), г/см3; т — масса навески высушенной руды или концентрата, г .
4.2. Массовую долю оксида хрома (III) (ХСг о, ) в процентах ъ рудах и концентратах, содержащих до 0,05 % ванадия, вычисляют по формуле
У __ У7 Сг 100
згде V7 — объем раствора соли Мора, израсходованный на титрование, с учетом величины контрольного опыта, см3;
Ci — массовая концентрация раствора соли Мора по оксиду хрома (III), г/см3.
13
С 7 ГОСТ 15845.1- 90
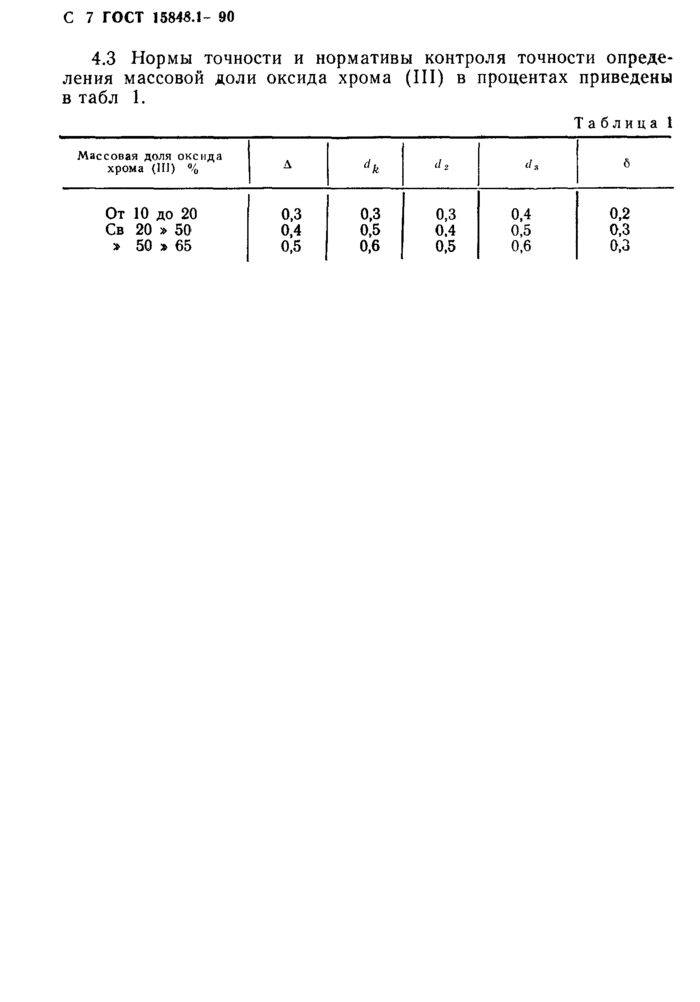
4.3 Нормы точности и нормативы контроля точности опреде* ления массовой доли оксида хрома (III) в процентах приведены в табл 1.
|
Таблица 1 | ||||||||||||||||||||||||
|
ГОСТ 15848Л—90 С. 8
ПРИЛОЖЕНИЕ
РУДЫ ХРОМОВЫЕ И КОНЦЕНТРАТЫ Определение содержания хрома. Титриметрический метод (ИСО 6331—83)
1. Область применения
Настоящий международный стандарт включает титриметрический метод определения хрома в хромовых рудах и концентратах, содержащих более 7% (ш/ш) хрома.
Настоящий стандарт следует применять вместе с ГОСТ 15348.0 (ИСО 6629).
2. Ссылка
ГОСТ 15848.0 (ИСО 6629). Хромовые руды и концентраты. Методы химического анализа. Обшие требования
3. Сущность метода
Сплавление навески материала с пероксидам натрия. Выщелачивание плава водой, подкисление серной кислотой и удаление избытка пероксида водэрода кипячением.
Окисление ионов хрома (III) до хромат-ионов пероксидисульфатом аммония в присутствии нитрата серебра в качестве катализатора.
Титрование храма (VI) раствором сульфата железа (II) аммония, конечную точку находят тли визуально, добавлением избытка сульфата железа (II) аммония и обратным титрованием, или прямым потенциометрическим титрованием
4. Реактивы
4.1. Пероксид натрия.
4.2 Серная кислота* q = 1,84 г/ом3.
4 3 Серная кислота, разбазленная 1:1.
4.4. Серная кислота, разбавленная I : 4
4.5 Ортофосфорная кислота, q = 170 г/см3.
4.6 Сульфат марганца (И), раствор 109 г/дм3
Растворяют 103 г сернокислого марганца (MnS04-7H20) в 1 дм3 воды.
4.7. Сульфат марганца (II), раствор 1 г/дм3 Смешивают 10 см3 раствора сульфата марганца (п. 4 6) с 1 дм3 воды,
4 8 Нитрат серебра, раствор 1 г/дм3.
Для обеспечения большей стабильности раствора нитрата серебра добавляют по 0,5 см3 азотной кислоты на каждый 1 дм3 раствора.
Хранят раствор в сосуде из темного стекла.
4.9. Пер оксид р сульфат аммония, раствор 200 г/дм3. Готсвят раствэр непосредственно перед употреблением.
4.19. Хлористый натрий, ра:твор 53 г/дм3. Растворяют 50 г хлористого натрия (NaCl) в 1 дм3 воды.
4.11 Перманганат калия, стандартный титрованный раствор (1/5 КМп04)« «0,1 моль/дм3.
4111 Приготовление раствора
Растворяют 32 г перманганата калия в 1000 см3 воды, переносят раствор в бутыль из темного стекла вместимостью 10 дм3, добавляют 9 дм3 воды, перемешивают и оставляют стоять 7—10 дней.
15
Пользуясь сифоном, переливают раствор в другую бутыль из темного стекла (тр>оку сифона вставляют в бутыль так, чтобы конец трубки находился на расстоянии 15 см от дна бутыли)
4.11.2. Установка титра раствора
Помещают 0,2 г безводного оксалата натрия, предварительно высушенного при 105—110°С, в коническую колбу вместимостью 250 см3, добавляют 75 см3 воды и растворяют при нагревании Добавляют 15 см3 раствора серной кислоты (п 4 3) и нагревают до 70— 80°С. Титруют раствором перманганата калия (п 4 П 1) до розовой окраски, не исчезающей в течение 1—2 мин.
Титр (Т) раствора перманганата калия, выраженный в граммах железа* рассчитывают по формуле
т- 0,2587
т=~гг— ,
где m — масса навески оксалата натрия, г;
V — объем раствора перманганата калия, израсходованный на титрование,
см3;
0,215137 — фактор пересчета оксалата натрия на хром.
4.12 Сульфат железа (II) аммония, стандартный титрованный раствор c(NH4)2Fe(S04)2 • 6Н2О^0,1 моль/дм3*
4.12.1. Приготовление раствора
Растворяют 39,5 г сульфата железа (II) аммония в 200 см3 раствора серкой кислоты (п 4 4), отфильтровывают раствор в мерную колбу вместимостью 1000 см3, доливают водой до метки и перемешивают.
412 2. Установка титра
Помещают 0„2 г бихромата калия, перекри ста л лизо ванного и высушенного при 18Э—20D°С до постоянной массы, в стакан вместимостью 600 ом3, растворяют в 200 см3 воды, добавляют 50 сад* раствора серной кислоты (п. 4.4), перемешивают и охлаждают Помещают электроды (п 5 11) в стакан и титруют раствором сульфата железа (И) аммония (п 4 12 1) до максимального отклонения стрелки милливольтметра (п 51 3).
Титр (Т\) раствора сульфата железа (II) аммония в г/см3 рассчитывают по формуле
пт * 3535
у ,
где m — масса бихромата калия, г,
V — объем раствора сульфата железа (II) аммония, израсходованный на титре ва н не;, ом3;
0,3535 — фактор пересчета бихромата калия на хром.
Титр раствора сульфата железа (II) аммония изменяется и должен контролироваться в каждой серии определений.
4123 Расчет соотношения между растворами сульфата железа (II) аммония и перманганата калия
Отбирают пипеткой или с помощью бюретки 29 см3 раствора сульфата железа (II) аммония в раствор контрольного опыта, предварительно оттитрованного раствором перманганата калия (п 4 11)) Затем добавляют 50—60 см3 воды и титруют снова раствором перманганата калия (и. 4.11) до появления розовой окраски, не исчезающей в течение 1 — 2 мин
где У —объем раствора перманганата калия, израсходованный на титрование,
V\ — объем раствора сульфата железа (II) аммония, взятый для титрования, см3.
16
ГОСТ 15848.1-90 С 10
4 13 Нитрит натрия, раствор 10 г/дм3. 4.14. Мочевина.
5. Аппаратура для потенциометрического титрования
5 1. Пара электродоз. индикаторный платиновый электрод и электрод срав нения каломельный или вольфрамовый
5 2 Магнитная мешалка.
5.3. Милливольтметр электронного типа с высоким полным сопротивлением для измерения pH, пригодный для записи отклонений потенциала в точке эквивалентности при титровании по выбранной схеме индикатор/электрод сравнения (п. 5.1).
6. Проведение анализа
6.1. Навеска материала. Для анализа берут 0,с г материала.
6 2 Разложение навески. Помещают навеску материала (п 6 2) в корундовый, никелевый или железный тигель и добавляют 3—4 г пироксида натрия (п. 4 1). Перемешивают содержимое тигля стеклянной палочкой, покрывают слоем пероксида натрия (1.—2 г) и осторожно нагревают при 400— 5С0°С, затем при 8О0-850°С, перемешивая содержимое тигля и поддерживая температуру постоянной до тех пор, пока не будет достигнута гомогенная масса расплава (5—7 мин). Затем тигель охлаждают, помещают в стакан вместимостью 600 см3 и выщелачивают плав 10 0^—150 см3 горячей воды Тигель обмывают водой Если частицы плава пристали к стенкам тигля, добавляют 7—3 капель раствора серной кислоты (п. 4 3) и 2—3 см3 воды. После полного растворения частиц плава соединяют полученный таким образом раствор с основным раствором и снова обмывают тигель водой.
Добавляют раствор серной кислоты (п. 4.3) до полного растворения осадка гидроксидов, разбавляют раствор водой до С00 —353 см3, добавляют 10 см3 серной кислоты (п. 4 2), 5 см3 ортофосфорной кислоты (п. 4 5) и кипятят в течение 20 —25 мин для разложения основной массы пероксида водорода.
Фильтруют раствор для отделения нерастворимого осадка через неплотный фильтр или лавсановую вату, собирая фильтрат в стакан вместимостью 800 см3. Промывают фильтр с осадком 6—8 раз горячей водой и отбрасывают его.
Дсбавляют 10 см3 раствора тнтрата серебра (п 4 8) п 1 см3 раствора сульфата марганца (И) (п. 4.7) в том случае, если руда содержит менее 0,1 % по массе марганца. Добавляют 25 ом3 раствора пероксид?сульфата аммония (п. 4.9) и нагревают раствор до появления малиновой окраски, что указывает на полноту окисления хрома Кипятят раствор в течение 12—15 мин для разрушения перик-сидисульфата аммония, добавляют 10 см3 раствора хлористого натрия (п 4.10) и снова кипятят 8— 10 мин для разрушения марганцевой кислоты и коагуляции осадка хлористого серебра. Добавляют 2 см3 раствора сернокислого марганца (п 4 7) и кипятят только 3 мин
Если розовая окраска появляется, продолжают анализ, как указано выше начиная со слов: «Китятят раствор в течение 12 — 15 миш>
6 3. Определение
6 3 1 Титрование с визуальным фиксированием точек эквивалентности Добавляют раствор сульфата железа (II) аммония (п 4 12) из бюретки в стакан, содержащий испытуемый раствор, до тех пор, пока цвет раствора не перейдет из желтого в зеленый (хром (VI) и ванадий (V) восстанавливаются до хрома (III) и ванадия (IV) Добавляют из бюретки еще 5—10 см3 раствора сульфата железа (II) аммония в избыток Титруют раствором перманганата калия (п 4.11) до розэвой окраски не исчезающей в течение 1—2 мин
Примечание. Одновременно перманганатом калия титруется ванадий (IV). Поэтому объем раствора сульфата железа (II) аммония соответствует только содержанию хрома.
I?