Методы определения микроколичеств пестицидов в продуктах питания, фураже, почве и воде (фосфорорганические и другие пестициды). Часть II
Купить бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Оглавление
Хлорофос
Хроматополярографическое определение хлорофоса в растениях
Принцип метода
Реактивы и посуда
Ход анализа
Определение метафоса и тиофоса в продуктах питания растительного происхождения
Принцип метода
Реактивы и растворы
Приборы и посуда
Описание определения
Определение карбофоса, метилмеркаптофоса, препарата М-81 и тиофоса в продуктах питания растительного происхождения
Принцип метода
Реактивы и растворы
Аппаратура и посуда
Ход анализа
Определение в вине и виноградном соке
Севин
Хроматографический качественный и колориметрический количественный методы определения севина в плодах
Принцип метода
Реактивы и растворы
Приборы и посуда
Ход анализа
Хроматографическое определение
Колориметрическое определение
Колориметрический метод определения севина в яблоках, сливах, вишнях, крыжовнике, землянике, черной смородине и плодово-ягодных консервах
Принцип метода
Реактивы и растворы
Приборы и посуда
Ход анализа
Построение калибровочного графика
Определение севина в фруктово-ягодных компотах и маринадах
Колориметрическое определение тетраметилтиурамдисульфида (ТМТД) в зернопродуктах
Принцип метода
Определение ТМТД в зернопродуктах
Реактивы и растворы
Приборы и посуда
Ход анализа
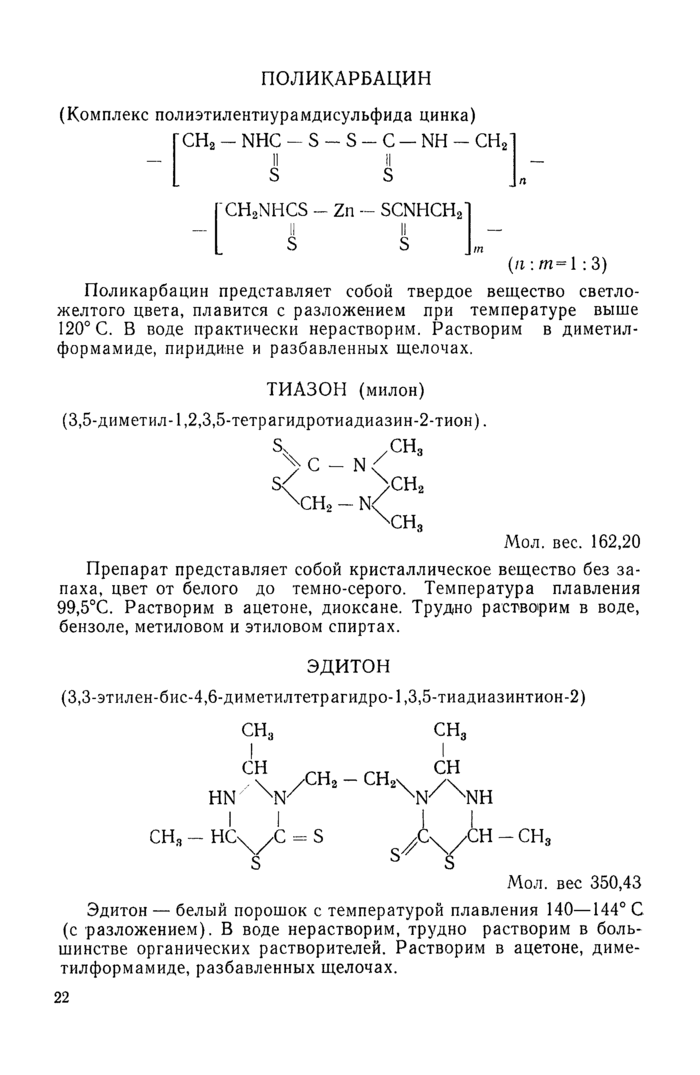
Колориметрический метод определения цирама, цинеба, поликарбацина, тиазона (милона) и эдитона в продуктах питания растительного происхождения и биосредах
Принцип метода
Реактивы и растворы
Приборы и посуда
Описание определения
Колориметрический метод определения диносеба в луке
Принцип метода
Реактивы и растворы
Приборы и посуда
Ход анализа
Полярографическое определение динитроортокрезола в почве
Принцип метода
Реактивы
Приборы и посуда
Ход анализа
Построение калибровочного графика
Приложение 1. Предельно допустимые остаточные количества ядохимикатов в продуктах питания
Приложение 2. Временные предельно допустимые остаточные количества пестицидов в кормах для сельскохозяйственных животных (в мг/кг)
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
Организации:
| 23.08.1967 | Утвержден | Заместитель главного санитарного врача СССР | |
|---|---|---|---|
| Разработан | Украинский научно-исследовательский институт защиты растений | ||
| Издан | Издательство Колос | 1968 г. |
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22
стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
ГОСУДАРСТВЕННАЯ КОМИССИЯ ПО ХИМИЧЕСКИМ СРЕДСТВАМ БОРЬБЫ С ВРЕДИТЕЛЯМИ, БОЛЕЗНЯМИ РАСТЕНИИ И СОРНЯКАМИ ПРИ МСХ СССР
МЕТОДЫОПРЕДЕЛЕНИЯ МИКРОКОЛИЧЕСТВ ПЕСТИЦИДОВ В ПРОДУКТАХ ПИТАНИЯ, ФУРАЖЕ, ПОЧВЕ И ВОДЕ
(ФОСФОРОРГАНИЧЕСКИЕ И ДРУГИЕ ПЕСТИЦИДЫ)
Часть II
Москва — 1968
ГОСУДАРСТВЕННАЯ КОМИССИЯ ПО ХИМИЧЕСКИМ СРЕДСТВАМ БОРЬБЫ С ВРЕДИТЕЛЯМИ, БОЛЕЗНЯМИ РАСТЕНИЙ И СОРНЯКАМИ ПРИ МСХ СССР
Утверждаю: Заместитель Главного санитарного врача СССР
Д. Н. ЛОРАНСКИЙ 23 августа 1967 г.
МЕТОДЫОПРЕДЕЛЕНИЯ МИКРОКОЛИЧЕСТВ ПЕСТИЦИДОВ В ПРОДУКТАХ ПИТАНИЯ, ФУРАЖЕ, ПОЧВЕ И ВОДЕ
(ФОСФОРОРГАНИЧЕСКИЕ И ДРУГИЕ ПЕСТИЦИДЫ)
Часть II
ИЗДАТЕЛЬСТВО «КОЛОС»
Москва —1968
водой до нейтральной реакции по лакмусу промывных вод, рассыпают тонким слоем и сушат при комнатной температуре до влажности 15%.
Натрий сернокислый безводный, химически чистый.
Аммоний молибденовокислый 0,02 М раствор в 10 н. серной кислоте. 6,18 г реактива растворяют в 250 мл 10 н. серной кислоты. Раствор рекомендуется хранить в склянке из темного стекла.
Окисляющая смесь. Готовят путем растворения 0,5 г растертого в порошок марганцовокислого калия в 10 мл серной кислоты, уд. вес Г,84. Реактив хранят в склянке с притертой пробкой. Срок годности реактива 5 дней.
Гидразин сернокислый, 0,13%-ный раствор.
Калий фосфорнокислый однозамещенный, стандартный раствор, содержащий 0,001 мг фосфора в 1 мл. Готовят следующим образом; 0,2742 г однозамещенного фосфорнокислого калия растворяют в 250 мл дистиллированной воды, подкисленной несколькими каплями серной кислоты. Раствор годен в течение 2—3 недель. 1 мл его вносят в мерную колбу на 250 мл и доливают слегка подкисленной водой до метки. Раствор готовят непосредственно перед употреблением. 1 мл его содержит 0,991 мг фосфора.
Аппаратура и посуда
Установка для хроматографирования. Перед хроматографированием колонку (стеклянная трубка, зауженная книзу, 200x20 мм) заполняют адсорбентом. Для этого в узкий конец помещают небольшой ватный тампон и сверху наливают взвесь адсорбента в органическом растворителе в таком количестве, чтобы после оседания высота слоя его была 5 см. На слой адсорбента насыпают слой безводного сернокислого натрия.
Прибор для отгонки растворителя с пришлифованными колбами из термостойкого стекла на 100 мл и 15—20 мл.
Пробирки колориметрические.
Широкогорлые склянки с притертыми пробками.
Делительные воронки на 300—500 мл.
Пипетки, мерные колбы на 250 мл, мерный цилиндр на 100 мл.
Водоструйный насос или аспиратор.
Баня парафиновая.
Электроплитка.
Термометр на 200° С.
Трубки резиновые, зажимы.
Ход анализа
100 г измельченного на овощной терке продукта переносят в стеклянную банку с притертой пробкой или делительную воронку, добавляют 60—75 мл растворителя и энергично встряхивают в течение 25—30 минут. Экстракт сливают в колбу на 100—150 мл.
10
К исследуемой пробе продукта вновь прибавляют 20—25 мл рас-творителя и продолжают экстракцию еще 10—15 минут. Экстракты объединяют и хроматографируют через слой адсорбента и безводного сернокислого натрия, предварительно смоченные растворителем. При хроматографии фосфатиды растения задерживаются адсорбентом, инсектицид остается в элюате.
В таблице приведены растворители и адсорбенты, соответствующие определенным ядохимикатам.
|
Препарат |
Растворитель |
Адсорбент |
|
Карбофос |
Хлороформ |
Окись алюминия |
|
Метилмеркаптофос |
Хлороформ |
Окись алюминия |
|
Препарат М-81 |
Хлороформ |
Диатомит |
|
Тиофос |
Хлороформ |
Окись алюминия, обработанная 2 н, соляной кислотой |
После хроматографирования колонку промывают 15 мл растворителя. Фильтрат переносят в колбу перегонного аппарата на 100 мл и отгоняют на водяной бане растворитель до объема 10—15 мл. Оставшийся раствор количественно переносят в колбочку на 15—20 мл и испаряют досуха под небольшим разряжением водоструйного насоса. К сухому остатку добавляют 2,5 мл концентрированной азотной кислоты, 0,1 мл окисляющей смеси. Колбочку осторожно встряхивают и помещают в парафиновую баню, нагретую до температуры не выше 65—70°. Температуру бани медленно поднимают до 175—180° С 1.
Исследуемый раствор нагревают до полного удаления паров азотной кислоты. После этого на электроплитке выпаривают оставшийся раствор досуха. Далее после охлаждения колбочки к сухому остатку прибавляют дистиллированную воду и раствор количественно переводят в колориметрическую пробирку, затратив на эту операцию 6—7 мл воды. Туда же вносят 1 мл 0,002 М раствора молибдата аммония. Пробирку встряхивают и нагревают на кипящей водяной бане в течение 10 минут. После охлаждения к раствору прибавляют 1,6 мл 13%-ного раствора сернокислого гидразина и доводят объем жидкости дистиллированной водой до 10 мл.
Пробирку вновь энергично встряхивают, нагревают на кипящей водяной бане 15 минут, охлаждают и сравнивают окраску исследуемого раствора с окраской растворов стандартной шкалы.
Стандартную шкалу готовят параллельно с пробой. Для приготовления ее в ряд колориметрических пробирок вносят 0; 1; 1,5... 5 мл стандартного раствора однозамещенного фосфорнокислого калия, что соответствует 0; 0,001; 0,0015 ... 0,005 мг фосфора. Объем жидкости во всех пробирках дистиллированной водой доводят до 7 мл, затем в пробирки со стандартными растворами вносят по 1 мл раствора молибдата аммония, пробирки встряхивают и помещают в кипящую водяную баню на 10 минут. После охлаждения растворов в каждую пробирку вносят 1,6 мл раствора сернокислого гидразина, дистиллированной водой объем жидкости доводят до 10 мл, пробирки энергично встряхивают и вновь помещают на 15 минут в кипящую водяную баню. По полученной серии стандартов строят калибровочный график, применяя при измерении величины светопоглощения красный светофильтр.
Количество препарата в мг/кг продукта вычисляют по формуле:
где
G — количество фосфора, найденное в пробе, мкг;
Р — навеска продукта, взятая для анализа, г;
10,64
7,43
7,94
9,39
К— коэффициент пересчета фосфора на исследуемый препарат. Значения К приведены в таблице.
Карбофос . . . , Метилмеркаптофос Препарат М-81 . , Тиофос.....
Определение в вине и виноградном соке
|
СЕВИН |
50 мл вина или виноградного сока помещают в склянку с притертой пробкой или делительную воронку емкостью 200—300 мл, прибавляют 50 мл серного эфира и энергично встряхивают в течение 10—15 минут. Эфирный экстракт с целью удаления влаги фильтруют через слой сернокислого натрия. Фильтрат собирают в колбочку перегонного аппарата и отгоняют растворитель. Дальнейший ход анализа и расчет аналогичны описанным выше, т. е. к сухому остатку прибавляют 2,5 мл азотной кислоты и 0,1 мл окисляющей смеси и т. д.
Ч/\^
(1-нафтил-Ы-метилкарбамат)
Мол. вес 201,2
12
Химически чистый севин — кристаллическое вещество белого цвета со слабым запахом. Устойчив на свету при повышенных температурах (до 70°) и хранении. В щелочных растворах быстро гидролизуется. В воде нерастворим, растворим в большинстве органических растворителей.
ХРОМАТОГРАФИЧЕСКИЙ КАЧЕСТВЕННЫЙ И КОЛОРИМЕТРИЧЕСКИЙ КОЛИЧЕСТВЕННЫЙ МЕТОДЫ ОПРЕДЕЛЕНИЯ СЕВИНА В ПЛОДАХ
Принцип метода 2
Основан на экстракции севина петролейным эфиром или другим органическим растворителем, очистке экстракта от мешающих определению примесей, омылении раствором едкого натра до 1-нафтола и сочетании последнего в щелочной или кислой среде с диазотированным п-нитроанилином, в результате чего получается азосоединение синего цвета.
Чувствительность хроматографического метода меньше 1 мкг, а колориметрического — 0,03—0,1 мг/кг.
Реактивы и растворы
Эфир петролейный, точка кипения 40—90°, перегнанный (или бензол х. ч.).
Метанол х. ч.
Натрий хлористый х. ч.
Бензол перегнанный.
Бумага для хроматографии.
Ацетон х. ч.
Натрий едкий х. ч.
Спирт н-бутиловый х. ч.
п-Нитрофенилдиазоний солянокислый свежеприготовленный. К 0,02%-ному раствору п-нитроанилина в 0,1 н. соляной кислоте доливают в 10 раз меньшее количество 0,8%-ного раствора нитрата натрия. Раствор готовят в колбочке, погруженной в ледяную воду.
Стандартный раствор севина. 100 мг севина, х. ч., растворяют в мерной колбе в 100 мл петролейного эфира или бензола. 1 мл этого раствора переносят в мерную колбу емкостью 100 мл и доводят до метки тем же растворителем. 1 мл раствора содержит 10 мкг севина.
Приборы и посуда
Сосуд для хроматографирования на бумаге.
Колбы круглодонные на 100—150 мл с пришлифованными нисходящими холодильниками.
Воронки делительные на 250 мл.
Пипетки емкостью 0,1 мл.
Колориметр.
Пульверизатор стеклянный.
Ход анализа
Навеску в 100 г (из средней пробы в 1 кг) заливают петролей-ным эфиром или бензолом. Через 24 часа эфир сливают и плоды ополаскивают тем же растворителем.
Экстракт отгоняют почти досуха на водяной бане. Остаток в колбе растворяют в 20 мл метанола, раствор переносят в делительную воронку емкостью 250 мл и к нему добавляют 30 мл дистиллированной воды. При этом выпадают воск и красящие вещества, которые удаляют взбалтыванием с 10 мл петролейного эфира в течение 2—3 минут. Взбалтывание проводят 3 раза общим количеством 30 мл петролейного эфира. Чтобы избежать образование эмульсии, в делительную воронку всыпают 2—3 г хлористого натрия. Затем воднометаноловый раствор трижды взбалтывают с 200 мл бензола: первый раз со 100 мл, а во второй и третий — с 50 мл. Севин переходит в бензол. Замеряют объем бензольного экстракта, сушат его безводным сернокислым натрием и используют для хроматографического или колориметрического определения.
Хроматографическое определение
7з бензольного экстракта упаривают на водяной бане до объема 0,3—0,5 мл и остаток в количестве 0,1 мл переносят пипеткой на полосу хроматографической бумаги в определенную точку. Затем колбу дважды промывают 0,2—0,4 мл бензола, который также наносят в ту же точку бумаги. Диаметр пятен на бумаге не должен превышать 1 см.
Исследуемые растворы наносят на бумагу в точки, находящиеся на расстоянии 3 см от нижнего края и 2,5 см от боковых краев. Между собой точки нанесения должны быть на расстоянии 3 см друг от друга. Затем полосу бумаги погружают в сосуд для хроматографирования в подвижный растворитель (80% дистиллированной воды и 20% ацетона) на глубину 1,2 см от нижнего края, п жидкости дают подняться на высоту 15—16 см, на что уходит приблизительно 2 часа. Затем бумагу из сосуда вынимают и растворитель испаряют на воздухе, после чего его опрыскивают 1,5%-ным раствором едкого натра в смеси метилового и н-бутило-
14
вого спиртов (1:1), в результате чего севин омыляется до 1-нафтола.
Хроматограммы проявляют после испарения спирта путем опрыскивания бумаги смесью 0,1%-ного раствора п-нитроанилина в 0,1 н. соляной кислоте с 4%-ным водным раствором нитрата натрия. Смесь указанных растворов готовят в отношении 10 : 1 в колбочке, помещенной в ледяную воду. В результате опрыскивания бумаги раствором хлористоводородной соли п-нитрофеиилдиазония происходит сочетание с 1-нафтолом и появляются синие пятна в тех местах на бумаге, где находился севин.
При анализе чистого препарата пятна получаются в виде синих кружков. Rf для севина при 25° равен приблизительно 0,76, а для 1-нафтола — 0,5.
При анализе севина из растительной ткани или плодов получают синие полосы, идущие снизу вверх по длине полосы бумаги.
Колориметрическое определение
Полученный, как описано выше, бензольный экстракт упаривают на водяной бане и остаток растворяют в 5 мл метанола, К этому раствору доливают 1 мл 2%-ного водного раствора едкого натрия для омыления севина до 1-нафтола и охлаждают раствор ледяной водой.
В колбе, которая находится в ледяной воде, готовят раствор паранитрофенилдиазония: к определенному количеству миллилитров 0,02%-ного раствора п-нитроанилина в 0,1 н. соляной кислоте добавляют в 10 раз меньшее количество 0,08%-ного раствора нитрата натрия. К охлажденному в ледяной воде омыленному раствору севина прибавляют 1 мл свежеприготовленного раствора солянокислого паранитрофенилдиазония. В результате сочетания паранитрофенилдиазония с 1 -нафтолом получается азосоединение синего цвета. В колбу вливают еще 5 мл метанола и оставляют на 2 часа в холодильнике до полного проявления окраски.
Параллельно с пробой строят калибровочный график. С этой целью к экстрактам контрольного образца, соответствующим 100 г определяемого продукта, прибавляют 0,25; 0,5; 1,5 мл стандартного раствора севина, что соответствует 2,5, 5,0, 10, 15 мкг севина, и проводят колориметрическое определение так, как описано ниже. Колориметрирование проводят с оранжевым светофильтром.
Количество севина в мг/кг вычисляют по формуле:
P-Vi
где
G — количество севина, найденное по калибровочному графику, мкг;
Р — навеска продукта, г;
15
Ki — объем бензольного экстракта, взятый для колориметрического определения, мл;
V — общий объем бензольного экстракта, мл.
КОЛОРИМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ СЕВИНА В ЯБЛОКАХ, СЛИВАХ, ВИШНЯХ, КРЫЖОВНИКЕ, ЗЕМЛЯНИКЕ, ЧЕРНОЙ СМОРОДИНЕ
и плодово-ягодных консервах
Принцип метода 3
Севин извлекают из растительных пищевых продуктов хлороформом. От примесей освобождают в метаноловом растворе добавлением водного раствора хлористого аммония с последующим фильтрованием через бумажный фильтр и хроматографированием через слой окиси алюминия.
Выделенный севин гидролизуют едким кали и образующийся 1-нафтол сочетают с хлористым п-нитрофенилдиазонием, в результате чего образуется азосоединение синего цвета, по которому и определяют количество севина в пробе.
Точность метода ± 5—10%.
Реактивы и растворы
Хлороформ X. ч.
Метанол х. ч.
Аммоний хлористый х. ч., 2%-ный водный раствор.
Смесь метанола и 2%-ного водного раствора хлористого аммония (1 : 1).
Алюминия окись для хроматографии II активности.
Натрий сернокислый безводный х. ч.
Калий едкий 0,1 н. раствор в метаноле.
Натрия нитрит х. ч., 0,8%-ный водный раствор.
п-Нитроанилин.
п-Нитрофенил хлористый, свежеприготовленный. К 0,02%-ному раствору п-нитроанилина в 0,1 н. соляной кислоте доливают в 10 раз меньшее количество 0,8%-ного водного раствора нитрита натрия. Раствор готовят в колбе, погруженной в ледяную воду.
Стандартный раствор севина: 10 мг севина, х. ч., растворяют в 100 мл хлороформа. 10 мл этого раствора переносят в мерную колбу емкостью 100 мл и доводят до метки хлороформом. 1 мл раствора содержит 10 мкг севина.
Приборы и посуда
Фотоэлектроколориметр.
Водяная баня.
Водоструйный насос.
Установка для хроматографирования, состоящая из колонки (стеклянная трубка, зауженная книзу, 17X400 мм) и колбы Бунзена. В колонку помещают ватный тампон, затем слой окиси алюминия 5—7 см и затем слой безводного сульфата натрия 1,5—2 см. Подготовленную колонку промывают хлороформом (10—15 мл).
Центрифуга.
Аппарат для встряхивания.
Воронки делительные емкостью 150—250 мл.
Колбы конические емкостью 50, 100 и 250 мл.
Цилиндры мерные на 25, 50, 250 и 500 мл.
Пипетки на 1, 5 и 10 мл.
Сосуды для экстракции емкостью 1,5—2 л.
Ход анализа
Пробу исследуемого растительного продукта весом 1—1,5 кг измельчают, тщательно перемешивают и навеску 100 г заливают хлороформом и оставляют на 16—18 часов. Полученный экстракт фильтруют через бумажный фильтр в колбу и отгоняют хлороформ при 35—40° С над кипящей водяной баней с помощью водоструйного насоса. Последние порции растворителя отгоняют без нагревания.
Для растворения сухого остатка в колбу приливают 10 мл метанола и осторожно ее подогревают, погружая в горячую воду, слегка потирая дно стеклянной палочкой. Затем добавляют 10 мл 2%-ного раствора хлористого аммония и помещают колбу в холодильник (лучше в замораживатель) на 20—30 минут.
При добавлении водного раствора хлористого аммония растворимость «воска» и пигментов в метаноле резко уменьшается и они выделяются в виде хлопьев. После охлаждения содержимое фильтруют через тройной бумажный фильтр. Фильтрование идет быстрее при использовании водоструйного насоса. Для этого стеклянную воронку с пробкой и плотно прилегающим фильтром (лучше двойным) вставляют в пробирку с отводом, который подключают к водоструйному насосу.
Содержимое колбы количественно переносят в воронку, споласкивая колбу дважды (по 3—5 мл) смесью метанола и 2%-ного раствора хлористого аммония (1 : 1), охлажденной до 0—5° С.
Фильтрат из пробирки переносят в делительную воронку и экстрагируют севин хлороформом, энергично встряхивая первый раз с 25 мл, второй — с 15 мл. Хлороформенный экстракт хроматографируют через колонку. Сначала пропускают первую порцию
17
экстракта 25 мл, затем вторую— 15 мл и промывают 15 мл хлороформа.
Полученный фильтрат количественно переносят в колбу и отгоняют хлороформ досуха, используя водоструйный насос. К сухому остатку прибавляют 5 мл 0,1 н. метанолового раствора едкого кали и, помешивая стеклянной палочкой, оставляют на 5 минут.
Полученный в результате гидролиза севина 1-нафтол определяют следующим образом.
В колбу, где протекал гидролиз севина, добавляют 1 мл солянокислого раствора п-нитрофенилдиазония, приготовленного перед употреблением, как указано в разделе «Реактивы и растворы». При взаимодействии в щелочной среде 1-нафтола и солянокислого п-нитрофенилдиазония образуется азосоединение синего цвета. В колбу доливают еще 5 мл метанола и помещают в холодильник на 30 минут. Затем раствор фильтруют через бумажный фильтр и колориметрируют при оранжевом светофильтре (длина волны 590 ммк) в кювете с толщиной слоя 10 мм.
В качестве холостой пробы при колориметрировании используется дистиллированная вода.
Расчет содержания севина производят по предварительно построенному калибровочному графику.
Построение калибровочного графика
Для построения калибровочного графика в колбы вносят 0,5; 1; 2,5; 5; 7,5; 10 мл стандартного раствора, содержащего 10 мкг севина в 1 мл хлороформа. Растворитель отгоняют на водяной бане с помощью водоструйного насоса и далее поступают, как описано для определения севина в растительной пробе с момента щелочного гидролиза.
Содержание севина в мг/кг продукта вычисляют по следующей формуле;
где
X — количество севина в продукте, мг/кг;
G — количество севина, найденное по калибровочному графику, мкг;
Р — навеска исследуемого продукта, г.
Определение севина в фруктово-ягодных компотах и маринадах
100 г исследуемой пробы (учитывать соотношение сиропа и ягод) после измельчения и тщательного перемешивания количественно переносят в колбу с притертой пробкой и заливают хлороформом с таким расчетом, чтобы покрыть навеску. Экстрагируют
18
севин путем встряхивания в течение 30 минут на аппарате для встряхивания. В случае образования стойкой эмульсии для разделения слоев следует воспользоваться центрифугой.
Центрифугирование проводят в течение 30 минут при 2500 об/мин. После центрифугирования удаляют верхний слой (сироп и ягоды) с помощью пипетки Мора и резиновой груши, а нижний, хлороформенный, сушат с помощью безводного сульфата натрия. Высушенный экстракт помещают в колбу для отгона растворителей и удаляют хлороформ на водяной бане с помощью водоструйного насоса. Дальнейший ход анализа аналогичен определению севина в сырых ягодах и фруктах.
КОЛОРИМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ТЕТРАМЕТИЛТИУРАМДИСУЛЬФИДА (ТМТД) В ЗЕРНОПРОДУКТАХ
сн3ч усн3
;nc-s-s-cn4
сн/ || || хсн3
S S
Мол. вес 240,44
Мелкокристаллический порошок желтовато-серого цвета, со специфическим запахом.
Температура плавления 155—156° С.
Практически нерастворим в воде, но растворим в большинстве органических растворителей (слабо—в этиловом спирте, несколько лучше — в эфире, хорошо — в ацетоне, хлороформе). Устойчив при хранении. Но подвергается разложению в кислой и щелочной средах, под действием сильных окислителей разрушается до серной кислоты и углекислого газа.
Принцип метода
Метод основан на образовании комплексного соединения — тиу-рамата меди, окрашенного в салатный цвет, при взаимодействии катиона меди с тетраметилтиурамдисульфидом в спиртовом растворе.
При содержании тетраметилтиурамдисульфида от 5 до 40 мкг в 1 мл раствора окраска подчиняется закону Ламберта — Бера.
Чувствительность метода — 5 мкг в 1 кг анализируемого продукта.
19
Редакционная комиссия:
3. И. Богомолова, Ф. П. Вайнтраубf Ф. Г. Днтловицкая, М. А. Клисенко, Л, А. Стемпковская
Ответственный редактор Е. С. Косматый
ОПРЕДЕЛЕНИЕ ТМТД В ЗЕРНОПРОДУКТАХ
Реактивы и растворы
Спирт этиловый, 96%-ный.
Спиртовый раствор хлорида меди, 1,0%-ный. Тетраметилтиурамдисульфид чистый, перекристаллизованный. 2—5 г ТМТД растворяют в 5 мл хлороформа, добавляют 5 мл этанола при помешивании, образующийся осадок отфильтровывают, промывают спиртом и сушат при 100° С.
Стандартный спиртовый раствор ТМТД, 50 мкг/мл.
Приборы и посуда
Пробирки.
Колбы.
Микропипетки.
Фотоэлектроколориметр ФЭК-56.
Ход анализа4
Исследуемый образец весом 20 г помещают в колбу и заливают равным или двойным количеством этилового спирта, в зависимости от характера объекта, и экстрагируют в течение 30 минут при периодическом встряхивании. Экстракт фильтруют и замеряют объем фильтрата. К 5 мл экстракта добавляют 0,1 мл 1%-ного спиртового раствора хлорида меди, подогревают до 50—60° и фото4 метрируют через 20—30 минут при 440 ммк (синий светофильтр № 4), пользуясь кюветами шириной 10 мм. В качестве контроля используют экстракт, не обработанный хлоридом меди.
Для построения калибровочного графика в ряд пробирок вносят последовательно 0,1; 0,2; 0,3; 0,4; 0,6; 0,8 мл стандартного рас4 твора, что соответствует 5; 10; 15; 20; 30; 40 мкг ТМТД, доводят этиловым спиртом объем жидкости до 5 мл, затем добавляют в каждую пробирку 0,1 мл 1%-ного спиртового раствора хлорида меди, нагревают на водяной бане (50—60°) в течение 20 минут. Далее раствор фотометрируют в кювете с рабочей длиной 10 мм в сравнении с этиловым спиртом, к которому добавлен 0,1 мл 1 %-ного спиртового раствора хлорида меди.
Расчет анализа производят по формуле:
Р ■ Vi
где
X — количество ТМТД в анализируемом продукте, мг/кг;
ХЛОРОФОС (диптерекс) (0,0-диметил-2,2,2-трихлор-1-оксиэтил-фосфонат)
СН3Оч
СНоО/
ЧР-СН-СС13
I
он
Мол. вес 257,45
Белое твердое вещество с точкой плавления 78—80°С, растворяется в воде при 25° до 15,4%, а также в хлороформе, бензоле, н-гек-сане, ацетоне, этиловом спирте и др.
В водных растворах хлорофос наиболее устойчив при pH 1—5. При pH выше 7 он быстро подвергается гидролизу с образованием ДДВФ (0, 0,-диметил-2,2-дихлорвинилфосфат), который при pH S' интенсивно разлагается на продукты, не обладающие токсичностью.
ХРОМАТОПОЛЯРОГРАФИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ХЛОРОФОСА В РАСТЕНИЯХ
Принцип метода 5
Метод определения остатков хлорофоса (ХФ) основан на экстракции его из пробы хлороформом, очистке экстракта от примесей растительного происхождения и продуктов его распада.
Реактивы и посуда
Хлорофос очищенный.
Хлороформ медицинский очищенный. н-Гексан перегнанный.
Этиловый спирт перегнанный.
Стандартный раствор ХФ. Приготовляют ацетоновый раствор «с содержанием ХФ 100 мкг/мл.
ДДВФ стандартный раствор в ацетоне, 100 мкг/мл.
Сернокислый натрий безводный.
Резорцин, 2%-ный раствор.
Карбонат натрия, х. ч. раствор.
Хлорид лития, 0,01 н. раствор.
Тетраметил-аммоний бромистый, 0,01 н. раствор.
Хроматографическая бумага марки «Б» Ленинградской фабрики.
Колбы конические 700 мл с притертой пробкой.
Воронки 0 12—14 см.
Аппарат для встряхивания.
Пульверизатор стеклянный.
Микропипетка на 0,1 мл с ценой деления 0,01 мл.
Камера для хроматографирования.
Электрическая водяная баня.
Полярограф.
Ход анализа
Навеску растения 100 г измельчают на терке или в фарфоровой ступке, переносят в коническую колбу и заливают хлороформом. 'Содержимое колбы встряхивают примерно около 1—1,5 часа на аппарате для встряхивания. Жидкость отделяют фильтрованием, экстракты соединяют и обезвоживают безводным сернокислым натрием. Растворитель отгоняют почти досуха на водяной бане. 'Остаток растворителя удаляют теплым воздухом (60°). Сухой остаток обрабатывают 4—5 раз дистиллированной водой (по 5—6 мл). Водные экстракты соединяют вместе, переносят в делительную воронку и промывают н-гексаном 3—4 раза, для чего последнего берут по 15 мл. Гексановый слой удаляют, а из водного слоя экстрагируют ХФ хлророформом 4—5 раз. Каждый раз хлороформа берут по 30—40 мл.
Хлороформенные экстракты соединяют, и растворитель на водяной бане отгоняют до объема 0,5 мл. Дальше остаток экстракта хроматографируют при комнатной температуре 4—5 часов. Подвижным растворителем служит петролейный эфир (температура кипения до 70°), насыщенный метанолом. На листок хроматографической бумаги, разделенный двумя прорезями на три полоски (7 см шириной и 48 см длиной), наносят параллельно две пробы — юдну для количественного, а другую — для качественного определения ХФ; на третью полоску наносят стандартный раствор ХФ.
После хроматографирования полоски бумаги вынимают из камеры и сушат на воздухе до полного удаления паров подвижного растворителя. Затем по линиям прореза хроматограмму разрезают на три части. Одну из них оставляют для количественного определения ХФ, а вторую и третью проявляют для установления места положения ХФ на хроматограмме.
Проявителем служит смесь — 2%-ный водный раствор резорцина + 1,0 М раствор карбоната натрия. После опрыскивания хроматограмму помещают в сушильный шкаф при температуре 50—55° на 10—15 минут. При этом на хроматограмме пятно Хф окрашивается в розовый цвет.
В этих условиях можно хроматографировать смесь ХФ и ДДВФ. На хроматограмме проявляются два пятна: первое
с /?/=0,14 для ХФ, а второе с /?/=0,76 для ДДВФ.
Для количественного определения остатков ХФ поступают следующим образом.
Пользуясь проявленной хроматограммой, на непроявленной хроматограмме черным карандашом отмечают участок отложения хлорофоса и вырезают его. Отрезанный кусочек бумаги разрезают на мелкие полоски, помещают их в пробирку с этиловым спиртом,, нагревают до 35° на водяной бане и экстрагируют из них ХФ. Экстракт количественно переносят в стаканчик для полярографи-рования, упаривают его досуха, прибавляют в качестве фона 3 мл; 0,01 н. водного раствора тетраметиламмонийбромида или 0,01 н. раствора хлорида лития и полярографируют.
Далее в электролизер прибавляют 0,1 или 0,2 мл стандартного-раствора с известным содержанием ХФ и снова полярографируют. По разности между высотой волны для испытуемого раствора-+ + стандарт и высотой волны испытуемого раствора находят высоту волны для проявленного стандарта.
Полярографирование проводят на полярографе любой маркш с выносным анодом, в качестве которого используют насыщенный каломельный электрод (потенциал его условно принимают за нуль). Анод с электролизером соединяют при помощи агар-агаро-вого ключа, приготовленного на растворе хлористого калия. Кислород из раствора удаляют пропусканием водорода в течение 20 мин. Водород получают электролизом 28—30%-ного раствора едкого-натра.
Измерение ведут при чувствительности гальванометра = или 1 /20- Волна ХФ на фоне 0,01 н. раствора тетраметиламмонийбромида появляется при потенциале 0,72 вольта.
Содержание хлорофоса в мг/кг пробы рассчитывают по формуле:
X__h ■ а
” (Л' — А) ■ Р ’
где
h — высота волны исследуемого раствора, мм;
h' — высота волны исследуемого раствора + стандартный раствор, мм;
а — количество ХФ, прибавленного со стандартным раствором, мкг;
Р — навеска растительной пробы, г.
Определение ХФ в яблоках и картофеле может быть проведено
S
полярографическим методом без предварительного хроматографического выделения его.
При полярографическом определении ХФ его извлекают из растительных проб хлороформом, растворитель отгоняют почти досуха, а следы растворителя удаляют теплым воздухом.
Из сухого остатка ХФ извлекают водным 0,01 н. раствором тет-раметиламмонийбромида или раствором 0,01 н. хлорида лития.
Раствор фильтруют через маленький бумажный фильтр. Фильтрат собирают и полярографируют, как описано выше.
ОПРЕДЕЛЕНИЕ МЕТАФОСА И ТИОФОСА В ПРОДУКТАХ ПИТАНИЯ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ
Принцип метода6
Метод определения метафоса и тиофоса в растительных пище-вых продуктах основан на экстракции препарата серным эфиром; отделении п-нитрофенола, могущего присутствовать в экстракте, путем промывания экстракта водным раствором едкой щелочи; щелочном гидролизе препарата с последующим колориметрическим определением в виде п-нитрофенолята.
Чувствительность определения — 0,05 мг/кг.
Реактивы и растворы
Стандартный раствор п-нитрофенола. 0,02 г п-нитрофенола (х. ч.) растворяют в мерной колбе на 100 мл дистиллированной водой. 10 мл этого раствора переносят в мерную колбу на 100 мл и доводят объем жидкости водой до метки. Стандартный раствор содержит 0,02 мг п-нитрофенола в 1 мл. Готовят его непосредственно перед употреблением.
Пергидроль, 30%-ный, х. ч.
Эфир серный, х. ч.
Натрий едкий, х. ч., 0,5%-«ый и 20%-ный водные растворы.
Натрий сернокислый безводный, х. ч.
Осветляющая смесь. Ее готовят путем смешения 45 г хлористого натрия и 5 г углекислого натрия. Реактивы хорошо перемешивают в ступке.
Приборы и посуда
Прибор для гидролиза — колба емкостью 50 мл с пришлифованным обратным холодильником.
Делительная воронка емкостью 250 мл.
Пробирки колориметрические.
Пипетки, мерные колбы на 100 мл, конические колбы и т. п.
Баня водяная.
Стеклянные фильтры № 1. Трубки резиновые, зажимы. Овощная терка.
Описание определения
150—200 г исследуемого продукта измельчают и экстрагируют в делительной воронке серным эфиром в течение часа.
Эфирную вытяжку отгоняют до объема 50—75 мл и переносят в сухую делительную воронку. Приливают 25 мл 0,5%-ного раствора едкого натра и энергично встряхивают 3—4 минуты. После разделения жидкостей отделяют водный слой и вновь промывают эфирный экстракт 0,5%-ным раствором едкого натра до тех пор, пока щелочной слой не будет бесцветным. К оставшемуся в делительной воронке эфирному раствору прибавляют 7—10 г безводного сернокислого натрия, несколько раз встряхивают и оставляют на 5—10 минут. После этого количественно переносят эфирный раствор в колбу прибора для гидролиза и медленно испаряют эфир на водяной бане досуха. К сухому остатку прибавляют 4—5 мл пергидроля, присоединяют колбу к холодильнику и кипятят до тех пор, пока жидкость в колбе не обесцветится. Колбу охлаждают, вносят по каплям 2 мл 20%-ного раствора едкого натра и осторожно нагревают с обратным холодильником 20 минут. В присутствии тиофоса (метафоса) раствор окрашивается в желтый цвет. После охлаждения вносят осветляющую смесь в таком количестве, чтобы она выпала в осадок. Жидкость несколько раз встряхивают и фильтруют через стеклянный фильтр № 1 в колориметрическую пробирку. Фильтрат промывают дистиллированной водой, доводят объем фильтрата до 10 мл. Через 20 минут сравнивают интенсивность окраски со стандартными растворами.
Стандартную шкалу готовят параллельно с пробой.
В ряд колориметрических пробирок вносят 0; 0,1; 0,2; 0,3; 1 мл стандартного раствора п-нитрофенола. Объем жидкости во всех пробирках доводят до 8 мл, прибавляют по 2 мл 20%-ного раствора едкого натра и оставляют на 20 минут. Шкала устойчива в течение 3—5 дней.
Можно пользоваться фотоколориметром любой системы. В этом случае по полученной серии стандартов строят калибровочный график, используя для измерений синий светофильтр.
Расчет анализа проводят по формуле:
V G • К
где
X — содержание тиофоса или метафоса в анализируемой пробе, мг/кг;
7
G — количество п-нитрофенола, найденное по стандартной шкале или калибровочному графику;
К — коэффициент пересчета п-нитрофенола, равный для мета-фоса 1,89 и для тиофоса 2,09;
Р — навеска пробы, г.
ОПРЕДЕЛЕНИЕ КАРБОФОСА, МЕТИЛМЕРКАПТОФОСА, ПРЕПАРАТА М-81 И ТИОФОСА В ПРОДУКТАХ ПИТАНИЯ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ
КАРБОФОС (малатион)
(1,2-дикарбэтоксиэтилдиметилдитиофосфат).
СН30
> Р - S — СН-СООС2Н6 СН3Сг I Мол. вес 330,37
СН2СООС2Н8
Химически чистый дикарбэтоксиэтилдиметилдитиофосфат представляет собой маслянистую бесцветную жидкость со слабым неприятным запахом. Хорошо растворяется в органических растворителях, в воде нерастворим. Выпускаемый промышленностью препарат — густая жидкость от светло-желтого до темно-коричневого цвета с сильным неприятным запахом.
МЕТИЛМЕРКАПТОФОС (метилсистокс, метилдеметон)
(p-меркаптоэтилдиметилтиофосфат).
сн30ч у5
Тионовый изомер J> Р — OCH2CH2SC2H5
CHSCK
. СН3Оч
Тиоловыи изомер \ Р - SCH2CH2SC2H5
СНзСК Мол. вес 230,29
Метилмеркаптофос — слегка окрашенная жидкость со специфическим неприятным запахом. Хорошо растворим в органических растворителях. Растворимость в воде тионового изомера — 0,03%, тиолового — 0,3%.
ПРЕПАРАТ М-81 (интратион) (0,0-диметил-р-этилмеркаптоэтилдитиофосфат).
СН3Оч />
Мол. вес 246,36
>Р- SCH2CH2SC2H6 СНоСК
Химически чистый препарат М-81 представляет собой прозрачную жидкость с неприятным запахом. Хорошо растворяется в органических растворителях.
ТИОФОС (паратион)
(0,0-диэтил-4-нитрофенилтиофосфат).
С2Н60
|
С2НбО |
Мол. вес 291,27
Чистый диэтил-4-нитрофенилтиофосфат — слабожелтая жидкость, застывающая при 6,0° С. Хорошо растворим в спиртах, ацетоне, эфире и других органических растворителях. Препарат разрушается под действием солнечного света.
Технический тиофос — коричнево-красная жидкость с характерным запахом. Технический продукт содержит различные примеси, главным образом п-нитрофенол.
Принцип метода *
Фосфорорганические ядохимикаты извлекают из растительных пищевых продуктов органическими растворителями, отделяют путем хроматографии от мешающих примесей и фосфатидов, присущих самому растению, разрушают смесью минеральных кислот и марганцовокислым калием до неорганического фосфата и определяют по фосфору в виде синего фосфорно-молибденового гетерополикомплекса.
Чувствительность определения — 0,15 мг препарата в 1 кг анализируемого продукта.
Реактивы и растворы
Хлороформ химически чистый, перегнанный. Необходим для определения метилмеркаптофоса, препарата М-81 и тиофоса.
Диатомит — порошок Каменец-Подольско-го месторождения, необходим для определения препарата М-81.
Алюминия окись для хроматографии Ф-1, К-2, ТУМХП
2962—54, влажность 15%. Необходима для определения метилмеркаптофоса и карбофоса.
Алюминия окись, обработанная соляной кислотой, необходима для определения тиофоса. 200 г окиси алюминия химически чистой заливают 300 мл 2 н. соляной кислоты на 10—12 часов. Смесь периодически перемешивают. После этого адсорбент промывают
* Разработан Киевским и.-и. институтом гигиены питания М3 УССР (М. А. Клисенко, Г. А. Исаева, К. К. Еношевская).
2—758
9
1
При определении особое внимание следует обращать на температуру водяной бани при отгонке хлороформа и на начальную температуру парафиновой бани. При определении метилмеркаптофоса температура водяной бани при стгонке хлороформа не должна быть выше 65°. Вследствие летучести препарата повышение температуры водяной бани ведет к снижению процента определения до 40—45. Так же снижаются результаты определения, если начальная температура парафиновой бани выше 70°.
21
2
Разработан Н.-и. институтом защиты растений юго-западных районов Молдавской ССР (Л. М. Фукельман).
13
3
Разработан Институтом питания АМН СССР (3. Н. Богомолова).
4
Метод разработан ВНИИЭВ (А. В. Николаев, Л. И. Устименко).
20
5
Разработан Украинским н.-и. институтом защиты растений (Е. С. Косматый, И. Б. Миронова, Л. Т. Бугаенко).
3;
6
Разработан Киевским н.-и. институтом гигиены питания М3 УССР (М. А. КлИсеико).
6