Методические указания по лабораторной диагностике везикулярной болезни и везикулярной экзантемы свиней
Купить бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Учебное издание содержит действующие методические указания, наставления и инструкции по лабораторной диагностике вирусных болезней животных, утвержденные Министерством сельского хозяйства СССР, РФ и Россельхознадзором РФ. Документы систематизированы по видам животных, в большинстве прошли многолетнюю аппробацию в Алтайской краевой ветеринарной лаборатории и включены в «Перечень нормативной документации, разрешенной для использования в государственных ветеринарных лабораториях при диагностике болезней животных, рыб, пчел, а также контроля безопасности сырья животного и растительного происхождения» (по состоянию на июль 2011 г.). Приводятся предметный указатель и библиографический список.
Предназначено для студентов, обучающихся по специальности «Ветеринария» и направлению «Ветеринарно-санитарная экспертиза», ветеринарных врачей и лаборантов ветеринарных лабораторий.
Оглавление
1. Общие положения
2. Взятие и подготовка материала для исследования
3. Обнаружение типоспецифического антигена в патологическом материале в РСК
4. Модифицированный метод РСК с учетом результатов фотоэлектроколориметрии
5. Выявление типоспецифического антигена в патологическом материале методом РДП
6. Выделение вируса в культуре клеток
7. Идентификация выделенного вируса с помощью метода иммунофлуоресценции (прямой вариант)
8. Идентификация и серотипирование выделенного вируса ВБС и ВЭС в реакции нейтрализации
9. Ретроспективная диагностика
10. Биологическая проба
11. Идентификация вируса ВБС и ВЭС и дифференциация их от вирусов ящура и везикулярного стоматита по физико-химическим свойствам
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.220 Ветеринария
- Раздел 11 ЗДРАВООХРАНЕНИЕ
Организации:
| Издан | Издательство Лань | 2015 г. |
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11
стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19
стр. 20
стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
ЛАБОРАТОРНАЯ ДИАГНОСТИКА ВИРУСНЫХ БОЛЕЗНЕЙ ЖИВОТНЫХ
ВЕТЕРИНАРНАЯ
|
П. И. Барышников, В. В. Разумовская |
МЕДИЦИНА
• САНКТ-ПЕТЕРБУРГ • •МОСКВА-• КРАСНОДАР--2015-
372 Лабораторная диагностика вирусных болезней животных
................................................................................I...............................................................................................................................................
|
Схема 5 Определение серотипа вирусов ВВС и БЭС | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
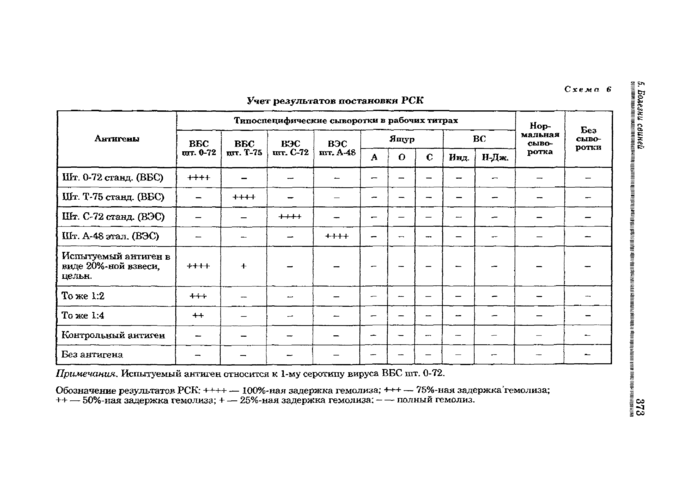
Учет РСК проводят по 100%-ному гемолизу. Главный опыт ставят по схеме 5.
Учет результатов проводят по схеме 6.
3.4. Положительной РСК считается в том случае, когда наблюдается 100%-ная или 75%-ная задержка гемолиза (четыре-три креста) в присутствии одной из типоспецифических сывороток и антигена из испытуемого материала при полной задержке гемолиза в контрольных пробирках с соответствующими специфическими антигенами и сыворотками и при полном гемолизе в пробирках с контрольным — нормальным антигеном и гетерологичными сыворотками.
При получении сомнительного результата (один-два креста) РСК повторяют.
При получении повторного сомнительного результата реакцию считают положительной.
При получении отрицательного результата в РСК (тепловой вариант с учетом по 100% -ному гемолизу) проводят постановку модифицированной РСК с регистрацией результатов фотоэлектроколориметрией.
|
= t'b - С* = = к = гу = сь = с = ге = съ = |
|
Схема € Учет результатов постановки РСК | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Примечания. Испытуемый антиген относится к 1-му серотипу вируса ВБС шт. 0-72. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Обозначение результатов РСК; -н~н--100%-ная задержка гемолиза; -ь-м- — 75%-ная задержка'гемолиза;
++ — 50%-ная задержка гемолиза; н--25%-ная задержка гемолиза;--полный гемолиз.
= СО = -3
= СО
Лабораторная диагностика вирусных болезней животных
lllllllUI|[IUllHIIHIIUMinillllll|nU[IIIIIIIIIIIUHtlllllHIUIIII№lllillltfllinitminnirnHlllMIIIIIIIIH«HllllllltlllllHIIIIUMIIWHIIIIi|ll
4, Модифицированный метод РСК с учетом результатов фотоэлектроколориметрии.
4.1. Данный метод используют для исследования проб патологического материала (везикул и везикулярной жидкости) с низкой комплементсвязывающей активностью. Метод основан на учете результатов гемолиза на спектрофотометре (фотоэлектроколориметре) с нефелометром.
4.2. Компоненты реакции;
■ испытуемый антиген, приготовленный, как указано в п. 2.2;
а два типоспецифических КС антигена вируса ВВС (0-72 и Т-75);
■ два типоспецифических КС антигена вируса ВЭС (С-72 и А-46);
■ контрольный (отрицательный) антиген;
Я две типоспецифические КС сыворотки к вирусу ВВС (0-72 и Т-75);
Я две типоспецифичеекие КС сыворотки к вирусу ВЭС (С-72 и А-48);
■ три типоспецифичеекие сыворотки к вирусу ящура типов А, О и С;
■ две типоспецифические сыворотки к вирусу везикулярного стоматита типов «Индиана» и «Нью-Джерси»;
■ контрольная (отрицательная) сыворотка;
■ гемолизин;
■ комплемент;
■ эритроциты барана, приготовленные на вероналовом буфере;
Ш физиологический раствор.
4.3. Приготовление стандартной суспензии эритроцитов. Эритроциты барана 3...4 раза отмывают и из осадка готовят 0,6.,.0,7%-ную взвесь на вероналовом буфере. Стандартную взвесь готовят по следующей схеме:
|
№ пробирок |
Суспензия отмытых эритроцитов <№|) |
Веронало-вый буфер (мл) |
Физиологический раствор |
Оптическая плотность |
|
1 |
0,26 |
1,76 |
3,0 |
0,51 |
|
2 |
0,26 |
1,76 |
3,0 |
0,60 |
|
3 |
0,26 |
1,76 |
3,0 |
0,49 |
5. Болваны свиней 375
.....................................................................................................................................................................................
В РСК используют взвесь эритроцитов, в которой средний показатель оптической плотности должен быть равен 0,50,
4,3.1, Примечание: Состав вероналового буфера:
■ барбитуровая кислота — 2,875 г;
■ барбитурат натрия— 1,875 г;
■ сернокислый магний 0,616 г;
■ хлористый кальций —- 0,080 г;
Я хлористый натрий — 45,5 г;
Я дистиллированная вода — 2 л.
Вначале в мерной колбе на 2 л растворяют барбитуровую кислоту в 500 мл подогретой дистиллированной воды, а затем все остальные компоненты с добавлением воды до метки. Раствор стерилизуют автоклавированием при 110°С в течение одного часа. Хранят до 2 мес. при 4°С, Перед употреблением разбавляют 2:3 дистиллированной водой.
4.4. Гемолитическая система. Готовят разведение гемолизина соответственно удвоенному его титру в обычной РСК, Смешивают равные объемы раствора гемолизина и стандартной суспензии эритроцитов. Смесь выдерживают в течение 15 мин при комнатной температуре.
4.5. Титрование комплемента проводят трехкратно. Комплемент разводят 1:200 и титруют по следующей схеме:
|
Комплемент 1:200 |
0,20 |
0,25 |
0,30 |
0,35 |
0,40 |
0,45 |
0,50 |
0,55 |
0,66 |
|
Веронал овый буфер |
1,3 |
1,76 |
1,20 |
1,16 |
1,10 |
1,05 |
1,00 |
0,95 |
0,90 |
|
30 мин при 5Т6С на водяной бане | |||||||||
|
Гемсистема |
0,5 | ||||||||
|
Физ. раствор |
3,0 | ||||||||
Учет результатов.
Полученные результаты наносят на миллиметровую бумагу и находят точку, соответствующую 50% -ному гемолизу эритроцитов (ОП = 0,25). В опыт берут 1,2 СН50 комплемента.
4.6. Постановка основного опыта. Готовят двукратные разведения испытуемого антигена от 1:5 до 1:400, а далее
376 Лабораторная диатостика вирусных болезней животных
HlllllllllllHllllllllll^ll1lllllllUllllliniMllinilllHIIIHIUllJiHIIIUIIt1H|l|IJnitrillllllilll1illllllttl|llllll|[|j|IIIIIJlllMll«talllllllllllllhllllJinillllllllllllHlllJJIIIIICr|k|ll«llliyilinil(ll!IIIHMIIIII^IU^lll
в зависимости от примерной исходной активности антиге-на. Разливают по 0,5 мл каждого разведения антигена. Количество пробирок зависит от числа специфических сы-вороток, взятых в опыт. Вносят по 0,5 мл рабочего разведения сывороток согласно титру в обычной РСК. Добавляют комплемент в рабочем разведении и инкубируют при 37°С в течение 30 мин. Затем вносят по 0,5 мл гемсисте-мы, выдерживают снова 30 мин при 37°С и проводят учет реакции.
4.7. Учет реакции. В левый кюветодержатель ФЭКН-57 ставят кювету с буфером, а в правый кюветодержатель — кювету с измеряемой пробой. Вращением правого барабана устанавливают стрелки прибора на нуль. Проводят отсчет показания прибора по правому барабану. Разница показания прибора на 0,15 и более между опытной пробиркой и контрольной — на антикомплементарность антигена + сыворотки, принимается за положительный результат. Разница 0,10...0,14 — за сомнительный, 0,10 и ниже — за отрицательный результат.
4.8. Настройку прибора ФЭКН-57 и измерение проводят по инструкции, прикладываемой к прибору.
Для измерения использует фотоэлектроколориметр с нефелометром. Учет результатов проводят с использованием кюветы на 10 мм при переключении на нефелометриче-ское измерение с красным светофильтром (№ 8).
При малых объемах материала объем каждого реагента можно уменьшить до 0,25 мл, добавить физраствора 1,6 мл. Измерение при этом проводят в кюветах на 5 мм.
5. Выявление типослецифического антигена в патологическом материале методом РДП.
5.1. Для постановки РДП используют 1,5%-ный агар, приготовленный на дистиллированной воде с добавлением 1,6% хлористого натрия. Для сохранения агара к нему добавляют 10% -ный раствор фенола из расчета 50 мл раствора на 1 л агара и 0,03 г мертиолята. Такой агар хранится в течение двух месяцев. Перед постановкой реакции его разливают в чашки Петри и штампом делают лунки (диаметр лунок 5 мм, расстояние между лунками 5 мм).
6. Болезни сейма 377
шл1№1»иимш1Н№1 niiiiiiH iHi« пин гпнипнпши ........ мини
5.2. Компоненты реакции:
■ испытуемые антигены, приготовленные, как указано в п. 2.2;
■ два контрольных типоспецифических антигена штаммов ВБС (0-72 и Т-75);
Л контрольный типоспецифический антиген штамма ВЭС (С-72);
к две типоспецифические сыворотки к штаммам ВБС{0- 72 и Т-75);
■ типоспецифическая сыворотка к штамму ВЭС (С-72);
■ типоспецифические сыворотки к 7 типам вируса ящура.
5.3. Постановка реакции. В центральные лунки вносят испытуемый и контрольный антигены, в периферические — типоспецифические сыворотки. Чашки инкубируют при 37°С. Учет реакции проводят через 24, 48 и 72 ч.
5.4. Учет реакции. Положительная реакция характеризуется образованием четкой, белого цвета одной или двух линий преципитации между антигеном и гомологичной сывороткой.
Возбудитель относят к тому виду (типу), с сывороткой которого испытуемый антиген дает положительную реакцию.
6. Выделение вируса в культуре клеток.
6.1. Для выделения вируса используют перевиваемую (ПП) или первично-трипсинизированную культуры клеток почки поросенка. Для заражения используют 10%-ную взвесь из стенок везикул, приготовленную, как указано в п. 2.3.
Одной исследуемой пробой заражают не менее 4...6 пробирок или флаконов с культурой клеток, внося в каждую пробирку по ОД мл (во флакон — по 0,5 мл) взвеси, предварительно удалив из пробирок питательную среду и промыв культуру клеток раствором Хенкса.
Пробирки выдерживают в течение 60 мин при комнатной температуре, после чего в них добавляют поддерживающую питательную среду (0,9 мл в пробирки, 10 мл — во флаконы) и инкубируют в течение 3...5 сут, не меняя
Лабораторная диагностика вирусных болезней животных
среды. Для контроля оставляют 4...6 пробирок с незара-женной культурой клеток.
6.2. Поддерживающая среда состоит из раствора Хенкса с 0,5% -ным гидролизатом лактальбумина с добавлением по 200ЕД/мл пенициллина и стрептомицина, с pH 7,2,..7,4.
6.3. Учет реакции. Для выявления цитопатического действия вируса в зараженных культурах их ежедневно просматривают под малым увеличением микроскопа в течение
3...5 дней. При наличии вируса ВВС или БЭС в исследуемом материале ЦПД обнаруживается через 24...48 ч. Оно характеризуется мелкоклеточной деструкцией по всему мо-нослою с последующим образованием мелких конгломератов и отслоением от стекла. Для вируса ВЭС характерно появление светопреломляющих округлых клеток по всему монослою с последующим образованием гроздевидных скоплений, которые затем также отслаиваются от стекла.
6.4. При наличии ЦПД-вируса на два креста (деструкция 50% клеток) проводят его идентификацию в РСК (как описано в п. 3) или в реакциях нейтрализации и иммунофлуоресценции.
7. Идентификация выделенного вируса с помощью метода иммунофлуоресценции (прямой вариант).
7.1. Метод иммунофлуоресценции используется только для идентификации вируса ВЭС,
7.2. Выделенный вирус выращивают в культуре клеток на покровных стеклах. При появлении ЦПД (через 6..,8 ч инкубации) покровные стекла вынимают из пробирок и многократно отмывают фосфатно-буферным раствором, затем стекла подсушивают на воздухе и фиксируют метиловым спиртом в течение 5 мин.
7.3. Для выявления вируса ВЭС используют специфическую флуоресцирующую сыворотку в рабочем разведении. Для контроля используют нормальную флуоресцирующую сыворотку в том же разведении.
7.4. Проведение реакции. Фиксированные препараты многократно отмывают фосфатно-буферным раствором, высушивают на воздухе в течение 10...20 мин и обрабатывают флуоресцирующей сывороткой. Для контроля одно-
5. Болезни свиней 379
......................................................................................................................................................................................
типные препараты обрабатывают нормальной флуоресцирующей сывороткой. Препараты помещают во влажную камеру и выдерживают в течение 30 мин при 37°С. Окрашенные препараты многократно промывают фосфатно-буферным раствором, высушивают на воздухе, покрывают эабуференным глицерином (9:1) и покровным стеклом и микроскопируют.
7.5. Оценка результатов. Положительной считается реакция, при которой в препарате наблюдается специфическое флуоресцирующее свечение клеток или цитоплазмы клеток не менее чем на два креста в трех и более полях зрения.
7.6. В сомнительных случаях окончательный диагноз на ВЭС ставят по результатам PH.
8. Идентификация и серотипирование выделенного вируса ВВС и ВЭС в реакции нейтрализации.
8.1. Идентификацию и серотипирование выделенного вируса проводят с помощью типоспецифических вирусней-трализующих сывороток:
■ две сыворотки к вирусам ВВС (к штаммам 0-72 и Т-75);
■ две сыворотки к вирусам ВЭС (к штаммам С-72 и А-46).
8.2. При необходимости дифференциации выделенного вируса от вируса ящура и вируса везикулярного стоматита в PH дополнительно используют сыворотки к указанным вирусам.
8.3. Постановка реакции. Выделенный вирус в культуре клеток отстаивают при комнатной температуре (20°С), затем центрифугируют при 3000 об/мин в течение 20 мин и иадосадочную жидкость используют для постановки PH, Из надосадочной жидкости готовят десятикратные разведения (от 10-1 до 10~б) на 0,5%-ном гидролизате лактальбу-мина и к 0,5 мл каждого разведения добавляют такой же объем типоспецифической сыворотки. В реакции используют в четырехкратном титре сыворотки, инактивированные при температуре 57°С в течение 30 мин. Смесь встряхивают, выдерживают при комнатной температуре в течение 60 мин. Затем по 0,2 мл каждой смеси вносят в пробирки с культурами и доливают в них поддерживающую среду до
Лабораторная диагностика вирусных болезней животных
объема 1 мл. Перед заражением проводят однократное от* мывание монослоя поддерживающей средой.
8.3.1. Контроли:
■ незараженная культура клеток;
и культура клеток, зараженная выделенным вирусом в
разведении от 10"1 до 10 е;
■ культура клеток, в которую внесены типоспецифиче-
ские сыворотки в разведении 1:10.
Культуры клеток инкубирует при 37°С и ежедневно просматривают под микроскопом.
8.4. Учет реакции. Культуры просматривают в течение 3...5 дней до выявления ЦПД в пробирках с культурой, зараженной вирусом.
По выявлении ЦПД определяют титр инфекционности выделенного вируса (предельное его разведение, которое вызывает ЦПД в 50% зараженных пробирок не менее, чем на два креста).
Предельное разведение вируса, дающее ЦПД, обозначают как одну дозу ТЦДБ0 (титр высчитывают по методу Рида и Менча). Индекс нейтрализации высчитывают по разности показателей ТЦД50 выделенного вируса в присутствии типоспецифических сывороток и определяют серотиповую принадлежность вируса.
0. Ретроспективная диагностика.
9.1. Для ретроспективной диагностики исследуют парные или однократко отобранные сыворотки переболевших животных. Сыворотки исследуют на наличие антител с помощью типоспецифических антигенов в РСК, РДП или PH.
9.2. Реакция связывания комплемента. РСК проводят в варианте длительного связывания.
Компоненты реакции:
■ типоспецифические антигены ВВС (штаммы 0*72 и Т-75);
■ типоспецифические антигены ВЭС (штаммы С-72 и А-48);
■ контрольный отрицательный антиген;
■ типоспецифические сыворотки к штаммам (0-72, Т-75,
С-72 и А-48);
■ контрольная отрицательная сыворотка;
■ испытуемые сыворотки, инактивированные;
5, Башни свиней 381
UiU№i|jUIUItniWllUIUILIUlLUIIILllU4Lll4l(UUU4IIUtlllbHIUUIIllllllllUIIUiLUUkHIUIIHI№tkUtllHIUIM1UIHnilUllaHI4mHI]tkU№ilMHIItUI№l)l|^lllimilUnillllhlMltlllHiaMmtnlllltlUHlllll
■ гемолизин к эритроцитам теленка;
■ комплемент.
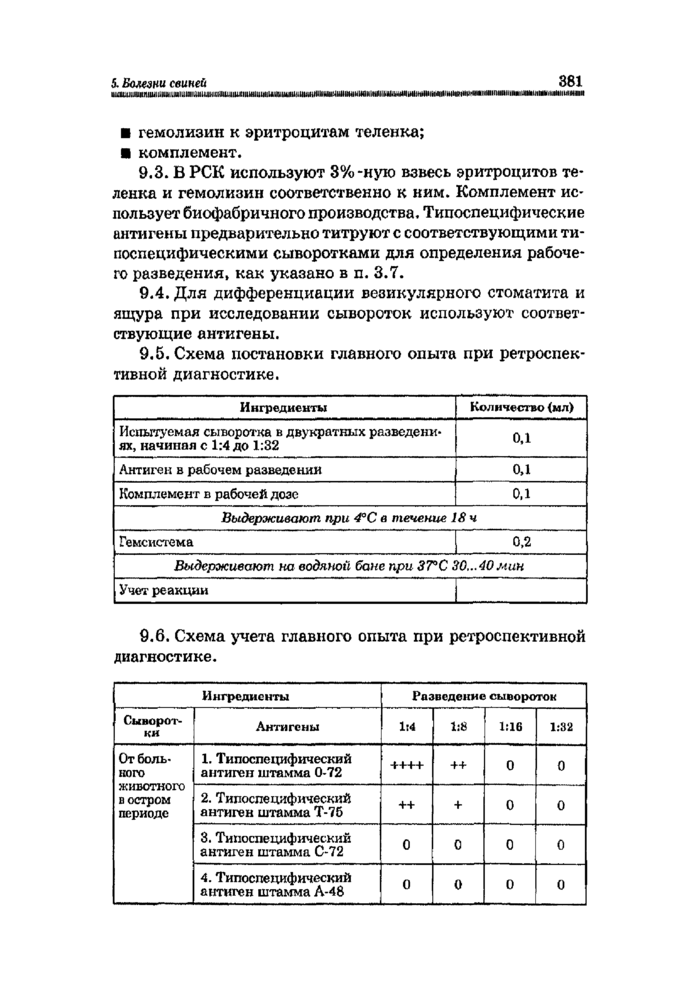
9.3. В РСК используют 3%-ную взвесь эритроцитов теленка и гемолизин соответственно к ним. Комплемент использует биофабричного производства, Тшюспецифические антигены предварительно титруют с соответствующими типоспецифическими сыворотками для определения рабочего разведения, как указано в п. 3.7.
9.4. Для дифференциации везикулярного стоматита и ящура при исследовании сывороток используют соответствующие антигены.
9.5. Схема постановки главного опыта при ретроспективной диагностике.
|
Ингредиенты |
Количество <мл) |
|
Испытуемая сыворотка в двукратных разведениях, начиная с 1:4 до 1:32 |
од |
|
Антиген в рабочем разведении |
ОД |
|
Комплемент в рабочей дозе |
ОД |
|
Выдерживают при 4°С в течение 18 ч | |
|
Гемсистема |
0,2 |
|
Выдерживают на водяной бане при ЗТ*С 30.-40 мин | |
|
Учет реакции J | |
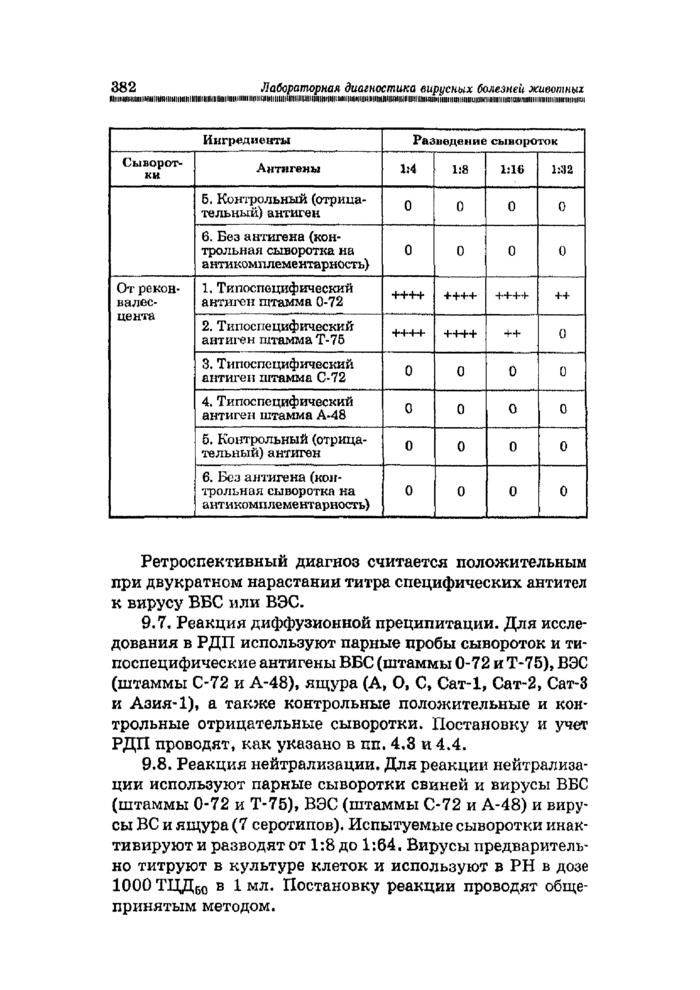
9.6. Схема учета главного опыта при ретроспективной диагностике.
|
Ингредиенты |
Разведение сывороток | ||||
|
Сыворот ки |
Антигены |
1:4 |
1:8 |
1:16 |
1:32 |
|
От больного животного в остром периоде |
1. Типоспецифический антиген штамма 0-72 |
++++ |
-и- |
0 |
0 |
|
2. ТипоспецифическиЙ антиген штамма Т-76 |
++ |
+ |
0 |
0 | |
|
3. Типоспецифический антиген штамма С-72 |
0 |
0 |
0 |
0 | |
|
4. Типоспецифический антиген штамма А-48 |
0 |
0 |
0 |
0 | |
ЛАБОРАТОРНАЯ ДИАГНОСТИКА ВИРУСНЫХ БОЛЕЗНЕЙ ЖИВОТНЫХ
Составители:П. И. Барышников,В. В. Разумовская
В. В. Разумовская
Издание второе, исправленное
ДОПУЩЕНО
Министерством сельского хозяйства РФ в качестве учебного пособия для студентов вузов, обучающихся по направлению подготовки ('специальности,) «Ветеринарий»
ДОПУЩЕНО
УМО вузов РФ по образованию в области зоотехнии и ветеринарии в качестве учебного пособия для студентов вузовг обучающихся по направлению подготовки (специальности) «Ветеринарий» (квалификация (степень) «Ветеринарный врач»)
ЛАНГ
• САНКТ-ПЕТЕРБУРГ • МОСКВА * КРАСНОДАР * •2015-
|
382 Лабораторная диагностика вирусных болезней животных ........................................................................................................................................................ Itlllf............................... | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Ретроспективный диагноз считается положительным при двукратном нарастаний титра специфических антител к вирусу ВВС или ВЭС.
9.7, Реакция диффузионной преципитации. Для исследования в РДП используют парные пробы сывороток и типоспецифические антигены ВВС (штаммы 0-72 и Т-75), ВЭС (штаммы С-72 и А-48), ящура (А, О, С, Сат-1, Сат-2, Сат-3 и Азия-1), а также контрольные положительные и контрольные отрицательные сыворотки. Постановку и учет РДП проводят, как указано в пп, 4,3 и 4.4.
9.8. Реакция нейтрализации. Для реакции нейтрализации используют парные сыворотки свиней и вирусы ВВС (штаммы 0-72 и Т-75), ВЭС (штаммы С-72 и А-48) и вирусы ВС и ящура (7 серотипов). Испытуемые сыворотки инактивируют и разводят от 1:8 до 1:64, Вирусы предварительно титруют в культуре клеток и используют в PH в дозе 1000 ТЦД50 в 1 мл. Постановку реакции проводят общепринятым методом.
ББК 48.7я73 Л 12
Л12 Лабораторная диагностика вирусных болезней животных / Сост, П. И. Барышников, Б. В. Разумовская: Учебное пособие. — 2-е изд., испр. — СПб,: Издательство «Лань», 2015.— 672с,: ил, — (Учебники для вузов. Специальная литература).
ISBN 978-5-8114-1882-4
Учебное издание содержит действующие методические указания, наставления и инструкции по лабораторной диагностике вирусных болезней животных, утвержденные Министерством сельского хозяйства СССР, РФ и Россельхознадзором РФ. Документы систематизированы по видам животных, в большинстве прошли многолетнюю аппробацию в Алтайской краевой ветеринарной лаборатории и включены в «Перечень нормативной документации, разрешенной для использования в государственных ветеринарных лабораториях при диагностике болезней животных, рыб, пчел, а также контроля безопасности сырья животного и растительного происхождения» (по состоянию на июль 2011 г.). Приводятся предметный указатель и библиографический список.
Предназначено для студентов, обучающихся по специальности «Ветеринария» и направлению «Ветеринарно-санитарная экспертиза», ветеринарных врачей и лаборантов ветеринарных лабораторий.
ББК 48.7я73
Рецензенты:
Я. Я. ГУСЛАВСКИЙ — доктор ветеринарных наук, профессор кафедры микробиологии, эпизоотологии, паразитологии и ВСЭ Алтайского государственного аграрного университета;
В. Я. ПЛЕШАКОВА — доктор ветеринарных наук, профессор, зав. кафедрой ветеринарной микробиологии, вирусологии и иммунологии Омского государственного аграрного университета им. П. А. Столыпина;
В. А СИНИЦЫН — доктор ветеринарных наук, зав. отделом ФГБУ «Новосибирская межрегиональная ветеринарная лаборатория*.
Обложка © Издательство «Лань», 2015 Е. А. ВЛАСОВА © Коллектив авторов, 2015 © Издательство «Лань»,
художественное оформление, 2015
366 Лабораторная диагностика вирусных болезней животных
IlNlllllllllll.................................................................................................................................................IIIIHII.....II............................................
ВЕЗИКУЛЯРНАЯ БОЛЕЗНЬ И ВЕЗИКУЛЯРНАЯ ЭКЗАНТЕМА
5.13,
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
по лабораторной Диагностике
ВЕЗИКУЛЯРНОЙ БОЛЕЗНИ И ВЕЗИКУЛЯРНОЙ ЭКЗАНТЕМЫ СВИНЕЙ (утверждены 16 июня 1979 г., б/н)
1. Общие положения.
1.1. Лабораторная диагностика везикулярной болезни (ВВС) и везикулярной экзантемы синей (ВЭС) заключается в:
■ обнаружении антигена в патологическом материале (везикулы, везикулярная жидкость) методами реакции связывания комплемента (РСК), реакции диффузионной преципитации (РДП);
■ выделении возбудителя из патологического материала в культуре клеток и его идентификации в серологических реакциях: иммунофлуоресценции (ИФ), РСК или реакции нейтрализации (PH);
■ выявлении антител в крови больных и переболевших животных (ретроспективная диагностика) в одной из серологических реакций РСК, РДП, PH;
я биологической пробе;
я исследовании физико-химических свойств выделенного вируса.
367
I III 1111 МИН j)l Hill II III! I Hill lillllfl ШИН Hill ......Illllllllllllllll
1.2. При диагностике везикулярной болезни и везикулярной экзантемы проводят дифференциацию везикулярного стоматита и ящура в РСК или РДП и биологической пробе с использованием сопутствующих каждой инфекции диагностических наборов, выпускаемых биологической промышленностью.
1.3. Лабораторный диагноз на везикулярную болезнь и везикулярную экзантему свиней ставят на основании положительных результатов исследования патологического материала на обнаружение антигена с помощью одной из'серологических реакций (РСК, РДП) или выделения возбудителя в РСК или PH или установления двукратного нарастания титра антител в организме животных с учетом эпизоотоло-гических и клинических данных.
1.4. Для постановки лабораторного диагноза методом обнаружения антигена в патологическом материале требуется 1...3 дня, для выявления вируса и его идентификации — до 10 дней, для выявления прироста антител в крови животных — от 2 до 4 недель,
2. Взятие и подготовка материала для исследования.
2.1. В лабораторию для исследования направляют стенки невскрывшихся везикул и везикулярную жидкость от
2...5 больных животных в количестве не менее 2 г. Везикулы от свиней берут с кожи «пятачкавенчика, мякишей или вымени, предварительно промыв эти участки кожи водой с антибиотиками (1000 ЕД пенициллина и стрептомицина на 1 мл). Стенки везикул срезают ножницами, помещают во флакон или пробирки, опечатывают и в термосе со льдом направляют в лабораторию с нарочным.
Для ретроспективной диагностики на исследование направляют пробы крови от 5... 10 переболевших животных.
2.2. В лаборатории везикулы отмывают физиологическим раствором, растирают в ступке и добавляют 1:5 фосфатно-буферный раствор с pH 7,2...7,4. После двукратного замораживания и оттаивания взвесь центрифугируют при 10 000 об/мин на холоде в течение 30 мин. Надосадочную жидкость исследуют в РСК на наличие антигена. Для РДП используют неразведенную везикулярную жидкость из
Лабораторная диагностика вирусных болезней животных
невскрывшихся везикул или 35...50%-ную взвесь на физиологическом растворе из стенок везикул.
2.3. Для выделения вируса в культуре клеток готовят 10%-ную взвесь из везикул на фосфатно-буферном растворе или питательной среде и, не подвергая замораживанию и оттаиванию, центрифугируют при 3000 об/мин в течение 20 мин. В надосадочную жидкость добавляют антибиотики по 1000 ЕД/мл пенициллина и стрептомицина и используют для заражения.
3. Обнаружение типоспецифического антигена в патологическом материале в РСК.
3.1. Компоненты реакции:
■ испытуемый антиген, приготовленный, как указано в п. 2.2;
■ два типоспецифических комплементсвязывающих (КС) антигена вируса ВВС (0-72 и Т-75);
■ два типоспецифических КС антигена вируса БЭС (С-72 и А-48);
■ контрольный (отрицательный) антиген;
■ две типоспецифических комплементсвязывающих сыворотки к вирусу ВВС (0-72 и Т-75);
■ две типоспецифических КС сыворотки к вирусу БЭС (С-72 и А-48);
■ контрольная (отрицательная) сыворотка;
■ гемолизин;
■ комплемент;
■ эритроциты барана (2% -ная взвесь).
3.2. Испытуемый антиген исследуют в двукратных разведениях, остальные антигены и сыворотки — в удвоенном титре.
3.3. Постановка реакции: реакцию ставят в пробирках, титрование гемолизина и комплемента проводят в объеме 2,5 мл, а основной опыт — в объеме 0,5 мл.
РСК проводят в четыре этапа: титрование гемолизина, титрование комплемента, титрование антигенов и сывороток в присутствии комплемента и постановка главного опыта.
369
5. Болезни свиней
lltlllHIIIIIIIIIIIIIIIIIIILIIIIIJIfllllllllllllllllllFIIIIIIIII»l|IHIHIIIiri1|l1MNII1IHlV|ll7«lltlirNljlllllllllllHIIIIIIJIIIIIIIIIinilllllllllllH!lllirillllllllClllllli|F|l|||||
3.3.1. Титрование гемолизина. Для титрования гемолизина готовят основное его разведение 1:100 (0,2 мл гемолизина и 9,8 мл физиологического раствора, с учетом того, что гемолизин в ампуле разведен глицерином), затем — раз-ведение 1:1000 и из этого разведения готовят все последующие по схеме 1.
Титром гемолизина считают наивысшее его разведение, дающее полный гемолиз эритроцитов.
Рабочим разведением гемолизина считают четырехкратную концентрацию его предельного титра с учетом консервирования глицерином.
Например, если предельный титр гемолизина 1:4000, рабочее разведение его составит 1:1000, то берут его в соот-
|
Схема 1 Приготовление разведений гемолизина | ||||||||||||||||||||||
| ||||||||||||||||||||||
|
Схема 2 |
|
Титрование гемолизина | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
|
Примечание: 0 — полный гемолиз; ++++ — полная задержка. | |||||||||||||||||||||||||||||||||||||||||||||||||
Лабораторная диагностика вирусных болезней животных
370
№1Ш1Ш1
ношении 2:1000 (0,2 мл гемолизина и 99,8 мл физиологического раствора).
Для приготовление гемсистемы используют гемолизин в рабочем разведении и смешивают с равным количеством 2%-ной взвеси эритроцитов и выдерживают при комнат-ной температуре в течение 10...15 мин.
3.3.2. Титрование комплемента. Комплемент титруют в разведении 1:20 в различных дозах по схеме 3.
|
Схема 3 Титрование комплемента | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Титром комплемента считают наименьшее его количество, при котором наступает полный гемолиз эритроцитов. Для титрования антигенов, сывороток и постановки главного опыта используют 2 дозы комплемента, которые соответствуют пробирке, находящейся через одну пробирку вправо от последней пробирки с полным гемолизом.
По схеме 3 полный гемолиз дают 2% комплемента, следовательно, рабочей дозой комплемента является разведение с содержанием 3% комплемента. Разведение готовят из цельного комплемента.
Например, по схеме 3 в опыт на 100 пробирок требуется 10 мл разведенного комплемента, для этого берут 0,3 мл цельного комплемента и добавляют 9,7 мл физиологического раствора.
371
......................................
3.3.3. Титрование типоспецифических антигенов. Титрование антигенов проводят с целью установления рабочей дозы антигена по схеме 4. Типоспецифические сыворотки используют в двойном титре.
|
Схема 4 Титрование типоспецифических антигенов | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Титром антигена считают его наибольшее разведение, давшее со специфической сывороткой задержку гемолиза не менее чем на три креста.
Рабочим разведением антигена считается удвоенный титр антигена. По схеме 4 рабочее разведение антигена будет равно 1:2.
3.3.4. Титрование типоспецифических сывороток проводят по схеме 4, используя разведения их до предельного татра, а антигены — в рабочих разведениях.
3.3.б. Постановка главного опыта РСК. Реакции связывания комплемента ставят в объеме 0,5 мл. Первую фазу реакции (фазу связывания комплемента) проводят на водяной бане при температуре 37°С в течение 20...30 мин. Вторую фазу (фазу выявления) также проводят на водяной бане при температуре 37°С в течение 20...30 мин.