Методика производства молекулярно-генетического исследования генно-инженерно-модифицированных организмов, используемых для производства кормов и кормовых добавок для животных, а также кормов и кормовых добавок для животных, полученных с применением таких организмов или содержащих такие организмы
Купить бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Методика устанавливает порядок проведения молекулярно-генетического исследования генно-инженерно-модифицированных организмов, используемых для производства кормов и кормовых добавок для животных, а также кормов и кормовых добавок для животных, полученных с применением таких организмов или содержащих такие организмы
Оглавление
I Общие положения
II Исследование ГМО, являющихся микроорганизмами
III Исследование ГМО растительного происхождения
IV Исследование ГМО животного происхождения
V Исследование продукции
Приложение. Таблица 1. Основные маркерные и селективные гены, являющиеся составляющими частями генно-инженерных конструкций микроорганизмов
Таблица 2. Основные генетические последовательности в геноме ГМО растительного происхождения
Таблица 3. Критерии эффективности методики идентификации ГМО
Таблица 4. Критерии эффективности методики полногеномного секвенирования
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.02.2020 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
Организации:
| 22.03.2019 | Утвержден | Минсельхоз России | 126 |
|---|
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10
стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18
стр. 19
ф
MHHHCfIPtTW 1РСГИЦНИ «С8НЩЙ И1ЕГШИ
ЗАРЕГИСТРИРОВАНО
Регистрационный Si
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РОССИЙСКОЙ ФЕДЕРАЦИИ
(Минсельхоз России)
ПРИКАЗ
от 22 марта 2019 г. № 126
Москва
Об утверждении Методики производства молекулярногенетического исследования генно-инженерно-модифицированных организмов, используемых для производства кормов и кормовых добавок для животных, а также кормов и кормовых добавок для животных, полученных с применением таких организмов или содержащих такие организмы
В соответствии с пунктом 13 Правил государственной регистрации генно-инженерно-модифицированных организмов, предназначенных для выпуска в окружающую среду, а также продукции, полученной с применением таких организмов или содержащей такие организмы, включая указанную продукцию, ввозимую на территорию Российской Федерации, утвержденных постановлением Правительства Российской Федерации от 23 сентября 2013 г. № 839 (Собрание законодательства Российской Федерации, 2013, №39, ст. 4991; 2014, №25, ст. 3317; 2017, № 28, ст. 4145; 2018, № 6, ст. 896; № 41, ст. 6260), приказываю:
Министр
Утвердить прилагаемую Методику производства молекулярногенетического исследования генно-инженерно-модифицированных организмов, используемых для производства кормов и кормовых добавок для животных, а также кормов и кормовых добавок для животных, полученных с применением таких организйЬв или содержащих такие организмы. 11 ! I
Д.Н. Патрушев
УТВЕРЖДЕНА
приказом Минсельхоза России
от 22 марта 2019 г. № 126
МЕТОДИКА производства молекулярно-генетического исследования генно-инженерно-модифицированных организмов, используемых для производства кормов и кормовых добавок для животных, а также кормов и кормовых добавок для животных, полученных с применением таких организмов или содержащих такие организмы
I. Общие положения
1. Настоящая Методика устанавливает порядок проведения молекулярногенетического исследования генно-инженерно-модифицированных организмов, используемых для производства кормов и кормовых добавок для животных, а также кормов и кормовых добавок для животных, полученных с применением таких организмов или содержащих такие организмы (далее - исследование, ГМО, продукция соответственно).
2. Исследование проводится организацией (испытательной лабораторией), аккредитованной в национальной системе аккредитации, с областью аккредитации, соответствующей исследованиям, указанным в настоящей Методике.
3. Результаты исследования ГМО оформляются заключением
о результатах исследования, составляемым на основании протоколов испытаний, которое должно содержать:
наименование заключения;
полное наименование и место нахождения организации (испытательной лаборатории), осуществившей проведение исследования;
наименование ГМО с указанием его таксономического статуса;
полное наименование и место нахождения, идентификационный номер налогоплательщика (ИНН) юридического лица, осуществляющего на территории Российской Федерации генно-инженерную деятельность в целях создания ГМО (далее - заявитель ГМО);
полное наименование и место нахождения юридического лица либо фамилия, имя, отчество (при наличии), место жительства индивидуального предпринимателя - изготовителя образцов ГМО;
вид предполагаемого целевого использования ГМО;
|
антибиотикоустойчивости (pBR322) | |
|
F1 оп |
Ориджин репликации плазмид (pBSKSII, pKEN-gfpmut2, pCR2.1 ТОРО) |
|
Транспозон Tn7L |
Фрагмент обеспечивает транспозицию рекомбинантных генов из плазмид в геном (pRK415-gfp) |
|
Г ен егшС |
Кодирует устойчивость к эритромицину, плазмидные вектора |
|
Ген cat |
Кодирует устойчивость к хлорамфениколу, плазмидные вектора |
|
R6K ori |
Ориджин репликации плазмид (pVIKl 12) |
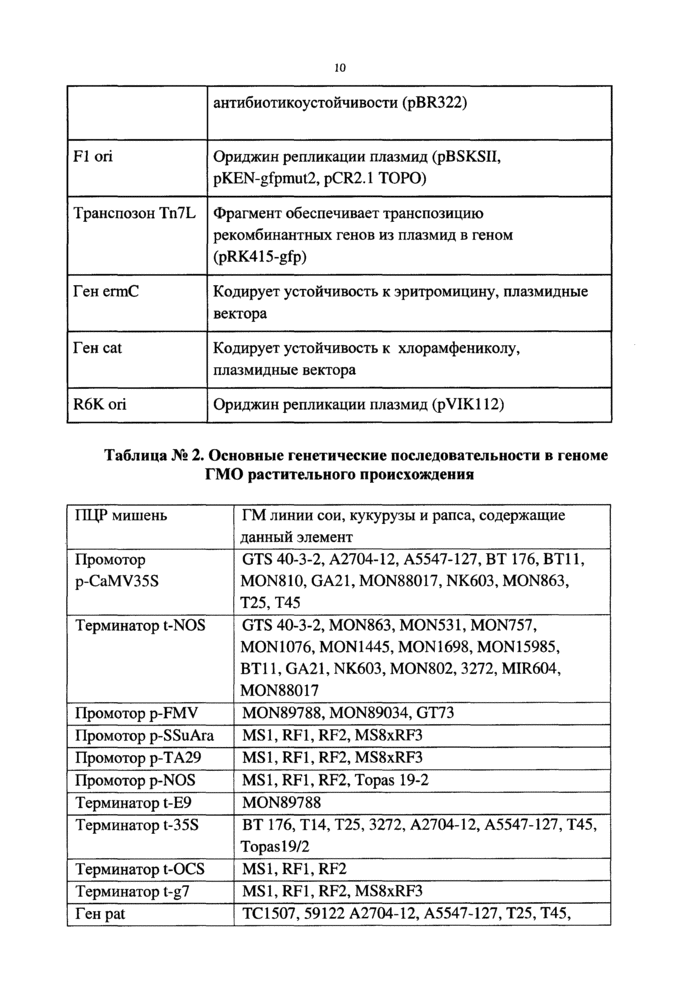
Таблица № 2. Основные генетические последовательности в геноме ГМО растительного происхождения
|
ПЦР мишень |
ГМ линии сои, кукурузы и рапса, содержащие данный элемент |
|
Промотор p-CaMV35S |
GTS 40-3-2, А2704-12, А5547-127, ВТ 176, ВТ11, MON810, GA21, MON88017, NK603, MON863, Т25, Т45 |
|
Терминатор t-NOS |
GTS 40-3-2, MON863, MON531, MON757, MON1076, MON1445, MON1698, MON15985, ВТ11, GA21, NK603, MON802, 3272, MIR604, MON88017 |
|
Промотор p-FMV |
MON89788, MON89034, GT73 |
|
Промотор p-SSuAra |
MSI, RF1, RF2, MS8xRF3 |
|
Промотор р-ТА29 |
MSI, RF1, RF2, MS8xRF3 |
|
Промотор p-NOS |
MSI, RF1, RF2, Topas 19-2 |
|
Терминатор t-E9 |
MON89788 |
|
Терминатор t-35S |
ВТ 176, T14, T25, 3272, A2704-12, A5547-127, T45, Topas 19/2 |
|
Терминатор t-OCS |
MSI, RF1, RF2 |
|
Терминатор t-g7 |
MSI, RF1, RF2, MS8xRF3 |
|
Г ен pat |
TCI507, 59122 A2704-12, A5547-127, T25, T45, |
|
ПЦР мишень |
ГМ линии сои, кукурузы и рапса, содержащие данный элемент |
|
Btl 1, DAS-59132-8, 281-24-236 Topas 19/2, DAS-44406-6, SYHT0H2, MZHGOJG, MON 87419 |
Выявление регуляторных элементов и целевых генов, используемых для получения ГМО растительного происхождения, осуществляется в соответствии с национальными и (или) межгосударственными стандартами, действующими в Российской Федерации.
Таблица № 3. Критерии эффективности методики идентификации ГМО
№
п/п
Характеристика
Описание
характеристики
Критерий
Методы оценки критерия
Специфичность
ПЦР
Способность ПЦР ПЦР тест-система
тест-системы выявлять только целевую ДНК
должна выявлять целевую ДНК.
ПЦР тест-система не должна давать ложноположительных результатов, в том числе выявлять ДНК близкородственных и неродственных биологических видов, в 100% проводимых исследований
Для оценки специфичности используют контрольные панели образцов. В состав панели входят образцы, содержащие целевую ДНК и не содержащие целевую ДНК
|
№ п/п |
__ Описание Характеристика характеристики |
Критерий |
Методы оценки критерия |
|
2 |
Чувствитель- Наименьшее |
Чувствительность |
Проводят |
|
ность ПЦР содержание копий |
должна быть не ниже |
исследования ряда | |
|
целевой ДНК, |
100 копий целевой |
десятикратных | |
|
которое может |
ДНК, например, |
разведений целевой | |
|
быть определено с |
плазмидной, в одной |
плазмидной ДНК | |
|
использованием |
ПЦР реакции |
с известной | |
|
данной ПЦР |
концентрацией | ||
|
методики, |
в двух повторах | ||
|
в первую очередь. |
каждое. Определяют | ||
|
зависит от свойств |
максимальное | ||
|
используемых |
разведение, при | ||
|
праймеров |
котором ДНК | ||
|
и зондов |
воспроизводимо | ||
|
выявляется (в двух | |||
|
повторах) |
|
№ п/п |
' Характеристика |
Описание характеристики |
Критерий |
Методы оценки критерия |
|
3 |
Эффективность ПЦР |
Характеризует прирост матрицы на каждом цикле амплификации |
Эффективность ПЦР должна быть не ниже 90%. Это соответствует значению наклона линейной области зависимости Ct от логарифма концентрации ДНК матрицы (slope): не ниже - 3,6 (приемлем диапазон slope 3,1-3,6) |
Для оценки эффективности ПЦР проводят амплификацию с рядом десятикратных разведений целевой плазм идной ДНК (пункт 2 настоящей таблицы) в двух повторах каждое. По результатам амплификации строят график зависимости Ct от логарифма концентрации ДНК 1 матрицы. Определяют наклон линейной области (slope). Эффективность ПЦР оценивают по I уравнению: Е = [10(-1/slope)]-1, в идеальном случае - при удвоении количества ПЦР продукта за один цикл: Е = 100%, (slope = -3, 32) |
|
№ п/п |
1 Характеристика |
Описание характеристики |
|
4 |
Предел |
Отражает |
|
обнаружения |
минимальное | |
|
ПЦР-тест |
количество | |
|
системы (LOD) |
биологического искомого объекта в исследуемом образце, которое может достоверно обнаружить данный метод |
i I
i
|
Критерий |
Методы оценки критерия |
|
Чем меньше искомого |
Готовят ряд |
|
биологического |
модельных образцов |
|
объекта способен |
с разным |
|
выявить метод, тем |
содержанием |
|
выше его |
целевой матрицы. |
|
чувствительность. |
Г отовят образцы |
|
Определяется |
целевого ГМО |
|
экспериментально, но |
ингредиента |
|
должен составлять не |
(от 5% до 0,001% |
|
более 0,1% |
содержания) в соответствующей матрице. Исследуют приготовленную панель с использованием |
i
i
ПЦР методики. Определяют минимальное содержание ГМО ингредиента в тотальной ДНК организма, при котором ГМО воспроизводимо выявляется (в десяти повторах)
|
№ |
Характеристика |
Описание |
Критерий |
Методы оценки |
|
п/п |
характеристики |
критерия | ||
|
5 |
Предел |
Наименьшее |
Предел должен быть |
Исследуют 10 |
|
количественного |
количество |
не более 0,1%. |
повторов 0,1 % ГМО | |
|
определения |
(концентрация) |
На пределе |
стандарта по ПЦР | |
|
(LOQ, |
вещества в |
чувствительности |
методике. | |
|
quantitation limit) |
образце, которое |
относительное |
Рассчитывают | |
|
может быть |
стандартное |
среднее значение | ||
|
количественно |
отклонение (RSD) не |
содержания ГМО | ||
|
оценено с |
должно превышать |
в образце и | ||
|
использованием |
20%. |
относительное | ||
|
методики |
Истинное значение |
стандартное | ||
|
с требуемой |
измеряемой величины |
отклонение (RSD). | ||
|
правильностью |
должно входить в |
Сравнивают | ||
|
и внутри |
полученный при |
рассчитанное | ||
|
лабораторной |
измерениях |
стандартное | ||
|
прецизионностью |
доверительный |
отклонение (RSD) | ||
|
интервал |
с критерием 20%. Также оценивают. | |||
|
_ |
входит ли истинное значение в доверительный интервал полученного среднего значения |
|
! 7 [Линейность Наличие линейной зависимости ! аналитического сигнала в I анализируемой пробе в пределах аналитической области методики. Оценивается как R2 коэффициент корреляции, определяющий верность модели линейной зависимости О от логарифма концентрации калибровочных образцов |
R2 коэффициент для Исследуют в двух калибровочных повторах 0,1 %, образцов должен быть 1,0% и 5% не менее 0,98% калибровочные ГМО стандарты по ПЦР методике. Строят калибровочную прямую (dCt от lgC), оценивают коэффициент I корреляции данных с линейной j зависимостью (R2)
|
|
№ п/п |
Характеристика |
- ■ Описание характеристики |
Критерий |
Методы оценки критерия |
|
8 ! I 1 и |
Правильность |
Правильность методики характеризуется отклонением среднего результата определений, выполненных с ее использованием, от значения, принимаемого за истинное |
Методика дает корректные результаты, если значения, принимаемые за истинные, лежат внутри доверительных интервалов соответствующих средних результатов анализов, полученных экспериментально по данной методике |
Готовят образцы из калибровочных стандартов 0,1 %, 1,0% и 5% с добавлением матриц различного происхождения (для этого смешивают стандарты с другими ингредиентами, сухим молоком, мясным фаршем, рыбной мукой). Исследуют образцы по ПЦР методике в двух повторах. Оценивают, входит ли истинное значение в диапазон погрешности полученного среднего значения для каждого образца |
При использовании методики, основанной на ПЦР, исследование включает последовательные процессы: подготовку проб, выделение нуклеиновых кислот из образцов, амплификацию заданных фрагментов нуклеиновых кислот, детекцию продуктов амплификации, анализ и интерпретацию результат.
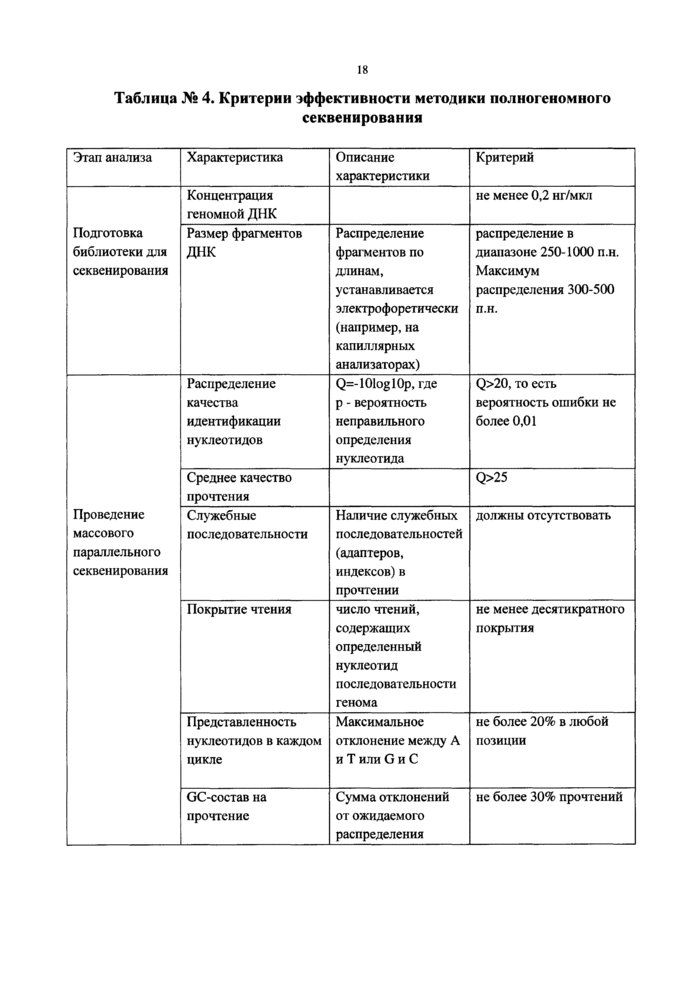
Таблица № 4. Критерии эффективности методики полногеномного
секвеннрования
|
Этап анализа |
Характеристика |
Описание характеристики |
Критерий |
|
Концентрация геномной ДНК |
не менее 0,2 нг/мкл | ||
|
Подготовка библиотеки для секвеннрования |
Размер фрагментов ДНК |
Распределение фрагментов по длинам, устанавливается электрофоретически (например, на капиллярных анализаторах) |
распределение в диапазоне 250-1000 п.н. Максимум распределения 300-500 п.н. |
|
Распределение качества идентификации нуклеотидов |
Q=-101ogl0p, где р - вероятность неправильного определения нуклеотида |
Q>20, то есть вероятность ошибки нс более 0,01 | |
|
Среднее качество прочтения |
Q>25 | ||
|
Проведение массового параллельного секвеннрования |
Служебные последовательности |
Наличие служебных последовательностей (адаптеров, индексов) в прочтении |
должны отсутствовать |
|
Покрытие чтения |
число чтений, содержащих определенный нуклеотид последовательности генома |
не менее десятикратного покрытия | |
|
Представленность нуклеотидов в каждом цикле |
Максимальное отклонение между А и Т или G и С |
не более 20% в любой позиции | |
|
GC-состав на прочтение |
Сумма отклонений от ожидаемого распределения |
не более 30% прочтений |
место депонирования и коллекционный номер (указывается для депонированных штаммов ГМО);
сведения о трансформационном событии в виде кода, сформированного согласно Общероссийскому классификатору трансформационных событий;
регистрационный номер свидетельства о государственной регистрации ГМО, предназначенного (предназначенных) для выпуска в окружающую среду, на основе которого (которых) создан ГМО, в отношении которого проведено исследование (в случае если ГМО создан на основе иного (иных) ГМО), либо указание на то, что ГМО не создан на основе иного (иных) ГМО;
регистрационный номер свидетельства о государственной регистрации ГМО для иного целевого использования (при наличии);
сведения о регистрации ГМО за рубежом (при наличии); оценку полноты документов и данных, представленных заявителем ГМО для исследования;
краткое содержание документов и данных, представленных заявителем ГМО для исследования;
описание образцов ГМО и исходного организма-реципиента, представленных заявителем ГМО для исследования, с указанием их количества, а также оценку их пригодности для проведения исследования;
выводы о результатах исследования: о молекулярно-генетической структуре ГМО, об отсутствии или наличии не заявленных генетических конструкций; об эффективности метода идентификации ГМО, сведения о соответствии генетической модификации природным (естественным) процессам;
фамилии, имена, отчества (при наличии), должности, места работы, ученые степени (при наличии) лиц, проводивших исследование; дату и номер заключения;
подпись руководителя организации (испытательной лаборатории), осуществившей проведение исследования.
4. Результаты исследования продукции оформляются заключением о результатах исследования, составляемым на основании протоколов испытаний, которое должно содержать:
наименование заключения;
полное наименование и местонахождение организации (испытательной лаборатории), осуществившей проведение исследования; наименование продукции;
полное наименование и место нахождения юридического лица, осуществляющего изготовление (поставку) продукции (далее - заявитель продукции);
регистрационный номер свидетельства о государственной регистрации ГМО, с применением которого получена продукция или который она содержит (указывается регистрационный номер свидетельства о государственной регистрации каждого ГМО, содержащегося в продукции или с применением, которого она получена);
специальные условия использования ГМО, с применением которого получена продукция или который она содержит (при наличии);
сведения о регистрации продукции за рубежом (при наличии); компонентный состав продукции, включая информацию о количестве ГМО (доля содержания в %);
оценка полноты представленных на экспертизу документов и данных, представленных заявителем продукции для исследования;
краткое содержание документов и данных, представленных заявителем продукции для исследования;
описание образцов продукции, представленных заявителем продукции для исследования, с указанием их количества, а также оценку их пригодности для проведения исследования;
выводы о наличии или отсутствии заявленного ГМО в образцах продукции; фамилии, имена, отчества (при наличии), должности, места работы, ученые степени (при наличии) лиц, проводивших исследование;
срок действия свидетельства о государственной регистрации продукции, соответствующий сроку действия свидетельства о государственной регистрации ГМО, с применением которого получена продукция или который она содержит. Если продукция получена с применением нескольких ГМО или содержит несколько ГМО, срок действия свидетельства о государственной регистрации продукции должен соответствовать минимальному сроку действия свидетельства о регистрации ГМО, с применением которого продукция получена или который продукция содержит;
дату и номер заключения;
подпись руководителя организации (испытательной лаборатории), осуществившей проведение исследования.
5. К заключению о результатах исследования ГМО или продукции должны прилагаться протоколы испытаний, на основании которых составлено соответствующее заключение, подписанные лицами, проводившими испытания.
6. Требования к проведению исследования приведены в приложении к настоящей Методике.
7. В случае если заявителем не представлены документы и данные, предусмотренные настоящей Методикой, и (или) образцы ГМО и исходного организма-реципиента или образцы продукции, пригодные для проведения
исследований, в количестве, необходимом для проведения исследований, исследование не проводится. Заявителю должен быть выдан мотивированный отказ в проведении исследования, подписанный руководителем организации (испытательной лаборатории), аккредитованной в национальной системе аккредитации, с областью аккредитации, соответствующей исследованиям, указанным в настоящей методике, в которую обратился заявитель для проведения исследования.
II. Исследование ГМО, являющихся микроорганизмами
8. В рамках исследования осуществляется анализ представленных заявителем ГМО документов и данных:
а) наименования ГМО с указанием его таксономического статуса;
б) полного наименования и места нахождения, идентификационного номера налогоплательщика (ИНН) заявителя ГМО;
в) полного наименования и место нахождения юридического лица либо фамилия, имя, отчество (при наличии), место жительства индивидуального предпринимателя - изготовителя образцов ГМО;
г) вид предполагаемого целевого использования ГМО;
д) сведений об исходном организме-реципиенте (таксономическая характеристика с указанием метода идентификации; источник выделения штамма: субстрат, географический пункт, дата выделения; методы идентификации штамма, кем идентифицирован (фамилия, имя, отчество (при наличии)), ссылка на использованные определители);
е) сведений о трансформационном событии в виде кода, сформированного согласно Общероссийскому классификатору трансформационных событий;
ж) информации об организмах-донорах вносимых генов (с указанием группы патогенности при наличии);
з) описания структуры генетической конструкции (внесенной или удаленной) и места ее локализации, характеристики встроенных или измененных генов;
и) информации о генетической модификации: описания метода модификации, структуры вектора, структуры вставки, расположения рекомбинантной ДНК (хромосома, плазмида, мобильные элементы), включая фланкирующие последовательности, включение в состав мобильных генетических элементов;
к) регистрационного номера свидетельства о государственной регистрации ГМО, предназначенного (предназначенных) для выпуска в окружающую среду, на основе которого (которых) создан ГМО, в отношении которого проводится
исследование (в случае если ГМО создан на основе иного (иных) ГМО), либо указания на то, что ГМО не создан на основе иного (иных) ГМО;
л) описания методики, позволяющей идентифицировать генетическую модификацию, в том числе описания нуклеотидных последовательностей, используемых праймеров, зондов и условий полимеразной цепной реакции (далее - ПЦР);
м) информации о месте депонирования и коллекционном номере штамма ГМО, паспорт штамма ГМО (для депонированных штаммов ГМО) либо информации о культурально-морфологических, физиолого-биохимических (ферментативных), антигенных, биологических свойствах и генетических особенностях штамма ГМО; об условиях культивирования: наименованиях питательных сред, pH среды, температуре и продолжительности выращивания, сроке хранения и периодичности пересева культуры штамма ГМО в нативной форме; о применяемом способе и условиях хранения штамма ГМО: в случае лиофилизации указывается продолжительность выращивания на питательной среде (возраст культуры), состав защитной среды, титр клеточной суспензии, режим высушивания, температура хранения, срок хранения; в случае криоконсервации указывается продолжительность выращивания на питательной среде (возраст культуры), состав защитной среды, титр клеточной суспензии, скорость замораживания (град/мин), температура хранения, срок хранения; о диссоциации культуры в зависимости от метода хранения (описание морфологических типов колоний на конкретной среде с подробным описанием типа колонии, сохраняющего полезный или диагностический признак); о среде, на которой заявителем предоставляется штамм ГМО; о количестве, дате приготовления и сроке годности образцов штамма ГМО (в случае непредоставления информации о месте депонирования и коллекционном номере штамма ГМО, паспорта штамма ГМО);
н) регистрационного номера свидетельства о государственной регистрации ГМО для иного целевого использования (при наличии);
о) информации о регистрации ГМО за рубежом (при наличии);
п) данных полногеномного секвенирования ГМО (при наличии).
Заявителем ГМО для исследования предоставляются образцы ГМО
и исходного организма-реципиента.
9. В рамках исследования осуществляются следующие испытания представленных заявителем образцов ГМО и исходного организма-реципиента:
а) проверка (валидация) методики идентификации ГМО, в том числе оценка чувствительности и специфичности данной методики в соответствии с критериями эффективности, указанными в таблице № 3 приложения к настоящей Методике;
б) подтверждение присутствия (отсутствия) заявленной генетической модификации в геноме ГМО;
в) подтверждение присутствия (отсутствия) маркерных и селективных генов в геноме ГМО, указанных в таблице № 1 приложения к настоящей Методике;
г) проведение полногеномного секвенирования ГМО, который содержится в продукции в жизнеспособном виде (в случае непредставления заявителем ГМО данных полногеномного секвенирования ГМО, представляющего собой плазмиду, бактерию, одноклеточное простейшее, животное, гриб), проведенного с использованием методики полногеномного секвенирования, соответствующей критериям эффективности, указанным в таблице № 4 приложения к настоящей Методике.
10. Полногеномное секвенирование ГМО проводится с использованием методики полногеномного секвенирования, соответствующей критериям эффективности, указанным в таблице № 4 приложения к настоящей Методике.
III. Исследование ГМО растительного происхождения
11. В рамках исследования осуществляется анализ представленных заявителем ГМО документов и данных, предусмотренных подпунктами «а» - «л» пункта 8 настоящей Методики, а также данных секвенирования вставки ГМО и бордерных последовательностей, не менее 100 нуклеотидов по флангам генома реципиента (при наличии).
Заявителем ГМО для исследования предоставляются образцы ГМО и исходного организма-реципиента.
12. В рамках исследования осуществляются следующие испытания представленных заявителем образцов ГМО и исходного организма-реципиента:
а) проверка (валидация) методики идентификации ГМО, в том числе оценка чувствительности и специфичности данной методики в соответствии с критериями эффективности, указанными в таблице № 3 приложения к настоящей Методике;
б) подтверждение присутствия (отсутствия) заявленной генетической модификации в геноме ГМО;
в) подтверждение присутствия (отсутствия) генетических последовательностей в геноме ГМО, указанных в таблице № 2 приложения к настоящей Методике.
IV. Исследование ГМО животного происхождения
13. В рамках исследования осуществляется анализ представленных заявителем ГМО документов и данных, предусмотренных подпунктами «а» - «л» пункта 8 настоящей Методики, а также данных секвенирования вставки ГМО и бордерных последовательностей, не менее 100 нуклеотидов по флангам генома реципиента (при наличии).
Заявителем ГМО для исследования предоставляются образцы ГМО и исходного организма-реципиента.
14. В рамках исследования осуществляются следующие испытания представленных заявителем образцов ГМО и исходного организма-реципиента:
а) проверка (валидация) методики идентификации ГМО, в том числе оценка чувствительности и специфичности данной методики в соответствии с критериями эффективности, указанными в таблице № 3 приложения к настоящей Методике;
б) подтверждение присутствия (отсутствия) заявленной генетической модификации в геноме ГМО;
в) подтверждение присутствия (отсутствия) незаявленных генетических последовательностей в геноме ГМО.
V. Исследование продукции
15. В рамках исследования осуществляется анализ представленных заявителем продукции документов и данных:
а) наименования продукции;
б) полного наименования и места нахождения заявителя продукции;
в) регистрационного номера свидетельства о государственной регистрации ГМО, с применением которого получена продукция или который она содержит (указывается регистрационный номер свидетельства о государственной регистрации каждого ГМО, содержащегося в продукции или с применением, которого она получена);
г) компонентного состава продукции, включая информацию
о количестве ГМО (доля содержания в %);
д) описания методики, позволяющей идентифицировать генетическую модификацию, в том числе описание нуклеотидных последовательностей, используемых праймеров, зондов, и условий ПЦР;
е) специальных условий использования ГМО, с применением которого получена продукция или который она содержит (при наличии);
ж) информации о регистрации продукции за рубежом (при наличии).
Заявителем продукции для исследования предоставляются образцы продукции.
16. В рамках исследования осуществляются следующие испытания представленных заявителем образцов продукции:
а) проведение идентификации заявленного (заявленных) ГМО в образцах продукции;
б) проведение скрининга для подтверждения присутствия заявленных генетических модификаций в образцах продукции.
Приложение
к Методике производства молекулярно-генетического исследования генно-инженерно-модифицированных организмов, используемых для производства кормов и кормовых добавок для животных, а также кормов и кормовых добавок для животных, полученных с применением таких организмов или содержащих такие организмы
Таблица № 1. Основные маркерные и селективные гены, являющиеся составляющими частями генно-инженерных конструкций микроорганизмов
|
Мишень |
Описание |
|
Ген LacZ |
Кодирует фермент b-галактозидазу. Используется в векторных плазмидных конструкциях (pCR2.1TOPO, pVIKl 12, pBSKSII), включает область полилинкера для клонирования рекомбинантных генов. При наличии данного фермента бесцветный субстрат X-gal превращается в окрашенный продукт, бактериальные колонии, экспрессирующие LacZ, имеют голубой цвет |
|
Г ен gfp |
Г ен зеленого флуоресцентного белка используется в ряде векторных плазмид для генно-инженерных манипуляций (pKEN-gfpmut2, pRK415-gfp) в качестве светящейся метки |
|
Ген amp |
Кодирует устойчивость к ампициллину, используется в ряде векторных плазмид для селекции по антибиотикоустойчивости (pBR322, pUC18, pBSKSII, pET,pCR2.1 ТОРО) |
|
Ген Km |
Кодирует устойчивость к канамицину, используется в ряде векторных плазмид для селекции по антибиотикоустойчивости (pVIKl 12, рМС212) |
|
Г ен tetO |
Кодирует устойчивость к тетрациклину, используется в ряде векторных плазмид для селекции по |