ГОСТ ISO 17993-2016
Качество воды. Определение 15-ти полициклических ароматических углеводородов (ПАУ). Метод высокоэффективной жидкостной хроматографии с флуоресцентным детектированием после экстракции жидкость-жидкость
Устанавливает метод высокоэффективной жидкостной хроматографии (ВЭЖХ) с флуоресцентным детектированием после экстракции жидкость-жидкость для определения 15-ти полициклических ароматических углеводородов (ПАУ) в питьевой, поверхностной и подземных водах в массовых концентрациях более 0,005 мкг/куб.дм (для каждого отдельного соединения) и в поверхностных водах в массовой концентрации выше 0,01 мкг/куб.дм.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Принцип метода
4 Влияющие факторы
5 Реактивы
6 Оборудование
7 Отбор проб
8 Порядок работы
9 Расчет результатов
10 Прецизионность
11 Отчет об испытаниях
Приложение А (справочное) Примеры хроматографических условий и колонок
Приложение В (справочное) Примеры конструкции специального оборудования
Приложение Д.А (справочное) Сведения о соответствии государственного стандарта ссылочному международному стандарту
25 страниц
| Дата введения | 04.01.2018 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Организации:
| 20.04.2016 | Утвержден | Евразийский совет по стандартизации, метрологии и сертификации | 87-П |
|---|---|---|---|
| 14.10.2016 | Утвержден | Госстандарт Республики Беларусь | 79 |
| Разработан | БелГИМ | ||
| Издан | БелГИСС | 2016 г. |
Water quality. Determination of 15 polycyclic aromatic hydrocarbons (PAH) in water by HPLC with fluorescence detection after liquid-liquid extraction
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1
стр. 2

стр. 3

стр. 4

стр. 5

стр. 6
стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14
стр. 15
стр. 16
стр. 17

стр. 18

стр. 19

стр. 20

стр. 21
стр. 22

стр. 23

стр. 24

стр. 25
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
КАЧЕСТВО ВОДЫ
Определение 15-ти полициклических ароматических углеводородов (ПАУ).
Метод высокоэффективной жидкостной хроматографии с флуоресцентным детектированием после экстракции жидкость-жидкость
ЯКАСЦЬ ВАДЫ
Вызначэне 15-щ полщыкл1чных араматычных вуглевадародау (ПАВ).
Метад высокаэфектыунай вадкаснай храматаграфМ з флуарэсцэнтным дэтэктыраваннем пасля экстракцьм вадкасць-вадкасць
(ISO 17993:2002, ЮТ)
Издание официальное
Г осстандарт Минск
(ИБ
Предисловие
Евразийский совет по стандартизации, метрологии и сертификации (ЕАСС) представляет собой региональное объединение национальных органов по стандартизации государств, входящих в Содружество Независимых Государств. В дальнейшем возможно вступление в ЕАСС национальных органов по стандартизации других государств.
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения,обновления и отмены».
Сведения о стандарте
1 ПОДГОТОВЛЕН республиканским унитарным предприятием «Белорусский государственный институт метрологии» (БелГИМ)
2 ВНЕСЕН Госстандартом Республики Беларусь
3 ПРИНЯТ Евразийским советом по стандартизации, метрологии и сертификации (протокол № 87-П от 20 апреля 2016 г.) 1
|
За принятие стандарта проголосовали: | |||||||||||||||||||||||||||
|
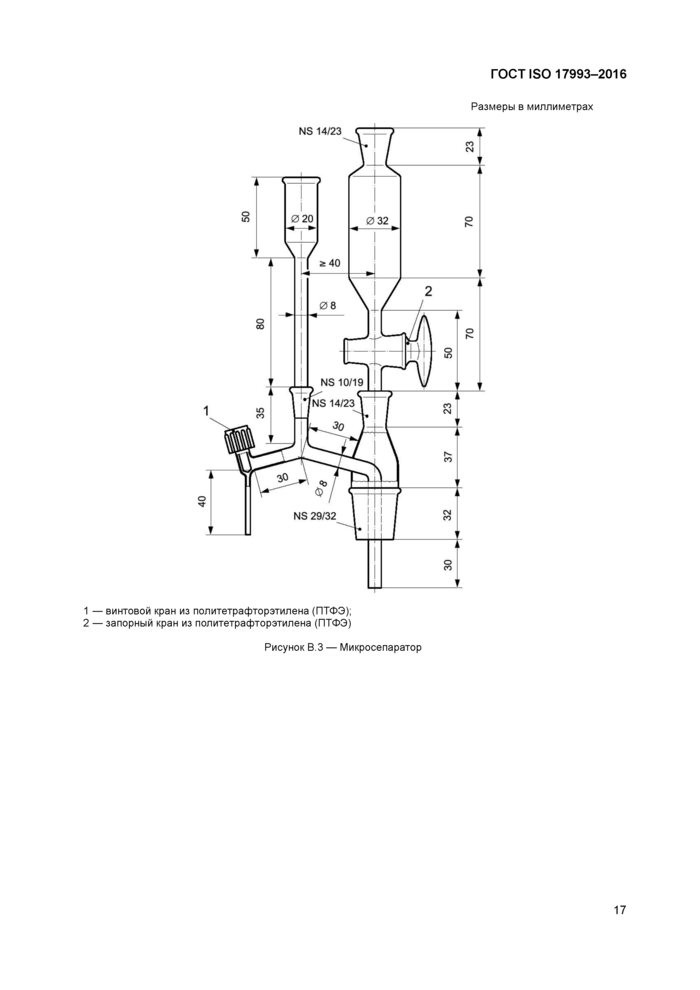
В пробу помещают перемешивающий стержень и бутыль закрывают крышкой. Затем тщательно перемешивают анализируемую пробу, используя магнитную мешалку (6.2) при установленных максимальных параметрах (1000 мин"1) в течение 60 мин. Затем пробу переносят в делительную воронку (6.3) и позволяют фазам разделиться в течение как минимум 5 мин. Разделение гексана с водой также может быть проведено с использованием микросепаратора (пример приведен на рисунке В.З).
Если в течение процесса экстракции образуется стойкая эмульсия, ее собирают в центрифужную пробирку (6.14) и центрифугируют в течение 10 мин при 3000 мин'1. Воду удаляют пипеткой Пастера (6.8), экстракт переносят в коническую колбу объемом 100 см3 (6.4). Экстракт высушивают в соответствии с 8.2.
Для экстракции проб сточных вод, а также проб воды с большим содержанием ПАУ, гомогенизированную пробу объемом 10-100 см3 переносят в коническую колбу объемом 250 см3 (6.4) с помощью пипетки и разбавляют водой до 200 см3. Затем добавляют 25 см3 гексана (5.1.2) и продолжают процедуру, описанную выше.
8.2 Высушивание экстракта
Экстракт пробы в гексане, полученный в соответствии с 8.1, переносят в коническую колбу объемом 100 см3 (6.4). Делительную воронку и центрифужную пробирку ополаскивают 5 см3 гексана (5.1.2) и добавляют к экстракту.
Экстракт высушивают с помощью сульфата натрия (5.3) интенсивным встряхиванием в течение не менее 30 мин.
Высушенный экстракт декантируют в концентрационную колбу (6.6). Коническую колбу дважды ополаскивают 5 см3 гексана (5.1.2) и добавляют в концентрационную колбу.
8.3 Обогащение
Высушенный экстракт пробы в гексане, полученный в соответствии с 8.2, выпаривают, например, при помощи роторного испарителя (6.9) с температурой бани 30 °С и постепенным понижением давления до 200 гПа до тех пор, пока экстракт не останется только в коническом дне концентрационной колбы (что соответствует объему около 2 см3).
Нельзя выпаривать экстракты досуха, поскольку это может привести к потере соединений, в структуру которых входит 2 или 3 кольца.
Осадок, образующийся на стенках стекла, растворяют при помощи шейкирующего устройства (6.10).
Очистку экстрактов проб сточных вод и проб неизвестной природы проводят методом, приведенным в 8.4.
В сконцентрированный экстракт добавляют 250 мм3 N, N-диметилформамида (5.1.2), затем 500 мм3 ацетона (5.1.2) и гомогенизируют смесь. Для гомогенизации вместо ацетона можно использовать дихпорметан (5.1.2) после добавления N, N-диметилформамида.
Гексан и ацетон полностью выдувают в слабом потоке азота (5.4), чтобы довести объем экстракта до 200-250 мм3. Обогащенный экстракт не должен содержать следовые количества гексана или ацетона, так как присутствие этих растворителей в анализируемом образце приводит к появлению мешающего влияния при анализе методом ВЭЖХ (4.2).
Экстракт доводят до известного объема (например, 2 см3) растворителем, который используется для приготовления рабочих стандартных растворов (5.9). Во избежание расширения формы пиков на хроматограмме объемная доля диметилформамида не должна превышать 20 %.
Обогащенный экстракт переносят в стеклянную пробирку для автодозатора (6.12), а при необходимости экстракт фильтруют через микрофильтр (6.11). Экстракт хранят в прохладном и темном месте до выполнения анализа.
8.4 Очистка экстракта
Для очистки экстракта используют колонки (пипетки Пастера (6.8)) или картриджи (6.13), заполненные не менее 0,5 г силикагеля (5.5). Силикагель в колонке или картридже промывают пятикратным объемом смеси дихпорметана/гексана (1:1), промывают таким же объемом гексана (5.1.2), не позволяя силикагелю высохнуть.
Растворители, используемые для очистки экстракта, высушивают с помощью активированных молекулярных сит (5.6).
Экстракт пробы в гексане (8.3) концентрируют до объема (500 ± 50) мм3 в слабом потоке азота (5.4).
Концентрированный экстракт переносят при помощи пипетки Пастера (6.8) на промытый гексаном силикагель и позволяют экстракту осесть на нем. Собирают элюат в стеклянную пробирку (6.14). 2
Концентрационную колбу ополаскивают 500 мм3 гексана (5.1.2), этот раствор переносят на колонку, позволяя ему осесть на частицах силикагеля.
ПАУ элюируют из колонки смесью дихлорметана/гексана (1 : 1). Картриджи, содержащие 0,5 г силикагеля, для элюирования ПАУ промывают смесью дихлорметана/гексана (1:1) объемом не менее 3 см3.
Можно использовать другие смеси растворителей-элюентов, если они обеспечивают такое же или лучшее извлечение.
К элюату добавляют 250 мм3 N, Л/-диметиформамида (5.1.2), смесь гомогенизируют встряхиванием и концентрируют (8.3) до объема 2 см3 с использованием, например, роторного испарителя (6.9), а затем потока азота (5.4) — до объема 200-250 мм3.
Экстракт разбавляют до известного объема (например, 2 см3) таким же растворителем, который используется для приготовления рабочих стандартных растворов (5.9).
8.5 Условия работы ВЭЖХ8.5.1 Общие положения
Систему ВЭЖХ настраивают в соответствии с инструкциями фирмы-производителя. Регулярно контролируют шум и дрейф нулевой линии на соответствие спецификации изготовителя. Если результаты испытаний не удовлетворяют допустимым величинам, необходимо выявить и устранить причины.
8.5.2 Хроматографическое разделение
Используют колонку и хроматографические условия, обеспечивающие эффективное разделение. Для выбора колонок и соответствующих градиентов (см. приложение А).
R
О)
А, В
Величину разрешения RAB между двумя хроматографическими пиками для соединений А и В определяют по формуле
где frA, frB — соответствующее время удерживания соединений А и В, выраженное в минутах
(/г,А > /г,в);
wb,A’wb,B — соответствующая ширина оснований пиков соединений А и В, выраженная в минутах.
Необходимо обеспечить такое разделение аценафтена (ас) и флуорена (П), чтобы величина разрешения Racf| = 1. Величина разрешения для остальных соединений RAB = 1,5. Величина разрешения хроматографических пиков, для которых происходило изменение длины волны и/или затухание сигнала, должна быть по крайней мере 2,5. Для обеспечения повторяемости результатов разделение производят при постоянной температуре (±0,5 °С).
Разделение бензо(дЫ)перилена и индено(1,2,3-сс1)пирена можно улучшить оптимизацией температуры колонки.
Максимальный объем инжекции зависит от внутреннего диаметра хроматографической колонки. Объем инжекции выбирают так, чтобы степень расширения сигнала была минимальной (типичная инжекция 10 мм3 для колонки с внутренним диаметром 3 мм).
Для разделения шести ПАУ, указанных в руководстве ЕС для питьевой воды, можно использовать изократический режим элюирования (рисунок А.3).
8.5.3 Детектирование
Для детектирования применяют флуоресцентный детектор, выбирают длины волн возбуждения и испускания, обеспечивающие соответствующие чувствительность и селективность. Типичная программа для длин волн представлена в таблице А.1.
При программировании длины волны следует избегать появления помех нулевой линии. Поэтому изменения в программу вносят тогда, когда величина разрешения между пиками составляет как минимум 2,5 (8.5.2).
Растворенный в элюенте кислород может вызвать уменьшение флуоресцентного сигнала, т. е. изменения концентрации кислорода влияет на воспроизводимость. Содержание кислорода в элюенте должно быть минимальным и постоянным, что достигается дегазацией элюента, например при помощи гелия или вакуума.
Изменение длины волны производят в момент, когда флуоресценция низкая. При высоком сигнале флуоресценции изменение длины волны может привести к смещению нулевой линии. После изменения длины волны повторная настройка нулевой линии влияет на параметры интегрирования и, следовательно, на результаты количественного анализа. Для обеспечения постоянной высоты пика можно изме- 3
нить длину волны и ослабление сигнала одновременно. Условия ослабления сигнала являются одними из критериев детектирования, которые не должны изменяться после калибровки. Если ослабление низкое, результирующее увеличение шума не должно привести к ухудшению интегрирования сигнала.
8.5.4 Идентификация индивидуальных соединений
Отсутствие пика на характеристическом для него времени удерживания при нормальной по всем другим аспектам хроматограмме предполагает отсутствие данного соединения в пробе. Если время удерживания соединения на хроматограмме анализируемой пробы совпадает с временем удерживания соединения на хроматограмме стандартного раствора, которая получена при тех же условиях (допустимое значение ±1 %, максимум 10 с), то предполагают, что данное соединение в пробе присутствует.
При необходимости результат проверяют одним из следующих методов:
- сравнением спектров возбуждения и испускания соединения в анализируемой пробе с такими же спектрами соединения в стандартном растворе при совпадении времени удерживания при тех же условиях;
- при более высоких концентрациях используется другой детектор, который не является причиной мешающего действия расширения флуоресцентного пика, например фотодиодная матрица, и сравниваются спектры поглощения веществ в анализируемой пробе и в стандартном растворе;
- применяя независимый метод, например газовую хроматографию.
8.6 Калибровка8.6.1 Общие положения
При оценке достоверности калибровки различают начальную калибровку, стандартную калибровку и стандартный контроль калибровки.
Начальную калибровку выполняют для определения рабочего диапазона концентраций и линейности функции калибровки в соответствии с ISO 8466-1, например, когда метод ВЭЖХ применяют впервые. В результате устанавливают окончательный рабочий диапазон концентраций и проводят стандартную калибровку. Эту калибровку необходимо повторять после технического обслуживания (например, замены колонки), после ремонта системы ВЭЖХ и в случае, если система не была в эксплуатации в течение длительного времени, а также при несоответствии критериям текущего контроля.
Проверка правильности начальной калибровки проводится с помощью стандартного контроля калибровки в каждой серии анализируемых проб.
8.6.2 Начальная калибровка
Предварительный рабочий диапазон калибровки устанавливают в результате анализа как минимум пяти рабочих стандартных растворов (5.9). Проверку линейности калибровки осуществляют в соответствии с ISO 8466-1.
8.6.3 Стандартная калибровка
После установления конечного рабочего диапазона калибровки анализируют не менее пяти рабочих стандартных калибровочных смесей (5.9). Рассчитывают функцию калибровки путем анализа линейной регрессии скорректированных площадей пиков. Фактическую чувствительность метода можно оценить по рассчитанной функции регрессии.
8.6.4 Стандартный контроль калибровки
Стандартный контроль проводят для того, чтобы установить, достоверна ли функция калибровки. Для этого анализируют один стандартный раствор после десяти испытуемых проб каждой аналитической серии. Концентрация этого стандартного раствора должна быть в пределах от 40 % до 80 % рабочего диапазона калибровки. Функцию калибровки считают достоверной, если результат не отклоняется более чем на 10 % от рабочей калибровочной кривой. Если это требование не выполняется, проводят перекалибровку системы в соответствии с 8.6.3.
8.7 Определение
Перед анализом проб систему ВЭЖХ стабилизируют и настраивают программу для длин волн в соответствии с найденными временами удерживания.
Примечание — Воспроизводимые значения времен удерживания обычно получают после двух или трех инжекций стандартного раствора (5.9).
Проводят анализ исследуемой пробы, калибровочных растворов и холостой пробы методом ВЭЖХ.
Пики каждой исследуемой пробы должны быть правильно проинтегрированы, при необходимости делают корректировку.
Если рассчитанная массовая концентрация вещества в испытуемой пробе превышает калибровочный диапазон, пробу разбавляют и повторяют измерение.
8.8 Извлечение
К 1000 см3 воды добавляют, например, 2 см3 рабочего стандартного раствора, приготовленного в соответствии с 5.9, и далее действуют как приведено в 8.1-8.5.
Определение извлечения ПАУ в пробах поверхностных вод проводят по методу стандартных добавок.
Среднее значение извлечения вещества /, rf, определяют по формулам:
П,;л,=^, (2)
Pi,Nsp
п
iN
п,- = ——, (3)
п
гДе "П/.л/
Р/,Л/са1
pi, Л/sp П
— извлечение вещества / при концентрационном уровне /V;
— измеренная массовая концентрация вещества / при концентрационном уровне N и рассчитанная с использованием функции калибровки, мкг/дм3;
— массовая концентрация добавки вещества / при концентрационном уровне Л/, мкг/дм3;
— число концентрационных уровней.
Для метода экстракции, приведенного в 8.1-8.5, среднее извлечение составляет 95 %. При выполнении этого условия поправочный коэффициент для извлечения д может быть опущен (раздел 9).
8.9 Измерение холостой пробы
Для контроля реактивов и правильности работы прибора регулярно проводят измерения холостых проб, анализируя 1000 см3 воды, не содержащей ПАУ, обработанной в соответствии с 8.1-8.5.
Если в холостых пробах обнаруживают любое из анализируемых веществ, выявляют причину и устраняют любые источники загрязнения.
9 Расчет результатов
Массовую концентрацию вещества /, по формуле (4)
р, в пробе воды, выраженную в мкг/дм3, рассчитывают
(У;-Ь;)Уе^
где у, — измеренная величина сигнала вещества /, выраженная, например, как площадь пика;
a, —угол наклона функции калибровки вещества /, так называемый фактор отклика данного ве
щества, выраженный, например, как площадь пика/(пг/мм3);
b, - — отрезок, отсекаемый функцией калибровки на оси ординат, выраженный, например, как
площадь пика;
Ve — объем экстракта, из которого была сделана инжекция, см3;
Vs — объем анализируемой пробы, см3; д, — среднее значение извлечения.
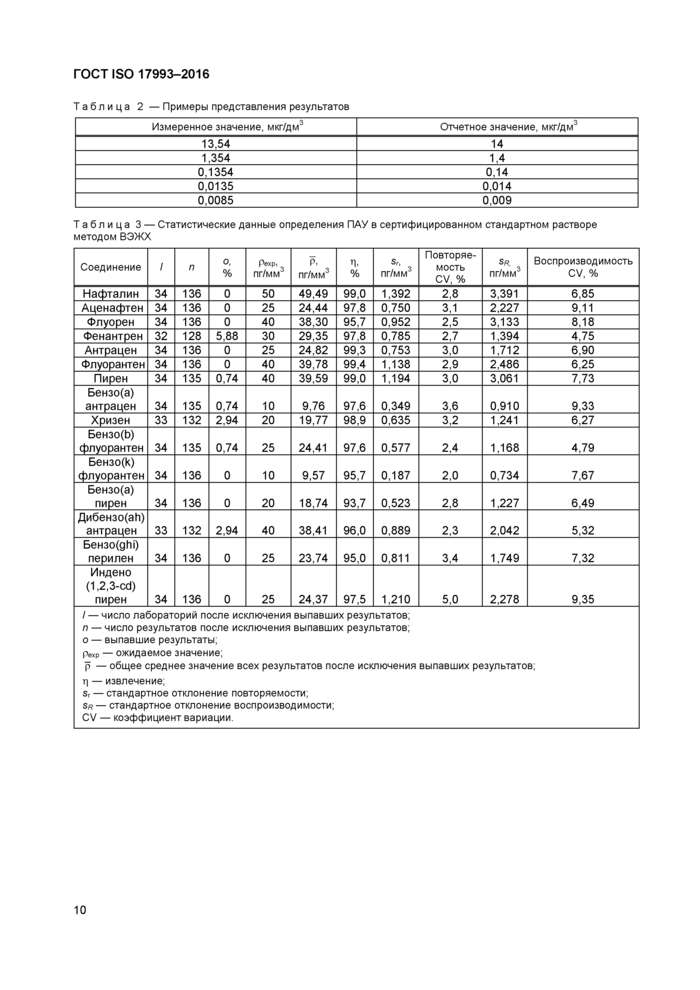
В отчете указывают массовую концентрацию ПАУ, мкг/дм3, с точностью не более двух значащих цифр. Для массовых концентраций < 0,01 мкг/л производят округление до самого близкого к 0,0001 мкг/дм3 значения. Примеры округления результатов приведены в таблице 2.
10 Прецизионность
Статистические данные, полученные по результатам межпабораторных испытаний, выполненных в Германии в 1996 г., представлены в таблицах 3 и 4. 4
|
Таблица 2 — Примеры представления результатов | ||||||||||||
|
|
Таблица 3 — Статистические данные определения ПАУ в сертифицированном стандартном растворе методом ВЭЖХ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10
|
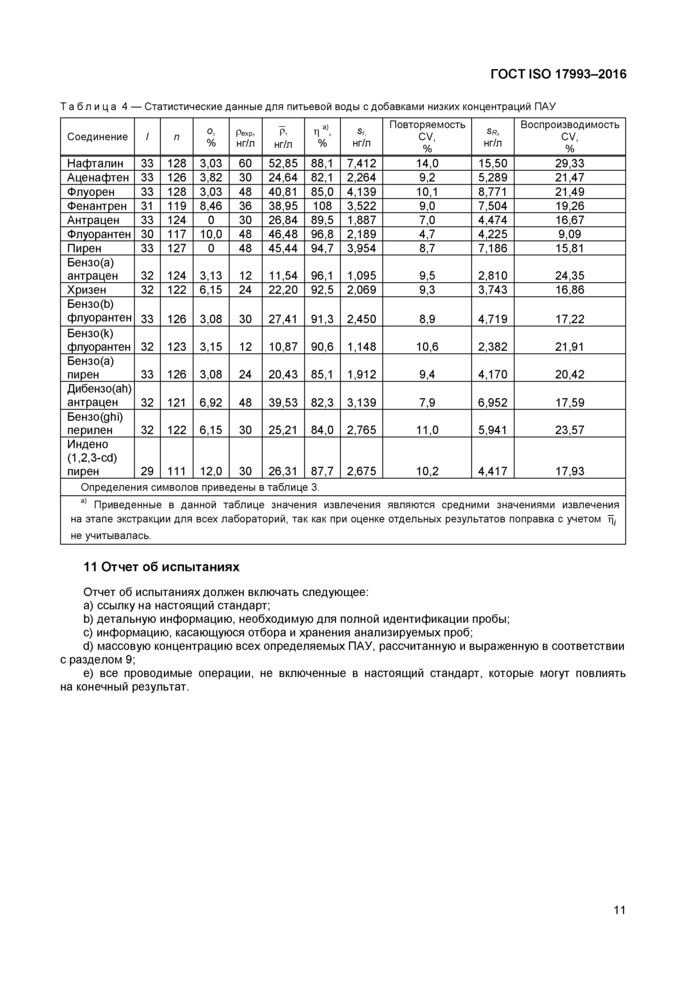
Таблица 4 — Статистические данные для питьевой воды с добавками низких концентраций ПАУ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
11 Отчет об испытаниях | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Отчет об испытаниях должен включать следующее:
a) ссылку на настоящий стандарт;
b) детальную информацию, необходимую для полной идентификации пробы;
c) информацию, касающуюся отбора и хранения анализируемых проб;
d) массовую концентрацию всех определяемых ПАУ, рассчитанную и выраженную в соответствии с разделом 9;
e) все проводимые операции, не включенные в настоящий стандарт, которые могут повлиять на конечный результат.
11
Приложение А (справочное)
Примеры хроматографических условий и колонок
Два примера (А и Б) хроматографических условий ВЭЖХ, программа градиентного элюирования и колонки, позволяющие разделять 16 ПАУ, приведены на рисунках А.1 и А.2. Типичные хроматограммы, полученные при этих условиях, также приведены на рисунках А.1 и А.2. Программируемые длины волн, используемые в этих хроматографических условиях и хроматограммах А и Б, представлены в таблице А.1.
а) Дополнительный компонент.
Третий пример хроматографических условий ВЭЖХ, условий работы детектора и колонок, при которых могут разделяться ПАУ, находящиеся в питьевой воде, а также типичная хроматограмма приведены на рисунке А.З. Для этого разделения использован изократический режим.
|
Таблица А.1 —Программируемые длины волны для хроматограмм А и Б | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Инструмент ВЭЖХ: HEWLETT-PACKARD HP 1046 FLD, щелевой; возбуждение: 12,5 нм; испускание: 25 нм. Примечание — Инструмент HP 1046 FLD приведен в качестве примера подходящей и коммерчески доступной системы ВЭЖХ с флуоресцентным детектором. Эта информация предоставляется для удобства пользователей настоящего стандарта и не является подтверждением ISO качества данной продукции. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
12
|
12 |
Идентификация пиков
1 — нафталин;
2 — аценафтен;
3 — флуорен;
4 — фенантрен;
5 — антрацен;
6 — флуорантен;
7 — пирен;
8 — бензо(а) антрацен;
9 — хризен;
10 — 6-метилхризен;
11 — бензо(Ь)флуорантен;
12 — бензо(к)флуорантен;
13 — бензо(а)пирен;
14 — дибензо(а1з)антрацен;
15 — бензо(дЫ)перилен;
16 — индено(1,2,3-сс1)пирен
Операционные условия
Инжекция: 5 мм3 калибровочного раствора с р, = 100 пг/мм3.
Колонка: «Bakerbond РАН 16 plus» длиной 250 мм и диаметром 3 мм.
Скорость потока растворителя: 0,5 см3/мин.
Температура: 25 °С.
Программа градиентного элюирования:
Время, мин: 0 5 35 45
Соотношение объемов: 50:50 50:50 100:00 100:00
Градиент: Начальные Изократический Линейный Изократический
условия
Элюент: Ацетонитрил/вода
Примечание — Колонка «Bakerboard РАН 16 plus» приведена в качестве примера подходящего и коммерчески доступного материала. Эта информация предоставляется для удобства пользователей настоящего стандарта и не является подтверждением ISO качества данной продукции.
Рисунок А. 1 —Хроматограмма А
13
Идентификация пиковa) t, мин 1 — нафталин; 2 — аценафтен; 3 — флуорен; 4 — фенантрен; 5 — антрацен; 6 — флуорантен; 7 — пирен; 8 — бензо(а)антрацен; |
9 — хризен; 10 — 6-метилхризен; 11 — бензо(Ь)флуорантен; 12 — бензо(к)флуорантен; 13 — бензо(а)пирен; 14 — дибензо(а1з)антрацен; 15 — бензо(дЫ)перилен; 16 — индено(1,2,3-сс1)пирен |
Операционные условия
Инжекция: 5 мм3 калибровочного раствора с р, = 100 пг/мм3. Колонка: «Nucleosil 5 С18 РАН» длиной 250 мм и диаметром 3 мм. Скорость потока растворителя: 0,5 см3/мин.
Температура: 25 °С.
45 100 : 00
Изократический
Программа градиентного элюирования:
Время, мин: 0 35
Соотношение объемов: 60:40 100:00
Градиент: Начальные условия Линейный
Элюент: Ацетон итрил/вода
Примечание — Колонка «Nucleosil 5 С18 РАН» приведена в качестве примера подходящего и коммерчески доступного материала. Эта информация предоставляется для удобства пользователей настоящего стандарта и не является подтверждением ISO качества данной продукции.
Рисунок А.2 — Хроматограмма Б
14
|
Р |
Идентификация пиков
1 — флуорантен;
2 — бензо(Ь)флуорантен;
3 — бензо(к)флуорантен;
4 — бензо(а)пирен;
5 — бензо(дЫ)перилен;
6 — индено(1,2,3-сс1)пирен;
7 — перилен
Операционные условия
Инжекция: 5 мм3 калибровочного раствора с р, = 100 пг/мм3.
Колонка: «Bakerbond РАН 16 plus» длиной 250 мм и диаметром 3 мм.
Скорость потока растворителя: 0,5 см3/мин.
Температура: 20 °С.
Изократическая программа: соотношение объемов: 50 : 50.
Элюент: ацетонитрил/вода.
Детектирование: длина волны возбуждения: 365 нм, щель 25 нм;
длина волны испускания: 470 нм, щель 50 нм.
Примечание — Колонка «Bakerboard РАН 16 plus» приведена в качестве примера подходящего и коммерчески доступного материала. Эта информация предоставляется для удобства пользователей настоящего стандарта и не является подтверждением ISO качества данной продукции.
Рисунок А.З —Хроматограмма С разделения ПАУ, обнаруженных в питьевой воде
15
5 ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 14 октября 2016 г. № 79 непосредственно в качестве государственного стандарта Республики Беларусь с 1 мая 2017 г.
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных (государственных) стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных (государственных) органов по стандартизации.
Приложение В (справочное)
Примеры конструкции специального оборудования
Примеры конструкции специального оборудования приведены на рисунках В.1-В.З.
Размеры в миллиметрах
NS 14/23
а — общий градуированный объем 2 см3 с ценой деления 0,1 см3.
Рисунок В.1 — Колба для концентрирования
Размеры в миллиметрах
Рисунок В.2 — Центрифужная пробирка с коническим дном и закручивающейся крышкой
16
Содержание
1 Область применения...........................................................................................................................1
2 Нормативные ссылки...........................................................................................................................1
3 Принцип метода...................................................................................................................................1
4 Влияющие факторы.............................................................................................................................3
5 Реактивы...............................................................................................................................................3
6 Оборудование......................................................................................................................................4
7 Отбор проб............................................................................................................................................5
8 Порядок работы....................................................................................................................................5
9 Расчет результатов..............................................................................................................................9
10 Прецизионность....................................................................................................................................9
11 Отчет об испытаниях..........................................................................................................................11
Приложение А (справочное) Примеры хроматографических условий и колонок..............................12
Приложение В (справочное) Примеры конструкции специального оборудования...........................16
Приложение Д.А (справочное) Сведения о соответствии государственного стандарта
ссылочному международному стандарту.................................................................18
IV
Введение
Полициклические ароматические углеводороды (ПАУ) встречаются практически во всех видах вод.
Эти соединения адсорбируются на твердой фазе (донные отложения, взвешенные вещества), а также растворяются в жидкой фазе.
Некоторые ПАУ могут вызывать онкологические заболевания. Согласно Директиве 98/83/ЕС по качеству воды максимально допустимый уровень бензо(а)пирена — 0,010 мкг/дм3, а суммы содержания четырех ПАУ [бензо(Ь)флуорантена, бензо(к)флуорантена, бензо(дЫ)перилена, индено(1,2,3-cd)-пирена] — 0,100 мкг/дм3
Предупреждение. Некоторые определяемые соединения предположительно могут быть канцерогенами. Ацетонитрил и гексан токсичны. Лица, использующие настоящий стандарт, должны быть знакомы со стандартной лабораторной практикой. Настоящий стандарт не ставит своей целью решение всех проблем безопасности, сопряженных с его использованием. Организация надлежащей практики обеспечения безопасности, охраны труда и обеспечения соответствия национальным законодательным актам относится к сфере ответственности пользователя.
V
_ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ_
КАЧЕСТВО ВОДЫ
Определение 15-ти полициклических ароматических углеводородов (ПАУ). Метод высокоэффективной жидкостной хроматографии с флуоресцентным детектированием после экстракции жидкость-жидкость
ЯКАСЦЬ ВАДЫ
Вызначэне 15-ф полщыктчных араматычных вуглевадародау (ПАВ) Метад высокаэфектыунай вадкаснай храматаграфм з флуарэсцэнтным дэтэктыраваннем пасля экстракцьм вадкасць-вадкасць
Water quality
Determination of 15 polycyclic aromatic hydrocarbons (PAH) in water by HPLC with fluorescence detection after liquid-liquid extraction
Дата введения — 2017-05-01
1 Область применения
Настоящий стандарт устанавливает метод высокоэффективной жидкостной хроматографии (далее — ВЭЖХ) с флуоресцентным детектированием после экстракции жидкость-жидкость для определения 15-ти полициклических ароматических углеводородов (далее — ПАУ) (см. таблицу 1) в питьевой, поверхностной и подземных водах в массовых концентрациях более 0,005 мкг/дм3 (для каждого отдельного соединения) и в поверхностных водах в массовой концентрации выше 0,01 мкг/дм3.
С некоторыми модификациями этот метод применяется для анализа сточных вод.
Метод применим для других ПАУ при условии проверки правильности метода для каждого случая.
2 Нормативные ссылки
Для применения настоящего стандарта необходимы следующие ссылочные стандарты. Для недатированных ссылок применяют последнее издание ссылочного стандарта (включая все его изменения).
ISO 5667-1:2006* Water quality — Sampling — Part 1: Guidance on the design of sampling programmes and sampling techniques (Качество воды. Отбор проб. Часть 1. Руководство по составлению программ и методик отбора проб)
ISO 5667-3:2012 Water quality — Sampling — Part 3: Preservation and handling of water samples (Качество воды. Отбор проб. Часть 3. Консервация и обработка проб воды)
ISO 8466-1:1990 Water quality — Calibration and evaluation of analytical methods and estimation of performance characteristics — Part 1: Statistical evaluation of the linear calibration function (Качество воды. Калибровка и оценка аналитических методов и определение эксплуатационных характеристик. Часть 1. Статистический метод оценки линейной калибровочной функции)
3 Принцип метода
Присутствующие в воде ПАУ извлекают гексаном. Экстракт концентрируется выпариванием, затем гексан заменяется на растворитель, используемый для анализа методом ВЭЖХ.
При необходимости экстракты поверхностных или других более загрязненных вод перед анализом очищаются на силикагеле.
* Действует взамен ISO 5667-2:1991.
Издание официальное
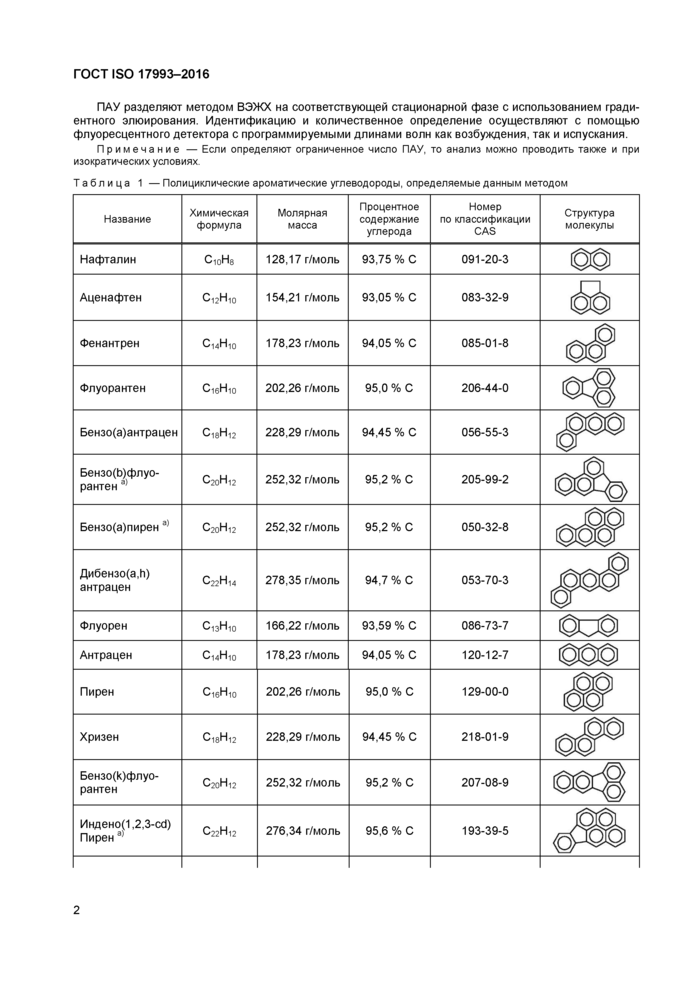
ПАУ разделяют методом ВЭЖХ на соответствующей стационарной фазе с использованием градиентного элюирования. Идентификацию и количественное определение осуществляют с помощью флуоресцентного детектора с программируемыми длинами волн как возбуждения, так и испускания.
Примечание — Если определяют ограниченное число ПАУ, то анализ можно проводить также и при изократических условиях.
|
Таблица 1 — Полициклические ароматические углеводороды, определяемые данным методом | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Окончание таблицы 1 | ||||||||||||||||||||||||
| ||||||||||||||||||||||||
4 Влияющие факторы
4.1 Отбор проб и экстракция
Для отбора проб используют посуду, изготовленную из материалов (предпочтительно сталь или стекло), которые не оказывают влияния на пробу. Необходимо избегать контакта с пластмассой и другими органическими материалами во время отбора проб, их хранения и экстракции.
При использовании автоматических пробоотборников нельзя применять резиновые или силиконовые трубки. Если невозможно избежать использования этих материалов, то контакт с ними необходимо свести к минимуму. Перед отбором пробы пробоотборное оборудование промывают отбираемой водой.
В качестве руководства используют ISO 5667-1 и ISO 5667-3.
Анализируемые пробы хранятся в местах, защищенных от прямого солнечного света и длительного воздействия света. Во время хранения проб возможны потери ПАУ вследствие адсорбции на стенках сосудов. Величина потерь зависит от продолжительности хранения.
4.2 Высокоэффективная жидкостная хроматография (ВЭЖХ)
Соединения, которые флуоресцируют, ослабляют сигнал и совместно элюируются с анализируемыми ПАУ, создают помехи при их определении. Эти влияющие факторы могут привести к недостаточному разрешению сигнала, что ведет к наложению пиков, и в зависимости от их величины могут повлиять на точность и прецизионность аналитических результатов. Пики несимметричной формы, а также более широкие, чем пики эталонных соединений свидетельствуют о мешающем влиянии. Такая проблема может возникнуть для нафталина и фенантрена в зависимости от селективности используемых фаз колонок.
Неполное удаление используемых при пробоподготовке растворителей (гексана, ацетона, хлористого метилена) может стать причиной плохой воспроизводимости времени удерживания, расширения формы пиков или появления двойных пиков, особенно в случае ПАУ, имеющих в своей структуре 2 или 3 кольца.
Разделение пиков дибензо(аб)антрацена и индено(1,2,3-сс1)пирена может быть критичным.
При неполном разрешении проверяется и, если необходимо, корректируется интегрирование пиков.
Обычно наблюдается плохое разрешение пиков перилена и бензо(Ь)флуорантена, но при выборе селективной длины волны (см. таблицу А.1) пик перилена гасится.
Так как перилен определяется изократическим методом для оценки ПАУ в питьевой воде (см. рисунок А.З), он должен включаться в этап калибровки.
5 Реактивы
При возможности используют реактивы только известной степени чистоты, например реактивы «для анализа следовых количеств» или «для ВЭЖХ анализа», а также дистиллированную воду или воду эквивалентной степени чистоты с минимальной флуоресценцией.
Наблюдения за холостой пробой дают гарантию того, что в реактивах не содержатся определяемые концентрации ПАУ (см. 8.9). 5
5.1 Растворители
5.1.1 Экстракционные растворители для экстракции:
- гексан, С6Н-|4;
- другие летучие растворители, если они обеспечивают эквивалентное или лучшее извлечение.
5.1.2 Растворители для очистки экстракта:
- дихлорметан, СН2С12 (см. примечание);
- гексан, C6Hi4;
- N, N-диметилформамид, (CH3)2NCHO;
- ацетон, С3Н60.
Примечание — Дихлорметан часто содержит стабилизаторы, например этанол или амилен, которые могут влиять на степень элюирования. В отсутствие стабилизаторов могут образовываться радикалы, которые вызывают разложение ПАУ. Наличие хлористого водорода является индикатором радикалов. Он экстрагируется водой из дихлорметана и измеряется значение pH воды.
5.1.3 Растворители для ВЭЖХ:
- ацетонитрил, CH3CN;
- метанол, СН3ОН.
5.2 Натрия тиосульфат пентагидрат, Na2S203-5H20.
5.3 Натрия сульфат, Na2S04, безводный, предварительно прокаленный при 500 °С.
5.4 Азот с объемным содержанием вещества, 99,999 % (об.).
5.5 Силикагель со средним размером частиц около 40 мкм, хранящийся в эксикаторе для обеспечения максимальной активности.
Примечание — Могут быть использованы готовые картриджи с силикагелем.
5.6 Молекулярные сита с диаметром пор 0,4 нм, полностью активированные.
5.7 Эталонные соединения (таблица 1).
Так как эти соединения являются токсичными веществами по своей природе, рекомендуется использовать готовые, предпочтительно сертифицированные стандартные растворы. Необходимо избегать их контакта с кожей.
5.8 Основные стандартные растворы
Растворы по 5.8.1 и 5.8.2 стабильны по крайней мере в течение года при хранении в темноте при комнатной температуре и в герметичных условиях.
5.8.1 Однокомпонентные основные стандартные растворы веществ, приведенные в таблице 1, приготовлены в ацетонитриле (5.1.3) в определенной массовой концентрации, например 10 мкг/см5.
Эти растворы используют для идентификации на хроматограмме одного из ПАУ.
5.8.2 Многокомпонентный основной стандартный раствор сертифицирован и приготовлен в ацетонитриле (5.1.3) в определенной массовой концентрации, например 10 мкг/см5 для каждого отдельного соединения.
5.9 Рабочие стандартные растворы
Разбавлением основного стандартного раствора (5.8.2) метанолом или ацетонитрилом (5.1.3) приготавливают как минимум пять калибровочных растворов.
Выбор растворителя зависит от состава мобильной фазы ВЭЖХ.
Например, переносят 50 мм5 основного стандартного раствора в мерную колбу объемом 5 см5 и доводят до метки ацетонитрилом. В 1 мм5 этого рабочего стандартного раствора содержится 100 пг соответствующих индивидуальных компонентов.
При хранении в темноте при комнатной температуре и в герметичных условиях эти растворы остаются стабильными по крайней мере в течение года.
Проверка массовой концентрации ПАУ в основном стандартном растворе возможна только путем сравнения с независимым, предпочтительно сертифицированным, стандартным раствором.
6 Оборудование
Стандартную лабораторную стеклянную посуду моют для исключения вредных воздействий. Стеклянную посуду моют, например, моющим нейтральным средством в горячей воде и высушивают при температуре 120 °С в течение 15-30 мин. После охлаждения посуду промывают ацетоном, закрывают и хранят в чистоте. 6
Нельзя использовать для анализов питьевой воды посуду, в которой находились пробы сточных вод или пробы с высокими концентрациями ПАУ.
6.1 Бутыли предпочтительно известной массы, объемом 1000 см3, из темного стекла, с узким горлышком, плоским дном, со стеклянной пробкой.
6.2 Магнитная мешалка со стержнями, покрытыми стеклом или политетрафторэтиленом (далее — ПТФЭ), используемая для перемешивания при экстракции растворителем.
6.3 Делительная воронка, объемом 1000 см3, с краном из ПТФЭ и стеклянной пробкой.
6.4 Конические колбы, объемом 100 и 250 см3, со стеклянными пробками.
6.5 Микрошприцы, объемом 500 и 1000 мм3.
6.6 Колба для концентрирования, объемом 100 см3 (рисунок В.1).
6.7 Центрифуга с ротором и центрифужными пробирками, с коническим дном, объемом 50 см3 (рисунок В.2).
6.8 Пипетки Пастера.
6.9 Испарительное устройство, например роторный испаритель, с вакуумным стабилизатором и водяной баней.
6.10 Шейкирующее устройство с регулируемой скоростью вращения.
6.11 Микрофильтр с гидрофильной мембраной, устойчивой к действию растворителей, с размером пор 0,45 мкм.
6.12 Стеклянные пробирки для автодозатора, объемом около 2 см3, с химически инертной крышкой, например с прокладкой из ПТФЭ.
6.13 Полипропиленовые или стеклянные картриджи, заполненные как минимум 0,5 г силикагеля (5.5).
6.14 Стеклянные пробирки, например градуированные центрифужные пробирки (цена деления — 0,1 см3), номинальным объемом 10 см3, со стеклянными пробками.
6.15 Высокоэффективный жидкостный хроматограф (ВЭЖХ) с флуоресцентным детектором и системой обработки данных, который включает:
6.15.1 Дегазатор для дегазации вакуумом или гелием.
6.15.2 Аналитический насос, способный обеспечивать бинарное градиентное элюирование.
6.15.3 Термостат для колонки, способный обеспечивать постоянство температуры с точностью ±0,5 °С.
6.15.4 Флуоресцентный детектор, оборудованный монохроматором и пригодный для программирования по меньшей мере шести пар длин волн, включая ослабление/усиление сигнала.
6.16 Аналитическая хроматографическая колонка, обеспечивающая разделение пиков в соответствии с требованием 8.5.2 (примеры приведены в приложении А).
7 Отбор проб
Пробы питьевой воды из водопроводного крана отбирают до стерилизации крана, которая проводится перед отбором проб для бактериологического анализа.
Пробу отбирают в бутыль из темного стекла (6.1). Для удаления хлора в пробы воды добавляют около 50 мг тиосульфата натрия (5.2).
Бутыль заполняют пробой (приблизительно 1000 см3) и хранят при температуре 4 °С в защищенном от света месте до проведения экстракции. Экстракцию проводят в течение 24 ч после отбора пробы во избежание потерь за счет адсорбции. Если невозможно проанализировать пробу в течение 24 ч, необходимо провести следующее: удалить часть пробы из бутыли, чтобы остаток составлял приблизительно (1000 ± 10) см3, определить массу анализируемой пробы путем взвешивания бутыли; затем добавить 25 см3 гексана (5.1.2) и хорошо встряхнуть. Подготовленную таким образом пробу следует хранить в течение 72 ч при температуре 4 °С в защищенном от света месте.
8 Порядок работы
8.1 Экстракция
Пробы гомогенизируют, например, при помощи магнитной мешалки. Затем удаляют часть пробы из бутыли, чтобы остаток составлял приблизительно (1000 ± 10) см3, определяют массу анализируемой пробы взвешиванием бутыли; затем добавляют 25 см3 гексана (5.1.2) и хорошо встряхивают. Для экстракции можно также использовать другие летучие растворители при условии, что они позволяют обеспечить эквивалентное или лучшее извлечение. 7
1
Настоящий стандарт идентичен международному стандарту ISO 17993:2002 «Water quality. Determination of 15 polycyclic aromatic hydrocarbons (PAH) in water by HPLC with fluorescence detection after liquid-liquid extraction» (Качество воды. Определение 15-ти полициклических ароматических углеводородов (ПАУ) в воде методом ВЭЖХ с флуоресцентным детектированием после экстракции жидкость-жидкость)
Международный стандарт разработан подкомитетом SC 2 «Физические, химические и биохимические методы» технического комитета ISO/TC 147 «Качество воды» Международной организации по стандартизации (ISO).
Перевод с английского языка (ел).
В стандарт внесены следующие редакционные изменения: единица измерения микролитр (мкл) заменена на кубический миллиметр (мм3), единица измерения миллилитр (мл) заменена на кубический сантиметр (см3); единица измерения литр (л) заменена на кубический дециметр (дм3); изменена нумерация сносок со сквозной на постраничную.
Официальные экземпляры международного стандарта, на основе которого подготовлен настоящий государственный стандарт, и международных стандартов, на которые даны ссылки, имеются в Национальном фонде ТИПА.
В разделе «Нормативные ссылки» и тексте стандарта ссылки на международные стандарты актуализированы.
Сведения о соответствии государственного стандарта ссылочному международному стандарту приведены в дополнительном приложении Д.А.
Степень соответствия — идентичная (IDT)
© Госстандарт, 2016
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
2
3
4
5
6
7