ГОСТ ISO 11930-2014
Продукция косметическая. Микробиология. Оценка антимикробной защиты косметической продукции
Устанавливает: - испытание на эффективность консервирования; - процедуру оценки общей антимикробной защиты косметической продукции, которая согласно ISO 29621 не считается продукцией низкого риска. В стандарте описана процедура интерпретации данных, полученных путем испытания на эффективность консервирования или оценки микробиологического риска, или того и другого.
Идентичен ISO 11930:2012
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Сущность метода
5 Испытание на эффективность консервирования
6 Общая оценка антимикробной защиты косметической продукции
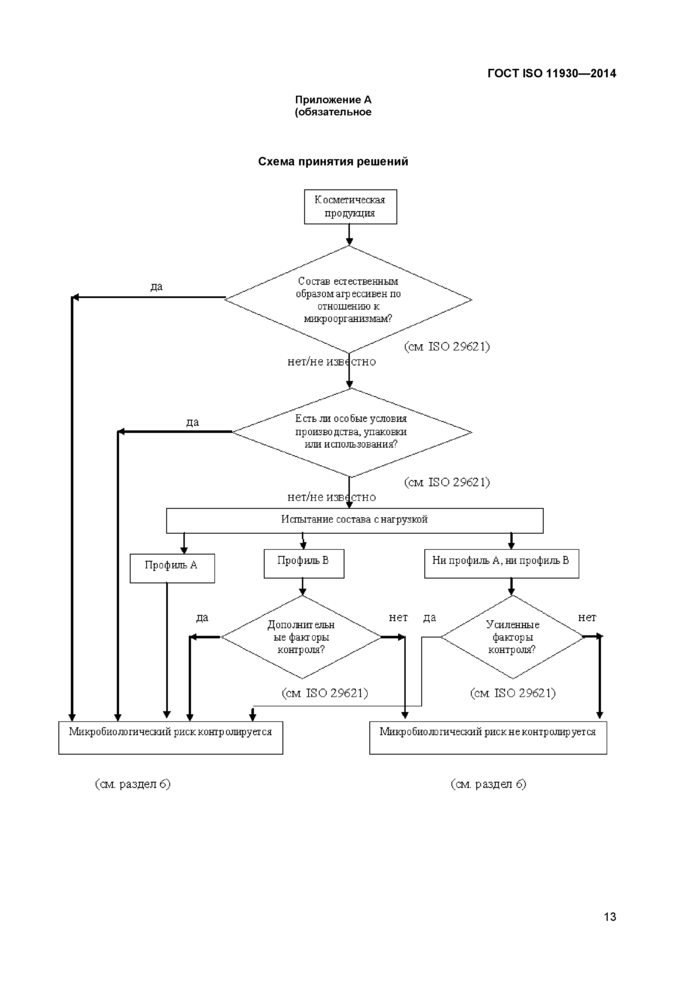
Приложение А (обязательное) Схема принятия решений
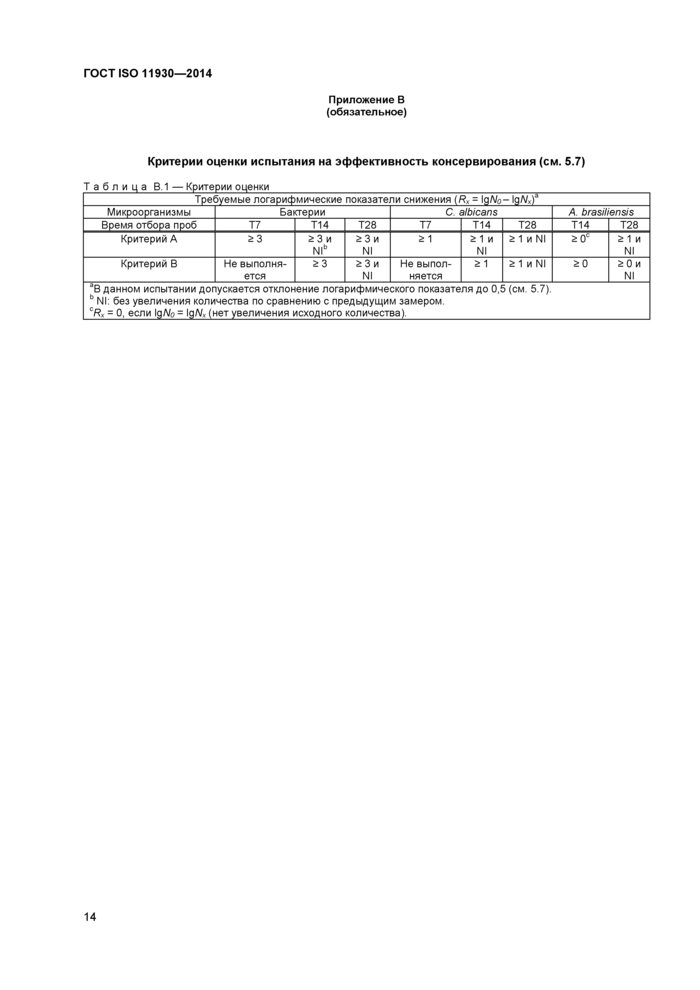
Приложение В (обязательное) Критерии оценки испытания на эффективность консервирования
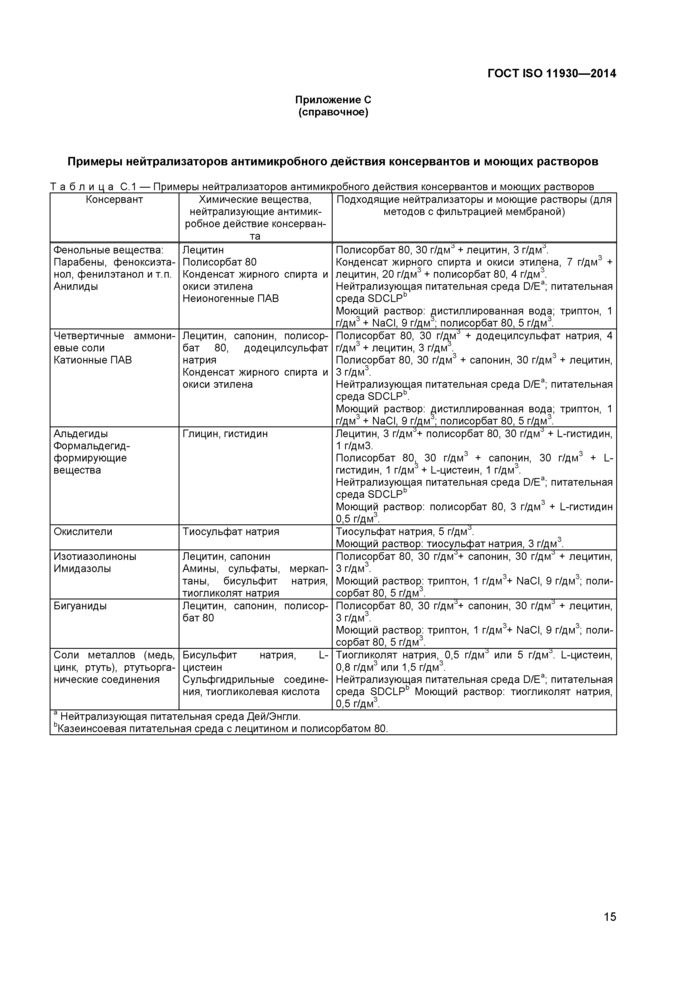
Приложение С (справочное) Примеры нейтрализаторов антимикробного действия консервантов и моющих растворов
Приложение D (справочное) Характеристики упаковки
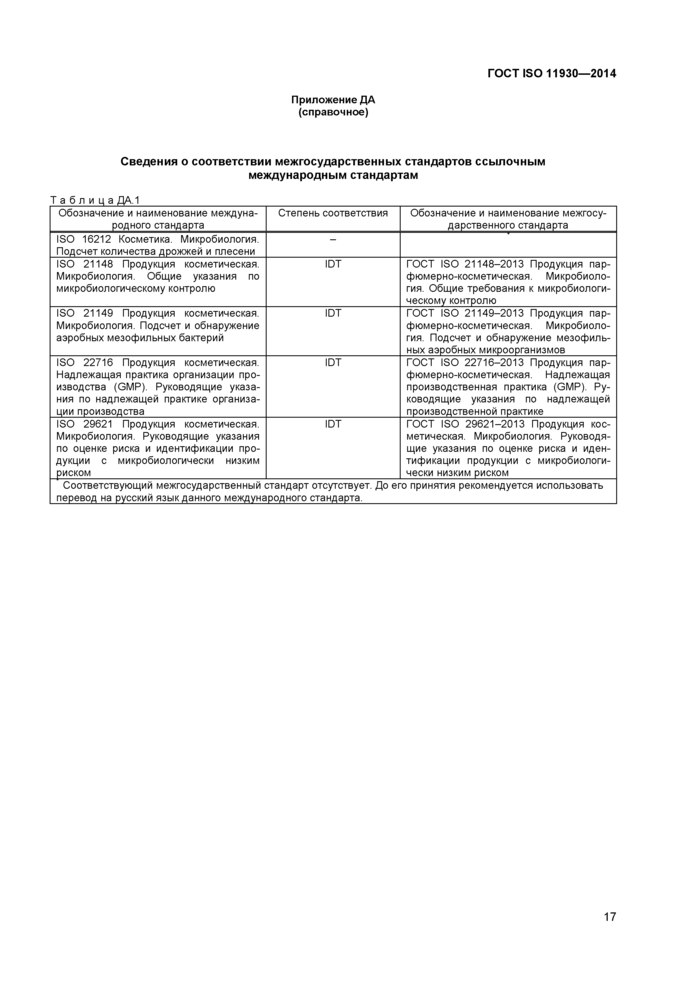
Приложение ДА (справочное) Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам
Библиография
24 страницы
| Дата введения | 01.01.2016 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 25.06.2014 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 45-2014 |
|---|---|---|---|
| 10.09.2014 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1065-ст |
| Разработан | АНО ПАРФЮМТЕСТ | ||
| Издан | Стандартинформ | 2015 г. |
Cosmetics. Microbiology. Evaluation of the antimicrobial protection of a cosmetic product
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
стр. 17
стр. 18
стр. 19

стр. 20
стр. 21

стр. 22

стр. 23

стр. 24
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
Продукция косметическая
МИКРОБИОЛОГИЯ
Оценка антимикробной защиты косметической продукции
(ISO 11930:2012, ЮТ)
Издание официальное
ГОСТ
ISO 11930— 2014
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные. правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Автономной некоммерческой организацией «ПАРФЮМТЕСТ» (АНО «ПАРФЮМТЕСТ») на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 25 июня 2014 г. № 45-2014)
|
За принятие проголосовали: | ||||||||||||||||||||||||
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 10 сентября 2014 г. №1065-ст межгосударственный стандарт ГОСТ ISO 11930-2014 введен в действие в качестве национального стандарта Российской Федерации с 01 января 2016 г.
5 Настоящий стандарт идентичен международному стандарту ISO 11930:2012 Cosmetics - Microbiology - Evaluation of the antimicrobial protection of a cosmetic product (Косметика. Микробиология. Оценка антибактериальной защиты косметического средства).
Международный стандарт разработан Техническим комитетом по стандартизации ISO/TC217 «Косметика» Международной организации по стандартизации (ISO).
Перевод с английского языка (ел).
Официальный экземпляр международного стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, имеется в Федеральном агентстве по техническому регулированию и метрологии Российской Федерации.
Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам приведены в дополнительном приложении ДА
Степень соответствия - идентичная (ЮТ).
Наименование настоящего стандарта изменено относительно наименования международного стандарта в целях соблюдения принятой терминологии
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
©Стандартинформ, 2015
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Введение
Настоящий стандарт используют для общей оценки антимикробной защиты косметическойпро-дукции.
Существует несколько способов антимикробной защитыкосметической продукции:
• химическое консервирование;
- характеристики, присущие продукции;
- конструкция упаковки;
- процесс производства.
В настоящем стандарте указана последовательность, в которой осуществляется оценка общей антимикробной защиты косметической продукции. Также в настоящем стандарте описан контрольный метод испытания на эффективность консервирования (Challengetesf) наряду с критериями его оценки.
Для установления уровня антимикробной защиты, необходимого для минимизации потребительского риска, используют данные, полученные при оценке риска (см. ISO 29621) или испытании на эффективность консервирования.
IV
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
Продукция косметическая МИКРОБИОЛОГИЯ Оценка антимикробной защиты косметической продукции
Cosmetics Microbiology Evaluation of the antimicrobial protection of a cosmetic product
Дата введения — 2016—01—01
1 Область применения
1.1 Общая информация
Настоящий стандарт устанавливает:
- испытание на эффективность консервирования:
- процедуру оценки общей антимикробной защиты косметической продукции, которая согласно ISO 29621 не считается продукцией низкого риска.
В настоящем стандарте описана процедура интерпретации данных, полученных путем испытания на эффективность консервирования или оценки микробиологического риска, или того и другого.
1.2 Испытание на эффективность консервирования
Это испытание является контрольным методом, который используют для оценки консервирования косметической продукции. Его применяют для косметической продукции, находящейся на рынке.
Для косметической продукции с низким микробиологическим риском проведение этого испытания не требуется (см. Приложение А и ISO 29621).
Это испытание первоначально разработано для косметической продукции, которая растворяется в воде или смешивается с ней. Для продукции, в состав которой вода входит в виде дисперсной фазы, может потребоваться адаптировать это испытание. Испытание, описанное в настоящем стандарте, подразумевает для каждого тест-микроорганизма помещение продукта в среду с калиброванной культурой, а затем измерение изменений в количестве микроорганизмов через определенные временные интервалы в течение определенного временного периода при определенной температуре.
Примечание - На основе этого контрольного метода можно разрабатывать собственные методы в ходе цикла разработки косметической продукции В подобном случае допускается изменение и расширение метода. чтобы учесть уже накопленные данные и различные факторы, такие как штаммы бактерий, среду, условия созревания, длительность воздействия, и т.п. Критерии соответствия можно адаптировать под конкретные цели Во время цикла разработки косметической продукции по мере необходимости можно использовать и другие методы для определения на эффективность консервирования продукции
1.3 Процедура оценки антимикробной защиты косметической продукции
Эта процедура основана на тщательном рассмотрении следующих моментов:
- результаты испытания на эффективность консервирования. Испытание на эффективность консервированиятребуется не для всех косметических продуктов (см. приложение А и ISO 29621):
- характеристики продуктов и данные, полученные при оценке микробиологического риска (см. ISO 29621). Анализ оценки микробиологического риска основан на комплексном подходе. В частности. он сочетает в себе такие факторы как: характеристики состава продукта, условия производства, характеристики упаковки, в которой продукт будет доставляться на рынок, рекомендации по использованию косметической продукции и. при необходимости, область применения и целевую аудиторию (см. приложение D).
Издание официальное
2 Нормативные ссылки
Для применения настоящего стандарта необходимы следующие ссылочные стандарты Для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных ссылок применяют последнее издание ссылочного стандарта (включая его изменения).
ISO 16212. Cosmetics - Microbiology - Enumeration of yeast and mould (Косметика. Микробиология. Подсчет количества дрожжей и плесени)
ISO 18415. Cosmetics - Microbiology - Detection of specified and non-specified microorganisms (Косметика. Микробиология. Выявление специфических и неспецифических микроорганизмов)
ISO 21148. Cosmetics - Microbiology - General instructions for microbiological examination (Продукция косметическая. Микробиология. Общие указания по микробиологическому контролю)
ISO 21149. Cosmetics - Microbiology - Enumeration and detection of aerobic mesophilic bacteria (Продукция косметическая. Микробиология. Подсчет и обнаружение аэробных мезофильных бактерий)
ISO 22716. Cosmetics - Good Manufacturing Practices (GMP) - Guidelines on Good Manufacturing Practices (Продукция косметическая. Надлежащая практика организации производства (GMP). Руководящие указания по надлежащей практике организации производства]
ISO 29621. Cosmetics - Microbiology -Guidelines for the risk assessment and identification of micro-biologically low-risk products (Продукция косметическая. Микробиология. Руководящие указания по оценке риска и идентификации продукции с микробиологически низким риском)
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку
3 Термины и определения
В настоящем стандарте применены термины no ISO 21148. а также следующие термины с соответствующими определениями:
3.1 масса (состав) косметического продукта (cosmetic formulation): Смесь сырья с количественно и качественно определенным составом.
3.2 косметическая продукция (cosmetic product): Готовая косметическая продукция, которая прошла все этапы производства, включая упаковку в контейнер для отгрузки.
3.3 антимикробная защита косметической продукции (antimicrobial protection of a cosmetic product): Способность косметической продукции преодолевать микробное загрязнение, которое может представлять потенциальный риск для потребителя.
Примечание - Полная антимикробная защита включает консервирование, особенности производственного процесса и защитную упаковку
3 4 консервирование массы косметического продукта (preservation of a cosmetic formulation): Набор средств, которые используют во избежание размножения микроорганизмов в косметическом продукте.
Пример - Консерванты, многофункциональные соединения, агрессивное сырье, крайние уровни pH, низкое значение активности воды.
3.5 контрольный метод (reference method): Метод, который применяют заинтересованные стороны для оценки продукта на рынке или в случае разногласий.
3.6 разработанный метод, «собственный метод» (development method, «in-house method»): Метод, который используют на этапе разработки продукта до его выхода на рынок.
3.7 потребитель (consumer): Конечный пользователь косметической продукции.
4 Сущность метода
В оценку антимикробной защиты косметической продукциивходят следующие элементы (см. приложение А).
2
a) Характеристики ее состава (см. ISO 29621) или результаты испытания на эффективность консервирования (если оно проводилось), или и то, и другое.
Испытание на эффективность консервирования описано в 5.1.
b) Характеристики косметической продукции в сочетании с условиями производства (см. ISO 22716 и ISO 29621), упаковочные материалы и, если на то есть основания, рекомендации по использованию продукции (см. ISO 29621).
В настоящем стандарте описана процедура интерпретации данных, полученных путем испытания на эффективность консервирования (если это уместно) или оценки микробиологического риска.
5 Испытание на эффективность консервирования
5.1 Общая информация
Оценку консервирования массы косметического продукта выполняют путем внесения в нее калиброванной культуры, подготовленной из соответствующих штаммов микроорганизмов. Количество выживших клеток микроорганизмов измеряют с определенными интервалами в течение 28 дней. Логарифмический показатель снижения количества клеток микроорганизмов для каждого периода времени и каждого штамма высчитывают и сравнивают с необходимыми минимальными значениями для критериев оценки А или В (см. приложение В).
При использовании контрольного метода отклонения от установленных процедур не допускаются. так как это может привести к получению недостоверных результатов. В ходе разработки продукта допускается использовать другие подходящие собственные разработанные методы для определения на эффективность консервирования продукции (см. 1.2).
До проведения испытания необходимо определить микробиологические качества продукции согласно ISO 21149 и ISO 16212. или ISO 18415.
Примечание - Микроорганизмы, изначально присутствующие в пробе для испытания, не должны мешать выделению микроорганизмов, применяемых в опыте
Во время испытания необходимо проверять и показывать нейтрализацию возможной антимикробной активности пробы для испытания (см. 5.5).
5.2 Материалы, оборудование, реактивы и питательные среды
В ISO 21148 указаны общие технические характеристики и инструкции. Если в составе используется вода, то нужно использовать дистиллированную или очищенную воду, как указано ISO 21148 (пункт 8.2).
5.2.1 Материалы
Используют стандартное оборудование микробиологической лаборатории (см. ISO 21148) и:
5.2.1.1 Стеклянные шарики диаметром от 3 до 4 мм.
5.2.1.2 Фильтр из пористого стекла с пористостью 2 (от 40 мкм до 100 мкм).
5.2.1.3 Колбы.
5.2.1.4 Стерильную стеклянную посуду подходящей вместимости с крышками.
5.2.1.5 Центрифугу с центробежной силой 2000 д.
5.2.2 Разбавители, нейтрализаторы и питательная среда
5.2.2.1 Общая информация
Если не указано иное, перед использованием все реактивы необходимо довести до температуры окружающей среды. При наличии можно использовать готовые к употреблению реактивы и среду.
5.2.2.2 Разбавитель
5.2.2.2.1 Состав
Панкреатический гидролизат казеина - 1.0 г.
Хлорид натрия - 8.5 г.
Вода -1000 см3.
5.2.2.2.2 Подготовка
Растворяют компоненты в воде, помешивая во время нагревания. Разливают в подходящую посуду. Стерилизуют в автоклаве при температуре 121 “С в течение 15 мин. После стерилизации уровень pH должен составить (7.0 ± 0.2) при измерении его при комнатной температуре.
5.2.2.2.3 Раствор полисорбата 80 (для подготовки взвеси спор A. brasiliensis)
Готовят раствор полисорбата 80 (0.5 г/дм3). Нагревают, помешивая, до полного растворения. Разливают раствор в подходящую посуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин.
3
5.2.2.3 Нейтрализатор
5.2.2.3.1 Общая информация
Необходимо продемонстрировать пригодность и эффективность нейтрапизующего агента по отношению к испытуемым штаммам и испытуемому продукту так, как это указано в 5.5.
Чаще всего применяют нейтрализатор, описанный в 5 2 2 3 2. Примеры других подходящих нейтрализаторов приведены в приложении С.
5.2.2.3.2 Питательная среда Eugon LT100
5.2.2.3.2.1 Общая информация
Эта среда содержит ингредиенты, которые нейтрализуют ингибиторы в пробе (лецитин и лоли-сорбат 80). а также диспергирующий агент октоксинол 9 (например. Triton Х100*’1>). Ее можно приготовить согласно 5.2.2.3.2.2 или из сухой питательной среды, согласно инструкциям производителя. Также можно использовать готовую среду.
5.2.2.3.2.2 Состав
Панкреатический гидролизат казеина - 15 г.
Папаиновый гидролизат сои - 5 г.
Хлорид натрия - 4 г.
L-цистеин - 0.7 г.
Сульфит натрия - 0.2 г.
Глюкоза - 5.5 г.
Яичный лецитин - 1 г.
Полисорбат 80 - 5 г.
Октоксинол 9 - 1 г.
Вода -1000 смэ.
5.2.2.3.2.3 Подготовка
Последовательно растворяют в кипящей воде полисорбат 80. октоксинол 9 и яичный лецитин до полного растворения. Растворяют другие компоненты, помешивая во время нагревания Разливают раствор в подходящуюлосуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин. Хорошо перемешивают после стерилизации, пока жидкость еще достаточно горячая, чтобы растворить выпавший осадок. После стерилизации уровень pH должен составить (7.0 ± 0.2) при измерении его при комнатной температуре.
5.2.2.4 Питательные среды
5.2.2.4.1 Общая информация
Питательную среду можно приготовить согласно 5.2.2.4 2 или из сухой питательной среды, согласно инструкциям производителя. Допускается использование готовой среды, если ее состав и/или ростовые качества близки к составу, указанному в 5.2.2.4.2.1.
5.2.2.4.2 Питательная среда для бактерий: трилтон-соевый агар (TSA) или агаризованная среда с соевым и казеиновым гидролизатами
5.2.2.4.2.1 Состав
Панкреатический гидролизат казеина - 15 г.
Папаиновый гидролизат сои - 5 г.
Хлорид натрия - 5.0 г.
Агар-агар -15.0 г.
Вода-1000 см3.
5.2.2.4.2.2 Подготовка
Растворяют компоненты или готовую сухую смесь питательной среды в воде, помешивая во время нагревания. Разливают раствор в лодходящуюлосуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин. Хорошо перемешивают после стерилизации, пока жидкость еще достаточно горячая, чтобы растворить выпавший осадок. После стерилизации и охлаждения уровень pH должен составить(7.3 ± 0.2) при измерении его при комнатной температуре.
5.2.2.4.3 Питательная среда для С. albicans: декстрозный агар Сабуро (SDA)
5.2.2.4.3.1 Состав
Декстроза - 40.0 г.
Пептоны - 5.0 г.
Панкреатический гидролизат казеина - 5.0 г.
Агар-агар - 15.0 г.
Вода - 1000 см3. 1 2
5.2.2.4.3.2 Подготовка
Растворяют компоненты или готовую сухую смесь питательной среды в воде, помешивая во время нагревания. Разливают раствор в подходящую посуду. Стерилизуют в автоклаве при температуре 121 ‘Св течение 15 мин. После стерилизации уровень pH должен составить (5,6 ± 0,2) при измерении его прикомнатной температуре
5.2.2.4.4 Питательная среда для A. brasiliensis: картофельный агар с декстрозой (PDA)
5.2.2.4.4.1 Состав
Картофельный настой (см. 5.2.2 4.4.2, Примечание 1) - 200,0 г.
Декстроза - 20.0 г.
Агар-агар (см. 5 2.2.4 4.2, Примечание 2) - 20,0 г.
Вода -1000 см3 4 5 6.
5.2.2.4.4.2 Подготовка
Растворяют компоненты или готовую сухую смесь питательной среды в воде, нагревая ее. Разливают раствор в подходящую посуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин. После стерилизации уровень pH должен составить (5.6 ± 0.2) при измерении его при комнатной температуре.
Примечание 1- Чтобы приготовить картофельный настой, можно воспользоваться сухим порошком, который есть в продаже, или прокипятить 200 г нарезанного, нечищеного картофеля в 1 дм5 воды в течение 30 мин Фильтруют с помощью марли, сохраняя жидкость
Примечание 2 - Приобретенные сухие смеси, содержащие менее 20 г/дм7 агар-агара, можно довести до необходимой концентрации, дополнительно добавив необходимое количество агар-агара
5.3 Штаммы микроорганизмов
Испытание проводят, используя следующие штаммы в качестве экспериментальных микроорганизмов:
- Pseudomonas aeruginosa АТССФ9027™1’, равноценные штаммы: С1Р®82 118™2>, или NCIMB®8626™31. или NBRC®13275™2', или КСТС®2513™'\ или другие равноценные местные коллекционные штаммы;
- Staphylococcus aureus АТСС®6538ТЫ. равноценные штаммы: С1Р®4 83™, или NCIMB®9518™. или NBRC®13276TM. или КСТС®3881™, или NCTC®10788™ или другие равноценные местные коллекционные штаммы;
- Escherichia coli АТСС®8739™, равноценные штаммы: С1Р®53.126™, или NCIMB®8545™, или NBRC®3972™, или КСТС®2571™, или NCTC®12923™, или другие равноценные местные коллекционные штаммы;
- Candida albicans АТСС®10231 ™. равноценные штаммы: IP 48.72™7>, или NCPF® 3179™8>, или NBRC®1594™, или КСТС®7965™, или другие равноценные местные коллекционные штаммы;
- Aspergillus brasiliensis (устаревшее название A niger) АТСС®16404™. равноценные штаммы: IP 1431. или 1М1®149007™или NBRC®9455™, или КСТС®6196™, или другие равноценные местные коллекционные штаммы.
Культура должна быть восстановлена в соответствии с процедурами, предусмотренными поставщиком референс штамма. Штаммы хранят в лаборатории согласно EN 12353 или в соответствии с другим подходящим методом.
5.4 Подготовка и учет калиброванных культур
5.4.1 Общая информация
Для проведения испытаний выполняют пересев штаммов, которые хранят в лаборатории (см. 5.3). чтобы получить исходные культуры и рабочие культуры.
5
Исходная культура - это конфлюэнтная культура, полученная путем посева культуры из хранилища штрихом на пробирки со скошенным агаром или на чашки Петри с помощью одноразового шарика. После инкубации исходная культура может храниться при температуре от 2 °С до 8 °С до двух месяцев и применяться для получения рабочих культур.
Из рабочей культуры, которую готовят непосредственно перед экспериментом, получают калиброванную суспензию (инокулят).
Исходную и рабочую культуры выращивают в одинаковых условиях инкубирования на одинаковой питательной среде (см. 5.4.2 и 5.4.3).
Примечание 1- Ограничение количества последовательных пересевов и использование конфлюэнтных культур, а не изолированных колоний, снижает риск изменения восприимчивости штаммов Стандартизация условий созревания и подготовки инокулята повышает воспроизводимость метода
Примечание 2 - Использование многоразовой посуды, которую хранят в замороженном виде, может привести к изменению восприимчивости штаммов, вызванному действием тепловых ударов Это может произойти. если посуду вынимают из морозильного шкафа, из нее извлекают один шарик, а затем посуду возвращают в шкаф
5.4.2 Подготовка суспензий бактерий и Candidaalbicans
5.4.2.1 Для подготовки рабочей культуры испытуемого микроорганизма необходимо подготовить субкультуру путем посева исходной культуры штрихом на пробирки со скошенным агаром или на чашки Петри (TSA для бактерий. SDA для С.albicans), чтобы получить конфлюэнтную культуру. Выращивают при температуре (32,5 ± 2.5) °С в течение 18 - 24ч.
Таким же образом готовят вторую субкультуру путем посева первой культуры и выращивают при температуре (32.5 ± 2.5) “С в течение 18 - 24 ч. Третью субкультуру можно вырастить таким же способом путем посева второй культуры. Вторая культура и третья (если она была выращена) образуют рабочую культуру.
Если нельзя получить вторую субкультуру своевременно, тогда допускается выдерживать первую культуру до 48 ч в инкубаторе при температуре (32.5 ± 2.5) °С. а затем использовать ее для подготовки второй субкультуры. В этом случае готовят третью субкультуру в течение 18 - 24 ч и используют ее в испытании.
Не рекомендуется готовить четвертую субкультуру из исходной культуры.
5.4.2.2 Берут 10 см разбавителя (см. 5.2.2 2) и помещают в подходящую стерильную посуду со стерильными стеклянными шариками массой около 5 г. Переносят клетки, выращенные в агаризован-ной среде, в разбавитель с помощью петель для посева. Клетки суспендируют в разбавителе, потерев петлю с небольшим количеством разбавителя о стенку посуды, чтобы отделить клетки.
5.4.2.3 Гомогенизируют суспензию, встряхивая посуду вручную или механическим способом в течение 3 мин. Отбирают верхнюю часть суспензии с помощью аспиратора (избегая контакта со стеклянными шариками) и переносят полученную суспензию в стерильную посуду.
5.4.2.4 Регулируют концентрацию клеток в суспензии с помощью растворителя (см. 5.2.2.2) согласно данным о калибровке, полученным в лаборатории (например, с помощью спектрофотометра, см. ISO 21148, приложение С). Концентрация должна составлять от 1 * 10 КОЕ/см'до 1 * 10® КОЕ/см3 для бактерий и от 1 * 10’ КОЕ/см^ до 1 * 10 КОЕ/см3 для С. albicans.
Калиброванный раствор используют в течение двух часов.
5.4.2.5 При выполнении эксперимента проверяют исходную концентрацию клеток в суспензии. N. Выполняют серию десятикратных разведений калиброванной суспензии с помощью растворителя (см. 5.2.2.2). Выполняют подсчет количества клеток путем переноса 1 см подходящих растворов (см. 5.6.2) в среду TSA для бактерий и SDA для С.albicans. Выращивают при температуре (32.5 ± 2,5) °С в течение 24-48 ч.
5.4.3 Подготовка взвеси спор A. brasiliensis (устаревшее название A. niger)
5.4.3.1 Для получения рабочей культуры тест-микроорганизма готовят суспензию клеток исходной культуры (на PDA) не старше двух месяцев в растворителе (см. 5.2.2.2) Выполняют посев, залив суспензию на поверхность среды PDA. помещенной в колбу или подходящее количество чашек Петри, чтобы получить конфлюэнтную культуру. Выращивают при температуре (22.5 ± 2.5) °С в течение 7-11 дней.
5.4.3.2 После выращивания переносят 10 см раствора полисорбата 80 (см. 5.2.2.2.3) в колбу. Осторожно отделяют споры от поверхности культуры, используя лопатку или стеклянные шарики.
Переносят суспензию в подходящую колбу и осторожно перемешивают со стеклянными шариками в течение примерно 1 мин. Фильтруют суспензию с помощью фильтра из пористого стекла с пористостью 2 (от 40 до 100 мкм).
5.4.3.3 Выполняют микроскопирование (увеличение *400), чтобы установить наличие проросших спор или фрагментов мицелия.
6
1
1 Tnton XI00® - пример доступного для приобретения продукта Данная информация приведена для удобства пользователей настоящего стандарта и не означает одобрение данного продукта организацией ISO
2
3
"АТСС® Американская коллекция типовых культур
4
‘ CIP® Коллекция Института Пастера
5
NCIMB® Национальная коллекция промышленных морских бактерий
6
41NBRC® Центр биологических ресурсов NITE. Япония КСТСФ Корейская коллекция типовых культур eiNCTC® Национальная коллекция типовых культур IP Институт Пастера
7
81NCPF® Национальная коллекция патогенных грибов w IMI Международный микологический институт. Великобритания