ГОСТ 8.134-98
Государственная система обеспечения единства измерений. Шкала pH водных растворов
Купить ГОСТ 8.134-98 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на шкалу рН водных растворов и устанавливает значения рН для воспроизведения этой шкалы в диапазоне от 0 до 14 в интервале температур от 0 до 95 °С.
- Заменяет ГОСТ 8.134-74 «Государственная система обеспечения единства измерений. Шкала pH водных растворов» ИУС 1-99
Переиздание. Март 2007 г.
Оглавление
1 Назначение и область применения
2 Инструментальное (практическое) определение значений рН
3 Шкала рН
3.1 Реперный буферный раствор (РБР)
3.2 Эталонные буферные растворы (ЭБР)
3.3 Рабочие эталоны рН (РЭ)
4 Информация, представляемая при записи результатов измерений рН (Х)
Приложение А Значения рН реперного буферного раствора
Приложение Б Приготовление реперного буферного раствора
| Дата введения | 01.07.1999 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.07.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
- Раздел 71.040 Аналитическая химия
- Раздел 71.040.40 Химический анализ
- Раздел 71.040 Аналитическая химия
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
- Раздел Электроэнергия
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
- Раздел 71.040 Аналитическая химия
- Раздел 71.040.40 Химический анализ
- Раздел 71.040 Аналитическая химия
- Раздел 71 ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
Организации:
| 28.05.1998 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 13-98 |
|---|---|---|---|
| 27.10.1998 | Утвержден | Государственный комитет Российской Федерации по стандартизации, метрологии и сертификации | 381 |
| Разработан | ГП ВНИИФТРИ | ||
| Издан | ИПК Издательство стандартов | 1999 г. | |
| Издан | ИПК Издательство стандартов | 2001 г. | |
| Издан | Стандартинформ | 2007 г. |
State system for ensuring the uniformity of measurement. pH Scale for aqueous solutions
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5
стр. 6
стр. 7

стр. 8

стр. 9
стр. 10

стр. 11
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ГОСУДАРСТВЕННАЯ СИСТЕМА ОБЕСПЕЧЕНИЯ ЕДИНСТВА ИЗМЕРЕНИЙ
ШКАЛА pH ВОДНЫХ РАСТВОРОВ
Издание официальное
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
Минск
Предисловие
1 РАЗРАБОТАН Государственным предприятием «Всероссийский научно-исследовательский институт физико-технических и радиотехнических измерений» (ГП ВНИИФТРИ) Госстандарта России
ВНЕСЕН Госстандартом России
2 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол № 13 от 28 мая 1998 г.)
За принятие проголосовали:
|
Наименование государства |
Наименование национального органа по стандартизации |
|
Азербайджанская Республика |
Азгосстандарт |
|
Республика Армения |
Армгосстандарт |
|
Республика Беларусь |
Госстандарт Беларуси |
|
Грузия |
Грузстандарт |
|
Республика Казахстан |
Госстандарт Республики Казахстан |
|
Киргизская Республика |
Киргизстандарт |
|
Республика Молдова |
Молдовастандарт |
|
Российская Федерация |
Госстандарт России |
|
Республика Таджикистан |
Таджикгосстандарт |
|
Туркменистан |
Главная государственная инспекция Туркменистана |
|
Республика Узбекистан |
Узгосстандарт |
|
Украина |
Госстандарт Украины |
3 Постановлением Государственного комитета Российской Федерации по стандартизации, метрологии и сертификации от 27 октября 1998 г. № 381 межгосударственный стандарт ГОСТ 8.134—98 введен в действие непосредственно в качестве государственного стандарта Российской Федерации с 1 июля 1999 г.
4 ВЗАМЕН ГОСТ 8.134-74
5 ПЕРЕИЗДАНИЕ. Март 2007 г.
© ИПК Издательство стандартов, 1999 © Стандартинформ, 2007
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания на территории Российской Федерации без разрешения Федерального агентства по техническому регулированию и метрологии
Редактор ТА. Леонова Технический редактор Н. С. Гришанова Корректор В.И. Баренцева Компьютерная верстка Л.А. Круговой
| ||||
|
Набрано во ФГУП «СТАНДАРТИНФОРМ» на ПЭВМ. Отпечатано в филиале ФГУП «СТАНДАРТИНФОРМ» — тип. «Московский печатник», 105062 Москва, Лялин пер., 6 |
ГОСТ 8.134-98
Содержание
1 Назначение и область применения............................................. 1
2 Инструментальное (практическое) определение значений pH......................... 1
3 Шкала pH................................................................ 2
3.1 Реперный буферный раствор (РБР)......................................... 2
3.2 Эталонные буферные растворы (ЭБР)....................................... 2
3.3 Рабочие эталоны pH (РЭ)................................................. 2
4 Информация, представляемая при записи результатов измерений pH (X)................. 5
Приложение А Значения pH реперного буферного раствора............................ 5
Приложение Б Приготовление реперного буферного раствора.......................... 6
III
ГОСТ 8.134-98МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
Государственная система обеспечения единства измеренийШКАЛА pH ВОДНЫХ РАСТВОРОВ
State system for ensuring the uniformity of measurements. pH Scale for aqueous solutions
Дата введения 1999—07—01
1 НАЗНАЧЕНИЕ И ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий стандарт распространяется на шкалу pH водных растворов и устанавливает значения pH для воспроизведения этой шкалы в диапазоне от 0 до 14 в интервале температур от 0 до 95 °С.
Величина pH (водородного показателя) соответствует отрицательному десятичному логарифму активности ионов водорода в растворе
pH = — lg <%. (1)
Это только понятийное определение, так как уравнение (1) включает в себя активность ионов водорода, которая не может быть непосредственно измерена и должна быть рассчитана с использованием определенных приближений, например метода, описанного в приложении А.
В терминах концентраций уравнение (1) может быть переписано в следующем виде:
pH = —lg(cHyH/c°) (2)
или
pH = — lg (ти ун / т°), (3)
где с° — молярная концентрация ионов водорода в стандартном состоянии, равная 1 моль-дм3; сн — молярная концентрация ионов водорода, моль-дм3;
пР — моляльность ионов водорода в стандартном состоянии, равная 1 моль- кг-1; ти — моляльность ионов водорода, моль- кг-1; ун, ун — коэффициенты активности ионов водорода в двух системах выражения концентрации.
2 ИНСТРУМЕНТАЛЬНОЕ (ПРАКТИЧЕСКОЕ) ОПРЕДЕЛЕНИЕ ЗНАЧЕНИЙ pH
Измеряют электродвижущие силы (ЭДС) Е{Х) и E{S) каждой из двух ячеек (I и II) с жидкостным соединением, содержащих исследуемый раствор Хи эталонный буферный раствор Sсоответственно:
Электрод
сравнения
Электрод
сравнения
КС1 (водный раствор концентрацией не менее 3,5 моль-кг-1)
КС1 (водный раствор концентрацией не менее 3,5 моль-кг-1)
Раствор X
Раствор S
Н2 (101325 Па)
Н2 (101325 Па)
Pt
I
Pt II
Температура обеих ячеек I и II должна быть одинаковой и давление водорода на водородных электродах идентичным. Солевые мостики заполняют концентрированным раствором КС1.
Значение pH раствора X, рН(Л), связано со значением pH эталонного раствора S, рН(5), следующим образом:
Издание официальное
E{S)-E{X)
(.RT/F) In 10 ’
(4)
рЩА)
рЩА) +
где R — универсальная газовая постоянная, равная (8,314510+0,000070) Дж-моль '-К +
Т — термодинамическая температура, К;
F— константа Фарадея, равная (9,648530+0,000002)-104 Кл-моль-1.
Величину (RT/F)\n\() = к называют коэффициентом наклона; его значения в температурном интервале от 0 до 95 °С приведены в таблице А. 1 приложения А.
Любые различия диффузионного потенциала жидкостного соединения между ячейками I и II включены в величину pH (А).
3 ШКАЛА pH
ЗЛ Реперный буферный раствор (РБР)
Шкала pH при некоторой заданной температуре определена уравнением (4) как прямая линия в координатах pH — Е(Х) с наклоном к, проходящая через точку, соответствующую значению pH, приписанному реперному буферному раствору (приведено в таблице 1). В указанной точке значение E(S) соответствует ЭДС ячейки II, содержащей реперный буферный раствор.
|
Таблица 1— Значения pH реперного буферного раствора (РБР) — раствора гидрофталата калия с моляльностью 0,05 моль-кг-1 при различных температурах | ||||||||||||||||||||||||||||||||||||||||||||||||
|
Определение значений pH, приписанных реперному буферному раствору pH, проводят в ячейке III без переноса:
Pt | Н2 (газ, р = 1 атм = 101325 Па) | РБР, Cl- | AgCl | Ag III
Процедура определения описана в приложении А.
В качестве реперного буферного раствора следует использовать раствор гидрофталата калия с моляльностью 0,05 моль-кг-1, приготовление и некоторые свойства которого приведены в приложении Б. Для этого раствора платиновый водородный электрод покрывают слоем губчатого палладия во избежание каталитического восстановления гидрофталата калия водородом. Расчет значения pH реперного буферного раствора включает условие Бейтса—Гуггенгейма для определения активности хлорид-ионов (уравнение А.4 приложения А).
3.2 Эталонные буферные растворы (ЭБР)
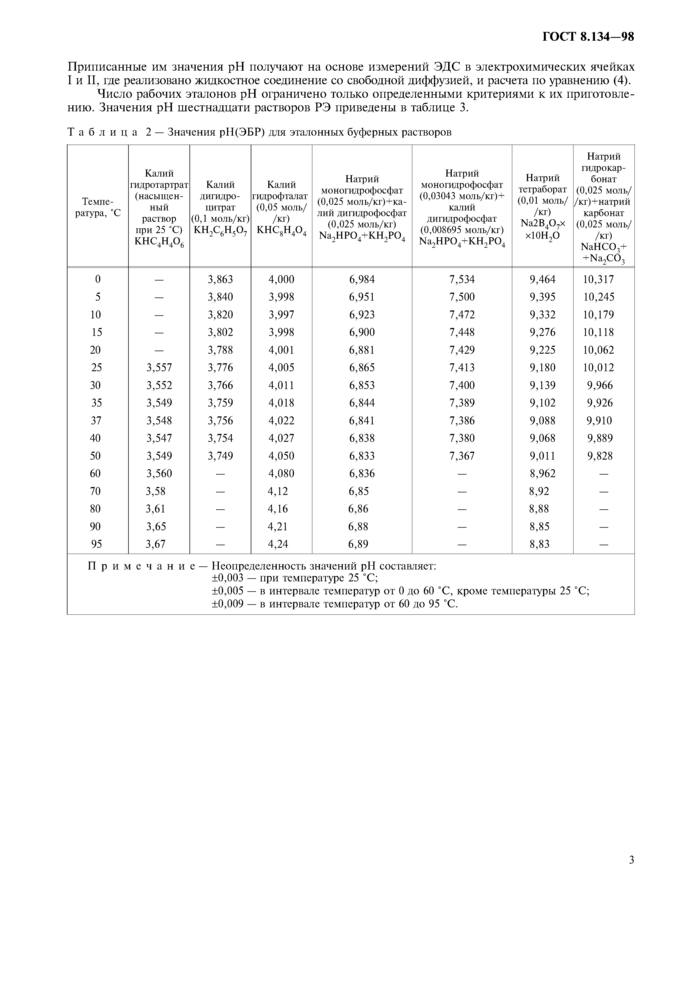
Значения pH также приписывают по результатам измерений в ячейке III шести другим буферным растворам, которые соответствуют определенным требованиям по воспроизводимости значений pH, стабильности, буферной емкости и простоте их изготовления. Эти растворы (в количестве семи, включая РБР) называют эталонными буферными растворами; экспериментально определенные значения pH, которые им приписаны, приведены в таблице 2.
Вычисленное по уравнению (4) на основе измеренных ЭДС ячеек I и II значение pH исследуемого водного раствора X может колебаться в зависимости от выбора эталонного буферного раствора в пределах +0,02.
Эталонные буферные растворы используют для научных исследований и для проведения международных сличений.
3.3 Рабочие эталоны pH (РЭ)
Рабочие эталоны pH (РЭ) определяют как производные от реперного буферного раствора.
Приписанные им значения pH получают на основе измерений ЭДС в электрохимических ячейках I и II, где реализовано жидкостное соединение со свободной диффузией, и расчета по уравнению (4).
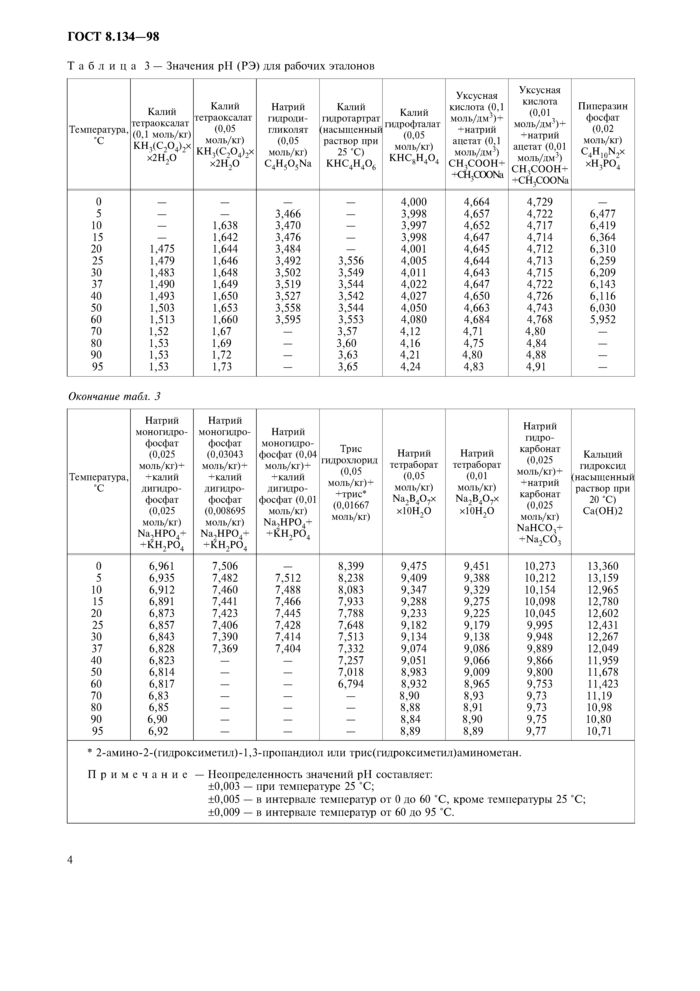
Число рабочих эталонов pH ограничено только определенными критериями к их приготовлению. Значения pH шестнадцати растворов РЭ приведены в таблице 3.
|
Таблица 2 — Значения рН(ЭБР) для эталонных буферных растворов | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3
|
Таблица 3 — Значения pH (РЭ) для рабочих эталонов | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Окончание табл. 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
* 2-амино-2-(гидроксиметил)-1,3-пропандиол или трис(гидроксиметил)аминометан. |
Примечание — Неопределенность значений pH составляет:
+0,003 — при температуре 25 °С;
+0,005 — в интервале температур от 0 до 60 °С, кроме температуры 25 °С; ±0,009 — в интервале температур от 60 до 95 °С.
ГОСТ 8Л34-984 ИНФОРМАЦИЯ, ПРЕДСТАВЛЯЕМАЯ ПРИ ЗАПИСИ РЕЗУЛЬТАТОВ ИЗМЕРЕНИЙ рН(А)
Буферные растворы, использованные для градуировки pH-метра, представляют с результатами измерения в следующем виде:
Система градуирована по РБР
с рН(РБР) = ... при ... К.
Система градуирована по двум эталонным буферным растворам с рЩЭБР;) = ... и рН(ЭБР2) = ... при ... К.
Система градуирована по двум рабочим эталонам pH с рЩРЭ^ = ... и рН(РЭ2) = ... при ... К.
ПРИЛОЖЕНИЕ А (справочное)
ЗНАЧЕНИЯ pH РЕПЕРНОГО БУФЕРНОГО РАСТВОРА
Процедура определения значений pH реперного буферного раствора, приведенных в таблице 1, основана на измерениях ЭДС ячейки III:
Pt | Н2 (газ, р = 1 атм = 101325 Па)| РБР, Cl“ (mcl) | AgCl | Ag III
при трех разных значениях концентрации хлорид-ионов та = 0,005 моль/кг; 0,010 моль/кг и 0,015 моль/кг.
ЭДС Е ячейки III определяют по уравнению:
Е = ЕР - к ■ lg [тн тС1 ун уС1 / (т0)2], (А.1)
где к — коэффициент наклона; тнаТнс1 — модальности и коэффициенты активности соответствующих ионов;
т° — модальность ионов в стандартном состоянии, численно равная 1 моль-кг-1;
И — стандартная ЭДС ячейки с водородным и хлорсеребряным полуэлементами (так как по определению стандартный потенциал водородного электрода равен нулю при всех температурах, то И соответствует стандартному потенциалу хлорсеребряного электрода), зависимость которой от температуры представлена в таблице А. 1.
Значение величины И определяют на основе измеренной ЭДС ячейки IV:
Pt | Н2 (газ, р = 1 атм = 101325 Па)|НС1 (0,01 моль/л) | AgCl | Ag IV
и вычисляют по уравнению (А.1), учитывая, что унуС1 = у2, где у+— средний ионный коэффициент активности соляной кислоты данной концентрации.
Уравнение (А.1) можно привести к следующему виду:
-lg (тн YH Та / т°) = (Е — ЕР)/к + lg (та / тР). (А.2)
Значение величины минус lg (тн ун уС1 / т°) = — lg (вн уС1) находят для трех концентраций хлорид-ионов та. По этим точкам в координатах минус lg (тн ун уС1 / т°) = / (тС1) проводят экстраполяцию к тС1 —> 0. Значения pH реперного буферного раствора вычисляют по формуле
pH = - lg (flH Jcl)m _^0 + lg (Yc)m ^0 » (A-3)
Cl Cl
где ионный коэффициент активности хлорид-ионов уС1 можно вычислить по условию Бейтса—Гуггенгей-ма по формуле
(А.4)
lgycl = - А (I/т0)1/2 / [1 + 1,5 (I/т°) V2]
(/<0,1 моль/кг),
где / — ионная сила раствора;
А — константа Дебая—Хюккеля (таблица А.1).
|
Температура, °С |
/°, мВ |
Коэффициент наклона к, мВ |
А |
|
0 |
236,55 |
54,199 |
0,4918 |
|
5 |
234,13 |
55,191 |
0,4952 |
|
10 |
231,42 |
56,183 |
0,4988 |
|
15 |
228,57 |
57,175 |
0,5026 |
|
20 |
225,57 |
58,168 |
0,5066 |
|
25 |
222,34 |
59,160 |
0,5108 |
|
30 |
219,04 |
60,152 |
0,5150 |
|
35 |
215,65 |
61,144 |
0,5196 |
|
40 |
212,08 |
62,136 |
0,5242 |
|
45 |
208,35 |
63,128 |
0,5291 |
|
50 |
204,49 |
64,120 |
0,5341 |
|
55 |
200,56 |
65,112 |
0,5393 |
|
60 |
196,49 |
66,104 |
0,5448 |
|
70 |
187,82 |
68,089 |
0,5562 |
|
80 |
178,73 |
70,073 |
0,5685 |
|
90 |
169,52 |
72,057 |
0,5817 |
|
95 |
165,11 |
73,049 |
0,5886 |
Таблица А.1 — Зависимость стандартной ЭД С ЕР, коэффициента наклона к и константы Дебая—Хюккеля А от температуры
ПРИЛОЖЕНИЕ Б (справочное)
ПРИГОТОВЛЕНИЕ РЕПЕРНОГО БУФЕРНОГО РАСТВОРА
Для приготовления реперного буферного раствора рекомендуется использовать гидрофталат калия*. Значение pH его раствора с модальностью 0,05 моль • кг-1, определенное по приложению А, не должно отличаться при 25 °С более чем на ±0,003 от значения 4,005. Значения при других температурах должны соответствовать данным таблицы 1 настоящего стандарта с максимальным отклонением ±0,005 в интервале температур от 0 до 60 °С (кроме температуры 25 °С) и ±0,009 — в интервале температур от 60 до 95 °С.
*
Перед взвешиванием навески для приготовления реперного буферного раствора необходимо высушить гидрофталат калия в течение двух часов при 110 °С. Используемая для разведения вода должна иметь удельную электропроводность % < 2 • 10~4 Ом-1 • м-1 при 20 °С. РБР готовят растворением 10,138 г гидрофталата калия в воде и доведением затем объема раствора до 1 л при температуре 20 °С. Молярная концентрация этого раствора равна 0,04964 моль • л-1 и плотность его — 1,00300 г ем-3 при 20 °С.
Рекомендуется использовать гидрофталат калия, поверенный в ГМНЦ ВНИИФТРИ.
УДК 543.257.1.085:006.354 МКС 71.040.40 Т88.5 ОКСТУ 0008
Ключевые слова: буферные растворы, реперный буферный раствор, эталонные буферные растворы, рабочие эталоны pH, тикала pH, электрохимическая ячейка
7