ГОСТ 32427-2013
Методы испытаний химической продукции, представляющей опасность для окружающей среды. Определение биоразлагаемости: 28-дневный тест
Купить ГОСТ 32427-2013 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает методы испытаний для определения способности химических веществ подвергаться биоразложению в аэробной водной среде.
Идентичен OECD Test No 301:1992
Оглавление
1 Область применения
2 Термины и определения
3 Основные требования к условиям, обеспечению и проведению испытаний химической продукции, представляющей опасность для окружающей среды, на определение биоразлагаемости в 28-дневном тесте
3.1 Общие принципы проведения испытаний
3.2 Информация об исследуемом веществе
3.3 Применение и подбор методов испытаний
3.4 Пороговые значения
3.5 Референтные (стандартные) вещества
3.6 Воспроизводимость экспериментов
4 Общие процедуры и реактивы для проведения испытаний химической продукции, представляющей опасность для окружающей среды, на определение биоразлагаемости в 28-дневном тесте
4.1 Вода
4.2 Питательная среда
4.3 Методы внесения тестируемого и референтного веществ
4.4 Посевная культура (инокулят)
4.5 Предварительная подготовка инокулята
4.6 Абиотический контроль
4.7 Количество колб и образцов
5 Данные и отчет о проведении эксперимента
5.1 Обработка результатов
5.2 Достоверность экспериментов
5.3 Отчет о проведении испытания
6 Метод А. Определение поглощения растворенного органического углерода
6.1 Общие сведения и принцип метода
6.2 Описание метода
6.3 Процедура эксперимента
6.4 Данные и отчет о проведении эксперимента
7 Метод В. Определение выделения диоксида углерода (СО2)
7.1 Общие сведения и принцип метода
7.2 Описание метода
7.3 Процедура эксперимента
7.4 Данные и отчет о проведении эксперимента
8 Метод С. Модифицированный тест MITI (I)
8.1 Общие сведения и принцип метода
8.2 Описание метода
8.3 Процедура эксперимента
8.4 Данные и отчет о проведении эксперимента
9 Метод D. Испытание в закрытом сосуде
9.1 Общие сведения и принцип метода
9.2 Описание метода
9.3 Процедура эксперимента
9.4 Данные и отчет о проведении эксперимента
10 Метод Е. Модифицированный тест ОЭСР
10.1 Общие сведения и принцип метода
10.2 Описание метода
10.3 Процедура эксперимента
10.4 Данные и отчет о проведении эксперимента
11 Метод F. Манометрический метод определения БПК
11.1 Общие сведения и принцип метода
11.2 Описание метода
11.3 Процедура эксперимента
11.4 Данные и отчет о проведении испытания
Приложение А (обязательное) Оценка способности к биоразложению химических веществ, обладающих вероятной токсичностью для инокулята
Приложение Б (обязательное) Определение способности к биодеградации плохо растворимых веществ
Приложение В (обязательное) Вычисление и определение соответствующих итоговых параметров
Приложение Г (обязательное) Корректировка потребления кислорода с учетом нитрификации
Приложение Д (рекомендуемое) Технические спецификации для метода А — Определение поглощения растворенного органического углерода
Приложение Е (рекомендуемое) Технические спецификации для метода В - Определение выделения диоксида углерода (СО2)
Приложение Ж (рекомендуемое) Технические спецификации для метода С - Модифицированный тест MITI (I)
Приложение И (рекомендуемое) Технические спецификации для метода В - Испытание в закрытом сосуде
Приложение К (рекомендуемое) Технические спецификации для метода Е - Модифицированный тест ОЭСР
Приложение Л (рекомендуемое) Технические спецификации для метода F - Манометрический метод определения БПК
Библиография
| Дата введения | 01.08.2014 |
|---|---|
| Добавлен в базу | 01.10.2014 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 05.11.2013 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 61-П |
|---|---|---|---|
| 22.11.2013 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 770-ст |
| Разработан | ФГУП ВНИЦ СМВ | ||
| Издан | Стандартинформ | 2014 г. |
Testing methods of chemicals of environmental hazard. Definition of biodegradability: 28-day test
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7
стр. 8

стр. 9
стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
ГОСТ
32427—
2013
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫОпределение биоразлагаемости: 28-дневный тест
(OECD, Test No301:1992, IDT)
Издание официальное
Москва
Стандартинформ
2014
Предисловие
Цели, основные принципы и порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский центр стандартизации, информации и сертификации сырья, материалов и веществ» (ФГУП «ВНИЦСМВ»)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (Росстандарт)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 5 ноября 2013 г. № 61-П)
За принятие проголосовали:
|
Краткое наименование страны по МК(ИС0 3166) 004—97 |
Код страны по МК (ИСО 3166) 004—97 |
Сокращенное наименование национального органа по стандартизации |
|
Азербайджан |
AZ |
Аз стандарт |
|
Армения |
AM |
Минэкономики Республики Армения |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Казахстан |
KZ |
Госстандарт Республики Казахстан |
|
Киргизия |
KG |
Кыргызстандарт |
|
Молдова |
MD |
Молдова-Стандарт |
|
Россия |
RU |
Росстандарт |
|
Таджикистан |
TJ |
Таджикстандарт |
|
Туркменистан |
TM |
Главгосслужба «Туркменстандартлары» |
|
Узбекистан |
UZ |
Узстандарт |
|
Украина |
UA |
Минэкономразвития Украины |
4 Настоящий стандарт идентичен международному документу OECD Test No 301:1992 «Ready Biodegradability» (Тест № 301 «Быстрая биоразлагаемость»).
Перевод с английского языка (еп).
Степень соответствия — идентичная (IDT)
5 Приказом Федерального агентства по техническому регулированию и метрологии от 22 ноября 2013 г. № 770-ст межгосударственный стандарт ГОСТ 32427-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 августа 2014 г.
6 ВВЕДЕН ВПЕРВЫЕ
7 ПЕРЕИЗДАНИЕ. Июль 2014 г.
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячных информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомления и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2014
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
4.5 Предварительная подготовка инокулята
Инокулят должен быть предварительно подготовлен к эксперименту, но не может быть предварительно адаптирован к исследуемому веществу. Предварительная подготовка заключается в аэрации (в питательной среде) активного ила или воды вторичных отстойников в течение 5—7 дней при температуре проведения испытания. В некоторых случаях предварительная подготовка увеличивает точность методов испытаний, уменьшая количество холостых результатов. Подобная подготовка не является необходимой для посевной культуры для метода MITI (метод С).
4.6 Абиотический контроль
При необходимости можно оценить способность исследуемого вещества к абиотическому разложению путем определения поглощения РОУ, потребления кислорода или выделения диоксида углерода в стерильных контрольных пробах, не содержащих посевной культуры. Стерилизация осуществляется мембранной фильтрацией (от 0,2 до 0,45 мкм) или добавлением соответствующего токсичного компонента необходимой концентрации. Если используется мембранная фильтрация, забор образцов осуществляется асептически для обеспечения стерильности. За исключением случаев, когда адсорбция исследуемого вещества была заранее исключена, испытания на биоразложение, такие как поглощение РОУ, особенно с использованием инокулята из активного ила, должны включать абиотический контроль с инокулятом и токсичным компонентом.
4.7 Количество колб и образцов
4.7.1 Необходимо использовать как минимум две колбы или емкости, содержащие исследуемое вещество и посевную культуру и, как минимум, две емкости, содержащие только посевную культуру. Одной емкости достаточно для проведения испытания с референтным веществом и инокулятом, а также, при необходимости, для исследования токсичности, абиотического разложения и контроля адсорбции. Для методов испытания а «закрытом сосуде» (метод D) и MITI (метод С) существуют специальные требования к количеству экспериментальных емкостей. Данные требования указаны в соответствующих разделах для каждого метода. Измерение РОУ и/или других характеристик для экспериментальной и контрольной емкостей необходимо проводить параллельно. Желательно измерения РОУ в других флаконах проводить в нескольких параллелях, однако это не всегда возможно.
4.7.2 Необходимо представить достаточное количество образцов и данных для оценки процента разложения в 10-дневном интервале, однако точный момент наступления лаг-фазы определить невозможно из-за широкого диапазона лаг-фаз и скоростей разложения вещества. В методе MITI (метод С) и при использовании автоматического респирометра в манометрическом методе определения ВПК (метод F), забор проб на потребление кислорода не представляет затруднений. В последнем методе ежедневный отбор данных является достаточным, если не используется автоматический респирометр. Специальные указания по отбору проб приведены в соответствующем разделе отдельно для каждого метода.
5 Данные и отчет о проведении эксперимента
5.1 Обработка результатов
5.1.1 При вычислении процента биоразложения D(, используют средние значения повторных измерений одного и того же параметра в экспериментальных емкостях и в контроле с посевной культурой. Формулы для вычисления приведены в соответствующем разделе отдельно для каждого метода. Процесс деградации представляется графически, и, при необходимости, на графике обозначается 10-дневный интервал. Необходимо вычислить и указать в отчете достигнутое разложение в процентах и величину плато или в конце эксперимента и/или в конце 10-дневного интервала, если это требуется. В манометрическом методе определения ВПК, азотсодержащие химические вещества могут повлиять на значение поглощения кислорода за счет процесса нитрификации (см. приложения В и Г). Кроме того, если ТПК не может быть вычислено в силу того, что состав тестируемого материала недостаточно определен, для вычисления процента биодеградации может использоваться величина ХПК. Однако, необходимо принять во внимание, что величина ХПК, как правило, не столь высока, как ТПК, поскольку некоторые химические вещества очень плохо окисляются в эксперименте на ХПК, что может привести к ошибочно высоким показателям биоразложения.
6
ГОСТ 32427-2013
5.1.2 Когда известны определенные химические аналитические данные, первичное биологическое разложение вычисляют по следующей формуле:
Sb~Sa
Dt---xioo, (1)
Sb
где Dt — первичная деградация за время t, %, обычно 28 дней;
Sg — остаточное количество исследуемого химического вещества в инокулированной питательной среде в конце исследования, мг;
Sb — остаточное количество исследуемого химического вещества в абиотическом контрольном эксперименте в конце исследования, мг.
5.2 Достоверность экспериментов
5.2.1 Эксперимент считают достоверным, если различие максимумов повторных величин разложения исследуемого вещества на плато, либо в конце эксперимента, либо в конце 10-дневного интервала (в зависимости от необходимости), составляет менее 20 % и, если процент биологического разложения референтного вещества достигает порогового значения, к 14 дню эксперимента. Если какое-либо условие из перечисленных выше не соблюдается, эксперимент необходимо повторить. В силу строгости методов низкие значения экспериментальных величин не обязательно означают, что исследуемое вещество не разлагается микроорганизмами в природных условиях, но указывают, что необходимо проведение дополнительной оценки способности к биоразложению.
5.2.2 Если в эксперименте на токсичность, содержащем как исследуемое, так и референтное вещества, в течение 14 дней демонстрируется менее, чем 35 % деградации (на основании РОУ) или менее, чем 25 % деградация (на основании полного ТПК или ТС02), исследуемое вещество может быть признано ингибирующим (см. приложение А). Серия экспериментов должна быть проведена повторно с более низкий концентрацией исследуемого вещества (если это может быть сделано без серьезного влияния на точность определения РОУ) и/или с более высокой концентрацией посевной культуры, но не более, чем 30 мг/л в пересчете на твердое вещество.
5.2.3 Прочие условия достоверности результатов испытаний, индивидуальные для различных методов, приведены в соответствующих разделах.
5.3 Отчет о проведении испытания
Отчет о проведении испытания должен включать нижеследующие разделы:
5.3.1. Исследуемое вещество.
5.3.1 Физическая природа и, при необходимости, физико-химические свойства.
5.3.2 Идентификационные данные.
5.3.2. Условия проведения испытания.
5.3.2.1 Инокулят: природа и источник образца, концентрация и предварительная подготовка.
5.3.2.2 Соотношение и характеристики промышленных сточных вод в сбросах (если это известно).
5.3.2.3 Продолжительность эксперимента, температура.
5.3.2.4 В случае исследования плохо растворимых веществ методы подготовки экспериментальных растворов/суспензий.
5.3.2.5 Используемый экспериментальный метод причины и научные обоснования любых изменений хода выполнения эксперимента.
5.3.3. Результаты эксперимента:
5.3.3.1 Данные эксперимента в табличной форме.
5.3.3.2 Любые наблюдаемые явления ингибирования.
5.3.3.3 Любая наблюдаемая абиотическая деградация.
5.3.3.4 Определенные химические аналитические данные при наличии.
5.3.3.5 Аналитические данные по промежуточным соединениям при наличии.
5.3.3.6 График зависимости разложения (в процентах) от времени для исследуемого и стандартных веществ, лаг-фазы, фазы деградации, 10-дневные интервалы и наклон кривой.
5.3.3.7 Удаление (в процентах) в плато — фазе, в конце эксперимента и/или в конце 10-дневного интервала.
5.3.4. Обсуждение результатов.
7
6. Метод А. Определение поглощения растворенного органического углерода
6.1 Общие сведения и принцип метода
6.1.1 Общие сведения относительно оценки способности к биоразложению приведены в разделе 5. Метод А может использоваться для нелетучих веществ, имеющих растворимость в воде, как минимум, 100 мг/л. Должно быть известно содержание углерода в исследуемом образце и, желательно, чистота или относительное содержание основных компонентов. Данный метод фактически идентичен ISO 7827—1984. Также метод А подобен методу Е (Модифицированному тесту ОЭСР), но допускает использование более высоких концентраций клеточной культуры.
6.1.2 Измеренный объем питательной среды с инокулянтом, содержащей известную концентрацию исследуемого вещества (от 10 до 40 мг РОУ/л) в качестве единственного номинального источника органического углерода, подвергается аэрации в темноте или при рассеянном свете при температуре (22 ± 2) °С. Процесс биологического разложения сопровождается анализом РОУ через короткие интервалы в течение 28-дневного периода. Степень биологического разложения вычисляется как процент величины выделенного РОУ (с поправкой на контрольный эксперимент с инокулянтом) от его первоначального количества. Первичная биоразлагаемость также может вычисляться с помощью дополнительного химического анализа тестируемого вещества, который проводится в начале и в конце инкубации.
6.2 Описание метода
6.2.1 Оборудование
При проведении эксперимента используется стандартное лабораторное оборудование, а также:
- конические колбы объемом от 250 мл до 2 л, в зависимости от объема, необходимого для анализа РОУ. Колбы должны быть тщательно вымыты (например, с использованием спиртового раствора соляной кислоты), промыты водой и высушены перед каждым экспериментом;
- аппарат для встряхивания — для размещения конических колб с автоматическим контролем температуры или с возможностью использования при постоянной комнатной температуре, достаточной мощности для поддержания аэробных условий во всех колбах;
- аппарат для фильтрации с подходящими мембранами;
- аппарат для измерения концентрации РОУ (DOC анализатор);
- прибор для определения растворенного кислорода (для проверки аэробных условий эксперимента);
- центрифуга.
6.2.2 Вода
6.2.3 Основные растворы для питательной среды
Готовят следующие основные растворы, реактивы, чда:
(a) калия дигидроортофосфат, КН2Р04 8,50 г
дикалия гидрофосфат, К2НР04 21,75 г
динатрия гидроортофосфат, дигидрат, Na2HP04-2H20 33,40 г
хлорид аммония, NH4CI 0,50 г
Растворяют в воде и доводят до 1 литра. pH раствора должен составлять 7.4.
(b) кальция хлорид безводный, СаС12 27,50 г
или
кальция хлорид дигидрат, СаС12-2Н20 36,40 г
Растворяют в воде и доводят до 1 л.
(c) магния сульфат гептагидрат, MgS04-7H20 22,50 г
Растворяют в воде и доводят до 1 литра.
(d) железа (III) хлорид гексагидрат, FeCI3-6H20 0,25 г
Растворяют в воде и доводят до 1 л.
Характеристики воды, которая должна использоваться в эксперименте, см. раздел 4.
Примечание — Для того, чтобы избежать необходимости приготовления данного раствора непосредственно перед использованием, в свежеприготовленный раствор добавляют одну каплю концентрированной соляной кислоты HCI или 0,4 г этилендиаминтетрауксусной кислоты (ЭДТА динатриевая соль) на 1 л.
Если в растворах образуются осадки, необходимо заменить их свежими растворами.
6.2.4 Приготовление питательной среды
10 мл раствора (а) смешивают с 800 мл воды, затем добавляют 1 мл растворов (Ь), (с) и (d) и доводят объем до 1 л.
6.2.5 Приготовление раствора тестируемых веществ
Если растворимость вещества превышает 1 г/л, то в небольшом количестве воды растворяют соответственно от 1 до 10 г исследуемого или референтного вещества и доводят объем до 1 л. В ином случае, готовят основные растворы в питательной среде или добавляют химическое вещество непосредственно к питательной среде, предварительно удостоверившись, что вещество растворилось.
6.2.6 Инокулят
Инокулят может быть получен из различных источников: активного ила, сточных вод, поверхностных вод, почв, или их смеси.
6.2.7 Инокулят из активного ила
6.2.7.1 Отбирают свежий образец активного ила из аэротенка очистных сооружений или из лабораторной установки переработки бытовых сточных вод. При необходимости отфильтровывают крупные частицы через мелкое сито, затем выдерживают раствор в аэробных условиях.
6.2.7.2 Другим способом активный ил, после удаления крупных частиц, отстаивают или центрифугируют (например, 1100 g в течение 10 минут). Удаляют надосадочную жидкость. Осадок промывают в питательной среде. Смешивают концентрированный ил с питательной средой, для получения концентрации от 3 до 5 г сухого веса на 1 л. Затем аэрируют.
6.2.7.3 Ил необходимо забирать с очистных сооружений, работающих в нормальном режиме. Если ил взят с крупнотоннажных очистных сооружений, или предполагается, что он содержит ингибиторы, его необходимо промыть. Повторно взвешенный ил после тщательного перемешивания отстаивают или центрифугируют, удаляют супернатант и снова повторно готовят суспензию промытого ила в дополнительном объеме питательной среды. Эту процедуру повторяют до тех пор, пока ил не будет очищен от взвешенных веществ или ингибиторов.
6.2.7.4 После приготовления суспензии активного ила, или из необработанного ила, непосредственно перед использованием определяют величину сухого остатка.
6.2.7.5 В дальнейшем можно гомогенизировать активный ил (от 3 до 5 г сухого веса 1 л). Обработку активного ила проводят в гомогенизаторе Уоринга в течение 2 минут на средней скорости. Гомогенизированный ил отстаивают в течение минимум 30 минут, или при необходимости дольше, и декантируют жидкость для использования в качестве посевного материала с концентрацией примерно 10 мл/л питательной среды.
6.2.8 Прочие источники посевной культуры
6.2.8.1 Другим способом инокулят может быть получен из вторичных отстойников очистных сооружений или лабораторной установки по переработке бытовых сточных вод. Отбирают свежий образец и сохраняют его в аэробных условиях во время транспортировки. Образец отстаивают в течение 1 часа или фильтруют его через грубую фильтровальную бумагу, отфильтрованные сточные воды или фильтрат выдерживают в аэробных условиях в течение необходимого времени. До 100 мл подобной посевной культуры может использоваться на 1 л питательной среды.
6.2.8.2 Еще одним источником посевной культуры могут служить природные поверхностные воды. В данном случае, забирают образец соответствующих поверхностных вод, например, вод реки, озера, и сохраняют в аэробных условиях в течение необходимого времени. При необходимости, проводят концентрирование посевной культуры фильтрацией или центрифугированием.
6.2.9 Предварительная подготовка инокулята
Инокулят должен быть предварительно подготовлен к условиям проведения эксперимента, но не может быть заранее адаптирован к тестируемому веществу. Предварительная подготовка заключается в аэрации активного ила (в питательной среде) или воды из вторичных отстойников в течение 5—7 дней при температуре проведения исследования. Предварительное создание условий иногда улучшает точность метода испытаний, уменьшая количество холостых значений.
9
6.2.10 Подготовка колб
6.2.10.1 В качестве образца: добавьте по 800 мл питательной среды в двухлитровые конические колбы и достаточное количество основных растворов исследуемого и референтного веществ в отдельные колбы так, чтобы концентрация химического эквивалента составляла от 10 до 40 мг РОУ/л. Измерьте значения pH и, при необходимости, доведите его до 7,4. Добавьте в колбы активный ил или другой источник посевной культуры, чтобы финальная концентрация не превышала 30 мг по сухому остатку/л. Также подготовьте контрольные пробы с посевной культурой в минеральной среде, но без добавления исследуемого или стандартного веществ.
6.2.10.2 При необходимости используют одну емкость для проверки возможной ингибирующей активности исследуемого вещества, внося инокулянт, содержащий сопоставимые концентрации исследуемого и референтного веществ в питательной среде.
6.2.10.3 Кроме того, если требуется, определите деградацию в абиотических условиях путем отстаивания исследуемого вещества в колбе простерилизованного неинокулированного раствора вещества. Стерилизация раствора проводится мембранной фильтрацией (от 0,2 до 0,45 мкм) или добавлением подходящего токсичного вещества в соответствующей концентрации.
6.2.10.4 Дополнительно, если ожидается, что исследуемое вещество значительно адсорбируется на стекле, иле и т. д., проводят предварительную оценку для определения вероятной степени адсорбции и, таким образом, пригодности метода для данного вещества (см. таблицу 1). Готовят колбу, содержащую исследуемое вещество, посевную культуру и стерилизующий агент.
6.2.10.5 Доводят объемы питательной среды во всех колбах до 1 литра и, после перемешивания, отбирают образец из каждой колбы для определения начальной концентрации РОУ в параллельных экспериментах (см. приложение В, пункт В.4). Закрывают горлышко колб (например, алюминиевой фольгой) таким образом, чтобы обеспечить свободный воздухообмен между колбой и окружающей атмосферой. Для начала эксперимента устанавливают емкости в аппарате для встряхивания.
6.2.11 Количество колб
В обычном случае используются следующие колбы:
- колбы 1 и 2, содержащие исследуемое вещество и посевную культуру (экспериментальная суспензия);
- колбы 3 и 4, содержащие только посевную культуру (контрольный эксперимент с посевной культурой);
- колба 5, содержащая референтное вещество и посевную культуру (контроль экспериментальных процедур); и, предпочтительно,
а также, при необходимости
- колба 6, содержащая исследуемое вещество и стерилизующий агент (абиотический стерильный контрольный эксперимент);
- колба 7, содержащая исследуемое вещество, посевную культуру и стерилизующий агент (контроль адсорбции);
- колба 8, содержащая исследуемое вещество, стандартное вещество и посевную культуру (контроль токсичности).
6.3 Процедура эксперимента
6.3.1 Определение растворенного органического углерода
В течение эксперимента определяют концентрацию РОУ в образцах из каждой колбы в параллельных экспериментах в определенных временных интервалах. Обязательно параллельное определение РОУ в экспериментальной суспензии и в контрольном эксперименте с посевной культурой. Желательно определять РОУ и в других колбах также параллельно, однако это не всегда возможно.
6.3.2 Отбор проб
Для каждого определения берут только минимально необходимый объем экспериментальной суспензии. Прежде, чем осуществлять отбор проб, необходимо устранить любые потери вследствие испарения путем добавления соответствующего количества воды. Тщательно перемешивают питательную среду до отбора образца так, чтобы материал, адсорбированный на стенках емкости, был смыт и растворен до отбора пробы. Сразу после отбора пробы ее фильтруют через мембранный фильтр или центрифугируют (см. приложение В, пункт 4). Анализ пробы, отфильтрованной или обработанной в центрифуге, проводят в тот же день, в ином случае, хранят при температуре от 2°С до 4°С в течение максимум 48 ч или при температуре ниже минус 18 в течение более длительного периода.
6.3.3 Частота отбора проб
Отобранное количество проб должно быть достаточным для оценки процента деградации в 10-дневный период. Точной схемы отбора проб не существует. Если анализ производится в день отбора проб, исходя из результатов данного анализа, необходимо оценить следующее время отбора пробы. Если пробы сохраняются, то отбор проб производится ежедневно или раз в 2 дня. Сначала необходимо провести анализ последней пробы (28 день) и, путем постепенного обратного отбора соответствующих образцов для анализа, можно получить качественное описание кривой биологического распада с относительно небольшим количеством определений. Конечно, если в последней пробе (28 день) демонстрируется отсутствие биоразложения, дальнейшего анализа проб проводить не нужно.
6.4 Данные и отчет о проведении эксперимента6.4.1 Обработка результатов
6.4.1.1 Данные эксперимента должны приводиться в прилагаемом отчете.
6.4.1.2 Процент деградации (Dt) в каждый период времени отбора пробы должен быть вычислен отдельно для каждой колбы, содержащей исследуемое вещество (т.е. колбы 1 и 2) с использованием средних значений параллельных измерений РОУ (см. технические спецификации (образец в приложении Д)) для того, чтобы можно было оценить достоверность эксперимента. Процент деградации вычисляется по формуле (2)
Ct~Cbl(t) Со ~ СЫ(о)
X 100,
(2)
где Dt — деградация в момент времени t, %;
С0 — начальная концентрация РОУ в инокулированной питательной среде, содержащей исследуемое вещество, мг РОУ/л;
Ct — средняя концентрация РОУ в инокулированной питательной среде, содержащей исследуемое вещество в момент времени t, мг РОУ/л;
СЫ(0) — начальная концентрация РОУ в контрольном эксперименте с посевной культурой, мг РОУ/л;
Cbj(t) — средняя концентрация РОУ в контрольном эксперименте в момент времени t, мг РОУ/л.
Все концентрации измеряются экспериментально.
6.4.1.3 Если эксперимент удовлетворяет критериям достоверности, необходимо представить ход процесса разложения на графике, используя средние данные для колб, содержащих исследуемое вещество. На графике необходимо представить 10-дневный интервал. В зависимости оттого, что необходимо, вычисляют и указывают в отчете процент удаления в плато-фазе в конце эксперимента и/или в конце 10-дневного интервала.
6.4.1.4 Если доступны определенные химические аналитические данные, вычисляют основную биодеградацию (см раздел 5).
6.4.1.5 Когда используется абиотический контроль, вычисляют процент абиотической деградации по формуле
% абиотической деградации =
cs(o)-cs(t■) Cs(o)
хЮО,
(3)
где CS(0j — концентрация РОУ в стерильном контрольном образце в день 0,
CS(t) — концентрация РОУ в стерильном контрольном образце в день t.
6.4.2 Достоверность экспериментов
Критерии достоверности приведены в разделе 5.
6.4.3 Отчет о проведении эксперимента
Отчет о проведении испытания должен содержать информацию в соответствии с разделом 5.
6.4.4 Пример представления результатов эксперимента Образцы представления результатов приведены в приложении Д.
11
7 Метод В. Определение выделения диоксида углерода (С02)7.1 Общие сведения и принцип метода
7.1.1 Общие сведения относительно оценки способности к биоразложению приведены в соответствии с 4. Необходимо ознакомиться с данным разделом до начала проведения испытания. Метод В может использоваться для нелетучих исследуемых веществ. Также должно быть известно содержание углерода в исследуемом образце и, желательно, чистота или относительное содержание основных компонентов.
7.1.2 Измеренный объем инокулированной минеральной питательной среды, содержащий известную концентрацию исследуемого вещества (от 10 до 20 мг РОУ или ТПК/л) в качестве единственного номинального источника органического углерода, подвергается аэрации путем пропускания через раствор воздуха, не содержащего диоксида углерода, с контролируемой скоростью в темноте или при рассеянном свете. В течение 28 дней эксперимента деградация сопровождается определением объема выделенного диоксида углерода (С02). Диоксид углерода С02 улавливается раствором гидроксида натрия или бария и его количество измеряется титрованием остаточного гидроксида или по содержанию неорганического углерода. Количество углекислого газа, полученного из исследуемого вещества (с учетом результатов контрольного эксперимента с посевной культурой), выражается в процентахТС02. Степень биологического разложения может быть также вычислена путем дополнительного анализа РОУ, проведенного в начале и в конце инкубации.
7.2 Описание метода7.2.1 Оборудование
При проведении эксперимента используется стандартное лабораторное оборудование, а также:
a) колбы, объемом 2—5 л, оснащеных аэрационной трубкой, практически достигающей основания колбы и выходного отверстия (трубка не должна мешать работе магнитной мешалки во время ее использования);
b) магнитные мешалки, используемые при исследовании плохо растворимых веществ;
c) поглотительные сосуды для улавливания С02;
d) устройство для управления и измерения газового потока;
e) аппарат для поглощения углекислого газа, аппарат для подготовки воздуха, очищенного от углекислого газа в ином случае может использоваться смесь кислорода и азота без С02 из газовых баллонов, в правильных соотношениях (20 % 02: 80 % N2);
f) устройство для определения углекислого газа титриметрически или в форме неорганического анализа углерода;
д) устройство для мембранной фильтрации (дополнительно);
h) анализатор РОУ (дополнительно).
7.2.2 Вода
Характеристики воды, которая должна использоваться в эксперименте, приведены в разделе 4.
7.2.3 Основные растворы для питательной среды
Необходимо подготовить основные растворы, как описано в пункте 6.2.3.
7.2.4 Подготовка питательной среды
Необходимо подготовить питательную среду, как описано в пункте 6.2.4.
7.2.5 Приготовление раствора тестируемых веществ
Необходимо подготовить раствор тестируемых веществ, как описано в пункте 6.2.5. Для плохо растворимых веществ см. приложение Б.
7.2.6 Инокулят
7.2.6.1 Инокулят может быть получен из различных источников: активный ил; сточные воды; поверхностные воды, почвы, или их смесь.
7.2.6.2 Инокулят из активного ила
Необходимо подготовить инокулят из активного ила, как описано в пункте 6.2.7.
7.2.6.3 Другие источники инокулята
Также инокулят может быть получен из вторичных отстойников очистных сооружений или лабораторной установки, перерабатывающей бытовые сточные воды, или из поверхностных водоемов. Для более подробных сведений см. 6.2.8.
12
ГОСТ 32427-20137.2.7 Предварительная обработка инокулята
Необходимо подготовить инокулят из активного ила, как описано в пункте 6.2.9
7.2.8 Подготовка колб
7.2.8.1 Приведем пример:
значения (объем и вес) представлены для пяти литровых колб, содержащих 3 л суспензии. Если используются меньшие объемы, необходимо соответственно изменять объемы, учитывая, что образовавшийся углекислый газ должен быть измерен точно. В каждую 5-литровую колбу добавляют 2 400 мл питательной среды. Затем в колбу добавляют соответствующий объем подготовленного активного ила так, чтобы концентрация взвешенных твердых частиц в окончательном растворе инокулированной смеси (3 л) не превышала 30 мг/л. В ином случае сначала разбавляют готовый активный ил до получения суспензии концентрацией от 500 до 1000 мг/л в питательной среде прежде, чем добавить аликвоту суспензии в 5-литровую колбу для достижения концентрации 30 мг/л; это гарантирует большую точность (также, могут использоваться и другие источники посевной культуры, см. 6.2.8). Затем проводят аэрацию данных инокулированных смесей в течение ночи воздухом, не содержащим С02, для очистки системы от углекислого газа.
7.2.8.2 В дублирующие колбы добавляют отдельно исследуемое и референтное вещества в виде известных объемов основных растворов так, чтобы обеспечивались концентрации от 10 до 20 мг РОУ или ТПК/л с учетом добавления тестируемых веществ; некоторые колбы оставляют без добавления тестирующих веществ для проведения контрольного эксперимента с посевной культурой. Плохорастворимые вещества добавляют непосредственно в колбы по весу или по объему или руководствуются приложением Б. Доводят объемы суспензий во всех колбах до 3 л путем добавления питательной среды, ранее обработанной воздухом без содержания С02.
7.2.8.3 При необходимости используют одну колбу для исследования возможных ингибирующих эффектов исследуемого вещества, добавив исследуемое и референтное вещества в тех же концентрациях, в которых они присутствуют в остальных колбах.
7.2.8.4 Также, при необходимости, определяют, подвергается ли исследуемое вещество разложению в абиотических условиях с использованием стерилизованного неинокулированного раствора химического вещества. Стерилизацию можно провести, добавив токсичное вещество в соответствующей концентрации.
7.2.8.5 Если используется раствор гидроксида бария, соединяют три поглотителя, содержащие 100 мл 0,0125 М раствора гидроксида бария каждый, последовательно с каждой 5 литровой колбой. Данный раствор не должен содержать осажденных сульфатов или карбонатов, их концентрация должна быть измерена непосредственно перед использованием. Если используется гидроксид натрия, то необходимо соединить два поглотительных сосуда, второй используется в качестве контрольного для подтверждения того, что весь углекислый газ был поглощен первым. Поглотительные сосуды, оснащенные пробкой, подходят для проведения эксперимента. Добавляют 200 мл 0,05 М раствора гидроксида натрия в каждую колбу. Этого достаточно для того, чтобы обеспечить поглощение всего диоксида углерода, выделяющегося при полном разложении исследуемого вещества. Поскольку даже свежеприготовленный раствор гидроксида натрия будет содержать следовые количества карбонатов, необходимо делать поправку на них в контрольном эксперименте.
7.2.8.6 Дополнительно могут быть отобраны пробы для анализа РОУ (см. приложение В) и/или определенного химического анализа.
7.2.9 Количество колб
В общем случае, используются следующие колбы:
- колбы 1 и 2, содержащие исследуемое вещество и посевную культуру (тестовая суспензия);
- колбы 3 и 4, содержащие только инокулянт (нулевой контроль);
- колба 5, содержащая референтное вещество и посевную культуру (контроль экспериментальных процедур); и, предпочтительно,
а также
- колба 6, содержащая исследуемое вещество и стерилизующий агент (абиотический стерильный контроль);
- колба 7, содержащая исследуемое вещество, посевную культуру и стерилизующий агент (контроль адсорбции);
- колба 8, содержащая исследуемое вещество, референтное вещество и посевную культуру (контроль токсичности).
13
7.3 Процедура эксперимента
Начинают эксперимент, пропуская воздух, не содержащий С02, через суспензию со скоростью от 30 до 100 мл/мин.
7.3.1 Определение С02
7.3.1.1 Обязательно регистрировать выделение С02 в исследуемых суспензиях и контрольных экспериментах с посевной культурой параллельно и, желательно, проводить параллельные измерения и для прочих экспериментальных сосудов.
7.3.1.2 В течение первых 10 дней рекомендуется, чтобы анализ С02 проводился каждый 2 или 3 день, а затем, по крайней мере, каждый 5 день до 28 дня так, чтобы мог быть выявлен 10-дневный интервал. В те дни, когда проводятся измерения С02, разъединяют ближайший к экспериментальной колбе поглотитель гидроксида бария и титруют раствор гидроксида 0,05 М раствором HCI с использованием фенолфталеина в качестве индикатора. Оставшиеся абсорберы перемещают на одно место ближе к испытательному сосуду и помещают новый абсорбер, содержащий 100 мл свежего 0,0125 М раствора гидроксида бария, в конце ряда. При необходимости, титрование проводят, например, когда наблюдается существенное осаждение в первой ловушке и прежде, чем оно появится во второй, или, по меньшей мере, еженедельно. В альтернативном варианте, с использованием в качестве абсорбента гидроксида натрия (NaOH), пробу раствора гидроксида натрия забирают из абсорбера, ближайшего к экспериментальной колбе с помощью шприца. Необходимый объем пробы будет зависеть от используемого метода анализа углерода, но проба не должна значительно изменять объема абсорбционного раствора в течение эксперимента. Введите образец в часть неорганического углерода в углеродном анализаторе для прямого анализа выделяемого углекислого газа. Анализ содержимого второй ловушки необходимо проводить только по окончании эксперимента для корректировки с учетом возможного выноса диоксида углерода.
7.3.1.3 На 28 день исследования отбирают произвольные пробы для анализа РОУ и/или специфического химического анализа. Добавляют 1 мл концентрированной соляной кислоты в каждую экспериментальную колбу и проводят аэрацию содержимого в течение ночи для удаления диоксида углерода, присутствующего в исследуемых суспензиях. На 29 день эксперимента проводят последний анализ выделенного углекислого газа.
7.4 Данные и отчет о проведении эксперимента7.4.1 Обработка результатов
7.4.1.1 Данные эксперимента должны быть приведены в прилагаемом отчете.
7.4.1.2 Количество выделенного С02 вычисляется по количеству гидроксида, оставшегося в экспериментальной колбе. Когда в качестве абсорбента используется 0,0125 М раствор Ва(ОН)2, его оставшееся количество оценивается титрованием 0,05 М раствором HCI (для титрования 100 мл Ва(ОН)2 необходимо 50 мл HCI).
7.4.1.3 Поскольку 1 ммоль С02 образуется на каждый 1 ммоль Ва(ОН)2, прореагировавшего до ВаС12, и 2 ммоль HCI, необходимого для титрования оставшегося Ва(ОН)2, и, учитывая, что молекулярная масса С02 составляет 44 г, количество выделенного С02, (мг) вычисляется по формуле
0,05 х (50 - млНС1,т ) х 44
(4)
- р~-= 1,1 х (50 - млНС1,титр).
Таким образом, в данном случае, коэффициент преобразования объема HCI, необходимого для титрования, к массе выделенного С02 (мг) составляет 1,1. Вычисляют количество С02, полученного только из инокулята и инокулята с исследуемым веществом, используя соответствующие величины, полученные при титровании; разница данных показателей представляет собой количество С02, полученного только из одного только исследуемого вещества. Например, если на титрование в эксперименте только с инокулятом затрачено 48 мл HCI, а в эксперименте с инокулятом и исследуемым веществом — 45 мл, то:
количество С02 от инокулята = 1,1 * (50 - 48) = 2,2 мг
количество С02 от инокулята и экспериментального вещества = 1,1 х (50 - 45) = 5,5 мг и, таким образом, количество С02, полученного от исследуемого вещества, составляет 3,3 мг.
7.4.1.4 Процент биодеградации вычисляется по формулам (5), (6).
% деградация=
мз С02’ выдел -X 100
Thco х мг Исслед.вещ-ва, добавл
(5)
или
% деградация=
мзС02' выдел
-х 100,
мгТПК, (Эобаале эксп *3,67
(6)
где 3,67 — коэффициент преобразования (44/12) для углерода к углекислому газу. Процент биодеградации рассчитывают после любого временного интервала путем сложения величин процента ТС02’ вычисленных для каждого из дней, до необходимого момента, в которые производилось измерение.
7.4.1.5 В случае, если в качестве абсорбента используется раствор гидроксида натрия, вычисляют количество выделенного С02 после каждого временного интервала на основании концентрации неорганического углерода и объема использованного абсорбента.
Процент биоразлагаемости вычисляют по формуле (7).
% от Thco
НУ, мгиссл вещ.в0 НУ, мгконтр
-х 100.
ТПК, MSfog какиссл. вещ-во
(7)
7.4.1.6 Процесс деградации необходимо представить на графике и обозначить 10-дневный интервал. Кроме того, необходимо вычислить и представить в заключительном отчете процент удаления в плато-фазе, в конце эксперимента и/или, при необходимости, по окончании 10-дневного интервала.
7.4.1.7 При необходимости вычислите удаление РОУ, используя соотношение (2).
7.4.1.8 Когда проводится абиотический контрольный эксперимент, процент абиотической деградации вычисляют по формуле (8).
СО2 произ. в стерил. колбе на 28 день, мг
% абиотическая деградация = -х 100. (8)
ThC02, мг
7.4.2 Достоверность экспериментов
7.4.2.1 Содержание неорганического углерода в суспензии тестируемого вещества в питательной среде в начале эксперимента должно составлять менее 5 % ОУ, и полный объем выделенного С02 в контрольном эксперименте с посевной культурой в обычном случае не должен превышать 40 мг/л питательной среды. Если полученные величины превосходят 70 мг С02/л, данные и техника проведения эксперимента должны быть пересмотрены.
7.4.2.2 Прочие критерии достоверности эксперимента, приведенные в разделе 7.4.3, также могут использоваться.
7.4.3 Отчет о проведении испытания
Отчет о проведении эксперимента должен включать информацию согласно разделу 5. Образцы представления результатов приведены в приложении Е.
15
ГОСТ 32427-2013Содержание
1 Область применения..................................................................1
2 Термины и определения...............................................................1
3 Основные требования к условиям, обеспечению и проведению испытаний химической
продукции, представляющей опасность для окружающей среды, на определение биоразлагаемости в 28-дневном тесте...................................................2
3.1 Общие принципы проведения испытаний .............................................2
3.2 Информация об исследуемом веществе..............................................3
3.3 Применение и подбор методов испытаний.............................................3
3.4 Пороговые значения...............................................................3
3.5 Референтные (стандартные) вещества...............................................4
3.6 Воспроизводимость экспериментов..................................................4
4 Общие процедуры и реактивы для проведения испытаний химической продукции, представляющей опасность для окружающей среды, на определение биоразлагаемости
в 28-дневном тесте...................................................................4
4.1 Вода............................................................................4
4.2 Питательная среда................................................................4
4.3 Методы внесения тестируемого и референтного веществ................................4
4.4 Посевная культура (инокулят).......................................................5
4.5 Предварительная подготовка инокулята..............................................6
4.6 Абиотический контроль............................................................6
4.7 Количество колб и образцов........................................................6
5 Данные и отчет о проведении эксперимента...............................................6
5.1 Обработка результатов............................................................6
5.2 Достоверность экспериментов......................................................7
5.3 Отчет о проведении испытания......................................................7
6 Метод А. Определение поглощения растворенного органического углерода....................8
6.1 Общие сведения и принцип метода..................................................8
6.2 Описание метода.................................................................8
6.3 Процедура эксперимента..........................................................10
6.4 Данные и отчет о проведении эксперимента..........................................11
7 Метод В. Определение выделения диоксида углерода (С02)................................12
7.1 Общие сведения и принцип метода.................................................12
7.2 Описание метода................................................................12
7.3 Процедура эксперимента..........................................................14
7.4 Данные и отчет о проведении эксперимента..........................................14
8 Метод С. Модифицированный тест MITI (I)...............................................16
8.1 Общие сведения и принцип метода.................................................16
8.2 Описание метода................................................................16
8.3 Процедура эксперимента..........................................................17
8.4 Данные и отчет о проведении эксперимента..........................................18
9 Метод D. Испытание в закрытом сосуде.................................................19
9.1 Общие сведения и принцип метода.................................................19
9.2 Описание метода................................................................19
9.3 Процедура эксперимента..........................................................21
9.4 Данные и отчет о проведении эксперимента..........................................22
8 Метод С. Модифицированный тест MITI (I)
8.1 Общие сведения и принцип метода
8.1.1 Общие сведения относительно оценки способности к биоразложению приведены в разделе 8.4. Необходимо ознакомиться сданным разделом до начала проведения испытания. При использовании Метода С должны быть известны химическая формула исследуемого вещества, его чистота или относительные пропорции основных компонентов, необходимые для вычисления ТПК. Исследование нерастворимых и летучих веществ может быть проведено при условии проведения предварительной подготовки. Нерастворимые вещества должны быть диспергированы, например, с использованием материала очень мелкого помола или ультразвука, но не растворителей или эмульгаторов. Для летучих веществ объем свободного пространства для газа в автоматическом респирометре должен быть сведен к минимуму.
8.1.2 Потребление кислорода в растворе или суспензии тестируемого вещества в питательной среде, инокулированной специально выращенными, неадаптированными микроорганизмами, измеряется автоматически в течение 28 дней затемненным изолированным респирометром при температуре (25 + 1)°С. Выделенный углекислый газ поглощается натронной известью. Биоразлагаемость выражается как потребление кислорода в процентах (с учетом данных контрольного эксперимента с посевной культурой) от теоретического потребления кислорода (ТПК). Основная биоразлагаемость в процентах также вычисляется из дополнительного специфического химического анализа, который проводится в начале и в конце периода инкубации, и, при необходимости, окончательная биоразлагаемость путем анализа РОУ.
8.2 Описание метода
8.2.1 Оборудование
8.2.1.1 При проведении эксперимента используется следующее стандартное лабораторное оборудование:
a) автоматический электролитический прибор для измерения ВПК или респирометр, обычно оборудованный 6 колбами (300 мл каждая), и оснащенный чашками для абсорбента С02;
b) лабораторная комната с постоянной температурой и/или водяной баней, способной поддерживать температуру (25 ± 1)°С или точнее;
c) установка для мембранной фильтрации (дополнительно);
d) анализатор углерода (дополнительно).
8.2.1.2 Вода
8.2.1.3 Основные растворы для минеральной среды
Подготовьте следующие основные растворы, реактивы, чда:
a) калия д и гидроортофосфат, КН2Р04 8,50 г
дикалиягидрофосфат, К2НР04 21,75 г
динатриягидроортофосфат, додекагидрат, Na2HP04-12H20 44,60 г
хлорид аммония, NH4CI 1,70 г
Растворяют в воде и доводят до 1 литра. pH раствора должен составлять 7.2.
b) магния сульфат, гептагидрат, MgS04-7H20 22,50 г
Растворяют в воде и доводят до 1 литра.
c) кальция хлорид, безводный, СаС12 27,50 г
Растворяют в воде и доводят до 1 литра.
d) хлорид железа (III), гексагидрат, FeCI3-6H20 0,25 г
Растворяют в воде и доводят до 1 литра. pH раствора должен составлять 7,2.
8.2.1.4 Подготовка минеральной среды
Характеристики воды, которая должна использоваться в эксперименте, приведены в разделе 7.4.
Отберите по 3 мл каждого раствора (а), (Ь), (с) и (d) и доведите растворы до 1 литра.
8.2.1.5 Основные растворы исследуемых веществ
Если растворимость вещества превышает 1 г/л, растворяют от 1 до 10 г, по необходимости, исследуемого и референтного веществ в воде и доводят раствор до 1 литра. В ином случае готовят растворы в питательной среде или добавляют исследуемое вещество непосредственно к питательной среде. Для подготовки плохо растворимых веществ см. 7.2.1.6.
16
10 Метод Е. Модифицированный тест ОЭСР...............................................23
10.1 Общие сведения и принцип метода................................................23
10.2 Описание метода...............................................................23
10.3 Процедура эксперимента.........................................................24
10.4 Данные и отчет о проведении эксперимента.........................................24
11 Метод F. Манометрический метод определения ВПК......................................25
11.1 Общие сведения и принцип метода................................................25
11.2 Описание метода...............................................................25
11.3 Процедура эксперимента.........................................................26
11.4 Данные и отчет о проведении эксперимента.........................................27
Приложение А (обязательное) Оценка способности к биоразложению химических веществ,
обладающих вероятной токсичностью для инокулята...........................28
Приложение Б (обязательное) Определение способности к биодеградации плохо растворимых
веществ.................................................................28
Приложение В (обязательное) Вычисление и определение соответствующих итоговых
параметров..............................................................29
Приложение Г (обязательное) Корректировка потребления кислорода с учетом нитрификации.....31
Приложение Д (рекомендуемое) Технические спецификации для метода А. Определение
поглощения растворенного органического углерода............................32
Приложение Е (рекомендуемое) Технические спецификации для метода В. Определение
выделения диоксида углерода (С02).........................................34
Приложение Ж (рекомендуемое) Технические спецификации для метода С.
Модифицированный тест MITI (I)............................................35
Приложение И (рекомендуемое) Технические спецификации для метода Г. Испытание
в закрытом сосуде........................................................37
Приложение К (рекомендуемое) Технические спецификации для метода Е. Модифицированный
тест ОЭСР...............................................................39
Приложение Л (рекомендуемое) Технические спецификации для метода F. Манометрический
метод определения БПК...................................................41
Библиография........................................................................43
IV
ГОСТ 32427-2013Введение
Настоящий стандарт содержит описание шести методов, позволяющих выявить способность химических веществ подвергаться биоразложению в аэробной водной среде. В настоящем стандарте приведено описание следующих методов:
метод А: поглощение растворенного органического углерода (РОУ);
метод В: выделение диоксида углерода С02 (Модифицированный тест Штурма);
метод С: MITI (I) (Тест Министерства Международной торговли и Промышленности, Япония);
метод D: испытание в закрытом сосуде;
метод Е: модифицированный тест ОЭСР;
метод F: манометрическое определение ВПК.
Метод А идентичен ISO 7827—1984. Методы В, D и Е представляют собой модифицированные версии более ранних Руководящих документов ОЭСР, принятых в 1981 г. Метод F является новым, подобным методу С, главное отличие состоит в используемой посевной культуре.
За время использования данных шести методов, включая межпабораторный тест (кольцевой тест) ОЭСР 1988 г., был получен обширный практический материал. Накопленный опыт и кольцевой тест подтвердили, что все эти методы могут использоваться для оценки способности микроорганизмов к разложению. Однако, в зависимости от физических характеристик исследуемого вещества, может быть выбран тот или иной метод.
Общие указания, включая характерные для всех шести методов, представлены ниже. Детальные описания отдельных методов даны в соответствующих разделах (методы от А до F).
V
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТМЕТОДЫ ИСПЫТАНИЙ ХИМИЧЕСКОЙ ПРОДУКЦИИ, ПРЕДСТАВЛЯЮЩЕЙ ОПАСНОСТЬДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫОпределение биоразлагаемости: 28-дневный тест
ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫОпределение биоразлагаемости: 28-дневный тест
Testing methods for chemicals of environmental hazard. Definition of biodegradability: 28-day test
Дата введения — 2014—08—01
1 Область применения
Настоящий стандарт устанавливает методы испытаний для определения способности химических веществ подвергаться биоразложению в аэробной водной среде.
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями.
2.1 10-дневный интервал (10-d window): 10 дней с момента достижения 10 % биодеградации.
2.2 биоразлагаемое вещество (inherently biodegradable): Классификация химических веществ, для которых существуют определенные доказательства способности к биодеградации (первичной или полной) в любом испытании на способность к биологическому разложению.
2.3 биохимическое потребление кислорода, мг 02, ВПК (biochemical oxygen demand (BOD)): Количество кислорода, потребляемое при биохимическом окислении исследуемого вещества микроорганизмами в аэробных условиях. Примечание — также выражается как количество кислорода в мг, потребляемого на мг исследуемого вещества.
2.4 лаг-фаза (lag phase): Период от инокуляции теста на разложение до увеличения процента деградации приблизительно до 10 %. Характеризуется вариабельностью и плохой воспроизводимостью.
2.5 легкоразлагаемое вещество (readily biodegradable): Произвольная классификация химических веществ, прошедших определенные испытания на окончательную биодеградацию; испытания проводятся в строгих условиях, что позволяет предположить, что данные химические вещества будут подвергаться быстрой и полной биодеградации в водной среде при аэробных условиях.
2.6 неорганический углерод; НУ (inorganic carbon): Углерод входящий в состав неорганических молекул.
2.7 общий органический углерод; ООУ (total organic carbon (TOC)): Общее содержание органического углерода в образце (суммарное содержание органического углерода в растворе и суспензии).
2.8 общий углерод ОУ (total carbon (ТС)): Общее содержание органического и неорганического углерода в исследуемом образце.
2.9 первичная биоразлагаемость (primary biodegradation): Изменение в химической структуре вещества, вызванное биологическим действием, приводящим к утрате специфических свойств данного вещества.
2.10 полная биоразлагаемость (аэробная) (ultimate biodegradation): Уровень разложения, достигаемый при полном использовании микроорганизмами химического вещества, приводящий к образованию углекислого газа, воды, минеральных солей и новых микробиологических клеточных элементов (прирост биомассы).
Издание официальное
2.11 пригодность к очистке (treatability): Подверженность веществ к удалению во время биологической обработки сточных вод без оказания негативного влияния на обычный ход процессов очистки. В общем случае, биоразлагаемые вещества поддаются очистке, что не является характерным для всех биоразлагаемых веществ. Учитываются также и абиотические процессы.
2.12 растворенный кислород, мг/л; РК (dissolved oxygen, (DO)): Концентрация кислорода, растворенного в водном образце.
2.13 растворенный органический углерод; РОУ (dissolved organic carbon (DOC)): Количество органического углерода, присутствующего в растворе после фильтрования через мембранный фильтр с размером пор 0,45 мкм или после центрифугирования с ускорением порядка 4000 г (порядка 40 000 м/сек2) в течение 15 мин.
2.13 теоретическое выделение углекислого газа Тсо , мг: (theoretical carbon dioxide (ThC02)): Количество углекислого газа, вычисленное, исходя из известного или измеренного содержания углерода в исследуемом веществе, образующееся при его полной минерализации. Примечание — также выражается как количество углекислого газа в мг, образующегося на мг исследуемого вещества.
2.14 теоретическое потребление кислорода, мг; ТПК (theoretical oxygen demand (ThOD)): Общее количество кислорода, необходимое для полного окисления исследуемого химического вещества.
Примечание — ТПК вычисляется из молекулярной формулы и также может быть выражено как количество кислорода, потребляемое на мг исследуемого вещества.
2.15 фаза деградации (degradation phase): Время от окончания периода лаг — фазы до времени, когда деградация достигнет 90 % от максимально возможного уровня.
2.16 химическое потребление кислорода, мг; ХПК (chemical oxygen demand (COD)): Количество кислорода, потребляемое при химическом окислении исследуемого вещества кипящим раствором бихромата калия в кислоте.
Примечание — Также выражается как количество кислорода в мг, потребляемое на мг исследуемого вещества.
3 Основные требования к условиям, обеспечению и проведению испытаний химической продукции, представляющей опасность для окружающей среды, на определение биоразлагаемости в 28-дневном тесте3.1 Общие принципы проведения испытаний
3.1.1 Раствор или суспензия исследуемого вещества в минеральной питательной среде высевается и инкубируется в аэробных условиях в темноте или при рассеянном свете. Количество РОУ в исследуемом растворе, получаемое от посевного материала (инокулята), должно сохраняться на минимально возможном уровне, по сравнению с количеством органического углерода тестируемого вещества.
3.1.2 Для определения поправки на эндогенные эффекты инокулята могут быть проведены параллельные контрольные эксперименты с посевным материалом, но без внесения исследуемого вещества. Следует учитывать, что эндогенная активность клеток в присутствии химического вещества не будет точно и полностью соответствовать эндогенной активности в контрольном эксперименте. Для проверки воспроизводимости эксперимента параллельно ставится референтная (стандартная) смесь.
3.1.3 В общем случае биоразлагаемость сопровождается определением таких параметров, как РОУ, выделение С02 и потребление кислорода. Для определения начала и окончания биологического распада необходимо проводить измерения в достаточно частых интервалах. При использовании автоматических респирометров измерение осуществляется непрерывно. В некоторых случаях измерения РОУ проводятся в дополнение к каким-либо другим параметрам, но обычно это делается только в начале и в конце эксперимента. Также для оценки основной деградации исследуемого вещества и определения концентрации каких-либо промежуточных продуктов может использоваться специфический химический анализ. Это условие является обязательным в методе MITI (метод С).
3.1.4 В общем случае эксперимент длится в течение 28 дней, однако он может быть завершен и раньше (до истечения 28 дней), то есть, как только кривая биоразложения выйдет на плато как минимум для трех определений. Также эксперимент может быть продлен по истечении 28 дней, когда кривая показывает, что биологический распад начался, но плато-фаза не была достигнута к 28 дню, однако в таких случаях химическое вещество не будет классифицировано как биоразлагаемое.
3.2 Информация об исследуемом веществе
3.2.1 Для выбора наиболее подходящего метода необходимо иметь сведения о растворимости химического вещества, давлении паров и адсорбционных характеристиках. Для вычисления теоретических значений и/или проверки измеренных величин ТПК, Тсо , РОУ, ООУ и ХПК необходимо знать химическую или структурную формулу исследуемого вещества. Для интерпретации полученных результатов, особенно в случаях, когда результат находится близко к пороговому значению, требуется информация о чистоте или относительном соотношении главных компонентов в исследуемом материале.
3.2.2 Информация о токсичности исследуемого вещества на бактериальную культуру (приложение А) может быть крайне необходимой для выбора подходящих экспериментальных концентраций и иметь существенное значение для правильной интерпретации низких показателей биоразложения.
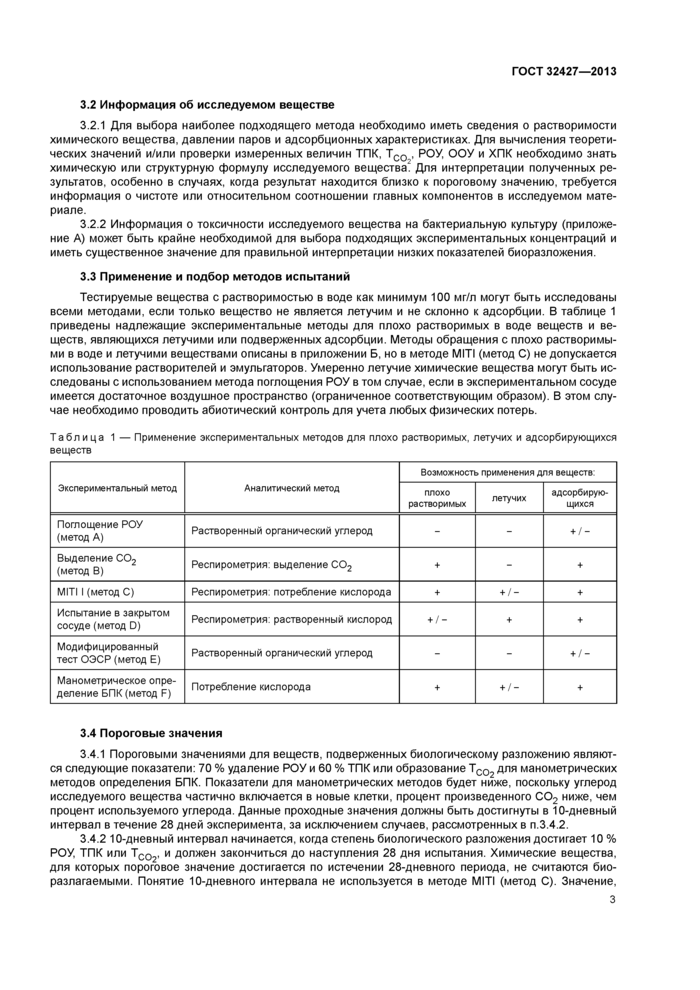
3.3 Применение и подбор методов испытаний
Тестируемые вещества с растворимостью в воде как минимум 100 мг/л могут быть исследованы всеми методами, если только вещество не является летучим и не склонно к адсорбции. В таблице 1 приведены надлежащие экспериментальные методы для плохо растворимых в воде веществ и веществ, являющихся летучими или подверженных адсорбции. Методы обращения с плохо растворимыми в воде и летучими веществами описаны в приложении Б, но в методе MITI (метод С) не допускается использование растворителей и эмульгаторов. Умеренно летучие химические вещества могут быть исследованы с использованием метода поглощения РОУ в том случае, если в экспериментальном сосуде имеется достаточное воздушное пространство (ограниченное соответствующим образом). В этом случае необходимо проводить абиотический контроль для учета любых физических потерь.
|
Таблица 1 — Применение экспериментальных методов для плохо растворимых, летучих и адсорбирующихся веществ | ||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||
3.4 Пороговые значения
3.4.1 Пороговыми значениями для веществ, подверженных биологическому разложению являются следующие показатели: 70 % удаление РОУ и 60 % ТПК или образование ТС02 Для манометрических методов определения ВПК. Показатели для манометрических методов будет ниже, поскольку углерод исследуемого вещества частично включается в новые клетки, процент произведенного С02 ниже, чем процент используемого углерода. Данные проходные значения должны быть достигнуты в 10-дневный интервал в течение 28 дней эксперимента, за исключением случаев, рассмотренных в п.3.4.2.
3.4.2 10-дневный интервал начинается, когда степень биологического разложения достигает 10 % РОУ, ТПК или ТСо2’ и должен закончиться до наступления 28 дня испытания. Химические вещества, для которых пороговое значение достигается по истечении 28-дневного периода, не считаются биоразлагаемыми. Понятие 10-дневного интервала не используется в методе MITI (метод С). Значение,
полученное в 14-дневном интервале, будет приемлемо в методе с использованием закрытого сосуда, если будет очевидно, что использование необходимого для оценки 10-дневного интервала количества сосудов затрудняет проведение эксперимента.
3.5 Референтные (стандартные) вещества
Для оценки правильности выполнения экспериментальных процедур проводят параллельное исследование референтных веществ, удовлетворяющих критериям способности к биоразложению. Исследование проводят в подходящих экспериментальных емкостях параллельно, как часть обычного эксперимента. В качестве стандартных веществ используют:
- анилин (свежедистиллированный);
- натрий уксуснокислый;
- натрия бензоат.
Данные стандартные вещества подвержены разложению во всех экспериментальных методах, даже в случаях, когда специально не вносится никакой инокулят.
3.6 Воспроизводимость экспериментов
Эксперименты по определению способности к биологическому разложению необходимо проводить как минимум дважды. В общем случае считается что, чем больше концентрация микроорганизмов, добавленных первоначально в экспериментальную среду, тем меньше будет расхождение между повторными экспериментами.
4 Общие процедуры и реактивы для проведения испытаний химической продукции, представляющей опасность для окружающей среды, на определение биоразлагаемости в 28-дневном тесте
Общие условия использования методов приведены в таблице 2. Оборудование и другие экспериментальные условия, имеющие отношение к определенному методу, описаны в соответствующем разделе отдельно для каждого метода.
4.1 Вода
При проведении исследования используется деионизированная или дистиллированная вода, не содержащая ингибирующих концентраций токсичных веществ (например, ионов Си2+). Содержание органического углерода в используемой воде не должно превышать 10 % от содержания органического углерода в тестовом материале. Высокая чистота используемой воды необходима для того, чтобы избежать получения холостых результатов. Загрязнение может появляться из-за содержания внутренних примесей и от ионообменных смол и продуктов жизнедеятельности микроорганизмов и водорослей. Для каждой серии экспериментов необходимо использовать воду только из одной партии, предварительно протестировав ее на содержание РОУ. Проведение такой проверки не является обязательным для метода D, однако величина потребления кислорода водой должна быть ниже (см. 9.4.1.1).
4.2 Питательная среда
Питательные среды готовят из основных растворов с соответствующей концентрацией минеральных компонентов, в частности, фосфата калия, фосфата натрия и хлорида аммония, хлорида кальция, сульфата магния и хлорида железа (III). Поскольку в методе Е используется очень бедная посевная культура, содержащая низкие концентрации микроэлементов и факторов роста, питательная среда для данного метода может быть обогащена дополнительными компонентами. Характеристики основных растворов минеральных солей, микроэлементов и факторов роста и используемые соотношения указаны в соответствующем разделе отдельно для каждого метода.
4.3 Методы внесения тестируемого и референтного веществ
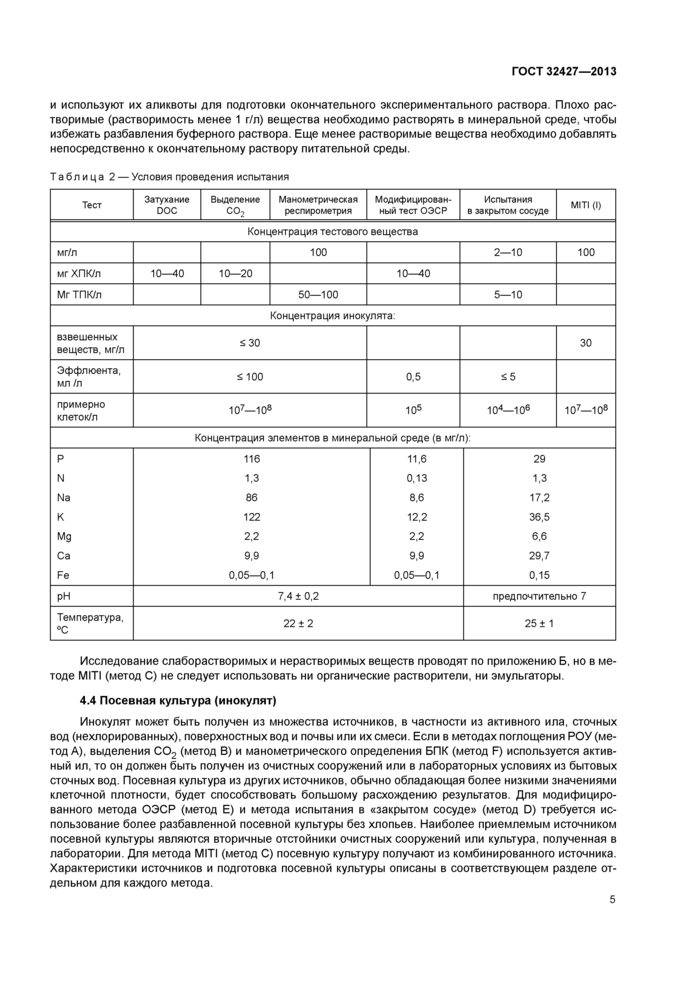
Метод, используемый для внесения тестируемого и референтного веществ к реакционной смеси, зависит от природы химического вещества, особенно от его растворимости в воде. Для веществ, обладающих растворимостью более 1 г/л, готовят основные растворы соответствующих концентраций 4
и используют их аликвоты для подготовки окончательного экспериментального раствора. Плохо растворимые (растворимость менее 1 г/л) вещества необходимо растворять в минеральной среде, чтобы избежать разбавления буферного раствора. Еще менее растворимые вещества необходимо добавлять непосредственно к окончательному раствору питательной среды.
|
Таблица 2 — Условия проведения испытания | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Исследование слаборастворимых и нерастворимых веществ проводят по приложению Б, но в методе MITI (метод С) не следует использовать ни органические растворители, ни эмульгаторы.
4.4 Посевная культура (инокулят)
Инокулят может быть получен из множества источников, в частности из активного ила, сточных вод (нехпорированных), поверхностных вод и почвы или их смеси. Если в методах поглощения РОУ (метод А), выделения С02 (метод В) и манометрического определения БПК (метод F) используется активный ил, то он должен быть получен из очистных сооружений или в лабораторных условиях из бытовых сточных вод. Посевная культура из других источников, обычно обладающая более низкими значениями клеточной плотности, будет способствовать большому расхождению результатов. Для модифицированного метода ОЭСР (метод Е) и метода испытания в «закрытом сосуде» (метод D) требуется использование более разбавленной посевной культуры без хлопьев. Наиболее приемлемым источником посевной культуры являются вторичные отстойники очистных сооружений или культура, полученная в лаборатории. Для метода MITI (метод С) посевную культуру получают из комбинированного источника. Характеристики источников и подготовка посевной культуры описаны в соответствующем разделе отдельном для каждого метода.
5