ГОСТ Р 57004-2016
Диагностика в онкологии. Алгоритм диагностики. Шейка матки. Лабораторный этап
Купить ГОСТ Р 57004-2016 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Разработан как руководство по организации и проведению диагностических мероприятий, в том числе с использованием метода жидкостной цитологии, для руководителей лечебно-профилактических учреждений, гинекологических отделений, женских консультаций, лабораторий, врачей-гинекологов, сотрудников женских консультаций, смотровых кабинетов, цитологических лабораторий. Стандарт разработан в соответствии с рекомендациями ВОЗ относительно мероприятий по борьбе с онкологическими заболеваниями шейки матки. ВОЗ также настоятельно рекомендует обратить особое внимание: - на организацию материально-технического обеспечения и укомплектованность кадрами; - обеспечение соответствующего профессионального уровня сотрудников путем организации регулярного повышения квалификации для них и контроля качества диагностических мероприятий. Стандарт распространяется на процедуры: - получения материала для исследования; - подготовки и доставки материала в лабораторию; - пробоподготовки; - документального оформления этих действий на каждом этапе.
Оглавление
1 Область применения
2 Термины, определения и сокращения
3 Получение цитологического материала
4 Подготовка и оформление материала
5 Отправка и транспортирование материала в лабораторию
6 Доставка и прием материала цитологической лабораторией
7 Лабораторный этап
Приложение А (рекомендуемое) Направление на цитологическое диагностическое исследование и результат исследования
Приложение Б (рекомендуемое) Журнал регистрации материала, поступающего в цитологическую лабораторию, и проведенных исследований
Приложение В (рекомендуемое) Требования к оборудованию и реактивам, используемым для проведения жидкостной цитологии гинекологического материала (эпителий шейки матки)
Приложение Г (рекомендуемое) Перечень и краткая характеристика необходимого оборудования и расходных материалов, применяемых при использовании метода жидкостной цитологии
Приложение Д (справочное) Системы оценки цитологических препаратов
Библиография
| Дата введения | 01.02.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
- Раздел Электроэнергия
- Раздел Экология
Организации:
| 01.07.2016 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 795-ст |
|---|---|---|---|
| Разработан | АНО ЦИТО | ||
| Издан | Стандартинформ | 2016 г. |
Diagnostics in oncology. Diagnostic algorithm. Cervix. Laboratory stage
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6
стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17
стр. 18

стр. 19

стр. 20
ГОСТР
57004—
2016
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫМ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
Диагностика в онкологии АЛГОРИТМ ДИАГНОСТИКИШейка матки Лабораторный этап
Издание официальное
|
Москва Стандартинформ 2016 |
Предисловие
1 РАЗРАБОТАН Автономной некоммерческой организацией «Центр инновационных технологий в онкологии» (АНО «ЦИТО»)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 216 «Диагностика в онкологии»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 1 июля 2016 г. № 795-ст
4 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ, 2016
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
7.2.3.4 пробирки поместить в центрифугу и центрифугировать в щадящем режиме (при 200 ref1), 2 мин.);
7.2.3.5 с помощью аспиратора убрать надосадочную жидкость и центрифугировать (при 800 ref, 10 мин.);
7.2.3.6 слить надосадочную жидкость2) полностью, резким движением перевернув штатив с пробирками на 180°;
7.2.3.7 с помощью «вортекс» перемешать образовавшийся клеточный осадок (~ 15 с);
7.2.3.8 перенос полученного клеточного осадка на предметные стекла проводить в соответствии с процедурой, установленной производителем оборудования;
7.2.3.9 аппарат для приготовления и окрашивания препаратов использовать в соответствии с руководством производителя оборудования;
7.2.3.10 приготовить препараты;
7.2.3.11 предметные стекла с нанесенным биоматериалом после окрашивания (если использовалось окрашивание по Папаниколау) промыть спиртом [опустив в емкость со спиртом или сливая спирт из пипетки (выше монослоя)]. Можно использовать специальный спрей для фиксации;
7.2.3.12 подсушить препарат;
7.2.3.13 подготовить покровные стекла необходимого размера;
7.2.3.14 на препарат в центр монослоя нанести монтирующую среду3);
7.2.3.15 заключить препарат под покровное стекпо/пленку;
7.2.3.16 монтировать вручную покровное стекло следующим образом:
- приложить покровное стекло ребром под углом к препарату и опустить, избегая образования воздушных пузырей,
- при необходимости слегка нажать на покровное стекло, удалить излишки монтирующей среды (с помощью ваты/марли со спиртом/ксилолом),
- дать препарату подсушиться (время зависит от монтирующей среды);
7.2.3.17 использовать автоматизированные приборы для заключения препаратов под покровное стекло или пленку в соответствии с руководством производителя оборудования;
7.2.3.18 препараты, приготовленные традиционным способом, окрашивают теми же методами,
что и препараты, приготовленные в рамках метода ЖЦ.
7.3 Хранение биоматериала
7.3.1 Нативный жидкостной биоматериал без добавления консервантов или транспортной жидкости, доставленный в лабораторию или оставшийся после взятия для исследования, можно хранить в холодильной камере при температуре от 2 до 10 °С не более 4 ч.
7.3.2 Биоматериал в транспортной среде в комнатных условиях при температуре от 15 до 30 °С можно хранить не более 4 недель, если иное не предусмотрено производителем транспортной среды или консерванта.
7.3.3 Биоматериал в транспортной среде можно хранить в холодильной камере при температуре от 2 до 10 °С не более 6 мес., если иное не предусмотрено производителем транспортной среды или консерванта.
7.3.4 Окрашенные препараты, по которым выявлена онкопатология или предопухолевые изменения, необходимо хранить в комнатных условиях (при температуре от 15 до 30 °С) в течение срока, установленного данным лечебным учреждением, но не менее 10 лет.
7.3.5 Окрашенные неинформативные препараты при температуре от 15 до 30 °С необходимо хранить 2 недели (для контроля качества).
7.3.6 Транспортную среду при температуре от 15 до 30 °С хранить не более 36 мес. (если производителем реагентов не предусмотрено иное).
7.3.7 Нативный биоматериал, поступивший в лабораторию на предметных стеклах, можно хранить в сухом помещении без ограничений до момента использования.
7.3.8 Утилизацию отходов осуществляют в соответствии с требованиями действующих нормативных документов [5], а также инструкциями к приборам, реагентам и расходным материалам, использующимся для приготовления препаратов методом ЖЦ в данной лаборатории.
7.4 Диагностический этап
7.4.1 Подготовленные к просмотру препараты в сопровождении направления в установленном порядке отправляют на диагностику.
7.4.1.1 К диагностике материала, приготовленного любым методом, допускается только персонал, прошедший обучение и допущенный на этом основании к работе руководителем лаборатории с оформлением соответствующего распоряжения (приказа) по лаборатории.
7.4.2 Для адекватной оценки препарата необходимо системно произвести просмотр всего клеточного материала (см. рисунок 5), а затем дать оценку качества препарата и его информативности.
|
Рисунок 5 — Наиболее эффективная схема направления просмотра препарата |
7.4.3 Необходимо сформулировать заключение, содержащее информацию:
7.4.3.1 о качестве препарата, его информативности;
7.4.3.2 о том, какое количество препаратов оценивают (описывают);
7.4.3.3 о причине, по которой препарат оценен исследователем как неинформативный или малоинформативный (при неинформативном или малоинформативном материале);
7.4.3.4 на предмет диагноза с указанием кода по МКБ-10 или описания препарата при невозможности выставления однозначного диагноза;
7.4.3.5 о причине, по которой исследователь счел невозможным указать точный диагноз;
7.4.3.6 в отношении рекомендаций по проведению дополнительных исследований или по повторному получению материала, если это необходимо для установления диагноза;
7.4.3.7 о дате исследования и ФИО выдавшего заключение.
7.5 Формулирование заключения
При оценке результатов цитологического исследования возможно использование классификации Папаниколау, Бетесда или традиционной, классической морфологической классификации (см. приложение Д). 4
Приложение А (рекомендуемое)
Направление на цитологическое диагностическое исследование и результат исследования
Министерство здравоохранения Медицинская документация
Российской Федерации Форма № 203/у-02
Утверждена приказом Минздрава России от 24.04.2003 № 174
Наименование учреждения
НАПРАВЛЕНИЕ
на цитологическое диагностическое исследование и результат исследования
ПЕРВИЧНО
ПОВТОРНО
(подчеркнуть)
1. Отделение _
История болезни №_
2. Лечащий врач (ФИО, тел.)
3. ФИО больного (полностью) _
4. Дата рождения _Пол: м (), ж ()
5. Страховая компания _№ страхового полиса _
6. Диагноз (при направлении на цитологическое исследование)
Серия
Код по М КБ-10
7. Краткий анамнез и важнейшие клинические симптомы:
8. Данные инструментального обследования (рентгенологического, УЗИ, КТ, эндоскопического
и др.) _
9. Проведенное лечение (оперативное, лучевое, химиотерапия; доза, дата начала и окончания
лечения) _
10. Локализация процесса и способ получения материала _
11. Объем и макроскопическое описание биологического материала, маркировка препаратов
12. Дата взятия биологического материала
ФИО врача, направившего материал
Подпись врача
13. Объем и макроскопическое описание доставленного биологического материала (заполняют в лаборатории):
9
(Оборотная сторона)
Наименование цитологической лаборатории, телефон
Результат цитологического исследования №_
Дата поступления материала_
Дата проведения исследования _
ФИО врача, проводившего исследование
Подпись
10
ГОСТ Р 57004-2016Приложение Б (рекомендуемое)Журнал регистрации материала, поступающего в цитологическую лабораторию,
и проведенных исследований
Журнал регистрации материала, поступающего в цитологическую лабораторию,
Б.1 Обязательные поля:
- дата поступления материала;
- номер исследования.
Примечание — Указывают в диапазоне в зависимости от количества препаратов. Далее ставится знак «/» (например, для пяти препаратов, поступивших 1 января 2002 г. первыми, номер будет 1—5/02, следующие два препарата — (6—7/02).
- первично/повторно;
- отделение (учреждение), приславшее материал;
- № истории болезни или Ю;
- лечащий врач (ФИО, тел.);
- ФИО больного (полностью);
- пол;
- дата рождения;
- диагноз (при направлении на цитологическое исследование), код по МКБ-10;
- важнейшие клинические данные;
- метод получения материала;
- откуда получен материал;
- характер материала;
- объем и макроскопическое описание биологического материала, маркировка препаратов;
- дата взятия биологического материала;
- ФИО врача, направившего материал;
- дата проведения исследования;
- результат цитологического исследования №;
- ФИО врача, проводившего исследование.
Б.2 Журнал должен быть прошнурован, пронумерован и скреплен печатью.
11
Приложение В (рекомендуемое)Требования к оборудованию и реактивам, используемым для проведения жидкостной цитологии гинекологического материала (эпителий шейки матки)
В.1 Общие требования
В.1.1 На все аппаратные средства, принадлежности, реагенты и расходные материалы комплекса для приготовления и окраски цитологических препаратов должны быть регистрационные удостоверения Федеральной службы по надзору в сфере здравоохранения и социального развития.
В.1.2 К оборудованию в обязательном порядке следует прилагать инструкцию на русском языке и подробное руководство пользователя.
В.1.3 Все компоненты оборудования (системы) должны быть приобретены у одного производителя либо про-изводитель/поставщик должен предоставить официальные сведения о совместимости с оборудованием других фирм.
В.2 Приготовление и окрашивание препаратов при проведении цитологических исследований
В.2.1 Технология взятия и доставки биологического материала должна предоставлять возможность переноса на предметное стекло без потерь всего биологического материала, взятого у пациентки.
В.2.2 Срок годности консервирующей жидкости для гинекологического материала при хранении при комнатной температуре (от 15 до 30 °С) должен составлять не менее 32 мес. со дня изготовления.
В.2.3 Срок хранения флакона с клеточным материалом при комнатной температуре должен составлять не менее 2 недель.
В.2.4 Оборудование должно предоставлять возможность получить готовый препарат как без содержания эритроцитов и слизи, так и при сохранении исходного их количества в препарате.
В.2.5 Транспортная жидкость, используемая для сохранения материала при транспортировании, не должна препятствовать проведению других видов исследования (ИЦХ, ПЦР и пр.).
В.2.6 При наличии в составе консерванта (транспортной жидкости) веществ, влияющих на выбор тактики при проведении дополнительных исследований, производитель или поставщик должны в письменном виде предоставить информацию, касающуюся этого вопроса, самостоятельно или по запросу пользователя.
В.2.7 Технология приготовления и окраски клеточного материала должна быть управляемой и допускать изменения в случае необходимости для подготовки препаратов из различного материала, в том числе негинекологического, жидкостей и пр.
В.2.8 Оборудование должно обеспечивать возможность:
- управления объемом клеточной суспензии;
- управления объемом переносимого на предметное стекло клеточного материала;
- одновременного приготовления серии идентичных препаратов из одного материала в количестве не менее чем 12 шт. (от 1 до 12);
- вносить изменения в ход работы и протоколы;
- обработки материала, не исключающей дальнейшего использования препарата как для традиционного цитологического исследования, так и для автоматизированного;
- использования оставшегося после приготовления препаратов клеточного материала в других видах исследований;
- приготовления нативных (неокрашенных) монослойных препаратов, не менее 90 в 1 ч;
- приготовления окрашенных монослойных препаратов, не менее 40 в 1 ч.
12
ГОСТ Р 57004-2016Приложение Г (рекомендуемое)Перечень и краткая характеристика необходимого оборудования и расходных материалов, применяемых при использовании метода жидкостной цитологии
Перечень и краткая характеристика необходимого оборудования и расходных материалов, применяемых при использовании метода жидкостной цитологии
Г.1 Техническое оснащение лаборатории для проведения метода ЖЦ:
- центрифуга лабораторная с качающимся ротором, приспособленным для центрифугирования пробирок диаметром 17 мм, объемом 15 мл, способная обеспечить центрифугирование 600 д;
- «вортекс» для пробирок с плавной регулировкой скорости встряхивания от 100 до 3000 rpm;
- прибор для автоматического приготовления клеточной суспензии, выполняющий начальный процесс обогащения клеточной суспензии (состоящий в очистке суспензии от эритроцитов, детрита и элементов воспаления): перемешивание образца и его извлечение из пробирки с консервантом, затем нанесение образца на плотный реагент в пробирку для центрифугирования;
- аппарат для автоматической окраски препаратов — прибор для окрашивания образцов или эквивалент, который предназначается для обработки микропрепаратов, автоматического переноса клеточных образцов из пробирок для центрифугирования в осадочную камеру, помещаемую на предметное стекло для микроскопа, автоматически окрашивает и промывает каждый микропрепарат;
- рабочая станция для управления прибором или эквивалент: системный блок с предустановленным программным обеспечением, монитор, клавиатура, мышь;
- аспиратор — система создания вакуума для удаления продуктов окрашивания: емкость, компрессор, комплект трубок не менее одного комплекта;
- считыватель штрих-кода.
Г.2 Расходные материалы:
- одноразовые пробирки из пластика диаметром 17 мм, вместимостью до 15 мл, с закручивающейся крышкой, выдерживающие центрифугирование при скорости 600 д;
- одноразовые стерильные виалы с транспортной средой;
- одноразовые стерильные цитологические щетки для забора материала с влагалищной части шейки матки;
- одноразовые стерильные цитологические щетки для забора материала из цервикального канала;
- предметные стекла для микроскопии с адгезивным покрытием (например, D-полилизиновым) или без оного — в зависимости от конкретной методики;
- набор одноразовых пастеровских пипеток для работы с жидкостью и клеточным осадком;
- при необходимости — пленка или покровные стекла для покрытия препаратов;
- консервирующая (транспортная) жидкость;
- красители, буферы, забуференная или дистиллированная вода, фиксаторы и спецрастворы в зависимости от способа окраски;
- одноразовые наконечники для переноса и дозирования материала;
- средство для промывания аппарата для автоматической окраски препаратов;
- контейнер для сбора и утилизации отходов класса В.
13
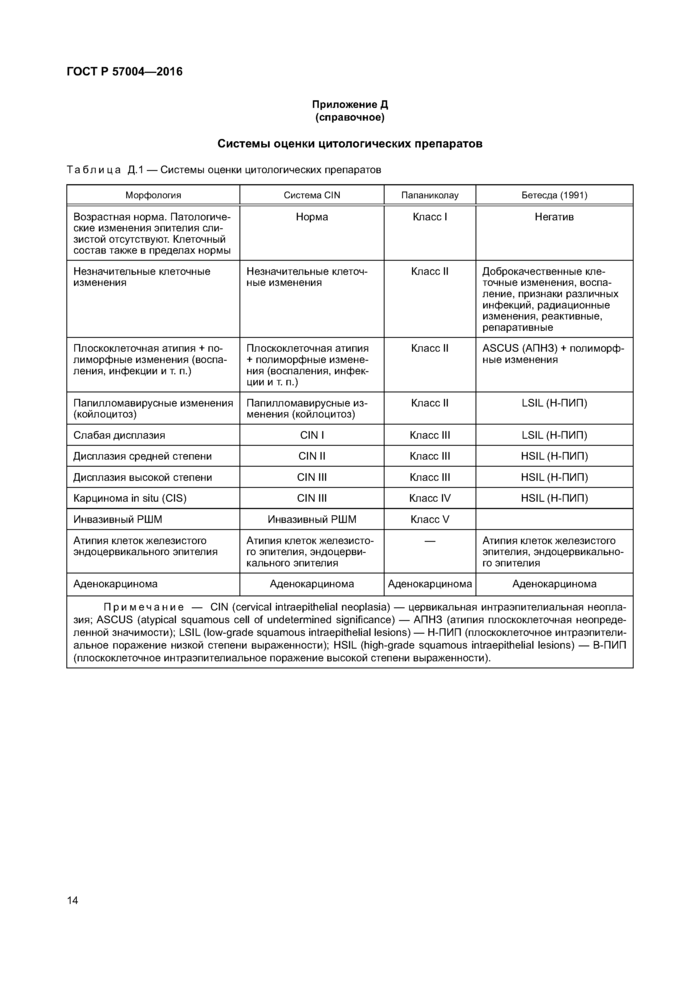
Приложение Д (справочное)
Системы оценки цитологических препаратов
Таблица Д.1 — Системы оценки цитологических препаратов
|
Морфология |
Система CIN |
Папаниколау |
Бетесда (1991) |
|
Возрастная норма. Патологические изменения эпителия слизистой отсутствуют. Клеточный состав также в пределах нормы |
Норма |
Класс 1 |
Негатив |
|
Незначительные клеточные изменения |
Незначительные клеточные изменения |
Класс II |
Доброкачественные клеточные изменения, воспаление, признаки различных инфекций, радиационные изменения, реактивные, репаративные |
|
Плоскоклеточная атипия + полиморфные изменения (воспаления, инфекции и т. п.) |
Плоскоклеточная атипия + полиморфные изменения (воспаления, инфекции и т. п.) |
Класс II |
ASCUS (АПНЗ) + полиморфные изменения |
|
Папилломавирусные изменения (койлоцитоз) |
Папилломавирусные изменения (койлоцитоз) |
Класс II |
LSIL (Н-ПИП) |
|
Слабая дисплазия |
CIN 1 |
Класс III |
LSIL (Н-ПИП) |
|
Дисплазия средней степени |
CIN II |
Класс III |
HSIL (Н-ПИП) |
|
Дисплазия высокой степени |
CIN III |
Класс III |
HSIL (Н-ПИП) |
|
Карцинома in situ (CIS) |
CIN III |
Класс IV |
HSIL (Н-ПИП) |
|
Инвазивный РШМ |
Инвазивный РШМ |
Класс V | |
|
Атипия клеток железистого эндоцервикального эпителия |
Атипия клеток железистого эпителия, эндоцервикального эпителия |
— |
Атипия клеток железистого эпителия, эндоцервикального эпителия |
|
Аденокарцинома |
Аденокарцинома |
Аденокарцинома |
Аденокарцинома |
|
Примечание — CIN (cervical intraepithelial neoplasia) — цервикальная интраэпителиальная неоплазия; ASCUS (atypical squamous cell of undetermined significance) — АПНЗ (атипия плоскоклеточная неопределенной значимости); LSIL (low-grade squamous intraepithelial lesions) — Н-ПИП (плоскоклеточное интраэпителиальное поражение низкой степени выраженности); HSIL (high-grade squamous intraepithelial lesions) — В-ПИП (плоскоклеточное интраэпителиальное поражение высокой степени выраженности). | |||
14
Библиография
[1] Руководство ВОЗ «Комплексная борьба с раком шейки матки: руководство по основам практики — 2 издание» (WHO, Comprehensive cervical cancer control: a guide to essential practice — 2nd ed)
[2] Международная статистическая классификация болезней и проблем, связанных со здоровьем — 10-й пересмотр (International Statistical Classification of Diseases and Related Health Problems — Teath Revision — Volume 3. Alphabetical Index)
[3] ВОЗ, Классификация опухолей женских репродуктивных органов [WHO Classification of Tumours of the Female Reproductive Organs (IARC WHO Classification of Tumours) Fourth Edition]
[4] Цитологическая классификация Бетесда (Cytology classification. The Bethesda System 2014)
[5] СанПиН 2.1.7.2790—10 «Санитарно-эпидемиологические требования к обращению с медицин
скими отходами»
15
УДК 616-006-072/-079:618.146(083.74)
ОКС 03.040, 11.040.01, 11.100.01
Ключевые слова: диагностика в онкологии, алгоритм диагностики, шейка матки, лабораторный этап
Редактор В.О. Самойленко Корректор Е.Р. Ароян Компьютерная верстка С.В. Косторновой
Сдано в набор 04.07.2016. Подписано в печать 12.08.2016. Формат 60 * 841/g. Гарнитура Ариал.
Уел. печ. л. 2,33.
Набрано в ИД «Юриспруденция», 115419, Москва, ул. Орджоникидзе, 11. www.jurisizdat.rn y-book@mail.ru
Издано во ФГУП «СТАНДАРТИНФОРМ», 123995, Москва, Гранатный пер., 4. www.gostinfo.rn info@gostinfo.ru
ГОСТ Р 57004-2016Содержание
1 Область применения..................................................................1
2 Термины, определения и сокращения ...................................................1
3 Получение цитологического материала..................................................2
4 Подготовка и оформление материала....................................................4
5 Отправка и транспортирование материала в лабораторию..................................4
6 Доставка и прием материала цитологической лабораторией.................................5
7 Лабораторный этап...................................................................5
Приложение А (рекомендуемое) Направление на цитологическое диагностическое
исследование и результат исследования......................................9
Приложение Б (рекомендуемое) Журнал регистрации материала, поступающего
в цитологическую лабораторию, и проведенных исследований..................11
Приложение В (рекомендуемое) Требования к оборудованию и реактивам,
используемым для проведения жидкостной цитологии гинекологического
материала (эпителий шейки матки).........................................12
Приложение Г (рекомендуемое) Перечень и краткая характеристика необходимого
оборудования и расходных материалов, применяемых при использовании
метода жидкостной цитологии.............................................13
Приложение Д (справочное) Системы оценки цитологических препаратов......................14
Библиография........................................................................15
Введение
В настоящем стандарте реализованы основные нормативные положения документов [1]—[4]. Настоящий стандарт разработан для внедрения в практику здравоохранения унифицированных алгоритмов проведения пробоподготовки, в том числе:
- для метода жидкостной цитологии с целью оптимизации и систематизации деятельности лечебно-профилактических учреждений и специалистов в области раннего выявления и диагностики рака;
- эффективной и своевременной (ранней) диагностики и лечения опухолей, масштабной борьбы против рака на региональном, национальном и глобальном уровнях в целях увеличения выживаемости, снижения смертности от онкологических заболеваний;
- обеспечения доступности лечения для пациентов, страдающих онкологическими заболеваниями. Настоящий стандарт может быть использован специалистами как методическое руководство при
осуществлении профессиональной деятельности, а также учреждениями здравоохранения и органами государственной власти при создании нормативных правовых актов.
IV
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Диагностика в онкологии
АЛГОРИТМ ДИАГНОСТИКИ
Шейка матки Лабораторный этап
Diagnostics in oncology. Diagnostic algorithm. Cervix. Laboratory stage
Дата введения —2017—02—01
1 Область применения
Настоящий стандарт разработан как руководство по организации и проведению диагностических мероприятий, в том числе с использованием метода жидкостной цитологии, для руководителей лечебно-профилактических учреждений, гинекологических отделений, женских консультаций, лабораторий, врачей-гинекологов, сотрудников женских консультаций, смотровых кабинетов, цитологических лабораторий.
Настоящий стандарт разработан в соответствии с настоятельными рекомендациями ВОЗ о мероприятиях по борьбе с онкологическими заболеваниями шейки матки.
ВОЗ также настоятельно рекомендует обратить особое внимание:
- на организацию материально-технического обеспечения и укомплектованность кадрами;
- обеспечение соответствующего профессионального уровня сотрудников путем организации регулярного повышения квалификации для них и контроля качества диагностических мероприятий.
Настоящий стандарт распространяется на процедуры:
- получения материала для исследования;
- подготовки и доставки материала в лабораторию;
- пробоподготовки;
- документального оформления этих действий на каждом этапе.
2 Термины, определения и сокращения
2.1 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1.1 аспиратор: Прибор, предназначенный для аспирации — вакуумного забора надосадочной жидкости.
2.1.2 виала: Контейнер с герметичной крышкой, содержащий транспортную жидкость, предназначенный для хранения и транспортирования клеточного материала.
2.1.3 мазок: Препарат, приготавливаемый путем нанесения и равномерного распределения (размазывания) биологического материала.
2.1.4 ПАП-тест: Данный тест является методом цервикального скрининга и используется для обнаружения потенциально предраковых и раковых процессов в шейке матки или цервикальном канале.
Издание официальное
Тест был изобретен Георгиосом Папаниколау и назван в честь это греческого врача. Подразумевает оценку полученного материала по системе Bethesda1).
2.1.5 транспортная жидкость: Специальная жидкость, использующаяся в жидкостной цитологии для сохранения и/или транспортирования материала. Как правило, представляет собой изотонический раствор с консервантами, фиксирующий и предохраняющий клетки от быстрого распада.
2.1.6 цитощетка: Щеточка для получения эндоцервикальных образцов.
2.1.7 cervex-brush: Щеточка для получения биоматериала из Т-зоны (зоны трансформации шейки матки) и влагалищной части шейки матки.
2.1.8 ID (identification): Уникальный идентификатор, который присваивается системой каждой отдельной записи или каждому пациенту.
2.2 Сокращения
В настоящем стандарте использованы следующие сокращения: аденокарцинома — АК;
Всемирная организация здравоохранения — ВОЗ; жидкостная цитология — ЖЦ; иммуноцитохимия — ИЦХ; информационная система — ИС;
лабораторная информационная менеджмент-система — ЛИМС; лабораторная информационная система — ЛИС; лечебно-профилактическое учреждение — ЛПУ;
Международная классификация болезней 10-го пересмотра — МКБ-10; полимеразная цепная реакция — ПЦР; рак шейки матки — РШМ; шейка матки — ШМ.
3 Получение цитологического материала
3.1 Сотрудники гинекологических и смотровых кабинетов ЛПУ, направляющие цитологический материал для исследования, должны быть информированы о том, каким методом осуществляют про-боподготовку [ЖЦ или традиционная (классическая) цитология] гинекологического материала в лаборатории, так как это влияет на выбор способа забора, хранения и транспортирования материала.
Материал для исследования следует забирать, готовить и транспортировать в лабораторию с учетом требований метода, используемого лабораторией.
Материал с шейки матки забирают с помощью одноразовых щеток различного типа (см. рисунки 1—2). Для получения более информативного материала рекомендуется использовать два вида щеток cervex-brush и цитощетки различных типов.
|
Рисунок 1 — Цитощетка или щеточка цервикальная |
Цитощетка должна быть со щетинками, расположенными под углом 90°. При заборе материала ее следует поворачивать на 90° не менее двух раз.
"0 Система Bethesda (TBS) представляет собой систему для оценки цитологической картины материала, полученного при биопсии шейки матки, и для формирования цитологического диагноза. Она была введена в 1988 г., и пересмотрена в 1991 и 2001 гг. Название происходит от места (Бетесда, Мэриленд) проведения конференции, на которой была утверждена к применению эта система.
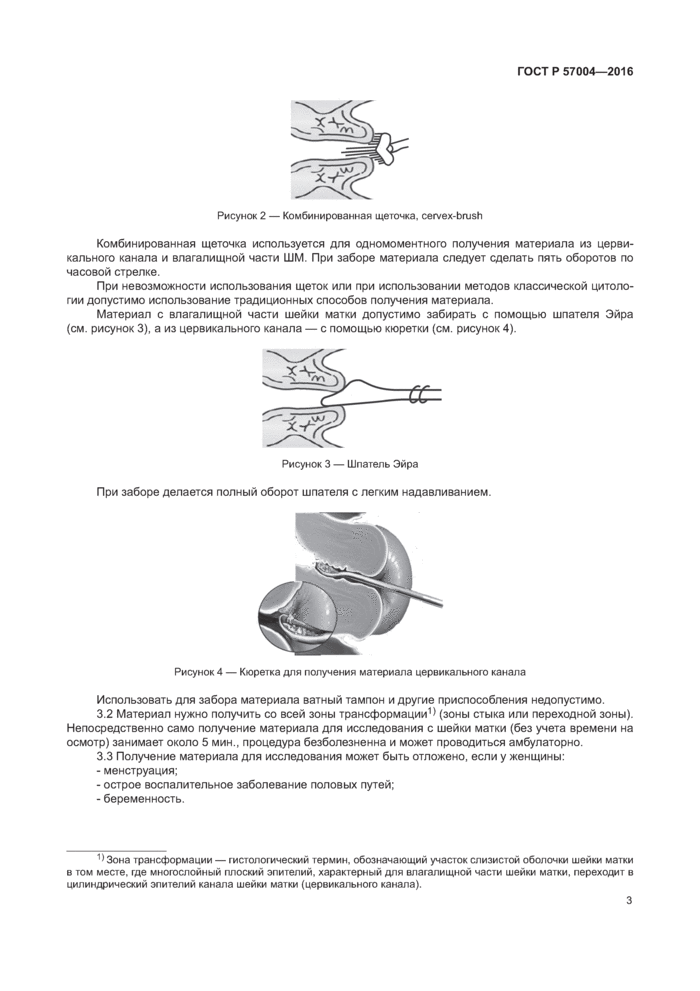
|
Рисунок 2 — Комбинированная щеточка, cervex-brush |
Комбинированная щеточка используется для одномоментного получения материала из цервикального канала и влагалищной части ШМ. При заборе материала следует сделать пять оборотов по часовой стрелке.
При невозможности использования щеток или при использовании методов классической цитологии допустимо использование традиционных способов получения материала.
Материал с влагалищной части шейки матки допустимо забирать с помощью шпателя Эйра (см. рисунок 3), а из цервикального канала — с помощью кюретки (см. рисунок 4).
|
Рисунок 3 — Шпатель Эйра |
При заборе делается полный оборот шпателя с легким надавливанием.
|
Рисунок 4 — Кюретка для получения материала цервикального канала |
Использовать для забора материала ватный тампон и другие приспособления недопустимо.
3.2 Материал нужно получить со всей зоны трансформации1) (зоны стыка или переходной зоны). Непосредственно само получение материала для исследования с шейки матки (без учета времени на осмотр) занимает около 5 мин., процедура безболезненна и может проводиться амбулаторно.
3.3 Получение материала для исследования может быть отложено, если у женщины:
- менструация;
- острое воспалительное заболевание половых путей;
- беременность. 5 6
4 Подготовка и оформление материала
4.1 Метод получения материала и приготовления препаратов, который будет использован в каждом конкретном случае, должен быть заранее четко согласован между лабораторией и отделением ЛПУ, что должно быть отражено в соответствующем документе.
4.2 При использовании метода классической цитологии материал после получения помещают на предметное стекло путем нанесения и равномерного распределения (размазывания) биологического материала вдоль стекла, избегая чрезмерного механического воздействия (чтобы не раздавить клетки). Одновременно с этим необходимо стремиться к получению тонкого монослоя.
Материал с шейки матки и материал из цервикального канала помещают на разные стекла, маркируемые соответственно нанесенному материалу.
Препараты подсушивают в течение нескольких минут на открытом воздухе (при использовании методов окраски по Паппенгейму, по Лейшману и др.) и могут транспортировать в лабораторию.
При использовании метода окраски по Папаниколау препараты требуют немедленной фиксации.
4.3 При использовании метода ЖЦ полученный материал необходимо немедленно перенести в транспортную жидкость в емкость — виалу, отделив саму щетку от рукоятки (если производителем щетки не предусмотрено иное), и герметично закрыть виалу с целью исключения возможности проливания и испарения содержимого.
4.3.1 Следует сразу же маркировать (подписать) виалу, используя простой карандаш, ручку (при наличии этикетки) или перманентный маркер.
4.4 При маркировке указывают фамилию, имя, отчество пациентки и/или ее Ю (в том случае, если сотрудник, получающий материал для исследования у пациентки, и лаборатория используют единую информационную систему). Возможно применение штрих-кодов и номеров, присваиваемых исследованию информационной системой, если используется штрихкодирование. В любом случае маркировка должна быть четкой, читаемой, надежно закрепленной на виале, не смываемой водой.
4.5 Абсолютно недопустимым является:
- использование для маркировки препаратов стеклографов, карандашей старого образца, водных маркеров;
- отправка для исследования немаркированного материала;
- отправка материала без сопровождающих документов;
- отсутствие в ЛПУ документально оформленного «прикрепления» к конкретной лаборатории, с указанием согласованных взаимных правил и требований, касающихся получения материала, приготовления препаратов, оформления, доставки материала для исследования, сроков доставки, повторных исследований, сроков проведения исследования и предоставления заключений и отчетов, порядка направления пациенток с выявленной патологией для обследования и лечения в другие ЛПУ и т. п.
5 Отправка и транспортирование материала в лабораторию
Сотрудник, отвечающий за этот этап работ, должен проверить соответствие представленного материала записи о нем в сопровождающем документе.
5.1 Материал, направляемый в лабораторию, сопровождается заполненным направлением на исследование (см. приложение А).
5.2 В направлении, прилагаемом к материалу, должна быть как минимум следующая информация:
- фамилия, имя, отчество пациентки;
- дата рождения;
- номер истории болезни/амбулаторной карты/другой номер, идентифицирующий пациентку;
- наименование запрашиваемого исследования (например, «направляется на цитологическое диагностическое исследование);
- причина обследования (указать диагноз или, например, «профилактический осмотр», «онкопоиск»);
- дата последней менструации, продолжительность менопаузы;
- количество виал с материалом и данные, какой материал в них содержится (например, соскоб с эндоцервикса, эктоцервикса), в случае штрихкодирования виал эту информацию указывают в направлении напротив каждого штрих-кода; 7
- дата и время сбора материала;
- фамилия лица, направившего материал на исследование.
При отсутствии информации для заполнения поля необходимо поставить прочерк.
Наличие пустых полей в бланке направления недопустимо.
5.3 Направление может быть оформлено в электронном виде при наличии ЛИС и должно давать доступ к указанной информации в рамках прав доступа каждого конкретного медицинского работника.
5.4 Порядок сбора материала из ЛПУ для отправки в цитологическую лабораторию должен быть четко согласован между отделением ЛПУ и лабораторией и прописан в соответствующем документе.
6 Доставка и прием материала цитологической лабораторией
6.1 Прием материала должен осуществлять ответственный сотрудник лаборатории, назначенный заведующим лабораторией или лицом, его замещающим, под подпись с указанием даты и времени доставки.
Порядок доставки и приема также должен быть согласован между отделением ЛПУ и лабораторией, что должно быть оформлено документально. Прием материала в лаборатории осуществляют непосредственно после его доставки. Сотрудник, отвечающий за этот этап работ, должен проверить соответствие представленного материала записи о нем в сопровождающем документе.
6.1.1 Лаборатория может отказаться от приема материала в том случае, если:
- отсутствует или не оформлена надлежащим образом сопровождающая документация;
- не маркирован материал;
- констатируется нарушение сохранности (целостности, герметичности) упаковки;
- очевидно нарушение условий сбора, хранения и/или транспортирования.
6.1.2 Отказ в приеме материала с указанием причины фиксируют в отдельном журнале1) и заверяют подписями представителей обеих сторон.
6.1.3 Регистрацию осуществляют в ЛИМС или при отсутствии информационной системы в бумажном журнале регистрации материала (см. приложение Б).
6.1.4 Форма журнала может быть свободной, но с указанием всех параметров исследования и с наличием всех граф, имеющихся в направлении.
7 Лабораторный этап7.1 Общие положения
На все оборудование, принадлежности, реагенты и расходные материалы для пробоподготовки цитологических препаратов должны быть представлены регистрационные удостоверения Федеральной службы по надзору в сфере здравоохранения и социального развития.
7.1.1 Все компоненты оборудования/систем должны быть приобретены у одного производителя, либо производитель/поставщик должен предоставить официальные сведения о совместимости с оборудованием других фирм.
7.1.2 К оборудованию в обязательном порядке следует прилагать инструкцию на русском языке и подробное руководство пользователя.
7.1.3 Все используемые реактивы для обработки и окраски биологического материала должны соответствовать срокам годности.
7.1.4 Сотрудник лаборатории (из числа среднего медицинского персонала) допускается к осуществлению пробоподготовки по методу ЖЦ после соответствующего распоряжения заведующего лабораторией.
7.1.5 Сотрудник, допускаемый к работе по методу ЖЦ, должен быть предварительно подготовлен и обучен работе с приборами у производителя (или его уполномоченного представителя). 8 9
7.1.6 Сотрудник, допускаемый руководителем лаборатории к работе, в том числе по методу ЖЦ, должен быть обучен методам контроля информативности материала путем микроскопии окрашенных
препаратов.
7.1.7 Следует обратить внимание на перечень характеристик рекомендованного к использованию оборудования для ЖЦ (см. приложение В и Г).
7.1.8 Для пробоподготовки материала с ШМ, производящегося с целью выявления и ранней диагностики рака методом ЖЦ, использование цитоцентрифуг нецелесообразно.
7.1.9 Каждая лаборатория составляет внутренний документ — «Инструкцию по подготовке материала для исследования методом ЖЦ».
7.1.10 В данном документе подробно, по пунктам, расписывают весь процесс приготовления препаратов на основе ЖЦ для данной лаборатории с указанием конкретного оборудования, в соответствии с рекомендациями производителя оборудования, используемого в лаборатории.
7.1.11В инструкции указывают, в том числе фирменные названия приборов, материалов, реагентов (названия растворов, включая фирменные, позволяющие их однозначно идентифицировать), номеров и/или названий программ, запускаемых на автоматических приборах, описание конкретных методик окраски, применяемых в данной лаборатории, названия форм и бланков, заполняемых в процессе выполнения методики.
Инструкция должна содержать следующие пункты:
- назначение процедуры;
- описание процедур;
- сбор материала;
- приготовление окрашенных цитологических препаратов методом ЖЦ.
Приложением к данной инструкции должны служить:
- перечень сотрудников, допущенных к работе по этому направлению (с указанием должностей сотрудников, принимающих участие в пробоподготовке и диагностике);
- ответственные за осуществление этих работ;
- оборудование;
- материалы;
- реагенты;
- процедуры;
- литература (при необходимости);
- перечень заполняемых форм.
7.1.12 Документ подписывает заведующий лабораторией; копии хранятся на рабочих местах непосредственных исполнителей методик.
7.2 Пробоподготовка
7.2.1 Материал для проведения исследования должен быть доставлен в лабораторию на маркированных предметных стеклах, а в случае использования метода ЖЦ — в маркированной емкости (виале) с транспортной жидкостью, количество которой варьирует в зависимости от объема и производителя виалы.
7.2.2 Пробопод готовку в рамках ЖЦ из доставленного в лабораторию материала в виалах необходимо произвести не позднее срока, указанного производителем. Например, не позднее четырех недель после получения материала, находящегося при комнатной температуре от 15 до 30 °С; при температуре холодильной камеры от 2 до 10 °С можно обрабатывать материал в течение полугода.
7.2.3 Этапы пробоподготовки1) (если производителем оборудования не предусмотрено иное):
7.2.3.1 содержимое виал перемешать;
7.2.3.2 консервирующую жидкость налить с помощью пипетки в пробирки для центрифугирования (~ 1/3 части пробирки);
7.2.3.3 для приготовления клеточной суспензии материал (~ 1/3 часть пробирки) перенести из виалы в пробирку в консервирующую жидкость (использовать аппарат для приготовления клеточной суспензии типа BD PrepMate™);
11 Аналогично ГОСТ Р 57005 (см. подраздел 7.3).
1
11 Relative centrifugal force — относительная центробежная сила, выражается в единицах g (гравитационная постоянная).
2
В дальнейшем слитую жидкость утилизировать в соответствии с правилами обращения с отходами категории В.
3
Главное требование к монтирующей среде — соответствие ее коэффициента преломления света к аналогичному показателю стекла. Виды монтирующих сред: канадский бальзам, глицерин-желатин, синтетическая, на основе полистирола и др.
7
4
5
^ Зона трансформации — гистологический термин, обозначающий участок слизистой оболочки шейки матки в том месте, где многослойный плоский эпителий, характерный для влагалищной части шейки матки, переходит в цилиндрический эпителий канала шейки матки (цервикального канала).
6
7
8
^Приказ Министерства здравоохранения СССР от4 октября 1980 г. № 1030 «Об утверждении форм первичной медицинской документации учреждений здравоохранения» (с изменениями на 31 декабря 2002 г.). Приказом Минздрава СССР от 5 октября 1988 г. № 750 настоящий приказ был признан утратившим силу, но до утверждения новых форм продолжают применяться формы, утвержденные данным приказом — письмо Минздравсоцразвития России от 30 ноября 2009 г. № 14-6/242888.
9