ГОСТ Р 55041-2012
Оптика офтальмологическая. Линзы контактные и средства ухода за ними. Руководство по клиническим испытаниям
Купить ГОСТ Р 55041-2012 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает руководство по клиническим испытаниям безопасности и эксплуатационных характеристик контактных линз и средств ухода за ними.
Содержит требования ISO 11980:2009
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Требования к клиническим испытаниям
Приложение А (справочное) Рекомендации к формированию концепции КИ
Приложение В (справочное) Оценка безопасности, физиологической эффективности и влияния на ткани глаз
Приложение С (справочное) Оценка визуальных, корригирующих характеристик, эффективности линз и степени приемлемости для субъектов
Приложение ДА (справочное) Сопоставление структуры настоящего стандарта со структурой примененного международного стандарта ИСО 11980:2009
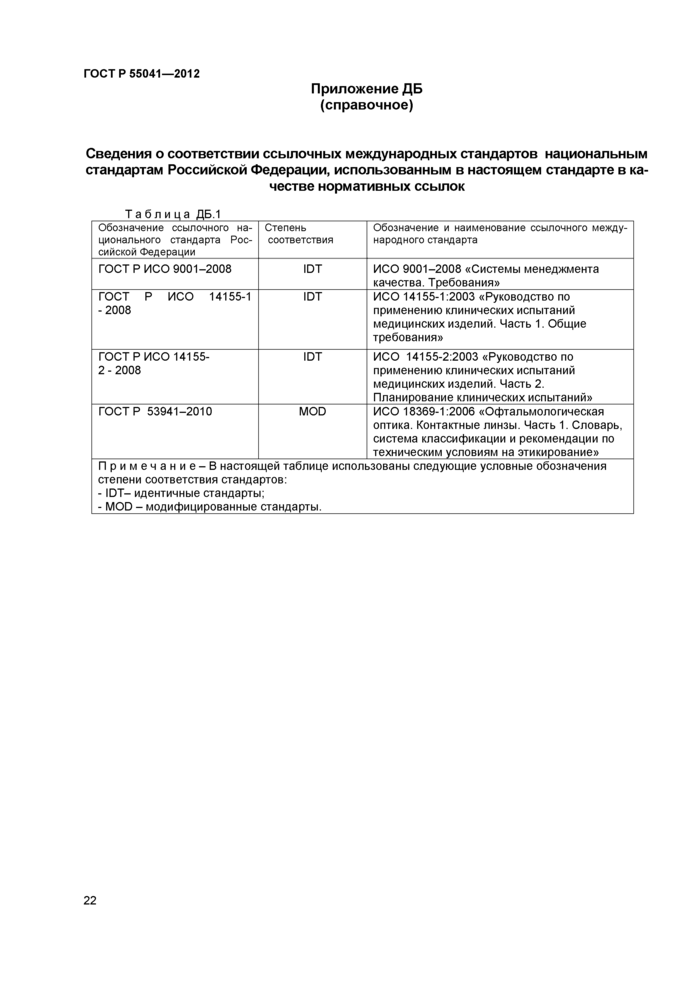
Приложение ДБ (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации, использованным в настоящем стандарте в качестве нормативных ссылок
Библиография
| Дата введения | 01.07.2014 |
|---|---|
| Добавлен в базу | 01.11.2014 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 01.11.2012 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 688-ст |
|---|---|---|---|
| Разработан | ТК 296 Оптика и оптические приборы | ||
| Разработан | ОАО ТКС-оптика | ||
| Разработан | ПК 7 Офтальмологическая оптика и приборы | ||
| Издан | Стандартинформ | 2014 г. |
Ophthalmic optics. Contact lenses and contact lens care products. Guidance for clinical investigations
- ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
ГОСТ Р ИСО 14155-1-2008Руководство по проведению клинических испытаний медицинских изделий. Часть 1. Общие требования. Заменен на ГОСТ Р ИСО 14155-2014.ГОСТ Р ИСО 14155-2-2008Руководство по проведению клинических испытаний медицинских изделий. Часть 2. Планирование клинических испытаний. Заменен на ГОСТ Р ИСО 14155-2014.- ГОСТ Р 53941-2010 Оптика офтальмологическая. Линзы контактные. Часть 1. Термины, определения и буквенные обозначения
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7
стр. 8

стр. 9

стр. 10
стр. 11

стр. 12
стр. 13
стр. 14
стр. 15
стр. 16
стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24
стр. 25

стр. 26

стр. 27
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ГОСТР 55041 — 2012 (ИСО
11980:2009)
ОПТИКА ОФТАЛЬМОЛОГИЧЕСКАЯ ЛИНЗЫ КОНТАКТНЫЕ И СРЕДСТВА УХОДА
ЗА НИМИ
Руководство по клиническим испытаниям
ISO 11980:2009
Ophthalmic optics - Contact lenses and contact lens care products - Guid ance for clinical investigations (MOD)
Издание официальное
|
Москва Ста н дарти нформ 2014 |
Предисловие
1 ПОДГОТОВЛЕН Открытым акционерным обществом «ТКС-оптика» совместно с рабочей группой ПК 7 «Офтальмологическая оптика и приборы» Технического комитета ТК 296 «Оптика и оптические приборы» на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 296 «Оптика и оптические приборы»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 1 ноября 2012 г. № 688-ст
4 Настоящий стандарт является модифицированным по отношению к международному стандарту ИСО 11980:2009 «Офтальмологическая оптика. Контактные линзы и средства ухода за ними. Руководство по клиническим испытаниям» (ISO 11980:2009 «Ophthalmic optics - Contact lenses and contact lens care products - Guidance for clinical investigations») путем:
- изменения его структуры для приведения в соответствие с правилами, установленными в ГОСТ 1.5 (подразделы 4.2 и 4.3);
- введения дополнительных фраз. При этом дополнительные фразы, включенные в текст стандарта для учета потребностей национальной экономики Российской Федерации и особенностей национальной стандартизации, выделены курсивом.
Сравнение структуры настоящего стандарта со структурой указанного международного стандарта приведено в дополнительном приложении ДА.
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты, сведения о которых приведены в дополнительном приложении ДБ
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок - в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (gost.ru)
© Стандартинформ, 2014
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ P 55041—2012
занесения в протокол необходимо классифицировать в этой категории любые изъязвления роговицы со следующими характеристиками:
1) центральная или парацентральная локализация;
2) проникновение в мембрану Боумана;
3) инфильтрат диаметром более 2 мм;
4) ассоциация с воспалением радужной оболочки более или равной 2-й степени;
5) ассоциация с любым повышением внутрилазного давления;
6) положительная культура на микроорганизмы;
7) увеличение размера или ухудшение состояния при последующих визитах;
b) любые центральные или парацентральные роговичные явления (такие, как васкуляризация), провоцирующие стойкое помутнение;
c) любые серьезные офтальмологически неблагоприятные события, включая скопление гноя и кровоизлияние в передней камере глаза;
d) любая неоваскуляризация в пределах центральной 6-миллиметровой зоны роговицы;
e) потеря остроты зрения на две и более строки тест-таблицы, не поддающаяся восстановлению;
f) любые случаи воспаления радужной оболочки глаза.
Важные, но не тяжелые неблагоприятные события должны включать следующее:
a) стерильные периферические не прогресирующие язвы;
b) любые симптоматические явления инфильтрации;
c) любые случаи появления пятен на роговице от 3-й степени и выше;
d) временную потерю остроты зрения при наилучшей коррекции на две и более строки тест-таблицы (на срок 2 недели и более);
e) случаи неоваскуляризации 2-й степени и более;
f) любые офтальмологические явления, требующие временного прекращения ношения линз на срок 2 недели и более.
А.З Требования к обработке результатов КИ
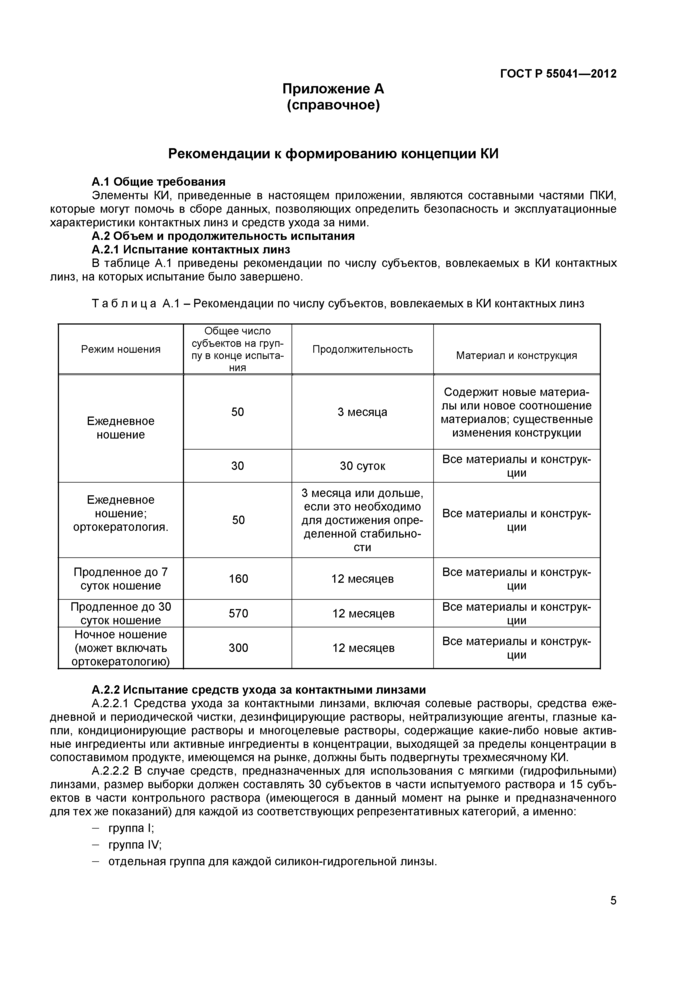
А.3.1 Таблицы А.2 - А.12 представляют собой рекомендованные сводные формы подведения результатов КИ. Для испытуемых и контрольных субъектов можно использовать отдельные таблицы. Не все таблицы применимы для всех категорий продукции.
А.3.2 Таблицу А.9 следует дублировать при каждом плановом визите для испытания с контактными линзами.
Примечание - Результаты измерения остроты зрения допускается оценивать по таблице Снеллена.
|
Таблица А.2- Число глаз, участвовавших в испытании, и распределение в зависимости от состояния | ||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||
|
ГОСТ P 55041—2012 Таблица А.З- Распределение глаз субъектов в зависимости от опыта ношения контакт-ныхлинз и от демографических данных_ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица А. 4 - Неблагоприятные события | ||||||||||||||||
| ||||||||||||||||
1
2
3
4
и т.д.________
_Общее число неблагоприятных событий, не связанных с испытуемым объектом:_
_ В связи с испытуемым объектом__
1
2
3
4
и т.д. _______
Общее число глаз, нуждающихся в лечении по причине неблагоприятных событий, вызванных испытуемым объектом:_
9
|
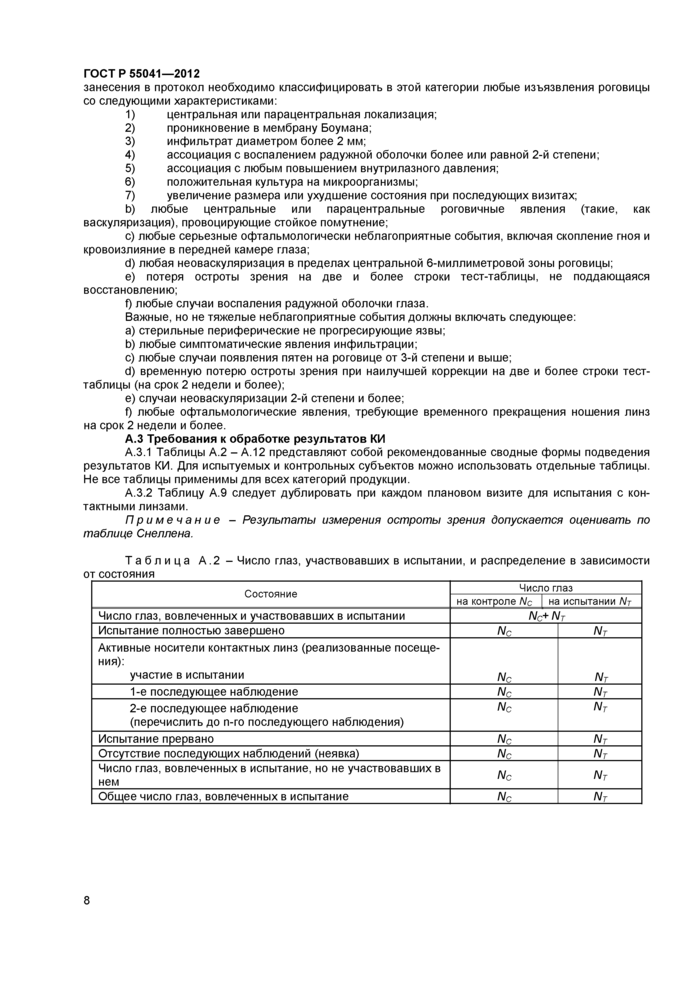
ГОСТ P 55041—2012 Таблица А.5 - Испытания со щелевой лампой (например, отека эпителия, изменения слезной пленки) по посещениям, в зависимости от числа глаз и встречаемости __ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица А.6 - Симптомы, проблемы и жалобы (например, дискомфорт) по посещениям, в зависимости от числа глаз и встречаемости ____ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
10
|
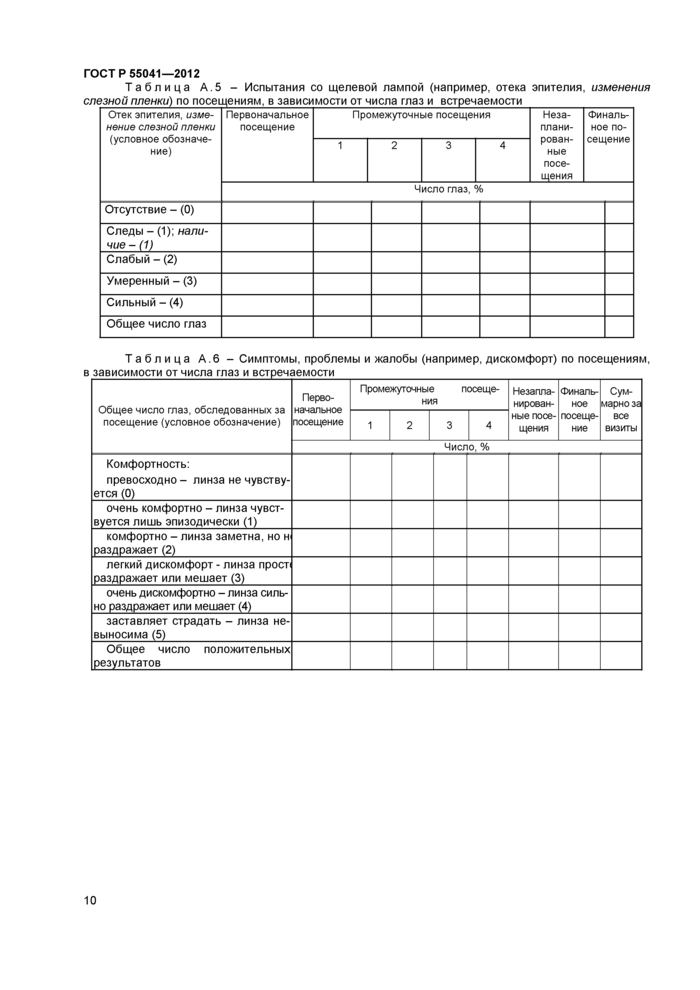
ГОСТ P 55041—2012 Таблица А.7 - Изменение кератометрии (по абсолютному значению) от первоначального обследования до финального визита по меридианам | |||||||||||
| |||||||||||
|
Среднее изменение кератометрии, дптр: Наименьшее изменение кератометрии, дптр: Наибольшее изменение кератометрии, дптр: | |||||||||||
Список горизонтальных (Г) и вертикальных (В) отсчетов по абсолютному значению кератометрии и их изменения между первоначальным обследованием и финальным визитом для глаз, у которых изменение более 1 дптр
Испытатель
Субъект
Глаз
Г/В
отсчет
Первоначальное
обследование
Финальный
визит
3)
Абсолютно^
изменени
еч
При-
ина
11 Кератометрические изменения приводят в диоптриях, а при кератоконусе дополняют картиной кератотопографии и корнеометрическими показателями.
2) Кератометрические изменения можно приводить в миллиметрах, где разность в 1,00 дптр эквивалентна разности на 0,20 мм.
3) Финальный визит для субъектов, завершивших испытание, или последний визит субъектов,
прервавших испытание._
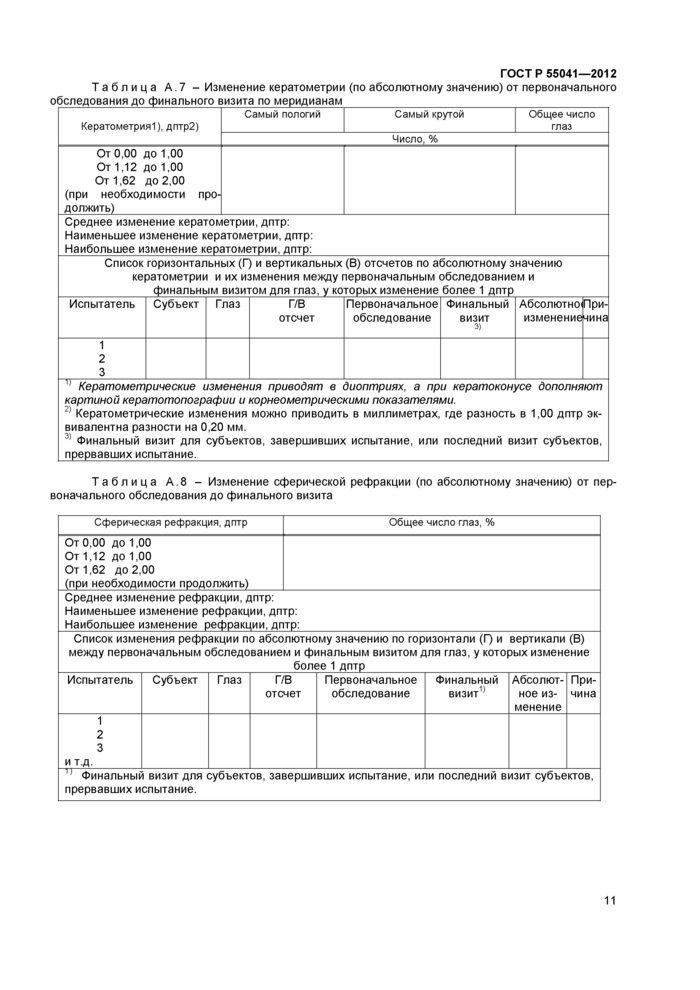
Таблица А.8 - Изменение сферической рефракции (по абсолютному значению) от первоначального обследования до финального визита
|
Сферическая рефракция, дптр |
Общее число глаз, % | |||||||
|
От 0,00 до 1,00 От 1,12 до 1,00 От 1,62 до 2,00 (при необходимости продолжить) | ||||||||
|
Среднее изменение рефракции, дптр: Наименьшее изменение рефракции, дптр: Наибольшее изменение рефракции, дптр: | ||||||||
|
Список изменения рефракции по абсолютному значению по горизонтали (Г) и вертикали (В) между первоначальным обследованием и финальным визитом для глаз, у которых изменение более 1 дптр | ||||||||
|
Испытатель |
Субъект |
Глаз |
Г/В отсчет |
Первоначальное обследование |
Финальный визит^ |
Абсолютное изменение |
При чина | |
|
1 2 3 и т.д. | ||||||||
|
и Финальный визит для субъектов, завершивших испытание, или последний визит субъектов, прервавших испытание. | ||||||||
11
ГОСТ P 55041—2012
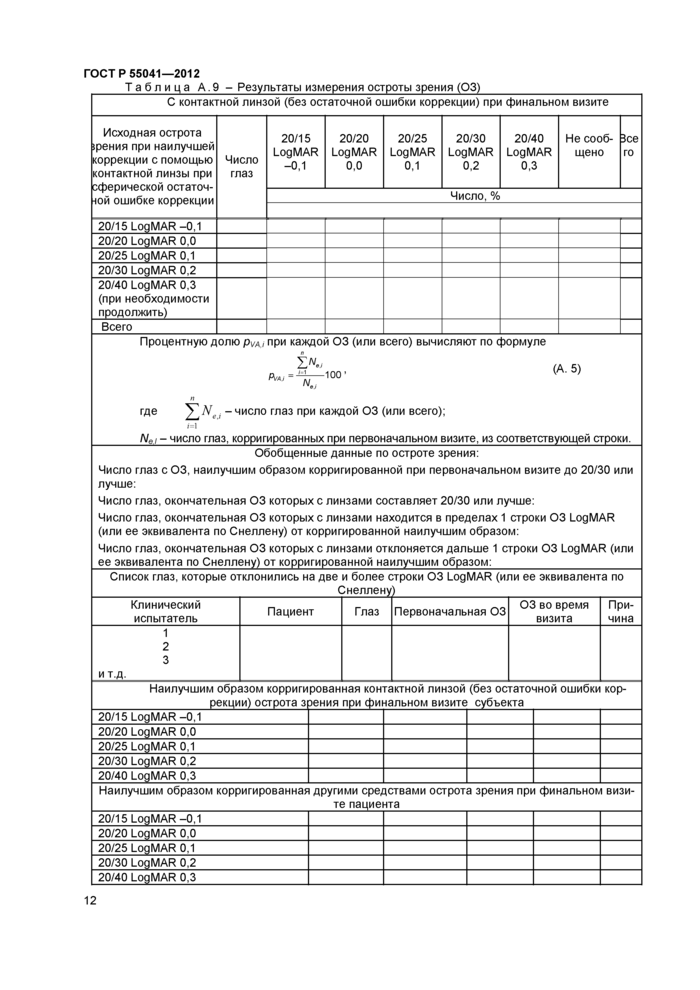
Таблица А.9 - Результаты измерения остроты зрения (03)
С контактной линзой (без остаточной ошибки коррекции) при финальном визите
Исходная острота (рения при наилучшей коррекции с помощью контактной линзы при сферической остаточной ошибке коррекции
Число
глаз
| |||||||||||||||||||||
|
Число, % |
20/15 LogMAR -0,1
20/20 Log MAR 0,0
20/25 LogMAR 0,1
20/30 LogMAR 0,2
20/40 LogMAR 0,3 (при необходимости продолжить)_
Всего
Процентную долю pVAJ при каждой 03 (или всего) вычисляют по формуле
2Х,
PvA,i
-100 ’
(А. 5)
где ^Nei - число глаз при каждой 03 (или всего);
;=1
Nei - число глаз, корригированных при первоначальном визите, из соответствующей строки.
Обобщенные данные по остроте зрения:
Число глаз с 03, наилучшим образом корригированной при первоначальном визите до 20/30 или лучше:
Число глаз, окончательная 03 которых с линзами составляет 20/30 или лучше:
Число глаз, окончательная 03 которых с линзами находится в пределах 1 строки 03 LogMAR (или ее эквивалента по Снеллену) от корригированной наилучшим образом:
Число глаз, окончательная 03 которых с линзами отклоняется дальше 1 строки 03 LogMAR (или ее эквивалента по Снеллену) от корригированной наилучшим образом:_
Список глаз, которые отклонились на две и более строки 03 LogMAR (или ее эквивалента по _Снеллену)_
Клинический
испытатель
Пациент
Глаз
Первоначальная 03
03 во время визита
При
чина
ит.д.
Наилучшим образом корригированная контактной линзой (без остаточной ошибки кор-рекции) острота зрения при финальном визите субъекта
20/15 LogMAR-0,1
20/20 LogMAR 0,0
20/25 LogMAR 0,1
20/30 LogMAR 0,2
20/40 LogMAR 0,3
Наилучшим образом корригированная другими средствами острота зрения при финальном визи-
те пациента_
20/15 LogMAR-0,1
20/20 LogMAR 0,0
20/25 LogMAR 0,1
20/30 LogMAR 0,2
20/40 LogMAR 0,3
ГОСТ P 55041—2012
|
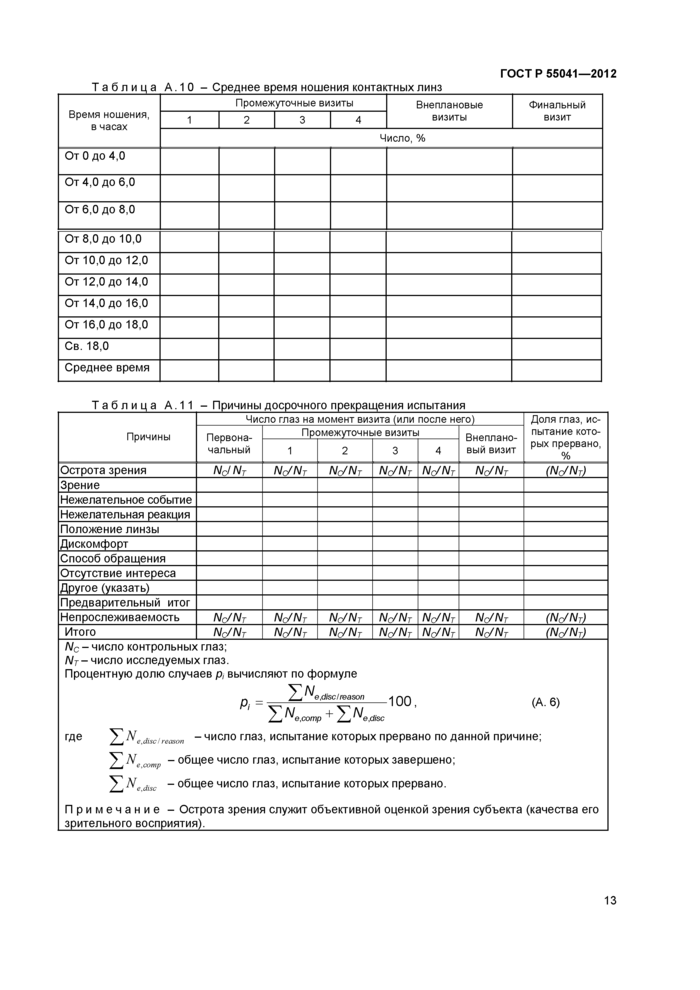
Таблица А.10 - Среднее время ношения контактных линз | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица А.11 - Причины досрочного прекращения испытания | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Л/с - число контрольных глаз;
Л/г- число исследуемых глаз.
Процентную долю случаев р, вычисляют по формуле
р _ ^ , ^е,disc/reason
Z/V^+Z^
-100,
(А. 6)
где
■е.сотр ' / 1' *e.disc
, disc/reason - число глаз, испытание которых прервано по данной причине; е сотр ~ общее число глаз, испытание которых завершено;
ZNe disc - общее число глаз, испытание которых прервано.
2Х5Х
Примечание - Острота зрения служит объективной оценкой зрения субъекта (качества его зрительного восприятия)._
13
|
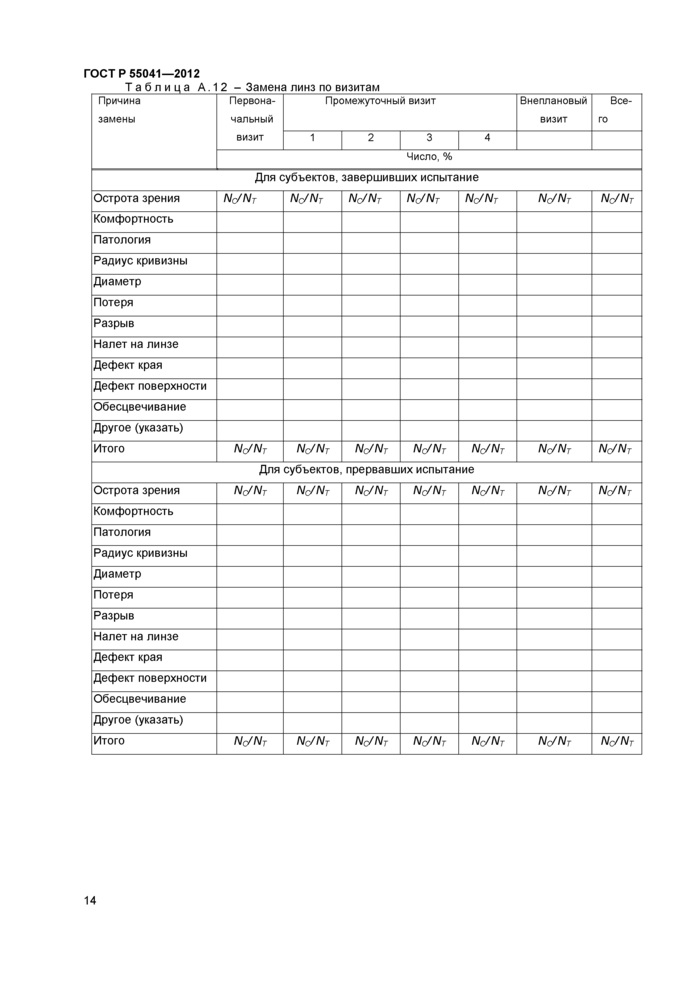
ГОСТ P 55041—2012 _Таблица А. 12 - Замена линз по визитам | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
14
Окончание таблицы А. 12
Л/с - число контрольных глаз;
Л/г- число испытуемых глаз.
Цель: обеспечение разверстки всех линз, замененных в процессе испытания, по причинам замены.
Линзы, замененные по причине остроты зрения, наличия патологии и другим физиологическим причинам, следует перечислить индивидуально с указанием конкретной причины замены и остроты зрения, достигнутой с заменяющей линзой.
Число и процентная доля относятся к числу глаз по каждой причине замены в соответствующей строке. Процентную долю случаев ре>гер/ вычисляют по формуле:
Pe/epl п
100
(А. 7)
|
/=1 |
где Л/е, - число глаз при каждом визите;
П
's^jNei - общее число глаз.
Примечание - Указать в протоколе конкретные причины по дефекту поверхности.
15
Приложение В (справочное)
Оценка безопасности, физиологической эффективности и влияния на ткани глаз
В.1 Общие требования
Оценку безопасности, физиологической эффективности и влияния на ткани глаз следует принимать во внимание методом регистрации при включении ее в ПКИ.
В.2 Отек роговицы В.2.1 Общие требования
В.2.1.1 Отек роговицы следует регистрировать отдельно для эпителия и тела роговицы.
В.2.2 Отек эпителия
В.2.2.1 Отек эпителия следует регистрировать по числу наблюдаемых микроцист:
0 - нет: отсутствие микроцист. Нормальная прозрачность;
1 - следы: от 1 до 20 микроцист. Едва различимое местное помутнение эпителия;
2 - слабый: от 21 до 50 микроцист. Слабое, но явное местное или общее помутнение эпителия;
3 - умеренный: от 51 до 100 микроцист. Значительное местное или общее помутнение эпителия;
4 - сильный: более 100 микроцист. Выраженная распространенная мутность эпителия, придающая роговице вид матового стекла или порождающая многочисленные слитные пузырьки.
Должно быть документировано наличие или отсутствие наполненных жидкостью или отходами кист с указанием их числа.
В.2.3 Отек тела роговицы
В.2.3.1 Отек тела роговицы следует регистрировать по следующей шкале:
0 - нет. Отсутствие отека;
1 - следы. Едва различимое помутнение;
2 - слабый. Слабая свильность роговицы (не более двух свилей);
3 - умеренный. Выраженная свильность роговицы (равная 3 свилям);
4 - сильный. Складки десцеметовой оболочки и более 4 выраженных свилей.
В.З Инфильтраты роговицы
В.3.1 Серьезность инфильтратов роговицы следует регистрировать по следующей шкале:
0 - нет. Отсутствие инфильтратов;
1 - следы. Отдельные или множественные инфильтраты эпителия диаметром менее 1 мм;
2 - слабые. Отдельные или множественные инфильтраты эпителия диаметром более или равным 1 мм и менее 2 мм;
3 - умеренные. Множественные инфильтраты эпителия диаметром более или равным 2 мм и менее 3 мм;
4 - сильные. Множественные плотные инфильтраты эпителия диаметром более или равным 3
мм;
В.3.2 Положение роговичных инфильтратов на роговице следует обозначать в соответствии с рисунком В.1.
Глубину роговичных инфильтратов следует характеризовать следующими аббревиатурами:
Е - эпительный;
/4S - переднероговичный;
Р- средне/заднероговичный
R - правый глаз; L - левый глаз; 1-C.no центру; 2- S: сверху; 3 - /V: к носу;4 - /: снизу; 5 - Т: к виску Рисунок В.1 - Способ регистрации положения роговичных инфильтратов
ГОСТ P 55041—2012
В.4 Правильность эндотелия
В.4.1 Правильность эндотелия следует регистрировать по следующей шкале:
0 - регулярная мозаика эндотелия;
1 - изолированные различия размеров клеток;
2 - едва заметные вариации размеров клеток или нерегулярности клеточного слоя;
3 - легко различимые вариации размеров клеток или нерегулярности клеточного слоя;
4 - явная нерегулярность клеточного слоя и потеря четкости межклеточных границ.
В.5 Васкуляризация роговицы
В.5.1 Наибольшую васкуляризацию роговицы следует отмечать по следующей шкале:
0 - нет. Отсутствие сосудистого проникновения;
1 - следы. Сосудистое проникновение менее 1,00 мм;
2 - слабая. Сосудистое проникновение от 1,00 до 1,50 мм;
3 - умеренная. Сосудистое проникновение от 1,50 до 2,00 мм;
4 - сильная. Сосудистое проникновение более 2,00 мм.
В.5.2 О глубине и положении сосудистого проникновения следует сообщать следующим образом:
Глубина: а) поверхностная;
Ь) в теле роговицы.
Положение: N - к носу; Т- к виску; / - снизу; S - сверху; CL - периферийно;
X-другое (описать).
В.6 Окрашивание роговицы под флуоресцеином
В.6.1 Окрашивание роговицы следует регистрировать по шкале:
0 - нет. Отсутствие окрашивания;
1 - следы. Минимальное поверхностное или точечное окрашивание:
a) бугорчатость, дискретное точечное окрашивание;
b) поверхностные отметки от ношения линз или следы посторонних тел;
2 - слабое. Местное или диффузное точечное окрашивание:
a) центральное или общее точечное окрашивание;
b) периферическое окрашивание, охватывающее меридиан от 3 до 9;
c) следы посторонних тел;
3 - умеренное. Плотное слитное окрашивание диаметром до 2 мм:
a) истирание роговицы;
b) след постороннего тела;
4 - сильное. Плотное слитное окрашивание диаметром свыше 2 мм.
□ - сделать отметку, если окрашивание связано с лежащим под ним инфильтратом.
□ - сделать отметку, если окрашивание не связано с лежащим под ним инфильтратом
В.6.2 Местоположение наблюдаемого окрашивания следует отметить в соответствии с рисунком В.1. Предпочтительно характеризовать это положение цифрами.
Примечания
1 Все наблюдения окрашивания роговицы следует проводить при воздействии синим светом в сочетании с желтым защитным светофильтром в системе наблюдения.
2 Рецидивную эрозию и изъязвление роговицы следует регистрировать в разделе «Прочие осложнения».
В.7 Наблюдения конъюнктивы
В.7.1 Лимбическую гиперемию следует регистрировать по шкале:
0 - нет. Отсутствие гиперемии;
1 - следы. Легкая лимбическая гиперемия (при слабой сегментации);
2 - слабая. Слабая лимбическая гиперемия (легкая по всей роговице);
3 - умеренная. Значительная лимбическая гиперемия (при выраженной сегментации);
4 - сильная. Тяжелая лимбическая гиперемия (выраженная по всей роговице).
В.7.2 Гиперемию глазного яблока следует зарегистрировать следующим образом:
0 - нет. Отсутствие гиперемии;
1 - следы. Легкая местная гиперемия;
2 - слабая. Диффузная гиперемия;
3 - умеренная. Выраженная местная или диффузная гиперемия;
4 - сильная. Диффузная эписклеральная или склеральная гиперемия.
В.7.3 Деформация конъюнктивы глазного яблока (0 - отсутствие; 1 - наличие):
правый глаз R_
левый глаз L _
Наличие или отсутствие хемоза (0 - отсутствие; 1 - наличие):
17
Введение
В настоящее время клинические испытания контактных линз и средств ухода за ними регламентируются по-разному в различных странах. Настоящий стандарт разработан с целью глобальной гармонизации. Внедрение настоящего стандарта будет представлять еще один шаг к взаимному признанию. Настоящий стандарт может также послужить основой выполнения некоторых концептуальных элементов по ГОСТ Р ИСО 9001.
ГОСТ P 55041—2012
правый глаз R левый глаз L
|
_____1— |
___ | ||
|
-- |
R L
R - правый глаз; L - левый глаз
Рисунок В.2 - Способ регистрации (по зонам конъюнктивы) квадрантов,
пораженных покраснением конъюнктивы (0 - отсутствие; 1 - наличие)
В.8 Наблюдения конъюнктивы век
В.8.1 Степень наибольшей реакции конъюнктивы век следует регистрировать по шкале:
0 - нет. Равномерный глянцевый вид конъюнктивы;
1 - следы. Легкая сыпь конъюнктивы с гладкой поверхностью;
2 - слабая. Незначительные или рассеянные бугорки или фолликулы диметром менее 1 мм;
3 - умеренная:
a) значительные или рассеянные бугорки или фолликулы диметром менее 1 мм и/или выраженная сыпь конъюнктивы;
b) окрашивание наружного участка одного века;
4 - сильная:
a) местные или сплошные бугорки или фолликулы диметром 1 мм и более;
b) окрашивание наружного участка более чем одного века.
В.8.2 Локализацию наибольшей реакции конъюнктивы век следует регистрировать для каждой из шести зон века (см. рисунок В.З).
R - веко правого глаза; L - веко левого глаза
|
Рисунок В.З - Зоны верхнего века В.9 Воспаление в передней камере Налет на эндотелии |
□ |
0 - отсутствие; 1 - наличие; |
|
Расширение передней камеры |
□ |
0 - отсутствие; 1 - наличие; |
|
Налет на роговой оболочке |
□ |
0 - отсутствие; 1 - наличие; |
|
Скопление гноя в передней камере |
□ |
0 - отсутствие; 1 - наличие. |
Верхнее веко: 1 - S - наружная тарзальная конъюнктива; 2 - С - средняя тарзальная конъюнктива; 3 -1 - внутренняя тарзальная конъюнктива; 4 - N - назальная тарзальная конъюнктива; 5 - Т-височная тарзальная конъюнктива; б - L - конъюнктива нижнего века (нижнее веко не изображено)
18
ГОСТ P 55041—2012НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИОПТИКА ОФТАЛЬМОЛОГИЧЕСКАЯ.ЛИНЗЫ КОНТАКТНЫЕ И СРЕДСТВА УХОДА ЗА НИМИРуководство по клиническим испытаниям
ОПТИКА ОФТАЛЬМОЛОГИЧЕСКАЯ.ЛИНЗЫ КОНТАКТНЫЕ И СРЕДСТВА УХОДА ЗА НИМИРуководство по клиническим испытаниям
Руководство по клиническим испытаниям
Ophthalmic optics. Contact lenses and contact lens care products. Guidance for clinical investigations
Дата введения - 2014—07—01
1 Область применения
Настоящий стандарт устанавливает руководство по клиническим испытаниям (далее - КИ) безопасности и эксплуатационных характеристик контактных линз и средств ухода за ними.
Примечание - Настоящий стандарт имеет целью гармонизировать регулирующие требования к проведению КИ, необходимых для получения клинических данных с целью установления требований маркетинга и этикетирования контактных линз и средств ухода за ними на мировом уровне. В тех случаях, когда национальная практика или регламенты законодательно нормируют некоторые требования, последние имеют преимущество перед настоящим стандартом.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 9001-2008 Системы менеджмента качества. Требования
ГОСТ Р ИСО 14155-1-2008 Руководство по применению клинических испытаний медицинских изделий. Часть 1. Общие требования
ГОСТ Р ИСО 14155-2-2008 Руководство по применению клинических испытаний медицинских изделий. Часть 2. Планирование клинических испытаний
ГОСТ Р 53941-2010 (ИСО 18369-1-2006) Офтальмологическая оптика. Линзы контактные. Часть 1. Термины, определения и буквенные обозначения
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год Если заменен ссылочный стандарт, на который дана недатированная ссылка, то рекомендуется использовать действующую версию этого стандарта с учетом всех внесенных в данную версию изменений. Если заменен ссылочный стандарт, на который дана датированная ссылка, то рекомендуется использовать версию этого стандарта с указанным выше годом утверждения (принятия). Если после утверждения настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение рекомендуется применять без учета данного изменения. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, рекомендуется применять в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены термины по ГОСТ Р ИСО 14155-1, ГОСТ Р
ИСО 14155-2, ГОСТР 53941 и [1].
4 Требования к клиническим испытаниям4.1 Общие требования
4.1.1 Должны применяться общие требования, относящиеся к КИ по ГОСТ Р ИСО 14155-1 и плану клинических испытаний (далее - ПКИ) по ГОСТ Р ИСО 14155-2, а также дополнительные требования, приведенные в 4.2.
Издание официальноеГОСТ P 55041—2012
4.1.2 Причинами досрочного прекращения КИ являются:
a) связанные с самой линзой;
b) связанные с состоянием глаза;
c) другие (см. таблицу All).
4.2 Дополнительные требования
4.2.1 Общие требования к концепции испытаний
4.2.1.1 Критерии отбора субъектов должны соотноситься с целями испытания и включать:
1) субъектов с нормальным зрением, не применяющих глазных медикаментов, в возрасте 18 лет и старше, за исключением случаев, когда испытания контактных линз проводятся по специальным показаниям для лиц моложе 18 лет, например, в случае применения ортокератологии или педиатрических афакических линз;
2) рефракцию линз в диапазоне имеющихся поверочных линз;
3) рефракцию не более 0,75 дптр (только для испытания корригирующих линз со сферической рефракцией);
4) наилучшую остроту зрения с корригирующими очками не ниже 20/25 (не выше Log MAR 0,1);
5) состояние конъюнктивы век;
6) состояние слезной пленки;
7) изменение pH слезы [до КИ - pH раствора, pH слезы (Duotest)];
8) соматический фактор (заболевание щитовидной железы, наличие сахарного диабета, другой эндокринной патологии, аллергический статус).
4.2.1.2 Критерии исключения из отбора субъектов должны соотноситься с целями испытания и должны включать:
1) любые инфекции, воспаление или другие отклонения от нормы переднего отдела глаза;
2) любые прогрессирующие глазные болезни в передней камере, противопоказанные для ношения контактных линз;
3) применение системных или глазных медикаментов, служащих противопоказанием для ношения контактных линз;
4) анамнез герпетического кератита;
5) анамнез хирургической коррекции рефракции или дефектов роговицы (за исключением случаев, когда исследуемые контактные линзы показаны для ношения при дефектах роговицы, кератоко-нусе или после операции хирургической коррекции рефракции);
6) результат обследования щелевой лампой, эквивалентный или более серьезный, чем наблюдение следов (с точностью не ниже 1-й степени);
7) васкуляризацию роговицы с проникновением более 1 мм;
8) наличие синдрома «сухого глаза»;
9) участие субъекта в клиническом испытании контактных линз или средств ухода за ними в предшествующие 30 дней.
4.2.1.3 ПКИ должен обеспечивать описание процедуры мониторинга для обеспечения стабильного качества сбора и регистрации данных.
4.2.1.4 ПКИ должен содержать план статистического анализа. Размер выборки должен быть обоснован и рассчитан по программе статистической обработки, утвержденной в установленном порядке.
4.2.2 Контактные линзы
4.2.2.1 Общие требования
КИ контактных линз, включая контактные линзы повседневного и длительного ношения, мягкие гидрогельные, силикон-гидрогельные и жесткие газопроницаемые, должны быть проведены по одной из форм, приведенных в 4.2.2.2 - 4.2.2.4.
Для ПКИ с целью демонстрации безопасности и эксплуатационных характеристик, а также специальных требований (например, комфортности), этикетирования или дополнительных показаний в клиническом протоколе должен быть заранее определен план статистического анализа (включая расчет размера выборки). ПКИ должен определить объективные результаты, чтобы способствовать выполнению этих требований.
Примечания
1 Межсубъектный контроль предпочтительнее внутрисубъектного вследствие потенциальной зависимости одного глаза от другого и предубеждения относительно соответствия субъекта.
2 В приложении А приведены рекомендации к формированию концепции КИ.
4.2.2.2 Перспективное испытание с одновременным контролем
Перспективное испытание с одновременным контролем следует применять для оценки гидро-гельных, силикон-гидрогельных и жестких газопроницаемых контактных линз. Должны применяться двустороннее перекрестное испытание или испытание контрлатеральными глазами (то есть внутрисубъекг-2
ГОСТ P 55041—2012
ное), или межсубъектный контроль. В случае применения межсубъектного контроля соотношение между числом испытуемых и контрольных субъектов должно составлять 2:1 или 1:1. Контрольная линза должна представлять собой контактную линзу, в данный момент присутствующую на рынке и используемую в том же режиме. Во избежание возможной предвзятости должны быть применены случайное распределение и маскирование (субъекта, испытателя и оценщика результатов испытания). Субъекты должны быть распределены равномерно между испытателями.
4.2.2.3 Испытание без контроля
В этом случае результаты сравнивают с предшествующим контролем. Альтернативные концепции испытаний, такие как предшествующий контроль, следует применять в случаях, когда заказчик располагает базой клинических данных по присутствующей на рынке контактной линзе, которая предназначена для использования в качестве объекта сравнения. Если применяется предшествующий контроль, то должна быть определена и соответствующим образом охарактеризована контрольная группа для сравнения с экспериментальной группой. Сопоставимость экспериментальной и контрольной групп должна быть продемонстрирована сравнением критериев отбора, демографическими данными, характеристиками рефракции, историей ношения контактных линз и примененным ПКИ.
4.2.2.4 Средства ухода за контактными линзами
Для оценки средств ухода за контактными линзами следует применять перспективное испытание с одновременным контролем по 4.2.2.2 и соблюдать общие требования по 4.2.2.1.
При испытании средств ухода за контактными линзами для большинства этих средств следует применять дневной график ношения контактных линз, с тем чтобы достичь наибольшего воздействия на субъекте средства ухода. Однако испытание линзы или средства для периодической чистки, применяемых с недельной периодичностью, может дать более ценные клинические данные в части их эффективности в том случае, когда привлеченные к испытанию субъекты подвержены пролонгированному воздействию по сравнению с аналогичным испытанием на субъектах с дневным ношением контактных линз.
При использовании ежедневного графика ношения безопасность является первоочередной задачей, поэтому необходимо после применения средства спустя один - два часа с момента надевания линзы нанести визит офтальмологу, с тем чтобы обнаружить изменение прозрачности роговицы как результат непосредственной токсической реакции.
Для средства ухода за контактными линзами с показаниями чистящего средства в конце КИ необходимо привести объективную оценку его чистящих свойств не менее чем на одной линзе, взятой у каждого субъекта.
Если изготовитель средства ухода за контактными линзами рекомендует на этикетке его применение с контактными линзами конкретного типа, совместимость средства с линзами данного типа должна быть подтверждена в ходе доклинических испытаний и КИ.
Если КИ не позволили собрать достаточно данных относительно применения средства с линзами конкретного типа (например, силикон-гидрогельными), необходимо отразить этот факт на этикетке средства.
4.2.3 Переменные параметры
4.2.3.1 Средства ухода за контактными линзами
В процессе КИ средств ухода за контактными линзами необходимо оценивать следующие переменные параметры:
a) отек роговицы;
b) инфильтраты роговицы;
c) неоднороодность эндотелия;
d) васкуляризацию роговицы;
e) пятнистость роговицы;
f) наличие воспаления глаз;
д) наличие воспаления век;
h) язву роговицы;
i) помутнение роговицы;
j) кровоизлияние в переднюю камеру глаза;
k) скопление гноя в передней камере глаза;
l) раздражение;
т) рубцы (шрамы) на роговице;
п) состояние конъюнктивы (покраснение, отек, буллезность).
В процессе КИ для подтверждения особых требований могут быть испытаны дополнительные переменные параметры.
Примечание - В приложении В приведены рекомендации по классификации некоторых таких переменных.
3
ГОСТ P 55041—2012
4.2.3.2 Контактные линзы
Помимо переменных параметров, перечисленных в 4.2.3.1, в процессе КИ контактных линз необходимо рассматривать следующие переменные параметры:
a) визуальные характеристики;
b) параметры рефракции;
c) кератометрические изменения;
d) центрирование линз;
e) подвижность линз;
f) смачиваемость передней поверхности линз;
д) налет на задней поверхности линз;
h) оценку субъектом комфортности;
i) оценку субъектом качества зрения;
j) оценку субъектом удобства манипулирования.
В процессе КИ для удовлетворения особых требований могут быть испытаны дополнительные переменные параметры.
Примечание - В приложении С приведены рекомендации по классификации некоторых таких переменных.
4.3 Прочие требования
Сведения о серьезных неблагоприятных событиях и обо всех нежелательных аппаратных дефектах должны быть запротоколированы по специальной форме и, при необходимости, направлены заказчику. Все прочие неблагоприятные офтальмологические события должны быть зарегистрированы в истории болезни стандартной формы и собраны вместе в ходе мониторинга.
4
ГОСТ P 55041—2012
Приложение А (справочное)Рекомендации к формированию концепции КИ
А.1 Общие требования
Элементы КИ, приведенные в настоящем приложении, являются составными частями ПКИ, которые могут помочь в сборе данных, позволяющих определить безопасность и эксплуатационные характеристики контактных линз и средств ухода за ними.
А.2 Объем и продолжительность испытания
А.2.1 Испытание контактных линз
В таблице А.1 приведены рекомендации по числу субъектов, вовлекаемых в КИ контактных линз, на которых испытание было завершено.
Таблица А.1- Рекомендации по числу субъектов, вовлекаемых в КИ контактных линз
|
Режим ношения |
Общее число субъектов на группу в конце испытания |
Продолжительность |
Материал и конструкция |
|
Ежедневное ношение |
50 |
3 месяца |
Содержит новые материалы или новое соотношение материалов; существенные изменения конструкции |
|
30 |
30 суток |
Все материалы и конструкции | |
|
Ежедневное ношение; ортокератология. |
50 |
3 месяца или дольше, если это необходимо для достижения определенной стабильности |
Все материалы и конструкции |
|
Продленное до 7 суток ношение |
160 |
12 месяцев |
Все материалы и конструкции |
|
Продленное до 30 суток ношение |
570 |
12 месяцев |
Все материалы и конструкции |
|
Ночное ношение (может включать ортокератологию) |
300 |
12 месяцев |
Все материалы и конструкции |
А.2.2 Испытание средств ухода за контактными линзами
А.2.2.1 Средства ухода за контактными линзами, включая солевые растворы, средства ежедневной и периодической чистки, дезинфицирующие растворы, нейтрализующие агенты, глазные капли, кондиционирующие растворы и многоцелевые растворы, содержащие какие-либо новые активные ингредиенты или активные ингредиенты в концентрации, выходящей за пределы концентрации в сопоставимом продукте, имеющемся на рынке, должны быть подвергнуты трехмесячному КИ.
А.2.2.2 В случае средств, предназначенных для использования с мягкими (гидрофильными) линзами, размер выборки должен составлять 30 субъектов в части испытуемого раствора и 15 субъектов в части контрольного раствора (имеющегося в данный момент на рынке и предназначенного для тех же показаний) для каждой из соответствующих репрезентативных категорий, а именно:
- группа I;
- группа IV;
- отдельная группа для каждой силикон-гидрогельной линзы.
5
ГОСТ P 55041—2012
Если изготовитель производит более одного типа линз и все производимые им линзы типоразмерного ряда имеют одинаковый общий химический состав, достаточно использовать только линзу с наивысшим содержанием воды.
А.2.2.3 В случае средств, предназначенных для использования с жесткими линзами, размер выборки должен составлять 15 или 30 субъектов в части испытуемого раствора и 15 субъектов в части контрольного раствора (имеющегося в данный момент на рынке и предназначенного для тех же показаний) для каждой из соответствующих групп материалов.
А.2.2.4 В случае растворов для контактных линз, не содержащих никаких новых активных ингредиентов по А.2.2.1, но содержащих какой-либо активный ингредиент в концентрации ниже интервала концентраций в имеющемся на рынке сопоставимом растворе, должно быть проведено КИ продолжительностью 1 месяц. В этом случае размер выборки должен составлять половину размера выборки, рекомендованного в А.2.2.2 и А.2.2.3, при таком же общем распределении субъектов.
А.2.3 Статистические данные для оценки продолжительности ношения
А.2.3.1 Общие требования
При первичном анализе безопасности необходимо, чтобы существенный аспект безопасности составляла частота серьезных и значительных неблагоприятных событий.
Нулевая гипотеза (Н0) исходит из того принципа, что частота конечных неблагоприятных событий в испытании (pi) за вычетом контрольной частоты конечных неблагоприятных событий (рс) больше или равна клинически несущественной разности (5) двух частот.
Альтернативная гипотеза (На) исходит из того принципа, что частота конечных неблагоприятных событий в испытании (pi) за вычетом контрольной частоты конечных неблагоприятных событий (рс) меньше клинически несущественной разности (5) двух частот.
H0\pt-Pc> 8; (А. 1)
На- Pt-Pc< s, (А. 2)
где pt - процент испытуемых субъектов;
рс - процент контрольных субъектов.
В случае распределения субъектов в пропорции 1:1 между испытательной и контрольной группами минимальное число п субъектов, на которых завершено испытание, необходимое для каждой испытательной группы, определяется формулой
„ (Z4,+ZMx)2[a(1-A) + Pc(1-Pc)]
П 2 > (А- А)
о
где а - уровень значимости (также называют частотой ошибок 1-го рода);
(1 - Р) - строгость испытания;
Z- квантиль стандартного нормального распределения.
Следующий пример иллюстрирует расчет применимости гипотез, сформулированных для КИ гидрогельных или силикон-гидрогельных контактных линз при продолжительном ношении длительностью 7 суток. При контрольной частоте рс и частоте испытания pt равной 0,033 (заданной по На), клинически несущественной разности 5 = 0,05, строгости (1 - Р) = 0,80 и уровне значимости а = 0,05 минимальное число субъектов в группе, на которых завершено испытание, составит
_ (0,84 +1,64)2 [0,033(1 - 0,033) + 0,033(1 - 0,033)]
П~ 0,052
Вышеприведенная формула действительна только при допущении альтернативной гипотезы На с условием, что частота неблагоприятных событий в испытании равна контрольной частоте: pt = рс. В случае, когда это допущение несправедливо, для получения приблизительного расчета размера выборки можно использовать следующую формулу:
„ (Z^+Z^)2[pf(1-pf) + pc(1-pc)]
П =- 5-. (А. 4)
(РгРс-§)2
Для КИ продленного 30-суточного ношения гидрогельных контактных линз в качестве контрольной линзы рекомендуется использовать линзу 7-суточного (6 ночей/7 дней) продленного ношения.
Нижеследующий пример иллюстрирует расчет на основании гипотез, которые признаны применимыми для многих КИ продленного 30-суточного ношения гидрогельных контактных линз. При
6
ГОСТ P 55041—2012
контрольной частоте рс = 0,033 и частоте испытания На = 0,053, клинически несущественной разности 5 = 0,05, строгости (1 - р) = 0,80 и уровне значимости а = 0,05 минимальное число субъектов, на которых завершено испытание, составит
_ (0,84 +1,64)2[0,053(1 - 0,053) + 0,033(1 - 0,033)] 560 П~ (0,053-0,033-0,05)2
Следует отрегулировать число вовлеченных в КИ субъектов для компенсации числа вышедших из него субъектов, которое обычно составляет 20 % - 25 % на протяжении годичного испытания контактных линз. Таким образом, для вышеприведенного примера КИ 7-суточного продленного ношения контактных линз рекомендуемый размер выборки следует довести примерно до 215 субъектов на группу. Для вышеприведенного примера КИ 30-суточного продленного ношения контактных линз рекомендуемый размер выборки следует довести примерно до 760 субъектов на группу.
В завершение испытания следует провести статистический анализ чувствительности (например, анализ со множественными введенными значениями) с тем, чтобы оценить устойчивость результата испытания с учетом недостающих испытаний в случае процента вышедших субъектов, превышающего минимальный.
А.2.3.2 Оценка гидрогельных, силикон-гидрогельных и жестких газопроницаемых контактных линз повседневного ношения
Размеры выборок рассчитывают таким образом, чтобы обеспечить с достаточной степенью достоверности получение минимум одного осложнения в функции ожидаемой частоты осложнений с доверительной вероятностью свыше 95 %, т.е. 5 % для испытательной группы из 60 субъектов, 10 % для испытательной группы из 30 субъектов. Таким образом, в группе из 30 субъектов, на которых завершено испытание, подвергнутых краткосрочному (90 суток) воздействию испытуемой продукции, в случае неблагоприятных событий, имеющих место у двух или трех субъектов, может составить угрозу биологической совместимости и принципиальной безопасности испытуемого объекта. Все испытания, имеющие результатом два и более случая неблагоприятных явлений, должны включать соответствующее обоснование, позволяющее определить безопасность и эффективность.
А.2.3.3 Оценка средств ухода за контактными линзами
Размеры клинических выборок рассчитывают таким образом, чтобы с доверительной вероятностью 95 % испытание давало, как минимум, одно осложнение с материалом данной категории, если фактическая частота осложнений более или равна 10 %. Это подразумевает, что завершенному краткосрочному (90 суток) испытанию воздействия испытуемого средства будут подвергнуты не менее 30 субъектов по каждой группе материалов. Испытания должны включать материалы всех групп интересующих материалов.
Все испытания, имеющие результатом два и более случая неблагоприятных явлений, должны включать соответствующее обоснование, позволяющее определить безопасность и эффективность.
А.2.4 Неблагоприятные события и отрицательное воздействие материалов
А.2.4.1 Общие требования
Неблагоприятные события следует дифференцировать:
- на вызванные материалом;
- не вызванные материалом.
Любые инфильтраты роговицы, изъязвления, неоваскуляризацию и т.п. следует изначально считать вызванными материалом, если только история болезни не доказывает другое их происхождение. Все изъязвления роговицы должны быть отмечены в протоколе испытания.
А.2.4.2 Серьезные неблагоприятные события
Серьезные неблагоприятные события - это такие явления, которые приводят или могут привести либо к стойкому ухудшению зрительной функции, либо к нарушению строения глаза и могут потребовать медицинского или хирургического вмешательства.
Серьезные неблагоприятные события могут включать следующие условия, создающие угрозу зрению после воздействия испытуемым объектом, не ограничиваясь ими:
а) язвы инфекционного происхождения (определяемые как прогрессирующая эрозия ткани роговицы). Предвестниками язв могут быть нерегулярные точечные инфильтраты (более 1 мм); активные повреждения с приподнятыми краями; существенная диффузная инфильтрация; проблемы в области от передней поверхности роговицы до середины стромы; эрозия с окрашенной поверхностью; отечность конъюктивы и века; реакция передней камеры (воспаление радужной оболочки); сильное покраснение глазного яблока и окружающих тканей. Симптомы язв инфекционного происхождения (микробный кератит) могут включать резкие болевые приступы; тяжелое покраснение; гнойные или слизистогнойные выделения; слезоточивость; светобоязнь. Для
7