ГОСТ Р 53594-2009
Продукция животноводства и корма. Иммуноферментный метод определения синтетических анаболических стимуляторов роста
Купить ГОСТ Р 53594-2009 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на корма, физиологические жидкости (моча), органы и ткани (мышцы, печень, глаза), а также шерсть животных и устанавливает иммуноферментный метод определения синтетических стимуляторов роста (метилтестостерона, 19-нортестостерона, дексаметазона, диэтилстильбестрола, тренболона, этинилэстрадиола и кленбутерола).
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины, определения и сокращения
4 Характеристика метода
5 Прецизионность метода
6 Требования к условиям выполнения измерений
7 Средства измерений, вспомогательное оборудование, реактивы и материалы
8 Подготовка к выполнению измерений
9 Проведение иммуноферментного анализа
10 Контроль точности результатов измерения
11 Интерпретация результатов испытаний
12 Требования безопасности
Приложение А (обязательное) Сведения по комплектации тест-систем
Приложение Б (рекомендуемое) Схема заполнения лунок планшета
Приложение В (рекомендуемое) Таблица для записи результатов анализа
| Дата введения | 01.01.2011 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Электроэнергия
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Экология
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.220 Ветеринария
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел Электроэнергия
- Раздел 11 ЗДРАВООХРАНЕНИЕ
- Раздел 11.220 Ветеринария
- Раздел 11 ЗДРАВООХРАНЕНИЕ
Организации:
| 15.12.2009 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 906-ст |
|---|---|---|---|
| Разработан | ФГУ ВГНКИ | ||
| Издан | Стандартинформ | 2010 г. |
Livestock products and feedstuffs. Immunoenzyme method of determination of the synthetic growth promoters
- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 24104-2001 Весы лабораторные. Общие технические требования
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ Р ИСО 5725-2-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
- ГОСТ Р ИСО 5725-3-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 3. Промежуточные показатели прецизионности стандартного метода измерений
- ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
- ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
- ГОСТ 20015-88 Хлороформ. Технические условия
- ГОСТ 245-76 Реактивы. Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 2652-78 Калия бихромат технический. Технические условия
- ГОСТ 27262-87 Корма растительного происхождения. Методы отбора проб
- ГОСТ 29224-91 Посуда лабораторная стеклянная. Термометры жидкостные стеклянные лабораторные. Принципы устройства, конструирования и применения
- ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
- ГОСТ 334-73 Бумага масштабно-координатная. Технические условия
- ГОСТ 4172-76 Реактивы. Натрий фосфорно-кислый двузамещенный 12-водный. Технические условия
- ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
- ГОСТ 4238-77 Реактивы. Квасцы алюмоаммонийные. Технические условия
ГОСТ 5208-81Спирт бутиловый нормальный технический. Технические условия. Заменен на ГОСТ 5208-2013.- ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
- ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
- ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269-79Мясо. Методы отбора образцов и органолептические методы определения свежести. Заменен на ГОСТ 7269-2015.- ГОСТ 8981-78 Эфиры этиловый и нормальный бутиловый уксусной кислоты технические. Технические условия
- ГОСТ 9805-84 Спирт изопропиловый. Технические условия
- ГОСТ 9968-86 Метилен хлористый технический. Технические условия
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5
стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15
стр. 16

стр. 17
стр. 18
стр. 19
ГОСТР
53594-
2009
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ПРОДУКЦИЯ ЖИВОТНОВОДСТВА И КОРМАИммуноферментный метод определения синтетических анаболических стимуляторов роста
Издание официальное
Москва
Стандартинформ
2010
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным учреждением «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГУ «ВГНКИ»)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 335 «Методы испытаний агропромышленной продукции на безопасность»
3 УТВЕРЖДЕН Приказом Федерального агентства по техническому регулированию и метрологии от 15 декабря 2009 г. № 906-ст
4 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок— в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2010
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ролизат охлаждают до (23 ± 5) °С, добавляют 5 см3 смеси этилацетата и изопропанола, перемешивают на приборе для встряхивания в течение 1 мин и центрифугируют в течение 5 мин при 4000 мин-1. Верхнюю органическую фазу переносят в круглодонную колбу вместимостью 50 см3. Экстракцию повторяют с тем же объемом смеси этилацетата и изопропанола. Органические фазы объединяют и упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — 1 мес.
8.4.5 Отобранный образец глаза, замороженный при температуре минус 20 °С, размораживают и разрезают тонким скальпелем с двух сторон. Талую внутриглазную жидкость собирают в стакан. От глаза отделяют сетчатку, объединяют с внутриглазной жидкостью и гомогенизируют. 1 г гомогената прогревают в сушильном шкафу в течение 10 мин при температуре 80 °С, охлаждают до комнатной температуры и центрифугируют в течение 10 мин при 4000 мин-1.
Срок хранения супернатанта при температуре минус 20 °С — 1 мес.
1 см3 супернатанта переносят механическим дозатором во флакон типа фалькон, добавляют 1 см3 трис-буфера молярной концентрацией 0,1 моль/дм3 и 1 см3 хлорной кислоты молярной концентрацией 0,1 моль/дм3 и перемешивают. Центрифугируют в течение 20 мин при 4000 мин-1. Супернатант переносят в новый флакон, pH доводят до (9,8 + 0,2), добавляя по каплям гидроокись натрия молярной концентрацией 1 моль/дм3 (1 н). Добавляют 2,5 см3 смеси этилацетата и изопропанола и перемешивают на приборе для встряхивания в течение 1 мин. Центрифугируют в течение 10 мин при 4000 мин-1. Верхний слой переносят в круглодонную колбу вместимостью 50 см3. Оставшийся нижний слой экстрагируют еще два раза, добавляя по 1,5 см3 смеси этилацетата и изопропанола. Верхние слои объединяют и упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — 1 мес.
8.5 Подготовка проб для проведения анализа содержания анаболиков1 в моче и печени
8.5.1 При определении содержания диэтилстильбестрола, метилтестостерона, 19-нортестосте-рона, тренболона, этинилэстрадиола и дексаметазона осуществляют гидролиз мочи. Для этого мочу центрифугируют в течение 10 мин при 3000 мин-1. Во флакон типа фалькон механическим дозатором вносят 0,5 см3 отцентрифугированной мочи, добавляют 3 см3 ацетатного буфера молярной концентрацией 0,05 моль/дм3 с pH (5,0 + 0,2) и 0,008 см3 глюкуронидазы/арилсульфатазы. Инкубируют в течение 18 ч при температуре 52 °С в водяной бане.
8.5.2 При определении содержания диэтилстильбестрола, метилтестостерона, 19-нортестосте-рона, тренболона, этинилэстрадиола и дексаметазона осуществляют гидролиз печени. Печень измельчают ножницами, освобождая от жира и соединительной ткани. 5 г измельченной печени помещают в сосуд для диспергирования, механическим дозатором вносят 5 см3 натрий-ацетатного буфера молярной концентрацией 0,05 моль/дм3 с pH (5,0 + 0,2) и гомогенизируют. 1 г гомогената переносят в чистый флакон типа фалькон, вносят 0,008 см3 глюкуронидазы/арилсульфатазы, инкубируют в течение 18 ч при температуре 52 °С в водяной бане.
8.5.3 При определении содержания диэтилстильбестрола, 19-нортестостерона, метилтестостерона и тренболона во флакон с гидролизатом мочи, полученным по 8.5.1, механическим дозатором вносят 3 см3 смеси гексана и бутанола и перемешивают в течение 30 с на приборе для встряхивания. Центрифугируют в течение 10 мин при 4000 мин-1. Верхний слой переносят в чистый флакон. Нижний слой экстрагируют повторно с тем же объемом смеси гексана и бутанола и центрифугируют в том же режиме. Верхние слои объединяют. В объединенные верхние слои вносят 3 см3 смеси метанола и дистиллированной воды и интенсивно перемешивают, отстаивают, нижний слой аккуратно переносят механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию смесью метанола и дистиллированной воды повторяют. Нижние слои объединяют и упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — 1 мес.
8.5.4 При определении содержания этинилэстрадиола и дексаметазона во флакон с гидролизатом мочи, полученным по 8.5.1, добавляют механическим дозатором 0,004 см3 раствора гидроокиси натрия молярной концентрацией 1 моль/дм3 (1 н), доводя pH до (7,0 + 0,2). Затем вносят 3,5 см3 три-хлорметана, перемешивают в течение 2 мин на приборе для встряхивания и центрифугируют в течение 10 мин при 4000 мин-1. Нижний слой переносят в круглодонную колбу вместимостью 50 см3. Верхний
слой экстрагируют повторно с тем же объемом трихлорметана и центрифугируют в том же режиме. Нижние слои объединяют и упаривают досуха на роторном испарителе при температуре 40 °С — 45 °С.
Срок хранения сухого остатка при температуре минус 20 °С — одна неделя.
8.5.5 При определении содержания этинилэстрадиола и дексаметазона во флакон с гидролизатом печени, полученным в соответствии с 8.5.2, добавляют механическим дозатором 0,001 см3 концентрированной соляной кислоты, доводя pH до (1,0 + 0,2). Затем вносят 3,5 см3 трихлорметана, экстрагируют в течение 20 мин на ультразвуковой бане и центрифугируют в течение 10 мин при 4000 мин-1. Нижний слой переносят в круглодонную колбу вместимостью 50 см3. Верхний слой экстрагируют повторно с тем же объемом трихлорметана и центрифугируют в том же режиме. Нижние слои объединяют и упаривают досуха на роторном испарителе при температуре 40 °С — 45 °С.
Срок хранения сухого остатка при температуре минус 20 С — одна неделя.
8.5.6 При определении содержания диэтилстильбестрола, 19-нортестостерона, метилтестосте-рона и тренболона во флакон с гидролизатом печени, полученным в соответствии с 8.5.2, механическим дозатором вносят 3 см3 метанола и экстрагируют в течение 20 мин на ультразвуковой бане. Центрифугируют в течение 10 мин при 4000 мин-1. Надосадочную жидкость (супернатант) аккуратно переносят механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию повторяют с тем же объемом метанола. После центрифугирования супернатанты объединяют. К осадку механическим дозатором добавляют 3 см3 смеси метанола и дистиллированной воды, помещают на 20 мин в ультразвуковую баню, центрифугируют в течение 10 мин при 4000 мин-1. Супернатанты объединяют, добавляют 2,0 см3 гексана, тщательно встряхивают и дают отстояться. Верхний гексановый слой отбрасывают. Обезжиривание супернатанта повторяют еще раз. Водно-метанольный слой после обезжиривания упаривают на роторном испарителе в течение 10 мин при температуре 50 °С — 55 °С для удаления метанола. В колбу с водным слоем вносят 5 см3 ТБМЭ, экстрагируют в течение 20 мин, перемешивая каждые 5 мин. Отстаивают до разделения фаз, верхний слой аккуратно переносят механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию ТБМЭ повторяют. Объединенные эфирные слои упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — 1 мес.
8.6 Подготовка проб для проведения анализа содержания анаболиков* в мышечной
ткани
8.6.1 При определении содержания диэтилстильбестрола, 19-нортестостерона, метилтестосте-рона и тренболона в мышечной ткани исследуемые образцы освобождают от жира и соединительной ткани. Пробу измельчают на мясорубке. Взвешивают 5 г фарша в сосуд для диспергирования, вносят механическим дозатором 5 см3 фосфатного буфера молярной концентрацией 0,067 моль/дм3 с pH (7,2 + 0,2) и гомогенизируют в течение 2 мин. В чистый флакон типа фалькон вносят 1 г гомогената и 3 см3 метанола, экстрагируют в течение 20 мин на ультразвуковой бане и центрифугируют в течение 10 мин при 4000 мин-1. Надосадочную жидкость (супернатант) аккуратно переносят механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию повторяют с тем же объемом метанола. После центрифугирования супернатанты объединяют. К осадку добавляют 3 см3 смеси метанола и дистиллированной воды, помещают на 20 мин в ультразвуковую баню, центрифугируют в течение 10 мин при 4000 мин-1. Супернатанты объединяют, добавляют 2,0 см3 гексана, тщательно встряхивают и дают отстояться. Верхний гексановый слой отбрасывают. Обезжиривание супернатанта повторяют еще раз. Водно-метанольный слой после обезжиривания упаривают в течение 10 мин при температуре 50 °С — 55 °С на роторном испарителе для удаления метанола. В колбу с водным слоем вносят 5 см3 ТБМЭ, экстрагируют в течение 20 мин, перемешивая каждые 5 мин. Отстаивают до разделения фаз. Верхний слой аккуратно переносят механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию ТБМЭ повторяют. Объединенные эфирные слои упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 С — 1 мес.
8.6.2 При определении содержания этинилэстрадиола и дексаметазона в мышечной ткани исследуемые образцы освобождают от жира и соединительной ткани. Пробу измельчают на мясорубке. Взвешивают 5 г фарша в сосуд для диспергирования, механическим дозатором вносят 5 см3 натрий-ацетатного буфера молярной концентрацией 0,1 моль/дм3 с pH (5,0 + 0,2) и гомогенизируют в течение 2 мин. 2 3
8.6.2.1 При определении содержания этинилэстрадиола во флакон типа фалькон вносят 1 г гомогената, механическим дозатором добавляют 3,5 см3 трихлорметана и экстрагируют в течение 20 мин на ультразвуковой бане. Центрифугируют в течение 10 мин при 4000 мин-1. Супернатант переносят механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию трихлормета-ном повторяют. Супернатанты объединяют и упаривают на роторном испарителе досуха при температуре 40 °С — 45 °С. Сухой остаток растворяют в 3 см3 водного метанола с массовой долей 75 %, добавляют к нему 1 см3 гексана, встряхивают в течение 1 мин на приборе для встряхивания, дают отстояться до разделения слоев и удаляют верхний слой. Процедуру обезжиривания гексаном повторяют еще раз, после чего нижний слой упаривают досуха на роторном испарителе при температуре 50 °С —55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — одна неделя.
8.6.2.2 При определении содержания дексаметазона во флакон типа фалькон вносят 2 г гомогената, мерным цилиндром добавляют 10 см3 смеси ацетонитрила и дистиллированной воды, перемешивают на приборе для встряхивания в течение 1 мин и экстрагируют в течение 20 мин на ультразвуковой бане. Центрифугируют в течение 20 мин при 3000 мин-1 при температуре 4 °С. 2,5 см3 супернатанта переносят механическим дозатором в чистый флакон типа фалькон. Добавляют 4 см3 гексана и 1 см3 хлористого метилена, перемешивают на приборе для встряхивания в течение 1 мин. Центрифугируют в течение 5 мин при 1000 мин-1. В круглодонную колбу вместимостью 50 см3 отбирают механическим дозатором 1 см3 средней фазы, что соответствует 0,2 г мышечной ткани, и упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — одна неделя.
8.7 Подготовка проб для проведения анализа содержания диэтилстильбестрола
и дексаметазона в корме
8.7.1 При определении содержания диэтилстильбестрола корм измельчают на электрической мельнице. Во флаконе типа фалькон с завинчивающейся крышкой взвешивают 1 г измельченного образца, мерным цилиндром вносят 10 см3 смеси метанола и дистиллированной воды, перемешивают в течение 5 мин на приборе для встряхивания и центрифугируют в течение 10 мин при 4000 мин-1. Супернатант (надосадочную жидкость) аккуратно переносят механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию повторяют, добавляя к осадку 5 см3 смеси метанола и дистиллированной воды. Супернатанты объединяют. Метанол упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — 1 мес.
8.7.2 При определении содержания дексаметазона корм измельчают на электрической мельнице. Во флакон типа фалькон вносят 2 г измельченного образца и 10 см3 смеси ацетонитрила и воды. Перемешивают на приборе для встряхивания в течение 1 мин и экстрагируют в течение 20 мин на ультразвуковой бане. Центрифугируют в течение 20 мин при 3000 мин-1 при температуре 4 °С. 2,5 см3 супернатанта переносят механическим дозатором во флакон типа фалькон. Добавляют 4 см3 гексана и 1,0 см3 хлористого метилена, перемешивают на приборе для встряхивания в течение 1 мин. Центрифугируют в течение 5 мин при 1000 мин-1. Механическим дозатором переносят 1 см3 средней фазы, что соответствует 0,2 г корма, в круглодонную колбу вместимостью 50 см3 и упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — одна неделя.
8.8 Приготовление рабочих растворов экстрактов испытуемых образцов для
проведения ИФА
8.8.1 При определении содержания кпенбутерола в моче, мышечной ткани, печени сухие экстракты, полученные в соответствии с 8.4.1 и 8.4.2, растворяют в 1 см3 дистиллированной воды. Сухой экстракт, полученный из глазного яблока в соответствии с 8.4.5, растворяют в 2 см3 дистиллированной воды. Тщательно перемешивают, обмывая дно и стенки колбы, переносят раствор механическим дозатором в пробирку типа эппендорф (далее — эппендорф) и центрифугируют в течение 10 мин при 7000 мин-1. 0,05 см3 супернатанта вносят механическим дозатором в чистый эппендорф, добавляют 0,45 см3 реактива № 3 из тест-системы в соответствии с приложением А, закрывают крышку и перемешивают.
Полученный раствор хранению не подлежит.
8.8.2 При определении содержания кпенбутерола в корме 0,05 см3 супернатанта, полученного в соответствии с 8.4.3, вносят механическим дозатором в чистый эппендорф, добавляют 0,45 см3 реактива № 3 из тест-системы в соответствии с приложением А, закрывают крышку и перемешивают.
ГОСТ Р 53594-2009
Срок хранения раствора при температуре от 2 °С до 8 °С — два дня.
8.8.3 При определении содержания кпенбутерола в шерсти сухой экстракт, полученный в соответствии с 8.4.4, растворяют в 0,8 см3 дистиллированной воды, тщательно перемешивают, обмывая дно и стенки колбы, переносят в эппендорф и центрифугируют в течение 10 мин при 7000 мин-1. Отбирают механическим дозатором 0,05 см3 супернатанта в чистый эппендорф, добавляют 0,45 см3 реактива № 3 из тест-системы в соответствии с приложением А и перемешивают.
Срок хранения раствора при температуре от 2 °С до 8 °С — два дня.
8.8.4 При определении содержания диэтилстильбестрола и 19-нортестостерона к сухим экстрактам мочи, печени и мышечной ткани, полученным в соответствии с 8.5.3, 8.5.6, 8.6.1, механическим дозатором добавляют 0,5 см3 реактива № 3 из тест-системы в соответствии с приложением А, тщательно обмывают дно и стенки колб и помещают на 10 мин в ультразвуковую баню. Раствор из колбы переносят механическим дозатором в эппендорф и центрифугируют в течение 10 мин при 7000 мин-1. Растворы разводят реактивом № 3 из тест-системы в соответствии с приложением А, для этого отбирают 0,02 см3 надосадочной жидкости в чистый эппендорф и добавляют реактив № 3 в количествах, указанных в таблице 2.
|
Таблица 2 | ||||||||||
|
Эппендорф закрывают крышкой и тщательно перемешивают.
Срок хранения раствора при температуре от 2 °С до 8 °С — два дня.
8.8.5 При определении содержания диэтилстильбестрола к сухому экстракту корма, полученному в соответствии с 8.7.1, добавляют механическим дозатором 1,0 см3 метанола, тщательно обмывая дно и стенки колбы, и помещают на 10 мин в ультразвуковую баню. Раствор из колбы переносят механическим дозатором в эппендорф, центрифугируют в течение 10 мин при 7000 мин-1. Вносят механическим дозатором 0,01 см3 надосадочной жидкости в чистый эппендорф, добавляют 0,99 см3 реактива № 3 из тест-системы в соответствии с приложением А, закрывают крышкой и тщательно перемешивают.
Срок хранения раствора при температуре от 2 °С до 8 °С — два дня.
8.8.6 При определении содержания метилтестостерона и тренболона к сухим экстрактам мочи, печени или мышечной ткани, полученным в соответствии с 8.5.3, 8.5.6, 8.6.1, добавляют механическим дозатором 0,5 см3 реактива № 3 из тест-системы в соответствии с приложением А, тщательно обмывают дно и стенки колбы и помещают на 10 мин в ультразвуковую баню. Раствор из колбы переносят в эппендорф, центрифугируют в течение 10 мин при 7000 мин-1, отбирают механическим дозатором 0,05 см3 надосадочной жидкости в чистый эппендорф, добавляют 0,35 см3 реактива № 3 из тест-системы в соответствии с приложением А, закрывают крышкой и тщательно перемешивают.
Срок хранения раствора при температуре от 2 °С до 8 °С — два дня.
8.8.7 При определении содержания этинилэстрадиола к сухим экстрактам мочи, печени или мышечной ткани, полученным в соответствии с 8.5.4,8.5.5 и 8.6.2, добавляют механическим дозатором 0,5 см3 реактива № 3 из тест-системы в соответствии с приложением А, тщательно обмывают дно и стенки колбы и помещают на 10 мин в ультразвуковую баню. Раствор из колбы переносят автоматической пипеткой в эппендорф и центрифугируют в течение 10 мин при 7000 мин-1. В чистый эппендорф отбирают 0,05 см3 надосадочной жидкости, добавляют 0,75 см3 реактива № 3 из тест-системы в соответствии с приложением А, закрывают крышкой и тщательно перемешивают.
Полученный раствор хранению не подлежит.
8.8.8 При определении содержания дексаметазона к сухим экстрактам мочи, печени, мышечной ткани или корма, полученным в соответствии с 8.5.4,8.5.5,8.6.3 и 8.7.2, добавляют механическим дозатором 0,5 см3 реактива № 3 из тест-системы, тщательно обмывают дно и стенки колбы и помещают на 10 мин в ультразвуковую баню. Раствор из колбы переносят в эппендорф и центрифугируют в течение 10 мин при 7000 мин-1. Из экстрактов мочи и печени отбирают в чистые эппендорфы механическим дозатором по 0,05 см3 надосадочной жидкости и добавляют по 0,45 см3 реактива № 3 из тест-системы в соответствии с приложением А. Из экстракта мышечной ткани отбирают 0,1 см3 и добавляют 0,3 см3
реактива № 3. Из экстракта корма отбирают 0,02 см3 и добавляют 0,46 см3 реактива № 3. Закрывают эппендорф крышкой и тщательно перемешивают.
Полученный раствор хранению не подлежит.
9 Проведение иммуноферментного анализа9.1 Общие положения
9.1.1 При проведении испытаний следует использовать реагенты и компоненты, входящие в один и тот же набор (тест-систему). Разбавление или замена реагентов из набора (тест-системы) другой серии не допускается.
9.1.2 Наборы (тест-системы) следует хранить при температуре от 2 °С до 8 °С в пределах срока хранения.
Категорически не допускается хранение при минусовой температуре и замораживание реагентов набора (тест-системы).
9.1.3 Окрашивание раствора хромогена является признаком его порчи и делает невозможным его применение для анализа.
9.2 Подготовка тест-системы к проведению анализа
9.2.1 Перед использованием тест-систему вынимают из холодильника и выдерживают при температуре (23 + 5) °С не менее 30 мин, после чего тщательно перемешивают содержимое флаконов. Реактив № 2 из тест-системы в соответствии с приложением А необходимо прогреть при температуре 37 °С до полного растворения кристаллов солей и тщательно перемешать.
9.2.2 После использования реагенты тест-системы сразу убирают в холодильник.
9.2.3 На всех стадиях необходимо избегать воздействия прямого солнечного света.
9.2.4 Для каждого реактива и раствора используют отдельные съемные наконечники дозаторов. Внесение растворов в лунки проводят осторожно, не касаясь наконечниками их дна и стенок.
9.2.5 Каждый исследуемый рабочий раствор экстрактов испытуемых образцов анализируют в дублях.
Примечание — Далее приведены расходы реактивов на два стрипа, что достаточно для анализа двух исследуемых образцов. Для другого числа образцов количество используемых стрипов и смешиваемых объемов реагентов изменяют в соответствии с количеством исследуемых образцов.
9.3 Приготовление рабочих растворов для проведения анализа
9.3.1 Для приготовления рабочего раствора отмывочного буфера «ОТ» в колбу вносят цилиндром 28 см3 воды, добавляют 1,47 см3 реактива № 2 из тест-системы в соответствии с приложением А, перемешивают, наносят маркировку «ОТ».
Срок хранения буфера «ОТ» в закрытой емкости при температуре от 2 °С до 8 °С — 1 мес.
9.3.2 Для приготовления рабочего раствора ферментного конъюгата «ФК» в пробирку вносят механическим дозатором 2,25 см3 реактива № 10 из тест-системы в соответствии с приложением А и 0,25 см3 реактива № 9 из тест-системы в соответствии с приложением А, перемешивают, наносят маркировку «ФК». Готовят непосредственно перед использованием.
Раствор хранению не подлежит.
9.4 Проведение испытания
9.4.1 Из планшета извлекают необходимое число стрипов. Неиспользованные стрипы тщательно заклеивают пленкой для заклеивания планшетов и хранят в упаковке при температуре от 2 °С до 8 °С в течение всего срока годности тест-системы.
9.4.2 В лунки планшета вносят механическим дозатором 0,1 см3 градуировочных растворов № 3 — КО, № 4 — К1, № 5 — К2, № 6 — КЗ, № 7 — К4, № 8 — К5 из тест-системы в соответствии с приложением А или 0,1 см3 рабочих растворов испытуемых образцов.
Каждый раствор вносят в двойной повторности (лунки-дубли).
Далее в каждую лунку вносят 0,05 см3 раствора № 1 —АТ. Стрипы заклеивают пленкой или закрывают крышкой, инкубируют в термостате при температуре 37 °С в течение 1 ч, после чего содержимое лунок сливают.
9.4.3 В лунки планшета механическим дозатором вносят 0,2 см3 раствора «ОТ», оставляют на 1—2 мин и сливают. Процедуру отмывки повторяют еще три раза. Остатки жидкости интенсивно стряхивают на чистую фильтровальную бумагу.
ГОСТ Р 53594-2009
9.4.4 В лунки планшета механическим дозатором вносят 0,15 см3 раствора «ФК», заклеивают пленкой или закрывают крышкой, инкубируют в течение 1 ч при 37 °С и отмывают, какуказано в 9.4.3.
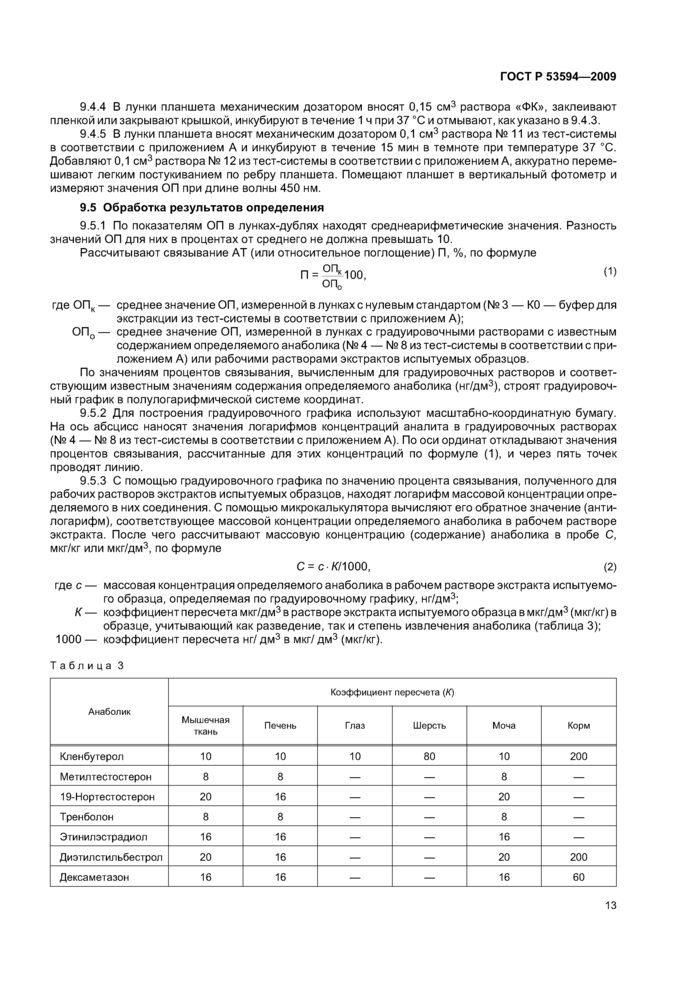
9.4.5 В лунки планшета вносят механическим дозатором 0,1 см3 раствора № 11 из тест-системы в соответствии с приложением А и инкубируют в течение 15 мин в темноте при температуре 37 °С. Добавляют 0,1 см3 раствора № 12 из тест-системы в соответствии с приложением А, аккуратно перемешивают легким постукиванием по ребру планшета. Помещают планшет в вертикальный фотометр и измеряют значения ОП при длине волны 450 нм.
9.5 Обработка результатов определения
9.5.1 По показателям ОП в лунках-дублях находят среднеарифметические значения. Разность значений ОП для них в процентах от среднего не должна превышать 10.
Рассчитывают связывание АТ (или относительное поглощение) П, %, по формуле
П = 2Пк_юо, С)
ОП0
где ОПк — среднее значение ОП, измеренной в лунках с нулевым стандартом (№3 — КО — буфер для экстракции из тест-системы в соответствии с приложением А);
ОП0 — среднее значение ОП, измеренной в лунках с градуировочными растворами с известным содержанием определяемого анаболика (№4 — № 8 из тест-системы в соответствии с приложением А) или рабочими растворами экстрактов испытуемых образцов.
По значениям процентов связывания, вычисленным для градуировочных растворов и соответствующим известным значениям содержания определяемого анаболика (нг/дм3), строят градуировочный график в полулогарифмической системе координат.
9.5.2 Для построения градуировочного графика используют масштабно-координатную бумагу. На ось абсцисс наносят значения логарифмов концентраций аналита в градуировочных растворах (№ 4 — № 8 из тест-системы в соответствии с приложением А). По оси ординат откладывают значения процентов связывания, рассчитанные для этих концентраций по формуле (1), и через пять точек проводят линию.
9.5.3 С помощью градуировочного графика по значению процента связывания, полученного для рабочих растворов экстрактов испытуемых образцов, находят логарифм массовой концентрации определяемого в них соединения. С помощью микрокалькулятора вычисляют его обратное значение (антилогарифм), соответствующее массовой концентрации определяемого анаболика в рабочем растворе экстракта. После чего рассчитывают массовую концентрацию (содержание) анаболика в пробе С, мкг/кг или мкг/дм3, по формуле
С = с/С/1000, (2)
где с — массовая концентрация определяемого анаболика в рабочем растворе экстракта испытуемого образца, определяемая по градуировочному графику, нг/дм3;
К — коэффициент пересчета мкг/дм3 в растворе экстракта испытуемого образца в мкг/дм3 (мкг/кг) в образце, учитывающий как разведение, так и степень извлечения анаболика (таблица 3); 1000 — коэффициент пересчета нг/ дм3 в мкг/ дм3 (мкг/кг).
|
Таблица 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
За окончательный результат принимают среднеарифметическое двух измерений, выполненных в условиях повторяемости, если выполняется условие приемлемости
|С1-С2|<0,01Ссрготн, (3)
где С1 и С2 — результаты определений массовой концентрации анаболика, полученные в условиях повторяемости, мкг/дм3 (мкг/кг);
Сср — среднеарифметическое результатов двух определений массовой концентрации анаболика в пробе, мкг/дм3 (мкг/кг); готн — предел повторяемости, приведенный в таблице 1, %.
9.5.4 Допускается использование любого программного обеспечения, позволяющего определять массовую концентрацию анаболика в пробе по средним значениям ОП, измеренным в лунках с градуировочными растворами и рабочими растворами экстрактов испытуемых образцов.
10 Контроль точности результатов измерения
10.1 Проверку приемлемости результатов измерений, полученных в условиях повторяемости (сходимости), промежуточной прецизионности и воспроизводимости, проводят с учетом требований ГОСТ Р ИСО 5725-6 (раздел 5).
11 Интерпретация результатов испытаний
11.1 Данный метод позволяет определять содержание анаболиков в пробах, превышающее значения, приведенные в таблице 4.
|
Таблица 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11.2 В случае обнаружения проб, в которых превышены значения, указанные в таблице 4, результаты ИФА требуют обязательного подтверждения арбитражным методом.
12 Требования безопасности
12.1 При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
12.2 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и электробезопасности при работе с электроустановками по ГОСТ 12.1.019, а также требованиям, указанным в технической документации на оборудование, необходимое при использовании тест-системы.
12.3 К выполнению измерений допускается лаборант или химик-аналитик, владеющий техникой ИФА и изучивший инструкции по применению тест-систем и инструкции по эксплуатации используемых приборов.
Приложение А (обязательное)
Сведения по комплектации тест-систем
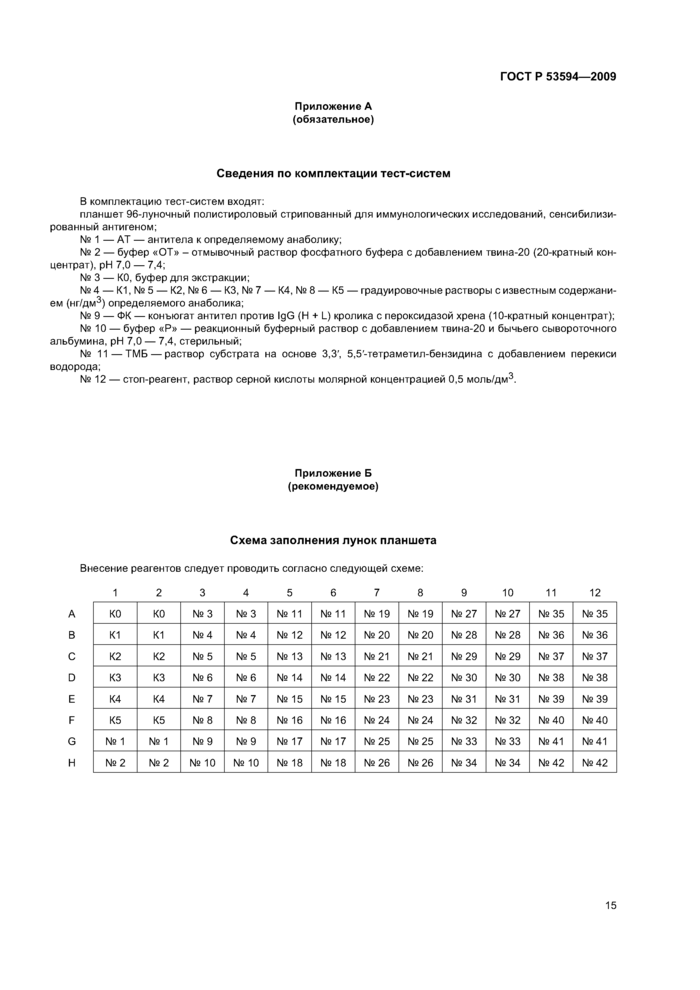
В комплектацию тест-систем входят:
планшет 96-луночный полистироловый стрипованный для иммунологических исследований, сенсибилизированный антигеном;
№ 1 — АТ — антитела к определяемому анаболику;
№ 2 — буфер «ОТ» - отмывочный раствор фосфатного буфера с добавлением твина-20 (20-кратный концентрат), pH 7,0 — 7,4;
№ 3 — КО, буфер для экстракции;
№ 4 — К1, № 5 — К2, № 6 — КЗ, № 7 — К4, № 8 — К5 — градуировочные растворы с известным содержанием (нг/дм3) определяемого анаболика;
№ 9 — ФК — конъюгат антител против IgG (Н + L) кролика с пероксидазой хрена (10-кратный концентрат);
№ 10 — буфер «Р» — реакционный буферный раствор с добавлением твина-20 и бычьего сывороточного альбумина, pH 7,0 — 7,4, стерильный;
№ 11 —ТМБ — раствор субстрата на основе 3,3', 5,5'-тетраметил-бензидина с добавлением перекиси водорода;
№ 12 — стоп-реагент, раствор серной кислоты молярной концентрацией 0,5 моль/дм3.
Приложение Б (рекомендуемое)
Схема заполнения лунок планшета
Внесение реагентов следует проводить согласно следующей схеме:
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 | |
|
А |
КО |
КО |
№3 |
№3 |
№ 11 |
№11 |
№ 19 |
№19 |
№ 27 |
№27 |
№ 35 |
№ 35 |
|
В |
К1 |
К1 |
№4 |
№4 |
№ 12 |
№12 |
№ 20 |
№ 20 |
№ 28 |
№28 |
№ 36 |
№ 36 |
|
С |
К2 |
К2 |
№5 |
№5 |
№ 13 |
№13 |
№21 |
№21 |
№ 29 |
№29 |
№ 37 |
№ 37 |
|
D |
КЗ |
КЗ |
№6 |
№6 |
№ 14 |
№14 |
№ 22 |
№ 22 |
№ 30 |
№30 |
№ 38 |
№ 38 |
|
Е |
К4 |
К4 |
№7 |
№7 |
№ 15 |
№15 |
№ 23 |
№ 23 |
№31 |
№31 |
№ 39 |
№ 39 |
|
F |
К5 |
К5 |
№8 |
№8 |
№ 16 |
№16 |
№24 |
№24 |
№ 32 |
№32 |
№ 40 |
№ 40 |
|
G |
№ 1 |
№ 1 |
№9 |
№9 |
№ 17 |
№17 |
№ 25 |
№ 25 |
№ 33 |
№33 |
№41 |
№41 |
|
Н |
№2 |
№2 |
№ 10 |
№ 10 |
№ 18 |
№18 |
№ 26 |
№ 26 |
№34 |
№34 |
№ 42 |
№ 42 |
15
Приложение В (рекомендуемое)
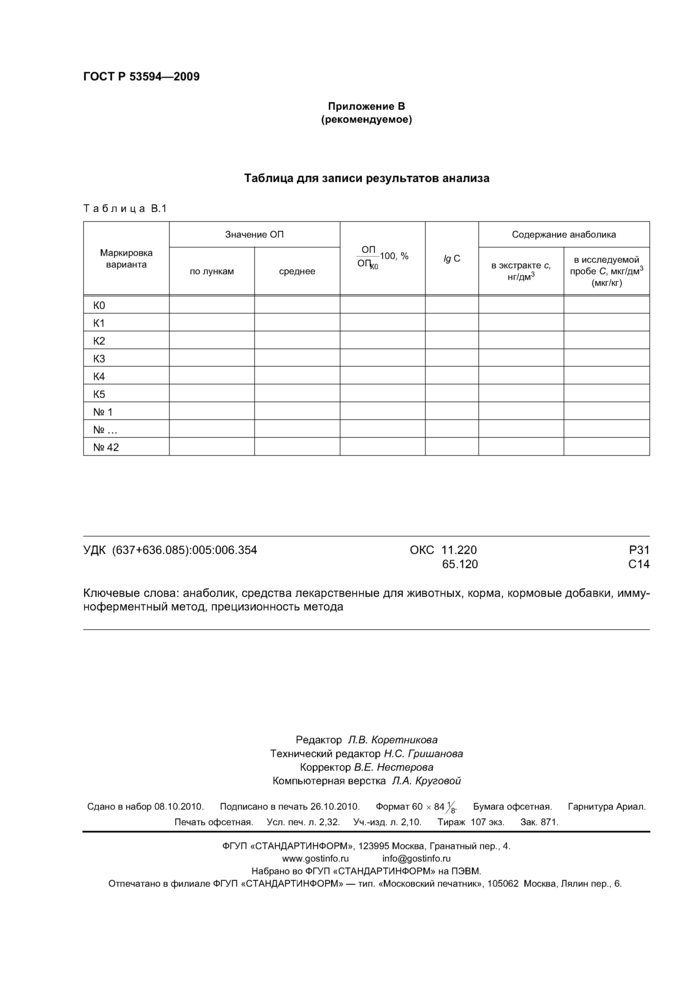
Таблица для записи результатов анализа
|
Таблица В.1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
УДК (637+636.085):005:006.354 ОКС 11.220 Р31
65.120 С14
Ключевые слова: анаболик, средства лекарственные для животных, корма, кормовые добавки, имму-ноферментный метод, прецизионность метода
Редактор Я В. Коретникова Технический редактор Н.С. Гоишанова Корректор В.Е. Нестерова Компьютерная верстка Л.А. Круговой
Сдано в набор 08.10.2010. Подписано в печать 26.10.2010. Формат 60 х 84^. Бумага офсетная. Гарнитура Ариал. Печать офсетная. Уел. печ. л. 2,32. Уч.-изд. л. 2,10. Тираж 107 экз. Зак. 871.
ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
Набрано во ФГУП «СТАНДАРТИНФОРМ» на ПЭВМ.
Отпечатано в филиале ФГУП «СТАНДАРТИНФОРМ» — тип. «Московский печатник», 105062 Москва, Лялин пер., 6.
ГОСТ Р 53594-2009Содержание
1 Область применения............................................1
2 Нормативные ссылки............................................1
3 Термины, определения и сокращения..................................2
4 Характеристика метода..........................................2
5 Прецизионность метода..........................................3
6 Требования к условиям выполнения измерений.............................3
7 Средства измерений, вспомогательное оборудование, реактивы и материалы............3
8 Подготовка к выполнению измерений...................................5
9 Проведение иммуноферментного анализа...............................12
10 Контроль точности результатов измерения..............................14
11 Интерпретация результатов испытаний................................14
12 Требования безопасности........................................14
Приложение А (обязательное) Сведения по комплектации тест-систем................15
Приложение Б (рекомендуемое) Схема заполнения лунок планшета..................15
Приложение В (рекомендуемое) Таблица для записи результатов анализа..............16
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ПРОДУКЦИЯ ЖИВОТНОВОДСТВА И КОРМА
Иммуноферментный метод определения синтетических анаболических стимуляторов роста
Livestock products and feedstuffs.
Immunoenzyme method of determination of the synthetic growth promoters
Дата введения — 2011—01—01
1 Область применения
Настоящий стандарт распространяется на корма, физиологические жидкости (моча), органы и ткани (мышцы, печень, глаза), а также шерсть животных и устанавливает иммуноферментный метод определения синтетических стимуляторов роста (метилтестостерона, 19-нортестостерона, дексамета-зона, диэтилстильбестрола, тренболона,этинилэстрадиола и кпенбутерола).
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р ИСО 5725-2-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерений
ГОСТ Р ИСО 5725-3-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 3. Промежуточные показатели прецизионности стандартного метода измерений ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.019-79 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 61-75 Реактивы. Кислота уксусная. Технические условия
ГОСТ 199-78 Реактивы. Натрий уксуснокислый 3-водный. Технические условия
ГОСТ 245-76 Натрий фосфорнокислый однозамещенный 2-водный. Технические условия
ГОСТ 334-73 Бумага масштабно-координатная. Технические условия
ГОСТ 1770-74 (ИСО 1042—83, ИСО 4788—80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 2652-78 Калия бихромат технический. Технические условия ГОСТ 3118-77 Реактивы. Кислота соляная. Технические условия
ГОСТ 4172-76 Натрий фосфорнокислый двузамещенный 12-водный. Технические условия
ГОСТ 4204-77 Реактивы. Кислота серная. Технические условия
ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 5208-81 Спирт бутиловый нормальный технический. Технические условия
ГОСТ 6552-80 Реактивы. Кислота ортофосфорная. Технические условия
Издание официальное
ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 6995-77 Реактивы. Метанол-яд. Технические условия
ГОСТ 7269-79 Мясо. Методы отбора образцов и органолептические методы определения свежести
ГОСТ 8981-78 Эфиры этиловый и нормальный бутиловый уксусной кислоты технические. Технические условия
ГОСТ 9805-84 Спирт изопропиловый. Технические условия
ГОСТ 9968-86 Метилен хлористый технический. Технические условия
ГОСТ 13496.0-80 Комбикорма, сырье. Методы отбора проб
ГОСТ 20015-88 Хлороформ. Технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 27262-87 Корма растительного происхождения. Методы отбора проб
ГОСТ 29224-97 (ИСО 386—77) Посуда лабораторная стеклянная. Термометры жидкостные стеклянные лабораторные. Принципы устройства, конструирования и применения
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины, определения и сокращения
3.1 В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1.1 тест-система: Набор (комплект) специально подобранных реагентов (реактивов) и составных частей, предназначенный для определения одного или нескольких конкретных веществ.
3.1.2 вспомогательный раствор: Раствор, приготовляемый заблаговременно и необходимый для приготовления других типов растворов.
3.1.3 рабочий раствор: Раствор одного или нескольких реактивов, приготовляемый непосредственно перед использованием и необходимый для выполнения процедуры анализа.
3.1.4 анаболик: Любая субстанция, способная поддерживать прирост мышечной ткани.
3.2 В настоящем стандарте применены следующие сокращения:
ИФА — иммуноферментный анализ;
ОП — оптическая плотность;
АГ — антиген;
АТ — антитела;
ФК — ферментный конъюгат;
ТБМЭ — трет-бутил-метиловый эфир;
ТМБ — 3, 3', 5,5'-тетраметил-бензидин.
4 Характеристика метода
4.1 Иммуноферментный метод основан на измерении содержания синтетических анаболических стимуляторов роста в пробах с помощью непрямого твердофазного конкурентного ИФА рабочих растворов экстрактов исследуемых образцов.
4.2 Непрямой твердофазный конкурентный ИФА основан на способности синтетических анаболических стимуляторов роста взаимодействовать со специфичными АТ в условиях конкуренции с белковым конъюгатом анаболика, нанесенным на поверхность лунок планшета, — твердофазным АГ.
4.3 Связавшиеся с твердой фазой АТ выявляют путем измерения интенсивности окрашивания конечного продукта реакции: вторичных антивидовых АТ, меченных пероксидазой хрена, с субстрат-хромоген ной смесью.
Аналитический сигнал (регистрируемое значение ОП), измеряющий степень взаимодействия АТ с АГ, обратно пропорционален массовой концентрации анаболика в рабочем растворе. 4
5 Прецизионность метода
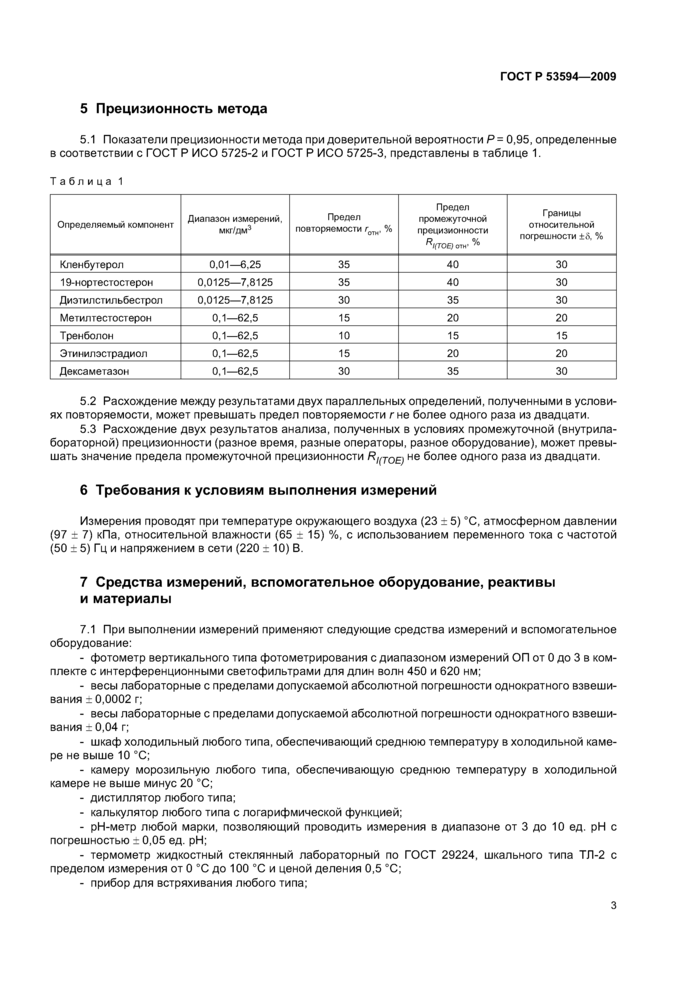
5.1 Показатели прецизионности метода при доверительной вероятности Р= 0,95, определенные в соответствии с ГОСТ Р ИСО 5725-2 и ГОСТ Р ИСО 5725-3, представлены в таблице 1.
|
Таблица 1 | ||||||||||||||||||||||||||||||||||||||||
|
5.2 Расхождение между результатами двух параллельных определений, полученными в условиях повторяемости, может превышать предел повторяемости г не более одного раза из двадцати.
5.3 Расхождение двух результатов анализа, полученных в условиях промежуточной (внутрила-бораторной) прецизионности (разное время, разные операторы, разное оборудование), может превышать значение предела промежуточной прецизионности R/fjoE) не более одного раза из двадцати.
6 Требования к условиям выполнения измерений
Измерения проводят при температуре окружающего воздуха (23 + 5) °С, атмосферном давлении (97 + 7) кПа, относительной влажности (65 + 15) %, с использованием переменного тока с частотой (50 + 5) Гц и напряжением в сети (220 + 10) В.
7 Средства измерений, вспомогательное оборудование, реактивы и материалы
7.1 При выполнении измерений применяют следующие средства измерений и вспомогательное оборудование:
- фотометр вертикального типа фотометрирования с диапазоном измерений ОП от 0 до 3 в комплекте с интерференционными светофильтрами для длин волн 450 и 620 нм;
- весы лабораторные с пределами допускаемой абсолютной погрешности однократного взвешивания + 0,0002 г;
- весы лабораторные с пределами допускаемой абсолютной погрешности однократного взвешивания + 0,04 г;
- шкаф холодильный любого типа, обеспечивающий среднюю температуру в холодильной камере не выше 10 °С;
- камеру морозильную любого типа, обеспечивающую среднюю температуру в холодильной камере не выше минус 20 °С;
- дистиллятор любого типа;
- калькулятор любого типа с логарифмической функцией;
- pH-метр любой марки, позволяющий проводить измерения в диапазоне от 3 до 10 ед. pH с погрешностью + 0,05 ед. pH;
- термометр жидкостный стеклянный лабораторный по ГОСТ 29224, шкального типа ТЛ-2 с пределом измерения от 0 °С до 100 °С и ценой деления 0,5 °С;
- прибор для встряхивания любого типа; 5
- микроизмельчитель тканей (гомогенизатор) любого типа с частотой вращения от 8000 до 24000 мин-1;
- шкаф сушильный любого типа, обеспечивающий поддержание температуры не менее (95 ± 5) °С;
- термостат любого типа, поддерживающий температуру (37 ± 1) °С;
- водяную баню любого типа, поддерживающую температуру (52 ± 1) °С;
- микроцентрифугу любого типа с частотой вращения 7000 мин-1;
- центрифугу с бакет-ротором и адаптером для флаконов типа фалькон объемом от 15 до 50 см5 и частотой вращения от 3000 до 10000 мин-1;
- ультразвуковую баню любого типа;
- роторный испаритель любого типа или устройство для испарения экстрактов, термостатируе-мый нагревательный модуль с системой отдувки растворителей инертным газом;
- мясорубку любого типа;
- электрическую мельницу любого типа;
- дозаторы механические с варьируемым объемом дозирования от 0,005 до 0,050; от 0,020 до 0,200; от 0,200 до 1,000 и от 1,000 до 5,000 см5 в комплектах со съемными одноразовыми наконечниками;
- колбы 1-50 (100,500)-2 по ГОСТ 1770;
- цилиндры 1(2,3)-10(100, 250)-1 поГОСТ 1770;
- воронки ВФ-1(2)-60-ПОР 500 ТХС по ГОСТ 25336;
- стакан Н-2-100 ТХС по ГОСТ 25336;
- колбы типов Кн-1-50-24/29 ТС и Кн-2-50-18 ТС по ГОСТ 25336;
- коническую колбу со шлифом и притертой пробкой типа Кн-1 -100-19/26 по ГОСТ 25336;
- пробирки типа П-1 -10-0,1 ХС по ГОСТ 25336;
- пробирки типа эппендорф вместимостью 1,5 см5;
- стеклянные или полипропиленовые флаконы типа фалькон с завинчивающейся крышкой для отбора проб вместимостью от 15 до 50 см5.
7.2 Допускается использование другого оборудования и средств измерения с метрологическими и техническими характеристиками не ниже указанных.
7.3 При выполнении измерений применяют следующие реактивы и материалы:
- тест-системы6 для непрямого твердофазного конкурентного ИФА в комплектации в соответствии с приложением А, которые предназначены для определения синтетических анаболических стимуляторов роста в диапазонах измерений массовых концентраций, мкг/дм5:
кпенбутерола..............................от 0,01 до 6,25;
метилтестостерона...........................от 0,1 до 62,5;
диэтилстильбестрола.........................от 0,0125 до 7,8125;
19-нортестостерона..........................от 0,0125 до 7,8125;
этинилэстрадиола...........................от 0,1 до 62,5;
тренболона...............................от 0,1 до 62,5;
дексаметазона.............................от 0,1 до 62,5;
- воду дистиллированную по ГОСТ 6709;
- спирт изопропиловый (изопропанол) по ГОСТ 9805, х.ч.;
- трис(гидроксиметил)аминометан с массовой долей основного вещества не менее 99 %;
- этиловый эфир уксусной кислоты (этилацетат) по ГОСТ 8981, х.ч.;
- кислоту хлорную массовой долей 57 %, х.ч.;
- кислоту соляную по ГОСТ 3118, концентрированную, плотностью 1,19 г/см5, х.ч.;
- спирт бутиловый (бутанол) нормальный технический по ГОСТ 5208, х.ч.;
- трихлорметан по ГОСТ 20015, х.ч.;
- гексан с содержанием основного вещества не менее 98 %, х.ч.;
- трет-бутил-метиловый эфир с массовой долей основного вещества не менее 98 %, х.ч.;
- метанол-яд по ГОСТ 6995, х.ч.;
ГОСТ Р 53594-2009
- метилен хлористый технический по ГОСТ 9968, х.ч.;
- ацетонитрил для хроматографии, ос.ч., с массовой долей основного вещества не менее 99,9 %;
- кислоту ортофосфорную по ГОСТ 6552, концентрированную, х.ч.;
- дигидрофосфат натрия 2-водный, ч.д.а., по ГОСТ 245;
- гидрофосфат натрия безводный, х.ч., по ГОСТ 4172;
- глюкуронидазу/арилсульфатазу из Helix pomatia с содержанием основного вещества 132500 ед./г;
- натрий уксуснокислый 3-водный по ГОСТ 199, х.ч.;
- натрия гидроокись по ГОСТ 4328, х.ч., растворы молярной концентрацией 5 и 1 моль/дм3;
- натрий хлористый по ГОСТ 4233, х.ч.;
- кислоту уксусную с массовой долей 20 % по ГОСТ 61;
- полиоксиэтиленсорбитан монолаурат (полисорбат 20, твин 20);
- кислоту серную по ГОСТ 4204, концентрированную;
- бихромат калия технический по ГОСТ 2652;
- бумагу масштабно-координатную по ГОСТ 334, марки Н-1.
7.4 Допускается использование других реактивов и материалов, по качеству не ниже указанных.
8 Подготовка к выполнению измерений8.1 Подготовка оборудования
8.1.1 При подготовке к проведению измерений лабораторную стеклянную посуду моют смесью водного раствора бихромата калия с концентрированной серной кислотой, многократно промывают водопроводной водой, ополаскивают дистиллированной водой и высушивают в сушильном шкафу.
8.1.2 Подготовку и проверку фотометра и pH-метра проводят в соответствии с руководствами по эксплуатации приборов.
8.2 Приготовление вспомогательных растворов для проведения подготовки проб
8.2.1 Для приготовления раствора соляной кислоты молярной концентрацией 0,1 моль/дм3 цилиндром вместимостью 10 см3 отмеряют 8,5 см3 концентрированной соляной кислоты (плотностью 1,19 г/см3), помещают в мерную колбу вместимостью 1 дм3, доводят объем раствора дистиллированной водой до метки, закрывают пробкой и тщательно перемешивают.
Срок хранения раствора при температуре (23 + 5) °С в вытяжном шкафу — 1 мес.
8.2.2 Для приготовления раствора хлорной кислоты молярной концентрацией 0,1 моль/дм3 цилиндром вместимостью 250 см3 отмеряют 169,4 см3 дистиллированной воды и переносят в коническую колбу вместимостью 200 см3. Затем цилиндром вместимостью 10 см3 отмеряют 2,0 см3 хлорной кислоты с массовой долей 57 % и переносят в ту же колбу, смесь перемешивают и закрывают пришлифованной пробкой.
Срок хранения раствора при температуре (23 + 5) °С в вытяжном шкафу— 1 мес.
8.2.3 Для приготовления раствора фосфорной кислоты молярной концентрацией 1 моль/дм3 в стакане взвешивают 9,8 г концентрированной ортофосфорной кислоты. С помощью стеклянной воронки кислоту переносят в мерную колбу вместимостью 100 см3. Стакан несколько раз обмывают дистиллированной водой, смывы переносят в мерную колбу, после чего объем доводят дистиллированной водой до метки.
Срок хранения раствора при температуре (23 + 5) °С в вытяжном шкафу— 1 мес.
8.2.4 Для приготовления трис-буфера молярной концентрацией 0,1 моль/дм3 с pH (9,5 + 0,2) навеску трис(гидроксиметил)аминометана массой 1,21 г количественно переносят в мерную колбу вместимостью 100 см3 и добавляют 50 см3 дистиллированной воды. Значение pH раствора доводят до (9,5 + 0,2), осторожно по каплям прибавляя и постоянно перемешивая раствор соляной кислоты молярной концентрацией 0,1 моль/дм3. Раствор в колбе доводят до метки дистиллированной водой и тщательно перемешивают.
Срок хранения раствора при температуре от 2 °С до 8 °С — 1 мес.
8.2.5 Для приготовления раствора ацетатного буфера молярной концентрацией 0,1 моль/дм3 с pH (5,0 + 0,2) навеску 3-водного уксуснокислого натрия массой 1,36 г количественно переносят в мерную колбу вместимостью 100 см3 и добавляют 50 см3 дистиллированной воды. Значение pH раствора доводят до (5,0 + 0,2) с помощью 20 %-ного раствора уксусной кислоты, прибавляя его осторожно по каплям и постоянно перемешивая. Раствор в колбе доводят до метки дистиллированной водой.
Срок хранения раствора при температуре от 2 °С до 8 °С — 1 мес. 7
8.2.6 Для приготовления раствора ацетатного буфера молярной концентрацией 0,05 моль/дм3 с pH (5,0 + 0,2) навеску 3-водного уксуснокислого натрия массой 0,68 г количественно переносят в мерную колбу вместимостью 100 см3 и добавляют 50,0 см3 дистиллированной воды. Значение pH раствора доводят до pH (5,0 + 0,2) с помощью 20 %-ного раствора уксусной кислоты, прибавляя его осторожно по каплям и постоянно перемешивая. Раствор доводят в колбе до метки дистиллированной водой.
Срок хранения раствора при температуре от 2 °С до 8 °С — 1 мес.
8.2.7 Для приготовления раствора ацетатного буфера молярной концентрацией 0,2 моль/дм3 с pH (5,2 + 0,2) навеску 3-водного уксуснокислого натрия массой 2,72 г количественно переносят в мерную колбу вместимостью 100 см3 и добавляют 50 см3 дистиллированной воды. Значение pH раствора доводят до (5,2 + 0,2), прибавляя 20 %-ный раствор уксусной кислоты осторожно по каплям и постоянно перемешивая. Объем раствора доводят в колбе до метки дистиллированной водой.
Срок хранения раствора при температуре от 2 °С до 8 °С — 1 мес.
8.2.8 Для приготовления раствора фосфатного буфера молярной концентрацией 0,067 моль/дм3 с pH (7,2 + 0,2) навески массами 7,67 г безводного гидрофосфата натрия, 2,02 г 2-водного дигидрофосфата натрия и 8,7 г хлорида натрия переносят количественно в мерную колбу на 1000 см3, растворяют в небольшом количестве (500 см3) дистиллированной воды. Значение pH раствора доводят до (7,2 + 0,2), осторожно по каплям прибавляя раствор фосфорной кислоты молярной концентрацией 1 моль/дм3 и постоянно перемешивая. Раствор в колбе доводят до метки дистиллированной водой.
Срок хранения раствора при температуре от 2 °С до 8 °С — 1 мес.
8.2.9 Для приготовления смеси метанола и воды цилиндром вместимостью 100 см3 отмеряют 60 см3 метанола и переносят в коническую колбу вместимостью 250 см3. Затем тем же цилиндром отмеряют 20 см3 дистиллированной воды и переносят в ту же колбу, смесь перемешивают и закрывают пришлифованной пробкой.
Срок хранения смеси при температуре (23 + 5) °С — 1 мес.
8.2.10 Для приготовления смеси гексана и бутанола цилиндром вместимостью 100 см3 отмеряют 80 см3 гексана и переносят в коническую колбу вместимостью 250 см3. Затем тем же цилиндром отмеряют 20 см3 бутилового спирта и переносят в ту же колбу, смесь перемешивают и закрывают пришлифованной пробкой.
Срок хранения смеси при температуре (23 ± 5) °С в вытяжном шкафу — 1 мес.
8.2.11 Для приготовления смеси этилацетата и изопропанола цилиндром вместимостью 250 см3 отмеряют 120 см3 этилового эфира уксусной кислоты и переносят в коническую колбу вместимостью 500 см3. Затем цилиндром вместимостью 100 см3 отмеряют 80 см3 изопропилового спирта, переносят в ту же колбу, смесь перемешивают и закрывают пришлифованной пробкой.
Срок хранения раствора при температуре (23 ± 5) °С в вытяжном шкафу — 1 мес.
8.2.12 Для приготовления смеси ацетонитрила и воды цилиндром вместимостью 100 см3отмеря-ют 70 см3 ацетонитрила и переносят в коническую колбу вместимостью 250 см3. Затем тем же цилиндром отмеряют 30 см3 дистиллированной воды, переносят в ту же колбу, смесь перемешивают и закрывают пришлифованной пробкой.
Срок хранения смеси при температуре (23 + 5) °С в вытяжном шкафу — 1 мес.
8.2.13 Для приготовления раствора водного метанола массовой долей 75 % цилиндром вместимостью 100 см3 отмеряют 75 см3 метанола и переносят в коническую колбу. Тем же цилиндром отмеряют 25 см3 дистиллированной воды, переносят в ту же колбу и перемешивают, тщательно закрывают пробкой.
Срок хранения раствора при температуре (23 ± 5) °С в вытяжном шкафу — 1 мес.
8.2.14 Для приготовления раствора твина-20 с массовой долей 0,2 % цилиндром вместимостью 100 см3 отмеряют 99,8 см3 дистиллированной воды и переносят в колбу вместимостью 100 см3. Механическим дозатором отбирают 0,2 см3 твина-20 и вносят в колбу с дистиллированной водой, тщательно смывая остатки твина-20 пипетированием. Раствор перемешивают и закрывают пробкой.
Срок хранения раствора при температуре (23 ± 5) °С не ограничен.
8.3 Общие правила подготовки проб
8.3.1 Отбор проб проводят в соответствии с ГОСТ 13496.0, ГОСТ 7269, ГОСТ 27262.
8.3.2 При отборе проб составляется акт с указанием:
- наименования и адреса места отбора пробы;
- даты отбора пробы;
- вида, возраста и пола животных (при отборе физиологических жидкостей от живых животных);
- наименования и количества отобранной пробы;
- фамилии, имени, отчества и подписи специалиста, проводившего отбор проб. 8
ГОСТ Р 53594-2009
8.3.3 Масса (объем, шт.) отбираемых образцов должна быть не менее:
- 200 г мышечной ткани без сухожилий;
- 100—300 г печени;
- 40 см3 мочи;
- один глаз;
- 100 г шерсти животных;
- корм в соответствии с ГОСТ 13496.0.
8.3.4 Каждый отобранный образец должен быть упакован в индивидуальную емкость и промаркирован с указанием:
- наименования и адреса места отбора пробы;
- даты отбора пробы;
- наименования и количества отобранной пробы.
8.3.5 Срок хранения отобранных образцов при температуре от 2 °С до 8 °С — 2 сут. При отсутствии возможности исследования образцов в течение двух суток образцы должны быть заморожены при температуре минус 20 °С со сроком хранения не более двух месяцев.
8.4 Подготовка проб для проведения анализа на содержание кленбутерола
8.4.1 При подготовке проб мочу центрифугируют в течение 10 мин при 4000 мин-1. Механическим дозатором отбирают 1 см3 отцентрифугированной мочи во флакон типа фалькон и добавляют 1 см3 раствора трис-буфера молярной концентрацией 0,1 моль/дм3 с pH (9,5 + 0,2) и 2,5 см3 смеси этилацета-та и изопропанола. Перемешивают в течение 5 мин и оставляют до расслоения фаз. Верхний слой отбирают механическим дозатором в круглодонную колбу вместимостью 50 см3. Экстракцию повторяют еще два раза, добавляя механическим дозатором по 1,5 см3 смеси этилацетата и изопропанола. Верхние слои объединяют и упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухих экстрактов при температуре минус 20 °С — 1 мес.
8.4.2 При подготовке проб мышечной ткани и печени исследуемые образцы освобождают от жира и соединительной ткани. Пробу измельчают на мясорубке. К 5 г фарша механическим дозатором добавляют 5 см3 ацетатного буфера молярной концентрацией 0,2 моль/дм3 с pH (5,2 ± 0,2) и гомогенизируют в течение 2 мин.
Во флакон типа фалькон взвешивают 2 г гомогената, добавляют механическим дозатором 1 см3 раствора хлорной кислоты молярной концентрацией 0,1 моль/дм3, перемешивают в течение 1 мин на приборе для встряхивания, после чего центрифугируют в течение 20 мин при 4000 мин'1. Надосадоч-ную жидкость (супернатант) переносят в чистый флакон. К осадку добавляют 1 см3 дистиллированной воды, перемешивают и снова центрифугируют в том же режиме. Супернатанты объединяют, pH доводят до (9,8 + 0,2) гидроокисью натрия молярной концентрацией 1 моль/дм3 (1 н). Добавляют 2,5 см3 смеси этилацетата и изопропанола, перемешивают в течение 1 мин и отстаивают. Верхний слой переносят автоматической пипеткой в круглодонную колбу вместимостью 50 см3. Экстракцию повторяют еще два раза, добавляя механическим дозатором по 1,5 см3 смеси этилацетата и изопропанола. Верхние слои объединяют и упаривают досуха на роторном испарителе при температуре 50 °С — 55 °С.
Срок хранения сухого остатка при температуре минус 20 °С — 1 мес.
8.4.3 При подготовке проб корма к навеске массой 1 г цилиндром вместимостью 25 см3 добавляют 15 см3 дистиллированной воды и интенсивно перемешивают в течение 5 мин. Центрифугируют в течение 10 мин при 4000 мин-1. Супернатант сливают в круглодонную колбу. К осадку повторно добавляют 5 см3 дистиллированной воды, перемешивают и еще раз центрифугируют в том же режиме. Супернатанты объединяют и исследуют в ИФА.
Срок хранения раствора при температуре от 2 °С до 8 °С — 1 сут.
8.4.4 Шерсть, отобранную для исследований, отмывают три раза водопроводной водой с перемешиванием. После каждой отмывки воду сливают декантацией, отжимая остатки воды из шерсти стеклянной палочкой, добавляют водный раствор твина-20 с массовой долей 0,2 %, вымачивают в течение 10 мин, сливают и отмывают три раза дистиллированной водой. Шерсть сушат в сушильном шкафу при температуре 80 °С.
Срок хранения подготовленной для исследований высушенной шерсти при температуре от 2 °С до 8 °С — один год.
0,1 г отмытой и высушенной шерсти взвешивают во флаконе типа фалькон с завинчивающейся крышкой, механическим дозатором добавляют 2,5 см3 гидроокиси натрия молярной концентрацией 5 моль/дм3 (5 н) и оставляют в сушильном шкафу на 10 мин при температуре 95 °С для гидролиза. Гид- 9
1
За исключением кленбутерола, для проведения анализа которого осуществляют подготовку проб в соответствии с 8.4.
2
* За исключением кленбутерола, для проведения анализа которого подготовку проб осуществляют в соответствии с 8.4.
3
4
5
6
Так как тест-системы используют для количественного определения анаболиков и входящие в состав тест-систем исходные компоненты предназначены для воспроизведения, хранения и передачи характеристик состава или свойств веществ (материалов), т.е. соответствуют требованиям, предъявляемым к стандартным образцам, то в соответствии с ФЗ РФ «Об обеспечении единства измерений» в сфере государственного регулирования обеспечения единства измерений следует применять стандартные образцы утвержденных типов, т.е. в установленном порядке тест-системы должны проходить процедуру утверждения типа стандартных образцов.
7
8
9