ГОСТ Р ИСО 9408-2016
Качество воды. Оценка биоразлагаемости органических соединений в водной среде. Метод оценки полной аэробной биоразлагаемости путем определения кислородной потребности в закрытом респирометре
Устанавливает метод оценки способности органических соединений и сточных вод к полному биологическому разложению в водной среде при заданной концентрации аэробных микроорганизмов путем определения потребности кислорода в закрытом респирометре. Стандарт применим к следующим органическим соединениям: a) растворимым в воде при условиях испытания; b) малорастворимым в воде при условиях испытания, для которых могут потребоваться специальные меры для получения хорошей дисперсии соединения (см. ИСО 10634); с) которые не контактируют и не взаимодействуют с абсорбентом СО2; d) летучим веществам при условии, что используется соответствующий респирометр или соответствующие условия (уменьшенное соотношение объема над жидкостью к объему жидкой среды); е) не подавляющим испытываемые организмы при концентрации, выбранной для испытания.
Идентичен ISO 9408:1999
Оглавление
1 Область применения
2 Термины и определения
3 Сущность метода
4 Условия испытания
5 Реактивы
6 Оборудование
7 Метод
8 Расчет и представление результатов
9 Достоверность результатов
10 Протокол испытания
Приложение А (справочное) Пример расчета теоретической потребности кислорода
Приложение В (справочное) Коррекция кислородного поглощения для интерференции нитрификацией
Приложение С (справочное) Пример кривой биологического разложения
Приложение D (справочное) Закрытый респирометр
Библиография
19 страниц
| Дата введения | 01.02.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Строительство
- Раздел Экология
Организации:
| 29.06.2016 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 738-ст |
|---|---|---|---|
| Разработан | ФГУП СТАНДАРТИНФОРМ | ||
| Разработан | ФГУП ВНИИ СМТ | ||
| Издан | Стандартинформ | 2016 г. |
Water quality. Evaluation of biodegradability of organic compounds in an aqueous medium. Method of evaluation of ultimate aerobic biodegradability by determination of oxygen demand in a closed respirometer
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14
стр. 15

стр. 16

стр. 17

стр. 18

стр. 19
ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ГОСТР ИСО 9408-2016
КАЧЕСТВО ВОДЫ
Оценка биоразлагаемости органических соединений в водной среде.
Метод оценки полной аэробной биоразлагаемости путем определения кислородной потребности в закрытом респирометре
(ISO 9408:1999, ЮТ)
Издание официальное
Ш
Москва
Стандартинформ
2016
Предисловие
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием «Всероссийский научно-исследовательский институт стандартизации материалов и технологий» (ФГУП «ВНИИ СМТ») на основе официального перевода на русский язык англоязычной версии стандарта, указанного в пункте 4 стандарта, который выполнен ФГУП «СТАНДАРТИНФОРМ»
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 326 «Биотехнологии»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 июня 2016 г. № 738-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 9408:1999 «Качество воды. Оценка биоразлагаемости органических соединений в водной среде. Метод оценки полной аэробной биоразлагаемости путем определения кислородной потребности в закрытом респирометре» (ISO 9408:1999 «Water quality — Evaluation of ultimate aerobic biodegradability of organic compounds in aqueous medium by determination of oxygen demand in a closed respirometer», IDT)
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 1.0-2012 (раздел 8). Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячно издаваемом информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
©Стандартинформ, 2016
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
II
Примечание — Поскольку COD химического вещества редко бывает таким же большим, как ThOD, то процентов разложение COD обычно выше процентного разложения ThOD, значение которого более точное и его следует использовать предпочтительнее.
8.1.3 Расчет удаления DOC
Когда определяется удаление DOC водорастворимого испытуемого соединения, для каждого испытательного сосуда FT рассчитывают процентное удаление растворенного органического углерода Dc, используя следующее уравнение (4):
(4)
где рсТ0 — массовая концентрация DOC, в миллиграммах на литр за время 0, в испытательном сосуде FT> мг/л;
Рсво — массовая концентрация DOC, за время 0, в сосуде контрольной пробы FB, мг/л;
Pdf— массовая концентрация DOC, за время f, в испытательном сосуде FT> мг/л;
Рсвг— массовая концентрация DOC, за время f, в сосуде контрольной пробы FB, мг/л.
Если рсТ0 рассчитывают из добавленного испытуемого соединения, то р сВ0 пренебрегают.
8.1.4 Расчет первичного биологического разложения
(5)
п - PS "Рт Us--
•100,
(5)
п - PS "Рт Us--
•100,
Когда проведены специальные анализы испытуемого соединения, рассчитывают процент биологического разложения Ds испытуемого соединения по сравнению с количеством испытуемого соединения в сосуде Fs в конце испытания, применяя уравнение (5).
где ps — массовая концентрация испытуемого соединения в испытательной колбе Fs за время t, мг/л; р т — массовая концентрация испытуемого соединения в испытательной колбе FT за время t, мг/л.
8.1.5 Контрольное соединение, абиотическая очистка и контроль ингибирования
Таким же образом рассчитывают степень биологического разложения и удаления DOC контрольного соединения Fc и, если включено, результат проверки абиотической очистки Fs и контроля ингибирования F,.
8.2 Представление результатов
Составляют таблицу измеренных значений BOD и процентов биологического разложения DThOD и/или Dcod для каждого испытательного сосуда и для каждого интервала измерения. В случае применения автоматических респирометров, могут выбираться соответствующие точки времени с автоматически наносимой кривой поглощения кислорода. Строят кривую биологического разложения (в процентах) в зависимости от времени и указывают лаг-фазу (скрытое время) и фазу разложения. Если получены сравнимые результаты для дублирующих испытательных сосудов FT (с разницей < 20 %), то строят среднюю кривую, в противном случае строят кривые для каждого сосуда (см. пример в приложении С). Таким же образом стоят кривую биологического разложения испытуемого соединения Fc и, если включено, график кривой проверки абиотической очистки Fs и кривой контроля ингибирования F,.
Определяют среднее значение процентного биологического разложения в фазе плато на кривой или используют наивысшее значение, например, когда кривая снижается в фазе плато, и указывают этот максимальный уровень биологического разложения как «степень биологического разложения испытуемого соединения» в протоколе испытания.
Информация о токсичности испытуемого соединения может помочь при интерпретации результатов испытания, показывая низкое биологическое разложение. Если в сосуде F, процент биологического разложения < 25 % и наблюдается недостаточное разложение испытуемого соединения в сосудах FT, то можно предположить, что испытуемое соединение является ингибитором. В этом случае испытание следует повторить при более низкой концентрации испытуемого вещества или другом инокуляте. Если в сосуде Fs (при включении проверки абиотической очистки) наблюдается значительный рост количества (> 10 %) BOD, то могут происходить процессы абиотического разложения.
Если определено удаление DOC, первичное разложение и/или нитрит/нитрат, то указывают измеренные и рассчитанные значения. Указываются измеренные значения pH.
ГОСТ Р ИСО 9408-20169 Достоверность результатов9.1 Критерий достоверности
9.1 Критерий достоверности
Испытание считается достоверным, если:
a) процентное разложение в сосуде Fc (проверка инокулята) составляет более 60 % на 14 день;
b) количество BOD в контрольной пробе FB в конце испытания, которое обычно составляет от 20 мг/л до 30 мг/л, не превышает 60 мг/л после 28 дней.
Если пункт а) или Ь) не выполняется, то испытание следует повторить, используя другой или лучше предварительно обработанный инокулят.
9.2 Ингибирование
Если в испытание включен сосуд F, (контроль ингибирования), предполагается, что испытуемое соединение подавляется, когда процент разложения контрольного соединения в сосуде F, становится ниже 40 % в конце испытания. В этом случае рекомендуется повторить испытание при более низкой концентрации испытуемого соединения.
9.3 Значение pH
Если значение pH в конце испытания выходят за пределы диапазона от 6 до 8,5 (в результате нитрификации азотосодержащего испытуемого соединения), и если процентное разложение испытуемого соединения составляет менее 60 %, то рекомендуется повторить испытание при более низкой концентрации испытуемого соединения, используя не нитрофицированный активный ил в качестве инокулята или увеличивая буферность неорганической среды. Об этом необходимо указывать в протоколе испытания.
10 Протокол испытания
В протокол испытания должна входить, как минимум, следующая информация:
a) ссылка на данный стандарт;
b) любая информация необходимая для идентификации испытуемого соединения;
c) все полученные данные измерений и расчетов (к примеру, в табличной форме), а также кривая разложения;
d) концентрация, ThOD и/или COD используемых испытуемых и контрольных соединений;
e) наименование использованного контрольного соединения и разложение, полученны с этим соединением;
f) источник, характеристики, концентрация или объем используемого инокулята и информация о любой предварительной обработке;
д) основные характеристики использованного респирометра;
h) температура инкубации при испытании;
i) если включено, процент удаления DOC или первичного биологического разложения;
j) если включено, процент разложения, полученного в сосуде Fs (абиотическая очистка);
k) если включено, процент разложения, полученного в сосуде F, (проверка ингибирования), и заявление о токсичности испытуемого соединения;
l) причины в случае отклонения испытания;
т) любое изменение стандартной процедуры или любого другого обстоятельства, которое может повлиять на результаты.
9
Приложение А (справочное)
Пример расчета теоретической потребности кислорода
А.1 Общие положения
Теоретическая потребность кислорода (ThOD) гипотетического вещества Сс Hh CLC! Nn Nana 00 Pp Ss относительной молекулярной массы может быть рассчитана по уравнению:
Д
NH,
16[2с + -(/? -cl -3n) + 3s + ^р + ^па -0] Мг
Этот расчет предполагает, что С минерализован до С02, Н до Н20, Р до Р205и Ыадо Na20. Галоген исключен как галогеноводород. Азот исключен как аммоний и не окислен до нитрита или нитрата. Предполагается что сера окислена до +\/1-валентного состояния.
В случае азотосодержащего соединения, азот может быть исключен после нитрификации, как нитрит или нитрат, при теоретических потребностях кислорода равных соответственно:
ThOD,
NO,
16[2c + -(/?-c/) + 3s + -n + |p + -na-0]
i\Z
А.2 Пример: глюкоза
Молекулярная формула С6Н1206 и молекулярная масса Мг = 180
16[2-6 + — -12-6]
ThOD = = 1,07 мг/мг соединения.
180
А.З Пример: натриевый п-додецилбензолсульфонат
Молекулярная формула C18H29S03Na и молекулярная масса Мг = 348
16[2-18+--29 + 3 + — -3]
ThOD =- = 2,34 мг/мг соединения.
А.4 Пример: ди-л-додециламин
Молекулярная формула (C12H25)2NH и молекулярная масса Мг = 353. Допускается полное нитратное образование, наблюдаемое при анализе.
ThOD =
16 [2 ■ 24 + --51+-] 2 2
348
= 3,44 мг/мг соединения.
10
ГОСТ Р ИСО 9408-2016Приложение В (справочное)Коррекция кислородного поглощения для интерференции нитрификацией
Коррекция кислородного поглощения для интерференции нитрификацией
Если происшедшая нитрификация была неполной, то наблюдаемое поглощение кислорода реакционной смесью может быть скорректировано на количество кислорода, использованного на окисление аммония до нитрита, и нитрита до нитрата, если определены изменения в концентрации во время инкубации нитрита и нитрата, учитывая следующие уравнения:
2NH4CI + 302 = 2HN02 + 2HCI + 2Н20; (В.1)
2HN02 + 02 = 2HN03. (В.2)
В итоге
2NH4CI + 402 = 2HN03 + 2HCI + 2Н20. (В.З)
Из уравнения (В. 1) поглощение кислорода, когда 28 г азота, содержащегося в хлориде аммония (1МН4С1), окислены до нитрита, равно 96 г, т. е. показателю 3,43 (96/28). Таким же образом из уравнения (В.З) поглощение кислорода, когда 28 г азота окислены до нитрата, равно 128 г, т. е. показателю 4,57 (128/28).
Поскольку реакции идут последовательно и выполняются различимыми и отличающимися видами бактерий, возможно увеличение или уменьшение концентрации нитритов. В случае уменьшения концентрации нитритов должна быть создана эквивалентная концентрация нитрата. Так, кислорода, поглощенного при образовании нитрата в 4,57 раза больше увеличения концентрации нитрат-N, в то время как кислорода связанного с образованием нитрита в 3,43 раза больше увеличения концентрации нитрита-N. С уменьшением концентрации, потеря кислорода в 3,43 раз больше уменьшения в концентрации.
Это означает:
|
°1 = 4,57 • ano3-n- |
(В.4) |
|
02 = 3,43 ■ Ano2n- |
(В.5) |
|
03 = - [3,43 • Ano3 n ]> |
(В.6) |
|
где 01 —кислород, поглощенный при образовании нитрата; 02 — кислород, поглощенный при образовании нитрита; 03 — потеря кислорода при исчезновении нитрита; ANo3 n — увеличение концентрации нитрат-N; ANo2 N — изменение концентрации нитрит-N. Так что, применяя уравнения (В.4) и (В.5) или (В.6): О4 = [4,57 • A|\io3 N ] ± [3,43 • Амо3 n!> |
(В-7) |
|
и тогда о5 = о6 - о4, |
(В-8) |
где 04 — поглощение кислорода в результате нитрификации;
05 — поглощение кислорода в результате окисления углерода;
Ое — суммарное наблюдаемое поглощение кислорода.
Альтернативно, если определен только суммарный окисленный азот, то поглощение кислорода в результате нитрификации может быть приравнено, в первом приближении, кувеличениюв4,57 раз концентрации окисленного азота.
Скорректированное значение поглощения кислорода в результате окисления углерода затем сравнивают с ThODNH3> как рассчитано в приложении А.
11
Приложение С (справочное)
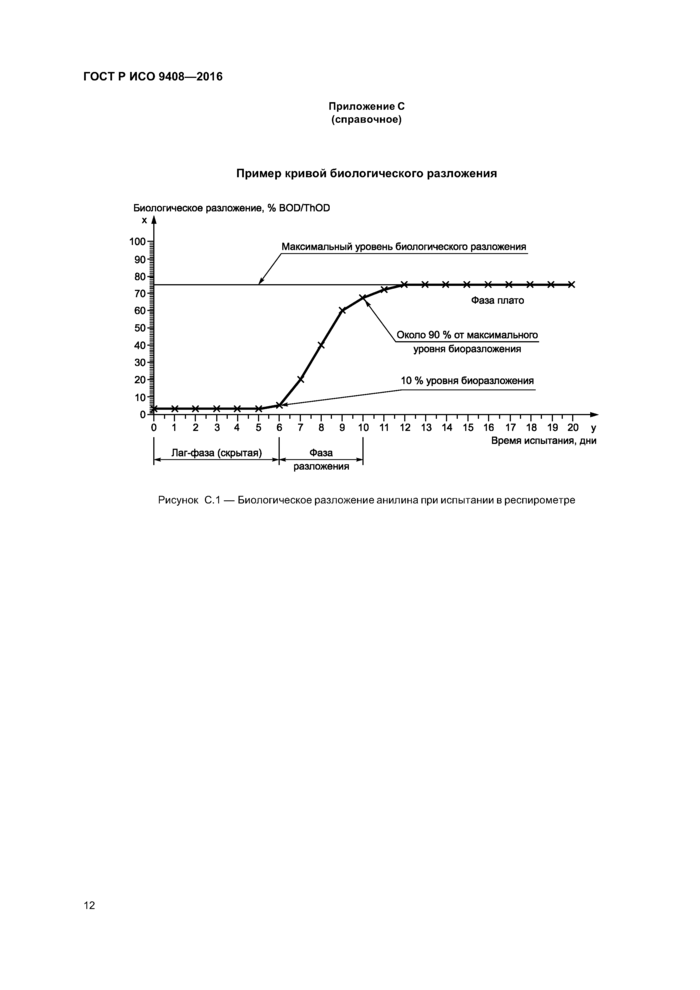
Пример кривой биологического разложения
|
Биологическое разложение, % BOD/ThOD |
|
Лаг-фаза (скрытая) Время испытания, дни |
Фаза
разложения
Рисунок С.1 — Биологическое разложение анилина при испытании в респирометре
12
Приложение D (справочное)
|
Закрытый респирометр |
|
1 — абсорбент СС>2- 2 — монитор; 3 — принтер, графопостроитель или компьютер; 4 — манометр; 5 — водяная баня; 6 — ’блок продуцирования кислорода; 7 — испытательный сосуд (колба); 8 — мешалка |
Рисунок D.1 — Принцип действия закрытого респирометра
Испытываемая смесь перемешивается магнитной мешалкой в испытательном сосуде, приблизительно на одну треть наполненном жидкостью. Если происходит биологическое разложение, микроорганизмы поглощают кислород и выделяют диоксид углерода. Кислород, находящийся в газовой фазе в сосуде, затем растворяется в жидкости. Диоксид углерода в верхней части сосуда абсорбируется и общее давление в сосудезатем уменьшается.
Падение давления, определенное манометром, используется для инициирования электролитического образования кислорода. После восстановления начального давления электролиз останавливается и монитором измеряется потребленное количество электричества. Количество потребленного электричества пропорционально поглощению кислорода. Это указывается на графопостроителе, принтере или непосредственно на компьютере.
13
Библиография
[1] ИСО 7827:1994, Качество воды. Определение способности органических соединений к полному аэробному биологическому разложению в водной среде. Метод с применением анализа растворенного органического углерода.
[2] ИСО 8192:1986, Качество воды. Тест по ингибированию поглощения кислорода активированным илом.
[3] ИСО 8245:1999, Качество воды. Руководство по определению содержания общего органического углерода (ТОС) и растворенного органического углерода (DOC).
[4] ИСО 9887:1992, Качество воды. Оценка способности каэробному биохимическому разложению органических соединений в водной среде. Полунепрерывный метод с применением активного ила.
[5] ИСО 9888, Качество воды. Оценка способности органических соединений к аэробному биологическому разложению в водной среде. Статические испытания (метод Цан-Велленса).
[6] ИСО 10634:1995, Качество воды. Руководящие указания по подготовке и обработке малорастворимых в воде органических соединений для последующей оценки их биоразложений в водной среде.
[7] ИСО 11923, Качество воды. Определение содержания взвешенных частиц путем фильтрации через стекловолокнистые фильтры.
[8] ИСО 15462, Качество воды. Выбор испытаний для оценки способности к биологическому разложению.
14
УДК 551.464.3:006.354 ОКС 13.060.70
Ключевые слова: качество воды, биоразлагаемость органических соединений, водная среда, полная аэробная биоразлагаемость, кислородная потребность, закрытый респирометр
15
Редактор И.А. Косорукова Технический редактор В.Ю. Фотиева Корректор И.А. Королева Компьютерная верстка А.Н. Золотаревой
Сдано в набор 06.07.2016. Подписано в печать 08.08.2016. Формат 60 х 84^. Гарнитура Ариал. Уел. печ. л. 2,32. Уч.-изд. л. 2,06. Тираж 34 экз. Зак. 1913.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Издано и отпечатано во ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
ГОСТ Р ИСО 9408-2016Содержание
1 Область применения...................................................1
2 Термины и определения.................................................1
3 Сущность метода.....................................................2
4 Условия испытания....................................................3
5 Реактивы..........................................................3
6 Оборудование.......................................................4
7 Метод............................................................4
8 Расчет и представление результатов........................................7
9 Достоверность результатов..............................................9
10 Протокол испытания..................................................9
Приложение А (справочное) Пример расчета теоретической потребности кислорода..........10
Приложение В (справочное) Коррекция кислородного поглощения для интерференции нитрификацией...................................................11
Приложение С (справочное) Пример кривой биологического разложения..................12
Приложение D (справочное) Закрытый респирометр...............................13
Библиография........................................................14
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИКАЧЕСТВО ВОДЫОценка биоразлагаемости органических соединений в водной среде.Метод оценки полной аэробной биоразлагаемости путем определения кислородной потребности в закрытом респирометре
Оценка биоразлагаемости органических соединений в водной среде.Метод оценки полной аэробной биоразлагаемости путем определения кислородной потребности в закрытом респирометре
Water quality. Evaluation of biodegradability of organic compounds in an aqueous medium.
Method of evaluation of ultimate aerobic biodegradability by determination of oxygen demand in a closed respirometer
Дата введения — 2017—02—01
1 Область применения
Настоящий стандарт устанавливает метод оценки способности органических соединений и сточных вод к полному биологическому разложению в водной среде при заданной концентрации аэробных микроорганизмов путем определения потребности кислорода в закрытом респирометре.
Настоящий стандарт применим к следующим органическим соединениям:
a) растворимым в воде при условиях испытания;
b) малорастворимым в воде при условиях испытания, для которых могут потребоваться специальные меры для получения хорошей дисперсии соединения (см. ИСО 10634);
c) которые не контактируют и не взаимодействуют с абсорбентом С02;
d) летучим веществам при условии, что используется соответствующий респирометр или соответствующие условия (уменьшенное соотношение объема над жидкостью к объему жидкой среды);
e) не подавляющим испытываемые организмы при концентрации, выбранной для испытания.
Наличие подавляющего действия может определяться, как установлено в 7.3, или путем применения любого другого метода определения подавляющего действия соединения на бактерии (см., например, ИС08192).
Примечание — Условия, описанные в настоящем стандарте, не всегда соответствуют оптимальным условиям, позволяющим получить максимальную степень биологического разложения.
Альтернативные методы биологического разложения см. ИСО 15462.
2 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
2.1 полное аэробное биологическое разложение (ultimate aerobic biodegradation): Разложение микроорганизмами химического соединения или органического вещества в присутствии кислорода до диоксида углерода, воды и минеральных солей любого из присутствующих элементов (минерализация) и продуцирование новой биомассы.
2.2 первичное биологическое разложение (primary biodegradation): Структурное изменение (трансформация) химического соединения микроорганизмами, ведущее к потере характерного свойства.
2.3 активный ил (activated sludge): Биомасса, продуцированная в аэробно обработанной сточной воде в результате роста бактерий и других микроорганизмов в присутствии растворенного кислорода.
2.4 концентрация взвешенных твердых частиц активного ила (concentration of suspended solids of activated sludge): Количество твердых частиц, полученных путем фильтрации или центрифугирования известного объема активного ила и высушивания примерно при 105 °С до постоянной массы.
Издание официальное
2.5 биохимическая потребность кислорода (biochemical oxygen demand, BOD): Массовая концентрация растворенного кислорода, поглощенная при установленных условиях аэробного биологического окисления химическим соединением или органическим веществом в воде.
Примечание — В данном случае она выражается в мг поглощения кислорода на мг (или г) испытуемого соединения.
2.6 химическая потребность кислорода (chemical oxygen demand, COD): Массовая концентрация кислорода, эквивалентная количеству установленного окислителя, поглощенного химическим соединением или органическим веществом, когда проба воды обработана окислителем при определенных условиях.
Примечание — В данном случае она выражается в мг поглощения кислорода на мг (или г) испытуемого соединения.
2.7 теоретическая потребность кислорода (theoretical oxygen demand, ThOD): Теоретическое максимальное количество кислорода, необходимое для полного окисления химического соединения, рассчитанное по молекулярной формуле.
Примечание — В данном случае оно выражается в миллиграммах требуемого кислорода на мг (или г)
испытуемого соединения.
2.8 растворенный органический углерод (dissolved organic carbon, DOC): Часть органического углерода в пробе воды, которую нельзя удалить установленным фазовым разделением.
Примечание — Примеры установленного фазового разделения—это центрифугирование при 40 ООО м/с1 в течение 15 мин или мембранная фильтрация с диаметром пор от 0,2 мкм до 0,45 мкм.
2.9 лаг-фаза (lag phase): Время от начала испытания до достижения адаптации и/или селекции разложившихся микроорганизмов и превышения степени биологического разложения химического соединения или органического вещества примерно на 10 % выше максимального уровня биологического разложения.
Примечание — Обычно выражается в днях.
2.10 максимальный уровень биологического разложения (maximum level of biodegradation): Максимальная степень биологического разложения химического соединения или органического вещества при испытании, выше которой биологическое разложение во время испытания не происходит.
Примечание — Обычно выражается в процентах.
2.11 фаза биологического разложения (biodegradation phase): Время от конца лаг-фазы испытания до достижения почти 90 % максимального уровня биологического разложения.
Примечание — Обычно выражается в днях.
2.12 фаза плато (plateau phase): Время от конца фазы биологического разложения до конца испытания.
Примечание — Обычно выражается в днях.
2.13 предварительное воздействие (pre-exposure): Предварительная инкубация инокулята (посевной культуры) в присутствии испытываемого химического соединения или органического вещества с целью усилить способность этого инокулята к биологическому разложению испытуемого материала путем адаптации и/или селекции микроорганизмов.
2.14 предварительная обработка (preconditioning): Предварительная инкубация инокулята (посевной культуры) при условиях последующего испытания в отсутствии испытуемого химического соединения или органического вещества с целью улучшения характеристик испытания путем акклиматизации микроорганизмов кусловиям испытания.
3 Сущность метода
Определение биологического разложения органических соединений аэробными микроорганизмами проводится с использованием статичной водной системы испытания. В органические соединения в контексте данного стандарта входят сточные воды. Испытываемая смесь состоит из неорганической среды, органического соединения в качестве единственного источника углерода и энергии при массовой концентрации органического углерода обычно 100 мг/л (но ее теоретическая потребность кислорода
ГОСТ Р ИСО 9408-2016
(ThOD) должна быть не менее 100 мг/л), и смешанного инокулята, полученного со станции очистки сточных вод или другого источника в округе.
Смесь перемешивается в закрытом испытательном сосуде, и определяется поглощение кислорода либо путем измерения количества кислорода, необходимого для сохранения постоянного объема газа в респирометре, либо путем измерения изменения объема или давления (или их комбинации) в приборе. Выделенный диоксид углерода абсорбируется соответствующим веществом в испытательном сосуде.
За разложением, продолжающимся в течение 28 дней или более, при необходимости, следует определение поглощения кислорода автоматически или вручную. Количество кислорода, поглощенного органическим соединением (после коррекции по сравнению с контрольной пробой), выражается процентным содержанием либо теоретической потребности кислорода (ThOD), рассчитанной по формуле соединения, либо химической потребности кислорода (COD).
Для достаточно хорошо растворимых в воде соединений может определяться (как вариант) удаление растворенного органического углерода (DOC) путем измерения концентрации DOC в начале и в конце инкубации для получения дополнительной информации о полном биологическом разложении.
4 Условия испытания
Инкубация должна происходить в темноте либо при рассеянном свете, в температурном диапазоне от 20 °С до 25 °С, который не должен меняться более чем на +1 °С.
5 Реактивы
Все реактивы должны быть известной степени чистоты.
5.1 Вода
Вода, дистиллированная или деионизированная, содержащая менее чем 1 мг/л DOC.
5.2 Среда испытания5.2.1 Состав
5.2.1.1 Раствора Растворяют:
калия безводный дигидрофосфат (КН2Р04) 8,5 г, калия безводный гидрофосфат (К2НР04) 21,75 г, натрия дигидрат гидрофосфата (Na2HP04 -2H20) 33,40 г, аммония хлорид (NH4CI) 0,5 г
в воде (5.1), доводят необходимым количеством воды до 1000 см2.
Чтобы проверить этот буферный раствор, рекомендуется измерить pH, который должен быть около 7,4. Если это не так, готовят новый раствор.
5.2.1.2 Раствор b
Растворяют 22,50 г гептагидрата сульфата магния (MgS04 • 7НгО) в воде (5.1), доводят необходимым количеством воды до 1000 см2.
5.2.1.3 Растворе
Растворяют 36,40 г дигидрата хлорида кальция (СаС12 • 2НгО) в воде (5.1), доводят необходимым количеством воды до 1000 см2.
5.2.1.4 Раствор d
Растворяют 0,25 г гексагидрата хлорида железа (III) (FeCI3 • 6Н20) в воде (5.1), доводят необходимым количеством воды до 1000 см2. Во избежание выпадения осадка этот раствор готовят свежим непосредственно перед использованием или добавляют каплю концентрированной хлороводородной кислоты (HCI).
5.2.2 Приготовление испытательной среды
Для приготовления 1000 см2 испытательной среды добавляют примерно к 800 см2 воды (5.1):
- 10 см2 раствора а;
- 1 см2 каждого из растворов b—d.
Доводят до 1000 см2 водой (5.1). Свежую испытательную среду готовят перед использованием. Растворы от а до с могут храниться до 6 месяцев в темноте при комнатной температуре.
5.3 Абсорбент диоксида углерода
Раствор гидроксида калия (около 10 моль/л), гранулы натровой извести или другой подходящий абсорбент.
5.4 Раствор хлорида ртути
Растворяют 1 гхлорида ртути (II) (НдС12) в 100 см3 воды (5.1).
5.5 Раствор гидроксида натрия
Растворяют гидроксид натрия (NaOH) в воде (5.1), чтобы получить раствор с концентрацией, начиная от 0,1 моль/л до 0,5 моль/л.
5.6 Раствор соляной кислоты
Разбавляют концентрированную соляную кислоту (HCI) в воде (5.1), чтобы получить раствор с концентрацией от 0,1 моль/л до 0,5 моль/л.
6 Оборудование
Обеспечивают полную чистоту всей стеклянной посуды и отсутствие как органических, так и токсических веществ.
6.1 Закрытый респирометр
Принцип действия закрытого респирометра приведен в приложении D. Респирометр содержит испытательные сосуды, в которые может подаваться и перемешиваться кислород, с непроницаемыми трубками для кислорода и диоксида углерода. Сосуды в респирометре находятся при постоянной комнатной температуре или в водяной бане с термостатическим контролем. Для испытаний летучих соединений, следует использовать соответствующий прибор или адаптированный кданной конкретной цели. Требуется соблюдение осторожности, чтобы не было потери соединения по причине самого прибора.
6.2 Водяная баня или постоянная комнатная температура (соблюдать с разделом 4)
6.3 Оборудование для измерения растворенного органического углерода
Прибор достаточной чувствительности для измерения растворенного органического углерода (DOC)(no выбору).
6.4 Устройство определения химической потребности кислорода (COD) (по выбору)6.5 Центрифуга или устройство для фильтрации
Центрифуга должна иметь возможность получения ускорения 4000 г.
Прибор для фильтрации оснащается мембранными фильтрами (с номинальным диаметром отверстия пор от 0,20 мкм и 0,45 мкм), которые не абсорбирует или выделяют органический углерод.
6.6 pH-метр, измеритель кислотности (обычное лабораторное оборудование)7 Метод7.1 Приготовление растворов для испытания7.1.1 Испытуемое соединение
7.1 Приготовление растворов для испытания7.1.1 Испытуемое соединение
Готовят основной раствор достаточно растворимого испытуемого соединения в испытательной среде (5.2) и добавляют соответствующее количество этого раствора в испытательные сосуды, чтобы получить окончательную массовую концентрацию испытуемого соединения 100 мг/л, но эквивалентную не менее 100 мг/л ThOD. В зависимости от свойств испытуемого соединения (т. н. токсичности) и цели испытания могут использоваться и другие концентрации. Соединения с низкой растворимостью в воде добавляют прямо в испытательные сосуды. Точно определяют добавленное количество. По требованию определяют COD испытуемого соединения, используя, например, ИСО 6060.
Примечание — О подробностях обращения с малорастворимыми соединениями см. ИСО 10634.
7.1.2 Раствор контрольного соединения
В качестве контрольного соединения используют органическое соединение с известным биологическим разложением, такое как анилин или бензойнокислый натрий, имеющим степень разложения более 60 %. Готовят основной раствор контрольного соединения в среде теста (5.2) таким же образом,
4
ГОСТ Р ИСО 9408-2016
как с растворимым в воде испытуемым соединением (7.1.1), чтобы получить окончательную массовую концентрацию 100 мг испытуемого соединения на литр среды испытания.
7.1.3 Раствор для проверки ингибирования
При необходимости (если отсутствует информация о токсичности испытуемого соединения) готовят раствор, содержащий, в среде теста (5.2), как испытуемое соединение (7.1.1), так и контрольное соединение (7.1.2), желательно при массовой концентрации для каждого 100 мг/л.
7.2 Приготовление инокулята (посевной культуры)7.2.1 Общие положения
Инокулят готовят, используя предпочтительно активный ил или следующие источники (7.2.2—7.2.4), или смесь этих источников, чтобы получить микрофлору, которая предлагает достаточную активность биологического разложения. Проверяют активность инокулята посредством контрольного соединения (7.1.2 и раздела 9). Значение BOD должно удовлетворять критерию достоверности (см. раздел 9). Чтобы уменьшить влияние контрольной пробы, полезно предварительно обработать инокулят аэрацией в течение до одной недели перед использованием. Используют соответствующий объем для инокуляции.
Примечание — Обычно инокулят не должен подвергаться предварительному воздействию испытуемым соединением, чтобы сделать возможный общий прогноз поведения разложения в окружающей среде. При некоторых обстоятельствах, в зависимости от цели испытания, предварительное воздействие может использоваться при условии, что об этом четко заявлено в результатах испытания (т. н. процентное биоразложение равно х %, при использовании инокулята с предварительным воздействием), и метод предварительного воздействия подробно описан в протоколе испытания. Инокуляте предварительным воздействием можно получить при лабораторных испытаниях на биологическое разложение, проведенных при разнообразных условиях (т. н. испытание Цан-Велленса (ИСО 9888) и испытание SCAS (ИСО 9887)) или из проб, собранных из мест, где существуют соответствующие условия окружающей среды (например, обрабатывающие заводы, связанные с подобными веществами или загрязненными зонами).
На основании практического опыта, соответствующий объем означает:
- объем, которыйдостаточен,чтобыдать флору, которая предлагает достаточную активность биологического разложения;
- объем, который разлагает контрольное соединение в известном процентном отношении (см. раздел 9);
- объем, который дает от 103 до 106 колониеобразующих единиц на миллилитр в окончательной смеси;
- объем, который дает не более чем эквивалент, равный 30 мг/л взвешенных твердых частиц активного ила в окончательной смеси;
- количество растворенного органического углерода, обеспеченного инокулятом, которое должно быть менее чем 10% от начальной концентрации органического углерода, введенного испытуемым соединением;
- обычно от 1 мл до 10 мл инокулята, достаточный для 1000 см3 испытательного раствора.
7.2.2 Инокулят со станции аэрации сточных вод (с активным илом)
Отбирают пробу активного ила, собранного из аэротенка производственной или лабораторной станции водоочистки, которая обрабатывает преимущественно коммунально-бытовые сточные воды. Хорошо перемешивают и определяют концентрацию взвешенных твердых частиц активного ила (используя, например, ИСО 11923). При необходимости, ил концентрируют путем осаждения так, чтобы объем ила, добавленный к испытуемой пробе был минимален, но при этом выполнялся критерий (7.2.1.). Если есть подозрения, что ил содержит ингибирующее вещество, его центрифугируют, промывают средой (5.2), повторно центрифугируют и ресуспендируют в среду. Пробу хранят в аэробных условиях и используют предпочтительно в день сбора. Используют соответствующий объем (см. 7.2.1) для получения 30 мг/л взвешенных твердыхчастиц в окончательной смеси.
7.2.3 Инокулят из сточной воды
Берут пробу сточной воды до или после очистки с производственной или лабораторной станции, имеющей дело преимущественно с коммунально-бытовыми сточными водами. При необходимости концентрируют пробу путем фильтрации или центрифугирования. Хорошо перемешивают и хранят пробу в аэробных условиях и используют предпочтительно в день сбора. Перед использованием дают пробе осесть в течение 1 ч и отбирают соответствующий объем надосадочной жидкости для инокуляции.
5
7.2.4 Инокулят из поверхностной воды
Берут пробу соответствующей поверхностной воды. При необходимости концентрируют пробу фильтрацией или центрифугированием. Хранят пробу в аэробных условиях и используют предпочтительно в день сбора. Используют соответствующий объем как инокулят.
7.3 Испытание
Устанавливают закрытый респирометр (см. 6.1 и пример, описанный в приложении D). Собирают необходимое количество сосудов для испытания, чтобы иметь:
- не менее двух испытательных сосудов (обозначенных FT) для испытуемого соединения (7.1.1);
- не менее двух сосудов для контрольных проб (обозначенные FB), содержащих среду испытания и инокулят;
- не менее одного сосуда для проверки процедуры (обозначен Fc), содержащий контрольное соединение (7.1.2);
- при необходимости, один сосуд для проверки возможного ингибирующегодействия испытуемого соединения (обозначен F,), содержащий раствор (7.1.3);
- при необходимости, один сосуд для проверки возможной абиотической очистки (обозначен Fs), содержащий испытуемое соединение (7.1.1) без инокулята, стерилизованный добавлением соответствующего неорганического токсичного соединения для предотвращения микробной активности. К примеру, используют 1 мл/л раствора хлорида ртути (II) (5.4). Через две недели после начала испытания при необходимости добавляют такое же количество токсического вещества.
Добавляют соответствующее количество среды испытания (5.2), инокулят (7.2), испытуемое (7.1) и контрольное соединения (7.1.2) в нужных концентрациях в соответствующие испытательные сосуды в соответствии с таблицей 1 для получения заданного окончательного объема испытания. Добавляют абсорбент (5.3) в отделения поглощения С02 в сосудах. Измеряют значение pH содержимого сосудов и регулируют при необходимости до 7,4 растворами 5.5 или 5.6.
Помещают испытательные сосуды в водяную баню или в комнату с постоянной температурой (6.2), выдерживают их до нужной температуры (см. раздел 4), герметизируют сосуды и, в случае автоматического респирометра делают все необходимые соединения, и запускают мешалку. Считывают показания биохимической потребности кислорода (поглощение кислорода) на манометрах (при ручной работе) или проверяют правильность работы регистратора автоматического респирометра. Применяют метод, предлагаемый изготовителем для соответствующего типа респирометра.
Если достигнут почти постоянный уровень поглощения кислорода (фаза плато) и дальнейшего биологического разложения не ожидается, испытание считается законченным. Обычно максимальный период испытания не должен превышать 28 дней. Испытание продлевают на одну или две недели, если очевидно, что разложение началось, но не достигло фазы плато.
В последний день испытания измеряют pH.
Если DOC постоянно контролируется, отбирают пробы соответствующего размера из испытательных сосудов в начале (время 0) и в конце (время f) периода испытания. Альтернативно, определяют начальное значение (время 0) в отдельно приготовленном сосуде или рассчитывают его из добавленного испытуемого соединения. Л ибо фильтруют эти пробы через мембранный фильтр или центрифугируют при 4000 г в течение 15 мин (см. 6.5). Если измерения DOC не проводятся в тот же день, то пробы хранят до 48 ч при 4 °С в темноте, в полностью герметично закупоренных стеклянных сосудах.
Примечание — Удаление DOC может происходить в результате биологического разложения, а также при абиотических процессах, таких как абсорбция на инокуляте или на стенке сосуда, или, в случае летучих испытуемых соединений, при перемешивании и абсорбции на трубках. Если вопроссвязан со смесями, может происходить выборочная абсорбция разных компонентов.
Если первичное биологическое разложение постоянно контролируется, определяют концентрацию испытуемого соединения, применяя специальный анализ в сосудах FT и Fs в конце испытания (время f).
|
Таблица 1 — Окончательное распределение испытуемых и контрольных соединений в испытательных сосудах | ||||||||||
|
|
Окончание таблицы 1 | ||||||||||||||||||||||||||||||
|
Если испытуемое соединение содержит азот, определяют окончательную концентрацию нитратов и нитритов сразу же в конце испытания или же на соответственно законсервированных пробах. В качестве альтернативы используют методику качественной капельной пробы на нитрит и нитрат на малом объеме реакционной смеси, отобранной из каждого сосуда, и применяют количественный метод, только если получен положительный результат. Если нитрификация произошла, корректируют поглощение кислорода (см. приложение В).
8 Расчет и представление результатов
8.1 Расчет8.1.1 Удельная биохимическая потребность кислорода
Выражают значения поглощения кислорода для каждого сосуда, полученные по показаниям респирометра, как биохимическую потребность кислорода. Рассчитывают удельную биохимическую потребность кислорода BS по формуле (1). Корректируют поглощение кислорода в случае нитрификации (см. 7.3 и приложение В).
РТС
где Bs — удельная биохимическая потребность кислорода, выраженная в миллиграммах кислорода на грамм испытуемого соединения;
Bt— измеренная биохимическая потребность кислорода испытуемого соединения FT за время t, мг/л;
BBt — измеренная биохимическая потребность кислорода контрольной пробы FB за время t, мг/л; Рте — массовая концентрация испытуемого соединения, г/л.
8.1.2 Процентное биологическое разложение
Биологическое разложение определяется как отношение удельной биохимической потребности кислорода либо к теоретической потребности кислорода (ThOD) (пример расчета приведен в приложении А), либо кхимической потребности кислорода (COD). Процент разложения определяют для каждого испытательного сосуда, используя уравнение (2) и/или (3).
°ThOD “
Bs
ThOD
100,
(2)
D,
COD
- Bs
COD
100,
(3)
где DTh0D — процентное биологическое разложение ThOD за время f;
DCod — процентное биологическое разложение COD за вре мя /;
Bs — удельная биохимическая потребность кислорода испытуемого вещества, выраженная в миллиграммах на грамм испытуемого соединения;
ThOD — теоретическая потребность кислорода, выраженная в миллиграммах на грамм испытуемого соединения;
COD — химическая потребность кислорода, определенная экспериментально, выраженная в миллиграммах на грамм испытуемого соединения.
7
1
2