ГОСТ Р ИСО 7198-2013
Имплантаты для сердечно-сосудистой системы. Трубчатые сосудистые протезы
В стандарте установлены требования к проведению испытаний, упаковке, маркировке, а также определены термины, относящиеся к протезам кровеносных сосудов (ПКС), предназначенным для замещения, обведения или создания шунта между сегментами сосудистой системы человека.
Идентичен ISO 7198:1998
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Общие требования
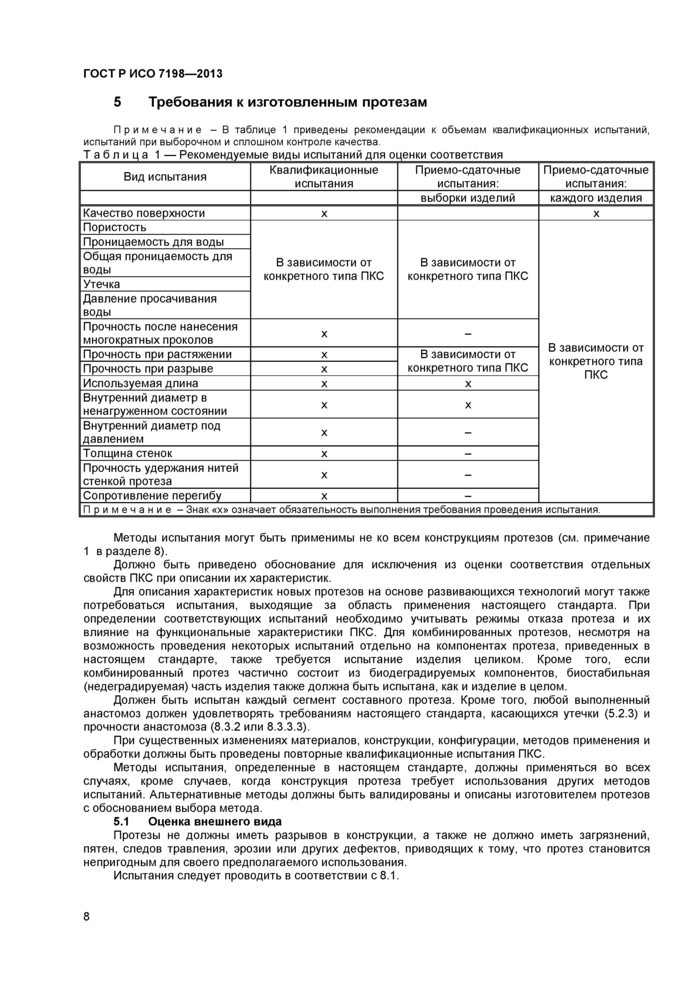
5 Требования к изготовленным протезам
6 Требования к in vivo доклинической и клинической оценкам
7 Отбор образцов
8 Методы испытания сосудистых протезов
9 In vivo доклинические и клинические методы испытания сосудистых протезов
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов национальным стандартам Российской Федерации
42 страницы
| Дата введения | 01.03.2015 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 08.11.2013 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 1490-ст |
|---|---|---|---|
| Разработан | ФГБУ НЦССХ им. А.Н. Бакулева РАМН | ||
| Издан | Стандартинформ | 2014 г. |
Cardiovascular implants. Tubular vascular prostheses
- ГОСТ Р ИСО 2960-99 Материалы текстильные. Определение прочности при продавливании и растяжения продавливанием методом диафрагмы
- ГОСТ Р ИСО 2859-1-2007 Статистические методы. Процедуры выборочного контроля по альтернативному признаку. Часть 1. Планы выборочного контроля последовательных партий на основе приемлемого уровня качества
ГОСТ Р ИСО 14155-1-2008Руководство по проведению клинических испытаний медицинских изделий. Часть 1. Общие требования. Заменен на ГОСТ Р ИСО 14155-2014.- ГОСТ Р ИСО 10993-1-2009 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10
стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18
стр. 19
стр. 20

стр. 21

стр. 22
стр. 23
стр. 24

стр. 25

стр. 26
стр. 27

стр. 28

стр. 29

стр. 30
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
(Щ)
ГОСТР ИСО 7198— 2013
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
Имплантаты для сердечно-сосудистой системы ТРУБЧАТЫЕ СОСУДИСТЫЕ ПРОТЕЗЫISO 7198:1998Cardiovascular implants — Tubular vascular prostheses(IDT)
Издание официальное
Cardiovascular implants — Tubular vascular prostheses(IDT)
Издание официальное
Издание официальное
ГОСТ РИСО 7198—2013
Предисловие
1 ПОДГОТОВЛЕН Федеральным государственным бюджетным учреждением «Научный Центр сердечно-сосудистой хирургии им. А Н. Бакулева» РАМН (ФГБУ «НЦССХ им. А Н. Бакулева» РАМН) на основе собственного аутентичного перевода на русский язык международного стандарта, указанного в пункте 4
2 ВНЕСЕН Управлением технического регулирования и стандартизации Федерального агентства по техническому регулированию и метрологии
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 08 ноября 2013 г № 1490-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 7198:1998 «Имплантаты для сердечно-сосудистой системы. Трубчатые сосудистые протезы» (ISO 7198:1998 «Cardiovascular implants — Tubular vascular prostheses»).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в ГОСТ Р 10-2012 (раздел 8) Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты в, а официальный текст изменений и поправок — в ежемесячном формационном указателе к Национальные стандарты» В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя шНациональные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (gost ni)
© Стандартинформ, 2014
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
II
ГОСТ РИСО 7198—2013
Содержание
1 Область применения.................................................................................................................1
2 Нормативные ссылки.................................................................................................................1
3 Термины и определения...........................................................................................................2
4 Общие требования....................................................................................................................4
5 Требования к изготовленным протезам..................................................................................8
6 Требования к in vivo доклинической и клинической оценке.................................................10
7 Отбор образцов.......................................................................................................................12
8 Методы испытания сосудистых протезов..............................................................................12
9 In vivo доклинические и клинические методы испытания сосудистых протезов...............32
Приложение ДА (справочное) Сведения о соответствии ссылочных
международных стандартов национальным стандартам
Российской Федерации.................................................................................37
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Имплантаты для сердечно-сосудистой системы ТРУБЧАТЫЕ СОСУДИСТЫЕ ПРОТЕЗЫ
Cardiovascular implants — Tubular vascular prostheses
Дата введения - 2015—03—01
1 Область применения
1.1 В настоящем стандарте установлены требования к проведению испытаний, упаковке, маркировке, а также определены термины, относящиеся к протезам кровеносных сосудов (ПКС). предназначенным для замещения, обведения или создания шунта между сегментами сосудистой системы человека.
Настоящий стандарт применим к ПКС, изготовленным из материалов биологического происхождения, синтетических тканей и синтетических нетекстильных материалов. Также приведено руководство по описанию составных и комбинированных протезов. Стандарт содержит требования к обозначению материалов и конструкции ПКС, а также к обозначению характерных и габаритных размеров ПКС. Стандарт также включает ссылки на требования к биосовместимости материалов и конструкций, изготовленных ПКС с учетом соответствующих частей ИСО 10993.
В настоящем стандарте также определены механические характеристики ПКС и установлены методы измерения и верификации размеров и механических характеристик, определенных изготовителем. Стандарт включает аспекты стерилизации ПКС и определяет требования к маркировке и упаковке.
1.2 В настоящем стандарте определены не все эксплуатационные характеристики и характерные размеры ПКС, но установлены достаточные методы верификации того, что номинальные значения, определенные изготовителем, находятся в допустимых пределах. Возможно, что данные методы должны быть дополнены другими методами при формировании программы испытаний для изделий конкретных типов.
Настоящий стандарт не применим к ПКС из тканей человека-донора, таким как ПКС с криоконсервацией. Также из области действия настоящего стандарта исключены сосудистые заплаты, тампоны и стенты.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие международные стандарты. Для датированных ссылок применяют только указанные издания. Для недатированных ссылок применяют самые последние издания (включая любые изменения и поправки).
ИСО 472:1998 Пластмассы. Словарь (ISO 472:1998. Plastics — Vocabulary)
ИСО 2076:1989 Ткани. Искусственные волокна. Родовые наименования (ISO 2076:1989, Textiles — Man-made fibres — Generic names)
ИСО 2859-1:1989 Процедуры отбора образцов для контроль по характеристикам. Часть 1. Схемы отбора образцов, для которых указан приемлемый уровень качества для последовательного контроля партий (ISO 2859-1:1989. Sampling procedures for inspection by attributes — Part 1: Sampling plans indexed by acceptable quality level (AQL) for lot-by-lot inspection)
ИСО 2859-2:1985 Процедуры отбора образцов для контроль по характеристикам. Часть 2. Схемы отбора образцов, для которых указан предельный уровень качества для контроля отдельных партий (ISO 2859-2:1985, Sampling procedures for inspection by attributes — Part 2: Sampling plans indexed by limiting quality (LQ) for isolated lot inspection)
ИСО 2960:1974 Ткани. Определение прочности на разрыв и растяжения при разрыве Диафрагмальный метод (ISO 2960:1974. Textiles — Determination of bursting strength and bursting distension — Diaphragm method)
Издание официальное
ИСО 5081:1977 Ткани. Тканые материалы. Определение предела прочности и удлинения (метод полос) ((ISO 5081:1977, Textiles — Woven fabrics — Determination of breaking strength and elongation (Strip method)]
ИСО 5084:1977 Ткани. Определение толщины тканых и трикотажных материалов (кроме тканых напольных покрытий) ((ISO 5084:1977, Textiles — Determination of thickness of woven and knitted fabrics (other than textile floor coverings)]
ИСО 10993-1:1997 Биологическая оценка медицинских изделий. Часть 1. Оценка и испытания (ISO 10993-1:1997, Biological evaluation of medical devices — Part 1: Evaluation and testing)
ИСО 14155:1996 Клиническая оценка медицинских изделий (ISO 14155:1996, Clinical investigation of medical devices)
ASTM D 76-93 Спецификации разрывных машин для тканей (ASTM D 76-93, Specification for tensile testing machines for textiles)
ASTM D 123-94 Терминология, касающаяся тканей (ASTM D 123-94, Terminology relating to textiles)
3 Термины и определения
В настоящем стандарте применены термины по ASTM D 76-93, ASTM D 123-94, а также следующие термины с соответствующими определениями:
3.1 аллотрансплантат: Имплантируемый материал, полученный из тканей животного того же
вида.
3.2 бифуркация: Место разделения единого сосудистого русла (торса или всего тела сосуда) на два ответвления (конечности).
3.3 биологический материал: Материал животного или растительного происхождения, который может быть изменен или обработан с помощью химических процессов, за исключением любых ископаемых материалов биологического происхождения (например, нефти).
3.4 биостабильность: Способность материала поддерживать свою физическую и химическую целостность после имплантации в живые ткани.
3.5 покрытие: Любой органический или неорганический материал, кроме живых клеток, специально наносимый изготовителем на основу протеза.
Примечание - Такое покрытие может быть предусмотрено как постоянное или как временное, оно может быть нанесено на внешние и/или внутренние поверхности и/или быть введено в структуру основы
3.6 податливость: Способность протеза упруго расширяться и сжиматься по окружности в ответ на пупьсирующее изменение давпения.
3.7 компонент: Материал, используемый во время производства, независимо от того, должен ли он остаться как соответствующий элемент изделия.
3.8 составной протез: Сосудистый протез, конструкция и/или материалы конструкции которого меняются от сегмента к сегменту на протяжении длины протеза (сравните 3.9).
Пример - Протез, проксимальная часть которого выполнена из трикотажного полотна с витыми нитями, а дистальная часть из кровеносного сосуда животного, обработанного альдегидом.
3.9 комбинированный протез: Однородный по длине сосудистый протез, стенки которого выполнены из нескольких материалов (сравните 3.8).
3.10 конфигурация: Геометрическая форма, конфигурация протеза
Пример - Прямой, бифуркационный, конический.
3.11 конструкция: Тип основы протеза.
Пример - Трикотажный, тканый, нетканый, из пористого полимера.
3.12 гофрирование: Создание на протезе складок или изгибов для обеспечения возможности удлинения и снижения вероятности перегиба.
3.13 волокно: Нить материала, выходящая из одного или более узла и заканчивающаяся в одном или более узле.
2
ГОСТ РИСО 7198—2013
3.14 реципиент: Лицо, которому имплантируется протез.
3.15 состояние готовности к имплантации: Состояние протеза, который перед имплантацией был подготовлен в соответствии с инструкциями изготовителя, а также состояние материала протеза, который был подвергнут соответствующим процессам стерилизации и/или иной подготовки.
Примечание - Подготовка не включает процедуры предварительной коагуляции (см 320). но включает любые рекомендованные методы промывки или вымачивания
3.16 общая проницаемость для воды: Объем чистой фильтрованной жидкости (с вязкостью, соответствующей вязкости воды), который проходит через стенки протеза за определенное время при определенном давлении.
3.17 утечка: Объем чистой фильтрованной жидкости (с вязкостью, соответствующей вязкости воды), который проходит через зазоры водонепроницаемого сосудистого протеза за определенный промежуток времени при определенном давлении.
Примечание - Утечка может происходить либо через мелкие дефекты стенок непрерывной трубки, либо через анастомоз, предусмотренный изготовителем
3.18 узел: Твердая область на материале, с которой начинаются и в которой собираются волокна.
3.19 пористость: Значение отношения объема пустот в материале к общему объему, занимаемому материалом, включая пустоты.
Примечание 1 - Пористость может быть выражена как процентное отношение объема пустот к общему объему материала на данной площади, как среднее расстояние между узлами, или как средний диаметр поры
Примечание 2 - Пористость - не то же самое, что утечка (см 3.17) или проницаемость для воды (см 3 34).
3.20 предварительная пропитка кровью: Процедура, в ходе которой осуществляется прохождение крови через стенки протеза и свертывание крови или отдельных ее фракций в порах протеза для снижения проницаемости стенки.
3.21 первичный компонент: Вещество, включенное в изготовленный протез, добавление которого предусмотрено изготовителем для улучшения характеристик ПКС.
3.22 протез: Любое изделие, заменяющее или замещающее анатомическую структуру или дефект в ней.
3.23 остаточный материал: Вещество, которое используется при изготовлении протеза, но для которого предусмотрено удаление или наличие которого не требуется в изготовленном протезе.
3.24 вторичный компонент: Вещество, которое может быть включено в изготовленный протез, но которое не определяет основные функциональные характеристики ПКС.
3.25 основа протеза: Сосудистый протез, на который наносится покрытие, соответствующее определению 3.5.
3 26 синтетический материал: Вещество небиологического происхождения, которое
изготовляется и/или полимеризуется с помощью химических или физических средств.
Примечание - Химически измененные материалы, полученные из ископаемых биологического происхождения, например, из нефти, считаются синтетическими
3.27 синтетический не текстильный протез: Сосудистый протез, изготовленный с
использованием не текстильных материалов.
Пример - Протезы, изготовленные из экструдированного полимера, пористого полимера.
3.28 синтетический текстильный протез: Сосудистый протез, изготовленный из синтетических нитей с применением технологий текстильного производства.
Пример - Протезы, изготовленные с помощью вязания, тканья, плетения синтетических нитей.
3.29 используемая длина: Длина протеза, готового к имплантации, измеренная при определенной фиксированной нагрузке.
Примечание - Для некоторых протезов нагрузка может быть нулевой
3.30 сосудистый протез, сосудистый графт: Протез, используемый для замены, обхождения или создания шунта между сегментами сосудистой системы.
3.31 велюр: Ткань с отрезным или петлевым ворсом или с ворсованной поверхностью.
3.32 пустоты: Часть стенки или сосудистого протеза, не занятая материалом конструкции (сравните 3.19).
3
Примечание - Это нечто иное, нежели пустоты в вязанной или тканой структуре
3.33 давление просачивания воды: Давление, под которым вода проникает со стороны внутренней стенки на внешнюю стенку сосудистого протеза.
3.34 проницаемость для воды, пористость для воды: Объем чистой фильтрованной воды, проходящей за определенный период времени через единицу площади материала протеза под определенным давлением.
Примечание 1- Проницаемость для воды обычно определяется как мл смг мин1 при приложении давления 16 кПа (120 мм рт ст).
Примечание 2 - Проницаемость для воды это не то же самое, что и пористость (см 3 19).
3.35 сенотрансплантат, гетеротрансплантат: Имплантируемый материал, выполненный из тканей животного вида, отличного от реципиента.
4 Общие требования
Следующие требования применимы ко всем сосудистым протезам, независимо от вида материала.
4.1 Обозначение конфигурации и размеров
Конфигурация сосудистых протезов должна определяться его геометрической структурой, например, прямой, бифуркационный или конический.
Примечание - Некоторые протезы могут быть изготовлены для специального применения, например, бифуркационный аорто-бедренный протез Такие протезы следует обозначать с указанием их предполагаемого клинического использования, а не просто как «бифуркационные»
4.1.1 Прямые сосудистые протезы постоянного сечения
Размеры прямых сосудистых протезов постоянного сечения должны определяться следующими характеристиками:
a) номинальный внутренний диаметр изделия в ненагруженном состоянии, выраженный в миллиметрах;
b) номинальный внутренний диаметр ПКС под давлением, выраженный в миллиметрах, при внутреннем давлении по крайней мере 16 кПа (120 мм рт. ст.), если данный диаметр изменяется под давлением более чем на 10 % (см. 5 6);
c) минимальная используемая длина, выраженная в сантиметрах.
4.1.2 Бифуркационные сосудистые протезы постоянного сечения
Размеры бифуркационных сосудистых протезов постоянного сечения должны определяться значением номинального внутреннего диаметра изделия в ненагруженном состоянии и минимальной используемой общей длиной основной трубчатой части протеза и ее ответвлений, выраженных в сантиметрах При необходимости должен быть также указан внутренний диаметр изделия под давлением (см. 4.1.1, перечисление Ь)].
4.1.3 Конические сосудистые протезы
Размер конических сосудистых протезов должны определяться номинальными внутренними диаметрами его концов в ненагруженном состоянии и минимальной используемой длиной, выраженными в сантиметрах. При необходимости должен быть также указан номинальный внутренний диаметр изделия под давлением [см 4.1.1, перечисление Ь)).
4.1.4 Другие конфигурации
Для других конфигураций должны быть указаны основная длина (длины), номинальный внутренний диаметр(ы) в ненагруженном состоянии, номинальный внутренний диаметр(ы) под давлением, выраженные, при необходимости в миллиметрах или сантиметрах.
4.2 Указание предполагаемого клинического применения
Предполагаемое клиническое применение должно быть сформулировано с указанием одного или нескольких пунктов из следующих перечислений:
a) для грудного отдела аорты и/или торакально-абдоминальный;
b) для абдоминального отдела аорты и/или подвздошной артерии, и/или бедренной артерии;
c) для периферических артерий, включая дополнительные к анатомическим (например, подвздошно-бедренная артерия);
d) для коронарных артерий;
e) для артериовенозного шунтирования для сосудистого доступа;
О прочие сосуды.
ГОСТ РИСО 7198—2013
4.3 Материалы и конструкция
4.3.1 Классификация
Протезы классифицируют путем отнесения к одной из следующих групп:
a) тканый синтетический (например, трикотажный, тканый);
b) нетканый синтетический (например, полученный из экструдированного полимера, пористого полимера);
c) биологический (например, аллотрансплантат, ксенотрансплантат);
d) составной;
e) комбинированный.
4.3.2 Номенклатура
4.3.2.1 Синтетические материалы
Описание синтетических материалов должно включать следующее:
a) родовое или химическое наименование в соответствии с ИСО 472 или ИСО 2076;
b) природу их химической обработки или модификации.
4.3.2.2 Биологические материалы
Описание биологических материалов должно включать в себя следующую информацию:
a) происхождение материала, т.е. род животного-донора:
b) тип и место расположения ткани (например, пупочная вена; сонная артерия) или тип материала (например, коллаген, альбумин);
c) общий тип химической обработки или химической модификации материала;
d) специальные характеристики любых биологических материалов (например, степень образования поперечных связей - «сшивки»).
4.3.2.3 Покрытия
Для покрытий должны быть определены их объем, стойкость и однородность.
Описание покрытий должно включать в себя следующую информацию, если применимо:
a) номенклатуру любых синтетических компонентов в соответствии с 4.3.2.1;
b) номенклатуру любых биологических компонентов в соответствии с 4.3.2.2.
4.3.2.4Жидкости для хранения
Описание жидкости для хранения должно включать в себя следующую информацию:
a) родовое или химическое наименование основных компонентов;
b) природу и тип возможных токсических воздействий.
4.3.2.50статочные химические вещества
Примечание - Остаточными химическими веществами считаются те жидкости для обработки или хранения протезов или их производные, которые могут быть выделены с протеза в состоянии его готовности к имплантации (см 3 15)
Описание остаточных химических веществ должно включать их специальные химические наименования, если это возможно; в противном случае следует использовать их общее химическое наименование.
4.4 Биосовместимость и биостабильность
4.4.1 Биосовместимость
Материалы, из которых изготовлены протезы, должны быть оценены на биосовместимость в состоянии готовности протеза к имплантации либо отдельно, либо как часть изготовленного протеза в соответствии с принципами и методами, рекомендованными в ИСО 10993-1.
При изменении материалов иУили основных методов обработки следует проводить повторную оценку ПКС на биосовместимость.
4.4.2 Биостабильность
Если конструкция протеза и его предполагаемое использование в качестве постоянного имплантата требуют, чтобы протез поддерживал некоторый минимальный уровень физической и химической целостности после имплантации в живые ткани в течение определенного периода времени, материалы, из которых выполнен протез, должны быть испытаны на биостабильность или отдельно, либо в составе изготовленного протеза.
Обоснование методов испытания и полученных значений биостабильности может включать.
a) оценку долговечности материалов, используемых в настоящее время при данных показаниях:
b) продолжительность ожидаемого времени работы протеза при данных показаниях к использованию с учетом функциональных и клинических характеристик других протезов и других видов лечения, доступных в настоящее время для использования при данных показаниях.
В некоторых случаях эти вопросы должны быть рассмотрены при анализе соотношения риска и пользы применения изделия.
5
4.5 Стерильность
Протезы следует поставлять в стерильном виде.
Примечание - При валидации процессов стерилизации необходимо принимать во внимание риски, обусловленные переносом патогенов протезами, изготовленными из тканей животных, включая человека
4.6 Общая информация и инструкция по применению
Каждый индивидуальный контейнер или общая упаковка, содержимое которых однородно, должны сопровождаться инструкцией по применению протеза. Инструкция по применению должна включать следующее:
a) показания к применению;
b) противопоказания, предупреждения и предостережения по применению;
c) рекомендуемые методы асептической обработки и подготовки протеза к имплантации, включая любые виды предварительной обработки, такие как предварительную промывку, предварительную коагуляцию и/или методы имплантации, если применимо;
d) выделенное утверждение «СТЕРИЛЬНО. НЕ СТЕРИЛИЗОВАТЬ ПОВТОРНО. ТОЛЬКО ДЛЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ», если применимо;
e) информацию по повторной стерилизации, если применимо;
0 предупреждение о наличии консервантов и/или вымываемых компонентов, если применимо;
д) рекомендации по хранению, если применимо;
h) дату публикации или номер редакции инструкции, отражающей изменения.
4.7 Упаковка
4.7.1 Индивидуальная упаковка
Каждый протез должен быть упакован в индивидуальную упаковку. Индивидуальная упаковка должна быть сконструирована таким образом, чтобы было четко видно, была ли упаковка когда-либо ранее вскрыта.
Индивидуальная упаковка должна быть сконструирована таким образом, чтобы обеспечивать сохранение стерильности протеза при нормальных условиях обращения, транспортирования и хранения и обеспечивать извлечение содержимого асептическим путем.
4.7.2 Внешняя упаковка
Каждая индивидуальная упаковка должна быть уложена во внешнюю упаковку, которая должна обеспечивать защиту внутренней упаковки от повреждений при хранении.
4.7.3 Транспортная упаковка
Каждая внешняя упаковка или несколько внешних упаковок, необязательно одного типа, могут быть упакованы в транспортную упаковку для защиты содержимого от повреждений при нормальных условиях обращения, транспортирования и хранения.
4.8 Маркировка
4.8.1 Этикетка упаковки
Каждый протез должен сопровождаться этикеткой (этикетками) на соответствующей упаковке (упаковках). На этикетке (этикетках) должна быть приведена, по меньшей мере, следующая информация:
a) наименование, адрес и/или торговое наименование изготовителя;
b) материал конструкции и тип конструкции (см. 4.3);
c) конфигурация (см. 4 1). Вместо письменного описания протеза может быть использован
символ (например. | = прямой. ^ = бифуркационный. |- = подвздошно-бедренный протез):
d) номинальная используемая длина (см. 5 4);
е) номинальный внутренний диаметр(ы) в ненагруженном состоянии (см. 5.5);
0 если применимо, номинальный внутренний диаметр(ы) под давлением (см. 5.6);
д) если применимо, пористость, средняя проницаемость для воды, общая проницаемость для воды/утечки и/или давление просачивания воды (см. 5.2);
h) выделенное утверждение «СТЕРИЛЬНО. НЕ СТЕРИЛИЗОВАТЬ ПОВТОРНО. ТОЛЬКО ДЛЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ» или эквивалентные фразы или символы, если применимо (см. 4.5);
О номер партии или серии в системе изготовителя;
j) номер партии стерилизации;
Примечание - Если номер партии или серии в системе изготовителя, [перечисление i)J, и номер партии стерилизации, [перечисление j)J, указывают на одну и ту же информацию, допускается указывать только один номер
к) дату стерилизации со сроком хранения или срок годности;
ГОСТ РИСО 7198—2013
О предостережение от использования устройства при вскрытой или поврежденной упаковке; т) рекомендации изготовителя по хранению, если применимо;
п) химические свойства всех жидкостей для хранения в индивидуальной упаковке с соответствующими предупреждениями об опасности;
о) если применимо, выделенное утверждение, касающееся требований или ограничений по предварительной коагуляции.
4.8.2 Стикеры для истории болезни пациента
Каждая упаковка протеза должна содержать, по меньшей мере, три этикетки-стикера для вклеивания в историю болезни пациента, получившего имплантат. Стикер должен включать следующую информацию:
a) наименование и адрес изготовителя;
b) наименование продукта;
c) номер партии в системе изготовителя и серийный номер стерилизации [см. примечание к 4 8.3. перечисление])];
d) референтный номер модели протеза (номер по каталогу изготовителя);
4.9 Отчеты об испытаниях
Примечание - Для некоторых испытаний отчет не требуется
4.9.1 Общие положения
В отчете об испытаниях должна быть приведена, по меньшей мере, следующая информация:
a) наименование изготовителя или дистрибьютора;
b) место и дата проведения испытаний;
c) номер партии и/или серийный номер;
d) спецификации изготовителя и/или дистрибьютора;
e) результаты испытаний;
f) утверждение о соответствии или несоответствии методам испытаний, определенным в соответствующих разделах настоящего стандарта.
4.9.2 Дополнительная информация
В дополнение к отчету об испытаниях в протокол следует внести следующую информацию:
a) материал(ы) изготовления в соответствии с 4.3;
b) конфигурацию и тип конструкции протеза;
c) размеры протеза в соответствии с 4.1,4.1.2, 4.1.3, 4.1.4;
d) утверждение, указывающее на то. был ли каждый образец протеза стерилизован или нет. и. если применимо, использованный метод стерилизации;
e) метод(ы) испытания в соответствии с содержанием разделов настоящего стандарта;
0 условия, включая средние значения и допуски для контролируемых сред, в которых выдерживался и/или испытывался протез;
д) число образцов и результаты для каждого образца; h) минимальные и максимальные зарегистрированные значения.
7