ГОСТ Р ИСО 11134-2000
Стерилизация медицинской продукции. Требования к валидации и текущему контролю. Промышленная стерилизация влажным теплом
Устанавливает требования к стерилизации влажным теплом, валидации и контролю процесса стерилизации. Стандарт распространяется на все процессы, использующие влажное тепло, включая насыщенный пар и паровоздушную смесь, и может использоваться во всех промышленных производствах, а также при изготовлении установок для стерилизации влажным теплом.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Определения
4 Общие положения
5 Оборудование
6 Разработка процесса стерилизации
7 Валидация процесса стерилизации
8 Текущая стерилизация влажным теплом
Приложение А Руководство по валидации и текущему контролю промышленной стерилизации влажным теплом
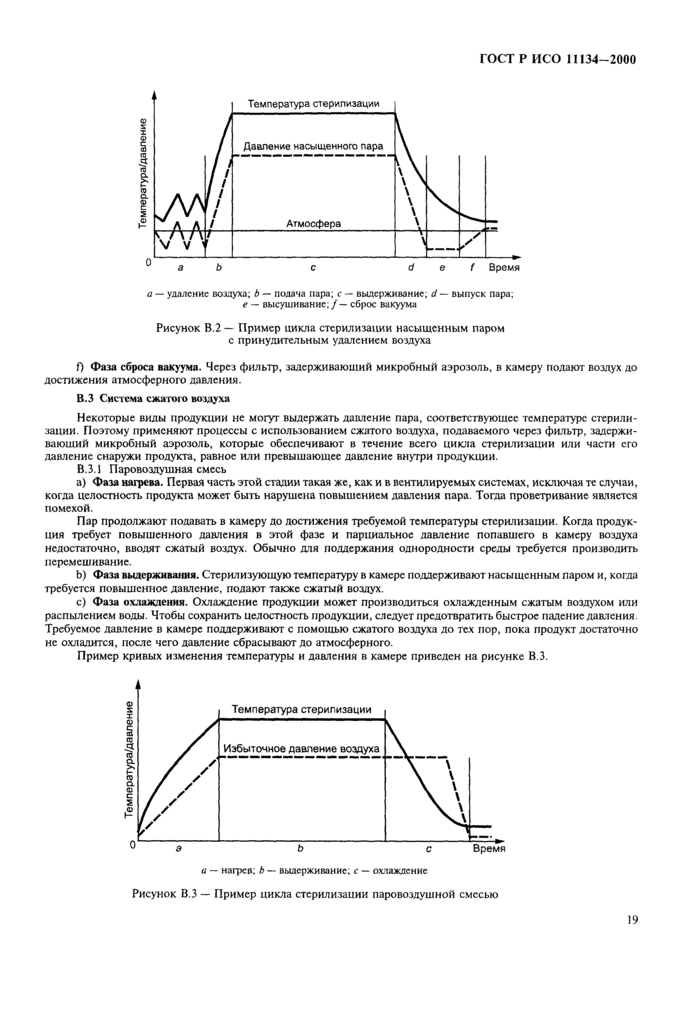
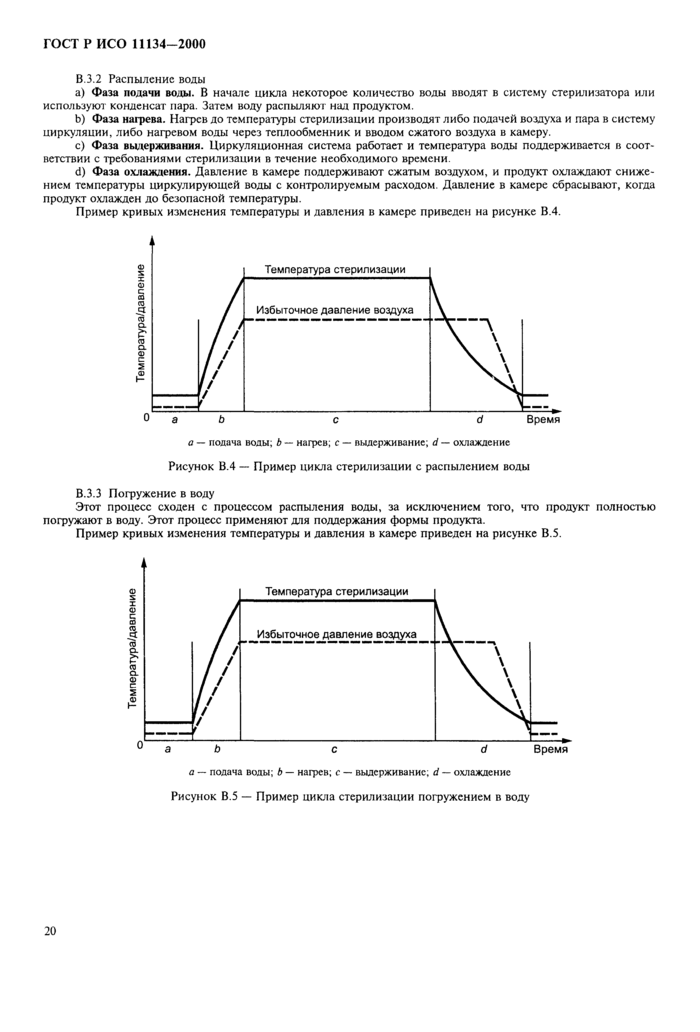
Приложение В Циклы стерилизации
Приложение С Библиография
27 страниц
| Дата введения | 01.01.2002 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.03.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 14.09.2000 | Утвержден | Госстандарт России | 224-ст |
|---|---|---|---|
| Разработан | Московская медицинская академия им. И.М. Сеченова | ||
| Разработан | АСИНКОМ | ||
| Издан | ИПК Издательство стандартов | 2001 г. |
Sterilization of health care products. Requirements for validation and routine control. Industrial moist heat sterilization
- ГОСТ Р ИСО 9001-96 Системы качества. Модель обеспечения качества при проектировании, разработке, производстве, монтаже и обслуживании
- ГОСТ Р ИСО 9002-96 Системы качества. Модель обеспечения качества при производстве, монтаже и обслуживании
- ГОСТ Р ИСО 9003-96 Системы качества. Модель обеспечения качества при окончательном контроле и испытаниях
- ГОСТ Р 51350-99 Безопасность электрических контрольно-измерительных приборов и лабораторного оборудования. Часть 1. Общие требования
- ГОСТ Р МЭК 61010-2-041-99 Безопасность электрических контрольно- измерительных приборов и лабораторного оборудования. Часть 2-041. Частные требования к лабораторным автоклавам, в том числе использующим пар для обработки медицинских материалов
- ГОСТ Р ИСО 11138-1-2000 Стерилизация медицинской продукции. Биологические индикаторы. Часть 1. Общие требования
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22
стр. 23
стр. 24

стр. 25

стр. 26

стр. 27
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Стерилизация медицинской продукции
ТРЕБОВАНИЯ К ВАЛИДАЦИИ И ТЕКУЩЕМУ КОНТРОЛЮ
Промышленная стерилизация влажным теплом
Издание официальное
БЗ 12-99/644
ГОССТАНДАРТ РОССИИ Москва
Предисловие
1 ПОДГОТОВЛЕН Ассоциацией инженеров по контролю микрозагрязнений (АСИНКОМ) и Московской медицинской академией им. И.М. Сеченова
ВНЕСЕН Техническим комитетом по стандартизации ТК 383 «Стерилизация медицинской продукции» Госстандарта России
2 ПРИНЯТ И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Госстандарта России от 14 сентября 2000 г. № 224-ст
3 Настоящий стандарт содержит аутентичный текст международного стандарта ИСО 11134—94 «Стерилизация медицинской продукции. Требования к валидации и текущему контролю. Промышленная стерилизация влажным теплом»
4 ВВЕДЕН ВПЕРВЫЕ
© ИПК Издательство стандартов, 2001
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта России
II
включать назначение ответственного лица для определения необходимости и объема повторяемых этапов первичной валидации.
При изменениях в оборудовании или системе контроля следует проводить оценку соответствия параметров процесса, которому подвергается загруженный продукт, данным первоначальной аттестации.
8 Текущая стерилизация влажным теплом8.1 Контроль процесса паровой стерилизации
8.1.1 Точность и надежность приборов, используемых для контроля каждого производственного цикла, должны периодически проверяться в соответствии с документацией на них.
8.1.2 Следует иметь документированные инструкции текущего контроля.
8.1.3 При каждом цикле должны составляться протоколы, содержащие:
a) дату;
b) название стерилизатора и заводской номер;
c) обозначение цикла;
d) фамилию и подпись оператора;
e) время начала цикла (реальное время);
f) давление в камере в течение данного цикла;
g) температуру в камере в течение данного цикла;
h) продолжительность поддержания критических параметров процесса;
i) описание загрузки и номер серии.
8.2 Контроль изменений
Система документирования должна гарантировать, что в оборудовании, процессе или материалах отсутствуют какие-либо изменения, способные ухудшить процесс стерилизации. Если такие изменения проводятся в плановом порядке, то новый цикл стерилизации должен быть валидирован. При нарушениях процесса, которые не могут быть отнесены на счет несоблюдения документации на процесс, следует рассмотреть необходимость повторной аттестации.
8.3 Периодическая проверка
Стерилизаторы следует подвергать плановой периодической проверке.
8.4 Микробиологические испытания
Если эффективность процесса основана на изучении или оценке бионагрузки на продукт, то:
a) метод определения или оценки бионагрузки должен быть валидирован и документирован;
b) должны быть предусмотрены средства, гарантирующие, что величина бионагрузки не выходит за установленные пределы;
c) должна быть приведена в действие непрерывная программа мониторинга бионагрузки с предписанной частотой и должным образом документированная.
8.5 Выгрузка стерилизованного продукта
При выгрузке продукта нужно, чтобы параметры процесса при мониторинге во время текущей стерилизации находились внутри валидированных пределов. Должна быть предусмотрена система разделения стерилизованных и нестерилизованных образцов. Только уполномоченное лицо имеет право выгрузить продукт после стерилизации.
8.6 Проверка операций
Контроль качества продукции и процесса производства и все протоколы должны рассматриваться в соответствии с требованиями ГОСТ Р ИСО 9001 не реже одного раза в 12 мес. Ответственные лица, прямо не участвующие в этих процедурах, должны гарантировать, что производственные инструкции, введенные при аттестации, действуют и выполняются.
8.7 Корректирующие действия
Процедуры и документация для корректирующих действий должны соответствовать требованиям ГОСТ Р ИСО 9001. Любые отклонения от документации и инструкций, обнаруженные во время эксплуатации, проверок, калибровки и обслуживания, должны быть рассмотрены лицом, уполномоченным определять необходимые действия и меры по устранению отклонений.
Любые принятые корректирующие действия должны быть документированы.
8.8 Протоколы
Протоколы, фиксирующие, что продукт стерилизован в соответствии со спецификациями, должны оформляться по ГОСТ Р ИСО 9001.
7
ПРИЛОЖЕНИЕ А (справочное)
Руководство по валидации и текущему контролю промышленной стерилизации влажным теплом
Примечание — Это приложение обеспечивает выполнение требований соответствующих пунктов настоящего стандарта.
А. 1 Область применения
Не рассматривается
А. 2 Нормативные ссылки
Не рассматривается
А.З Определения
Не рассматривается
А.4 Общие положения
А.4.1 Ответственность и обучение персонала
Не рассматривается
А.4.2 Требования к продукту
А.4.2Л Создание продукта
При использовании влажного тепла для стерилизации к продукту предъявляются следующие требования:
a) способность выдерживать действие влаги и относительно больших значений температуры и давления, а также скорости их изменения;
b) облегчение контакта между стерилизующим агентом и всеми поверхностями, подлежащими стерилизации;
c) сохранение стерильности (в тех частях, которые должны быть стерильными) при правильном хранении.
Эти пункты должны соблюдаться при создании продукта. Простые изменения в составе продукции,
которые не приводят к изменению характеристик продукта, могут создавать трудности при стерилизации и валидации.
Не допускается вносить никаких изменений в продукт до тех пор, пока не будут учтены упомянутые выше факторы, и, если необходимо, проведена валидация.
А.4.2.2 Выбор материалов
Важным критерием при выборе материалов является их способность противостоять воздействию физических нагрузок, сопровождающих процесс стерилизации влажным теплом. Для некоторых материалов существенно, чтобы они были легко проницаемы для воздуха и пара. Следует разработать и выполнять инструкции, чтобы обеспечить соответствие качества материалов, используемых в производстве, качеству материалов, которые использовались при проведении валидации. Если улучшение одного качества приводит к ухудшению другого, то любое изменение качества может потребовать ревалидации.
А.4.3 Требования к упаковке
Требования, предъявляемые к созданию продукта (А.4.2.1) и выбору материалов (А.4.2.2), относятся и к упаковке. Таким образом, чтобы обеспечить должное транспортирование и обращение со стерильным материалом, упаковка должна быть рассчитана на обеспечение требований длительного хранения. Продукт и его упаковка должны выдерживать скорость изменения температуры и давления во время цикла стерилизации.
Эта упаковка должна состоять не менее чем из двух слоев, которые должны включать:
a) первичную упаковку, в которую помещается продукт; под первичной упаковкой может пониматься и сам продукт, у которого стерильна только внутренняя поверхность (например, внутренняя поверхность трубки);
Примечания
1 Гарнитура и запорные устройства должны обеспечивать стерильность продукта внутри упаковки. Они должны быть разработаны и валидированы по тем же стандартам, что и материал первичной упаковки.
2 Чтобы свести к минимуму загрязнение продукта частицами и микроорганизмами после удаления наружного слоя, первичная упаковка может состоять более чем из одного слоя.
b) вторичную упаковку, содержащую одну или более первичных упаковок, которые должны обеспечивать защиту продукта при хранении и перемещении внутри предприятия у пользователя;
c) транспортную тару, защищающую продукцию и вторичную упаковку при транспортировании вне предприятия.
Для стерильной продукции общая конструкция упаковки должна обеспечивать функции первичной упаковки, вторичной упаковки и транспортной тары так, как это описано выше. Для жидких стерильных продуктов в тубах упаковка должна выполнять, по крайней мере, функции вторичной упаковки и транспортной
ГОСТ Р ИСО 11134-2000
тары. Таким образом, конструкция всех упаковок должна обеспечивать их прочность, чтобы защищать продукт во время перемещения и транспортирования.
Во время стерилизации продукт должен быть, по крайней мере, в первичной упаковке. Стерилизация продукта во вторичной упаковке или транспортной таре обычно не применяется.
Требования к процессу стерилизации упаковки противоречат общим требованиям надлежащей защиты продукта. Компромисс может быть достигнут путем выбора упаковочного материала или обеспечения равномерности упаковки перед стерилизацией и во время ее.
При заключении контракта на стерилизацию должно быть предусмотрено использование временных второго и третьего слоев упаковки на время транспортирования перед стерилизацией.
А. 5 Оборудование
А. 5.1 Документация
А.5.1.1 Данные об оборудовании
Не рассматривается
А.5.1.2 Безопасность
Для предупреждения пользователя о потенциальной опасности, связанной с эксплуатацией оборудования, должны быть письменные инструкции.
Оборудование, включая сосуды под давлением, должно соответствовать требованиям ГОСТ Р 51350 и ГОСТ Р МЭК 61010-2-041 и дополнительно, где необходимо, национальным правилам безопасности, действующим в стране пользователя.
Должна быть предусмотрена защита от случайного включения системы, пока двери камеры не будут закрыты, герметизированы и заперты. Стерилизатор должен быть снабжен средствами, предотвращающими разгерметизацию дверей камеры, находящейся под давлением. Если нет признаков отклонения от нормальной работы, то двери стерилизатора должны разгерметизироваться, отпираться и открываться только по окончании цикла стерилизации. Стерилизатор также должен быть снабжен средствами, обеспечивающими возвращение камеры к атмосферному давлению и открытие загрузочной(ых) двери(ей), если имеет место неисправность в процессе автоматического цикла.
Если загрузка, выгрузка или обслуживание требуют входа в камеру, должны быть предусмотрены меры, предусматривающие открывание закрытых дверей, при этом ключ должен быть вынут и взят оператором перед входом в камеру, или должны быть приняты меры аварийного выключения изнутри камеры.
А. 5 Л. 3 Руководства и инструкции
Покупателю должна быть предоставлена инструкция по подготовке к монтажу, проведению монтажа, эксплуатации стерилизующей системы, а также проведению технического обслуживания.
А.5.1.3.1 Инструкции по монтажу должны включать:
a) общие размеры и массу стерилизующей системы;
b) тип электроснабжения, напряжение, частоту и мощность;
c) скорость потока и давление пара, воды и подаваемого сжатого воздуха;
d) уровень звукового давления.
А.5.1.3.2 Инструкции по безопасной и эффективной эксплуатации стерилизующей системы должны включать:
a) область применения, тип загрузки, род упаковки;
b) производительность;
c) описание возможных циклов стерилизации;
d) описание контролируемых приборов и индикаторов;
e) описание устройств безопасности;
f) инструкции по безопасности;
g) инструкции на случай неисправности.
А.5Л.З.З Инструкции по техническому обслуживанию и ремонту должны включать:
a) состав работ по обслуживанию;
b) рекомендуемую периодичность или графики обслуживания;
c) электрические диаграммы и схемы;
d) гидравлические планы и схемы;
e) перечень запчастей;
f) инструкции по технике безопасности.
А.5.1.3.4 Должны быть предусмотрены, документированы и валидированы методы, средства и программное обеспечение, необходимые для эксплуатации и обслуживания системы контроля оборудования. Валидация может быть независимой или проведенной изготовителем программного обеспечения с соблюдением требований соответствующих стандартов серии ГОСТ Р ИСО 9000.
А.5.1.4 Монтаж
После монтажа стерилизатора в месте его эксплуатации должна быть проведена серия проверок и испытаний. Изготовитель, поставщик и покупатель должны прийти к соглашению по поводу назначения ответственного лица за проведение таких проверок и испытаний.
9
А.5.2 Эксплуатационные характеристики стерилизатора, технологические среды и источники энергии, материалы, принадлежности и средства контроля
А.5.2.1 Эксплуатационные характеристики
Эксплуатационные характеристики стерилизатора должны быть проверены в соответствии с программой испытаний, учитывающей необходимые национальные правила и стандарты.
А.5.2.2 Технологические среды и источники энергии
А.5.2.2.1 Пар
Стерилизатор должен быть предназначен для работы с насыщенным паром или предварительно подготовленной паровоздушной смесью. При использовании пара сухость его должна быть не менее 95 %, а объемная доля неконденсированных газов не более 3,5 %. Перегрев не должен превышать 5 °С. Гарантия непрерывного контроля качества пара достигается контролем конденсата, который не должен содержать контаминантов в количестве, которое может ухудшить процесс стерилизации, повредить стерилизатор или нарушить целостность продукта. Флуктуации давления пара перед редуктором не должны превышать 10 % и коэффициент редукции не должен быть более 2:1.
А.5.2.2.2 Воздух
А.5.2.2.2.1 Стерилизатор должен быть предназначен для работы со сжатым воздухом, свободным от капельной влаги, профильтрованным до 5 мкм и содержащим не более 0,5 мг/м3 масла в нормальном воздухе. Сжатый воздух должен проходить через микробиологический фильтр, находящийся в точке потребления. Фильтр должен задерживать частицы размером более 0,3 мкм с эффективностью не менее 99,5 %.
А.5.2.2.2.2 Для стерилизаторов, которые требуют подачи воздуха в камеру непосредственно из атмосферы, воздух должен проходить очистку через фильтр с эффективностью не менее 99,5 % по частицам размером более 0,3 мкм.
А.5.2.2.2.3 Герметичная продукция не требует микробиологической фильтрации подаваемого в камеру воздуха. В случае применения проницаемой упаковки может произойти проникновение микроорганизмов при вакуумировании, нагреве и наличии влаги, которое при нормальных условиях не наблюдается. Герметичная упаковка также может стать проницаемой, если имеет место выделение компонентов, вызванное проникновением тепла и/или внутренним вакуумом, причиной которого является охлаждение воздуха внутри продукта.
А.5.2.2.3 Вода
Вода для образования пара и вода для прямого охлаждения не должна содержать загрязнений (контаминантов) в концентрациях, способных ухудшить условия процесса стерилизации, нанести вред стерилизатору или стерилизуемому продукту (таблица А.1). Вода для вакуумных систем должна быть кипяченой, подаваться при температуре не более 15 °С, жесткость ее должна быть менее или равна 0,2 ммоль/дм3.
|
Таблица АЛ — Типовые пределы концентрации загрязнений в паре и/или воде, контактирующих с продукцией и/или ее упаковкой | ||||||||||||||||||||||||||
|
А.5.2.2.4 Электроснабжение
Стерилизатор должен быть предназначен для работы при напряжении, равном ±10 % номинального питающего напряжения. Стерилизатор должен быть рассчитан на работу от системы электропитания, обеспеченной одновременной изоляцией всех фаз от главного кабеля, при этом каждая фаза должна иметь отдельный предохранитель.
А.5.2.3 Материалы
Используемые материалы должны выдерживать воздействие пара и конденсата, не должны приводить к снижению качества пара и выделять какие-либо вещества в количествах, опасных для здоровья.
ГОСТ Р ИСО 11134-2000
Соединения трубопроводов и фитинги должны обеспечивать плотность при высоком давлении и вакууме. Рабочие трубопроводы пара и воды при температуре выше 70 °С должны иметь теплоизоляцию. Трубопроводы холодной воды должны быть изолированы. Проект системы трубопроводов должен предусматривать возможность дренажа и стерилизации.
Линии трубопроводов не должны напрямую соединяться с канализацией, чтобы избежать обратного тока жидкости. Теплообменники должны исключать попадание внешней жидкости в систему циркуляции.
Соединения должны предусматривать соответствующее размещение датчиков температуры, чтобы определять распределение температуры и теплопередачу в продукте. Стерилизаторы с вакуумным режимом должны быть снабжены кабелями, соединенными с камерой, для присоединения испытательных приборов.
А.5.2.4 Принадлежности
Не рассматривается.
А.5.2.5 Система контроля и регистрации
Цикл стерилизации должен контролироваться с помощью автоматической программы, которая основана на проведении одного или более предварительных циклов стерилизации. Должны быть приняты меры предосторожности при установке ступенчатых параметров предварительных циклов стерилизации. Вход в контрольное устройство должен быть ограничен с помощью специального ключа, кода или инструмента.
При обслуживании, испытаниях и в любых неотложных случаях должны быть предусмотрены средства, позволяющие переходить к ручному управлению. Во время ручного управления любые устройства безопасности не должны прекращать свою работу.
Регистрирующее устройство может быть аналоговым или цифровым и должно обеспечивать непрерывную запись значений величин параметров процесса во время цикла стерилизации. Фактическая скорость изменения температуры и давления может превышать значение, показываемое приборами контроля.
А.5.2.6 Контролирующие программы
Изготовитель стерилизатора отвечает за качество программного обеспечения. По праву собственника изготовитель стерилизатора может решить не раскрывать перечень источников программного обеспечения. В этом случае изготовитель обязан предоставить пользователю утвержденный протокол валидации, который включает в себя указание на то, по каким показателям и стандартам проведена валидация.
Работа электромеханических или других средств контроля должна быть также валидирована.
А.5.3 Приборы контроля
А.5.3.1 Точность приборов
А.5.3.1.1 Контрольное устройство температуры должно быть:
a) цифровым или аналоговым;
b) с точностью ±1 % в диапазоне шкалы от 50 до 150 °С;
c) отрегулировано с точностью (±0,5 °С) от величины температуры стерилизации;
d) с защищенным от разрушения датчиком;
e) приспособлено для использования ключа, кода или инструмента без разборки прибора.
A.5.3.L2 Устройство контроля давления должно быть:
a) цифровым или аналоговым;
b) с точностью ±1,6 % или лучше в диапазоне шкалы от 0 до 5 бар;
c) с защищенным от разрушения датчиком;
d) приспособлено для использования ключа, кода или инструмента без разборки прибора.
А.5.3.1.3 Таймер должен иметь точность не менее ±1 % или лучше для периодов времени более 5 мин и не менее ±2,5 % — для периодов времени до 5 мин.
По возможности следует вычислять систематическую ошибку, которая должна корректироваться с использованием соответствующих поправочных коэффициентов.
А.5.3.2 Калибровочные эталоны
Не рассматривается
А.5.3.3 Эталонные приборы для стерилизатора
Эталонные приборы для стерилизатора должны обеспечивать выявление дрейфа приборов контроля или изменений в процессе работы. Обе измерительные системы должны иметь одни и те же калибровочные программы. Качество исполнения эталонных приборов должно быть эквивалентным или превосходить качество контролирующих систем.
Максимальное допустимое отклонение между двумя измерительными системами должно быть установлено при проектировании системы, изменении процесса или на этапе квалификации оборудования. Измерительная система подлежит повторной калибровке, если различия между двумя измерениями превосходят указанные пределы.
А.5.3.4 Калибровочные программы
Чтобы гарантировать точное и значимое измерение, калибровочная программа должна быть документирована. Калибровочная программа должна иметь ссылку на требования стандартов, письменные калибровочные процедуры и указания на точность приборов.
Приборы должны быть калиброваны в соответствии с инструкциями изготовителя, и калибровка должна проводиться в пределах 2 °С от величины температуры стерилизации.
11
Организация, обеспечивающая калибровку, должна быть проверена на наличие компетентного персонала, способного проводить калибровку с требуемой степенью точности. Необходимо письменное документирование проводимых работ.
А. 5.4 Техническое обслуживание
График технического обслуживания должен быть построен на основе данных, предоставленных изготовителями стерилизатора, приборов и оборудования, исходя из общих задач и проверок, выполняемых на предприятии, и на основе опыта эксплуатации. График обслуживания и периодичность проведения работ должны быть основаны на рекомендациях изготовителя и специалиста, имеющего опыт обслуживания. Кроме того, следует учесть задачи эксплуатации, обеспечения безопасности и эффективности работы.
На каждую работу по обслуживанию должна быть составлена инструкция на основе документации изготовителя.
Специально назначенный работник должен подписывать и датировать все записи, относящиеся к выполнению как плановых, так и внеплановых работ, и отмечать, что все необходимые работы и проверки проведены удовлетворительно и в полном объеме. При выявлении отклонений следует установить причину этих отклонений и устранить ее.
Проверка документации о проведении технического обслуживания проводится с целью установить:
a) возникшие дефекты;
b) изменения, предусмотренные графиком обслуживания;
c) изменения, вызванные любыми работами по обслуживанию;
d) необходимость в дополнительном обучении обслуживающего персонала;
e) правильность оформления документации о проведенном обслуживании, включая наличие даты и подписи.
А. 6 Разработка процесса стерилизации
Примечание — См. также приложение В.
А.6.1 .Выбор типа цикла стерилизации зависит от конфигурации продукции и способности продукта и упаковки выдерживать воздействие температуры и давления, а также общей тепловой нагрузки.
А.6.1.1 Стерилизация медицинской продукции влажным теплом может оказаться сложным процессом из-за возможной неоднородности типов продукции, упаковки и конфигурации загружаемых сосудов. Факторы, которые могут оказать влияние на стерилизацию медицинской продукции влажным теплом, приведены в таблице А.2.
|
Таблица А.2 — Факторы, которые могут влиять на устройства или компоненты или повредить их при стерилизации влажным теплом | ||||||||||||
|
В продукции, содержащей много элементов, могут быть труднодоступные для пара места, в которых эффект стерилизации не будет достигнут. В этом случае может потребоваться стерилизация сухим теплом и соответствующая разработка цикла стерилизации (например, с использованием индикаторных микроорганизмов).
А.6.1.2 Анализ разрабатываемого цикла может быть проведен в исследовательском сосуде, если показана эквивалентность его с сосудом, в котором находится продукт.
Процессы стерилизации влажным теплом могут быть разработаны для наиболее узкого диапазона температур в стерилизационной камере. Процессы стерилизации с использованием насыщенного пара и предварительного вакуумирования являются более легкими для контроля, тогда как, например, цикл с применением паровоздушной смеси или воды под давлением может иметь более широкий диапазон температур. Процесс валидации заключается в проведении последовательности повторяющихся циклов, и может служить надежной основой для демонстрации адекватности желаемого контроля. В течение всего времени обработки температура в камере не должна:
а) отличаться более чем на 3 °С от температуры стерилизации, являющейся минимально допустимым пределом;
12
ГОСТ Р ИСО 11134-2000
b) колебаться более чем в пределах ±1 °С;
c) отличаться одна от другой более чем на ±2 °С (в разных точках).
Во время стерилизации устройства или компонента влажным теплом образец должен выдерживать стрессовые воздействия температуры, давления и, возможно, процесса эвакуации. Если упакованные устройства стерилизуются влажным теплом, то нужно предусмотреть соответствующее высушивание упаковочного материала после стерилизации, чтобы сохранить стерилизующие барьерные свойства.
А.6.1.3 Наиболее легкий с точки зрения контроля и валидации процесс стерилизации влажным теплом
— процесс с использованием насыщенного пара с механическим удалением воздуха. Такой процесс включает единственный компонент, единственную фазу процесса, которые исключительно просто контролировать. Две наиболее важные характеристики этого процесса — это способность удалять воздух из плотных пористых предметов и поддерживать условия насыщенного пара. Избыточная влажность может быть следствием загрузки влажных пористых предметов, повреждения упаковки или загрязнения.
Создание атмосферы насыщенного пара продувкой воздухом или использование гравитационного перемещения воздуха не гарантирует, что в атмосфере будет только один элемент — пар. Для пористых материалов большое значение имеет удаление воздуха. Способ загрузки камеры стерилизатора является критическим для обеспечения удаления воздуха из упаковки и создания адекватного потока пара для перемещения воздуха. В последнем случае, например, требуется достаточное количество вертикальных каналов в схеме загрузки продуктов. Для таких циклов может потребоваться дополнительная валидация или установка температурных датчиков с высокой плотностью размещения в объеме камеры.
А.6.1.4 Стерилизация влажным теплом герметичных контейнеров с жидкостями и газами может лотре-бовать внешнего давления, большего, чем при простом нагреве. Если содержащаяся в контейнере жидкость является водой (или раствором со сходными физическими свойствами), то давление пара, создаваемого в фазах подогрева и выдержки, не должно превышать давление теплоносителя. Однако дополнительное давление создается нагревом паровой среды (например, воздуха) и испарением жидкости, которая повышает давление пара. Обычно это достигается добавлением внешнего давления сверх величины, требуемой для обеспечения фаз подогрева и выдержки. Это компенсирует внутреннее давление, определяемое внутренней температурой и давлением пара, большими, чем охлаждаемая среда.
Добавление воздуха к пару может применяться для получения требуемого повышения давления. Эти системы однако очень трудно запустить и валидировать. Чтобы обеспечить необходимое перемешивание пара и воздуха в камере необходимо предусмотреть установку принудительного смешения. Важно, чтобы схема загрузки обеспечивала эффективную циркуляцию пара между упаковками.
А.6.1.5 Может применяться распыление воды под давлением. Это снимает проблему смешения воздуха и пара, но проблемы адекватного распределения и течения теплоносителя остаются. В этом случае часто прибегают к высокому расходу воды для ограничения теплопередачи к продукту' и предотвращения значитель-ного повышения температуры сверху донизу и дефицита поступления тепла. Большой объем используемой воды требует соответствующей обработки как микробиологической (например, контроль пирогенов), так и химической, чтобы предотвратить появление существенных отложений на упаковке.
А.6.2 Скорость микробиологической деструкции при стерилизации влажным теплом зависит от температуры пара, давления пара во время стерилизации, проницаемости материала упаковки для пара и воздуха, доступности путей для прохождения пара и воздуха в устройствах и компонентах или физиологического статуса бионагрузки, связанной с продуктом.
А.6.2.1 Математические и графические методы, разработанные с учетом летальности (часто выражаемой через физический критерий /), могут использоваться на основе данных о температуре продукции. Расчет величины Fна основе физических параметров процесса приведен в [2]—[4]. Определения величин F, FQ, Ви z приводятся в разделе 3. Чтобы выбрать величину F, нужно знать величины D и z.
Чем больше величина D, тем больше устойчивость микроорганизма к термической деструкции. Величина Сможет отклоняться от кривой логарифма числа выживших микроорганизмов в течение времени стерилизации; время десятикратного снижения числа микроорганизмов может быть измерено потом непосредственно.
При вычислении F0 для определения цикла летальности используют температуру 121,1 °С и величину z~
— 10 °С. Данные о температуре продукта в течение всего процесса (нагревание, выдержка, охлаждение) преобразовывают для вычисления эквивалентной летальности при температуре 121,1 °С, математически или графически интегрируют для получения физической летальности, выражаемой в минутах, эквивалентной выдержке при температуре 121,1 °С. Например, если z = 10 °С, летальность за 1 мин при температуре 114 °С эквивалентна летальности за 0,2 мин при температуре 121,1 °С. Некоторые программы позволяют рассчитывать величину F всего процесса стерилизации непрерывно, используя данные от одного или более датчиков температуры, размещенных в продукте. Описание специальных методов приведено в [3] и др.
Для расчета величины F, используемой при разработке наилучшего цикла стерилизации, должны быть проведены предварительные исследования по выбору мест расположения датчиков контроля температуры. Эти исследования должны включать изучение распределения температуры в загруженном стерилизаторе для нахождения слабо прогреваемых мест внутри зон стерилизации камеры, определения воспроизводимости и обнаружения мест с наименьшей температурой в зоне стерилизации во время процесса. Эти исследования должны показать, что датчики температуры находятся в низкотемпературной зоне продукта, или для выбранного места расположения датчика температуры должно быть дано документированное обоснование. Если размер
13
упаковки, контейнера или наполняемый объем малы, то нужно обратить внимание на возможные эффекты теплопередачи вдоль зонда и внутри продукта или на необходимость введения зонда на нужную глубину, чтобы минимизировать ошибки теплопередачи от пара. Для минимизации этого эффекта нагрева можно использовать малогабаритный проволочный датчик.
Для точного расчета величины / требуется калибровка системы измерения температуры. До начала расчета цикла летальности поправочные коэффициенты должны быть определены по индивидуальным показаниям приборов. Расчет величины Г основан на допущении, что резистентные штаммы в бионагрузке имеют величину Z, примерно равную 10 °С, и определяется кинетикой отмирания первого порядка при наличии атмосферы насыщенного пара.
Следует определить соотношение между расчетной величиной F\ полученной на основе измерения физических параметров, и экспериментальной величиной F, полученной подсчетом выживших микроорганизмов в продукте/стерилизующей среде (величины D и z).
Данные по летальности, полученные при использовании физических моделей, должны увязываться с результатами соответствующих микробиологических экспериментов.
А.6.2.2 Данные о температуре, полученные при проведении повторностей, используются для получения параметра, соответствующего наименьшему летальному эффекту (например, при минимальных значениях времени и температуры). Другие факторы, которые могут отрицательно влиять на рассчитанный процесс гибели и отклоняющиеся во время проведения исследования, включают начальную температуру продукта, температуру камеры/рубашки, продолжительность нагрева и охлаждения и конфигурацию загрузки. Перечень таких факторов может быть продолжен.
А.6.3 Между изделиями и упаковками, подлежащими стерилизации, существует много общего. Например, между многими изделиями могут быть лишь незначительные различия по длине туб или наличию принадлежностей, которые не влияют на приспособленность продуктов к стерилизации. К тому же многие упаковки могут состоять из одного и того же материала, слегка отличаясь лишь размерами. Общий подход заключается в классификации продуктов и упаковок по их сходству и затем в оценке того, какие условия в этих классах приводят к наибольшим проблемам. Группы продуктов и упаковок могут быть использованы при совершенствовании процессов стерилизации и решении микробиологических проблем, сертификации или валидации стерилизаторов, в разработке других методов оценки качества или тестирования продуктов. Документация о результатах исследований и разумном обосновании расположения зондов должна обосновать отнесение наиболее трудно стерилизуемых продуктов и упаковок к своим группам. Различные методы могут применяться для валидации процессов стерилизации упаковок хирургических изделий и инструментов, компонентов, товаров, растворов, других продуктов, контейнеров и закрытых сосудов. Поэтому могут потребоваться различные инструкции по стерилизации влажным теплом этих различных продуктов.
Для разработки и эффективного использования процессов стерилизации паром могут быть использованы два подхода: метод избыточного воздействия и метод бионагрузки.
А.6.3.1 Метод избыточного воздействия традиционно используют для разработки промышленного режима паровой стерилизации. Подход базируется на предпосылке, что процесс стерилизации должен быть рассчитан на инактивацию высокой концентрации микроорганизмов, которая не обязательно соответствует бионагрузке перед стерилизацией. Этот метод называется методом избыточного воздействия потому, что условия цикла стерилизации, рассчитанные на уничтожение микроорганизмов с учетом дополнительного коэффициента безопасности, должны быть значительно более строгими, чем это требуется для инактивации бионагрузки продукции.
Следует иметь в виду, что величина D расчетной микробиологической концентрации и микробной бионагрузки продукта может различаться в различных средах (растворах), и в разных местах, таких как контейнеры. Поэтому исходное число или расчетную концентрацию микроорганизмов выбирают на основе устойчивости популяции спор в реальных условиях стерилизации.
При использовании метода избыточного воздействия необходимо принимать во внимание возможную термическую деградацию продукта и упаковки или контейнера. Результатом избыточного термического воздействия могут быть усиленная химическая деградация, увеличение образования частиц и ограниченный срок хранения продукта.
Изготовитель должен получить данные для типовой бионагрузки, соответствующей загружаемому продукту. Эти данные не должны превышать тех значений, которые наиболее часто получаются при использовании метода бионагрузки.
А.6.3.2 Метод бионагрузки включает два подхода: абсолютный метод бионагрузки и комбинированный метод биологического индикатора/бионагрузки.
Метод абсолютной бионагрузки включает скрининг продукта на наличие термоустойчивых микроорганизмов, например, используя изолят из бионагрузки (полученный для контроля процесса стерилизации продукта), который является представителем наиболее устойчивых микроорганизмов популяции. Изолят может быть размножен, инокулирован на/или в продукт и использован в исследованиях оценки процесса стерилизации для прямой демонстрации желаемой вероятности выживаемости бионагрузки продукта. Типовую бионагрузку, используемую в расчетах, принимают равной средней бионагрузке плюс утроенное стандартное отклонение.
При микробиологической оценке стерилизации продукта комбинированным методом «биологический индикатор/бионагрузка» может потребоваться проведение инактивации начальной концентрации до установ-
14
ГОСТ Р ИСО 11134-2000
ленного логарифмического уровня Относительная устойчивость и популяция используемого контрольного микроорганизма должна сравниваться со средним числом и термоустойчивостью микроорганизмов — типичных представителей бионагрузки продукта Сравнение должно показать, что предварительно определенный уровень микробиологических имитаторов дает уверенность в том, что желаемый уровень вероятности выживания бионагрузки достигнут Этот метод основан на бионагрузке Следовательно, вычисление бионагрузки и определение устойчивости должны проводиться так же, как при абсолютном методе бионагрузки
А 6 4 Стерилизованная продукция не должна храниться в помещениях с большими перепадами влажности, давления и температуры
А 6 5 Эффект стерилизации влажным теплом выражается вероятностной функцией тепловой энергии, времени, влажности, числа микроорганизмов, находящихся в продукте (бионагрузки) и термоустойчивости этих микроорганизмов
А 6 6 Для демонстрации устойчивости к воздействию влажного тепла с учетом бионагрузки используют следующие виды споровых микроорганизмов Clostridium sporogenes, Bacillus coagulans, В subtihs и В stearother-mophilus
Необходимо принимать в расчет такие факторы, как захват микроорганизмов продукцией, контакт продукции с загрязненными жидкостями во время производства и/или использование материалов, которые могут поддерживать рост микроорганизмов
Количество выявленных сохранившихся после обработки теплом жизнеспособных спор может колебаться в зависимости от времени между обработкой и культивированием от условий культивирования Следовательно, такие условия должны тщательно контролироваться и документироваться
Метод избыточного воздействия основан на том, что процесс стерилизации приводит к инактивации биологических индикаторов с учетом дополнительного коэффициента безопасности Биологический индикатор состоит из определенного числа (например, между 103 и 106) устойчивых к влажному теплу спор Популяция индикатора необязательно должна соответствовать бионагрузке Если продукт требует условий сухого тепла, то следует также использовать такие микроорганизмы как В subtihs 5230 или В subtihs var mger (АТСС 9372) Условия стерилизации для инактивации биологического индикатора методом избыточного воздействия более строгие, чем те, которые требуются для гибели бионагрузки
Характеристики температуры и влажности многих систем могут отличаться от тех, которые имеют место в растворе Результирующая скорость инактивации микроорганизмов может отставать В некоторых случаях достижение эффекта инактивации биологического индикатора, соответствующего величине 12Д требует избыточного термического воздействия
Устойчивость биологического индикатора может быть определена с помощью фракционирования времени воздействия с оценкой степени летальности как функции предложенных параметров процесса Степень летальности может быть измерена проращиванием и подсчетом выживших микроорганизмов с целью построения кривой скорости отмирания или применением анализа конечной точки, когда используются методы тестов стерильности В последнем случае время воздействия выбирают таким образом, что самые короткие экспозиции дают рост всех проб, самые продолжительные экспозиции не дают роста, а промежуточные экспозиции дают рост в некоторых пробах
А 6 7 Биологические индикаторы широко используют для оценки летальности различных комбинаций параметров процесса, продуктов и упаковок Системы биологических индикаторов с известной устойчивостью прямо измеряют фактическую летальность в определенных местах продукта как результат использования переменных параметров
Индикаторные микроорганизмы, используемые в производстве, как правило, более устойчивы к стерилизации, чем типовая бионагрузка Разработка цикла стерилизации должна включать демонстрацию этой устойчивости Могут также применяться следующие методы изоляция, проращивание и оценка устойчивости выявленных микроорганизмов бионагрузки или выдержка продукта с типовой бионагрузкой в коротких циклах обработки с контролем стерильности продукта
Число и устойчивость изолятов могут быть использованы для расчета летального эффекта процесса применительно к бионагрузке Однако проращивание микроорганизмов бионагрузки может изменить их устойчивость Если используются короткие циклы выдерживания, то они должны быть выбраны так, чтобы позволить провести экстраполяцию результатов
А 6 8 Метод абсолютной бионагрузки требует постоянного учета продукции и реализации программы отслеживания устойчивости Достаточные данные о бионагрузке должны быть получены путем использования ранее полученных зарегистрированных данных Частота оценки бионагрузки зависит от качества и разброса ранее полученных данных, вида стерилизуемых продуктов, процесса производства и типа процесса стерилизации При измерении производственной среды должен быть предусмотрен дополнительный контроль бионагрузки
Устойчивость бионагрузки может быть определена выдержкой проб продукта, содержащего бионагрузку, в последовательно увеличивающихся циклах установленного режима стерилизации и затем в передаче стерильных тестов для определения числа выживших микроорганизмов или положительных проб, относящихся к различным по длительности экспозициям [3], [5] Альтернативным методом определения устойчивости микроорганизмов бионагрузки может служить их изоляция и проращивание, последующая инокуляция на продукт или соответствующий носитель, однако проращивание может изменить устойчивость бионагрузки Также
15
следует определить устойчивость других микробиологических индикаторных систем, которые могут быть использованы для текущего биологического контроля.
Для режима стерилизации, основанного на оценке бионагрузки, и определения числа и видов связанных с продуктом микроорганизмов, требуется часто проводить скрининг бионагрузки. Во время производства продукции следует брать репрезентативные пробы от каждой производственной установки. Программа контроля бионагрузки должна быть предназначена для оценки всевозможных изменений в компонентах продуктов и их производстве, производственной среде или производственном процессе, которые могут оказывать значительное влияние на бионагрузку.
А. 7 Валидация процесса стерилизации
Валидация процесса стерилизации влажным теплом является валидацией стерилизатора, продукта и концепции загрузки. Действия по валидации включают в себя:
a) проверку конструкции стерилизатора на соответствие требованиям к процессу стерилизации;
b) определение фактической эффективности и воспроизводимости цикла с учетом вида продукта и концепции загрузки;
c) оценку возможных изменений продукта, которые могут произойти в процессе стерилизации.
Если какие-либо изменения, даже направленные на улучшение, будут произведены в продукте, упаковке, системе загрузки, цикле стерилизации или стерилизаторе, то результаты первичной валидации должны считаться недействительными до тех пор, пока не будет произведена оценка влияния этих изменений на эффективность стерилизации.
Работа по валидации может быть значительной по объему, так как для демонстрации воспроизводимости процесса необходимо большое число точек и проведение повторных измерений. Объем работы можно уменьшить, установив более строгие допуски для физических параметров (следовательно, обеспечив однородность их внутри камеры и загрузки). Данные по летальному эффекту, полученные в другом стерилизаторе (например, в исследовательском аппарате) при тех же режимах стерилизации, должны быть распространены на промышленный сосуд, подвергшийся валидации.
Принцип надежной и уверенной валидации требует проведения изменений только после оценки последствий, к которым они могут привести. Если нет системы тщательного документирования любого фактора, то изменения могут остаться незамеченными и ревалидация не будет проведена.
Ответственное лицо (7.3) должно показать свою компетенцию в вопросах валидации и стерилизации.
А.8 Текущая стерилизация влажным теплом
А.8.1 Контроль процесса паровой стерилизации
После завершения исследований и проведения валидации изготовитель должен выбрать необходимую контрольную аппаратуру, оборудование и технологические приемы для обеспечения стерильности продукции и эффективности процесса.
До начала эксплуатации стерилизатора лица, ответственные за стерилизацию, должны удостовериться, что все оборудование и приборы для обслуживания и калибровки полностью укомплектованы, и в протоколах проведения аттестации содержатся сведения о видах загружаемых объектов, подлежащих стерилизации.
Планы текущего контроля должны включать испытания, проверки и периодичность их проведения, необходимые для того, чтобы обеспечить поддержание параметров цикла стерилизации, установленных во время аттестации, или других параметров, соответствующих этим значениям.
В некоторых обстоятельствах целесообразно в дополнение к текущему контролю использовать специальные дополнительные методы контроля процесса, такие как прямое измерение температуры продукции.
А.8.2 Контроль изменений
Система контроля изменений предназначена для определения необходимости проведения аттестации в оснащенном состоянии или в эксплуатации. Рекомендуется проводить повторную аттестацию, если произведены существенные изменения в системе стерилизации (основном оборудовании или программном обеспечении), продукте или упаковке, которые могут повлиять на эффективность процесса стерилизации. Ниже приводятся примеры (необязательно всеобъемлющие) изменений, которые могут потребовать повторной аттестации, если отсутствуют данные, подтверждающие правильность хода процесса:
a) допустимые колебания характеристик продукции — значительные изменения в материале продукции или проектные допуски, которые могут влиять на скорость нагрева продукции;
b) условия проветривания продукции — значительные изменения в барьерной функции, которую выполняет проветривание стерильным воздухом (например, от вентилируемых к невентилируемым контейнерам или от одного типа фильтра с разными величинами эффективности к другому);
c) конструкция (характеристика) продукта — значительные изменения состава продукции, включая композицию материалов или их плотность (где требуется обеспечить проникание тепла), которые могут повлиять на эффективность процесса стерилизации;
d) упаковка — изменения, которые могут повлиять на эффективность микробиологического барьера, существенные изменения в конструкции упаковки (например, переход от жесткого контейнера к эластичному мешочку), или замена поставщика, которая может значительно повлиять на физические свойства и проникание пара;
ГОСТ Р ИСО 11134-2000
Содержание
1 Область применения........................................................ 1
2 Нормативные ссылки....................................................... 1
3 Определения.............................................................. 1
4 Общие положения.......................................................... 3
5 Оборудование............................................................. 3
6 Разработка процесса стерилизации............................................. 5
7 Валидация процесса стерилизации............................................. 6
8 Текущая стерилизация влажным теплом......................................... 7
Приложение А Руководство по валидации и текущему контролю промышленной стерилизации
влажным теплом................................................ 8
Приложение В Циклы стерилизации.............................................18
Приложение С Библиография..................................................21
III
ГОСТ Р ИСО 11134-2000
e) оборудование — изменения, которые могут повлиять на способность поддерживать установленные эксплуатационные параметры или привести к произвольному изменению скорости проникания пара в продукцию;
f) процесс — изменения в процессе, которые могут привести к существенному изменению способа поддержания и регулирования параметров процесса (например, изменения в программном обеспечении системы контроля процесса);
g) загрузка продукции или плотность загрузки — изменения предварительно валидированной конфигурации загрузки, которые могут влиять на передачу тепла и влаги в загрузке;
h) теплоноситель — изменения соотношения «пар—воздух» в паровоздушном процессе.
А.8.3 Периодические испытания
Чтобы избежать нерегистрируемых и случайных изменений, следует проводить периодическую аттестацию (полностью или частично) в оснащенном состоянии и в эксплуатации. Интервал между периодическими аттестациями должен определяться по характеристикам процесса стерилизации и текущим документированным данным процесса. Интервал может варьироваться в зависимости от полученных ранее данных, которые демонстрируют воспроизводимость процесса и его соответствие параметрам, установленным документацией.
А.8.4 Микробиологические испытания
Следует заранее определить факторы (сезонные и производственные), которые могут повлиять на колебание видов, количество и устойчивость микроорганизмов к воздействию процесса стерилизации. Если режим стерилизации выбран на основе метода избыточного воздействия, то отсутствует необходимость часто собирать большое число данных.
Если режимы стерилизации выбраны на основе оценки бионагрузки, то биологические индикаторы следует выбирать и использовать с учетом предварительно проведенного микробиологического тестирования во время разработки цикла стерилизации и проведения валидационных исследований. Для текущего мониторинга должны использоваться те же виды микроорганизмов, что и в предварительных исследованиях, или они должны соответствовать им по устойчивости к воздействию влажного тепла. Это позволит установить зависимость между микробиологической инактивацией в текущем процессе стерилизации и данными, используемыми для разработки и контроля цикла стерилизации. Для текущего контроля обычно требуется меньшее число индикаторов, чем для аттестации в эксплуатации.
А.8.5 Выгрузка стерильной продукции
Решение о выгрузке продукта должно приниматься на основе оценки всех доступных данных, включая данные, полученные во время стерилизации при критических параметрах процесса. Кроме того, для продукции, подлежащей стерилизации в окончательной упаковке, некоторые контрольные органы могут потребовать проведения тестирования готовой продукции или тестирования с помощью биологических индикаторов.
Изменение цвета: Чтобы отличить обработанные и необработанные объекты друг от друга, могут использоваться химические индикаторы. Наряду с этим могут использоваться физическое разделение или организационные меры (этикетирование).
А. 8.6 Аудит операций
Не рассматривается.
А.8.7 Корректирующие действия
Не рассматриваются.
А.8.8 Регистрация
Чтобы обеспечить поддержание эксплуатационных параметров в пределах, установленных при валидации, результаты профилактического обслуживания и калибровки приборов следует документировать с достаточной детализацией.
17
Введение
Производство безопасной и стерильной медицинской продукции предъявляет высокие требования к методам стерилизации и контроля. Настоящий стандарт содержит основные элементы правил стерилизации медицинских препаратов влажным теплом в производстве.
Стерильный препарат — это препарат, который не содержит живых микроорганизмов. Даже производимые в контролируемых условиях препараты перед стерилизацией могут содержать микроорганизмы. Такие препараты по определению являются нестерильными. Цель процесса стерилизации — разрушение микробиологических контаминантов (загрязнений), находящихся в нестерильных продуктах.
Деструкция микроорганизмов физическими и химическими методами подчиняется экспоненциальному закону. Следовательно, можно рассчитать конечную вероятность выживания микроорганизмов независимо от стерилизующей дозы или способа обработки.
Вероятность выживания является функцией числа и типа (штамма) микроорганизмов, находящихся в продукте, процесса гибели при стерилизации и, в отдельных случаях, окружающей среды, в которой находятся микроорганизмы в период обработки.
Из этого следует, что стерильность конкретного объекта в общем числе стерилизуемых объектов в абсолютном смысле не может быть гарантирована. Вероятность нестерильное™ каждой индивидуальной единицы продукта подтверждается математически. Например, вероятность 10~6 означает, что в среднем из миллиона единиц продукции одна или менее одной единицы может оказаться нестерильной.
Требования к системам качества при проектировании (разработке), производстве, снабжении, монтаже и обслуживании даны в стандартах серии ИСО 9000.
Международные стандарты серии ИСО 9000 определяют некоторые процессы как «специальные», если результат не может быть полностью проверен последующим контролем и испытанием продукции. Стерилизация является примером специального процесса, поскольку ее эффективность не может быть проверена контролем продукта. Поэтому процесс стерилизации должен быть валидирован до практического применения и подлежит текущему контролю, а оборудование — необходимому обслуживанию.
IV
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
Стерилизация медицинской продукции
ТРЕБОВАНИЯ К ВАЛИДАЦИИ И ТЕКУЩЕМУ КОНТРОЛЮ
Промышленная стерилизация влажным теплом
Sterilization of health саге products.
Requirements for validation and routine control.
Industrial moist heat sterilization
Дата введения 2002—01—01
1 Область применения
Настоящий стандарт устанавливает требования к стерилизации влажным теплом, валидации и контролю процесса стерилизации.
Стандарт распространяется на все процессы, использующие влажное тепло, включая насыщенный пар и паровоздушную смесь, и может использоваться во всех промышленных производствах, а также при изготовлении установок для стерилизации влажным теплом. В настоящем стандарте не рассматриваются непромышленные установки стерилизации влажным теплом, но изложенные принципы могут быть полезны для тех, кто применяет стерилизацию влажным теплом в таких установках.
В настоящем стандарте не рассматриваются системы обеспечения качества, которые необходимы для контроля на всех стадиях производства.
Примечание — Основные требования настоящего стандарта могут применяться при стерилизации фармацевтической продукции, но для нее могут потребоваться другие технические и руководящие указания.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты:
ГОСТ Р ИСО 9001-96 Системы качества. Модель обеспечения качества при проектировании, разработке, производстве, монтаже и обслуживании
ГОСТ Р ИСО 9002-96 Системы качества. Модель обеспечения качества при производстве, монтаже и обслуживании
ГОСТ Р ИСО 9003-96 Системы качества. Модель обеспечения качества при окончательном контроле и испытаниях
ГОСТ Р ИСО 11138-1-2000 Стерилизация медицинской продукции. Биологические индикаторы. Часть 1. Общие положения
ГОСТ Р 51350-99 (МЭК 61010-1—90) Электрооборудование для проведения измерений, управления и лабораторного использования. Требования безопасности. Часть 1. Общие требования ГОСТ Р МЭК 61010-2-041-99 Электрооборудование для проведения измерений, управления и лабораторного использования. Часть 2-041. Частные требования к паровым автоклавам для обработки медицинских материалов и для лабораторных процессов
3 Определения
В настоящем стандарте применяются следующие термины с соответствующими определениями:
3.1 паровоздушная смесь (air-steam mixture): Однородная смесь воздуха и насыщенного пара, используемая для стерилизации.
Примечание — Воздух используют для компенсации давления, возникающего в герметичных контейнерах и превышающего давление насыщенного пара.
Издание официальное
3.2 бионагрузка (bioburden); Популяция жизнеспособных микроорганизмов в сырье, материалах, конечном продукте и/или в упаковке.
3.3 аттестация: Процесс документированного рассмотрения и утверждения пригодности, осуществляемый на завершающей стадии программы валидации с целью разрешения выпуска продукции.
3.4 величина D (D value): Время выдержки при определенных условиях обработки, необходимое для уменьшения популяции конкретного тест-микроорганизма в 10 раз.
3.5 электромеханический контроль (electromechanical control): Контрольная система, использующая механические средства (например, копиры или перфокарты) для согласования и подачи электрических сигналов.
3.6 средства контроля производственной среды (environmental controls): Средства контроля и мероприятия, принятые в производственных помещениях с целью регулирования бионагрузки.
Примечание — Сюда могут входить воздушные и жидкостные фильтры, дезинфекция поверхностей, рабочая одежда персонала и организационные меры.
3.7 величина F (/'value): Мера способности тепловой стерилизационной обработки инактивировать микроорганизмы.
3.8 величина (^b value): Величина F, рассчитанная при температуре 121,1 °С, величине z, равной 10 °С, и величине Д равной 1 мин.
3.9 конструкционные материалы (materials of construction): Материалы, из которых изготовлено оборудование для стерилизации.
3.10 микробиологический тест (microbiological challenge): Биологические индикаторы, тест-пакеты с биологическими индикаторами или инокулированный продукт, которые содержат известную популяцию микроорганизмов и могут быть использованы для проверки циклов стерилизации.
3.11 влажное тепло (moist heat): Тепло, источником которого является вода (в жидком или парообразном состоянии) под давлением.
3.12 стерилизация влажным теплом (moist heat sterilization): Обработка с использованием влажного тепла для получения стерильной продукции.
3.13 первичная упаковка (primary packaging): Элемент упаковочной системы, который сохраняет стерильность продукции.
3.14 летальность процесса (process lethality): Способность процесса стерилизации инактивировать микроорганизмы.
Примечание — Летальность определяют путем количественной оценки гибели микроорганизмов или путем установления и измерения требуемых физических параметров.
3.15 система носителя продукта (product carrier system): Устройство для размещения продукта и его упаковки при стерилизации.
Примечание — Система носителя должна предохранять продукт от повреждения и обеспечивать равномерный доступ стерилизующего агента.
3.16 приемка (комиссионная приемка, комиссионная проверка) (commissioning): Получение и документирование доказательства того, что оборудование поставлено и смонтировано в соответствии с документацией и работает в определенных допусках при условии соблюдения инструкций по эксплуатации.
3.17 повторная приемка (повторная комиссионная приемка, повторная комиссионная проверка) (recommissioning): Повторение приемки полностью или частично для подтверждения надежности процесса.
3.18 ревалидация (revalidation): Комплекс документированных процедур для подтверждения ранее проведенной валидации;
3.19 насыщенный пар (saturated steam): Водяной пар в состоянии равновесия между конденсацией и испарением.
3.20 имитатор загрузки (simulated product load): Загрузка, заменяющая целевую загрузку и обеспечивающая эквивалентное или большее противодействие обработке.
3.21 стерильный (sterile): Не содержащий жизнеспособных микроорганизмов.
Примечание — На практике состояние абсолютного отсутствия микроорганизмов не может быть доказано.
3.22 стерилизация (sterilization): Валидированный процесс освобождения продукта от всех форм жизнеспособных микроорганизмов.
Примечание — При стерилизации процесс отмирания микроорганизмов описывается экспоненциальным законом. Следовательно, наличие микроорганизмов в конкретном объекте может быть выражено в вероятностном виде. Эта вероятность может быть снижена до весьма малой величины, но она никогда не может быть снижена до нуля.
2
3.23 цикл стерилизации (sterilization cycle): Заданная последовательность рабочих стадий, предназначенных для достижения стерилизации и выполняемых в закрытой камере.
3.24 разработка процесса стерилизации (sterilization process development): Исследования и разработка воспроизводимого процесса, с помощью которого продукт может быть стерилизован без повреждения до желаемого значения вероятности сохранения нестерильных единиц.
3.25 валидация (validation): Документированная процедура получения, протоколирования и интерпретации результатов, необходимых для демонстрации того, что процесс неизменно дает продукт, соответствующий предварительно определенным требованиям.
Примечание — Валидация включает три действия: комиссионную проверку, проверку процесса на соответствие требованиям и аттестацию в эксплуатации.
3.26 величина z (z value): Изменение температуры, необходимое для изменения величины D в 10 раз.
3.27 продукт (product): Общее понятие для обозначения сырья, промежуточных продуктов и готовой продукции.
4 Общие положения4.1 Ответственность и подготовка персонала
Ответственность за монтаж и обслуживание стерилизаторов влажным теплом, валидацию и текущий контроль стерилизации влажным теплом, а также выпуск стерилизованной продукции должна быть возложена на квалифицированный персонал, как это предусмотрено в ГОСТ Р ИСО 9001 или ГОСТ Р ИСО 9002.
4.2 Требования к продукту
Продукт должен быть изготовлен в соответствии с документацией на него, требованиями безопасности и эффективности при максимальном числе циклов стерилизации, предусмотренном для данного продукта. Если необходима какая-то подготовка перед стерилизацией (например, очистка), она должна быть валидирована как часть процесса стерилизации. Продукт и материалы должны быть совместимы с изменениями среды внутри стерилизационной камеры, происходящими во время цикла стерилизации.
4.3 Требования к упаковке
4.3.1 Общие положения
Упаковка должна состоять, по крайней мере, из первичной и вторичной упаковок.
Первичная упаковка, а также вторичная упаковка (если предусмотрена стерилизация и во вторичной упаковке) должны соответствовать требованиям, предъявляемым к процессу стерилизации.
4.3.2 Проницаемость упаковки
Упаковка должна обеспечивать условия стерилизации на поверхности или внутри продукта как за счет удаления воздуха, так и проникновения пара, или, для непроницаемой упаковки (например, флаконов для жидкости), за счет теплопередачи.
5 Оборудование5.1 Документация
5.1.1 Данные об оборудовании
Для каждой системы стерилизации должна быть одна или более информационных табличек, закрепленных на оборудовании и содержащих следующую информацию на языке пользователя:
a) наименование и адрес изготовителя;
b) заводской номер или иное обозначение оборудования;
c) расчетное давление в камере и максимальная рабочая температура;
d) давление в рубашке камеры (если необходимо);
e) отметка инспектора надзора и идентификационная маркировка сосуда;
f) дата изготовления сосуда.
5.1.2 Безопасность
Должно быть документально подтверждено соответствие системы стерилизации требованиям безопасности ГОСТ Р 51350 и ГОСТ Р МЭК 61010-2-041 или другим нормативным документам, действующим на территории страны пользователя.
3
5.1.3 Руководства и инструкции
Для каждого стерилизатора должна быть дана на языке, согласованном с пользователем, следующая обязательная информация (приложение А):
a) инструкции по монтажу системы стерилизации, достаточные для безопасной и эффективной работы оборудования;
b) перечень конструктивных материалов, подвергаемых действию стерилизующего агента или непреднамеренному контакту с продуктом;
c) инструкции по безопасной и эффективной работе, включая рекомендации по предельно допустимым значениям температуры и давления в сосуде, а также меры предосторожности;
d) инструкции и рекомендуемый график технического обслуживания;
e) руководство по ремонту, включая перечень рекомендуемых заменяемых частей;
f) схемы камеры, показывающие ее форму и конструкцию, трубопроводы и принципиальные схемы системы контроля, рекомендуемые схемы монтажа и перечень запасных частей всех ответственных узлов системы;
g) схема управления процессом и/или программное обеспечение, необходимое для работы и обслуживания системы контроля (см. 5.2.6). Любые поставляемые программы должны сопровождаться документацией, подтверждающей проведение их валидации и лицензионный уровень.
5.1.4 Дополнительная информация
Стерилизатор влажным теплом должен иметь документацию, включающую порядок его монтажа и проведения испытаний.
5.2 Эксплуатационные характеристики стерилизатора, технологические среды и источники энергии, материалы, принадлежности и средства контроля
5.2.1 Эксплуатационные характеристики
Системы стерилизации влажным теплом должны быть выполнены в соответствии с нормативными документами на оборудование стерилизации, принятыми в стране пользователя.
5.2.2 Технологические среды и источники энергии
5.2.2.1 Чистота и качество пара должны быть стандартизованы и подтверждены экспериментально.
5.2.2.2 Чистота сжатого воздуха, используемого в стерилизационной камере, должна быть такова, чтобы безопасность препарата не нарушалась.
5.2.2.3 Во всех случаях стерилизации продуктов, упакованных в проницаемую для воздуха упаковку, требуется, чтобы окружающий воздух, поступающий в камеру при сбросе вакуума, проходил через фильтр, который задерживает микроорганизмы.
5.2.2.4 Вода, используемая в стерилизаторе для охлаждения продукта, должна быть стандартизована и проверена на соответствие требованиям, установленным при разработке продукта. Это должно быть документировано.
5.2.2.5 Электропитание, подводимое к системе стерилизации, должно соответствовать требованиям изготовителя.
5.2.3 Материалы
Материалы и компоненты, используемые при конструировании системы стерилизации, должны сводить к минимуму риск микробиологической и химической контаминации.
5.2.4 Принадлежности
В системах, предназначенных для размещения продукта, пар должен равномерно проникать во внутренние полости камеры и/или обеспечивать нормальную теплопередачу. Система носителя должна обеспечивать дренаж конденсата и/или охлаждающей воды, предотвращать повреждение продукта и сохранять целостность загруженного материала.
5.2.5 Системы контроля и регистрации данных
Должны контролироваться и записываться следующие параметры процесса:
a) температура;
b) время;
c) давление;
d) скорость изменения температуры и давления, если требуется сохранение целостности продукта.
Записывающее устройство и система контроля должны быть независимыми и выполненными таким образом, чтобы подавать сигнал тревоги в случае, если различия между контролируемыми и записываемыми переменными превышают допустимые пределы.
4
5.2.6 Программы контроля
Программные средства, используемые для управления и контроля процесса стерилизации (микропроцессорные или электромеханические), должны быть валидированы. Контрольные программы должны быть оформлены документально. Правильность их работы должна быть продемонстрирована как при имитации процесса, так и в реальном процессе. Любые последующие изменения следует документировать аналогичным образом, оценивать с точки зрения необходимости ревалидации и согласовывать с пользователем.
5.3 Требования к приборам
5.3.1 Точность приборов
5.3.1.1 Точность приборов, применяемых для валидации, должна превышать точность управляющей и записывающей систем.
5.3.1.2 Датчики температуры и давления должны гарантировать установленную точность.
5.3.2 Эталоны калибровки
Точность эталонов, применяемых для калибровки измерительных приборов, должна быть определена, и калибровка должна прослеживаться до национального эталона, как это предусмотрено ГОСТ Р ИСО 9003.
5.3.3 Обязательные контрольные приборы стерилизатора
Стерилизатор должен быть оснащен отдельной измерительной системой, обеспечивающей получение информации о том, что измеряемые контрольными приборами температура и давление в каждом цикле стерилизации находятся в указанных пределах.
5.3.4 Программа калибровки
Следует документировать и выполнять необходимые инструкции по калибровке всех контролирующих, показывающих и записывающих приборов, применяемых для валидации и текущего контроля цикла стерилизации. Эти инструкции должны соответствовать требованиям ГОСТ Р ИСО 9001 - ГОСТ Р ИСО 9003.
5.4 Техническое обслуживание
5.4.1 Стерилизатор должен обслуживаться в соответствии с документально оформленным графиком планово-предупредительного обслуживания.
5.4.2 Лицо, выполняющее техническое обслуживание, должно иметь документ, подтверждающий успешное прохождение им обучения по обслуживанию конкретного стерилизатора (стерилизаторов).
5.4.3 Работы по проведению каждого планового обслуживания и их периодичность должны быть определены и документированы.
5.4.4 Стерилизатор не должен использоваться до тех пор, пока не будут проведены и документально оформлены все плановые и внеплановые работы по техническому обслуживанию.
5.4.5 Документация о проведении технического обслуживания должна храниться совместно с документацией на оборудование.
5.4.6 График технического обслуживания, инструкции по обслуживанию и документация о его проведении должны периодически рассматриваться ответственным лицом.
6 Разработка процесса стерилизации
6.1 Всегда, за исключением случаев, при которых согласно документации существует риск для продукта, должна применяться стерилизация насыщенным паром. Там, где используются другие методы (например, паровоздушные смеси), должна быть показана воспроизводимость внутренней среды в камере.
Паровоздушные смеси следует применять только вместе с эффективной циркуляцией, создающей однородную тепловую среду внутри стерилизатора. Если используют паровоздушную смесь и необходимо проникновение пара в стерилизуемый объект, система циркуляции должна обеспечивать однородность паровоздушной смеси внутри загружаемых объектов.
6.2 Разработка цикла стерилизации должна предусматривать воспроизводимость его во время текущего процесса.
6.3 Должно быть показано обеспечение условий стерилизации продукта при вновь разработанных циклах стерилизации влажным теплом.
6.4 Качество любого продукта после стерилизации не должно ухудшаться при обращении и хранении его на участке стерилизации.
5
6.5 Риск сохранения нестерильное™ единицы продукции должен приниматься таким, чтобы вероятность выживания микроорганизмов была достаточно низкой и продукция была безопасной для использования.
6.6 Если используют индикаторные микроорганизмы, то они должны выбираться с учетом особенностей процесса стерилизации и соответствовать требованиям ГОСТ Р ИСО 11138-1.
6.7 Достигнутая требуемая вероятность выживаемости бионагрузки должна быть подтверждена расчетом.
6.8 Для процессов стерилизации, основанных на величине бионагрузки, должна быть предусмотрена соответствующая программа, которая определяет число и резистентность бионагрузки перед стерилизацией.
7 Валидация процесса стерилизации
7.1 Программа валидации должна осуществляться на основе утвержденного протокола по ГОСТ Р ИСО 9002.
7.2 Следует провести приемку каждого стерилизатора после монтажа и валидировать процесс стерилизации при изменениях в продукции или условиях проведения процесса, а также в новом стерилизационном оборудовании.
7.3 Валидация должна быть поручена ответственному лицу, имеющему опыт проведения такой работы.
7.4 Валидация процесса должна состоять из комиссионной приемки систем, аттестации в эксплуатации и сертификации.
7.4.1 Комиссионная приемка должна включать:
a) демонстрацию соответствия эксплуатационным характеристикам, указанным в документации;
b) проверку документации на оборудование;
c) демонстрацию соответствия качества и работоспособности используемых средств;
d) проверку калибровки рабочих и контрольных приборов;
e) если необходимо, демонстрацию эффективности системы удаления воздуха.
7.4.2 Аттестация в эксплуатации должна показать:
a) воспроизводимость процесса (проведением достаточного количества циклов);
b) однородность показателей в пределах указанных лимитов внутри камеры и загруженного объекта (с помощью достаточного количества циклов и датчиков);
c) соотношение между контрольными и фактическими параметрами;
d) зависимость между физическими параметрами и летальностью микроорганизмов по данным литературы и проведенным исследованиям;
e) соответствие требованиям при максимальной и минимальной загрузке (или смеси специфических продуктов);
f) репрезентативность имитирующей загрузки (если она применяется) по отношению к реальной загрузке;
g) то, что используемая для аттестации загрузка, которая будет применяться повторно, перед повторным использованием возвращается к указанным условиям;
h) соответствие продукта и упаковки документации после стерилизации и, если нужно, повторной стерилизации.
7.4.3 Должно быть определено число датчиков температуры для проведения аттестации в эксплуатации и повторной аттестации в эксплуатации. Должно быть приведено документальное свидетельство достаточности этого числа датчиков в соответствии с данными, полученными во время исследования процесса стерилизации.
7.4.4 До и после каждой программы последовательных испытаний следует проверять срок действия калибровки используемых при валидации систем измерения температуры.
7.5 На этапе завершения валидации следует рассмотреть и утвердить полученные данные.
7.6 Ревалидация должна быть проведена после существенного ремонта системы стерилизации, который может повлечь за собой изменение эффективности процесса. Ревалидация должна также проводиться не реже чем один раз в 12 мес.
7.7 Процедуры ревалидации, проверки и изменения процесса, системы стерилизации (оборудования и программы) продукта и упаковки должны быть документированы. Процедуры должны
6