ГОСТ Р ИСО 10993-12-2009
Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и контрольные образцы
Устанавливает методы приготовления проб и выбора контрольных образцов, используемых для оценки биологического действия материалов и медицинских изделий в биологических системах в соответствии со стандартами серии ИСО 10993, и включает в себя: - выбор материала для исследования; - выбор репрезентативной части изделия; - приготовление исследуемой пробы; - экспериментальный контрольный образец; - выбор контрольных образцов и требования к ним; - выбор контрольных образцов для доказательства применимости тест-системы и/или для относительного сравнения биологической активности изучаемой пробы; - приготовление экстрактов. Стандарт не распространяется на материалы или изделия, содержащие биоткани.
- Заменяет ГОСТ Р ИСО 10993.12-99 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и стандартные образцы» ИУС 7-2010
Идентичен ISO 10993-12:2007
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Основные требования
5 Контрольные образцы
5.1 Общие положения
5.2 Сертификация контрольных образцов для исследования биологической безопасности
6 Использование контрольных образцов для экспериментального контроля
7 Выбор образца для исследования
8 Приготовление исследуемой пробы и контрольного образца
9 Выбор репрезентативных частей изделия
10 Приготовление экстрактов из исследуемых материалов
10.1 Основные положения
10.2 Контейнеры для экстракции
10.3 Условия и методы экстракции
10.4 Условия экстракции для определения опасности и оценки риска в режиме преувеличенного использования
11 Отчет об исследовании
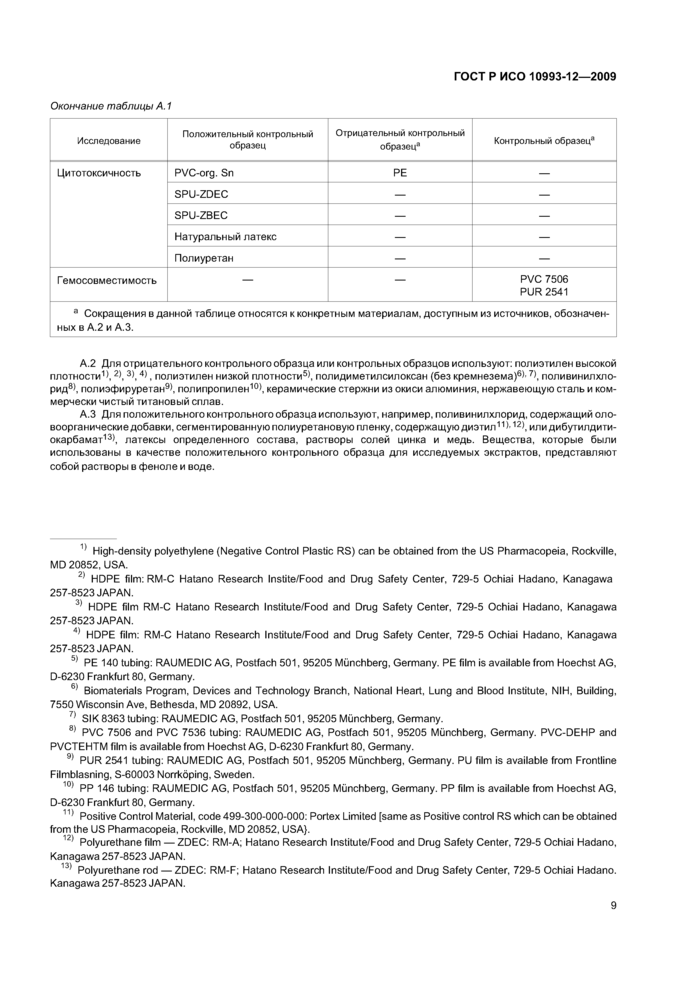
Приложение А (справочное) Экспериментальный контрольный образец
Приложение В (справочное) Основные принципы и методы приготовления проб и выбора образцов
Приложение С (справочное) Принципы экстракции исследуемых образцов
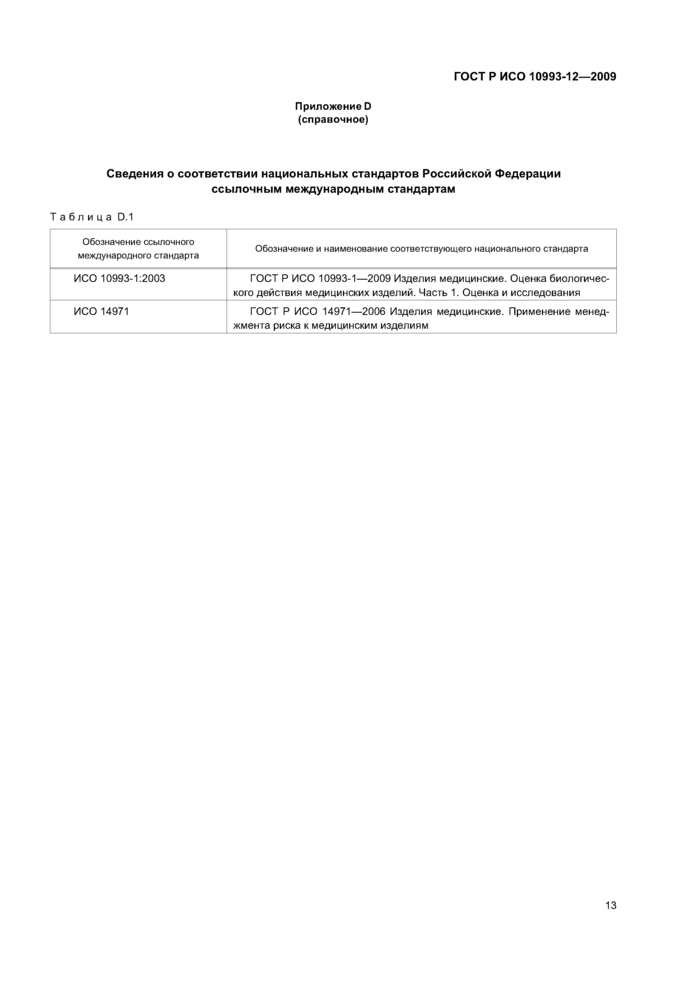
Приложение D (справочное) Сведения о соответствии национальных стандартов Российской Федерации ссылочным международным стандартам
Библиография
20 страниц
| Дата введения | 01.09.2010 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.01.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 02.12.2009 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 538-ст |
|---|---|---|---|
| Разработан | АНО ИМБИИТ | ||
| Издан | Стандартинформ | 2010 г. |
Medical devices. Biological evaluation of medical devices. Part 12. Sample preparation and control materials
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13

стр. 14

стр. 15

стр. 16
стр. 17

стр. 18

стр. 19

стр. 20
ГОСТ Р исо
10993-12-
2009
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙЧасть 12Приготовление проб и контрольные образцы
Часть 12Приготовление проб и контрольные образцы
ISO 10993-12:2007
Biological evaluation of medical devices — Part 12: Sample preparation and
reference materials (IDT)
Издание официальное
го
ID
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН Автономной некоммерческой организацией «Институт медико-биологических исследований и технологий» (АНО «ИМБИИТ»)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 422 «Оценка биологического действия медицинских изделий»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 2 декабря 2009 г. № 538-ст
4 Настоящий стандарт идентичен международному стандарту ИСО 10993-12:2007 «Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и стандартные образцы» (ISO 10993-12:2007 «Biological evaluation of medical devices — Part 12: Sample preparation and reference materials»).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены 8 дополнительном приложении D
5 ВЗАМЕН ГОСТ Р ИСО 10993.12-99
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
©Стандартинформ. 2010
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
Содержание
1 Область применения...................................................1
2 Нормативные ссылки..................................................1
3 Термины и определения................................................1
4 Основные требования..................................................3
5 Контрольные образцы..................................................3
5.1 Общие положения.................................................3
5.2 Сертификация контрольных образцов для исследования биологической безопасности.....3
6 Использование контрольных образцов для экспериментального контроля.................4
7 Выбор образца для исследования..........................................4
8 Приготовление исследуемой пробы и контрольного образца.........................4
9 Выбор репрезентативных частей изделия.....................................5
10 Приготовление экстрактов из исследуемых материалов............................5
10.1 Основные положения..............................................5
10.2 Контейнеры для экстракции..........................................5
10.3 Условия и методы экстракции.........................................5
10.4 Условия экстракции для определения опасности и оценки риска в режиме преувеличенного
использования..................................................7
11 Отчет об исследовании................................................8
Приложение А (справочное) Экспериментальный контрольный образец...................8
Приложение В (справочное) Основные принципы и методы приготовления проб и выбора образцов . . 10
Приложение С (справочное) Принципы экстракции исследуемых образцов................11
Приложение D (справочное) Сведения о соответствии национальных стандартов Российской Федерации ссылочным международным стандартам .........................13
Библиография........................................................14
III
Введение
Соблюдение положений стандартов серии ИСО 10993 «Оценка биологического действия меди-цинских изделий» позволит обеспечить системный подход к исследованию биологического действия медицинских изделий.
Целью этих стандартов не является безусловное закрепление единообразных методов исследований и испытаний за группами однородных медицинских изделий в соответствии с принятой классификацией их по виду и длительности контакта с организмом человека. Поэтому планирование и проведение исследований и испытаний должны осуществлять специалисты, имеющие соответствующую подготовку и опыт в области санитарно-химической, токсикологической и биологической оценок медицинских изделий.
Стандарты серии ИСО 10993 являются руководящими документами для прогнозирования и исследования биологического действия медицинских изделий на стадии выбора материалов, предназначенных для их изготовления, а также для исследований готовых изделий.
В серию ИСО 10993 входят следующие части под общим названием «Оценка биологического действия медицинских изделий»:
Часть 1—Оценка и исследования;
Часть 2 — Требования к обращению с животными;
Часть 3 — Исследования генотоксичности. канцерогенности и токсического действия на репродуктивную функцию;
Часть 4 — Исследования изделий, взаимодействующих с кровью;
Часть 5 — Исследование на цитотоксичность: методы in vitro;
Часть 6 — Исследование местного действия после имплантации;
Часть 7 — Остаточное содержание этиленоксида после стерилизации;
Часть 9 — Основные принципы идентификации и количественного определения потенциальных продуктов деградации;
Часть 10 — Исследования раздражающего и сенсибилизирующего действия;
Часть 11 —Исследования общетоксического действия;
Часть 12 — Приготовление проб и стандартные образцы;
Часть 13 — Идентификация и количественное определение продуктов деградации полимерных медицинских изделий;
Часть 14 — Идентификация и количественное определение продуктов деградации изделий из керамики;
Часть 15 — Идентификация и количественное определение продуктов деградации изделий из металлов и сплавов;
Часть 16 — Моделирование и исследование токсикокинетики продуктов деградации и вымывания;
Часть 17 — Установление пороговых значений для вымываемых веществ;
Часть 18 — Исследование химических свойств материалов;
Часть 19 — Исследование физико-химических, морфологических и топографических свойств материалов;
Часть 20 — Принципы и методы исследования иммунотоксического действия медицинских изделий.
Настоящий стандарт содержит требования и методы приготовления исследуемых проб, и выбор стандартных образцов для проведения исследований с целью оценки биологического действия медицинских изделий.
Методы приготовления проб должны учитывать назначение, природу материала и методы оценки биологического действия, включая используемые модельные среды, продолжительность контакта с организмом и другие параметры.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ ОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Часть 12 Приготовление проб и контрольные образцы
Medical devices. Biological evaluation of medical devices.
Part 12. Sample preparation and control materials
Дата введения — 2010—09—01
1 Область применения
Настоящий стандарт устанавливает методы приготовления проб и выбора контрольных образцов, используемых для оценки биологического действия материалов и медицинских изделий (далее — изделий) в биологических системах в соответствии со стандартами серии ИСО 10993. и включает в себя:
- выбор материала для исследования:
- выбор репрезентативной части изделия:
- приготовление исследуемой пробы:
- экспериментальный контрольный образец:
- выбор контрольных образцов и требования к ним;
- выбор контрольных образцов для доказательства применимости тест-системы и/или для относительного сравнения биологической активности изучаемой пробы:
- приготовление экстрактов.
Настоящий стандарт не распространяется на материалы или изделия, содержащие биоткани.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие нормативные документы. При датированной ссылке применимо только указанное издание. При ссылке без даты применимо последнее издание указанного документа, включая все поправки;
ИСО 10993-1:2003 Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования
ИСО 14971 Изделия медицинские. Применение менеджмента риска к медицинским изделиям
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 контрольный раствор: Раствор, применяемый для приготовления экстракта, хранящийся в идентичной емкости и подвергающийся тем же условиям, что и раствор с исследуемым материалом во время экстракции, но не содержащий его.
Примечание — Контрольный раствор предназначен для оценки возможных погрешностей, вызванных емкостью, используемой при экстракции, экстрагирующей жидкостью и процессом экстракции.
3.2 стандартный образец (CMR): Образец вещества (материала) с установленными по результатам испытаний значениями одной или более величин, характеризующих состав или свойство этого вещества (материала) и дающих возможность точного определения количественных характеристик с отклонениями на установленном доверительном уровне.
Издание официальное
3.3 экспериментальный контрольный образец: Образец вещества с хорошо изученными реакциями, которое используется в конкретной тест-системе для помощи при оценке реакций тест-системы на предмет воспроизводимости и соответствия.
3.4 экстракт: Раствор, полученный в результате экстракции исследуемого материала или контрольного материала.
3.5 гомогенность: Свойство материала и его взаимоотношение с биологической конечной точкой, при которых его однородная структура или состав позволяют последовательно вызывать или последовательно не вызывать конкретный биологический ответ.
Примечание — Контрольный образец называют гомогенным, если биологический ответ на конкретное испытание находится в рамках обозначенных пределов неопределенности испытания, вне зависимости от партии или серии исходного материала для стандартного образца.
3.6 отрицательный контрольный образец: Любой достаточно охарактеризованный образец материала или вещества, который, подвергаясь исследованию поолисанной методике, показывает пригодность этой методики для получения воспроизводимого, соответствующего отрицательного, нереактивного или минимального ответа в тест-системе.
Примечание — На практике в качестве отрицательного контрольного образца используют контрольные образцы, но также возможно применение фоновых и экстрагируемых растворов.
3.7 положительный контрольный образец: Любой достаточно охарактеризованный образец материала или вещества, который, подвергаясь исследованию поолисанной методике, показывает пригодность этой методики для получения воспроизводимого, соответствующего положительного или реактивного ответа в тест-системе.
3.8 контрольный образец: СО: Образец материала или вещества с установленными значениями одной или более величин, характеризующих состав или свойство этого вещества (материала), предназначенный для калибровки аппаратуры, оценки метода измерения или определения количественных характеристик материала.
(ИСО Руководство 30, определение 2.1)
Примечание — В настоящем стандарте контрольным образцом является любой достаточно определенный образец ма гериала или вещества, который, подвергаясь исследованию по описанной методике, показывает пригодность методики для получения воспроизводимого, предсказуемого результата. Результат может быть положительным или отрицательным.
3.9 стабильность количественных характеристик: Способность материала поддерживать конкретный установленный биологический ответ в рамках обозначенных пределов при хранении при обозначенных условиях в течение определенного периода времени.
3.10 исследуемый материал: Материал, изделие, часть изделия либо его компонент, пробу которого отбирают для биологического или химического исследования.
3.11 моделируемая экстракция: Экстракция, проводящаяся методом, моделирующим использование изделия, и демонстрирующая соответствие требованиям настоящего стандарта оценкой уровней вымываемых из изделий материалов, которые воздействуют на пациента или пользователя при соответствующем использовании изделия.
Примечав и е — Аналитическая лаборатория обязана продемонстрировать, что моделируемая экстракция проводится при условиях наибольшей требовательности к предполагаемому использованию. Моделирование использовании изделия проводится с учетом того, что изделию присваивается наиболее строгая возможная категория по длительности воздействия, а также принимаются во внимание задействованные ткани и температура воздействия.
3.12 преувеличенная экстракция: Любая экстракция, предназначенная для получения большего количества выделяемого химического компонента по сравнению с количеством, вырабатываемым при моделируемых условиях использования.
Примечание — Преувеличенная экстракция можетпривестикхимическимизменениям экстрагируемого материала или вещества.
3.13 ускоренная экстракция: Любая экстракция, определяющая измерения материалов, вымываемых из изделия или материала, используя условия, которые сокращают время вымывания веществ в экстрагирующую жидкость, но не приводят к химическим изменениям экстрагируемых веществ.
Примечание — Примерами условий ускоренной экстракции являются, повышенная температура, возбуждение. смена экстрагирующей жидкости и т.д.
2
3.14 исчерпывающая экстракция: Экстракция до момента, когда количество вымываемого материала в последующей экстракции составляет менее чем 10 % количества, обнаруженного в первоначальной экстракции, или до момента, когда аналитически значительное повышение совокупных уровней вымываемого материала не наблюдается.
Примечание — Так как исчерпывающий характер обнаружения осадков продемонстрировать невозможно, применяется определение исчерпывающей экстракции, приведенное выше. Также см. приложение С.
4 Основные требования
4.1 Как описано в ИСО 14971, при определении опасности и оценке риска медицинских изделий опасность, возникающая в результате изменений в процессе производства или недостаточного контроля производственного процесса, должна быть учтена при планировании и подготовке образцов для испытаний и приготовлении экстрактов из этих изделий. Особое внимание следует уделять остаточным веществам этих производственных процессов, например остаточным веществам, очистителям и дезинфектантам.
4.2 Так как ИСО 10993 описывает множество различных систем биологических исследований, необходимо свериться с индивидуальными стандартами для определения пригодности данных рекомендаций для конкретных тест-систем.
4.3 Экспериментальный контрольный образец используют для подтверждения методики тестирования и/или для сравнения результатов разных материалов. В зависимости от того, какой метод исследования биологического действия используют, в качестве подходящего может быть выбран отрицательный или положительный контрольный образец либо контрольный раствор.
Примечание — Один и тот же контрольный образец может быть использован в различных методах исследования и может допускать перекрестные ссылки на другие установленные материалы и методы исследования. Дополнительное руководство по выбору экспериментального контрольного образца приведено в приложении А. Использование положительного контрольного образца для испытаний in vivo может зависеть от норм благополучия животных.
5 Контрольные образцы
5.1 Общие положения
Контрольные образцы предоставляют специализированные организации. Эти организации определяют объем химических, физических и биологических характеристик. Имеющиеся в продаже образцы изделий, применяемых в медицинской практике, могут быть использованы в качестве контрольных образцов.
Примечание 1 — См. Руководство ИСО 35.
Стандартный образец выбирают с учетом его высокой степени чистоты, специфических характеристик, соответствия предполагаемому применению и общей доступности. Специфические химические, физические и биологические характеристики определяют при межлабораторных исследованиях в трех или более лабораториях и предоставляются исследователю поставщиком.
Примечание 2 — Для пользователей желательно получение заверения от поставщиков контрольных образцов или стандартных образцов, что эти материалы будут доступны пользователю по меньшей мере пять лет. Вторым, менее желательным, вариантом является публикация источников контрольных образцов или стандартных образцов «открытой формулы» материала, т.е. публикация исходных материалов и деталей обработки, необходимых для обеспечения однородных партий контрольных образцов.
5.2 Сертификация контрольных образцов для исследования биологической безопасности
5.2.1 Квалификация контрольного образца является процедурой, которая устанавливает численное или количественное значение биологического ответа материала при определенных условиях испытания, обеспечивая воспроизводимость ответа, как в лабораторных, таки в межлабораторных условиях. Диапазон биологических ответов, связанных с материалом, устанавливают путем лабораторных исследований.
5.2.2 Материалы сертифицируются поставщиками контрольных образцов. Поставщик определяет предельные химические и физические характеристики. Отдельные лаборатории, использующие контрольные образцы, определяют биологическую характеристику, необходимую для утверждения контрольного образца для определенного испытания или процедуры. Материалы, имеющиеся в прода-
же. могут использоваться как контрольные образцы, если они сертифицированы и пригодны для испытаний.
5.2.3 Сертификация контрольного образца является процедурой, которая устанавливает качественное или количественное значение биологического ответа материала при определенных условиях испытания. Этот процесс служит для утверждения испытания материала на конкретный ответ и приводит к выдаче сертификата. Биологический ответ на материал устанавливают путем межлабораторных исследований.
6 Использование контрольных образцов для экспериментального контроля
6.1 Контрольные образцы или стандартные образцы используются в биологических испытаниях как контрольные материалы, демонстрирующие пригодность процедуры для получения воспроизводимого результата, положительного и/или отрицательного. Любой материал, используемый таким образом, характеризуется при каждой процедуре биологического испытания, для которой хотят использовать материал. Материал, охарактеризованный и затем сертифицированный для одного контрольного метода исследования или ответа, например гиперчувствительности замедленного типа, не должен использоваться как контрольный образец для другого, например цитотоксичности, без дополнительного утверждения.
Примечание — Использование контрольного образца облегчает сличение результатов в разных лабораториях и помогает при оценке воспроизводимости результатов испытания в отдельных лабораториях. Для сравнения биологического ответа желательно использовать контрольные образцы с диапазоном ответных реакций, например минимальный, средний или резкий.
6.2 Контрольные образцы, используемые в качестве экспериментального контроля, должны удовлетворять установленным требованиям к качеству, гарантируемому процедурами изготовителя и испытательной лаборатории. Они должны сопровождаться сведениями об источнике, изготовителе, степени чистоты и типе. Контрольные образцы обрабатывают согласно положениям раздела 8.
6.3 Контрольные образцы, используемые в качестве экспериментального контроля, должны находиться в том же классе материалов, что и исследуемый образец, т.е. полимер, керамика, металл, коллоид и тд Тем не менее чистые химические вещества могут быть использованы для экспериментального контроля процедур испытаний, основанном на механизме действия, например пробы на генотоксич-ность и на иммунную гиперчувствительность замедленного типа.
7 Выбор образца для исследования
7.1 Исследованию подвергают изделие в готовом к применению виде или материалы, обработанные также, как и готовое изделие (см. ИС010993-1). или соответствующие экстракты любого из вышеперечисленного. Выбор исследуемой пробы должен быть обоснован.
Примечание — В случае материалов, отверждаемых in situ, могут быть необходимы различные исследуемые образцы, отражающие отвержденный материал и его неотверждениое состояние.
7.2 В случае необходимости испытания экстракта применяют такую же процедуру выбора пробы для исследования.
8 Приготовление исследуемой пробы и контрольного образца
8.1 Исследуемые пробы и контрольные образцы необходимо обрабатывать в условиях, исключающих контаминацию. Вещества, образовавшиеся в процессе производства, очистки, стерилизации и т.п., следует считать неотъемлемой частью изделия, его части или компонента.
Примечани е — Дополнительное руководство по приготовлению растворов контрольных образцов приведено в приложении В.
a) Работу с исследуемыми пробами стерильных изделий и контрольных образцов следует проводить с учетом требований асептики, если это соответствует методике исследования.
b) Если на исследование поступают нестерильные изделия, которые должны быть стерилизованы перед применением в медицинской практике, то такие образцы перед исследованием стерилизуют методом, рекомендованным изготовителем. Работу с ними проводят с учетом требований асептики, если это соответствует методике исследования.
с) Если исследуемые пробы чистят перед стерилизацией, при выборе и работе с исследуемой пробой должно быть учтено влияние процесса очистки и очистителя.
8.2 Если для исследования необходимы стерильные исследуемые пробы, должно быть учтено влияние стерилизации.
8.3 Если исследуемые пробы и контрольные образцы требуется разрезать на части, какописанов 10.3.3, перечисление Ь), следует учитывать влияние поверхностей, не подвергавшихся ранее обработке. например просветов или поверхностей среза. При разрезании медицинских изделий на типичные образцы следует использовать технические приемы, исключающие контаминацию.
9 Выбор репрезентативных частей изделия
9.1 Если невозможно провести исследование целого изделия, каждая отдельная часть готового к применению изделия, контактирующая с тканями организма, должна быть представлена в исследуемой пробе в соответствующих пропорциях.
a) Образцы изделий с поверхностным покрытием должны содержать материал покрытия и основной материал, даже если субстрат не контактирует с тканями.
b) Образец должен содержать типичную часть соединения и/или склейки, если при производстве части изделия, входящей в контакт с пациентом, использовали адгезив, радиочастотное соединение или склейку растворителем.
9.2 Композитные материалы исследуют как конечные изделия.
9.3 Если в состав изделия входят различные материалы, при выборе образца необходимо учесть потенциальные возможности синергизма и других взаимодействий.
9.4 Образец может быть выбран с учетом максимального воздействия тест-системы на компоненты изделия с известной потенциальной биологической активностью.
10 Приготовление экстрактов из исследуемых материалов
10.1 Основные положения
Если исследование требует применения экстрактов, модельная среда и условия процесса экстракции должны соответствовать свойствам и назначению готового к применению изделия, а также цели исследования, например определение опасности, вычисление риска или оценка риска. При выборе условий экстракции необходимо учитывать физико-химические свойства материалов изделия, вымываемых веществ или остаточных веществ. Для отдельных биологических исследований, описанных в других стандартах серии ИСО 10993, существуют особые требования к приготовлению экстрактов из образцов. В этом случае требования соответствующих стандартов ИС0 10993 будут иметь приоритет по сравнению с требованиями настоящего стандарта.
Примечание — Дополнительное руководство по экстракции образцов приведено в приложении С.
10.2 Контейнеры для экстракции
10.2.1 Экстракцию проводят в чистых, химически инертных, герметичных емкостях, имеющих минимальное свободное пространство.
10.2.2 Для обеспечения того, чтобы емкости для экстракции не загрязнили модельную среду, такие емкости должны быть:
a) боросиликатными стеклянными пробирками с крышками/пробками на инертной прокладке [например, лоли(тетрафлуороэтилен)];
b) другими инертными емкостями для экстракции согласно требованиям для конкретных материалов и/или процедур экстракции.
10.3 Условия и методы экстракции
10.3.1 Условия экстракции основываются на существующей практике и обоснованы предоставлением стандартного подхода, который во многом является приемлемым преувеличением использования изделия. Экстракцию следует проводить при одном из режимов, приведенных ниже:
a) (37;1)°Свтечение(72г2)ч;
b) (50 г 2) °С в течение (72 г 2) ч;
c) (70 г 2) "С в течение (24 г 2) ч;
d) (121 ±2)вСвтечение(1 :0,1)ч.
Примечание — Экстракции при температуре (37 i1)°C в течение (24 ± 2) ч в культуральной среде может быть приемлемой для исследования цитотоксичности. См. ИСО 10993-5.
5
Условия экстракции, описанные выше, используемые для предоставления масштабов потенциального риска, для оценки риска изделия или материала, основываются на предшествующем опыте. Могут быть использованы и другие условия экстракции, имеющие место при клиническом использовании либо предоставляющие адекватную оценку потенциальной опасности; но в этом случае они должны быть описаны и обоснованы.
Экстракция является сложным процессом, на который оказывают влияние время, температура, соотношение площади поверхности и объема, экстрагирующая среда и фазовое равновесие1 > материала. Необходимо учитывать влияние высокой температуры и других условий на кинетику экстракции и идентичность модельных сред при проведении ускоренной или преувеличенной экстракции.
Например, при использовании повышенных температур существуют две возможности:
1) энергия высокой температуры может вызвать увеличенное образование поперечных связей и/или полимеризацию полимера и. таким образом, снизить количество свободного мономера для миграции из полимера;
2) высокая температура может вызвать формирование продуктов деградации, которые обычно не присутствуют в готовом изделии в условиях клинического применения.
10.3.2 Для материалов, растворяющихся или всасывающихся в условиях клинического применения, необходимо следовать условиям экстракции, описанным в 10.3.1. По возможности, экстракцию проводят при использовании соответствующей экстрагирующей жидкости и условий времени/температуры для имитации воздействия. Может быть необходимо полное растворение.
10.3.3 Для определения необходимого объема экстрагирующей жидкости можно использовать стандартную площадь поверхности. Такая площадь включает общую площадь обеих сторон образца и исключает неопределенные неровности поверхности. Если конфигурация образца не позволяет определить площадь поверхности, необходимо использовать соотношение масса/объем экстрагирующей жидкости. См. таблицу 1.
a) Возможно использование других соотношений площади поверхности и объема модельной среды, например связанных с оценкой пористых материалов, если они моделируют условия клинического применения или дают оценку потенциальной опасности.
b) Материалы необходимо разрезать на мелкие части перед экстракцией для улучшения погружения в экстрагирующую среду, кроме тех случаев, когда это неприемлемо (например, см. 10.3.4). Например, для полимеров приемлемы части размерами примерно 10 х 50 мм или 5х 25 мм.
|
Таблица 1 — Стандартные площади поверхности и обьемы экстрагирующей жидкости | |||||||||||||||||||||
| |||||||||||||||||||||
|
Примечание — 8 настоящее время нет стандартизованных методов исследования абсорбентов и гид-роколлоидов. поэтому предлагается следующий порядок: Определяют обьем экстрагирующей жидкости, абсорбируемой на каждый 0,1 г или 1,0см2 материала. Затем, при проведении экстракции материала, добавляют этот дополнительный обьем на каждый 0.1 г или 1,0 см2 мо-1 дельной среды.___ |
Фазовое равновесие твердою материала во время экстракции определяет относительное содержание аморфной и кристаллической фаз. Для аморфной фазы температура фазового перехода (стеклования) Тд определяет подвижность полимерной цепи и скорость диффузии в данной фазе. Обычно скорость диффузии при температуре выше Тд значительно выше скорости диффузии при более низкой температуре. В кристаллической фазе скорость диффузии наиболее низка. Условия экстракции не должны изменять фазового равновесия материала. Изменение фазового равновесия может повлечь за собой изменение количества и структуры экстрагируемых веществ. В изменении фазового равновесия можно удостовериться, используя метод сканирующей дифференциальной калориметрии.