ГОСТ Р ЕН 14254-2010
Изделия медицинские для диагностики in vitro. Одноразовые емкости для сбора образцов у человека (кроме крови)
Купить ГОСТ Р ЕН 14254-2010 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает требования и методы исследования для одноразовых вакуумных и невакуумных емкостей, предназначенных изготовителями для первичного размещения и сохранения образцов, кроме крови, взятых из тела человека в целях диагностического исследования in vitro. Стандарт не определяет требования к иглам для взятия образцов, держателям игл или другим приспособлениям, используемым вместе с емкостями для образцов.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Материалы
5 Номинальная вместимость жидкости
6 Линии градуировки и заполнения
7 Проектирование
8 Конструкция
9 Стерильность и специальные микробиологические состояния
10 Добавки
11 Информация, предоставляемая изготовителем
Приложение А (обязательное) Тесты номинальной вместимости, градуировочной линии и минимального свободного пространства для невакуумных емкостей до и включая 30 куб. см номинальной вместимости
Приложение В (обязательное) Тесты номинальной вместимости, градуировочной линии и минимального свободного пространства для невакуумных емкостей больше чем 30 куб. см номинальной вместимости
Приложение С (обязательное) Тесты на втянутый объем и минимальное свободное пространство для вакуумных емкостей
Приложение D (обязательное) Тест на протекание крышки емкости
Приложение Е (обязательное) Тест на прочность емкости, предназначенной для центрифугирования
Приложение ZA (справочное) Соответствие настоящего стандарта основным требованиям Европейской Директивы 98/79/ЕС
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов ссылочным национальным стандартам Российской Федерации
Библиография
| Дата введения | 01.03.2012 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
In vitro diagnostic medical devices. Single-use receptacles for the collection of specimens, other than blood, from humans
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
стр. 17

стр. 18

стр. 19

стр. 20
ГОСТ Р ЕН 14254-2010
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ ДЛЯ ДИАГНОСТИКИ
IN VITRO
Одноразовые емкости для сбора образцов у человека (кроме крови)
EN 14254: 2004
In vitro diagnostic medical devices — Single-use receptacles for the collection of specimens, other than blood, from humans (IDT)
Издание официальное
|
Москва Стандартинформ 2011 |
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН Лабораторией проблем клинико-лабораторной диагностики Научно-исследовательского центра Государственного образовательного учреждения высшего профессионального образования «Московская медицинская академия им. И.М. Сеченова Росздрава» на основе собственного аутентичного перевода на русский язык стандарта, указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 380 «Медицинские изделия для диагностики in vitro»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 12 ноября 2010 г. № 457-ст
4 Настоящий стандарт идентичен международному стандарту ЕН 14254:2004 «Изделия медицинские для диагностики in vitro. Одноразовые емкости для сбора образцов у человека, кроме крови» (EN 14254:2004 «/л vitro diagnostic medical devices — Single-use receptacles for the collection of specimens, other than blood, from humans»).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных (региональных) стандартов соответствующие им национальные стандарты Российской Федерации и межгосударственные стандарты, сведения о которых приведены в дополнительном приложении ДА
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2011
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ Р ЕН 14254-2010Приложение В (обязательное)Тесты номинальной вместимости, градуировочной линии и минимального свободного пространства для невакуумных емкостей больше чем 30 см3 номинальной вместимости
В.1 Реактивы и приборы
Тесты номинальной вместимости, градуировочной линии и минимального свободного пространства для невакуумных емкостей больше чем 30 см3 номинальной вместимости
В.1.1 Вода, соответствующая требованиям ЕН ИСО 3696 при температуре от 20 °С до 25 °С.
В.1.2 Измерительный цилиндр, как указано в ИСО 4788, достаточного объема для выполнения теста.
В.2 Условия выполнения теста
В.2.1 Тест должен быть выполнен в условиях окружающей среды при 101 кПа и 20 °С, при отклонениях от этих параметров должна быть сделана соответствующая коррекция.
В.2.2 Подлежащая тестированию емкость должна быть неиспользованной и иметь линию заполнения, или градуировочную линию.
В.З Процедуры теста
В.3.1 Гравиметрический анализ
В.3.1.1 Взвешивают пустую емкость с точностью как можно ближе к 0,01 г.
В.3.1.2 Если емкость не поставляется в собранном состоянии, соединяют держатель с наконечником отсасывающего устройства в соответствии с инструкцией изготовителя. Если емкость не поставляется как вакуумная, следует произвести отсасывание до номинального объема отсасывания.
В.3.1.3 Вводят наконечник отсасывающего устройства в воду. Опустошают емкость в течение по меньшей мере 1 мин или наполняют в соответствии с инструкцией изготовителя.
В.3.1.4 Удаляют держатель и наконечник отсасывающего устройства, осушают поверхность емкости, если необходимо, и вновь взвешивают емкость с точностью до 0,01 г, чтобы определить количество отсасываемой воды.
Примечание — Метод, описанный в приложении А, может быть адаптирован.
В.З.2 Волюметрический метод
В.3.2.1 Наполняют бюретку.
В.3.2.2 Соединяют наконечник отсасывающего устройства с системой бюретки.
В.3.2.3 Заполняют систему водой, чтобы убедиться, что мертвое пространство системы заполнено водой. В.3.2.4 Отмечают объем в бюретке с точностью до 0,1 см3 (объем А).
В.3.2.5 Соединяют наконечник отсасывающего устройства с емкостью.
В.3.2.6 Позволяют емкости наполниться.
В.3.2.7 Отмечают уровень в бюретке с точностью до 0,1 см3 (объем В).
В.3.2.8 Рассчитывают объем выпущенной воды, вычитая объем В из объема А. 1
Приложение С (обязательное)Тесты на втянутый объем и минимальное свободное пространство для вакуумных емкостей
С.1 Реактивы и приборы
С.1.1 Вода, соответствующая требованиям ЕН ИСО 3696 при температуре от 20 °С до 25 °С.
С.1.2 Аналитические весы точностью до 0,001 г и достаточной емкостью весов для данного теста.
С.1.3 Держатель и наконечник дозатора, соединенные в соответствии с рекомендациями изготовителя емкости для образцов.
С.1.4 Подставка для поддержания емкости в вертикальном положении при взвешивании на местах (опция).
С.1.5 Пипетка или подобное устройство.
С.2 Условия выполнения теста
С.2.1 Тест должен быть выполнен в условиях окружающей среды при 101 кПа и 20 °С, при отклонениях от этих параметров должна быть сделана соответствующая коррекция.
С.2.2 Подлежащие тестированию емкость, держатель и наконечник отсасывающего устройства должны быть неиспользованными.
С.З Процедуры теста
С.3.1 Взвешивают пустую емкость.
С.3.2 Если емкость не поставляется в собранном состоянии, соединяют держатель с наконечником отсасывающего устройства в соответствии с инструкцией изготовителя. Если емкость не поставляется как вакуумная, следует произвести отсасывание до номинального объема отсасывания.
С.3.3 Вводят наконечник отсасывающего устройства в воду. Опустошают емкость в течение по меньшей мере 1 мин или наполняют в соответствии с инструкцией изготовителя.
С.3.4 Удаляют держатель и наконечник отсасывающего устройства, осушают поверхность емкости, если необходимо, и вновь взвешивают емкость с точностью до 0,01 г, чтобы определить количество отсасываемой воды.
С.3.5 Удаляют крышку, добавляют воду из пипетки или подобного устройства, чтобы мениск достиг уровня края контейнера.
Примечание — В соответствии с требованиями настоящего стандарта 1000 см3 воды рассматривают как 1000 г.
С.3.6 Определяют минимальное свободное пространство путем вычитания номинальной вместимости из общего объема воды в контейнере. 2
ГОСТ РЕН 14254—2010Приложение D (обязательное)Тест на протекание крышки емкости
D.1 Реактивы и приборы
Тест на протекание крышки емкости
D.1.1 Раствор, приготовленный путем растворения 2,3 г флуоресцеина натрия (уранин, номер CAS 518-47-8)1) в 100 см3 водного раствора 0,15 см3/дм3 хлористого натрия (NaCI, номер CAS 7647-14-5), содержащего 60 г/дм3 декстрана (номер CAS 9004-54-0) или эквивалента.
D.1.2 Вода, не проявляющая признаков флуоресценции при просмотре при облучении ультрафиолетовым светом в темном помещении (D.2.3) наблюдателем с нормальным или корректированным до нормального зрением без увеличения.
D.1.3 Резервуар для раствора флуоресцеина натрия (D.1.1). При тестировании невакуумной емкости резервуар должен быть прикреплен к пластиковой трубке (длина 1 м признана подходящей), снабженной краном. При тестировании вакуумных емкостей резервуар должен оставаться открытым.
D.1.4 Источник ультрафиолетового света, излучающий свет одной длины волны 475 нм.
D.1.5 Миксер роллерного или иного типа, рекомендованный изготовителем контейнера.
D.1.6 Изогнутый гаечный ключ, если требуется.
D.2 Процедуры теста для невакуумных емкостей, предназначенных для хранения при температуре
выше 0 °С
D.2.1 Наполняют резервуар раствором (D.1.1).
D.2.2 Удаляют крышку из емкости, открывают кран на трубке резервуара и направляют струю раствора в емкость, чтобы наполнить ее до номинальной вместимости, стремясь не загрязнить реагентом контейнер и край контейнера. Вставляют крышку в емкость в точном соответствии с указаниями изготовителя. Плотно вставляют колпачок поверх края пробирки.
D.2.3 Наблюдатель с нормальным или корректированным до нормального зрением без увеличения осматривает емкость в темном помещении под ультрафиолетовым светом, чтобы убедиться в отсутствии загрязнения поверхности реактивом. При необходимости смывают загрязнение водой, просматривая под ультрафиолетовым светом, как указано выше.
D.2.4 Помещают емкость в миксер роллерного типа на 2 мин или перевертывают емкость, как рекомендовано изготовителем. Погружают емкость верхней стороной вниз в сосуд, содержащий не более 100 см3 воды, но достаточно, чтобы крышка была полностью покрыта водой. Оставляют на 60 мин при температуре от 15 °С до 25 °С. Удаляют емкость из воды и обследуют под ультрафиолетовым светом, как указано в D.2.3.
D.3 Процедуры теста для невакуумных емкостей, предназначенных для хранения при температуре
0 °С или ниже
D.3.1 Наполняют резервуар раствором (D.1.1).
D.3.2 Удаляют крышку из емкости, открывают кран на трубке резервуара и направляют струю раствора в емкость, чтобы наполнить ее до номинальной вместимости, стремясь не загрязнить реагентом контейнер и край контейнера. Вставляют крышку в емкость в точном соответствии с указаниями изготовителя. Плотно вставляют колпачок поверх края пробирки.
D.3.3 Переворачивают емкость и помещают ее на 2 ч в минимально низкую температуру, указанную изготовителем.
D.3.4 Через 2 ч вынимают емкость и помещают ее, перевернув, в сосуд, содержащий не более 100 см3 воды, но достаточно, чтобы крышка была полностью покрыта водой.
D.3.5 Инкубируют сосуд, содержащий перевернутую емкость, при температуре 37 °С в течение минимум 2 ч или до того времени, пока раствор полностью не растает.
D.3.6 Через 2 ч или когда раствор полностью растает, удаляют сосуд из инкубатора и содержат 2 ч в перевернутом виде при комнатной температуре.
D.3.7 Осматривают под ультрафиолетовым светом (см. D.2.4).
D.4 Процедуры теста для вакуумных емкостей
D.4.1 Наполняют резервуар раствором (D.1.1). 3 4
D.4.2 Присоединяют держатель от наконечника отсасывающего устройства, если они применяются, к емкости в соответствии с инструкцией изготовителя. Откачивают из емкости, если она не поставлена уже вакуумной, до номинальной вместимости.
D.4.3 Вводят наконечник отсасывающего устройств в резервуар и заполняют вакуумную емкость в течение 2 мин или заполняют в соответствии с инструкцией изготовителя.
D.4.4 Отделяют емкость от держателя и наконечника отсасывающего устройства, если они применяются, и наблюдатель с нормальным или корректированным до нормального зрением без увеличения осматривает емкость в темном помещении под ультрафиолетовым светом, чтобы убедиться в отсутствии загрязнения поверхности реактивом. При необходимости смывают загрязнение водой, просматривая под ультрафиолетовым светом, как указано выше.
D.4.5 Помещают емкость в миксер роллерного типа на 2 мин или перевертывают емкость, как рекомендовано изготовителем. Погружают емкость верхней стороной вниз в сосуд, содержащий не более 100 см3 воды, недостаточно, чтобы крышка была полностью покрыта водой. Оставляют на 60 мин при температуре от 15 °С до 25 °С. Удаляют емкость из воды и обследуют под ультрафиолетовым светом, как указано в D.4.4.
10
ГОСТ РЕН 14254—2010
Приложение Е (обязательное)
Тест на прочность емкости, предназначенной для центрифугирования
Е.1 Реактивы и приборы
Е.1.1 Вода, соответствующая требованиям ЕН ИСО 3696 при температуре от 20 °С до 25 °С.
Е.1.2 Центрифуга с поворачивающимся устройством, способным придать основанию ускорение в продольной оси до 3000 gn в течение 10 мин или то ускорение, которое рекомендовано изготовителем емкости.
Примечание — gn = 9,80665 м/с2.
Е.2 Условия выполнения теста
Е.2.1 Тест должен быть выполнен в условиях окружающей среды при 101 кПа и 20 °С, при отклонениях от этих параметров должна быть сделана соответствующая коррекция.
Е.2.2 Подлежащая тестированию емкость должна быть неиспользованной.
Е.З Процедуры теста
Е.3.1 Наполняют емкость водой до номинальной вместимости, используя метод, рекомендованный изготовителем, удаляют и перемещают крышку, когда это необходимо, и отсасывая номинальную вместимость воды в вакуумную емкость, если она поставлена без вакуума.
Е.З.2 Помещают емкость в корзинку центрифуги соответственно инструкции изготовителя и убеждаются, что центрифуга правильно уравновешена.
Е.3.3 Центрифугируют наполненную емкость, подвергая ее основание продольному ускорению при 3000 gn в течение 10 мин или так, как указано изготовителем, исключая время, необходимое для достижения указанного ускорения.
Е.З.4 После того, как центрифуга остановится, осторожно вынимают емкость из корзины центрифуги и обследуют ее для обнаружения повреждений.
11
Приложение ZA (справочное)
Соответствие настоящего стандарта основным требованиям Европейской Директивы 98/79/ЕС
|
Таблица ZA.1 — Соответствие настоящего стандарта Европейской Директиве 98/79/ЕС | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
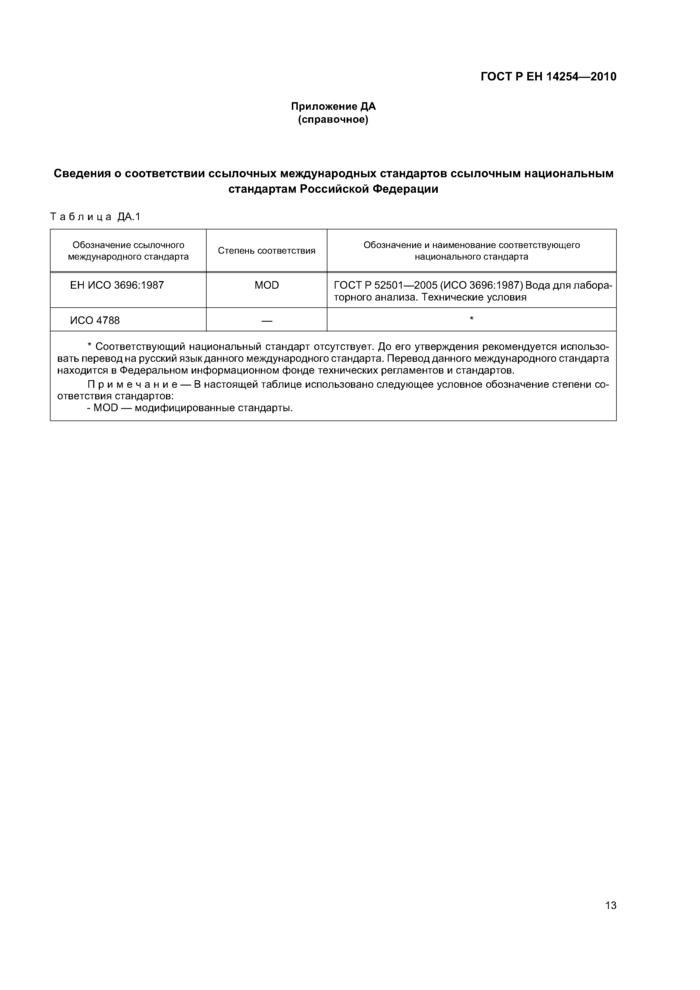
Приложение ДА (справочное)
Сведения о соответствии ссылочных международных стандартов ссылочным национальным
стандартам Российской Федерации
|
Таблица ДА. 1 | ||||||||||||
| ||||||||||||
13
ГОСТ P EH 14254—2010
Библиография
[1]
[2]
[3]
[4]
[5]
[6]
[7]
[8]
[9]
[10]
[11]
[12]
[13]
[14]
[15]
EN 375 EN 550 EN 552 EN 554 EN 829
EN 980 EN 1041 EN 14820 ISO 7000 ISO 15223
UN 602 UN 650
Information supplied by manufacturer with in vitro diagnostic reagents for professional use Sterilization of medical devices — Validation and routine control of ethylene oxide sterilization Sterilization of medical devices — Validation and routine control of sterilizing by irradiation Sterilization of medical devices — Validation and routine control of sterilization by moist heat In vitro diagnostic systems — Transport packages for medical and biological speciments — Requirements, tests
Graphical symbols for use in the labeling of medical devices Information supplied by manufacturer with medical devices Single-use containers for human venous blood specimen collection Graphical symbols for use on equipment — Index and synopsis
Medical devices — Symbols to be used with medical device labels, labeling and information to be supplied
Dangerous Goods Regulations — Packing Instruction 602 Dangerous Goods Regulations — Packing Instruction 650
Council Directive of 27 June 1967 on the approximation of laws, regulations and administrative provisions relating to the classification, packaging and labeling of dangerous substances (67/548/EEC), OJ, 1967, № 1, 196
Council Directive 93/42/EEC of 14 June 1993 concerning medical devices OJ, 1993, № 1, 169
Directive 98/79/EC of the European Parliament and of the Council of 27 October 1998 on in vitro diagnostic medical
devices, 1998, № L 331.
14
УДК 61:006.354 ОКС 11.100 Р20
Ключевые слова: изделия медицинские для диагностики in vitro, емкость, вакуумная емкость, образец
15
Редактор Н.В. Таланова Технический редактор В.Н. Прусакова Корректор М.И. Першина Компьютерная верстка Л.А. Круговой
Сдано в набор 22.08.2011. Подписано в печать 07.09.2011. Формат 60 х 84^. Гарнитура Ариал. Уел. печ. л. 2,32. Уч.-изд. л. 1,74. Тираж 90 экз. Зак. 830.
ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru
Набрано во ФГУП «СТАНДАРТИНФОРМ» на ПЭВМ.
Отпечатано в филиале ФГУП «СТАНДАРТИНФОРМ» — тип. «Московский печатник», 117418 Москва, Нахимовский проспект, 31, к. 2.
ГОСТ РЕН 14254—2010
Содержание
1 Область применения............................................1
2 Нормативные ссылки............................................1
3 Термины и определения..........................................1
4 Материалы.................................................2
5 Номинальная вместимость жидкости...................................3
6 Линии градуировки и заполнения.....................................3
7 Проектирование..............................................3
8 Конструкция.................................................4
9 Стерильность и специальные микробиологические состояния.....................4
10 Добавки..................................................4
11 Информация, предоставляемая изготовителем............................5
Приложение А (обязательное) Тесты номинальной вместимости, градуировочной линии
и минимального свободного пространства для невакуумных емкостей
до и включая 30 см3 номинальной вместимости.....................6
Приложение В (обязательное) Тесты номинальной вместимости, градуировочной линии
и минимального свободного пространства для невакуумных емкостей больше
чем 30 см3 номинальной вместимости..........................7
Приложение С (обязательное) Тесты на втянутый объем и минимальное свободное
пространство для вакуумных емкостей..........................8
Приложение D (обязательное) Тест на протекание крышки емкости..................9
Приложение Е (обязательное) Тест на прочность емкости, предназначенной
для центрифугирования.................................11
Приложение ZA (справочное) Соответствие настоящего стандарта основным требованиям
Европейской Директивы 98/79/ЕС............................12
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов
ссылочным национальным стандартам Российской Федерации...........13
Библиография................................................14
Введение
Хотя персонал медицинских лабораторий, постоянно обрабатывая потенциально инфицированные образцы, предпринимает соответствующие защитные меры и использует безопасные методики, положения Европейской Директивы 98/79/ЕС требуют сведения до минимума риска, связанного с возникновением инфекции, вызванной медицинскими изделиями для диагностики in vitro, содержащими инфицированные или потенциально инфицированные материалы. Данное требование Европейской Директивы связано с разработкой и производством медицинских изделий для диагностики in vitro. Изготовители обязаны обеспечить такие конструктивные особенности и производственные процедуры, которые сводят риск применения изделия до минимума.
Директива не устанавливает требований к следующим аспектам:
- общие вопросы защиты работников и меры, которые должны быть предприняты, когда подвергаются обработке в лаборатории или местах производства инфицированные или потенциально инфицированные материалы;
- транспортирование инфицированных товаров;
- пути и процессы утилизации.
IV
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИИЗДЕЛИЯ МЕДИЦИНСКИЕ ДЛЯ ДИАГНОСТИКИ IN VITRO Одноразовые емкости для сбора образцов у человека (кроме крови)
In vitro diagnostic medical devices. Single-use receptacles for the collection of specimens,
other than blood, from humans
Дата введения — 2012—03—01
1 Область применения
Настоящий стандарт устанавливает требования и методы исследования для одноразовых вакуумных и невакуумных емкостей, предназначенных изготовителями для первичного размещения и сохранения образцов, кроме крови, взятых из тела человека в целях диагностического исследования in vitro.
Примечание 1 — Требования и методы исследования для одноразовых вакуумных и невакуумных емкостей для образцов венозной крови установлены ЕН 14820.
Примечание 2 — Несмотря на то, что желательно, чтобы емкость была сконструирована таким образом, чтобы содержимое не выливалось при открывании емкости, настоящий стандарт не устанавливает процедуры исследования для этой цели, поскольку невозможно предложить объективный и воспроизводимый тест.
Настоящий стандарт не определяет требования к иглам для взятия образцов, держателям игл или другим приспособлениям, используемым вместе с емкостями для образцов.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие нормативные документы:
ЕН ИСО 3696 Вода для использования в лабораторных исследованиях (ИСО 3696:1987)
ИСО 4788 Лабораторная стеклянная посуда. Градуированные мерные цилиндры
3 Термины и определения
В настоящем стандарте использованы следующие термины с соответствующими определениями:
3.1 емкость (receptacle): Сосуд, вакуумный или невакуумный, предназначенный для размещения образца, с приспособлениями и добавками, закрытый крышкой.
3.2 вакуумная емкость (evacuated receptacle): Емкость, предназначенная для сбора образца с помощью вакуума, который или уже создан изготовителем, или создан пользователем непосредственно перед сбором образца жидкости.
3.3 контейнер (container): Часть емкости для сбора образца без крышки и приспособлений, содержащая образец.
Примечание — В зависимости от предполагаемого применения часть емкости без крышки, содержащая образец, может также носить название «пробирка», «бутылка», «флакон» или иные подобные названия.
3.4 крышка (closure): Компонент, с помощью которого закрывают контейнер.
3.5 принадлежность емкости (receptacle accessory): Компонент внутри емкости, предназначенный изготовителем для того, чтобы способствовать сбору или смешиванию, или разделению образца.
Пример — Ложки для проб, предназначенные для сбора плотных образцов.
Издание официальное
3.6 держатель и наконечник для всасывания (holder and suction tip): Устройство, которое предназначено для присоединения к вакуумной емкости для облегчения сбора жидкого образца.
3.7 первичная упаковка (primary pack): Наименьшая упаковка емкости.
3.8 внутренность емкости (receptacle interior): Внутренняя поверхность контейнера емкости и поверхность любой принадлежности емкости, обращенная к образцу.
3.9 добавка (additive): Вещество, отличающееся от неотделимых от поверхности веществ, которыми она обработана, помещенное внутрь емкости для облегчения сохранения образца или предназначенное для реакции с образцом, для выполнения предназначенного анализа.
Пример — Плотная питательная среда.
3.10 номинальная вместимость жидкости (nominal liquid capacity): Объем образца, который емкость может вместить плюс объем любой добавки.
Примечание — Этот объем указан на этикетке и/или в инструкции по применению.
3.11 свободное пространство (free space): Избыточная вместимость или верхнее пространство, которое позволяет адекватно перемешивать содержимое емкости.
Примечание — Этот объем определен тестами минимального свободного пространства, описанными в приложениях А, В и С.
3.12 линия номинального заполнения (nominal fill line): Отметка на контейнере или его этикетке, указывающая номинальную вместимость жидкости контейнера.
Примечание — Контейнер может быть помечен более чем одной линией номинального заполнения.
3.13 заполняемая вместимость (filling capacity): Объем жидкого образца, необходимый для достижения требуемого соотношения добавки и образца.
3.14 линия минимального заполнения (minimum fill line): Отметка на контейнере или его этикетке, указывающая минимальный объем образца, необходимый для получения правильного результата теста, для выполнения которого предназначен образец.
3.15 линия максимального заполнения (maximum fill line): Отметка на контейнере или его этикетке, указывающая максимальный объем образца, позволяющий получить правильный результат теста, для выполнения которого предназначен образец.
3.16 градуировочная линия (graduation line): Отметка на контейнере или его этикетке, позволяющая установить объем жидкого образца.
Примечание — На контейнере могут быть нанесены более одной градуировочной линии.
3.17 втянутый объем (draw volume): Количество жидкого образца, втянутое в вакуумную емкость.
3.18 срок годности (expire date): Дата, позднее которой емкость не должна использоваться.
3.19 закручивание крышки (closure torque): Крутящее усилие, определенное изготовителем, необходимое для закручивания крышки с винтовой нарезкой, с помощью гаечного ключа, достаточное для герметичного закрытия емкости.
3.20 гравиметрический анализ (gravimetric analysis): Метод определения объема жидкости путем ее взвешивания и коррекции по относительной плотности.
3.21 волюметрический анализ (volumetric analysis): Метод определения объема жидкости с помощью бюретки.
3.22 образец (specimen): Биологический материал, полученный для определения свойств или измерения одной или нескольких величин.
4 Материалы
4.1 Если емкость предназначена для сбора образца с целью специфического исследования, в отношении которого материал крышки или контейнера, или внутреннего покрытия, или добавки, или принадлежностей может повлиять на окончательный результат исследования, тогда изготовитель должен указать в прилагаемой инструкции, или на этикетке, или на упаковке (см. также 11.7) максимальный объем загрязнения данным веществом и применяемый аналитический метод. За валидацию пригодности материала в отношении предполагаемого специфического использования емкости несет ответственность изготовитель.
Примечание 1 — Настоящий стандарт не устанавливает процедуру валидации пригодности материала.
ГОСТ Р ЕН 14254-2010
Примечание 2 —Для некоторых редко применяемых исследований пределы интерференции могут быть не установлены, и пользователю рекомендуется проконсультироваться с изготовителем.
Примечание 3 — Контейнер должен быть изготовлен из материала, который позволяет ясно видеть содержимое контейнера при визуальном рассмотрении наблюдателем с нормальным или коррелированным до нормального зрением без увеличения при равномерном освещении от 300 до 700 лк, если освещение видимым или ультрафиолетовым светом не вызывает разрушения содержимого.
Примечание 4 — Если контейнер сделан из материала, который не позволяет видеть содержимое, чтобы его рассмотреть, крышку можно открыть.
4.2 При визуальном изучении материал емкости должен быть свободен от постороннего содержимого.
4.3 Емкости, содержащие добавки, поддерживающие микробы, должны быть подвергнуты вали-дированному процессу удаления микробного загрязнения от добавок или внутренней поверхности емкости. За валидацию этого процесса несет ответственность изготовитель.
Примечание — Относительно валидации и рутинного контроля процедуры стерилизации см. ЕН 550, ЕН 552 и ЕН 554.
5 Номинальная вместимость жидкости
5.1 Для невакуумных емкостей с номинальной вместимостью жидкости до и включая 30 см5 и для всех вакуумных емкостей при тестировании в соответствии с методами, указанными в приложениях А или С, объем добавленной воды вместе с объемом имеющейся добавки должен быть в пределах + 10 % номинальной вместимости.
5.2 Для невакуумных емкостей с номинальной вместимостью жидкости больше, чем 30 см5, объем добавленной воды должен быть в пределах + 10 % номинальной вместимости при исследовании, как указано в приложении В.
5.3 Для емкостей с добавкой или для емкостей, предназначенных для сбора жидких суспензий, которые могут оседать, должна быть предусмотрена возможность смешивания. Если свободное пространство предназначено для облегчения смешивания, этого пространства должно быть достаточно для смешивания механическим или ручным способом при исследовании в соответствии с приложениями А, В и С. За валидацию адекватности процесса смешивания несет ответственность изготовитель.
Примечание — Настоящий стандарт не устанавливает процедуру валидации.
6 Линии градуировки и заполнения6.1 Градуировочные линии
При тестировании невакуумных емкостей любой вместимости с градуировочными линиями в соответствии с методами, указанными в приложениях А и В, объем воды должен быть от 90 % до 110 % объема, указанного градуировочной линией.
6.2 Линия минимального заполнения
Вакуумные емкости, которые имеют линию минимального заполнения на контейнере или этикетке контейнера, следует заполнять таким образом, чтобы мениск жидкости достигал или превышал положение линии, когда тестирование производят в соответствии с методом, указанным в приложении С.
6.3 Линия максимального заполнения
Вакуумные емкости, которые имеют линию максимального заполнения на контейнере или этикетке контейнера, следует заполнять таким образом, чтобы мениск жидкости достигал, но не превышал положение линии, когда тестирование производят в соответствии с методом, указанным в приложении С.
7 Проектирование
7.1 Крышка не должна пропускать жидкость при тестировании на протекание по методу, указанному в приложении D. Емкость должна проходить тест на протекание, если не наблюдается флюоресценции.
Примечание — Настоящий стандарт не устанавливает процедуру теста, если емкости предназначены изготовителем для хранения в жидком азоте.
7.2 Когда крышка должна быть удалена, чтобы дать доступ к содержимому емкости, должно быть предусмотрено, насколько это может быть обосновано и практически осуществлено, чтобы она могла быть удалена с помощью захвата пальцами или механическими средствами таким образом, чтобы часть крышки, которая может быть загрязнена из-за контакта с образцом, не могла коснуться пальцев или механического устройства для открывания.
7.3 Видимость образца не должна быть затруднена наличием этикетки, надпечатки или маркировки.
7.4 Неиспользованная и сухая этикетка должна быть пригодна для маркировки с помощью письменного приспособления, как указано изготовителем.
7.5 Маркировка и этикетка на емкости должны оставаться закрепленными и читаемыми после пребывания на воздухе при (4 + 1) °С не менее, чем 72 ч.
7.6 Если изготовитель утверждает, что емкость пригодна для хранения при температурах сверх нормальных пределов окружающей среды, этикетка, использованный адгезив и маркировка должны сохраняться на своем месте, в сухом состоянии и быть читаемыми при крайних температурных пределах, указанных изготовителем в течение по меньшей мере 72 ч при каждом установленном пределе.
8 Конструкция
8.1 Емкости должны выдерживать четыре цикла удаления и закручивания крышки в соответствии с инструкцией изготовителя без поломок, трещин, изгибов и других видимых дефектов при проведении тестов в соответствии с приложениями А, В, С и D. Когда первоначальное открытие емкости привело к разрушению крышки, данные требования должны быть применены к следующей крышке.
Примечание — Трудно подтвердить характеристики одиночной процедуры теста на прочность. Приведенные выше требования предполагают имитацию механического стресса, связанного с наполнением емкости, хранением, транспортированием и удалением пробы. Требования для транспортирования образца в емкости см. [11], [12].
8.2 Емкости, предназначенные для центрифугирования, должны выдерживать минимальное ускорение в 3000 g (или ускорение, указанное изготовителем) в продольной оси без поломок, трещин, изгибов и других видимых дефектов и тестирование в соответствии с приложением Е.
8.3 При визуальном изучении емкость не должна иметь торчащего острого края, выступа или шероховатости поверхности, способной порезать, проколоть или порвать палец или перчатки пациента или пользователя.
9 Стерильность и специальные микробиологические состояния
9.1 Если изготовитель утверждает, что внутренняя поверхность неоткрытой и неиспользованной емкости или целая емкость стерильны или находятся в специальном микробиологическом состоянии, внутренность контейнера и любая принадлежность или добавка должны быть подвергнуты валидиро-ванному процессу, предназначенному для достижения данного утверждения. За валидацию процесса стерилизации несет ответственность изготовитель.
Примечание — Относительно валидации и рутинного контроля см. ЕН 550, ЕН 552 и ЕН 554.
9.2 Стерильность обязательна, когда система сбора предназначена для культуры образца и когда емкость содержит питательную среду.
10 Добавки
10.1 Действительное количество добавки в каждой емкости должно быть в пределах, установленных изготовителем.
10.2 Максимальный допускаемый доверительный интервал жидкой добавки должен быть от 90 % до 110%. 6
ГОСТ РЕН 14254—2010
Примечание — Количество добавки в емкости должно быть определено, если соответствуют условия, с поправкой на относительную плотность любой жидкости путем гравиметрического анализа с использованием весов с точностью до 0,001 г.
10.3 За валидацию выбора добавки, включая питательную среду, ее эффективность и специфицированные пределы концентрации, несет ответственность изготовитель.
Примечание — Настоящий стандарт не устанавливает метод тестирования.
10.4 Изготовитель должен обеспечить пригодность физической формы охарактеризованной добавки для своего предназначения.
Примечание — Добавки могут быть внесены в различных физических формах, например в виде раствора, сухого остатка из высушенного раствора, лиофилизированного или в виде порошка.
11 Информация, предоставляемая изготовителем
11.1 К каждой емкости должна прилагаться информация, необходимая для правильного использования с учетом умений и знаний потенциального пользователя и позволяющая идентифицировать изготовителя. Эта информация должна быть размещена на самой емкости, если позволяет пространство, и/или в инструкции по применению, и/или на первичной упаковке.
Примечание — Предполагается, что изготовители могут использовать электронные средства, например Интернет, как дополнительные способы сообщения практической и функциональной информации, касающейся продукта, конечному пользователю.
11.2 Если это практично и соответствует условиям, информация, необходимая для правильного и безопасного использования, может быть размещена на самой емкости и/или, если возможно, на первичной упаковке. Если размещение всей информации на емкости не практично, информация должна быть размещена на упаковке и/или в инструкции по применению, предоставляемой с одной или несколькими емкостями.
11.3 Если емкость поставляется специально для определения или обнаружения определенного вещества, максимальное значение уровня загрязнения веществом должно быть нанесено непосредственно на емкость или на этикетку, если возможно, и/или в инструкцию по применению, и/или на первичную упаковку.
11.4 Если это соответствует условиям, на этикетку должны быть нанесены следующие детали, которые могут быть изображены в виде символов:
a) наименование или торговая марка и адрес изготовителя;
b) детали, определенно необходимые пользователю для идентификации емкости и содержимого упаковки;
c) когда это соответствует условиям, слово «стерильно» или утверждение, указывающее на специальное микробиологическое состояние или состояние чистоты;
d) код партии, с предшествующим словом «ЮТ» или номер серии;
e) если необходимо, указание даты (год, месяц, при необходимости, число), до которой емкость или ее часть могут быть безопасно использованы без ухудшения функциональных характеристик;
f) в случае оценки функциональных характеристик — слова «только для оценки функциональных характеристик»;
д) когда это соответствует условиям, утверждение, указывающее использование емкости in vitro;
h) любые особые условия хранения и/или обработки;
i) когда это приемлемо, любые особые оперативные инструкции;
j) когда это приемлемо, идентичность и концентрация любой добавки;
k) номинальная вместимость жидкости в емкость;
l) линия заполнения, когда это необходимо;
т) соответствующие предостережения или необходимые предосторожности.
11.5 Если предполагаемое использование емкости не ясно для пользователя, изготовитель должен ясно указать предполагаемое применение в инструкции по применению или, если это соответствует условиям, на этикетке.
11.6 Если емкость пригодна для хранения при температуре ниже 0 °С, это должно быть ясно указано на контейнере или на этикетке, и/или в инструкции по применению, и/или на первичной упаковке.
11.7 Если емкость пригодна для хранения в жидком азоте, это должно быть ясно указано на контейнере или на этикетке, и/или в инструкции по применению, и/или на первичной упаковке. 7
Приложение А (обязательное)Тесты номинальной вместимости, градуировочной линии и минимального свободного пространства для невакуумных емкостей до и включая 30 см3 номинальной вместимости
А.1 Реактивы и приборы
А.1.1 Вода, соответствующая требованиям ЕН ИСО 3696 при температуре от 20 °С до 25 °С.
А.1.2 Бюретка, градуированная по 0,1 см3 (точно до ±0,1 см3), вместимостью 50 см3 с краном внизу или сбоку.
А.2 Условия выполнения теста
А.2.1 Тест должен быть выполнен в условиях окружающей среды при 101 кПа и 20 °С, при отклонениях от этих параметров должна быть сделана соответствующая коррекция.
А.2.2 Подлежащая тестированию емкость должна быть неиспользованной и иметь линию заполнения, или градуировочную линию.
А.З Процедуры теста
А.3.1 Закрывают кран бюретки и заполняют ее до нулевой отметки.
А.3.2 Удаляют пробку емкости и помещают контейнер под струю бюретки.
А.3.3 Осторожно направляют струю воды в контейнер до положения мениска у первой градуировочной линии, при ее наличии, или линии заполнения, затем закрывают кран.
А.3.4 Отмечают объем воды, выпущенной из бюретки, с точностью до ± 0,1 см3.
А.3.5 Если контейнер имеет градуировочную линию, повторяют этапы А.3.3 и А.3.4 для каждой градуировочной линии до достижения мениском положения линии заполнения. Отмечают объем с точностью до ± 0,1 см3.
А.3.6 Для емкостей с жидкой добавкой ее объем должен быть учтен.
А.3.7 Продолжают заполнение водой из бюретки до верхнего края контейнера и отмечают объем выпущенной из бюретки воды с точностью до ± 0,1 см3. Определяют минимальное свободное пространство путем вычитания номинальной вместимости из общего объема воды в контейнере. 8
1
2
3
^ CAS номер — номер Chemical Abstract Service Registry.
4
5
6
7
8