СТБ ISO 8069-2012
Молоко сухое. Определение содержания молочной кислоты и лактатов
Купить СТБ ISO 8069-2012 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает ферментный метод определения содержания молочной кислоты и лактатов во всех видах сухого молока.
Оглавление
1 Область применения
2 Термины и определения
3 Сущность метода
4 Реактивы
5 Аппаратура
6 Отбор проб
7 Приготовление
7.1 Подготовка пробы
7.2 Навеска
7.3 Контрольное испытание
7.4 Приготовление раствора и удаление белка
8 Процедура
8.1 Проверка активности реактивов
8.2 Определение
9 Вычисление и представление результатов
9.1 Вычисление
9.2 Представление результатов
10 Прецизионность
10.1 Межлабораторные испытания
10.2 Повторяемость
10.3 Воспроизводимость
11 Протокол испытания
Приложение А (обязательное) Правила надлежащей лабораторной практики (GLP) для проведения ферментного анализа
Библиография
| Дата введения | 01.01.2021 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Завершение срока действия | 01.03.2014 |
| Актуализация | 01.01.2021 |
Организации:
| 20.04.2012 | Утвержден | Госстандарт Республики Беларусь | 21 |
|---|---|---|---|
| Разработан | БелГИСС | ||
| Издан | БелГИСС | 2012 г. |
Dried milk. Determination of content of lactic acid and lactates
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6
стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
МОЛОКО СУХОЕ
Определение содержания молочной кислоты и лактатов
МАЛАКО СУХОЕ
Вызначэнне змяшчэння малочнай Хелаты i лактатау
(ISO 8069:2005, ЮТ)
Издание официальное
Г осстандарт Минск
(п5
УДК 637.143.07:637.146.4(083.74)(476) МКС 67.100.10 КП 03 ЮТ
Ключевые слова: сухое молоко, молочная кислота, лактаты
Предисловие
Цели, основные принципы, положения по государственному регулированию и управлению в области технического нормирования и стандартизации установлены Законом Республики Беларусь «О техническом нормировании и стандартизации».
1 ПОДГОТОВЛЕН научно-производственным республиканским унитарным предприятием «Белорусский государственный институт стандартизации и сертификации» (БелГИСС)
ВНЕСЕН Госстандартом Республики Беларусь
2 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 20 апреля 2012 г. № 21
3 Настоящий стандарт идентичен международному стандарту ISO 8069:2005 Dried milk - Determination of content of lactic acid and lactates (Молоко сухое. Определение содержания молочной кислоты и лактатов).
Международный стандарт разработан техническим комитетом по стандартизации ISO/TC 34 «Сельскохозяйственные пищевые продукты» Международной организации по стандартизации (ISO).
Перевод с английского языка (еп).
Официальный экземпляр международного стандарта, на основе которого подготовлен настоящий государственный стандарт, имеется в Национальном фонде ТИПА.
Степень соответствия — идентичная (ЮТ)
4 ВВЕДЕН ВПЕРВЫЕ
© Госстандарт, 2012
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
Издан на русском языке
А.3.5 Не измеряют коэффициент поглощения кюветы при испытании пробы или в контрольном испытании относительно пустой кюветы (из-за рассеивания света).
А.3.6 Содержимое кюветы перемешивают пластмассовой лопаткой или закрывая кювету парафильмом и осторожно переворачивая.
А.3.7 Удаляют воздушные пузырьки со стенок кюветы, используя лопатку. Оптическую сторону кюветы стараются не царапать.
А.3.8 Для измерения при испытании пробы и контрольном испытании всегда используют одинаковые кюветы для измерения.
А.3.9 Стеклянные или кварцевые кюветы всегда устанавливают в держателе в одинаковое положение. Для этой цели помечают одну оптическую сторону кюветы.
А.4 Фотометры и спектрофотометры
А.4.1 Используют спектрофотометр (пропускная способность <10 нм), фильтр-фотометр, оснащенный интерферирующим фильтром (пропускная способность <10 нм), или фотометр линейного спектра, оснащенный ртутной лампой. Измерения, осуществляемые с использованием спектрофотометра или фильтр-фотометра, должны проводиться при максимуме поглощения NADH или NADPH, то есть 340 нм. Измерения, осуществляемые с использованием фотометра линейного спектра с ртутной лампой, должны проводиться при 365 нм или 334 нм.
Примечание - Молярные коэффициенты поглощения NADH и NADPH, измеренные при 334 нм, 340 нм и 365 нм,
составляют:
a) NADH и NADPH при 334 нм (Нд): 6,18 х ю6 см2/моль;
b) NADH и NADPH при 340 нм: 6,3 х ю6 см2/моль;
c) NADPH при 365 нм (Нд): 3,5 хЮ6 см2/моль;
d) NADH при 365 нм: 3,4 х ю6 см2/моль.
А.4.2 Между коэффициентом поглощения и концентрацией NADH или NADPH должна существовать линейная зависимость в пределах коэффициента поглощения 2,0. Линейную зависимость проверяют следующим образом:
a) отбирают пипеткой 2,00 мл дистиллированной воды в кювету и измеряют коэффициент поглощения А0 относительно воды;
b) отбирают пипеткой 0,10 мл раствора NADH (0,5 мг/мл) в кювету; перемешивают содержимое ячейки и измеряют коэффициент поглощения А1.
Вычисляют уменьшенный коэффициент поглощения Ат, по формуле
д1=(А-д))х|1. (1)
Повторяют процедуру проверки линейной зависимости 14 раз, как описано выше.
После каждой пары измерений вычисляют уменьшенный коэффициент поглощения Ат по формуле
А»=(А-Д)х-' (2)
3,0
где Ап - коэффициент поглощения, полученный при измерении л;
V - объем содержимого ячейки при измерении п.
Для каждого измерения строят график зависимости объема раствора NADH, находящегося в кювете, от соответствующего уменьшенного коэффициента поглощения. Корреляционное значение измерений должно быть > 0,99.
А.5 Автоматические пипетки и другие пипетки-дозаторы
А.5.1 Автоматические пипетки и другие пипетки-дозаторы используются согласно инструкциям изготовителя.
А.5.2 Для каждой пипетки используются соответствующие наконечники.
А.5.3 Характеристики вместимости и повторяемости автоматических пипеток и других пипеток-дозаторов периодически проверяют (например, ежемесячно) следующим образом.
Мензурку с водой взвешивают на протяжении времени t. Пипеткой отбирают или переливают 1 х порцию воды в мензурку и взвешивают ровно (t + 1) мин после первого взвешивания. Повторяют
СТБ ISO 8069-2012
процедуру отбора пипеткой или дозирования девять раз. Взвешивают мензурку без отбора пипеткой или дозирования в момент (t + 11), (t + 12), (t + 13), (t + 14) и (t + 15) мин. Вычисляют на основе данных взвешиваний потери на испарение в минуту. Вычисляют вместимость и повторяемость пипетки или пипетки-дозатора, учитывая потерю воды на испарение.
А.5.4 Теплопередача от ладони руки при продолжительном использовании может повлиять на вместимость некоторых автоматических пипеток.
Находят и отбраковывают пипетки, имеющие данную зависимость, посредством процедуры, описанной в А.5.3.
А.5.5 Непосредственно перед применением несколько раз ополаскивают наконечник пипетки рас-твором/суспензией, которую необходимо отобрать. Для каждого испытуемого раствора используют новый наконечник для пипетки.
А.5.6 Пипеткой отбирают буферный, ферментный, коферментный и испытуемый растворы, помещая наконечник пипетки как можно глубже в различные углы кюветы.
Небольшие количества ферментных растворов/суспензий 10-50 мкп могут дозироваться на лопатку, которую опускают в кювету и перемешивают с помощью нее содержимое ячейки.
А.5.7 Необходимо избегать загрязнения.
А.6 Дополнительная полезная информация
А.6.1 Возможность нарушения и грубых ошибок проверяют посредством определения коэффициентов поглощения двух растворов с различными концентрациями анализируемого вещества. Полученные коэффициенты поглощения должны быть пропорциональны концентрациям анализируемого вещества.
А.6.2 Для проверки ферментной (ых) реакции (й) используют стандарт. Стандарт должен рассматриваться, как общепринятый стандарт.
Примечание - Эталонные образцы подтвержденной чистоты могут быть получены от организаций, таких как
Национальный институт стандартов и технологий (NIST) или Европейское бюро по стандартам (BCR).
А.6.3 Испытание на восстановление выполняют в присутствии испытуемого раствора. Количество добавленного анализируемого вещества должно быть приблизительно таким же, как и количество анализируемого вещества, уже присутствующего в испытуемом растворе.
А.6.4 Для каждой кюветы используют одну пластмассовую лопатку, при этом каждую лопатку используют только один раз.
Примечание - Допустимо не учитывать количество жидкости, оставшейся на лопатке.
9
| ||||||||||
|
водимости стандартного метода измерения) |
[5] Leenheer J. and Jans J.A. Bulletin of the IDF, No. 207, 1986, pp. 122 - 132 Leenheer J. и Jans J.A., (Бюллетень IDF)
10
Ответственный за выпуск В. Л. Гуревич
Сдано в набор 17.05.2012. Подписано в печать 29.05.2012. Формат бумаги 60x84/8. Бумага офсетная. Гарнитура Arial. Печать ризографическая. Уел. печ. л. 1,62 Уч.-изд. л. 0,80 Тираж экз. Заказ
Издатель и полиграфическое исполнение: Научно-производственное республиканское унитарное предприятие «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) ЛИ № 02330/0552843 от 08.04.2009. ул. Мележа, 3, комн. 406, 220113, Минск.
СТБ ISO 8069-2012Содержание
1 Область применения............................................................................................................................1
2 Термины и определения......................................................................................................................1
3 Сущность метода..................................................................................................................................1
4 Реактивы................................................................................................................................................1
5 Аппаратура............................................................................................................................................2
6 Отбор проб............................................................................................................................................3
7 Приготовление......................................................................................................................................3
7.1 Подготовка пробы..........................................................................................................................3
7.2 Навеска...........................................................................................................................................3
7.3 Контрольное испытание................................................................................................................3
7.4 Приготовление раствора и удаление белка................................................................................3
8 Процедура.............................................................................................................................................3
8.1 Проверка активности реактивов...................................................................................................3
8.2 Определение..................................................................................................................................4
9 Вычисление и представление результатов.......................................................................................5
9.1 Вычисление....................................................................................................................................5
9.2 Представление результатов.........................................................................................................6
10 Прецизионность....................................................................................................................................6
10.1 Межлабораторные испытания....................................................................................................6
10.2 Повторяемость.............................................................................................................................6
10.3 Воспроизводимость.....................................................................................................................6
11 Протокол испытания.............................................................................................................................6
Приложение А (обязательное) Правила надлежащей лабораторной практики (GLP)
для проведения ферментного анализа.........................................................................7
Библиография..........................................................................................................................................10
III
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬМОЛОКО СУХОЕ Определение содержания молочной кислоты и лактатовМАПАКО СУХОЕ Вызначэнне змяшчэння малочнай к1слаты i лактатау
МАПАКО СУХОЕ Вызначэнне змяшчэння малочнай к1слаты i лактатау
Dried milk
Determination of content of lactic acid and lactates
Дата введения 2013-01-011 Область применения
Настоящий стандарт устанавливает ферментный метод определения содержания молочной кислоты и лактатов во всех видах сухого молока.
2 Термины и определения
В настоящем стандарте применяют следующий термин с соответствующим определением:
2.1 содержание молочной кислоты и лактатов (lactic acid and lactates content): масса веществ, определенная посредством процедуры, которая установлена в настоящем стандарте.
Примечание - Выражается в миллиграммах молочной кислоты на 100 г сухого обезжиренного остатка.
3 Сущность метода
Пробу сухого молока восстанавливают в теплой воде, осаждают жир и белки, фильтруют пробу. Полученный фильтрат обрабатывают ферментами и биохимическими реактивами, добавляемыми одновременно, но действующими последовательно:
a) L-лактат дегидрогеназа (L-LDH) и D-лактат дегидрогеназа (D-LDH) в присутствии никотинамид-аденин-динуклеотида (NAD) окисляют лактат до пирувата и восстанавливают NAD до NADH;
b) глутамат-пируват-трансаминаза (GPT) в присутствии L-глутамата видоизменяет пируват в L-аланин и преобразует L-глутамат в а-кетоглутарат.
Измеряют массовую долю образовавшегося NADH, эквивалентную массовой доле молочной кислоты и лактатов в пробе, посредством спектрофотометрического измерения при длине волны 340 нм.
4 Реактивы
Все реактивы должны быть аналитического качества. Вода, используемая в приготовлении растворов ферментов, должна быть дистиллирована как минимум дважды и без примесей. Вода, используемая в других целях, должна быть дистиллирована или иметь равнозначную чистоту.
4.1 Раствор гексацианоферрата (II) калия, c(K4[Fe(CN)6]-3H20) = 35,9 г/л.
Растворяют 35,9 г тригидрата гексацианоферрата (II) калия в воде. Доводят объем раствора водой до 1000 мл и перемешивают.
4.2 Раствор сульфата цинка, c(ZnS04-7H20) = 71,8 г/л.
Растворяют 71,8 г гептагидрата сульфата цинка в воде. Доводят объем раствора водой до 1000 мл и перемешивают.
4.3 Растворы гидроксида натрия.
4.3.1 Раствор гидроксида натрия I, c(NaOH) = 10 моль/л.
Растворяют 400 г гидроксида натрия в воде. Доводят объем раствора водой до 1000 мл и перемешивают.
4.3.2 Раствор гидроксида натрия II, c(NaOH) = 0,1 моль/л.
Растворяют 4,0 г гидроксида натрия в воде. Доводят объем раствора водой до 1000 мл и перемешивают.
4.4 Раствор глицерина (С3Н803), с объемным содержанием глицерина 50 %.
Издание официальное
4.5 Раствор сульфата аммония, c[(NH4)2S04] = 3,2 моль/л.
Растворяют 422,84 г сульфата аммония в воде. Доводят объем раствора водой до 1000 мл и перемешивают.
4.6 Буферный раствор, pH 10.
Растворяют 7,92 г глицилглицина (C4H8N2O3) и 1,47 г L-глутаминовой кислоты (C5HgN04) приблизительно в 80 мл воды. Устанавливают pH до (10,0 ± 0,1) при температуре 20 °С раствором гидроксида натрия I (4.3.1). Доводят объем раствора водой до 1000 мл и перемешивают.
Раствор устойчив 3 мес при температуре хранения в холодильной камере от 0 °С до + 5 °С.
4.7 Раствор никотинамид-аденин-динуклеотида (NAD).
Растворяют 350 мг никотинамид-аденин-динукпеотида (C21H27N7O14P2) в 10 мл воды.
Раствор устойчив 4 нед при температуре хранения в холодильной камере от 0 °С до + 5 °С. Во время использования сосуд с раствором должен быть погружен в емкость с колотым льдом.
4.8 L-лактат дегидрогеназа (L-LDH), суспензия, полученная из мышечной ткани свиньи.
Растворяют 10 мг суспензии L-лактат дегидрогеназы в 1 мл раствора глицерина (4.4). Значение
pH полученной суспензии должно быть приблизительно 7. Удельная активность суспензии L-лактат дегидрогеназы (L-LDH, ЕС 1.1.1.27) должна быть не менее 5500 единиц/мл при 25 °С. При несоответствии установленным требованиям готовят другую суспензию L-LDH.
Суспензия L-LDH устойчива 12 мес при температуре хранения в холодильной камере от 0 °С до +5 °С. Во время использования сосуд с раствором должен быть погружен в емкость с колотым льдом.
4.9 D-лактат дегидрогеназа (D-LDH), суспензия, полученная из Lactobacillus leichmannii.
Растворяют 5 мг суспензии D-LDH в 1 мл раствора сульфата аммония (4.5). Значение pH полученной суспензии должно быть приблизительно 6. Удельная активность суспензии D-лактат дегидрогеназы (D-LDH, ЕС 1.1.1.28) должна быть не менее 1500 единиц/мл при 25 °С. При несоответствии установленным требованиям готовят другую суспензию D-LDH.
Суспензия D-LDH устойчива 12 мес при температуре хранения в холодильной камере от 0 °С до +5 °С. Во время использования сосуд с раствором должен быть погружен в емкость с колотым льдом.
4.10 Глутамат-пируват-трансаминаза (GPT), суспензия, полученная из свиного сердца.
Растворяют 20 мг суспензии GPT в 1,0 мл раствора сульфата аммония (4.5). pH полученной суспензии должен быть приблизительно 7. Удельная активность суспензии глутамат-пируват-трансами-назы (GPT, ЕС 2.6.1.2) должна быть не менее 1600 единиц/мл при 25 °С. При несоответствии установленным требованиям готовят другую суспензию GPT.
Добавляют 1,0 мл раствора сульфата аммония (4.5) в 1 мл суспензии, содержащей 20 мг GPT, и перемешивают. Центрифугируют полученные 2,0 мл суспензии, содержащей 10 мг GPT/мл, с радиальным ускорением 4000 g в течение 10 мин. Переливают 1,0 мл чистой надосадочной жидкости и отбрасывают, а оставшуюся суспензию используют.
Суспензия GPT устойчива 12 мес при температуре хранения в холодильной камере от 0 °С до + 5 °С. Во время использования сосуд с раствором должен быть погружен в емкость с колотым льдом.
4.11 Раствор L-лактата лития.
Растворяют 50 мг L-лактата лития (C3H503Li) в воде. Доводят объем раствора водой до 500 мл и перемешивают.
4.12 Раствор D-лактата лития.
Растворяют 50 мг D-лактата лития (C3H503Li) в воде. Доводят объем раствора водой до 500 мл и перемешивают.
5 Аппаратура
Используют стандартное лабораторное оборудование, в том числе, следующее:
5.1 Аналитические весы с точностью до 1 мг и ценой деления 0,1 мг.
5.2 Мензурка вместимостью 50 мл.
5.3 Градуированный цилиндр вместимостью 50 мл.
5.4 Мерные колбы с одной отметкой вместимостью 100 мл.
5.5 Пипетки вместимостью 0,02 мл, 0,05 мл, 0,2 мл, 1,0 мл и 2,0 мл.
5.6 Градуированные пипетки вместимостью 5 мл и 10 мл, с ценой деления 0,1 мл.
5.7 Стеклянные фильтровальные воронки диаметром 7 см.
5.8 Фильтровальная бумага средней плотности, диаметром 15 см, не содержащая молочной кислоты и лактатов.
5.9 Стеклянная палочка.
2
СТБ ISO 8069-2012
5.10 Пластмассовые лопатки, способные перемешивать пробу ферментной смеси в спектрометрической кювете.
ути п см.
ТМ 1)
5.11 Спектрофотометр, способный измерять при длине волны 340 нм, оборудованный кюветами с оптической длиной п
5.12 Парафильм.6 Отбор проб
В лабораторию предоставляют представительную пробу. Она не должна быть повреждена или изменена во время транспортирования или хранения.
Процедура отбора проб не описана в настоящем стандарте. Рекомендованный метод отбора проб приведен в ISO 707.
Пробу хранят в условиях, предотвращающих ее порчу и изменение состава.
7 Приготовление7.1 Подготовка пробы
Пробу продукта помещают в контейнер вместимостью, в два раза превышающей объем пробы, с герметично закрывающейся крышкой, тщательно перемешивают, энергично встряхивая и переворачивая контейнер.
В процессе подготовки пробы необходимо исключить ее контакт с атмосферой, чтобы свести к минимуму абсорбцию влаги.
7.2 Навеска
В мензурке вместимостью 50 мл (5.2) взвешивают 1,0 г пробы с точностью до 1 мг.
7.3 Контрольное испытание
Контрольное испытание проводят в порядке, установленном в 7.4 и 8.2, с использованием всех реактивов, но без пробы продукта.
7.4 Приготовление раствора и удаление белка
7.4.1 Навеску (7.2) растворяют приблизительно в 20 мл воды температурой от 40 °С до 50 °С, перемешивая стеклянной палочкой (5.9) или подходящим средством. Содержимое мензурки количественно переносят в мерную колбу вместимостью 100 мл с одной отметкой (5.4), ополаскивая мензурку водой. Содержимое колбы охлаждают до температуры приблизительно 20 °С.
7.4.2 К раствору (7.4.1) последовательно добавляют 5,0 мл раствора гексацианоферрата (II) калия (4.1), 5,0 мл раствора сульфата цинка (4.2) и 10,0 мл раствора гидроксида натрия II (4.3.2), тщательно перемешивая после добавления каждого реагента. Доводят объем раствора водой до 100 см1 2. Снова тщательно перемешивают раствор и выдерживают 30 мин при комнатной температуре.
7.4.3 Содержимое колбы фильтруют через фильтровальную бумагу (5.8), отбрасывая первую порцию фильтрата.
Допустимо использовать центрифугирование в качестве альтернативы фильтрации.
8 Процедура
ПРЕДУПРЕЖДЕНИЕ - При проведении измерений следует избегать загрязнений, в том числе связанных с поглощением влаги или конденсацией ее на стенках сосудов.
8.1 Проверка активности реактивов
8.1.1 При приготовлении новой порции реактивов (4.6 - 4.10 включительно) и хранении готовых реактивов без использования более 2 нед, или при возобновлении аналитической работы после периода хранения, или при других обоснованных обстоятельствах проверяют активность реактивов.
8.1.2 В две мерные колбы вместимостью 100 мл с одной отметкой (5.4) вносят по 10 мл раствора L-лакгата лития (4.11). В две другие мерные колбы вместимостью 100 мл с одной отметкой (5.4) вносят по 10 мл раствора D-лакгата лития (4.12). Определяют концентрацию L-молочной кислоты и лактатов и содержание D-молочной кислоты и лактатов растворов в двух парах колб вместимостью 100 мл, действуя в порядке, установленном в 7.4.2, 7.4.3 и 8.2.
8.1.3 Концентрацию лактата лития wL, в миллиграммах на литр, вычисляют по формулам:
a) для раствора L-лактата:
wL = 341 х А,
b) для раствора D-лактата:
wL = 346 х А,
где А - численное значение коэффициента поглощения при 340 нм, вычисленное в соответствии с 8.2.1 и 8.2.2;
341 - численное значение параметра после замещения молекулярной массы L-лакгата лития (Мг = 96,1) и конечного объема (Vi = 2,24 мл) в 9.1 после того, как восстановление L-лактата оценено;
346 - численное значение параметра после замещения молекулярной массы D-лактата лития (И = 96,1) и конечного объема (Vi = 2,27 мл) в 9.1 после того, как восстановление D-лактата оценено.
8.1.4 Принимая во внимание чистоту L-лактата лития и D-лактата лития, определенная концентрация L- или D-лактата лития при проверке активности реактивов должна составлять (100 ± 5) % концентрации приготовленных растворов (8.1.2).
Если определяемое значение не попадает в этот интервал, проверяют реактивы, технику измерения, точность пипеток и дозаторов, а также исправность спектрофотометра. После этого тестирование повторяют до получения удовлетворительных результатов.
8.2 Определение
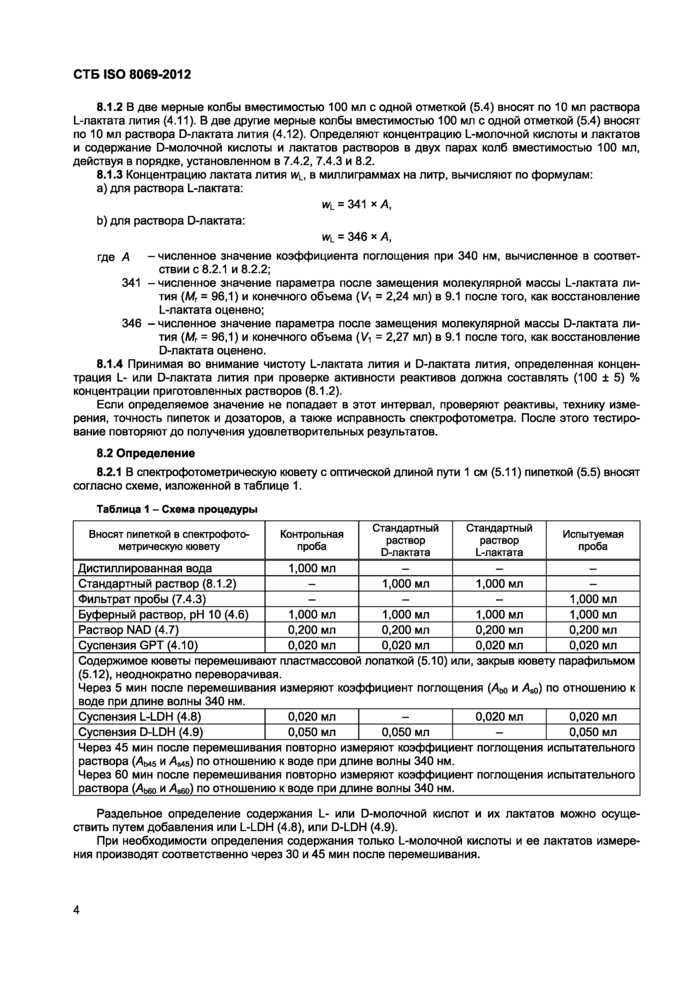
8.2.1 В спекгрофотометрическую кювету с оптической длиной пути 1 см (5.11) пипеткой (5.5) вносят согласно схеме, изложенной в таблице 1.
|
Таблица 1 - Схема процедуры | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Раздельное определение содержания L- или D-молочной кислот и их лактатов можно осуществить путем добавления или L-LDH (4.8), или D-LDH (4.9).
При необходимости определения содержания только L-молочной кислоты и ее лактатов измерения производят соответственно через 30 и 45 мин после перемешивания.
СТБ ISO 8069-2012
(1)
(1)
8.2.2 Вычисляют фактическое значение коэффициента поглощения А, используемое в вычислении (9.1), по формуле
А - [(Або - Ао) - 4(Або - А45)] - [(Аво - Ао) - 4(Або - ^Ь4б)1.
где Аео -численное значение коэффициента поглощения испытуемого раствора, измеренное через 60 мин по 8.2.1;
Ао -численное значение коэффициента поглощения испытуемого раствора, измеренное по 8.2.1;
Аде -численное значение коэффициента поглощения испытуемого раствора, измеренное через 45 мин по 8.2.1;
Аео -численное значение коэффициента поглощения раствора контрольного испытания, измеренное через 60 мин по 8.2.1;
Ао -численное значение коэффициента поглощения раствора контрольного испытания, измеренное по 8.2.1;
^М5 -численное значение коэффициента поглощения раствора контрольного испытания, измеренное через 45 мин по 8.2.1.
В некоторых случаях протекает вялотекущая побочная реакция. Изменение коэффициента поглощения, вызванное этой реакцией, исключают экстраполяцией коэффициента поглощения на нулевой момент времени.
(2)
Если требуется определить содержание только L-молочной кислоты и ее лактатов (см. 8.2.1), измерения проводят соответственно через 30 и 45 мин, соответственно. В таком случае вычисление проводят по измененной формуле
А - [(As45 — Ао) — 3(А45 — Азо)] — [Иь45 “ Ао) — 3(Аь45 — Азо)],
где Азо - численное значение коэффициента поглощения испытуемого раствора, измеренное через 30 мин по 8.2.1;
Ао -численное значение коэффициента поглощения раствора контрольного испытания, измеренное через 30 мин по 8.2.1.
8.2.3 Если увеличение коэффициента поглощения, вычисленного согласно 8.2.2, превышает 0,500 единиц, повторяют процедуры, установленные в 8.2.1 - 8.2.3, разбавляя фильтрат раствора навески (7.4.3) и раствор для контрольного испытания (7.3) соответствующим количеством воды.
9 Вычисление и представление результатов9.1 Вычисление
Вычисляют содержание молочной кислоты и лактатов wL, выраженное в миллиграммах молочной кислоты на 100 г обезжиренного сухого остатка, по формуле
(3)
где А - численное значение коэффициента поглощения при 340 нм, вычисленное согласно 8.2.2;
Мг - относительная молекулярная масса молочной кислоты, равная 90,1; к - молярный коэффициент поглощения NADH при 340 нм, равный 6,3 * 106 см2/моль;
/ - оптическая длина пути спектрофотометрической кюветы, равная 1 см;
т - масса навески (7.3), г;
V-\ - общий объем жидкости в спектрофотометрической кювете (см. 8.2.1), мл:
- при определении L- и D-молочной кислоты и их лактатов, равный 2,29 мл,
- при определении только L-молочной кислоты и ее лактатов, равный 2,24 мл,
- при определении только D-молочной кислоты и ее лактатов, равный 2,27 мл;
V2 - объем фильтрата (см. 7.4.3) в спектрофотометрической кювете (см. 8.2.1), мл;
V3 - объем фильтрата (см. 7.4.3), взятый для разбавления (см. 8.2.3), в случае необходимости, мл;
У4 - объем подготовленного раствора по 7.4.2, равный 100 мл;
V5 - объем разведенного фильтрата (см. 8.2.3), в случае необходимости, мл; ws - массовая доля сухого обезжиренного остатка в пробе, %.
Примечание - Определение содержания жира не является частью метода, установленного в настоящем стандарте. Рекомендуемый метод определения содержания жира в сухом молоке установлен в ISO 1736. 3
9.2 Представление результатов
Результаты испытания выражают в целых числах.
10 Прецизионность10.1 Межлабораторные испытания
Величины повторяемости и воспроизводимости были получены на основе результата межпабо-раторного испытания, осуществленного в соответствии с ISO 5725 2).
Подробная информация по межпабораторному испытанию на прецизионность метода была опубликована (см. [5]). Значения, полученные на основе данного межпабораторного испытания, могут не применяться для диапазонов концентрации и матриц, отличных от данных.
10.2 Повторяемость
Абсолютная разность между двумя независимыми результатами измерений, полученными с использованием одного и того же метода на идентичных пробах материала в одной лаборатории одним оператором на одном оборудовании в течение короткого промежутка времени, не должна превышать более чем в 5 % случаев следующих значений:
a) для среднеарифметического значения содержания молочной кислоты и лактатов < 60 мг на 100 г сухого обезжиренного остатка: 10 мг/100 г;
b) для среднеарифметического значения содержания молочной кислоты и лактатов > 60 мг на 100 г сухого обезжиренного остатка: 15 % (условно) от среднеарифметического значения содержания.
10.3 Воспроизводимость
Абсолютная разность между двумя независимыми результатами измерений, полученными с использованием одного и того же метода на идентичных пробах материала в разных лабораториях разными операторами на различном оборудовании, не должна превышать более чем в 5 % случаев следующих значений:
a) для среднеарифметического значения содержания молочной кислоты и лактатов < 100 мг на 100 г сухого обезжиренного остатка: 15 мг/100 г;
b) для среднеарифметического значения содержания молочной кислоты и лактатов > 100 мг на 100 г сухого обезжиренного остатка: 20 % (условно) от среднеарифметического значения содержания.
11 Протокол испытания
Протокол испытания должен включать:
a) всю информацию, необходимую для полной идентификации пробы;
b) метод отбора проб, если он известен;
c) метод испытания со ссылкой на настоящий стандарт;
d) все детали, не описанные в настоящем стандарте или необязательные, вместе с подробностями любых непредвиденных случайностей, которые могут повлиять на результат (ы) анализа;
e) полученные результаты или окончательный заявленный результат, если была проверена повторяемость.
2> ISO 5725:1986 Прецизионность методов измерений. Определение повторяемости и воспроизводимости стандартного метода измерения посредством использования межлабораторных испытаний (в настоящее время отменен) был использован для получения данных о прецизионности.
СТБ ISO 8069-2012Приложение А
(обязательное)
Правила надлежащей лабораторной практики (GLP) для проведенияферментного анализаА.1 Введение
А.1 Введение
Правила надлежащей лабораторной практики для ферментных анализов в меньшей степени изучены в отличие от правил для других химических анализов. На указанные правила необходимо обратить внимание для получения правильных и точных результатов. Перед проведением анализов необходимо ознакомиться с правилами GLP, описанными ниже.
А.2 Реактивы
А.1.1 Используются только реактивы установленного качества (удельная активность, концентрация, загрязняющие вещества с ферментной активностью, растворитель).
А.1.2 Используются только коферменты установленного качества (степень чистоты, солевая или кислотная форма, загрязняющие вещества).
А.1.3 Все реактивы, кроме ферментов и коферментов, должны быть аналитического качества.
А.1.4 Вода для приготовления ферментных растворов и других реактивов должна быть дважды дистиллированной.
А.1.5 Вода для приготовления испытуемых растворов должна быть дистиллированной или деионизированной.
А.1.6 Реактивы и ферментные суспензии/растворы хранят согласно инструкциям (как правило, при температуре от 2 °С до °8 С).
А.1.7 Ферментные суспензии не замораживают.
А.1.8 По окончании срока хранения реактива его либо утилизируют, либо проверяют качество, добавляя его различные количества в стандартные растворы. Полученный коэффициент поглощения должен быть пропорциональным концентрациям.
А.1.9 Температура буферных растворов, взятых из холодильной камеры, должна быть доведена до комнатной температуры перед добавлением в испытуемую смесь.
А.З Фотометрические и спектрофотометрические кюветы
А.3.1 Используют стеклянные или пластмассовые кюветы с оптической длиной пути 1 см.
Примечание - Пластмассовые кюветы имеют следующие преимущества перед стеклянными кюветами:
a) являются более дешевыми (одноразовыми);
b) возможно проведение большего числа анализов;
c) в одной партии пластмассовые кюветы имеют относительно равный коэффициент поглощения.
А.3.2 Всякий раз при использовании новой партии кювет необходимо контролировать их оптическую длину пути по отношению к оптической длине пути прецизионной кюветы (например, кварцевая кювета) следующим образом.
Прецизионную кювету и пластмассовую кювету наполняют водой и измеряют коэффициент поглощения А, каждой кюветы относительно воды. После ополаскивания кюветы наполняют раствором NADH (приблизительно 0,15 мг/мл) и снова измеряют коэффициент поглощения А2 относительно воды. Высчитывают (А2 - А|) для прецизионной кюветы и пластмассовой кюветы. Если разница (А2 - А^) между двумя типами кювет превышает 0,5 % измерения фактического значения коэффициента поглощения для прецизионной кюветы, тогда вычисляют среднюю разницу в процентах и учитывают ее для длины пути/в формуле (3).
А.3.3 Всегда используют чистые кюветы без механических повреждений. Оптическую сторону кювет протирают или чистят только мягкой тканью.
А.3.4 Не рекомендуется измерять коэффициент поглощения кювет при испытании пробы относительно коэффициента поглощения кюветы в контрольном испытании без полученной информации о значении величины коэффициента поглощения при контрольном испытании. Измеряют коэффициент поглощения при испытании пробы и при контрольном испытании относительно воды и высчитывают разницу.
7
1
11 Парафильм ™ является примером коммерчески доступной продукции. Эта информация дается для удобства пользователей данного документа и не является рекламой ISO или IDF этих продуктов.
2
3