СТБ EN 14122-2012
Продукты пищевые. Определение витамина В1 методом высокоэффективной жидкостной хроматографии (ВЭЖХ)
Купить СТБ EN 14122-2012 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает метод определения витамина В1 в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ). Витамин В1 представляет собой массовую долю общего тиамина вместе с его фосфорилированными производными.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Реактивы
5 Аппаратура
6 Методика
7 Вычисление
8 Прецизионность результатов испытаний
9 Протокол испытаний
Приложение A (справочное) Примеры хроматограмм высокоэффективной жидкостной хроматографии
Приложение B (справочное) Данные прецизионности
Приложение C (справочное) Альтернативные системы высокоэффективной жидкостной хроматографии
Библиография
| Дата введения | 01.01.2013 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Организации:
| 28.05.2012 | Утвержден | Госстандарт Республики Беларусь | 26 |
|---|---|---|---|
| Разработан | Научно-производственное республиканское УП БелГИСС | ||
| Издан | БелГИСС | 2012 г. |
Foodstuffs. Determination of vitamin B1 by HPLC
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9
стр. 10
стр. 11
стр. 12
стр. 13
стр. 14

стр. 15

стр. 16
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКТЫ ПИЩЕВЫЕ
Определение витамина методом высокоэффективной жидкостной хроматографии (ВЭЖХ)
ПРАДУКТЫ ХАРЧОВЫЯ
Вызначэнне в1тамшу Bi метадам высокаэфектыунай вадкаснай храматаграфМ (ВЭВХ)
(EN 14122:2003, ЮТ)
Издание официальное
Г осстандарт Минск
<л5
УДК 664:543.645.5:543.544.5.068.7(083.74)(476) МКС 67.050 КП 06 ЮТ
Ключевые слова: продукты пищевые, определение, витамин В-i, высокоэффективная жидкостная хроматография
Предисловие
Цели, основные принципы, положения по государственному регулированию и управлению в области технического нормирования и стандартизации установлены Законом Республики Беларусь «О техническом нормировании и стандартизации».
1 ПОДГОТОВЛЕН научно-производственным республиканским унитарным предприятием «Белорусский государственный институт стандартизации и сертификации» (БелГИСС)
ВНЕСЕН Госстандартом Республики Беларусь
2 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 28 мая 2012 г. № 26
3 Настоящий стандарт идентичен европейскому стандарту EN 14122:2003 Foodstuffs - Determination of vitamin B-] by HPLC [Продукты пищевые. Определение витамина В-] методом высокоэффективной жидкостной хроматографии (ВЭЖХ)], включая поправку АС:2005.
Европейский стандарт разработан техническим комитетом CEN/TC 275 «Анализ пищевых продуктов. Горизонтальные методы» Европейского комитета по стандартизации (CEN).
Перевод с английского языка (еп).
Официальные экземпляры европейского стандарта, на основе которого подготовлен настоящий государственный стандарт, и стандарт, на который дана ссылка, имеются в Национальном фонде ТИПА.
Степень соответствия - идентичная (IDT)
4 ВВЕДЕН ВПЕРВЫЕ
© Госстандарт, 2012
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
Издан на русском языке
СТБ EN 14122-2012
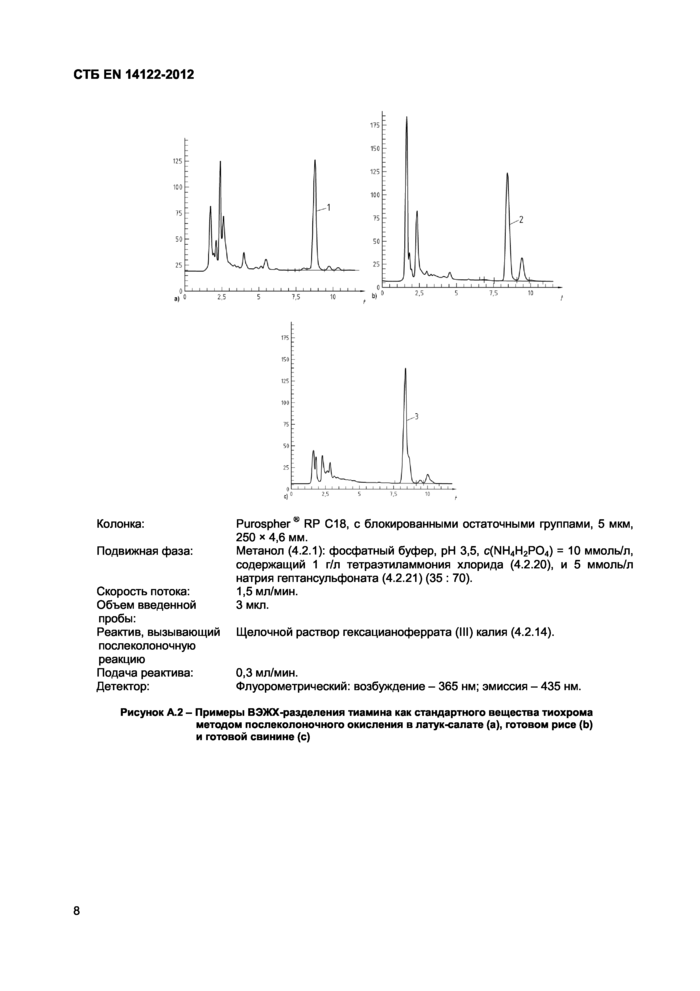
Колонка: Purospher® RP C18, с блокированными остаточными группами, 5 мкм,
250 х 4,6 мм.
Подвижная фаза: Метанол (4.2.1): фосфатный буфер, pH 3,5, c(NH4H2P04) = 10 ммоль/л,
содержащий 1 г/л тетраэтиламмония хлорида (4.2.20), и 5 ммоль/л натрия гептансульфоната (4.2.21) (35 : 70).
Скорость потока: 1,5 мл/мин.
Объем введенной 3 мкп.
пробы:
Реактив, вызывающий Щелочной раствор гексацианоферрата (III) калия (4.2.14).
послеколоночную
реакцию
Подача реактива: 0,3 мл/мин.
Детектор: Флуорометрический: возбуждение - 365 нм; эмиссия - 435 нм.
Рисунок А.2 - Примеры ВЭЖХ-разделения тиамина как стандартного вещества тиохрома методом послеколоночного окисления в латук-салате (а), готовом рисе (Ь) и готовой свинине (с)
8
СТБ EN 14122-2012Приложение В
(справочное)
Данные прецизионности
Согласно руководящим указаниям сертификационного исследования, организованного Европейской комиссией и Программой стандартных измерений и испытаний (EU SMT), данные, представленные в таблице В.1, были установлены в ходе межлабораторного испытания [9]. Исследование проводил Научно-исследовательский институт пищевых продуктов, г. Норвич, Великобритания, по поручению Европейского бюро стандартов. Данные, представленные в таблице В.2 и таблице В.З, были установлены в ходе межлабораторного испытания во Франции [8].
|
Таблица В.1 - Данные прецизионности для муки из цельного зерна, сухого молока, овощной смеси и свиной печени | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Таблица В.2-Данные прецизионности для раствора для парентерального питания, продукта детского питания, порошкового молока, муки с фруктами и дрожжей | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Окончание таблицы В.2 | ||||||||||||||||||||||||||||||
|
|
Таблица В.З-Данные прецизионности для крупяного продукта, шоколадного порошка и пищевой добавки | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
10
Приложение С
(справочное)
Альтернативные системы высокоэффективной жидкостной хроматографии
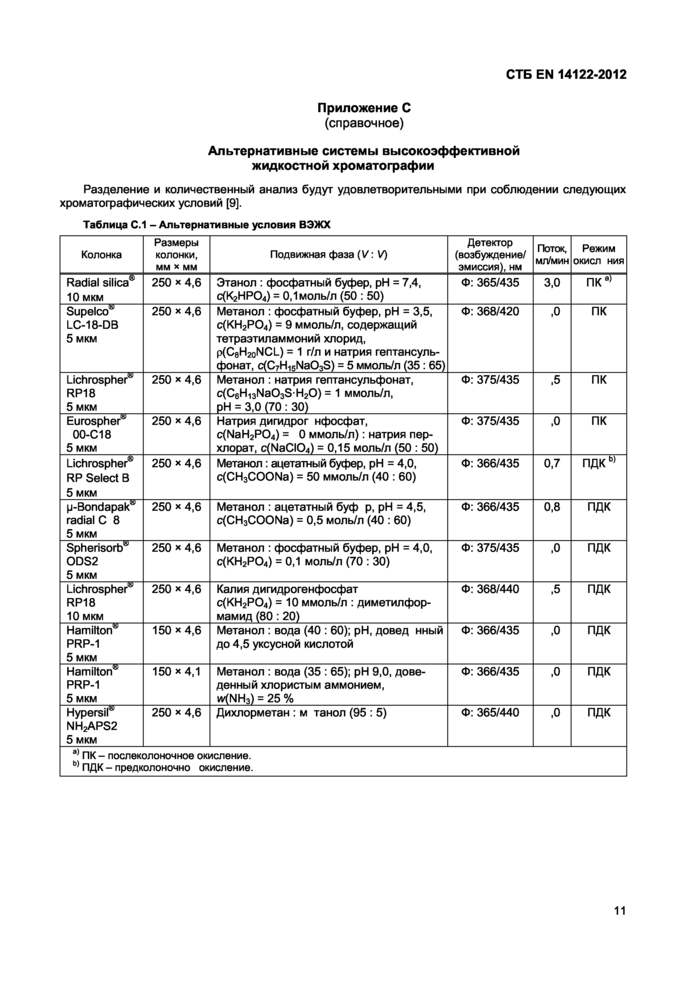
Разделение и количественный анализ будут удовлетворительными при соблюдении следующих хроматографических условий [9].
|
Таблица С.1 - Альтернативные условия ВЭЖХ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
СТБ EN 14122-2012Библиография
[1] Bognar A.: Bestimmung von Riboflavin und Thiamin in Lebensmitteln mit Hilfe der Hochleistungs-flussigkeitschromatographie (HPLC). Deutsche Lebensm. Rundschau 77 98 43 - 436 [Определение рибофлавина и тиамина в пищевых продуктах с помощью высокоэффикгивной жидкостной хроматографии (ВЭЖХ)]
[2] Hasselmann С. Franck D. Grimm, Р., Diop, Р.А. and Soules С.: High-performance liquid chromatographic analysis of thiamin and riboflavin in dietic foods. J. Micronutr. Anal. 5 989 269 - 279 (Высокоэффикгивный хроматографический анализ тиамина и рибофлавина в диетических пищевых продуктах)
[3] Bognar, A.: Determination of vitamin В-] in food by High-Performance-Liquid-Chromatography and post-column derivatization. Fresenius J. Anal. Chem. 343 992 55 - 56
(Определение витамина В методом высокоэффективной жидкостной хроматографии и после-колоночным окислением)
[4] Hagg, М. and Kumpulainen, J.: Thiamin and riboflavin contents in domestic and imported cereal products in Finland. J. Food Comp. Anal. 6, 1993 299 - 306
(Содержание тиамина и рибофлавина в отечественных и импортируемых в Финляндию крупяных продуктах)
[5] Arella, F., Lahely, S., Bourguignon J. В. and Hasselmann, C.: Liquid chromatographic determination of vitamin В and B2 in foods. A collaborative study. Food Chem. 56 996 8 -86 (Жидкостное хроматографическое определение витамина В и В2 в пищевых продуктах).
[6] Eitenmiller, R. R. and Landen W. О.: Vitamin Analysis for the Health and Food Sciences. CRC Press Boca Raton London New York, Washington, D.C. 999 27 - 297
(Анализ витаминов для валеологии и науки о продуктах питания)
[7] Dawson R.M.C. Elliott D. С. Elliot, W. H. and Jones, К.: Data for Biochemical Research. Oxford Science Publication 3rd. ISBN 0 9 855299 8, 989
(Данные биохимического исследования)
[8] Hagg, M.: Effect of various commercially available enzymes in the liquid chromatographic determination with external standardization of thiamin and riboflavin in foods. J. AOAC Int. 77 994 68 - 686 (Эффект различных имеющихся в продаже ферментов в жидкостном хроматографическом определении при внешней стандартизации тиамина и рибофлавина в пищевых продуктах)
[9] Finglas Р. М. Scott К. J. Witthoft, С. М., van den Berg Н. and de Froidmont-Gortz I.: The certification of the mass fractions of vitamins in four reference materials: Wholemeal flour (CRM 2 ) milk powder (CRM 421), lyophilised mixed vegetables (CRM 485) and lyophilised pig’s liver (CRM 487). EUR-report 8320 Office for Official Publications of the European Communities Luxembourg 999 [Сертификация массовых долей витаминов в четырех эталонных материалах: муке из цельного зерна (CRM 2 ) сухом молоке (CRM 421) лиофилизированной овощной смеси (CRM 485) и лиофилизированной свиной печени (CRM 487)]
[10] Takashi U. Yukiko Т. Kohei М. Mari, Т., Kaname, К.: Simultaneous determination of 2 ( -hydro-xyethyl)thiamin and thiamin in foods by high performance liquid chromatography with post-column derivatisation. Vitamins (Japan) 64, 1990, 379 - 385
(Одновременное определение 2(1-гидроксиэтил)тиамина и тиамина в пищевых продуктах методом высокоэффективной жидкостной хроматографии с послеколоночным окислением)
[11] Takashi U. Yukiko Т. Kohei М. Masako, М., Kaname К.: Distribution and stability of 2( -hydro-xyethyl) thiamin and thiamin in foods. Vitamins (Japan), 65 99 249 - 256 (Распределение и стабильность 2(1-гидроксиэтил) тиамина и тиамина в пищевых продуктах)
12
Ответственный за выпуск В. Л. Гуревич
Сдано в набор 13.08.2012. Подписано в печать 25.09.2012. Формат бумаги 60x84/8. Бумага офсетная. Гарнитура Arial. Печать ризографическая. Уел. печ. л. 1,86 Уч.- изд. л. 1,08 Тираж экз. Заказ
Издатель и полиграфическое исполнение: Научно-производственное республиканское унитарное предприятие «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) ЛИ № 02330/0552843 от 08.04.2009. ул. Мележа, 3, комн. 406, 220113, Минск.
СТБ EN 14122-2012
Содержание
1 Область применения..............................................................................................................................1
2 Нормативные ссылки.............................................................................................................................1
3 Сущность метода....................................................................................................................................1
4 Реактивы..................................................................................................................................................1
5 Аппаратура..............................................................................................................................................3
6 Методика.................................................................................................................................................4
7 Вычисление.............................................................................................................................................5
8 Прецизионность результатов испытаний.............................................................................................6
9 Протокол испытаний...............................................................................................................................6
Приложение А (справочное) Примеры хроматограмм высокоэффективной
жидкостной хроматографии............................................................................................7
Приложение В (справочное) Данные прецизионности...........................................................................9
Приложение С (справочное) Альтернативные системы высокоэффективной
жидкостной хроматографии..........................................................................................11
Библиография..........................................................................................................................................12
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬПРОДУКТЫ ПИЩЕВЫЕ Определение витамина Bi методом высокоэффективной жидкостной хроматографии (ВЭЖХ)ПРАДУКТЫ ХАРЧОВЫЯ Вызначэнне в1тамшу Bi метадам высокаэфектыунай вадкаснай храматаграфм (ВЭВХ)
ПРАДУКТЫ ХАРЧОВЫЯ Вызначэнне в1тамшу Bi метадам высокаэфектыунай вадкаснай храматаграфм (ВЭВХ)
Foodstuffs Determination of vitamin Bi by HPLC
Дата введения 2013-01-011 Область применения
Настоящий стандарт устанавливает метод определения витамина Bi в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ). Витамин Bi представляет собой массовую долю общего тиамина вместе с его фосфорилированными производными.
2 Нормативные ссылки
Для применения настоящего стандарта необходим следующий ссылочный документ. Для датированных ссылок применяют только указанное издание ссылочного документа.
EN ISO 3696:1995 Вода для лабораторного анализа. Технические требования и методы испытаний
3 Сущность метода
Тиамин извлекают из пищевых продуктов путем кислотного гидролиза с последующим дефосфорилированием, используя ферментативную обработку, и определяют его количество методом ВЭЖХ с предколоночным или послеколоночным окислением в тиохром [1] - [6].
4 Реактивы4.1 Общие положения
В ходе анализа используют только реактивы признанной аналитической чистоты и воду не ниже первой степени чистоты в соответствии с EN ISO 3696:1995 или бидистиллированную воду.
4.2 Химические реактивы и растворы
4.2.1 Метанол для ВЭЖХ, массовая доля w(CH3OH) > 99,8 %.
4.2.2 Раствор уксусной кислоты, концентрация вещества с(СН3СООН) = 0,02 моль/л.
4.2.3 Изобутанол, w(C4Hi0O) 2: 98 %.
4.2.4 Дигидрофосфат натрия, w(NaH2P04) > 99,8 %.
4.2.5 Соляная кислота, w(HCI) = 36 %.
4.2.6 Соляная кислота, с(НС1) = 0,1 моль/л.
4.2.7 Серная кислота, c(H2S04) = 0,05 моль/л.
4.2.8 Гидроксид натрия, w(NaOH) > 99 %.
4.2.9 Раствор гидроксида натрия, массовая концентрация p(NaOH) = 150 г/л.
4.2.10 Раствор гидроксида натрия, w(NaOH) = 200 г/л.
4.2.11 Гексацианоферрат (III) калия, w{K3[Fe(CN)6]} > 99 %.
4.2.12 Раствор гексацианоферрата (III) калия, p{K3[Fe(CN)6]} = 10 г/л.
Издание официальное
4.2.13 Щелочной раствор гексацианоферрата (III) калия (предколоночное окисление),
p{K3[Fe(CN)6]} = 0,4 г/л.
2,0 мл раствора гексацианоферрата (III) калия (4.2.12) помещают в мерную колбу вместимостью 50 мл и объем доводят до метки раствором гидроксида натрия (4.2.9). Раствор используют свежеприготовленным.
4.2.14 Щелочной раствор гексацианоферрата (III) калия (послеколоночное окисление),
p{K3[Fe(CN)6]} = 0,5 г/л.
2,5 мл раствора гексацианоферрата (III) калия (4.2.12) помещают в мерную колбу вместимостью 50 мл и объем доводят да метки раствором гидроксида натрия (4.2.10).
4.2.15 Фермент для дефосфорилирования, способный гидролизовать связанный тиамин из пищевых продуктов 1).
4.2.16 Раствор ацетата натрия, с(СН3С001Ча-ЗН20) = 2,5 моль/л.
4.2.17 Раствор ацетата натрия, с(СН3С001Ча-ЗН20) = 0,5 моль/л.
4.2.18 Подвижные фазы ВЭЖХ
Примеры соответствующих смесей с объемными долями метанола (4.2.1) от 10 % до 50 % в воде или использования фосфатного или ацетатного буфера представлены в приложении С. Также представлен вариант подвижной фазы с использованием ион-парного реагента.
4.2.19 Фосфатный буфер (pH 3,5), с(КН2Р04) = 9,0 ммоль/л.
4.2.20 Тетраэтиламмоний хлорид, w(C3H 0NCI) > 98 %.
4.2.21 Натрия гептансульфонат, w(C7H15Na03S) 2: 98 %.
4.2.22 Ацетатный буфер (pH 4,0), с(СН3СООН) = 50 ммоль/л.
4.3 Стандартные вещества4.3.1 Общие положения
Тиамина хлорид гидрохлорид может быть получен от различных поставщиков. Чистота стандартных веществ тиамина может меняться, и поэтому необходимо определить концентрацию калибровочного раствора методом ультрафиолетовой (УФ) спектрометрии (см. 4.4.4).
4.3.2 Тиамина хлорид гидрохлорид, w(Ci H17CIN4OSHCI) > 99 %.
4.3.3 Тиамина монофосфат хлорид, w(Ci H17CIN404PS) > 98 %.
4.3.4 Тиамина пирофосфат хлорид (кокарбоксилаза), w(Ci2HigCIN407P2S) > 98 %.
4.4 Исходные растворы
4.4.1 Тиамина хлорид гидрохлорид, р(^ H17CIN4OSHCI) «0,1 мг/мл.
Растворяют 10 мг стандартного вещества тиамина хлорида гидрохлорида (4.3.2) в 100 мл соляной кислоты (4.2.6). Раствор можно хранить в течение 4 нед при температуре 4 °С.
4.4.2 Тиамина монофосфат, p(Ci2H17CIN404PS) «0,1 мг/мл.
Растворяют 10 мг стандартного вещества тиамина монофосфат хлорида (4.3.3) в 100 мл соляной кислоты (4.2.6). Раствор можно хранить в течение 4 нед при температуре минус 20 °С.
4.4.3 Тиамина пирофосфат, p(Ci2HigCIN407P S)« 0,1 мг/мл.
Растворяют 10 мг стандартного вещества тиамина пирофосфат хлорида (4.3.4) в 100 мл соляной кислоты (4.2.6).
4.4.4 Проверка концентрации
10 мл исходного раствора тиамина хлорида гидрохлорида (4.4.1) помещают в мерную колбу вместимостью 100 мл и раствором соляной кислоты (4.2.6) доводят до метки. Оптическую плотность данного раствора измеряют при максимальной длине волны 247 нм в кювете с длиной оптического пути 1 см относительно раствора соляной кислоты (4.2.6) в эталонной кювете, используя УФ-спекгрометр (5.2). Массовую концентрацию исходного раствора р, мг/мл, рассчитывают по формуле 1 2
СТБ EN 14122-2012
(1)
с
421
(1)
с
421
где £247 - величина поглощающей способности раствора при максимальной длине волны 247 нм;
421 - коэффициент поглощающей способности тиамина хлорида гидрохлорида в
0,1 моль/л соляной кислоты (см. [7]);
10 - коэффициент разбавления.
4.5 Стандартные растворы
4.5.1 Тиамина хлорид гидрохлорид, р(С12Н1 CIN4OS HCI) « от 1 до 10 мкг/мл.
В мерную колбу вместимостью 100 мл переносят пипеткой от 1 до 10 мл исходного раствора тиамина хлорида гидрохлорида (4.4.1) и объем доводят до метки соляной кислотой (4.2.6). Раствор можно хранить в течение 1 мес при температуре 4 °С в темном месте.
4.5.2 Тиамина монофосфат, p(Ci2Hi CIN4O4PS)« от 1 до 10 мкг/мл.
В мерную колбу вместимостью 100 мл переносят пипеткой от 1 до 10 мл исходного раствора тиамина монофосфата (4.4.2) и объем доводят до метки соляной кислотой (4.2.6). Раствор можно хранить в течение 1 мес при температуре 4 °С в темном месте.
4.5.3 Тиамина пирофосфат, p(C12H19CIN40 P2S) « от 1 до 10 мкг/мл.
В мерную колбу вместимостью 100 мл переносят пипеткой от 1 до 10 мл исходного раствора тиамина пирофосфата (4.4.3) и объем доводят до метки соляной кислотой (4.2.6). Раствор можно хранить в течение 1 мес при температуре 4 °С в темном месте.
5 Аппаратура5.1 Общие положения
Используют стандартное лабораторное оборудование, стеклянную посуду и следующее:
5.2 УФ-спектрометр
Пригодный для измерения абсорбции при определенной длине волны.
5.3 Автоклав или нагревательный прибор
Запарник-автоклав или варочный аппарат, работающий под давлением, со считывающим устройством давления или температуры, электронагревательный прибор или водяная баня.
5.4 Система высокоэффективной жидкостной хроматографии
Состоит из насоса, устройства ввода проб, флуоресцентного детектора с длиной волны возбуждения и эмиссии, установленной на уровнях 366 и 420 нм соответственно (см. приложение С), а также устройства для обработки данных (интегратора).
5.5 Колонки для ВЭЖХ5.5.1 Общие положения
Можно использовать другие размеры частиц или колонок, вместо указанных в настоящем стандарте. Параметры разделения должны быть адаптированы к таким материалам, чтобы гарантировать эквивалентные результаты. Критерием эффективности подходящих аналитических колонок является разделение анализируемых веществ 2 до базовой линии.
5.5.2 Предколоночное окисление
Аналитические колонки, например Lichrospher® 60 RP Select В 2, размер частиц 5 мкм, диаметр от 4,0 до 4,6 мм, длина от 100 до 250 мм.
5.5.3 Послеколоночное окисление
Аналитические колонки, например Supelco® LC-18-DB 2, размер частицы 5 мкм, диаметр от 4,0 до
4,6 мм, длина от 100 до 250 мм. 3
5.6 Фильтровальное устройство
Фильтрация подвижной фазы, а также раствора анализируемой пробы через мембранный фильтр с размером пор 0,45 мкм до использования или ввода проб увеличит срок службы колонок.
5.7 Послеколоночный реакторный насос и трубка для окисления
Подходящая система подачи реактива, Т-образная соединительная трубка и трубка для окисления (10 м х 0,33 мм).
6 Методика6.1 Подготовка анализируемой пробы
Гомогенизируют анализируемую пробу. Твердые продукты измельчают в соответствующей мельнице и перемешивают. Чтобы не подвергать пробу воздействию высокой температуры в течение длительного времени, должны быть приняты такие меры, как предварительное охлаждение.
6.2 Подготовка раствора анализируемой пробы6.2.1 Экстракция
В конической колбе взвешивают от 2 до 10 г анализируемой пробы с точностью до 1 мг. Добавляют от 60 до 200 мл соляной (4.2.6) или серной кислоты (4.2.7). Уровень pH раствора не должен быть выше 3,0. Накрывают колбу предметным стеклом и автоклавируют навеску при температуре 121 °С в течение 30 мин или нагревают ее при температуре 100 °С в течение 60 мин.
Примечание - Исследования, проводимые Европейским бюро стандартов, показали, что можно применять обширный диапазон условий для кислотного гидролиза (температура от 95 °С до 130 °С, время от 15 до 60 мин). Чем выше температура, тем короче должно быть время.
6.2.2 Ферментативная обработка
После охлаждения до комнатной температуры pH экстракта доводят до оптимального уровня для используемого фермента раствором ацетата натрия (4.2.16) или (4.2.17) и добавляют подходящее количество фермента для дефосфорилирования (4.2.15). Выдерживают смесь при оптимальной температуре в течение оптимального времени для используемого фермента. После охлаждения до комнатной температуры переливают раствор в защищенную от света мерную колбу, используя дистиллированную воду или другой соответствующий растворитель, и доводят до заданного объема Ve.
Для каждого используемого фермента необходимо установить оптимальный уровень pH, оптимальное время и температуру выдержки.
Чтобы обеспечить оптимальное дефосфорилирование, ферментативный этап следует проверить на пробах с известным содержанием тиамина монофосфат хлорида (4.3.3) или тиамина пирофосфат хлорида (4.3.4) и вещества, похожего по типу на вещество анализируемой пробы. Данное вещество должно быть сертифицировано эталонным веществом.
Если для дефосфорилирования используют Така-диастазу, количество тиамина, внесенное с ферментом, следует учитывать при расчете результата.
Примечание 1 - Для определения точности результатов испытаний, указанных в настоящем стандарте, для дефосфорилирования использовали Така-диастазу при следующих условиях. Уровень pH экстракта довели до pH = 4,0 раствором ацетата натрия (4.2.16) или (4.2.17) и добавили 100 мг Така-диастазы на грамм пробы. Смесь выдерживали при температуре от 37 °С до 46 °С в течение от 16 до 24 ч.
Примечание 2 - Дефосфорилирование может зависеть от состава пробы и используемого фермента. Полное дефосфорилирование может быть выполнено за более короткое время, см. [8].
6.2.3 Окисление тиамина в тиохром6.2.3.1 Предколоночное окисление
Пипеткой переносят по 1 мл ферментативно обработанной пробы (6.2.2), градуировочного раствора (4.5.1) или холостого раствора в подходящие колбы, добавляют 1 мл щелочного раствора гек-сацианоферрата (III) калия (4.2.13). Взбалтывают раствор анализируемой пробы в течение фиксированного периода времени (10 с), дают отстояться в течение установленного периода времени (1 мин) и вводят в систему ВЭЖХ с обращенно-фазовой колонкой (см. таблицу С.1).
Допускается окисленный раствор извлекать 1,5 мл изобутанола (4.2.3) и полученный экстракт вводить в колонку (с Н3РО4). Чтобы удалить мешающие соединения и защитить колонку для ВЭЖХ, рекомендуется нейтрализовать или выполнить очистку методом твердофазной экстракции (см. [5]). Примечание - Окислительное преобразование тиамина в тиохром может быть ингибировано полифенолами, содержащимися в некоторых пищевых продуктах. Данный феномен часто встречается в пищевых продуктах, содержащих какао, но также может наблюдаться в других пищевых продуктах. Если есть подозрение на наличие
4
СТБ EN 14122-2012
данной проблемы, рекомендуется проверить степень извлечения, добавив в экстракт пробы соответствующий объем стандартного раствора тиамина до реакции окисления. Если степень извлечения признана низкой, рекомендуется выполнить очистку экстракта пробы с применением катионообменной смолы или использовать ВЭЖХ с послеколоночным окислением.
6.2.3.2 Идентификация при предколоночном окислении
Вводят одинаковые соответствующие объемы калибровочных растворов, а также растворов анализируемой пробы в систему ВЭЖХ. Идентифицируют тиохром путем сравнения времени удержания индивидуальных пиков на хроматограммах, полученных для раствора анализируемой пробы и для раствора стандартного вещества. Идентификация пиков также может быть выполнена путем добавления стандартного вещества в раствор анализируемой пробы.
Разделение и количественный анализ проводят при соблюдении следующих экспериментальных условий (см. также рисунок А.1 и приложение С по условиям для альтернативных систем ВЭЖХ).
Колонка: Lichrospher® RP Select В, 5 мкм, 250 х 4,0 мм.
Подвижная фаза: Метанол (4.2.1): ацетатный буфер (4.2.22).
Скорость потока: 0,7 мл/мин.
Объем введенной пробы: 20 мкл.
Детектор: Флуорометрический: возбуждение - 366 нм и эмиссия - 435 нм.
6.2.3.3 Послеколоночное окисление
Окисляют тиамин в тиохром, применяя послеколоночную реакцию в присутствии раствора гекса-цианоферрата (4.2.14). Непрерывно добавляют (0,3 мл/мин) реактив для окисления через Т-образную соединительную трубку в элюент для ВЭЖХ для образования тиохрома.
Примечание - Этап послеколоночного окисления зависит от концентрации гидроксида натрия. Высокие концентрации в растворе для окисления можно компенсировать более низкой скоростью нагнетания и наоборот.
6.2.3.4 Идентификация при послеколоночном окислении
Вводят одинаковые соответствующие объемы калибровочных растворов, а также растворов пробы в систему ВЭЖХ. Идентифицируют тиохром путем сравнения времени удержания индивидуальных пиков на хроматограммах, полученных для раствора анализируемой пробы и для раствора стандартного вещества. Идентификацию пиков можно также выполнить, добавив стандартные вещества в раствор анализируемой пробы.
Разделение и количественный анализ признаются удовлетворительными при соблюдении следующих экспериментальных условий (см. также рисунок А.2 и приложение С по условиям для альтернативных систем ВЭЖХ).
Колонка: Supelco® LC-18-DB, 5 мкм, 250 х 4,6 мм.
Подвижная фаза: Метанол (4.2.1): фосфатный буфер (4.2.19), одержащий 1 г/л
тетраэтиламмония хлорида (4.2.20) и 5 ммоль/л натрия гептан-сульфоната (4.2.21) (35 : 65).
Скорость потока: 1,0 мл/мин.
Объем введенной пробы: 20 мкл.
Реактив, вызывающий после- Щелочной раствор гексацианоферрата (III) калия (4.2.14). колоночное окисление
Подача реактива: 0,3 мл/мин.
Детектор: Флуорометрический: возбуждение - 368 нм; эмиссия - 440 нм.
Примечание - Анализ некоторых проб, например сырой свинины, может показать дополнительный пик
1-гидрокси-тиамина или 2(1-гидроксиэтил)тиамина на хроматограмме, см. [10] и [11].
6.3 Определение
Для выполнения определения методом внешней калибровки интегрируют площади пиков или определяют высоты пиков раствора анализируемой пробы и сравнивают результаты с соответствующими значениями стандартных растворов с ближайшей площадью пика или высотой или используют калибровочную кривую. Проверяют линейность калибровки.
7 Вычисление
Вычисление выполняют по калибровочной кривой или используют соответствующие программы интегратора или следующую упрощенную процедуру. Рассчитывают массовую долю витамина Вч w, выраженного как тиамина хлорид гидрохлорид, мг/100 г пробы, по формуле
5
4з*схУе;; loo
(2)
(2)
Д, х ms 10ОО ’
где As - площадь или высота пика тиохрома, полученные при хроматографировании раствора анализируемой пробы, в единицах площади или высоты;
Ast - площадь или высота пика тиохрома, полученные при хроматографировании стандартного раствора, в единицах площади или высоты;
Ve - объем раствора анализируемой пробы (6.2.2), мл;
р - массовая концентрация раствора тиамина хлорида гидрохлорида (4.5.1), мкг/мл; ms - масса пробы, г;
100 - коэффициент пересчета содержимого на 100 г;
1000 - коэффициент пересчета мкг/100 г в мг/100 г.
В протокол вносят результат витамина мг/100 г, выраженного как тиамин хлорид гидрохлорид. Если результат необходимо выразить как тиамин (Ci2H17CIN4OS), то результат умножают на коэффициент 0,892.
8 Прецизионность результатов испытаний
8.1 Общие положения
Данные прецизионности различных методов ВЭЖХ для определения тиамина была установлена в 1996 г. в ходе международных сравнительных исследований, организованных Европейской комиссией и Программой стандартных измерений и испытаний на образцах муки из цельного зерна (CRM 121), сухого молока (CRM 421), овощной смеси (CRM 485) и лиофилизированной свиной печени (CRM 487). Полученная статистическая информация представлена в приложении В.
8.2 Повторяемость
Абсолютная разность между двумя отдельными результатами испытаний, полученными на идентичном анализируемом материале одним оператором, использующим одно и то же оборудование в течение самого короткого промежутка времени, практически возможного, не должна превышать предел повторяемости г более чем в 5 % случаев.
Значения для тиамина хлорид гидрохлорида:
Мука из цельного зерна х = 0,452 мг/100 г г = 0,043 мг/100 г
Сухое молоко х = 0,645 мг/100 г г= 0,071 мг/100 г
Овощная смесь х = 0,295 мг/100 г г = 0,039 мг/100 г
Свиная печень х = 0,807 мг/100 г г = 0,088 мг/100 г
8.3 Воспроизводимость
Абсолютная разность между двумя отдельными результатами испытаний, полученными на идентичном материале двумя лабораториями, не должна превышать предел воспроизводимости R более чем в 5 % случаев. Значения для тиамина хлорид гидрохлорида:
Мука из цельного зерна х = 0,452 мг/100 г R = 0,190 мг/100 г
Сухое молоко х = 0,645 мг/100 г R = 0,243 мг/100 г
Овощная смесь х = 0,295 мг/100 г R = 0,178 мг/100 г
Свиная печень х = 0,807 мг/100 г R = 0,623 мг/100 г
9 Протокол испытаний
Протокол испытаний должен содержать следующие данные:
a) всю информацию, необходимую для полной идентификации пробы;
b) ссылку на настоящий стандарт или используемый метод;
c) дату и метод отбора проб (если известны);
d) фамилию, имя, отчество и подпись ответственного лаборанта;
e) дату получения пробы;
f) результаты испытания и единицы, в которых выражаются результаты;
д) любые особенности, которые наблюдались в ходе проведения испытания; h) любые операции, не установленные в методе или рассматриваемые как дополнительные, которые могут повлиять на результаты.
6
СТБ EN 14122-2012
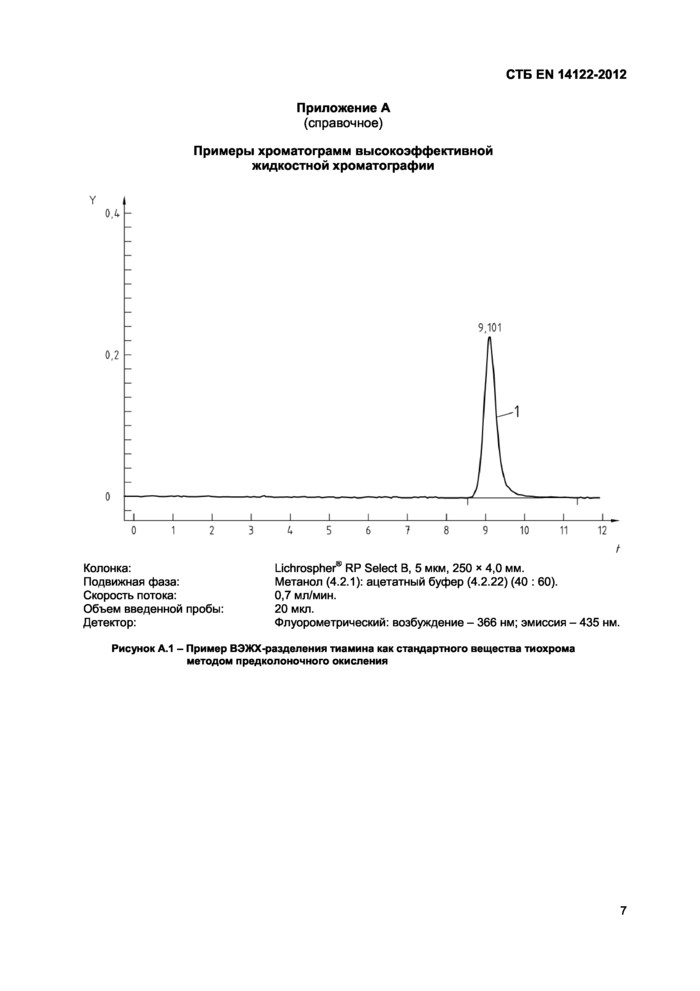
Приложение А
(справочное)
Примеры хроматограмм высокоэффективной жидкостной хроматографии
Колонка: Lichrospher® RP Select В, 5 мкм, 250 * 4,0 мм.
Подвижная фаза: Метанол (4.2.1): ацетатный буфер (4.2.22) (40 : 60).
Скорость потока: 0,7 мл/мин.
Объем введенной пробы: 20 мкл.
Детектор: Флуорометрический: возбуждение - 366 нм; эмиссия - 435 нм.
Рисунок А.1 - Пример ВЭЖХ-разделения тиамина как стандартного вещества тиохрома методом предколоночного окисления
7
1
11 Примером подходящего фермента для дефосфорилирования является Така-диастаза № Т00040, изготовитель - Pfalz & Bauer, Waterbury, СТ 06708, USA. Эта информация приводится для удобства пользователей настоящего стандарта и не является рекламой CEN указанного продукта. Могут использоваться эквивалентные продукты, если они приведут к тем же результатам.
2
3
Подходящие силикагелевые наполнители для колонок, имеющиеся в продаже: Lichrosorb® Si 60, Spherisorb® Si, Hypersil® Si и Lichrospher® 100 DIOL. Подходящие наполнители для ОФ-колонок: Spherisorb® ODS, ц-Bondapak radial Cl 8, Supelco® LC-18-DB и Hypersil® ODS. Эта информация приводится для удобства пользователей настоящего стандарта и не является рекламой CEN указанных продуктов.
3