СТБ EN 12821-2012
Продукты пищевые. Определение содержания витамина D методом высокоэффективной жидкостной хроматографии. Определение холекальциферола (D3) или эргокальциферола (D2)
Купить СТБ EN 12821-2012 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает метод определения витамина D3 (холекальциферол) или витамина D2 (эргокальциферол) в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ). Стандарт распространяется только на определение витаминов D3 или D2.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Реактивы
5 Аппаратура
6 Проведение испытаний
7 Расчет
8 Прецизионность
9 Протокол анализа
Приложение A (справочное) Примеры применяемых полупрепаративных систем высокоэффективной жидкостной хроматографии
Приложение B (справочное) Примеры применяемых условий экстракции и омыления
Приложение C (обязательное) Примеры применяемых полупрепаративных и аналитических хроматограмм
Приложение D (справочное) Данные по прецизионности измерений
Приложение E (справочное) Дополнительный этап предварительной очистки для определения витамина D с использованием препаративной тонкослойной хроматографии
Библиография
| Дата введения | 01.01.2013 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Организации:
| 28.05.2012 | Утвержден | Госстандарт Республики Беларусь | 26 |
|---|---|---|---|
| Разработан | Научно-производственное республиканское УП БелГИСС | ||
| Издан | БелГИСС | 2012 г. |
Foodstuffs. Determination of vitamin D by high performance liquid chromatography. Measurement of cholecalciferol (D3) or ergocalciferol (D2)
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10
стр. 11
стр. 12
стр. 13
стр. 14
стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКТЫ ПИЩЕВЫЕ
Определение содержания витамина D
методом высокоэффективной жидкостной хроматографии. Определение холекальциферола (D3) или эргокальциферола (D2)
ПРАДУКТЫ ХАРЧОВЫЯ
Вызначэнне змяшчэння вп-амшу D
метадам высокаэфектыунай вадкаснай храматаграфМ.
Вызначэнне холекальцыферолу (D3) або эргакальцыферолу (D2)
(EN 12821:2009, ЮТ)
Издание официальное
Г осстандарт Минск
as
УДК 664:543.645.5(083.74)(476) МКС 67.050 КП 06 ЮТ
Ключевые слова: пищевые продукты, витамин D, холекальциферол D3, эргокальциферол D2, высокоэффективная жидкостная хроматография
Предисловие
Цели, основные принципы, положения по государственному регулированию и управлению в области технического нормирования и стандартизации установлены Законом Республики Беларусь «О техническом нормировании и стандартизации».
1 ПОДГОТОВЛЕН научно-производственным республиканским унитарным предприятием «Белорусский государственный институт стандартизации и сертификации» (БелГИСС)
ВНЕСЕН Госстандартом Республики Беларусь
2 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 28 мая 2012 г. № 26
3 Настоящий стандарт идентичен европейскому стандарту EN 12821:2009 Foodstuffs - Determination of vitamin D by high performance liquid chromatography - Measurement of cholecalciferol (D3) or ergocalcif-erol (D2) (Продукты пищевые. Определение содержания витамина D методом высокоэффективной жидкостной хроматографии. Определение холекальциферола (D3) или эргокальциферола (D2)).
Европейский стандарт разработан техническим комитетом по стандартизации CEN/TC 275 «Анализ пищевых продуктов. Горизонтальные методы» Европейского комитета по стандартизации (CEN).
Перевод с английского языка (еп).
Официальные экземпляры европейского стандарта, на основе которого подготовлен настоящий государственный стандарт, и европейского стандарта, на который дана ссылка, имеются в Национальном фонде ТИПА.
Степень соответствия - идентичная (ЮТ)
4 ВВЕДЕН ВПЕРВЫЕ
© Госстандарт, 2012
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
Издан на русском языке
СТБ EN 12821-2012Приложение А
(справочное)
Примеры применяемых полупрепаративных систем высокоэффективной жидкостной хроматографии
Таблица А.1 - Примеры полупрепаративных систем ВЭЖХ, которые использовались для очистки анализируемых растворов проб участниками сертификационных испытаний витамина D по EU МАТ (Программа измерений и испытаний Европейского союза) [8]
|
Колонка |
Размеры, мм |
Подвижная фаза, (V + V) |
Детектор, X |
|
Polygosil® 60, 5 мкм |
250*8 |
изооктан + изобутанол (99 + 1) |
265 нм |
|
LiChrospher® Si 60, 5 мкм |
250*4 |
л-гексан + 2-пропанол (99 + 1) |
265 нм |
|
LiChrospher® Si 100, 5 мкм |
250*8 |
л-гексан + 2-пропанол (98 + 2) |
265 нм |
|
ц Porasil® silica |
300 * 3,9 |
л-гексан + THF + 2-пропанол (98 + 1+1) |
265 нм |
|
Partisil® РАС, 5 мкм |
250 * 4,6 |
л-гексан + изоамиловый спирт (99 + 1) |
265 нм |
|
Lichrosorb ® Si 60 |
250*4 |
л-гексан + 2-пропанол + THF (98 + 1+1) |
265 нм |
|
Lichrosorb® Si 60 |
250*4 |
л-гексан + 2-пропанол (95 + 5) |
265 нм |
|
Lichrosorb® Si 60 |
250*4 |
л-гексан + 2-пропанол (97 + 3) |
265 нм |
|
Все торговые наименования предназначены исключительно для удобства пользователей настоящего стандарта. Это не является рекламой названных видов продукции со стороны CEN. | |||
Таблица А.2 - Примеры аналитических систем ВЭЖХ, используемых для определения витамина D в растворах с исследуемой пробой, которые использовались участниками сертификационных испытаний EU МАТ [8]
|
Колонка |
Размеры, мм |
Подвижная фаза, (V + V) |
Детектор, X |
|
Hypersil® ODS, 5 мкм |
250 * 4,6 |
метанол |
265 нм |
|
LiChrospher® 100 RP, 18,5 мкм |
250*4 |
метанол + вода (95 + 5) |
264 нм |
|
Vydac® 201ТР54 |
250 * 4,6 |
метанол + вода (93 + 7) |
265 нм |
|
Vydac® 201ТР54 |
250 * 4,6 |
ацетонитрил + метанол (80 + 20) |
265 нм |
|
Shperisorb® ODS 2, 5 мкм |
250 * 4,6 |
ацетонитрил + дихлорметан + метанол (93 + 4 + 3) |
диодная матрица |
|
Nucleosil® Cis, 5 мкм |
250*4 |
ацетонитрил + метанол (70 + 30) |
265 нм |
|
Zorbax® ODS |
250 * 4,6 |
ацетонитрил + метанол (95 + 5) |
265 нм |
|
Все торговые наименования предназначены исключительно для удобства пользователей настоящего стандарта. Это не является рекламой названных видов продукции со стороны CEN. | |||
9
Приложение В
(справочное)
Примеры применяемых условий экстракции и омыления
Приведенные в качестве примеров условия экстракции и омыления использовались участниками сертификационных испытаний EU МАТ [8] для определения витамина D. Масса проб приведена в граммах жира (для маргарина 82%-ной жирности, для сухого молока 27%-ной жирности).
|
Таблица В.1 - Примеры аналитических систем ВЭЖХ, которые использовались для определения витамина D в анализируемых растворах проб участниками сертификационных испытаний EU МАТ [8] | ||||||||||||||||||
| ||||||||||||||||||
10
СТБ EN 12821-2012Приложение С
(обязательное)
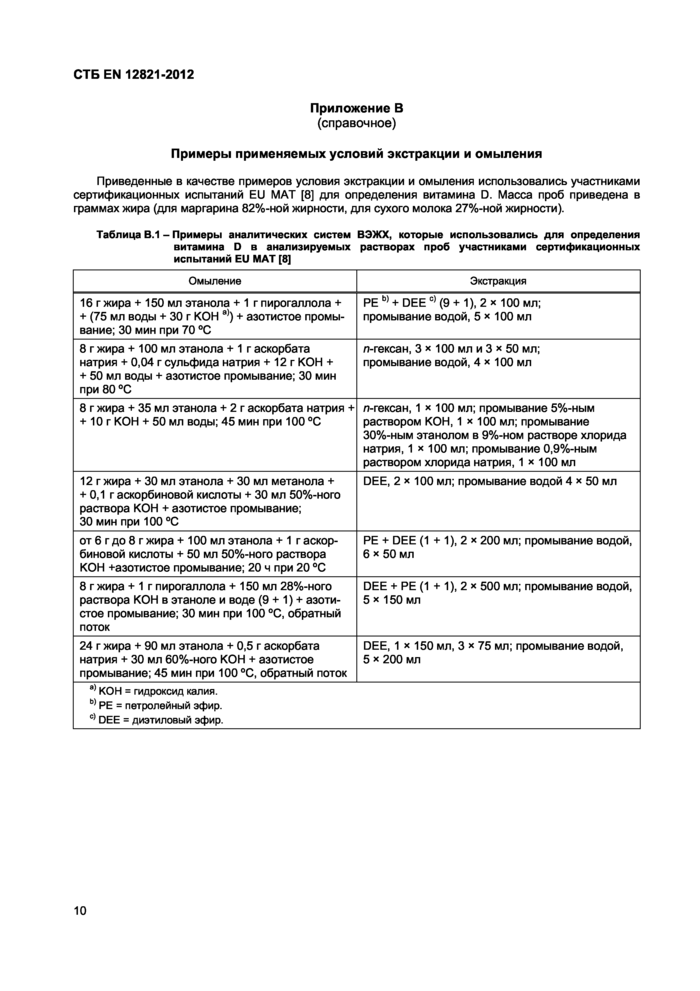
Примеры применяемых полупрепаративных и аналитических хроматограмм
X
X - время, мин; У - сигнал, условные единицы; 1 - витамин D в сухом молоке; 2 - витамин D в стандарте
Рисунок С.1 - Типичная хроматограмма нормально-фазной полупрепаративной ВЭЖХ омыленного и жидкого/сухого молока (CRM 421) и стандарта витамина D (витамин D2 и витамин D3)
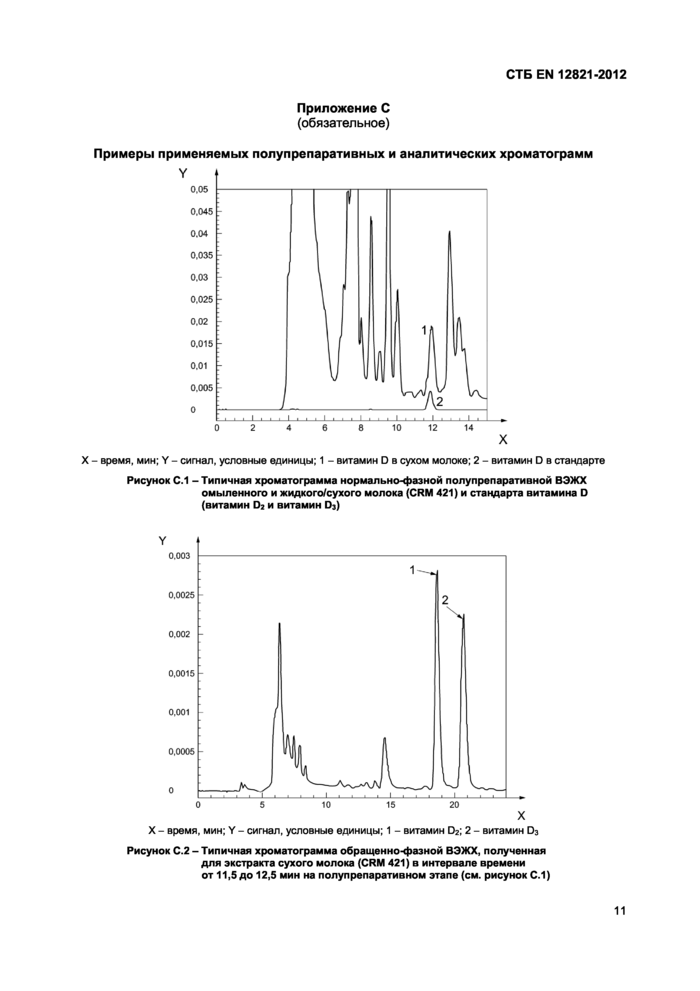
X - время, мин; Y - сигнал, условные единицы; 1 - витамин D2; 2 - витамин D3
Рисунок С.2 - Типичная хроматограмма обращенно-фазной ВЭЖХ, полученная для экстракта сухого молока (CRM 421) в интервале времени от 11,5 до 12,5 мин на полупрепаративном этапе (см. рисунок С.1)
11
Приложение D
(справочное)
Данные по прецизионности измерений
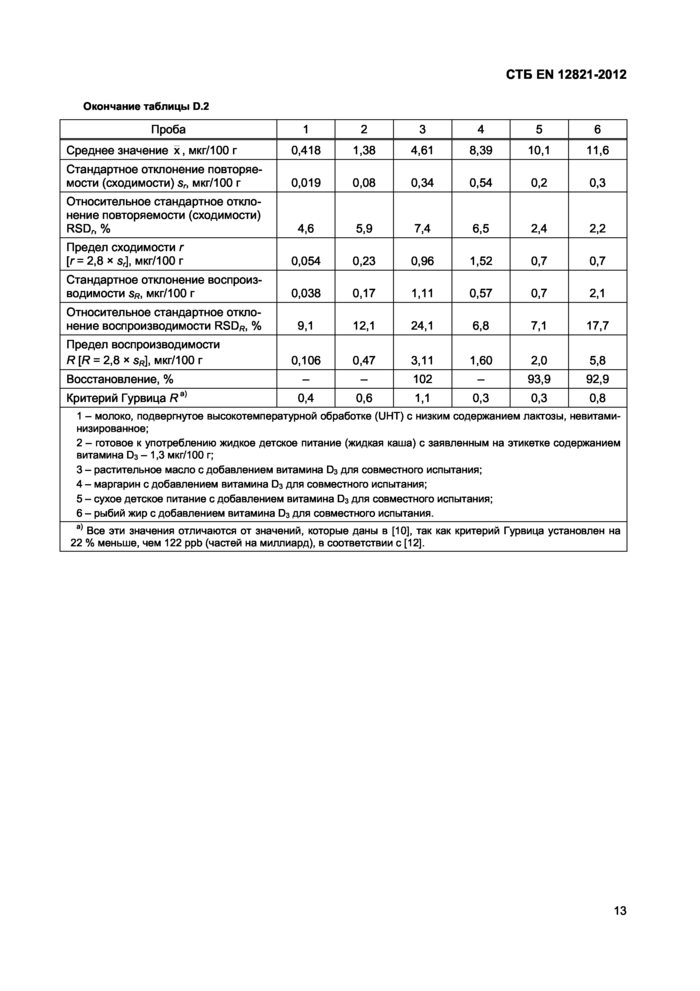
Характеристики маргарина (CRM 122), приведенные в таблице D.1, были определены в ходе межлабораторных сличений [8] в соответствии с Руководством по сертификационным испытаниям EU МАТ, [8]. Исследование было организовано правительственной химической лабораторией, Великобритания.
Характеристики молока, жидкого детского питания, растительного масла, маргарина, сухого детского питания и рыбьего жира (см. примечание к таблице D ) были определены в ходе межлабораторных сличений [8] в соответствии с Руководящими указаниями АОАС по процедурам совместных испытаний для оценки характеристик метода анализа [13]. Исследование было организовано NMKL (Скандинавским комитетом по анализу пищевых продуктов) [11]. Применявшийся метод включает омыление, экстракцию, концентрирование, препаративную ВЭЖХ и аналитическую ВЭЖХ.
|
Таблица D.1 - Данные по прецизионности измерений для маргарина и сухого молока | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица D.2-Данные по прецизионности измерений для молока, жидкого детского питания, растительного масла, маргарина, сухого детского питания и рыбьего жира | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Окончание таблицы D.2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
13
Приложение Е
(справочное)
Дополнительный этап предварительной очистки для определения витамина D с использованием препаративной тонкослойной хроматографииЕ.1 Дополнительный этап предварительной очистки с использованием препаративной тонкослойной хроматографии (TLC)
Е.1.1 Общие положения
Описанный метод тонкослойной хроматографии широко используется для предварительной очистки экстрактов витамина D перед введением препаративной ВЭЖХ. Он был проверен на кормах для поросят с 50 мкг/кг витамина D.
Он имеет следующие преимущества:
- зоны, содержащие витамин D, могут быть легко визуализированы с помощью UV-излучения. В зависимости от матрицы в отношении каждой пробы принимают решение о минимальном размере зоны для разделения D2/D3. Таким образом можно свести к минимуму помехи матрицы.
- использование многоэтапной разработки пластин для тонкослойной хроматографии может дополнительно улучшить разделение зон D2/D3 и зоны матрицы.
Недостатком этого метода является то, что он не может выполняться автоматически. Время переключения является ограниченным. Более подробная информация по данному методу приведена в [11].
Е.1.2 Сущность метода
Кратная часть сырого экстракта после омыления очищается с помощью препаративной тонкослойной хроматографии. С образца, содержащего витамин D2/D3, делают соскоб на пластину, которую перемещают в небольшую колонку для экстрагирования витамина D2/D3. Объем данного экстракта уменьшают перед применением аналитической ВЭЖХ.
Е.1.3 Реактивы
Е.1.3.1 Пластины для TLC, например силикагель 60 F 254, Merck 5715 \ 0,25 мм, 20 х 20 см.
Е.1.3.2 Бутилгидрокситолуол.
Е.1.3.3 л-гексан.
Е.1.3.4 Метанол.
Е.1.3.5 Ацетон.
Е.1.3.6 Диэтиловый эфир.
Е.1.3.7 Растворитель для проявления пластины для TLC, смесь 88 мл п-гексан, 2 мл метанола, 10 мл ацетона и 10 мг бутилгидрокситолуола.
Е.1.3.8 Растворитель для элюирования изолированной зоны витамина D2/D3, смесь 60 мл диэтилового эфира и 40 мл л-гексана.
Е.1.3.9 Стандартный раствор витамина D3, 250 мкг/мл в метаноле.
Е.1.4 Оборудование
Е.1.4.1 ТСХ камера 20 к 20 см для проявления пластин для TLC.
Е.1.4.2 Шприц 1 мл газонепроницаемый или подходящая система нанесения проб для TLC.
Е.1.4.3 UV-лампа, 254 нм.
Е.1.4.4 Открытая трубчатая стеклянная колонка, диаметр 1 см, длина около 15 см, запорный кран из политетрафторэтилена.
Е.1.4.5 Небольшой шпатель с острой кромкой.
Е.1.5 Методика
Наполняют проявочную камеру растворителем (Е.1.3.8) и ждут около 2 ч для пропитывания.
Выпаривают подходящую кратную часть сырого экстракта после омыления досуха при пониженном давлении и сразу же повторно растворяют его в 2 мл л-гексана. Наносят 1 мл из этого раствора
^Силикагель 60 F 254, Merc 5715 является примером подходящего продукта, доступного на рынке. Данная информация представлена исключительно для удобства пользователей настоящего стандарта. Это не является рекламой названных изделий со стороны CEN.
СТБ EN 12821-2012
в нескольких навесках на пластину для TLC (Е. 1.3.1), чтобы получить зону длиной 10 см и не шире 1 см. Для локализации и идентификации наносят от 5 до 10 мкп стандартного раствора витамина D3 (Е.1.3.9) на обе стороны этой зоны.
Проявляют пластину дважды почти до верхнего края. Для улучшения сортировки может оказаться целесообразным проявлять пластину в несколько этапов. Перед началом новой сортировки после последнего запуска растворитель выпаривают в потоке азота. Визуализируют выделенную зону витамина D2/D3, используя UV-излучение (Е.1.4.3), и отмечают карандашом (от 0,5 до 1,5 см). Соскабливают соответствующую зону шпателем (Е.1.4.5) на лист бумаги и переносят ее в открытую трубчатую колонку (Е.1.4.4), заполненную 10 мл растворителя (Е.1.3.8).
Витамин D2/D3 элюируют 5 раз в 10 мл растворителя (Е.1.3.8). Выпаривают комбинированные элюаты досуха при пониженном давлении и сразу же растворяют в 1 мл растворителя ВЭЖХ (раствор пробы).
Е.2 Дополнительный этап очистки с использованием колоночной хроматографииЕ.2.1 Методика
Метод очистки используют в колонке, изготовленной из полиэтиленгликоль-целита. Недостатком данного метода очистки является то, что он не может быть выполнен автоматически. Время проведения операций является ограниченным.
Е.2.2 Реактивы
Е.2.2.1 Петролейный эфир, диапазон кипения от 40 °С до 60 °С, дистиллированный.
Е.2.2.2 Петролейный эфир, диапазон кипения от 60 °С до 70 °С, дистиллированный.
Е.2.2.3 Диатомовая земля, кальцинированный поток кальцинированной соды CAS № 68855-54-9.
Е.2.2.4 Сульфат натрия.
Е.2.2.5 Полиэтиленгликоль 600.
Е.2.3 Оборудование
Е.2.3.1 Ротационный испаритель с водяной баней при 40 °С.
Е.2.3.2 Взрывозащищенный высокоскоростной измельчитель.
Е.2.3.3 Хроматографические трубки, длина 30 см, внутренний диаметр 2,5 см, оснащенные краном в нижней части для штепсельной вилки из политетрафторэтилена. Длина 10 см, внутренний диаметр 1,4 см, суженный в нижней части и оснащенный 100 мл резервуаром в верхней части.
Е.2.3.4 UV-лампа, ручная модель для длинноволнового света (366 нм).
Е.2.4 Методика
Е.2.4.1 Подготовка колонки
Готовят суспензию из 25 г диатомовой земли (Е.2.2.3) и 200 мл петролейного эфира (Е.2.2.2) в измельчителе (Е.2.3.2). При перемешивании быстро добавляют 15 мл полиэтиленгликоля (Е.2.2.5) и продолжают перемешивание в течение примерно 20 с.
Альтернативный метод подготовки суспензии с использованием метода, который производит эквивалентное измельчение в порошок полиэтиленгликоля на веществе-носителе. Наливают небольшое количество петролейного эфира (Е.2.2.2) в хроматографическую трубку (Е.2.3.3), помещают на дно деаэрированную ватную пробку и покрывают ее 1-сантиметровым слоем сульфата натрия (Е.2.2.4). Наливают суспензию в бутылку и уплотняют колонку с использованием поршня на стержне до тех пор, пока длина завершенных измерений колонки не достигнет примерно 15 см. В то же время удаляются излишки петролейного эфира. Заливают сверху 1-сантиметровым слоем сульфата натрия.
Е.2.4.2 Изготовление раствора пробы, элюирование и сбор элюата
Перекачивают экстракт из колбы с круглым дном и промывают колбу с использованием трех партий петролейного эфира (Е.2.2.2) примерно по 3 мл из каждой партии. Они также должны быть прокачены в колонку. Элюируют, используя петролейный эфир (Е.2.2.2). Удаляют первые 30 мл элюата. Собирают следующие 50 мл элюата. Продолжают этап очистки SPE (Е.З).
15
Е.З Дополнительный этап очистки с использованием SPEЕ.3.1 Методика
Настоящий раздел описывает метод очистки с использованием SPE и окиси кремния. Недостатком данного метода очистки является то, что он не может быть выполнен автоматически. Время проведения операций является ограниченным.
Е.3.2 Реактивы
Е.3.2.1 л-гептан р.а.
Е.3.2.2 Диэтиловый эфир.
Удаляет пероксиды путем ежедневной дистилляции осадка КОН после использования.
Е.3.2.3 Петролейный эфир, диапазон кипения от 40 °С до 60 °С, дистиллированный.
Е.3.3 Оборудование
Е.3.3.1 Картридж для твердофазной экстракции Silica, приблизительно 700 мг.
Е.3.3.2 Конические колбы с притертым соединением В 29.
Е.3.4 Выпаривают элюат и растворяют его в 10 мл гептана (Е.3.2.1). Активируют картридж (Е.3.3.1) с 10 мл гептана. Готовят и элюируют 10 мл экстракта пробы. Промывают, используя 10 мл 6%-ного раствора диэтилового эфира (Е.3.2.2) в гептане и элюируют с использованием 20 мл 20%-ного раствора диэтилового эфира (Е.3.2.2) в гептане. Собирают элюат в коническую колбу (Е.3.3.2), испаряют и растворяют его в 1 - 2 мл петролейного эфира (Е.3.2.3). Продолжают этап очистки TLC или полу-препартивной ВЭЖХ.
16
СТБ EN 12821-2012Библиография
[1] Johnson, Н., Hessel, Н. and Thorzell, К. Internal J. Vitamin and Nutr. Res., 1987, 57, 357 - 365 (Витамины и питательные вещества)
[2] Johnson, Н., Halen, В., Hessel, Н., Nyman, A. and Thorzell, К. Internat. J. Vitamin and Nutr. Res., 1989, 59, 262-268
(Витамины и питательные вещества)
[3] Reynolds, S. L. and Judd, H. J. The Analyst, 1984, 109, 489 - 492 (Аналитик)
[4] Bognar, A. Z. Lebensm. Unters. Forsch., 1992, 194, 469 - 475 (Исследование продуктов питания)
[5] Van den Berg, J. Agric. Fd. Chem., 1986, 34, 264 - 268
[6] Mattila, P. J., Piironen, V., Backman, C., Asunmaa, A., Uusi-Rauva, E. and Koivistoinen, P., J. Food Comp. Anal., 1992, 5, 281 - 290
(Состав и анализ продуктов питания)
[7] Lumley, I. D., Lawrence, P. R. J. Micronutrient Anal., 1990, 7, 301 -313 (Анализ микроэлементов в пище)
[8] Finglas, Р. М., van den Berg, H. and de Froidmont-Gortz, I., 1997. The certification of the mass fractions of vitamins in three reference materials: margarine (CRM 122), milk powder (CRM 421), and lyophilized Brussels sprouts powder (CRM 431). EUR-Report 18039, Commission of the European Union, Luxemburg
(Сертификация массовых долей витаминов в трех эталонных материалах: маргарин (CRM), порошковое молоко (CRM 421), лиофилизированный порошок брюссельской капусты (CRM 431))
[9] The Pharmaceutical Codex, incorporating the British Pharmaceutical Codex, 11th Edition, The Pharmaceutical Press, 1979
[10] Staffas, A., Nyman, A., J. AOAC Int., 2003, 86, 400 - 406
[11] Methode 13.8.1 (Method 13.8.1): Die Bestimmung von Vitamin D - Verfahren; in: Methodenbuch 3.4. Erganzungslieferung 1997. VDLUFA Verlag Deutschland
(Определение витамина D. Метод ВЭЖХ)
[12] Thompson, M. 2000, 125, 385 - 386
[13] AOAC International 1995, AOAC Official Methods Program, Associate Referee's Manual on development, Study, Review, and Approval Process. Part IV AOAC Guidelines for Collaborative Studies p. 23 - 51 (Программа официальных методов AOAC, руководство рецензентов ассоциации по разработке, анализу, проверке и одобрению процесса. Часть IV. Руководящие указания АОАС по совместным исследованиям)
[14] ISO 5725:1986 Precision of test methods - Determination of repeatability and reproducibility for a
standard test method by inter-laboratory tests
(Точность (правильность и прецизионность) методов и результатов измерений. Определение сходимости и воспроизводимости для стандартного метода испытаний при проведении межлабораторных испытаний)
17
Ответственный за выпуск В. Л. Гуревич
Сдано в набор 24.07.2012. Подписано в печать 10.09.2012. Формат бумаги 60x84/8. Бумага офсетная. Гарнитура Arial. Печать ризографическая. Уел. печ. л. 2,32 Уч.-изд. л. 1,20 Тираж экз. Заказ
Издатель и полиграфическое исполнение: Научно-производственное республиканское унитарное предприятие «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) ЛИ № 02330/0552843 от 08.04.2009. ул. Мележа, 3, комн. 406, 220113, Минск.
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКТЫ ПИЩЕВЫЕ Определение содержания витамина D методом высокоэффективной жидкостной хроматографии. Определение холекальциферола (D3) или эргокальциферола (D2)
ПРАДУКТЫ ХАРЧОВЫЯ Вызначэнне змяшчэння в1тамину D метадам высокаэфектыунай вадкаснай храматаграфМ. Вызначэнне холекальцыферолу (D3) або эргакальцыферолу (D2)
Foodstuffs
Determination of vitamin D by high performance liquid chromatography. Measurement of cholecalciferol (D3) or ergocalciferol (D2)
Дата введения 2013-01-01
1 Область применения
Настоящий стандарт устанавливает метод определения витамина D3 (холекальциферол) или витамина D2 (эргокальциферол) в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ).
Витамин D3 содержится преимущественно в пищевых продуктах животного происхождения, а витамин D2 - в лесных грибах. Оба витамина могут использоваться для получения обогащенных пищевых продуктов. Настоящий стандарт не распространяется на пищевые продукты, которые содержат как витамин D3, так и витамин D2.
Кроме активности основных форм витамина D, витамина D3 и витамина D2, соответствующие метаболиты 25-гидроксивитамин D и 1,25-дигидроксивитамин D также вносят свой вклад в активность витамина D.
Настоящий стандарт распространяется только на определение витаминов D3 или D2.
Стандарт обеспечивает основу для аналитических методов. Он предназначается для создания схемы, согласно которой экспериментатор сможет проводить необходимые анализы в соответствии со стандартной процедурой. Данный метод был валидирован в результате проведения межлабораторных сличений на обогащенных и необогащенных образцах таких пищевых продуктов, как маргарин, молоко, сухое молоко, жидкое питание для грудных детей, молочных смесях, растительных и рыбных жирах при концентрациях от 0,4 мкг/100 г до 14 мкг/100 г. Дополнительные данные по валидации приведены в приложении D.
2 Нормативные ссылки
Для применения настоящего стандарта необходим следующий ссылочный стандарт. Для недатированных ссылок применяют последнее издание ссылочного стандарта (включая все его изменения).
EN ISO 3696:1995 Вода для лабораторного анализа. Технические требования и методы испытаний (ISO 3696:1987)
3 Сущность метода
Витамины D2 и D3 омыляют в пищевых продуктах с использованием спиртового раствора гидроксида калия и экстрагируют с помощью подходящего растворителя. Определение витамина D2 или D3 в растворе экстракта пробы осуществляют посредством полупрепаративной нормально-фазной колонки методом ВЭЖХ с последующим определением на аналитической обращенно-фазной колонке.
Если необходимо определить витамин D3, витамин D2 используют в качестве внутреннего стандартного вещества. При определении витамина D2 используют в качестве внутреннего стандартного вещества витамин D3.
Издание официальное
Содержание витамина D определяют ультрафиолетовой (UV) спектрометрией, причем пики идентифицируют на основе времени удерживания и дополнительно по спектральным UV-профилям, если для определения используется диодная матрица. Определение проводят с помощью метода внутреннего стандартного вещества, используя площадь или высоту пиков, см. [1] - [8].
4 Реактивы4.1 Общие положения
Используют реактивы только признанной аналитической чистоты и воду не ниже 1 степени по EN ISO 3696, если иное не указано по ходу проведения анализа.
4.2 Метанол.
4.3 Этанол, объемная доля ф(С2Н5ОН) = 100 %.
4.4 Этанол, объемная доля ф(С2Н5ОН) = 96 %.
4.5 Сульфат натрия безводный.
4.6 Растворы КОН для омыления в соответствующих концентрациях, например массовая концентрация р(КОН) = 50 г/100 мл или р(КОН) = 60 г/100 мл, или спиртовые растворы, например 28 г КОН в 100 мл смеси этанол/вода с объемной долей этанола 90 %.
4.7 Антиокислительные реагенты: такие, как аскорбиновая кислота, аскорбат натрия, пирогаллол, сульфид натрия (Na2S) или бутилгидрокситолуол (ВНТ).
4.8 Растворители и экстрагирующие растворители: эфир диэтиловый (не содержащий перекиси), дихпорметан, эфир петролейный, л-гексан, этилацетат или соответствующие их смеси.
4.9 Подвижные фазы для ВЭЖХ4.9.1 Примеры смесей растворителей для нормально-фазной полупрепаративной ВЭЖХ
Примеры соответствующих смесей растворителей (даны в объемных долях) для нормальной фазы полупрепаративной ВЭ>Ю( включают:
л-гексан : 2-пропанол (98 : 2), (99 : 1) или (95 : 5);
л-гексан : изоамиаловый спирт (99 : 1);
л-гексан : 2-пропанол + тетрагидрофуран (98 : 1 : 1);
изоокган : изобутанол (99 : 1);
л-гептан : 2-пропанол (97 : 3).
4.9.2 Примеры растворителей и смесей растворителей для аналитической обращенно-фазной ВЭЖХ
Примеры соответствующих растворителей и смесей растворителей (даны в объемных долях) для аналитической обращенно-фазной ВЭЖХ включают: метанол;
метанол : вода (95 : 5) или (93 : 7);
ацетонитрил : метанол (80 : 20), (90 : 10) или (70 : 30);
ацетонитрил, хлороформ : метанол (93 : 4 : 3).
4.10 Стандартные вещества
4.10.1 Стандартное вещество эргокальциферол (витамин D2), М(С28Н440) = 396,7 г/моль. Стандартное вещество витамин D2 должно иметь наивысшую степень чистоты из всех возможных
(массовая доля более 98 %) и должно храниться в соответствии с инструкциями изготовителя (в темном месте, обычно при температуре ниже 4 °С).
4.10.2 Стандартное вещество холекальциферол (витамин D3), М(С27Н440) = 384,6 г/моль. Стандартное вещество витамин D3 должно иметь наивысшую степень чистоты из всех возможных
(массовая доля более 98 %) и должно храниться в соответствии с инструкциями изготовителя (в темном месте, обычно при температуре ниже 4 °С).
4.11 Исходные растворы4.11.1 Исходный раствор витамина D2
Взвешивают 100 мг витамина D2 (4.10.1) с точностью до 1 мг и помещают в мерную колбу объемом 100 мл, растворяют в этаноле (4.4) и этанолом доводят раствор до метки. Такой раствор содержит 1 мг/мл витамина D2. Раствор хранят в защищенном от света месте при температуре ниже 4 °С. 1
СТБ EN 12821-2012
Рассчитывают массовую концентрацию исходного раствора и массовую долю стандартного вещества витамина D2 методом, описанным в 4.12.1.
Полученный раствор остается стабильным в течение 6 мес при температуре минус 18 °С.
4.11.2 Исходный раствор витамина D3
Взвешивают 100 мг витамина D3 (4.10.2) с точностью до 1 мг и помещают в мерную колбу объемом 100 мл, растворяют в этаноле (4.4) и доводят этанолом раствор до метки. Такой раствор содержит 1 мг/мл витамина D3. Раствор хранят в защищенном от света месте при температуре ниже 4 °С.
Рассчитывают массовую концентрацию исходного раствора и массовую долю стандартного вещества витамина D в соответствии с методом, описанным в 4.12.2.
Полученный раствор остается стабильным в течение 6 мес при температуре минус 18 °С.
4.12 Стандартные растворы
4.12.1 Стандартный раствор витамина D2
Отмеряют пипеткой 1 мл исходного раствора витамина D2 и помещают в мерную колбу объемом 100 мл, растворяют этанолом (4.4) и доводят этанолом до метки. Такой раствор содержит около 10 мкг/мл витамина D2. Раствор готовят в день использования.
Примечание - Массовую концентрацию стандартного раствора можно регулировать в случае необходимости соответствовать требованиям проведения анализа.
Измеряют абсорбцию стандартного раствора витамина D2 в кварцевой кювете на 1 см при длине волны 265 нм относительно этанола (4.4). Рассчитывают массовую концентрацию витамина D2 pD2, в микрограммах на миллилитр стандартного раствора, по формуле
(Ъ2 —
Л265 ЧМР2Ч1000 бЧ6
(1)
где А265 Mq2
Е
б
1000
величина поглощения стандартного раствора витамина D2 при 265 нм; молярная масса витамина D2 (MD2 = 396,7 г/моль);
коэффициент молярной абсорбции витамина D2 (здесь: е = 18 843 м1/моль, рассчитанный из значения £^, [9]);
длина оптического пути кварцевой кюветы, см; коэффициент пересчета размерности.
4.12.2 Стандартный раствор витамина D3
Отмеряют пипеткой 1 мл исходного раствора витамина D3, помещают в мерную колбу объемом 100 мл и доводят этанолом (4.4) до метки. Такой раствор содержит около 10 мкг/мл витамина D3. Раствор готовят в день использования.
Примечание - Массовую концентрацию стандартного раствора можно регулировать в случае необходимости соответствовать требованиям проведения анализа.
Измеряют абсорбцию стандартного раствора витамина D в кварцевой кювете на 1 см при длине волны 265 нм относительно этанола (4.4). Рассчитывают массовую концентрацию витамина D3 pD2, в микрограммах на миллилитр стандартного раствора, по формуле
„ Л265 ЧМРЗЧ1000
где А2в 5 /Цэз
Е
б
1000
величина поглощения стандартного раствора витамина D при 265 нм; молярная масса витамина D3 (MD = 384,6 г/моль);
коэффициент молярной абсорбции витамина D3 (здесь: е = 18461 м1/моль, рассчитанный из значения £]*, [9]);
длина оптического пути кварцевой кюветы, см; коэффициент пересчета размерности.
4.13 Внутренние стандартные растворы4.13.1 Внутренний стандартный раствор витамина D2
Отмеряют пипеткой 1 мл исходного раствора витамина D2 (4.12.1) и помещают в мерную колбу объемом 100 мл, растворяют в этаноле (4.4) и этанолом доводят раствор до метки. Раствор готовят в день использования.
3
4.13.2 Внутренний стандартный раствор витамина D3
Отмеряют пипеткой 1 мл исходного раствора витамина D3 (4.12.2) и помещают в мерную колбу объемом 100 мл, растворяют в этаноле (4.4) и доводят этанолом раствор до метки. Раствор готовят в день использования.
Примечание - При определении витамина D3 витамин D2 используется в качестве внутреннего стандартного вещества. При определении витамина D2 витамин D3 используется в качестве внутреннего стандартного вещества.
4.14 Полупрепаративный стандартный раствор витамина D2 и витамина D3
Отмеряют пипеткой 5 мл стандартного раствора витамина D2 (4.12.1) и 5 мл стандартного раствора витамина D3 (4.12.2) в колбу ротационного испарителя и осторожно удаляют растворитель (при температуре не выше 40 °С). Повторно растворяют остатки в 100 мл подвижной фазы полупре-паративной ВЭЖХ (4.9.1).
В случае необходимости концентрацию полупрепаративного стандартного раствора можно изменять в зависимости от системы ВЭЖХ (5.4 и 5.5).
4.15 Аналитический стандартный раствор витамина D2 и витамина D3
Пипеткой переносят 5 мл стандартного раствора витамина D2 и 5 мл стандартного раствора витамина D3 в колбу ротационного испарителя и тщательно удаляют растворитель (при температуре не выше 40 °С). Повторно растворяют остатки в 50 мл подвижной фазы аналитической ВЭЖХ (4.9.2).
5 Аппаратура5.1 Общие положения
Обычное лабораторное оборудование и, в частности, следующее:
5.2 UV-спектрометр, предназначенный для измерения при длине волны 265 нм.
5.3 Ротационный испаритель с водяной баней и вакуумным устройством.
Примечание - Для заполнения вакуума рекомендуется использовать азот.
5.4 Полупрепаративная система ВЭЖХ, состоящая из насоса, приспособления для инжектирования пробы, детектора ультрафиолетового излучения, приспособлений для сбора установленных кратных порций элюента колонки и самописца или интегратора.
5.5 Аналитическая система ВЭЖХ, состоящая из насоса, устройства для инжектирования пробы, UV-детекгора и самописца интегратора или аналогичного устройства для сбора данных.
5.6 Колонки ВЭЖХ
5.6.1 Колонка полупрепаративной нормальной фазы, например силикагелевая или с циано-аминовой сшивкой, размер частиц - 5 мкм, диаметр - от 4,0 до 8,0 мм, длина - от 250 до 300 мм. Более подробная информация приведена в приложении А.
5.6.2 Колонка аналитическая обращенно-фазная, например, с обращенной фазой С18, размер частиц - 5 мкм, диаметр - от 4,0 до 4,6 мм, длина - 250 мм. Более подробная информация приведена в приложении А.
5.6.3 Наполнители
Можно использовать другие размеры частиц и параметры колонки, чем указанные в настоящем стандарте, но аналитик должен быть уверен в том, что обеспечивается необходимое отделение витаминов D от примесей и что будут получены эквивалентные результаты.
5.7 Фильтровальное устройство
Фильтровальные устройства в крупногабаритном или малогабаритном исполнении для фильтрования, соответственно, подвижных фаз ВЭЖХ и растворов проб, имеющие, например, поры размером приблизительно 0,45 мкм.
Примечание - Фильтрование подвижной фазы, а также раствора пробы через мембранный фильтр перед использованием или инжектированием обычно увеличивает срок службы колонок.
6 Проведение анализа6.1 Общие положения
Витамин D2 и витамин D3 чувствительны к ультрафиолетовому излучению и окисляющим воздействиям (например, воздействию атмосферного кислорода). Поэтому необходимо исключить ультра- 2
СТБ EN 12821-2012
фиолетовое излучение, используя лабораторную посуду из янтарного стекла, алюминиевую фольгу или материалы, поглощающие UV-излучение. К растворам, содержащим экстрагированные витамины, следует добавлять антиокислительные реагенты, а также использовать ток азота. Растворители должны испаряться при пониженном давлении с использованием ротационного испарителя при температуре не выше 40 °С.
6.2 Подготовка пробы для анализа
Анализируемую пробу гомогенизируют. Крупный материал полностью измельчают и гомогенизируют в блендере для пищевых продуктов. Чтобы проба в течение длительного времени не подвергалась воздействию высоких температур, в целях предосторожности ее заранее охлаждают. После этой подготовки следует незамедлительно проводить анализ пробы. Пробы следует защищать от света.
6.3 Приготовление анализируемого раствора пробы6.3.1 Омыление
Навеску исследуемого образца массой 10 - 30 г помещают в колбу, добавляют этанол (4.4), воду, антиокислительный реагент (4.7) и раствор гидроксида калия (4.6), хорошо перемешивают. Омыление проводят в токе азота. Антиокислительные реагенты следует добавлять перед добавлением раствора гидроксида калия. Можно также добавлять сульфид натрия (4.7) во избежание окислительных каталитических воздействий от следов металлов.
При определении витамина D3 в колбу для омыления добавляют пипеткой соответствующее количество внутреннего стандартного раствора витамина D2 (4.13.1). Количество добавленного внутреннего стандартного раствора витамина D2 должно соответствовать количеству витамина D3, ожидаемого в пробе. Если определяют содержание витамина D2, тогда в качестве внутреннего стандарта добавляют стандартный раствор витамина D3 (4.13.2).
В ходе выполнения процедуры анализа следует производить отбор пробы, которая не содержит внутренний стандарт, чтобы не происходило наложения матрицы пробы во время удерживания внутреннего стандарта.
В таблице 1 приведены примеры применяемых количественных соотношений реактивов:
|
Таблица 1 - Примеры количественных соотношений реактивов | ||||||||||
|
Обычное время омыления составляет от 20 до 45 мин при температурах от 70 °С до 100 °С. Омыление можно проводить также в течение ночи (примерно 16 ч) при комнатной температуре, при этом остальные условия должны остаться неизменными.
Если после омыления и охлаждения на поверхности омыленной смеси присутствует жир или масло, то необходимо добавить дополнительное количество раствора гидроксида калия в этаноле и увеличить время омыления.
Примечание - Условия, подходящие для омыления пробы маргарина и пробы сухого молока, приведены в приложении В.
6.3.2 Экстрагирование
Во избежание образования эмульсий в подвергнутый омылению раствор пробы следует добавить столько воды, чтобы соотношение спирта и воды в конечном растворе составляло 1:1.
Экстрагируют витамины D2 и D3 из охлажденной омыленной смеси, используя подходящий растворитель или смесь растворителей (4.8) и повторяют данную процедуру от двух до четырех раз с объемами в диапазоне от 100 до 200 мл. Промывают водой объединенные экстракты до нейтральной реакции pH (обычно 5 раз с объемами от 50 л до 100 мл).
Примечание - Некоторые методы предписывают промывание до нейтральной реакции 3%-ным или 5%-ным раствором гидроксида калия в 0,9%-ном растворе хлорида натрия, которому приданы буферные свойства раствором ацетата натрия (2,6 моль/л) (pH = 7) или похожими смесями. Условия экстрагирования, которые оказались подходящими для пробы маргарина и пробы сухого молока, приведены в приложении В.
6.3.3 Концентрирование
Экстракты проб выпаривают в ротационном испарителе (5.3) при сниженном давлении и максимальной температуре не выше 40 °С. Перед выпариванием в экстракт пробы рекомендуется доба-
5
вить антиокислительный реагент (например, 2 мл бутилгидрокситолуола (ВНТ) в л-гексане с концентрацией 1 мг/мл).
В концентрированный экстракт пробы необходимо добавлять абсолютный этанол (4.3) или безводный сульфат натрия (4.5), чтобы способствовать удалению следов воды (азеотропная дистилляция).
На данной стадии проведения анализа с целью исключения потенциальных посторонних воздействий можно провести дополнительную очистку экстракта пробы. В этом случае необходимо использовать полностью валидированную (утвержденную) методику.
Примечание - Приложение Е устанавливает три различных метода дополнительной очистки. Всегда полезно комбинировать метод дополнительной очистки с использованием колоночной хроматографии (Е.2) и метод с использованием SPE (solid phase extraction - твердофазная экстракция) (Е.З), как было показано для пищевых продуктов, например для маргарина и растительного масла. Метод дополнительной очистки с использованием препаративной тонкослойной хроматографии TLC (thin layer chromatography) (Е.1) предпочтительнее использовать для кормов и добавок, например, в таблетках или капсулах. При испытаниях добавок он может применяться при необходимости с Е.З.
6.3.4 Разведение
Остаток повторно растворяют в небольшом заданном количестве растворителя, который совместим с полупрепаративной системой ВЭЖХ. Добавление небольшого количества безводного сульфата натрия устраняет оставшиеся следы воды.
6.4 Калибровка
Для калибровки полупрепаративной (5.6.1) и аналитической (5.6.2) систем ВЭЖХ, а также для оценки пригодности этих систем используют стандартные растворы витамина D (4.12.1) и витамина D3 (4.12.2).
6.5 Обеспечение пригодности системы ВЭЖХ
Хроматографируют смешанный полупрепаративный стандартный раствор витаминов D2 и D3 (4.14), используя полупрепаративную систему ВЭЖХ (5.6.1) до тех пор, пока единственный пик витамина D не будет элюирован с воспроизводимым временем удержания. Это позволяет точно установить диапазон фракции витамина D из экстрактов пробы.
Хроматографические условия полупрепаративной ВЭЖХ должны устанавливаться так, чтобы достигалось оптимальное отделение витамина D от токоферолов и других примесей из исходного пищевого продукта. Примеры хроматограмм указаны в приложении С.
Хроматографируют смешанный аналитический стандартный раствор витаминов D2 и D3 (4.15), используя аналитическую систему ВЭЖХ, и настраивают хроматографические условия так, чтобы разделение витаминов D2 и D3 составляло как минимум 98 % (т. е. коэффициент разделения должен составлять более 1,0) и чтобы эти витамины были отделены от всех примесей из исходного пищевого продукта.
6.6 Определение6.6.1 Полупрепаративная ВЭЖХ
Инжектируют кратную порцию концентрированного экстракта пробы в полупрепаративную систему ВЭЖХ (5.6.1) и собирают фракцию витамина D в заданном отрезке диапазона. Временной интервал для сбора фракции должен быть заранее установлен с использованием стандартного раствора витамина D (6.5). Диапазон должен быть достаточно широким для сбора всех фракций витамина D, но при этом достаточно узким для исключения попадания токоферолов или других примесей.
Типичная полупрепаративная хроматограмма показана в приложении С.
6.6.2 Аналитическая ВЭЖХ
Фракцию из заданного отрезка диапазона для полупрепаративной ВЭЖХ выпаривают до сухого состояния и повторно растворяют в растворителе, совместимом с подвижной фазой аналитической ВЭЖХ.
Кратные порции экстракта пробы инжектируют в аналитическую систему ВЭЖХ, после чего идентифицируют пики витаминов D2 и D3 (6.6.3). Пики витаминов D2 и D3 должны быть отделены от примесей из исследуемой пробы пищевого продукта.
Типичная аналитическая хроматограмма показана в приложении С.
6
СТБ EN 12821-20126.6.3 Идентификация
Идентифицируют витамины D2 и D3, сравнивая время удержания на хроматограммах анализируемого раствора пробы со временем удержания стандартных растворов при одинаковых хроматографических условиях (6.5). Использование детектора диодной матрицы позволяет тщательно проверить ультрафиолетовые спектры пиков витамина D и оценить чистоту пиков. Эту проверку можно также осуществлять путем повторной хроматографии экстракта пробы при различных длинах волн UV-детекгора.
6.6.4 Количество определений
Следует проводить не менее двух независимых определений.
6.7 Метод внутреннего стандарта и коэффициент чувствительности
Рассчитывают коэффициент чувствительности Rf витамина D3 в сравнении с D2 по методу внутреннего стандарта, используя заданные стандартные концентрации (4.13) по формуле
_ STD3
JSTD2
(3)
R, =
^етп3 Ч Р
nSTD2 4PSTD3
где j4Std3 - полученная для стандартного раствора витамина D3 площадь пика или высота пика; ASTD2 - полученная для стандартного раствора витамина D2 площадь пика или высота пика; Pstd2 - массовая конце трация витамина D2 в стандартном растворе, мкг/мл;
Pstd3 - массовая конце трация витамина D3 в стандартном растворе, мкг/мл.
7 Расчет
Массовую долю витамина D3 wD3, мкг/100 г, рассчитывают по формуле
(4)
w _^sd34/s4100 03 ASD24Rf4 т’
где Is - масса в испытуемом образце внутреннего стандарта витамина D2, мкг; т - масса пробы, взятой для омыления, г;
Rf - см. уравнение (3); j4SD3 - полученная для витамина D3 площадь пика или высота пика в растворе пробы; ^sd2 ~ полученная для витамина D2 площадь пика или высота пика в растворе пробы.
8 Прецизионность8.1 Краткий статистический обзор
Данные прецизионности различных методов ВЭЖХ для определения витамина D3 были получены в 1994 г. при проведении международных сличительных испытаний, организованных по Программе измерений и испытаний стандартов Европейской комиссии, на пробе маргарина (сертифицированный референсный материал - CRM 122) и на пробе сухого молока (CRM 421) и позволили получить статистические данные, указанные в приложении D.
Данные по прецизионности, полученные на овсяной каше и сухом молоке, были получены при проведении межлабораторных сличений посредством метода, использующего расчеты, основанные на внешнем стандарте в соответствии с ISO 5725:1986, и приведены в приложении D.
Данные по прецизионности, полученные на молоке, жидких молочных смесях для питания грудных детей, растительном масле, маргарине, молочных смесях для питания грудных детей и рыбьем жире, были установлены в межлабораторных сличениях в соответствии с Руководящими указаниями АОАС по процедурам совместных испытаний для утверждения метода анализа (см. приложение D).
Данные, полученные в ходе проведения этих сличительных испытаний могут оказаться неприменимыми для других диапазонов концентрации определяемого вещества и матриц проб, отличающихся от приведенных в приложении D.
8.2 Повторяемость (сходимость)
Абсолютная разность между двумя отдельными результатами, полученными одним наблюдателем на идентичном анализируемом материале с помощью одной и той же аппаратуры в течение как можно более короткого отрезка времени, не должна превышать значения предела сходимости г более чем в 5 % случаев.
7
|
СТБ EN 12821-2012 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
9 Протокол анализа
Протокол анализа должен содержать как минимум следующие данные:
a) всю информацию, необходимую для идентификации пробы;
b) ссылку на настоящий стандарт или используемый метод;
c) результаты и единицы измерения, в которых они выражены;
d) дату и метод отбора проб (если он известен);
e) дату поступления проб;
f) дату проведения анализа;
д) любые особенности, отмеченные в ходе проведения анализа;
h) любые наблюдения, не установленные настоящим методом или рассматриваемые в качестве дополнительных, которые могут повлиять на результаты.
8
1
2