МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ Государственное образовательное учреждение высшего профессионального образования НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
ВОДЫ ПОДЗЕМНЫЕ.
МЕТОДИКА ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ КАРБОНАТ ГИДРОКАРБОНАТ-ИОНОВ И СВОБОДНОЙ УГОЛЬНОЙ КИСЛОТЫ ТИТРИМЕТРИЧЕСКИМ И ПОТЕНЦИОМЕТРИЧЕСКИМ МЕТОДАМИ
Регистрационный номер в Информационном фонде по обеспечению единства измерений ФР.1.31.2011.09190
Аттестована аккредитованной метрологической службой ТПУ Аттестат об аккредитации № РОСС RU 01.00143-08 от 03.04.08
Томск 2010
СВЕДЕНИЯ О МЕТОДИКЕ
РАЗРАБОТАНА Проблемной научно-исследовательской лабораторией гидрогеохимии научно-образовательного центра «Вода» Национального исследовательского Томского политехнического университета 634050, г. Томск, пр. Ленина, 2, стр.5 тел/факс: (3822) 41-90-68 e-mail: unpc_voda@tpu.ru
Центром метрологии ТПУ
634050, г. Томск, пр. Ленина, 30, тел/факс: (3822) 41-67-29 e-mail: metrolog@tpu.ru
СВЕДЕНИЯ ОБ АТТЕСТАЦИИ
АТТЕСТОВАНА аккредитованной метрологической службой
Томского политехнического университета,
аттестат об аккредитации № РОСС RU 01.00143-08 от 03.04.08
634050, г. Томск, пр. Ленина, 30, тел/факс: (3822) 41-67-29 e-mail: metrolog@tpu.ru
Свидетельство об аттестации методики измерений МУ 08-47/262, выдано 8 декабря 2010 г.
СВЕДЕНИЯ О РЕГИСТРАЦИИ Регистрационный номер в Информационном фонде по обеспечению единства измерений
ФР 1.31.2011.09190
Введена впервые
9 ПОДГОТОВКА К ВЫПОЛНЕНИЮ ИЗМЕРЕНИЙ
9.1 Подготовка лабораторной посуды
Новую лабораторную стеклянную посуду, пипетки промывают азотной кислотой и многократно дистиллированной водой.
9.2 Приготовление растворов
Для приготовления реактивов используют дистиллированную воду, предварительно освобожденную от С02 кипячением в течение 15 мин, а затем быстро охлажденную. Воду хранят в колбе, закрытой хлоркальциевой трубкой, заполненной натронной известью не более 1 месяца.
9.2.1 Раствор соляной кислоты молярной концентрации
С(/УС/)=0,5 моль/дм3 готовят в соответствии с инструкцией по приготовлению растворов из ГСО или стандарт-титров (0,1 моль/дм3), используя для разведения дистиллированную воду. При использовании стандарт-титра или ГСО молярной концентрации 0,1 моль/дм3 объем раствора доводят до 200 см3; при использовании ГСО молярной концентрации 1,0 моль/дм3-до 2,0 дм3.
9.2.2 Раствор соляной кислоты молярной концентрации
С(НС/)=0,1 моль/дм3 готовят в соответствии с инструкцией по приготовлению растворов из ГСО или стандарт-титров, используя для разведения дистиллированную воду.
Допустимо приготовление раствора соляной кислоты концентрации С(НС/)= 0,1 моль/дм3 по ГОСТ 4919.2: в мерную колбу вместимостью 1000 см3 с небольшим количеством обессоленной воды осторожно вводят 8,5 см3 концентрированной соляной кислоты (плотность 1,19 г/см3) (9,0 см3 при плотности 1,17 г/см3), после чего доводят объем раствора до метки дистиллированной водой. В этом случае коэффициент поправки к концентрации соляной кислоты устанавливают по раствору натрия углекислого С(Ма2С03) = 0,1 моль/дм3 согласно ГОСТ 25794.1. Коэффициент поправки основного раствора рекомендуется проверять один раз в месяц.
Основной раствор соляной кислоты хранят в закрытой стеклянной посуде при комнатной температуре в местах, защищенных от попадания прямых солнечных лучей. Срок хранения 6 месяцев.
6
9.2.3 Раствор соляной кислоты молярной концентрации
С (НС1) я 0,05 моль/дм3
В мерную колбу вместимостью 500 см3 помещают 250 см3 раствора соляной кислоты молярной концентрации 0,1 моль/дм3, объем раствора доводят до метки дистиллированной водой и тщательно перемешивают. Поправочный коэффициент устанавливают каждый раз перед использованием.
Раствор соляной кислоты хранят в закрытой стеклянной посуде при комнатной температуре в местах, защищенных от попадания прямых солнечных лучей. Срок хранения раствора 3 месяца.
9.2.4 Раствор соляной кислоты молярной концентрации
С (ЯС/) = 0,02 моль/дм3
В мерную колбу вместимостью 500 см3 помещают 100 см3 раствора соляной кислоты молярной концентрации 0,1 моль/дм3, объем раствора доводят до метки дистиллированной водой и тщательно перемешивают.
Раствор соляной кислоты хранят в закрытой стеклянной посуде при комнатной температуре в местах, защищенных от попадания прямых солнечных лучей. Срок хранения раствора 3 месяца.
9.2.5 Раствор гидроксида натрия молярной концентрации
С (NaOH) = 0,1 моль/дм3 готовят в соответствии с инструкцией по приготовлению растворов из стандарт-титров, используя для разведения дистиллированную воду.
Раствор хранят в закрытой емкости из полимерного материала при комнатной температуре в местах, защищенных от попадания прямых солнечных лучей. Срок хранения раствора 1 месяц.
9.2.6 Образцовые буферные растворы с аттестованным значением pH 4,01; 6,86 и 9,18 при температуре 25 °С (для потенциометрического титрования)
Образцовые буферные растворы с аттестованными значениями pH 4,01; 6,86 и 9,18 при температуре 25 “С готовят и хранят в соответствии с инструкцией к стандарт-титрам буферных растворов для рН-метрии.
7
9.2.7 Индикаторы
9.2.7.1 Раствор метилового оранжевого с массовой долей 0,1%
Навеску (0,1 ±0,005) г метилового оранжевого помещают в мерную склянку на 100 см3, добавляют 80 см3 горячей дистиллированной воды, после охлаждения доводят объем раствора до метки дистиллированной водой.
Реактив хранят в склянке из темного стекла. Раствор устойчив в течение года.
3.2.7.2 Раствор фенолфталеина с массовой долей 1%
Навеску (1,0±0,1) г фенолфталеина помещают в мерную склянку на 100 см3, добавляют 80 см3 этилового спирта и доводят до метки дистиллированной водой. С целью нейтрализации полученной жидкости добавляют раствор щелочи с (NaOH) = 0,1 моль/дм3 (до появления устойчивой слабой розовой окраски).
Реактив хранят в склянке из темного стекла. Раствор устойчив в течение 6 месяцев.
9.3 ПРЕДВАРИТЕЛЬНАЯ ПОДГОТОВКА ПРОБ
Если в анализируемой воде присутствуют взвешенные вещества, пробу предварительно фильтруют через бумажные обеззоленные или стеклянные фильтры.
9.4 ПОДГОТОВКА ПРИБОРА
Подготовку pH-метра, стеклянного и хлорсеребряного электродов к работе проводят в соответствии с руководством по эксплуатации pH-метра и паспортами на электроды.
Градуировку pH-метра проводят по образцовым буферным растворам в соответствии с руководством по эксплуатации pH-метра и инструкцией по применению буферных растворов.
Проверку pH-метра и электродов осуществляют в соответствии с руководством по эксплуатации pH-метра или в случае отсутствия указаний в руководстве - при проведении каждой серии анализов по любым двум буферным растворам. Если отклонение измеренной величины pH от заданной превышает 0,05 ед. pH, то градуировку pH-метра проводят заново.
8
10 ТИТРИМЕТРИЧЕСКИЙ МЕТОД С ВИЗУАЛЬНЫМ ФИКСИРОВАНИЕМ
КОНЕЧНОЙ ТОЧКИ ТИТРОВАНИЯ
10.1 Сущность метода
Определение карбонат-(С032") и гидрокарбонат-ионов (HCOf) проводят путем последовательного титрования соляной кислотой молярной концентрации 0,1 или 0,5 моль/дм3 в зависимости от ожидаемой концентрации карбонат- и гидрокарбонат-ионов. Методика применима для анализа вод в диапазоне значений pH от 3,5 до 9,5.
Первая стадия соответствует оттитровыванию ионов СО32~ до НСО~, по окончании первой стадии pH раствора составляет примерно 8,3, поэтому первую точку конца титрования устанавливают по фенолфталеину.
Во второй стадии ионы НСО~ оттитровываются до НгСОъ, по окончании раствор имеет значение рН~4,5, поэтому вторую точку конца титрования устанавливают по метиловому оранжевому.
Титрование проводят по схеме (рисунок 2).
|
|
Рисунок 2 - Схема последовательного определения карбонат- и гидрокарбонат-ионов |
Методика не применима для анализа вод, содержащих анионы гуминовых и других природных органических кислот. В этом случае результат анализа следует
9
представлять как общую щелочность пробы, а не только содержание карбонат- и гидрокарбонат-ионов.
При определении ионов карбонатной системы рекомендуется избегать контакта пробы воды с атмосферой.
Определение свободной угольной кислоты возможно в водах, не содержащих ионов, обуславливающих свободную кислотность (Я+, HS~, -СООН).
Определение свободной угольной кислоты (С02) в водных растворах основано на количественном переводе С02 в НС02 с последующим определением гидрокарбонат-ионов титриметрическим методом. В качестве титранта используют раствор гидроксида натрия молярной концентрации c(NaOH) = 0,1 моль/дм3. Точку эквивалентности фиксируют по изменению окраски раствора с использованием индикатора фенолфталеина.
|
|
Титрование |
|
Проба + 3-5 капель |
|
раствором NaOH |
|
фенолфталеина; |
|
до pH 4 |
|
раствор бесцветный |
|
со2 +он~ -> нсо; |
|
|
|
слабо-розовая окраска |
Рисунок 3 - Схема определения свободной угольной кислоты
10.2 Выполнение измерений массовой концентрации карбонат-, гидрокарбонат-ионов и свободной угольной кислоты
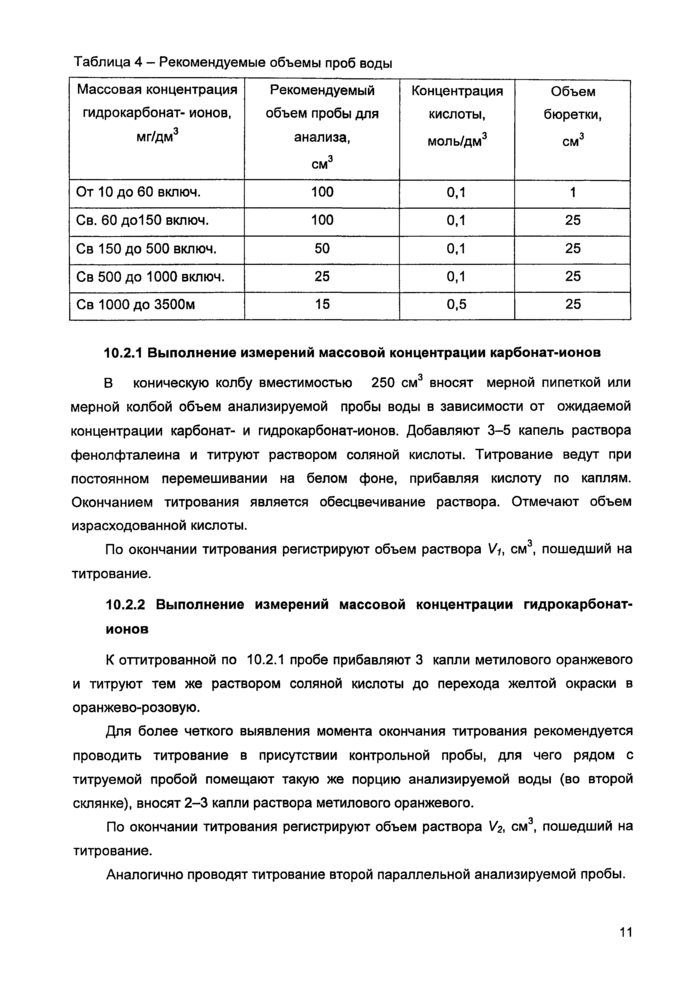
В зависимости от ожидаемой концентрации карбонат- и гидрокарбонат-ионов в качестве титранта используют соляную кислоту молярной концентрации 0,1 или 0,5 моль/см3. Рекомендуемый объем пробы воды, концентрация титранта и объем бюретки приведены в таблице 4.
Одновременно проводят анализ двух параллельных проб.
10
|
Таблица 4 - Рекомендуемые объемы проб воды |
|
Массовая концентрация гидрокарбонат- ионов, мг/дм3 |
Рекомендуемый объем пробы для анализа, см3 |
Концентрация
кислоты,
моль/дм3 |
Объем
бюретки,
см3 |
|
От 10 до 60 включ. |
100 |
0,1 |
1 |
|
Св. 60 до 150 включ. |
100 |
0,1 |
25 |
|
Св 150 до 500 включ. |
50 |
0,1 |
25 |
|
Св 500 до 1000 включ. |
25 |
0,1 |
25 |
|
Св 1000 до 3500м |
15 |
0,5 |
25 |
|
10.2.1 Выполнение измерений массовой концентрации карбонат-ионов
В коническую колбу вместимостью 250 см3 вносят мерной пипеткой или мерной колбой объем анализируемой пробы воды в зависимости от ожидаемой концентрации карбонат- и гидрокарбонат-ионов. Добавляют 3-5 капель раствора фенолфталеина и титруют раствором соляной кислоты. Титрование ведут при постоянном перемешивании на белом фоне, прибавляя кислоту по каплям. Окончанием титрования является обесцвечивание раствора. Отмечают объем израсходованной кислоты.
По окончании титрования регистрируют объем раствора Vi, см3, пошедший на титрование.
10.2.2 Выполнение измерений массовой концентрации гидрокарбонат-
ионов
К оттитрованной по 10.2.1 пробе прибавляют 3 капли метилового оранжевого и титруют тем же раствором соляной кислоты до перехода желтой окраски в оранжево-розовую.
Для более четкого выявления момента окончания титрования рекомендуется проводить титрование в присутствии контрольной пробы, для чего рядом с титруемой пробой помещают такую же порцию анализируемой воды (во второй склянке), вносят 2-3 капли раствора метилового оранжевого.
По окончании титрования регистрируют объем раствора V2, см3, пошедший на титрование.
Аналогично проводят титрование второй параллельной анализируемой пробы.
11
10.2.3 Выполнение измерений массовой концентрации гидрокарбонат-
ионов в отсутствии карбонат-ионов
В коническую колбу вместимостью 250 см3 вносят мерной пипеткой или мерной колбой объем анализируемой пробы воды в зависимости от ожидаемой концентрации гидрокарбонат-ионов. Рекомендуемые объемы проб воды приведены в таблице 4. Добавляют 3 капли раствора метилового оранжевого и титруют раствором соляной кислоты. Титрование ведут при постоянном перемешивании на белом фоне, прибавляя кислоту по каплям. Окончанием титрования является изменение цвета раствора из желтого в оранжево-розовую.
По окончании титрования регистрируют объем раствора V2, см3, пошедший на титрование.
Аналогично проводят титрование второй параллельной анализируемой пробы.
10.2.4 Выполнение измерений массовой концентрации свободной
угольной кислоты
Рекомендуемый объем пробы воды и объем бюретки приведены в таблице 5. В коническую колбу вместимостью 1000 (500) см3 вносят мерной колбой (цилиндром) объем анализируемой пробы воды в соответствии с рекомендациями таблицы 5.
|
Таблица 5 - Рекомендуемые объемы проб воды и объем бюретки |
|
Массовая концентрация свободной угольной кислоты, мг/дм3 |
Рекомендуемый объем пробы для анализа, см3 |
Объем бюретки, см3 |
|
От 2,0 до 8,0 включ. |
500 |
1 |
|
Св.8,0 до 60 включ. |
500 |
10 |
|
Св.60 до 100 включ. |
250 |
10 |
|
Добавляют 3-5 капель раствора фенолфталеина и титруют жидкость раствором гидроксида натрия молярной концентрации c(NaOH) = 0,1 моль/дм3 до появления слабого розового окрашивания. Появляющаяся розовая окраска быстро исчезает из-за медленной реакции гидратации по уравнению
С02+Н20 = Н2С0г
Титрование ведут до устойчивой окраски раствора, не исчезающей и не бледнеющей в течение 3-5 минут. Регистрируют расход раствора гидроокиси натрия до достижения устойчивой окраски индикатора.
12
По окончании титрования по бюретке отсчитывают объем раствора гидроксида натрия а , пошедший на титрование.
Аналогично проводят титрование второй параллельной анализируемой пробы.
11 МЕТОД ПОТЕНЦИОМЕТРИЧЕСКОГО ТИТРОВАНИЯ
11.1 Сущность метода
Потенциометрический метод основан на установлении конечной точки титрования по зависимости равновесного потенциала индикаторного электрода от состава раствора. Для определения гидрокарбонат- и карбонат-ионов в качестве индикаторного применяют стеклянный электрод. Титрование проводят в две стадии: до значения pH 8,2 (определение карбонат-ионов) и pH 4,5 (определение гидрокарбонат-ионов).
Одновременно проводят анализ двух параллельных проб.
11.2 Выполнение измерений массовой концентрации карбонат- и гидрокарбонат- ионов
В зависимости от ожидаемой концентрации ионов используют соляную кислоту молярной концентрации 0,02; 0,05, 0,1 или 0,5 моль/см3. Рекомендуемый объем пробы и концентрация титранта приведены в таблице 6.
|
Таблица 6 - Рекомендуемые объемы проб воды и концентрации соляной кислоты |
|
Массовая концентрация |
Рекомендуемый объем |
Концентрация соляной |
|
гидрокарбонат ионов, |
пробы для анализа, |
кислоты, |
|
мг/дм3 |
см3 |
моль/дм3 |
|
От 10 до 50 включ. |
50 |
0,02 |
|
Св. 50 до 150 включ. |
25 |
0,02 |
|
Св.150 до 600 включ. |
25 |
0,05 |
|
Св.600 до 1500 включ. |
25 |
0,1 |
|
Св.1500 до 6000 включ. |
25 |
0,5 |
|
В стакан вместимостью 250 (100) см3 вносят объем анализируемой пробы воды. В раствор погружают стеклянный (индикаторный) и хлорсеребряный (электрод сравнения) электроды. Стакан устанавливают на магнитную мешалку и перемешивают со скоростью, при которой не образуется воронка. Титрование ведут раствором соляной кислоты при постоянном перемешивании до pH 8,2, вблизи точки эквивалентности прибавляя кислоту по каплям.
По окончании титрования по бюретке регистрируют объем раствора Vi, см3, пошедший на титрование карбонат-ионов.
13
Продолжают титрование пробы воды тем же раствором соляной кислоты до pH4,5, близи точки эквивалентности прибавляя кислоту по каплям.
По окончании титрования регистрируют объем раствора Vz, см3, пошедший на титрование гидрокарбонат-ионов.
Аналогично проводят титрование второй параллельной анализируемой пробы.
11.3 Выполнение измерений массовой концентрации гидрокарбонат-ионов
в отсутствии карбонат-ионов
В стакан вместимостью 250 (100) см3 вносят объем анализируемой пробы воды. В раствор погружают стеклянный и хлорсеребряный электроды. Стакан устанавливают на магнитную мешалку, титрование ведут раствором соляной кислоты при постоянном перемешивании до pH4,0, близи точки эквивалентности прибавляя кислоту по каплям.
По окончании титрования по бюретке отсчитывают объем раствора V2, см3, пошедший на титрование
Аналогично проводят титрование второй параллельной анализируемой пробы.
14
12.1 Массовую концентрацию карбонат-ионов (Ссо?_), мг/дм3 вычисляют по формуле
„ _ 2VX • С-30-1000
LCOl у
Массовую концентрацию гидрокарбонат-ионов (Снсо.), мг/дм3, вычисляют по
формуле (при титровании по разделам 10.2.3 и 11.3 Vt=0)
„ (F2-F,)-C-6M000
CHCOi у '
где Vi- объем раствора соляной кислоты, пошедший на титрование, с фенолфталеином, см3;
V2- объем раствора соляной кислоты, пошедший на титрование, с метиловым оранжевым, см3;
С - молярная концентрация раствора соляной кислоты, моль/дм3;
30 - эквивалентный вес карбонат-ионов;
61 - эквивалентный вес гидрокарбонат-ионов;
V - объем пробы воды, взятый на анализ, см3.
Формулы расчетов даны с учетом того, что коэффициент поправки растворов HCI равен 1.
12.2 Массовую концентрацию свободной угольной кислоты Сс0г, мг/дм3, вычисляют по формуле
„ я-С-44-1000
ССОг - у
а- объем раствора гидроксида натрия, пошедший на титрование, см3;
С - молярная концентрация раствора гидроксида натрия, моль/дм3;
44 - эквивалентный вес С02 в данной реакции;
V - объем пробы воды, взятый на анализ, см3
Формула расчета дана с учетом того, что коэффициент поправки раствора гидроокиси натрия молярной концентрации c(NaOH) = 0,1 моль/дм3 равен 1.
12.3 Вычисления проводят для каждой из двух параллельных проб, получая Х{ и Х2 соответственно.
15
Министерство образования и науки РФ Государственное образовательное учреждение высшего профессионального образования «НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» АККРЕДИТОВАННАЯ МЕТРОЛОД^Н^А^ СЛУЖБА ТПУ (Аттестат об аккредитации Ха РОС^Ш^ИадЙ^ от 03.04.08)
him iu1t> VI
lb
2010 г.
<ЙВйагаи*
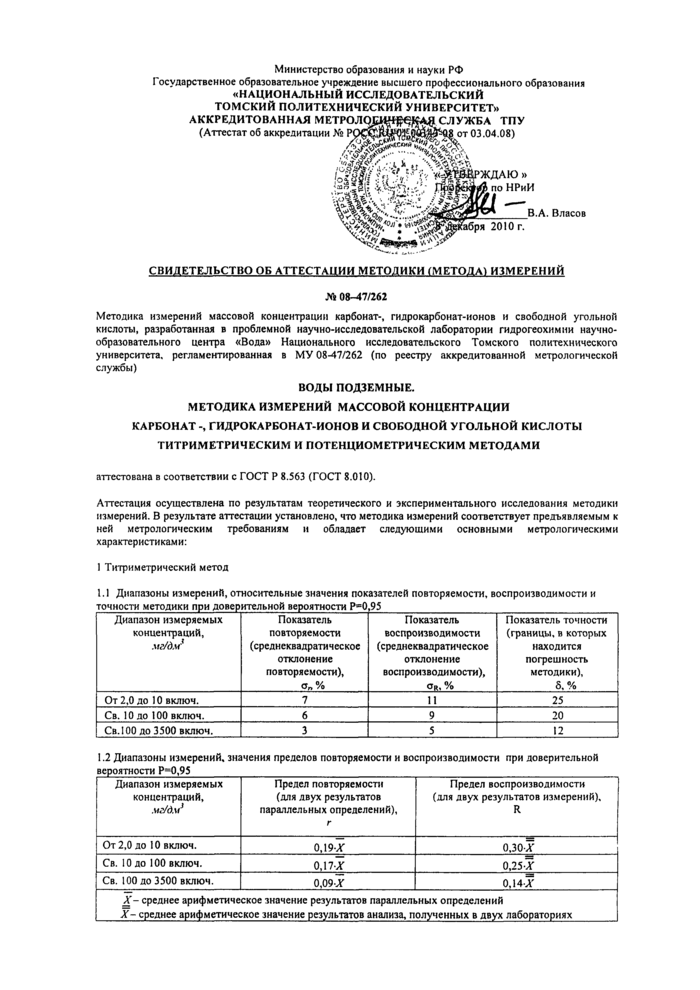
СВИДЕТЕЛЬСТВО ОБ АТТЕСТАЦИИ МЕТОДИКИ (МЕТОЛА) ИЗМЕРЕНИЙ
№ 08-47/262
Методика измерений массовой концентрации карбонат-, гидрокарбонат-ионов и свободной угольной кислоты, разработанная в проблемной научно-исследовательской лаборатории гидрогеохимии научнообразовательного центра «Вода» Национального исследовательского Томского политехнического университета, регламентированная в МУ 08-47/262 (по реестру аккредитованной метрологической
службы)
ВОДЫ ПОДЗЕМНЫЕ.
МЕТОДИКА ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ КАРБОНАТ ГИДРОКАРБОНАТ-ИОНОВ И СВОБОДНОЙ УГОЛЬНОЙ КИСЛОТЫ ТИТРИМЕТРИЧЕСКИМ И ПОТЕНЦИОМЕТРИЧЕСКИМ МЕТОДАМИ
аттестована в соответствии с ГОСТ Р 8.563 (ГОСТ 8.010).
Аттестация осуществлена по результатам теоретического и экспериментального исследования методики измерений. В результате аттестации установлено, что методика измерений соответствует предъявляемым к ней метрологическим требованиям и обладает следующими основными метрологическими характеристиками:
1 Титриметрический метод
|
1.1 Диапазоны измерений, относительные значения показателей повторяемости, воспроизводимости и |
|
Диапазон измеряемых концентраций, мг/дм3 |
Показатель
повторяемости
(среднеквадратическое
отклонение
повторяемости),
Or. % |
Показатель
воспроизводимости
(среднеквадратическое
отклонение
воспроизводимости),
Or, % |
Показатель точности (границы, в которых находится погрешность методики),
5, % |
|
От 2,0 до 10 включ. |
7 |
11 |
25 |
|
Св. 10 до 100 включ. |
6 |
9 |
20 |
|
Св.ЮО до 3500 включ. |
3 |
5 |
12 |
|
|
1.2 Диапазоны измерений, значения пределов повторяемости и воспроизводимости при доверительной вероятности Р=0,95___ |
|
Диапазон измеряемых |
Предел повторяемости |
Предел воспроизводимости |
|
концентраций. |
(для двух результатов |
(для двух результатов измерений). |
|
мг/дм3 |
параллельных определений), г |
R |
|
От 2,0 до 10 включ. |
0,19-Х |
о.золг |
|
Св. 10 до 100 включ. |
ом-х |
0,25-Х |
|
Св. 100 до 3500 включ. |
0,09-Х |
0,14-Х |
|
X- среднее арифметическое значение результатов параллельных определений |
|
X- среднее арифметическое значение результатов анализа, полученных в двух лабораториях |
|
13 ПРОВЕРКА ПРИЕМЛЕМОСТИ РЕЗУЛЬТАТОВ АНАЛИЗА, ПОЛУЧЕННЫХ В
УСЛОВИЯХ ПОВТОРЯЕМОСТИ
13.1 Рассчитывают среднее арифметическое значение двух результатов единичных анализов X, и Х2, полученных согласно разделам 10,11,12:
(1)
13.2 Вычисляют абсолютное значение предела повторяемости, используя относительные значения, приведенные в таблицах 7 и 8:
г = 0,01 • (готн, %) • ~Х. (2)
13.3 Определяют расхождение между двумя параллельными результатами анализа и сравнивают с пределом повторяемости, проверяя условие:
\Х,-Х2\йг. (3)
Если условие (3) выполняется, то оба результата считаются приемлемыми и в качестве окончательного результата принимают среднее арифметическое значение, вычисленное по формуле (1).
13.4 Если условие (3) не выполняется, получают еще один результат анализа
(Хз).
13.5 Сравнивают максимальное расхождение с критической разностью, используя относительные значения, приведённые в таблицах 7 и 8:
(Хщ.-Хш)*СЯ<”, (4)
о® =o,oi-(c«Sw %) • х.
|
Таблица 7 - Относительные значения пределов повторяемости для двух результатов единичного анализа и критической разности для трех результатов анализа при Р=0,95 Титриметрический метод |
|
Диапазон концентраций, мг/дм3 |
Предел повторяемости (относительное значение между двумя результатами анализа), готн. % |
Относительное значение критической разности для трех результатов анализа
С/^ 95 OTHi % |
|
От 10 до 100 включ. |
17 |
20 |
|
От 100 до 3500 включ. |
8 |
10 |
|
Окончание снилегсльстна №08-47/262
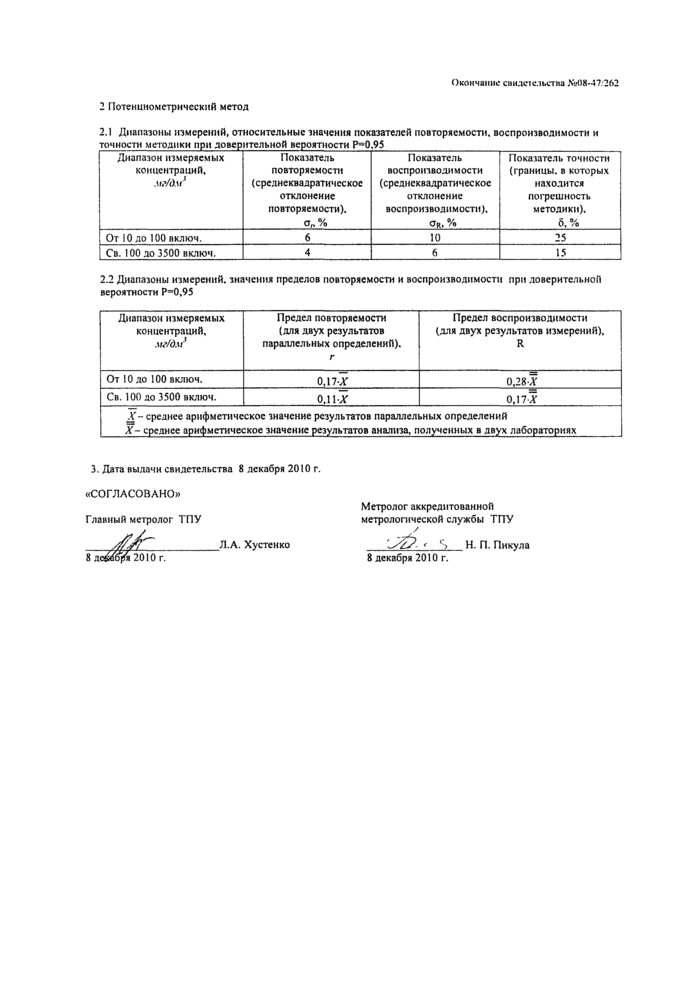
2 Потенциометрический метод
|
2.1 Диапазоны измерений, относительные значения показателей повторяемости, воспроизводимости и точности методики при доверительной вероятности Р=0,95__ |
|
Диапазон измеряемых концентраций, мг/дм* |
Показатель повторяемости (среднеквадратическое отклонение повторяемости), ап % |
Показатель воспроизводи мости (среднеквадратическое отклонение воспроизводимости),
Or, % |
Показатель точности (границы, в которых находится погрешность методики),
5, % |
|
От 10 до 100 включ. |
6 |
10 |
25 |
|
Св. 100 до 3500 включ. |
4 |
6 |
15 |
|
|
Диапазон измеряемых концентраций, мг/длг |
Предел повторяемости (для двух результатов параллельных определений). г |
Предел воспроизводимости (для двух результатов измерений), R |
|
От 10 до 100 включ. |
0,17-Х |
0.28 X |
|
Св. 100 до 3500 включ. |
0,11-Х |
0,17Х |
|
X- среднее арифметическое значение результатов параллельных определений
X- среднее арифметическое значение результатов анализа, полученных в двух лабораториях |
2.2 Диапазоны измерений, значения пределов повторяемости и воспроизводимости при доверительной вероятности Р=0,95
3. Дата выдачи свидетельства 8 декабря 2010 г. «СОГЛАСОВАНО»
|
Главный метролог ТПУ |
|
Л.А. Хустенко |
Метролог аккредитованной метрологической службы ТПУ
/
< S Н. П. Пикула 8 декабря 2010 г.
СОДЕРЖАНИЕ
1 Область применения.................................................................................1
2 Термины и определения............................................................................1
3 Приписанные характеристики погрешности метода...............................2
4 Средства измерений, вспомогательные устройства, реактивы
и материалы................................................................................................3
5 Требования безопасности и охраны окружающей среды.......................5
6 Требования к квалификации оператора..................................................5
7 Условия выполнения анализа..................................................................5
8 Отбор и хранение проб..............................................................................5
9 Подготовка к выполнению измерений......................................................5
10 Титриметрический метод с визуальным фиксированием конечной
точки титрования...........................................................................................9
10.1 Сущность метода............................................................................9
10.2 Выполнение измерений массовой концентрации карбонат-,
гидрокарбонат-ионов и свободной угольной кислоты.........................10
11 Потенциометрический метод..................................................................13
11.1 Сущность метода............................................................................13
11.2 Выполнение измерений массовой концентрации карбонат-,
гидрокарбонат-ионов..............................................................................13
12 Обработка результатов...........................................................................15
13 Проверка приемлемости результатов анализа, полученных в
условиях повторяемости..............................................................................16
14 Проверка приемлемости результатов анализа,
полученных в условиях воспроизводимости...............................................17
15 Оформление результатов измерений....................................................18
16 Контроль качества результатов анализа...............................................19
Приложение А. Нормативные ссылки.........................................................24
Приложение Б. Библиография.....................................................................26
1 ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий документ (МУ 08-47/262) распространяется на природные подземные воды: пресные, солоноватые, соленые, рассолы и устанавливает методику измерений массовой концентрации карбонат-, гидрокарбонат-ионов и свободной угольной кислоты титриметрическим методом с визуальным или потенциометрическим фиксированием конечной точки титрования.
Методика позволяет определять карбонат-, гидрокарбонат-ионы в диапазоне концентраций от 10 до 3500 мг/дм3, свободную угольную кислоту в диапазоне концентраций от 2 до 100 мг/дм3.
Определение карбонат- и гидрокарбонат-ионов проводят последовательным титрованием одной и той же пробы раствором соляной кислоты с визуальным или потенциометрическим фиксированием конечной точки титрования.
Потенциометрическое титрование рекомендуется при анализе мутных, цветных вод. Метод потенциометрического титрования является арбитражным.
Определение свободной угольной кислоты проводят титрованием пробы раствором гидроксида натрия с визуальным фиксированием конечной точки титрования.
2 ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
В настоящем документе применены термины по ГОСТ 30813, ГОСТ Р 52361, а также следующие термины:
2.1 общая минерализация: Показатель количества содержащихся в воде растворенных веществ: анионов, катионов, недиссоциированных молекул и биологически активных компонентов (исключая газы). Минерализация выражается в г/дм3.
Примечание - В зависимости от значения общей минерализации подземные воды подразделяют на пресные, солоноватые, соленые и рассолы (таблица 1).
|
Таблица 1 - Классификация подземных вод по общей минерализации* |
|
Подземные воды |
Общая минерализация, г/дм3 |
|
Пресные |
От 0,01 до 1,0 |
|
Солоноватые |
Св. 1,0 до 10,0 |
|
Соленые |
Св. 10,0 до 50,0 |
|
Рассолы |
Св. 50,0 |
|
|
*) Из книги: Короновский Н.В., Якушова А.Ф. «Основы геологии» |
2.2 карбонатная система: Содержащиеся в подземных водах (карбонатных и гидрокарбонатных по преобладающему аниону) молекулы и ионы НгСОг, С02, НСО~, СО\~, находящиеся в равновесиях:
СОг +H10++H1COi
н2со3<г>н++нсо; нсо; <-> я=+со32-
Распределение ионов карбонатной системы в зависимости от значения pH воды показано на рисунке 1.
со2 \ нсо; \ СОз2'
-i-А-
4,5 8,3 рН
Рисунок 1 - Распределение ионов карбонатной системы в зависимости от pH
3 ПРИПИСАННЫЕ ХАРАКТЕРИСТИКИ ПОГРЕШНОСТИ МЕТОДИКИ
3.1 Методика измерений массовой концентрации гидрокарбонат-, карбонат-ионов и свободной угольной кислоты в пробах подземных вод обеспечивают получение результатов с погрешностью, не превышающей значений, приведенных в
таблицах 2 и 3.
|
Таблица 2 - Относительные значения приписанных характеристик случайной (показатель воспроизводимости, показатель повторяемости) и общей (показатель точности) погрешности, Р=0,95 Титриметрический метод |
|
Диапазон измерений, мг/дм3 |
Показатели |
|
повторяемости |
воспроизводимости, |
точности |
|
Or, % |
CTR, % |
б, % |
|
От 10,0 до 100 включ. |
6 |
9 |
20 |
|
Св. 100 до 3500 включ. |
3 |
5 |
12 |
|
|
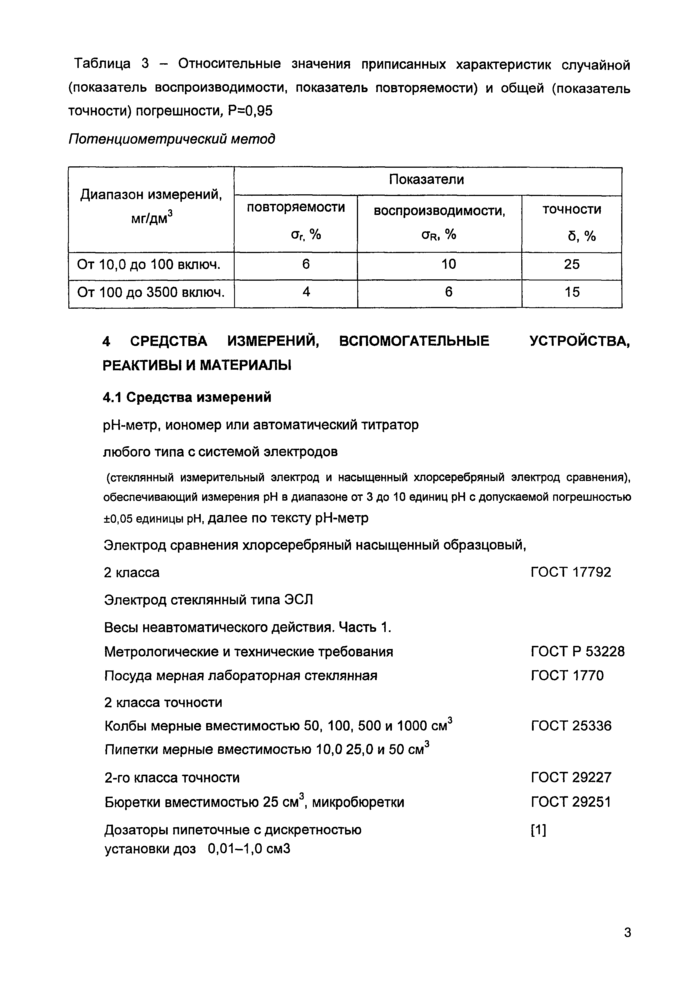
Таблица 3 - Относительные значения приписанных характеристик случайной (показатель воспроизводимости, показатель повторяемости) и общей (показатель точности) погрешности, Р=0,95 Потенциометрический метод |
|
Диапазон измерений, мг/дм3 |
Показатели |
|
повторяемости |
воспроизводимости, |
точности |
|
Or, % |
or. % |
5, % |
|
От 10,0 до 100 включ. |
6 |
10 |
25 |
|
От 100 до 3500 включ. |
4 |
6 |
15 |
|
|
4 СРЕДСТВА ИЗМЕРЕНИЙ, ВСПОМОГАТЕЛЬНЫЕ УСТРОЙСТВА, РЕАКТИВЫ И МАТЕРИАЛЫ |
4.1 Средства измерений
pH-метр, иономер или автоматический титратор любого типа с системой электродов
(стеклянный измерительный электрод и насыщенный хлорсеребряный электрод сравнения), обеспечивающий измерения pH в диапазоне от 3 до 10 единиц pH с допускаемой погрешностью ±0,05 единицы pH, далее по тексту рН-метр
Электрод сравнения хлорсеребряный насыщенный образцовый,
2 класса ГОСТ 17792
Электрод стеклянный типа ЭСЛ
Весы неавтоматического действия. Часть 1.
Метрологические и технические требования ГОСТ Р 53228
Посуда мерная лабораторная стеклянная ГОСТ 1770
2 класса точности
Колбы мерные вместимостью 50, 100, 500 и 1000 см1 ГОСТ 25336
Пипетки мерные вместимостью 10,0 25,0 и 50 см1
2-го класса точности ГОСТ 29227
Бюретки вместимостью 25 см1, микробюретки ГОСТ 29251
Дозаторы пипеточные с дискретностью [1]
установки доз 0,01-1,0 см3
Допускается использовать другое оборудование и приборы, позволяющие воспроизводить метрологические характеристики, указанные в данной методике анализа.
4.2 Стандартные образцы
При выполнении измерений используют государственные стандартные образцы состава раствора соляной кислоты (1,0 моль/дм3) со следующими метрологическими характеристиками:
• аттестованное значение
(интервал аттестованных значений), моль/дм3 0,95 -1,05
• границы значений относительной погрешности - не более 1,0% при Р=0,95
4.3 Вспомогательные устройства и материалы
Стаканы химические вместимостью 100 и 250 см3 ГОСТ 25336
Цилиндры мерные ГОСТ 1770
Фильтры обеззоленные [2]
Воронки стеклянные ГОСТ 25336
Колбы конические вместимостью 250 см3 ГОСТ 25336
Капельницы для однократной дозировки ГОСТ 2533
Холодильник стеклянный ГОСТ 25336
Магнитная мешалка любого типа
4.4 Реактивы
Кислота соляная, ос.ч ГОСТ 14261
или кислота соляная, х.ч. ГОСТ 3118
Кислота соляная, стандарт-титр [3]
Натрия гидроксид, стандарт-титр [4]
Стандарт-титры для приготовления буферных растворов - рабочих эталонов
с аттестованным значением pH 4,01; 6,86 и 9,18 ГОСТ 8.135
Метиловый оранжевый, ч.д.а ГОСТ 10816, [5]
Фенолфталеин [6]
Калий хлористый ГОСТ 4234
Вода дистиллированная ГОСТ 6709
или вода для лабораторного анализа
(далее по тексту дистиллированная вода) ГОСТ Р 52501
4
5 ТРЕБОВАНИЯ БЕЗОПАСНОСТИ И ОХРАНЫ ОКРУЖАЮЩЕЙ СРЕДЫ
5.1 При выполнении анализов необходимо соблюдать правила техники безопасности, установленные при работе с токсичными, едкими и легковоспламеняющимися веществами по ГОСТ 12.1.005.
5.2 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004.
5.3 Лаборатория должна иметь средства пожаротушения по ГОСТ 12.4.009.
5.4 При работе с электроустройствами должны соблюдаться правила электробезопасности в соответствии с ГОСТ 12.1.019.
6 ТРЕБОВАНИЯ К КВАЛИФИКАЦИИ ОПЕРАТОРА
Анализ по данной методике может проводить химик-аналитик, имеющий опыт работы в химической лаборатории и владеющий техникой титриметрического и потенциометрического анализа.
7 УСЛОВИЯ ВЫПОЛНЕНИЯ АНАЛИЗА
При приготовлении растворов и проведении измерений соблюдают следующие внешние условия: температура окружающей среды (15 - 30) °С; относительная влажность воздуха не более 80% при 25 °С; атмосферное давление (630 - 800) мм.рт.ст. или (84,0 - 106,7) кПа.
Выполнение измерений потенциометрическим методом проводят в условиях, рекомендуемых в руководстве по эксплуатации к прибору.
8 ОТБОР И ХРАНЕНИЕ ПРОБ
Метод отбора и хранения проб - по ГОСТ Р 51592 «Вода. Общие требования к отбору проб». Пробу анализируют сразу после отбора. Длительное хранение проб, соприкасающихся с воздухом, приводит к смещению равновесия в карбонатной системе. При невозможности проведения анализа сразу после отбора пробы необходимо хранить в плотно закрытых склянках не более 1 месяца. Для исследований с повышенной точностью - хранить в запаянных ампулах, откачав предварительно воздух из свободного пространства.
5
1