МР 3.3.1.0001-10
Эпидемиология и вакцинопрофилактика инфекции, вызываемой Haemophilus influenzae типа b
Купить МР 3.3.1.0001-10 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
В документе изложены современные представления об инфекции, вызываемой бактерией вида Haemophilus influenzae типа b (Hib) и также называемой Hib-инфекцией. Рассмотрены эпидемиологические особенности Hib-инфекции, представлены данные о заболеваемости Hib-инфекцией в Российской Федерации и странах мира. Особое внимание уделено проблеме вакцинопрофилактике Hib-инфекции. Дана характеристика конъюгированных Hib-вакцин, рассмотрены медицинские показания и противопоказания к их применению, возможны побочные реакции, а также порядок проведения вакцинации этими препаратами.
Оглавление
1. Область применения
2. Нормативные ссылки
3. Общие положения
3.1. Характеристика возбудителя, клинические формы и эпидемиологические особенности Hib-инфекции
3.2. Оценка заболеваемости Hib-инфекцией в разных странах мира и значимость проблемы профилактики Hib-инфекции для здравоохранения
3.3. Заболеваемость Hib-инфекцией в Российской Федерации
4. Диагностика и учет случаев Hib-инфекции
5. Мероприятия в очаге инфекции
6. Профилактика Hib-инфекции
6.1. Вакцинопрофилактика Hib-инфекции
6.2. Характеристика конъюгированных вакцин для профилактики Hib-инфекции и правила их применения
6.2.1. Моновакцины против Hib-инфекции
6.2.2. Комбинированные вакцины, содержащие Hib-компонент
6.2.3. Иммуногенность и эпидемиологическая эффективность вакцин для профилактики Hib-инфекции
6.2.4. Противопоказания к применению конъюгированных вакцин для профилактики Hib-инфекции
6.2.5. Реакции на введение конъюгированной вакцины для профилактики Hib-инфекции
6.3. Рекомендуемые схемы вакцинопрофилактики Hib-инфекции
7. Сочетание прививок против Hib-инфекции с национальным календарем профилактическтх прививок
7.1. Применение комбинированных вакцин, содержащих Hib-компонент, при иммунизации в рамках национального календаря профилактических прививок
7.2. Применение моновакцины против Hib-инфекции в сочетании с прививками национального календаря профилактических прививок
7.3. Проведение "наверстывающей" вакцинации после введения Hib-вакцины в календарь прививок
8. Иммунизация детей против Hib-инфекции в отдельных регионах Российской Федерации по эпидемиологическим показаниям
9. Селективная иммунизация против Hib-инфекции
10. Эпидемиологический надзор за Hib-инфекцией
11. Санитарно-просветительные мероприятия для усиления профилактики Hib-инфекции
Список литературы
Список сокращений
| Дата введения | 31.03.2010 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот документ находится в:
Организации:
- Федеральный закон 52-ФЗ О санитарно-эпидемиологическом благополучии населения
- СП 3.3.2.1248-03 Условия транспортирования и хранения медицинских иммунобиологических препаратов
- СП 3.1/3.2.1379-03 Общие требования по профилактике инфекционных и паразитарных болезней
- МУ 3.3.1891-04 Организация работы прививочного кабинета детской поликлиники, кабинета иммунопрофилактики и прививочных бригад
- 5487-I Основы законодательства Российской Федерации об охране здоровья граждан
- МУК 4.2.1887-04 Лабораторная диагностика менингококковой инфекции и гнойных бактериальных менингитов
- МУ 3.3.1.1095-02 Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок. Методические указания
- МУ 3.3.1.1123-02 Мониторинг поствакцинальных осложнений и их профилактика. Методические указания
- СП 3.3.2342-08 Обеспечение безопасности иммунизации
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11
стр. 12
стр. 13

стр. 14

стр. 15

стр. 16

стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
Страница 1
Государственное санитарно-зпндемнологическое нормирование _Российской Федерации_
3.3.1. ВАКЦИНОПРОФИЛАКТИКА
Эпидемиология и вакцинопрофилактика инфекции, вызываемой Haemophilus influenzae типа b
Методические рекомендации МР 3.3.1.0001—10
Издание официальное
Москва *2010
Страница 2
Федеральная служба по надзору в сфере зашиты прав потребителей и благополучия человека
3.3.1. ВАКЦИНОПРОФИЛАКТИКА
Эпидемиология и вакцинопрофилактика инфекции, вызываемой Haemophilus influenzae типа b
Методические рекомендации MP3J.1.0001—10
Страница 3
ББК51.9
Э71
Э71 Эпидемиология и вакцинопрофилактика инфекции, вызываемой Haemophilus influenzae типа b: Методические рекомендации.—М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2010.—32 с.
ISBN 978—5—7508—0888—5
1. Разработаны Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека (Е. Б. Ежлова, А. А. Мельникова); ФГУН «Центральный научно-исследовательский институт эпидемиологии» Роспотребнадзора (А. Е. Платонов, М. К. Николаев. И. С. Королева, О. В. Платонова); ФГУН ГИСК им. Л. А. Тарасевича Роспотребнадзора (Н. А. Озерецковский, М. А. Горбунов, Т. И. Немировская); ТУ Роспотребнадзора по Ярославской области (Т. А. Дружинина).
2. У тверждены и введены в действие руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г. Г. Онищенко 31.03.2010.
ЪЬК 51.9
Редакторы Н. В. Кожока, Е. В. Николаева Технический редактор Г. И. Климова
Формат 60x88/16
Подписано в печать 22 06.10 Тираж 500 экз
Печ. л. 2,0 Заказ 40
Федеральная служба по надзору в сфере защиты прав потребителей и благополучия человека 127994. Москва, Валко вс кий пер., д 18. стр. 5,7
Оригинал-макет подготовлен к печати и тиражирован отделом издательского обеспечения Федерального центра гигиены и эпидемиологии Роспотребнадзора 117105, Москва, Варшавское ш, 19а Отделение реализации, тел /факс 952-50-89
С Роспотребнадзор, 2010 С Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2010
Страница 4
MP 3.3.1.0001—10
Содержание
1. Область применения ............................................................................................4
2. Нормативные ссылки...........................................................................................5
3. Общие положения................................................................................................6
3.1. Характеристика возбудителя, клинические формы
и эпидемиологические особенности Hib-инфекции....................................6
3.2. Оценка заболеваемости Hib-инфекциеЙ в разных
странах мира и значимость проблемы профилактики Hib-инфекции для здравоохранения............................................................8
3.3. Заболеваемость Hib-инфехцией в Российской Федерации.......................10
4. Диагностика и учет случаев Hib-инфекции......................................................13
5. Мероприятия в очаге инфекции........................................................................14
6. Профилактика Hib-инфекции............................................................................16
6.1. Вакцинопрофилактика Hib-инфекции........................................................16
6.2. Характеристика конъюгированных вакцин для профилактики
Hib-инфекции и правила их применения....................................................16
6.2.1. Моновакцины против Hib-инфекции ..................................................17
6.2.2. Комбинированные вакцины, содержащие Hib-компоненг...............19
6.2.3. Иммуногенность и эпидемиологическая эффективность
вакцин для профилактики Hib-инфекции.............................................21
6.2.4. Противопоказания к применению конъюгированных
вакцин для профилактики Hib-инфекции.............................................22
6.2.5. Реакции на введение конъюгированной вакцины для
профилактики Hib-инфекции................................................................22
6.3. Рекомендуемые схемы вакцинопрофилактики Hib-инфекции.................23
7. Сочетание прививок против Hib-инфекции с национальным
календарем профилактических прививок........................................................23
7.1. Применение комбинированных вакцин, содержащих
Hib-компонент, при иммунизации в рамках национального календаря профилактических прививок.......................................................................23
7.2. Применение моновакцины против Hib-инфекции в сочетании с
прививками национального календаря профилактических прививок.....24
7.3. Проведение «наверстывающей» вакцинации после введения
Hib-вакцины в календарь прививок............................................................24
8. Иммунизация детей против Hib-инфекции в отдельных регионах
Российской Федерации по эпидемическим показаниям..................................24
9. Селективная иммунизация против Hib-инфекции...........................................25
10. Эпидемиологический надзор за Hib-инфекциеЙ..............................................27
11. Санитарно-просветительные мероприятия для усиления
профилактики Hib-инфекции.............................................................................28
Список литературы.................................................................................................30
Список сокращений................................................................................................32
3
Страница 5
УТВЕРЖДАЮ Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Главный государственный санитарный врач Российской Федерации
Г. Г. Онищенко
31 марта 2010 г.
3.3.1. ВАКЦИМОПРОФИЛАКТИКА
Эпидемиология и вакцинопрофилактика инфекции, вызываемой Haemophilus influenzae типа b
Методические рекомендации _МР 33.1.0001—10_
1. Область применения
В настоящем документе изложены современные представления об инфекции, вызываемой бактерией вида Haemophilus influenzae типа b (Hib) и также называемой Hib-инфекцией. Рассмотрены эпидемиологические особенности Hib-инфекции, представлены данные о заболеваемости Hib-инфекцией в Российской Федерации и странах мира. Особое внимание уделено проблеме вакцинопрофилактики Hib-инфекции. Дана характеристика конъюгированных Hib-вакцин, рассмотрены медицинские показания и противопоказания к их применению, возможные побочные реакции, а также порядок проведения вакцинации этими препаратами.
Реализация положений методических рекомендаций направлена на совершенствование профилактики заболеваний, вызываемых гемофиль-ной палочкой Haemophilus influenzae типа b, снижение уровня инвалидности и смертности от Hib-инфекции.
Методические рекомендации предназначены для лечебно-профилактических учреждений, независимо от их организационно-правовой формы и формы собственности, осуществляющих в установленном порядке деятельность в области иммунопрофилактики инфекционных заболеваний, а также для органов, осуществляющих государственный санитарно-эпидемиологический надзор.
Страница 6
MP 3.3.1.0001—10
2. Нормативные ссылки
1. Федеральный закон от 30 марта 1999 г. № 52-ФЗ «О санитарно-эпидемиологическом благополучии населения» (с изменениями от
30 декабря 2001 г., 10 января, 30 июня 2003 г., 22 августа 2004 г., 9 мая,
31 декабря 2005 г.).
2. Федеральный закон от 17 сентября 1998 г. № 157-ФЗ «Об иммунопрофилактике инфекционных болезней» (с изменениями от 7 августа 2000 г., 10 января 2003 г., 22 августа, 29 декабря 2004 г., 30 июня 2006 г.).
3. Федеральный закон от 22.07.1993 № 5487-1 «Основы законодательства Российской Федерации об охране здоровья граждан» (с изменениями от 24 декабря 1993 г., 2 марта 1998 г., 20 декабря 1999 г., 2 декабря 2000 г., 10 января, 27 февраля, 30 июня 2003 г., 29 июня, 22 августа, 1, 29 декабря 2004 г., 7 марта, 21, 31 декабря 2005 г., 2 февраля, 29 декабря 2006 г., 24 июля, 18 октября 2007 г.).
4. Федеральный закон от 24.07.1998 № 124-ФЗ «Об основных гарантиях прав ребенка в Российской Федерации» (с изменениями от 20 июля 2000 г., 22 августа, 21 декабря 2004 г.).
5. Приказ Министерства здравоохранения Российской Федерации от 27.06.2001 № 229 «О национальном календаре профилактических прививок и календаре профилактических прививок по эпидемическим показаниям» (в ред. от 17.01.2006 № 27, от 11.01.2007 № 14, от 30.10.07 № 673).
6. Санитарно-эпидемиологические правила СП 3.1/3.2.1379—03 «Общие требования по профилактике инфекционных и паразитарных болезней».
7. Санитарно-эпидемиологические правила СП 3.3.2342—08 «Обеспечение безопасности иммунизации».
8. Санитарно-эпидемиологические правила СП 3.3.2.1248—03 «Условия транспортирования и хранения медицинских иммунобиологических препаратов».
9. Методические указания МУ 3.3.1891—04 «Организация работы прививочного кабинета детской поликлиники, кабинета иммунопрофилактики и прививочных бригад».
10. Методические указания МУ 4.2.1887—04 «Лабораторная диагностика менингококковой инфекции и гнойных бактериальных менингитов».
И. Методические указания МУ 3.3.1.1123—02 «Мониторинг поствакцинальных осложнений и их профилактика».
5
Страница 7
MP 3.3.1.0001—10
12. Методические указания МУ 3.3.1.1095—02 «Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок».
3. Общие положевия
3,1. Характеристика возбудителя, клинические формы и эпидемиологические особенности И lb-инфекции
Возбудителем гемофильной инфекции является бактерия Haemophilus influenzae - мелкая коккобактерия из семейства Pasteurellaceae. Исходя из химического строения и антигенных свойств полисахаридной капсулы бактерии, выделяют 6 серотипов Н. influenzae: a, b, с, d, е, f; известны также и бескапсульные штаммы. Генетически серотипы существенно различаются и представляют собой изолированные субпопуляции Н. influenzae. Бактерия является обычным представителем микрофлоры слизистой оболочки верхних дыхательных путей человека и передается, как правило, воздушно-капельным путем. Уровень носитель-ства Н. influenzae варьирует в зависимости от эпидемических условий от 5 до 80 %. Сравнительно редко инфицирование Н. influenzae приводит к развитию клинических форм заболевания, спектр которых очень широк и зависит от серотипа возбудителя, но среди них преобладают заболевания верхних и нижних дыхательных путей.
Наиболее часто тяжелые формы заболевания вызываются Н. influenzae серотипа b или сокращенно Hib. Инфекция, вызываемая этим возбудителем, называется Hib-инфекцией.
Фактором патогенности бактерии Hib является капсульный полисахарид - полирибозил-рибитол-фосфат (PRP), который обеспечивает подавление комплемент-зависимой бактериолитической активности крови и фагоцитарной активности лейкоцитов. Капсульный полисахарид является основным антигеном, к которому вырабатываются антитела при заболевании Hib-инфекцией или здоровом носительстве Hib-бактерий [16].
Уровень носительства бактерий Н. influenzae типа b у детей варьирует обычно от 1 до 10%, но в условиях скученности и формирования новых детских коллективов может достигать 40 %.
Спектр антибиотикорезистентности Hib-бактерий зависит как от географического места изоляции, так и от вида материала, из которого изолирован штамм (мазок из носоглотки, спинномозговая жидкость и др.). Показано, что резистентность к пенициллину может достигать 25 % у штаммов, изолированных из спинномозговой жидкости и/или крови де-
6
Страница 8
MP 3.3.1.0001—10
тей в г. Москве. Имеются данные о том, что подобная картина типична и для других регионов Российской Федерации [1, 5,7,9,16,22].
Различают «инвазивные» формы Hib-инфекции, при которых возбудитель обнаруживается в жидкостях и тканях организма, стерильных в нормальных условиях (кровь, спинномозговая жидкость, перитонеальная и плевральная жидкости и т. п.), и «неинвазивные» формы, к которым относится «небактериемическая» пневмония (при отсутствии возбудителя в крови), ОРЗ (ринофарингит), конъюнктивит и т. п. К «инвазивным» формам Hib-инфекции относятся пневмония, септицемия, эпи-глоттит, септический артрит, остеомиелит, перикардит, эндокардит, целлюлит [16]. Наиболее тяжелой и наиболее исследованной формой Hib-инфекции является гнойный бактериальный менингит (ГБМ) [1,3, 5, 10, 11, 24]. Выявление и диагностика иных форм Hib-инфекции крайне затруднены.
Резервуаром и источником возбудителя Hib-инфекции является инфицированный человек (больные .любой клинической формой и в первую очередь здоровые носители). Путь передачи - воздушнокапельный. Распространение заболевания носит убиквитарный характер. Среди инвазивных форм Hib-инфекции около 50 % случаев составляет Hib-менингит. Предполагают, что заболеваемость неинвазивными формами Hib-инфекции как минимум в 5—10 раз выше, чем заболеваемость Hib-менингитом [7, 16, 22].
Наиболее часто, в 90—95 % случаев, Hib-менингитом заболевают дети в возрасте от 1 месяца до 5 лет. У детей более раннего возраста и старше 5 лет Hib-менингиты практически не встречаются. Это обусловлено тем, что у детей первых месяцев жизни присутствуют материнские антитела против Hib, а у детей старше 5 лет успевает развиться приобретенный иммунитет [1,9, 10, 11,16].
В развивающихся странах жаркого климата до 60—80 % заболевших Hib-менингитом составляют дети моложе 1 года; в развитых странах умеренного климата пик заболеваемости приходится обычно на возраст от 1 до 2 лет, менее 40 % заболевших составляют дети до года [ 15]. Имеются указания на то, что заболеваемость Hib-эпиглоттитом смещена в сторону более старших возрастных групп (дети от 3 до 9 лет), а заболеваемость Hib-пневмонией - в сторону младшей возрастной группы (дети до года).
У заболевших Hib-менингитом в возрасте старше 10 лет чаще всего выявляются тяжелые индивидуальные отягощающие факторы: анатомические (травмы черепа, назальная ликворея, spina bifida и др.) или им-
7
Страница 9
MP 3.3.1.0001—10
мунологические (дефициты компонентов системы комплемента и другие иммунодефициты).
Заболевания Hib-менингитом носят спорадический характер: не описано существенных циклических подъемов или спадов заболеваемости на определенной территории; возникновение очагов (два и более заболевших) в детских учреждениях и семьях наблюдается крайне редко. Сезонные колебания заболеваемости, если и существуют в некоторых экологических условиях, невелики и не имеют принципиального значения.
3.2. Оценка заболеваемости Hib-инфекциеи в разных странах мира и значимость проблемы профилактики Hib-инфекции для здравоохранения
Приведенные в этом разделе данные о заболеваемости Hib-менин-гитом основаны на результатах 229 исследований, проведенных в 1950—2000 гг. во всех частях света, и описывают ситуацию до введения Hib-вакцины в календарь прививок [15].
Средняя заболеваемость Hib-менингитом до начала вакцинации составила 18 случаев на 100 тыс. детей в возрасте до 5 лет в год, минимальная - 2 на 100 тыс. детей, максимальная - 60 случаев на 100 тыс. детей. Летальность при Hib-менингите равнялась в среднем 10%, варьируя от 1 до 40 %. Из всех случаев ГБМ среди детей до 5 лет на Hib-менингит приходилось в среднем 40 % (от 12 до 73 %).
Региональные различия заболеваемости Hib-менингитом существенны. До введения вакцинопрофилактики против Hib-инфекции наибольшая заболеваемость регистрировалась в Африке (в среднем 58 случаев на 100 тыс. детей в возрасте до 5 лет в год) и на американском континенте (в среднем 30 случаев на 100 тыс. детей в возрасте до 5 лет в год). Заболеваемость в странах тихоокеанского бассейна была существенно ниже: средняя - 16 случаев на 100 тыс. детей в возрасте до 5 лет в год. Летальность при Hib-менингите составляла в Африке 17—38 %, на американском континенте - 4—15 %, в странах тихоокеанского бассейна 2—17 % [15].
В Северной Америке и Австралии были выявлены этнико-куль-турные группы с особо высокой заболеваемостью Hib-менингитом, от 150 до 500 случаев на 100 тыс. детей в возрасте до 5 лет в год: индейцы апачи и навахо, эскимосы Аляски, австралийские аборигены [16].
В европейских странах заболеваемость Hib-менингитом была относительно низка: средняя - 16 случаев на 100 тыс. детей в возрасте до 5 лет
Страница 10
MP 3.3.1.0001—10
в год. Летальность составляла 3 %. Из всех случаев ГБМ среди детей до 5 лет на Hib-менингит приходилось в среднем 39%. Доля детей моложе 1 года среди всех заболевших Hib-менингитом составляла в среднем 41 %. Региональные различия существуют и в группе европейских стран: заболеваемость Hib-менингитом была в целом выше на западе и севере Европы, чем на юге и востоке [15].
Таким образом, приведенные оценки с учетом региональных особенностей эпидемиологии Hib-менингита и численности детского населения в различных странах позволяют предположить, что в мире ежегодно имеют место не менее 250 тыс. случаев Hib-менингита, обусловливающих около 40 тыс. смертей [15]. Доля тяжелых инвалидизирую-щих последствий Hib-менингита, в первую очередь глухоты разной степени выраженности, составляет даже при условиях адекватного лечения 15—20% [16].
По оценкам ВОЗ, показатель заболеваемости другими инвазивными формами Hib-инфекции, помимо Hib-пневмонии и менингита, составлял в Европе до введения вакцинопрофилактики от 3 до 10 случаев на 100 тыс. детей до 5 лет в год (около 40 % от показателя заболеваемости Hib-менингитом) при летальности порядка 0,5 %, а заболеваемость Hib-пневмонией в Европе до введения вакцинопрофилактики составляла порядка 150—300 случаев на 100 тыс. детей до 5 лет в год, т. е. в 10—20 раз больше, чем заболеваемость Hib-менингитом [7, 16,21]. Летальность при Hib-пневмонии у детей в развитых странах составляла предположительно около 0,5 %.
С учетом широкой распространенности Hib-пневмонии ВОЗ предполагает «по меньшей мере 3 млн случаев серьезного заболевания, вызванного Hib, ежегодно и около 380 тыс. смертей от Hib-инфекции» [16, 22]. Поэтому борьба с Hib-инфекцией, в первую очередь с помощью средств специфической профилактики - вакцинопрофилактики, входит в число приоритетных задач ВОЗ, и конъюгированная Hib-вакцина рекомендована для введения в календарь прививок всех стран [22, 25]. К настоящему моменту 119 стран мира пошли по этому пути, в т. ч. 38 из 52 европейских стран - членов ВОЗ [18]. В результате было достигнуто 90—99 % снижение заболеваемости инвазивными формами Hib-инфекции в этих странах [18, 20]. В частности, в группе 17 европейских стран, для которых существуют надежные данные эпидемиологического надзора за Hib-менингитом, средний показатель заболеваемости снизился с 15 случаев на 100 тыс. детей моложе 5 лет в год в период до введения Hib-вакцинации до 0,3 случаев на 100 тыс. детей моложе 5 лет в год
9
Страница 11
MP 3.3.1.0001—10
в 1999—2006 гг. на фоне массовой иммунизации детей Hib-вакциноЙ, начиная с возраста 2—3 месяца. Благодаря проводимой иммунизации в Исландии, Словакии, Финляндии, Норвегии и Франции заболеваемость Hib-менингитом снизилась на 99 %; в Ирландии, Чехии, Польше, Италии и Великобритании - на 90—95 % [15, 17]. Объективными препятствиями к внедрению Hib-вакцины являются недостаточная изученность бремени этого заболевания и экономические затруднения [19, 22]. Большинство исследований (74 из 83, или 89 %), проведенных в странах, которые впоследствии ввели Hib-вакцинацию, указывали на заболеваемость Hib-менингитом выше 10 случаев на 100 тыс. детей моложе 5 лет в год. Напротив, в 55 % (11 из 20) исследований, проведенных в странах, которыми не принято решение о массовой Hib-вакцинации, была выявлена заболеваемость Hib-менингитом ниже 10 случаев на 100 тыс. детей моложе 5 лет [20].
3.3. Заболеваемость Hib-инфекцией в Российской Федерации
В связи с низким уровнем диагностики и регистрации гемофильной инфекции в Российской Федерации данные ее статистического учета не отражают истинного уровня заболеваемости.
Максимально полно и точно была оценена заболеваемость ГБМ, в т. ч. Hib-менингитом, у детей до 5-летнего возраста в ходе специально проведенных исследований с помощью современных методов диагностики и системы активного эпидемиологического надзора в ряде субъектов Российской Федерации - в г.г. Москве (2000—2001 гг.), Мурманске, Туле, Нижнем Новгороде, Новосибирске (2004—2005 гг.), а также в г.г. Иркутске, Улан-Удэ, Якутске и Владивостоке (2007—2008 гг.) [9, 11].
В г. Москве за 2 года в 8 профильных стационарах было выявлено 209 случаев ГБМ, что соответствовало заболеваемости 30,4 на 100 тыс. детей от 1 месяца до 5 лет в год. 87 % случаев было лабораторно расшифровано: 22% от числа расшифрованных случаев составил Hib-менингит. На менингококковый менингит пришлось 65 % случаев ГБМ в этой возрастной группе, а на пневмококковый - 7 %. Выявленная заболеваемость Hib-менингитом равнялась 5,7 случая на 100 тыс. детей до 5 лет в год; её скорректированная методом Hib-RAT оценка [23], учитывающая, что среди 13 % ^диагностированных случаев ГБМ также могли встречаться Hib-менингиты, составила 6,5 случая на 100 тыс. детей до 5 лет в год. Многолетний средний показатель летальности при Hib-менингите в г. Москве составлял около 6 % [3, 5,9].
Страница 12
MP 3.3.1.0001—10
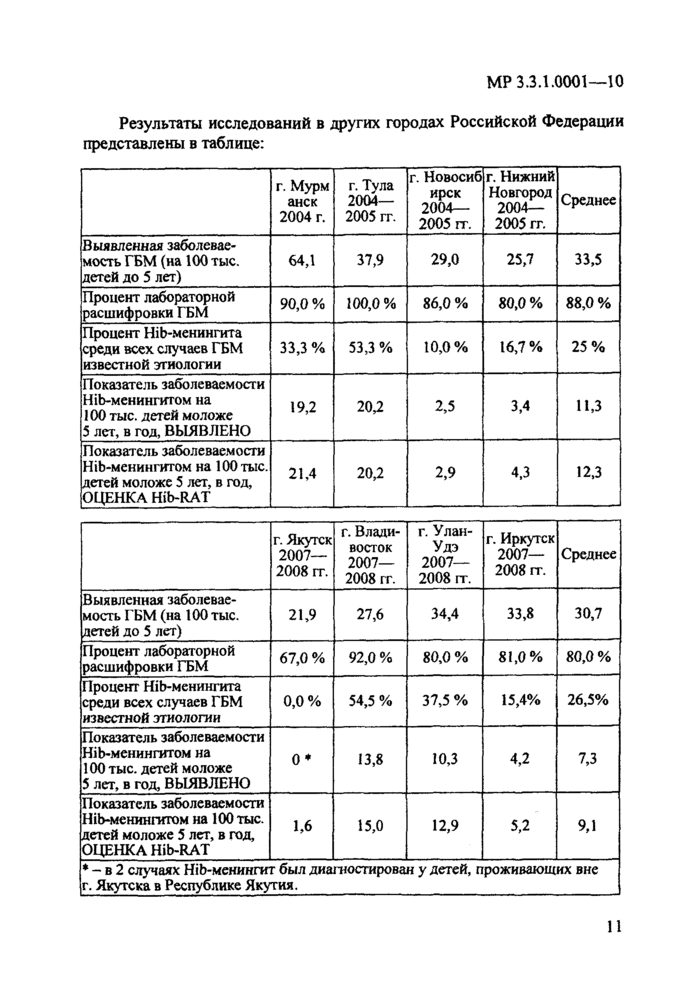
Результаты исследований в других городах Российской Федерации представлены в таблице:
г. Мурм анск 2004 г.
г. Тула 2004— 2005 гг.
г. Новосиб ирск 2004— 2005 гг.
г. Нижний Новгород 2004— 2005 гг.
Среднее
Выявленная заболеваемость ГБМ (на 100 тыс. детей до 5 лет)
64,1
37,9
29,0
25,7
33,5
Процент лабораторной расшифровки ГБМ
90,0%
100,0%
86,0 %
80,0%
88,0 %
Процент Hib-менингита среди всех случаев ГБМ известной этиологии
33,3 %
53,3 %
10,0%
16,7 %
25%
Показатель заболеваемости Hib-менингитом на 100 тыс. детей моложе 5 лет, в год, ВЫЯВЛЕНО
19,2
20,2
2,5
3,4
11,3
Показатель заболеваемости Hib-менингитом на 100 тыс. детей моложе 5 лет, в год, ОЦЕНКА Hib-RAT
21,4
20,2
2,9
4.3
12.3
г. Якутск 2007— 2008 гг.
г. Владивосток 2007— 2008 гг.
г. Улан-Удэ 2007— 2008 гг.
г. Иркутск 2007— 2008 гг.
Среднее
Выявленная заболеваемость ГБМ (на 100 тыс. детей до 5 лет)
21,9
27,6
34,4
33,8
30,7
Процент лабораторной расшифровки ГБМ
67,0 %
92,0 %
80,0 %
81,0%
80,0 %
Процент Hib-менингита среди всех случаев ГБМ известной этиологии
0,0%
54,5 %
37,5 %
15,4%
26,5%
Показатель заболеваемости Hib-менингитом на 100 тыс. детей моложе 5 лет, в год, ВЫЯВЛЕНО
0*
13,8
10,3
4,2
7,3
Показатель заболеваемости Hib-менингитом на 100 тыс. детей моложе 5 лет, в год, ОЦЕНКА Hib-RAT
1,6
15,0
12,9
5,2
9,1
• - в 2 случаях Hib-мснингит был диш пости рован у детей, проживающих вне г. Якутска в Республике Якутия.
11
Страница 13
MP 3.3.1.0001—10
Таким образом, несмотря на выраженные региональные различия, при условии адекватной лабораторной диагностики Hib-менингит в Российской Федерации выявляется повсеместно. В ряде регионов заболеваемость превышает 15 случаев на 100 тыс. детей до 5 лет в год [11].
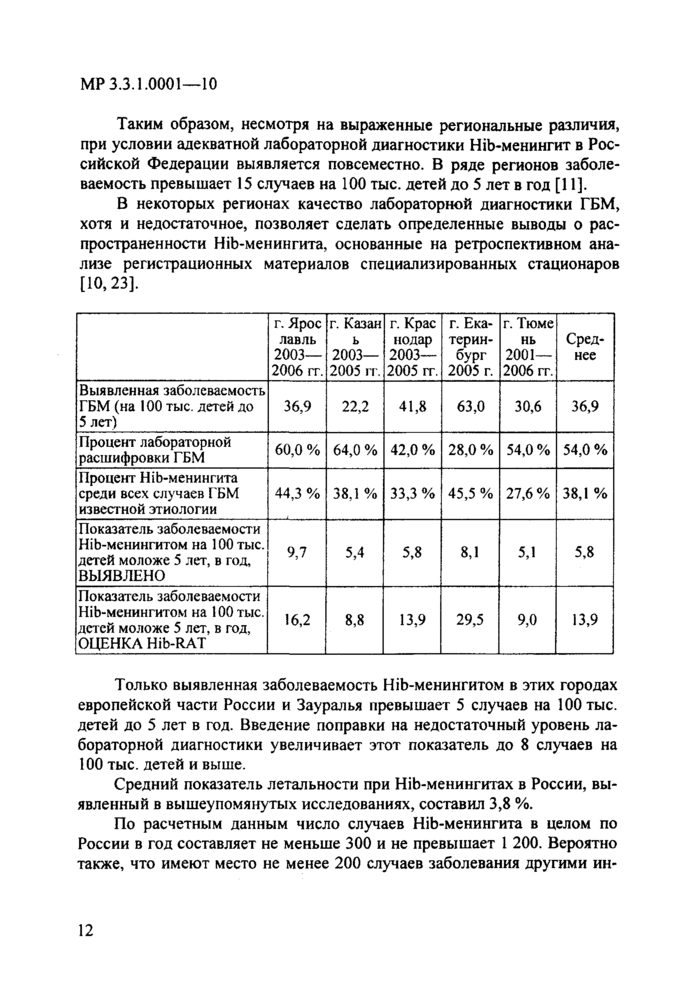
В некоторых регионах качество лабораторной диагностики ГБМ, хотя и недостаточное, позволяет сделать определенные выводы о распространенности Hib-менингита, основанные на ретроспективном анализе регистрационных материалов специализированных стационаров [10,23].
г. Ярое лавль 2003— 2006 гг.
г. Казан ь
2003— 2005 гг.
г. Крас нолар 2003— 2005 гг.
г. Екатеринбург 2005 г.
г. Тюме нь 2001— 2006 гг.
Сред
нее
Выявленная заболеваемость ГБМ (на 100 тыс. детей до 5 лет)
36,9
22,2
41,8
63,0
30,6
36,9
Процент лабораторной расшифровки ГБМ
60,0 %
64,0 %
42,0 %
28,0 %
54,0%
54,0 %
Процент Hib-менингита среди всех случаев ГБМ известной этиологии
44,3 %
38,1%
33,3 %
45,5 %
27,6%
38,1 %
Показатель заболеваемости Hib-мснингитом на 100 тыс. детей моложе 5 лет, в год, ВЫЯВЛЕНО
9,7
5,4
5,8
8,1
5,1
5,8
Показатель заболеваемости Hib-менингитом на 100 тыс. детей моложе 5 лет, в год, ОЦЕНКА Hib-RAT
16,2
8,8
13,9
29,5
9,0
13,9
Только выявленная заболеваемость Hib-менингитом в этих городах европейской части России и Зауралья превышает 5 случаев на 100 тыс. детей до 5 лет в год. Введение поправки на недостаточный уровень лабораторной диагностики увеличивает этот показатель до 8 случаев на 100 тыс. детей и выше.
Средний показатель летальности при Hib-менингитах в России, выявленный в вышеупомянутых исследованиях, составил 3,8 %.
По расчетным данным число случаев Hib-менингита в целом по России в год составляет не меньше 300 и не превышает 1 200. Вероятно также, что имеют место не менее 200 случаев заболевания другими ин-
12
Страница 14
MP 3.3.1.0001—10
вазивными формами Hib-инфекции (не менингитом и не пневмонией, т. е. эпиглоттитом, сепсисом и т. п.).
По расчетам заболеваемость Hib-пневмонией в Российской Федерации составляет не менее 150 на 100 тыс. детей моложе 5 лет в год или около 10 тыс. случаев в целом.
При летальности Hib-менингита в 5 % и Hib-пневмонии в 0,5 % такая заболеваемость должна приводить не менее чем к 80 летальным исходам от Hib-инфекции в год. Таким образом, в современных российских условиях Hib-инфекция занимает одно из первых мест среди причин смерти детей (до 17 лет) от инфекционных заболеваний, уступая только туберкулезу, ВИЧ-инфекции, менингококковой инфекции, острым кишечным инфекциям и вирусным гепатитам [7].
4. Диагностика и учет случаев Hib-инфекции
Регистрация и учет случаев Hib-менингита и гемофильной инфекции в целом производится в соответствии со схемой оповещения, предусмотренной в лечебно-профилактических учреждениях и учреждениях Роспотребнадзора.
Основанием для постановки диагноза Hib-менингита являются только результаты комплексного бактериологического исследования образцов спинномозговой жидкости (СМЖ) и крови больного, включающего [3,9,24]:
• посев образцов на адекватные среды, обеспечивающие рост Hib-бактерий;
• некультуральные методы, направленные на выявление полисахаридного антигена Hib-бактерий (с помощью реакции латекс-агглютинации) или ДНК Hib-бактерий (с помощью специфической полимеразной цепной реакции (ПЦР) в образцах СМЖ.
Посев образцов, идентификация выросших бактерий и учет результатов производится в соответствии с требованиями методических указаний МУ 4.2.1887—04 «Лабораторная диагностика менингококковой инфекции и гнойных бактериальных менингитов». Все диагностические лаборатории, производящие посев образцов СМЖ, взятых у детей с подозрением на менингит, должны быть обеспечены «шоколадным» агаром, приготовленным на бараньей крови и обогащенным X и V факторами роста.
Поскольку классические бактериологические методы (посев образцов) даже в условиях идеального применения способны обеспечить этиологическую расшифровку не более 40—50 % случаев ГБМ, необхо-
13
Страница 15
MP 3.3.1.0001—10
димо их дополнение некультуральными методами, с помощью которых можно обеспечить расшифровку до 60—80% ГБМ (при применении реакции латекс-агглютинации) и до 80—90% ГБМ (при применении ПЦР) [9, 11]. При постановке реакций латекс-агглютинации и ПЦР используются тест-системы, зарегистрированные в Российской Федерации, в соответствии с утвержденными инструкциями.
Диагноз Hib-менингита считается установленным, если у больного с клиническими проявлениями нейроинфекции:
1) из образца СМЖ выделена бактерия Я influenzae типа b (в случае если бактерия Я. influenzae типа b выделена из крови при отрицательном результате посева СМЖ, диагноз Hib-менингита может быть поставлен ребенку с клиническими и ликворологическими проявлениями ГБМ);
2) или в образце СМЖ выявлен полисахаридный антиген Hib - с помощью реакции латекс-агглютинации;
3) или в образце СМЖ выявлена ДНК Hib - с помощью ПЦР.
По результатам комплексного исследования бактериологическими и некультуральными методами для постановки диагноза Hib-менингита достаточно выполнения одного из вышеперечисленных условий [3,9,24].
В случае если серотип выделенной бактерии Я. influenzae не удается определить, ставится диагноз «гемофильный менингит».
При этом культуральные и некультуральные методы должны обеспечивать возможность выявления и других основных возбудителей ГБМ: бактерий N. meningitidis и 5. pneumoniae. Не согласующиеся результаты (высев из образца СМЖ двух и более видов бактерий, положительная реакция латекс-агглютинации или ПЦР по отношению к антиге-ну/ДНК нескольких возбудителей, несогласующиеся данные, полученные разными диагностическими методами) не дают основания для установления этиологии ГБМ. В этом случае исследование должно быть повторено и приняты меры по проверке условий забора и доставки материала, качества тест-систем и по повышению качества диагностической работы в целом.
Целевой показатель: выявление и учет не менее 95 % случаев ГБМ у детей до 5 лет на территории при этиологической расшифровке не менее 60 % случаев ГБМ [24].
5. Мероприятия в очаге инфекции
Госпитализация больного Hib-инфекцией осуществляется по клиническим показаниям. Больные с менингитом или подозрением на ме-
Страница 16
MP 3.3.1.0001—10
нингит немедленно должны быть госпитализированы в инфекционный стационар или специализированные отделения и боксы. Больные с пневмонией и другими клиническими формами заболевания возможной Hib-этиологии госпитализируются в зависимости от тяжести заболевания. Они могут лечиться на дому, если в семье или квартире отсутствуют другие дети младше 5 лет, при условии регулярного медицинского наблюдения. Эпидемиологическое обследование в очаге инфекции направлено на выявление источников возбудителя инфекции и определение круга лиц, подвергшихся риску заражения. Все лица, общавшиеся с больным в детском коллективе или семье, подвергаются медицинскому осмотру. Особое внимание следует обратить на детей и взрослых с острыми респираторными заболеваниями, отитами, назофарингитами, гайморитами. При выявлении таких детей в коллективе рекомендуется их изолировать на дому, а при выявлении в семьях - не допускать в детские коллективы до полного выздоровления. Взрослых больных указанными заболеваниями рекомендуется отстранить от работы в детских коллективах до излечения. Здоровые дети и взрослые могут быть допущены в организованные коллективы без ограничений. Бактериологическое обследование лиц, контактных с больным любой формой Hib-инфекции, проводить не рекомендуется.
В детских дошкольных учреждениях и домах ребенка в группах, включающих детей моложе 5 лет, в течение десяти дней с момента изоляции больного Hib-инфекцией не рекомендуется приём новых или временно отсутствовавших детей, а также перевод детей и персонала в другие группы.
В очаге организуются дезинфекционные мероприятия, как и при других острых бактериальных респираторных заболеваниях.
Зарубежные источники допускают в качестве меры экстренной профилактики применение рифампицина (20 мг/кг/сутки в 1—2 приема per os в течение 4 дней) всем членам семей, где есть не вакцинированные против Hib-инфекции дети в возрасте до 5 лет [16]. Однако в связи с почти полным отсутствием очаговости Hib-инфекции в Российской Федерации и возможными отрицательными последствиями химиопрофилактики (побочные реакции, дисбактериоз, селекция устойчивых штаммов), антибиотикотерапия здоровых контактных лиц не рекомендуется. Исключением могут являться семьи и коллективы, где есть дети из «групп риска» (см. далее), и очаги, в которых в течение двух месяцев выявляется два и более случаев инвазивной Hib-инфекции: в этом слу-
Страница 17
MP 3.3.1.0001—10
чае показано проведение вышеуказанного курса антибиотикопрофилак-тики у детей и взрослых и вакцинация детей до 5 лет в очаге [16].
6. Профилактика Hib-инфекции
Профилактика направлена на снижение заболеваемости Hib-инфекцией, ликвидацию генерализованных форм этой инфекции, снижение показателей инвалидности и смертности среди детей раннего возраста.
Неспецифическая профилактика сводится к соблюдению правил личной гигиены и здорового образа жизни.
Более 90 % заболеваний Hib-инфекцией и смертей от Hib-инфекции можно предотвратить с помощью надлежащим образом организованной вакцинопрофилактики [25].
6. /. Вакцинопрофилактики Hib-инфекции
Основной мерой профилактики Hib-инфекции является вакцинация детей первого года жизни конъюгированной Hib-вакциной. Сравнение частоты заболевания Hib-инфекцией, включая Hib-менингит, у вакцинированных и не вакцинированных детей показало в большинстве проведенных за рубежом испытаний 90—95 % эффективность вакцинации. Массовое использование Hib-вакцины, в частности введение Hib-вакцины в календарь профилактических прививок, приводит также к существенному снижению носительства Hib-бактерий, отчасти, вероятно, в силу снижения заболеваемости Hib-инфекцией. В свою очередь, уменьшение носительства Hib-бактерий способствует снижению заболеваемости Hib-инфекцией у не привитых детей и взрослых. В результате после введения Hib-вакцины в календарь профилактических прививок в большинстве развитых стран достигнуто 90—99 % снижение заболеваемости генерализованными (инвазивными) формами Hib-инфекции [1,18, 20,22,25].
При организации иммунопрофилактики Hib-инфекции необходимо руководствоваться действующими нормативными и методическими документами по организации и проведению вакцинопрофилактики инфекционных заболеваний, а также инструкциями по применению иммунобиологических препаратов.
6.2. Характеристика конъюгированных вакцин для профилактики Hib-инфекции и правила их применения
В Российской Федерации зарегистрированы конъюгированные Hib-вакцины двух зарубежных производителей, хотя число вакцин, разре-
Страница 18
MP 3.3.1.0001—10
шенных к применению в разных странах мира, выше. Все вакцины имеют одинаковое строение и состоят из PRP-полисахарида, связанного с белком-носителем. Опыт их использования не выявил существенных различий в реактогенности, иммуногенности и эффективности, поэтому они в равной мере могут быть использованы для вакцинопрофилактики. В случае если курс предусматривает 3—4 введения конъюгированной Hib-вакцины ребенку, допустимо применение вакцин различных производителей в ходе курса иммунизации [16,22,25].
В настоящее время разработана и успешно прошла клинические испытания отечественная конъюгированная Hib-вакцина, находящаяся в процессе регистрации. Состав препарата не отличается от состава зарубежных аналогов и его иммунологическая активность соответствует активности зарубежных вакцин против гемофилыюй инфекции.
6.2.1. Моновакцины против Hib-инфекции
Низкая иммуногенность полисахаридных вакцин у детей первых лет жизни послужила причиной конструирования вакцинных препаратов на основе конъюгатов. Конъюгат представляет собой ковалентное химическое соединение полисахаридного антигена PRP, который выступает в роли гаптена, и белка-носителя. Белково-полисахаридный комплекс распознается макрофагами и Т-лимфоцитами, индуцируя Т-зависимый (тимус-зависимый) иммунный ответ. Т-зависимыЙ иммунный ответ на конъюгат качественно и количественно отличается от иммунного ответа, индуцируемого введением одного полисахарида:
• это более сильный ответ, особенно у детей первых лет жизни;
• повторные применения вакцины, сконструированной на основе конъюгированного антигена, индуцируют ответ вторичного типа или бустер-ответ;
• доминируют высокоавидные антитела - IgG;
• формируется иммунологическая память.
При конструировании вакцины для профилактики Hib-инфекции в качестве белка-носителя используют: дифтерийный анатоксин, мутантный нетоксичный вариант дифтерийного токсина CRM197, белок наружной мембраны N. meningitidis серогруппы В, столбнячный анатоксин. Зарегистрированные в Российской Федерации вакцины содержат в качестве белка-носителя столбнячный анатоксин.
Данные вакцины содержат большие полисахаридные полимеры PRP, которые ковалентно связаны со столбнячным анатоксином посред-
17
Страница 19
MP 3.3.1.0001—10
ством 6-углеродного спейсера. В результате конъюгации формируется сложная трёхмерная пространственная структура антигена. В целях длительного сохранения стабильности вакцина выпускается в лиофилизи-рованном виде. Перед применением лиофилизат растворяют водой для инъекций или буферным раствором, не содержащим адъювантов или антибиотиков.
В каждой дозе вакцины содержатся: лиофилизат - полисахарид Haemophilus influenzae тип b 10 мкг, конъюгированный с 30 мкг столб* нячного анатоксина (оба типа зарегистрированных вакцин); трометамол - 0,6 мг (первый вариант вакцины); стабилизатор - сахароза, 42,5 мг (первый вариант вакцины) или лактоза, 10 мг (второй вариант вакцины); растворитель - 0,4 %-й раствор натрия хлорида (первый вариант вакцины) или 0,9 %-й раствор натрия хлорида для инъекций (второй вариант вакцины).
Вакцины выпускаются во флаконе, содержащем одну дозу вакцины в лиофилизированном виде. К флакону прилагается шприц, флакон или ампула, содержащие 0,5 мл растворителя.
Вакцина представляет собой порошок или плотную массу белого или серовато-белого цвета. Растворитель - прозрачная бесцветная жидкость, без запаха, свободная от видимых механических включений.
В соответствии с инструкцией по применению вакцину вводят внутримышечно или подкожно. Пациентам с тромбоцитопенией и другими нарушениями свертывающей системы крови вакцину вводят подкожно.
Вакцина для профилактики Hib-инфекции может быть введена одновременно (в один день) с другими вакцинами Национального календаря профилактических прививок (кроме БЦЖ, БЦЖ-М), а также инактивированными вакцинами календаря прививок по эпидемическим показаниям (кроме антирабической вакцины). При этом препараты должны быть введены разными шприцами в разные участки тела.
Срок годности препарата составляет 3 года. Транспортирование и хранение конъюгированной вакцины для профилактики Hib-инфекции осуществляется в соответствии с требованиями СП 3.3.2.1248—03 при температуре от 2 до 8 °С, вакцина замораживанию не подлежит.
АКДС вакцина + Hib-вакцина
Лиофилизированная вакцина для профилактики Hib-инфекции может быть смешана в одном шприце с комбинированной АКДС-вакциной, если это разрешено инструкциями по их применению.
Страница 20
MP 3.3.1.0001—10
В настоящее время для смешивания разрешена одна такая вакцина -адсорбированная бесклеточная АКДС-вакцина для профилактики дифтерии, столбняка, коклюша.
Бесклеточная АКДС-вакцина содержит дифтерийный анатоксин, столбнячный анатоксин и три очищенных коклюшных антигена (коклюшный анатоксин, филаментозный гемагглютинин и белок наружной мембраны пертактин с молекулярной массой 69 кДа, адсорбированные на гидроксиде алюминия). В одной дозе вакцины (0,5 мл) содержатся активные ингредиенты - не менее 30 международных единиц (ME) дифтерийного анатоксина, не менее 40 ME столбнячного анатоксина, 25 мкг коклюшного анатоксина, 25 мкг филаментозного гемагтлютинина и 8 мкг пертактина; другие ингредиенты - алюминий (в виде гидроксида алюминия) - 0,5 мг, 2-феноксиэтанол (консервант) - 2,5 мг, натрия хлорид - 4,5 мг, вода для инъекций - до 0,5 мл. Остаточное содержание формальдегида - не более 0,2 мг/мл.
6.2.2. Комбинированные вакцины, содержащие Hib-компонент
Анализ изменений календарей профилактических прививок развитых стран за последние 15 лет показал, что основной мировой тенденцией является внедрение в педиатрическую практику комбинированных вакцин [1,2, 16,22,25].
Использование комбинированных вакцин:
а) снижает инъекционную нагрузку на ребенка, что способствует существенному улучшению восприятия вакцинации родителями и обществом в целом, увеличению охвата прививками детского населения на основе добровольного и осознанного выбора родителями профилактической вакцинации;
б) позволяет уменьшить нагрузку на медицинских работников и родителей, вызванную необходимостью дополнительных посещений ребенком поликлиники только с целью вакцинации;
в) снижает затраты на хранение и транспортирование вакцин, требующих поддержания холодовой цепи, а также расходы, связанные с персоналом, осуществляющим обеспечение холодовой цепи;
г) снижает число нежелательных реакций в поствакцинальном периоде, поскольку при использовании зарегистрированных комбинированных вакцин не происходит суммирование нежелательных явлений; тем самым снижаются и расходы, связанные с мониторингом поствакцинальных осложнений и социальной поддержкой лиц с поствакциналь-