ГОСТ Р ИСО/ТС 10993-19-2009
Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 19. Исследования физико-химических, морфологических и топографических свойств материалов
Содержит сводку параметров и методов тестирования, которые могут быть использованы для идентификации и определения физико-химических, морфологических и топографических (ФМТ) свойств материалов, используемых в медицинских изделиях. Такая оценка ограничена только теми параметрами, которые имеют отношение к биологическим свойствам и конкретной области применения медицинского изделия (клиническое применение, длительность использования), даже если эти параметры не согласуются с клинической эффективностью.
Идентичен ISO/TS 10993-19:2006.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Символы и сокращения
5 Основные принципы
6 Процедура определения свойств материалов
6.1 Общие положения
6.2 Качественная оценка
6.3 Эквивалентность материала
6.4 Количественные данные
6.5 Количественная оценка
7 Характеристические параметры и методы
8 Отчет о полученных данных
Приложение А (справочное) Принципы для оценки эквивалентности материала
Приложение В (справочное) Наночастицы. Специальное пояснение принципов оценки эквивалентности материала и биологических свойств
Приложение С (справочное) Сведения о соответствии национальных стандартов Российской Федерации ссылочным международным стандартам
Библиография
16 страниц
| Дата введения | 01.09.2010 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Завершение срока действия | 01.01.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел Электроэнергия
Организации:
| 02.12.2009 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 539-ст |
|---|---|---|---|
| Разработан | АНО ИМБИИТ | ||
| Издан | Стандартинформ | 2010 г. |
Medical devices. Biological evaluation of medical devices. Part 19. Tests physico-chemical, morphological and topographical characterization of materials
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5
стр. 6

стр. 7

стр. 8
стр. 9
стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
<Ш>
АЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
ГОСТ Р ИСО/ТС
10993-19-
2009
ИЗДЕЛИЯ МЕДИЦИНСКИЕ ОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Часть 19
Исследования физико-химических, морфологических и топографических свойств материалов
Ison'S 10993-19:2006 Biological evaluation of medical devices — Part 19: Physico-chemical, morphological and topographical characterization of materials (IDT)
Издание официальное
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация в Российской Федерации. Основные положения»
Сведения о стандарте
1 ПОДГОТОВЛЕН Автономной некоммерческой организацией «Институт медико-биологических исследований и технологий» (АНО «ИМБИИТ»)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 422 «Оценка биологического действия медицинских изделий»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 2 декабря 2009 г. № 539-ст
4 Настоящий стандарт идентичен международному стандарту ИСОЯС 10993-19:2006 «Оценка биологического действия медицинских изделий. Часть 19. Исследования физико-химических, морфологических и топографических свойств материалов» (ISO/TS 10993-19:2006 «Biological evaluation of medical devices —Part 19: Physico-chemical, morphological and topographical characterization of materials»).
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им национальные стандарты Российской Федерации, сведения о которых приведены в дополнительном приложении С
5 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты». а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ.2010
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ Р ИСОГГС 10993-19—2009
Содержание
1 Область применения...................................................1
2 Нормативные ссылки..................................................1
3 Термины и определения................................................1
4 Символы и сокращения.................................................1
5 Основные принципы...................................................2
6 Процедура определения свойств материалов...................................3
6.1 Общие положения..................................................3
6.2 Качественная оценка................................................3
6.3 Эквивалентность материала...........................................4
6.4 Количественные данные..............................................4
6.5 Количественная оценка..............................................4
7 Характеристические параметры и методы.....................................4
8 Отчет о полученных данных..............................................6
Приложение А (справочное) Принципы для оценки эквивалентности материала..............7
Приложение В (справочное) Наночастицы. Специальное пояснение принципов оценки эквивалентности материала и биологических свойств .........................8
Приложение С (справочное) Сведения о соответствии национальных стандартов Российской
Федерации ссылочным международным стандартам......................8
Библиография........................................................9
Введение
Соблюдение положений стандартов серии ИСО 10993 «Оценка биологического действия медицинских изделий» позволит обеспечить системный подход к исследованию биологического действия медицинских изделий.
Целью этих стандартов не является безусловное закрепление единообразных методов исследований и испытаний за группами однородных медицинских изделий в соответствии с принятой классификацией их по виду и длительности контакта с организмом человека. Поэтому планирование и проведение исследований и испытаний должны осуществлять специалисты, имеющие соответствующую подготовку и опыт в области санитарно-химической, токсикологической и биологической оценок медицинских изделий.
Стандарты серии ИСО 10993 являются руководящими документами для прогнозирования и исследования биологического действия медицинских изделий на стадии выбора материалов, предназначенных для их изготовления, а также для исследований готовых изделий.
В серию ИСО 10993 входят следующие части под общим названием «Оценка биологического действия медицинских изделий»:
Часть 1 — Оценка и исследования:
Часть 2 — Требования к обращению с животными;
Часть 3 — Исследования генотоксичности, канцерогенности и токсического действия на репродуктивную функцию:
Часть 4 — Исследование изделий, взаимодействующих с кровью;
Часть 5 — Исследование на цитотоксичность: методы in vitro:
Часть 6 — Исследование местного действия после имплантации;
Часть 7 — Остаточное содержание этиленоксида после стерилизации;
Часть 9 — Основные принципы идентификации и количественного определения потенциальных продуктов деградации;
Часть 10 — Исследования раздражающего и сенсибилизирующего действия;
Часть 11 — Исследование общетоксического действия;
Часть 12 — Приготовление проб и стандартные образцы;
Часть 13 — Идентификация и количественное определение продуктов деградации полимерных медицинских изделий;
Часть 14 — Идентификация и количественное определение продуктов деградации изделий из керамики;
Часть 15 —Идентификация и количественное определение продуктов деградации изделий из металлов и сплавов;
Часть 16 — Моделирование и исследование токсикокинетики продуктов деградации и вымывания:
Часть 17 — Установление пороговых значений для вымываемых веществ;
Часть 18 — Исследование химических свойств материалов;
Часть 19 — Исследования физико-химических, морфологических и топографических свойств материалов;
Часть 20 — Принципы и методы исследования иммунотоксического действия медицинских изделий.
ИСО 14971 указывает на то, что при анализе токсикологического риска следует принимать во внимание природу материала.
ИСО 10993-1 формулирует рамки структурной программы оценки биологической безопасности. ИСО 10993-1, раздел 3. устанавливает, что при выборе материалов, используемых при изготовлении медицинского оборудования, главным критерием должно быть его соответствие конкретному применению. Это относится к характеристикам и свойствам материала, включающим химические, токсикологические, физические, электрические, морфологические и механические свойства. Эту информацию необходимо получить до любых биологических испытаний. ИСО 10993-1, 7.2 отмечает, что важным аспектом качества программы является постоянное развитие методов биологической оценки.
Определение и оценка физико-химических, морфологических и топографических свойств материалов. используемых в конечном медицинском изделии, важны для оценки биологических свойств изделий и материалов, из которых они изготовлены. Такая информация может быть использована для:
- оценки биологических свойств медицинских изделий в целом (ИСО 10993);
- поиска новых перспективных материалов и/или процессов, способствующих более эффективному использованию данного медицинского оборудования.
Состав материалов, используемых при изготовлении, находится под контролем изготовителя этих материалов. Другие же характеристики, в основном, определяются требованиями, предъявляемыми к конечному медицинскому изделию, а также процессами изготовления изделий, используемыми производителем.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ИЗДЕЛИЯ МЕДИЦИНСКИЕ ОЦЕНКА БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ МЕДИЦИНСКИХ ИЗДЕЛИЙ
Часть 19
Исследования физико-химических, морфологических и топографических свойств материалов
Medical devices. Biological evaluation of medical devices. Part 19.
Tests of physico-chemical, morphological and topographical characterization of materials
Дата введения — 2010—09—01
1 Область применения
Настоящий стандарт содержит сводку параметров и методов тестирования, которые могут быть использованы для идентификации и определения физико-химических, морфологических и топографических (ФМТ) свойств материалов, используемых в медицинских изделиях. Такая оценка ограничена только теми параметрами, которые имеют отношение к биологическим свойствам и конкретной области применения медицинского изделия (клиническое применение, длительность использования), даже если эти параметры не согласуются с клинической эффективностью.
2 Нормативные ссылки
Для датированных ссылок необходимо использовать только то издание, которое указано в ссылке. Для недатированных ссылок следует применять последнее издание документа со всеми прилагаемыми поправками.
ИС010993-1 Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования
ИСО 10993-18 Оценка биологического действия медицинских изделий. Часть 18. Исследование химических свойств материалов
3 Термины и определения
В настоящем стандарте применены термины по ИСО 10993-1, ИСО 10993-18, а также следующие термины с соответствующими определениями:
3.1 физико-химический: Имеющий отношение к физической химии (материалов).
3.2 морфологический: Имеющий отношение к форме, контурам и микроструктурной организации (материалов).
3.3 топографический: Имеющий отношение к особенностям поверхности (материалов).
4 Символы и сокращения
В настоящем стандарте применены следующие сокращения:
- НЧ — наночастицы;
- ФМТ — физико-химические, морфологические и топографические.
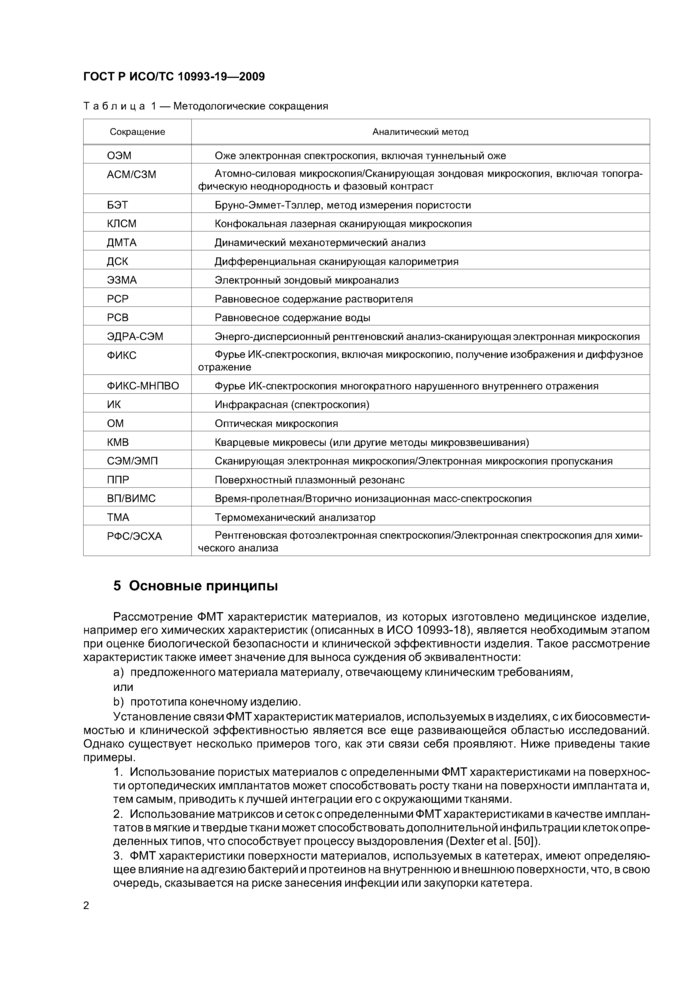
Сокращения, приведенные в таблице 1. применены в пункте 7.
Издание официальное
|
Таблица 1 — Методологические сокращения | ||||||||||||||||||||||||||||||||||||||||||
|
5 Основные принципы
Рассмотрение ФМТ характеристик материалов, из которых изготовлено медицинское изделие, например его химических характеристик (описанных в ИСО 10993-18). является необходимым этапом при оценке биологической безопасности и клинической эффективности изделия. Такое рассмотрение характеристик также имеет значение для выноса суждения об эквивалентности:
a) предложенного материала материалу, отвечающему клиническим требованиям, или
b) прототипа конечному изделию.
Установление связи ФМТ характеристик материалов, используемых в изделиях, с их биосовместимостью и клинической эффективностью является все еще развивающейся областью исследований. Однако существует несколько примеров того, как эти связи себя проявляют. Ниже приведены такие примеры.
1. Использование пористых материалов с определенными ФМТ характеристиками на поверхности ортопедических имплантатов может способствовать росту ткани на поверхности имплантата и, тем самым, приводить к лучшей интеграции его с окружающими тканями.
2. Использование матриксов и сеток с определенными ФМТ характеристиками в качестве имплантатов в мягкие и твердые ткани может способствовать дополнительной инфильтрации клетокопре-деленных типов, что способствует процессу выздоровления (Dexter et al. (50)).
3. ФМТ характеристики поверхности материалов, используемых в катетерах, имеют определяющее влияние на адгезию бактерий и протеинов на внутреннюю и внешнюю поверхности, что, в свою очередь, сказывается на риске занесения инфекции или закупорки катетера.
ГОСТ Р ИСОГГС 10993-19—2009
4. Изменение микро топографии поверхности, например нанесение микроцарапин или другой определенной картинки, оказывает влияние на адгезию и направление движения клеток определенных типов на поверхности (Alaerts et al. [46]. Dewez et al. [49]).
5. Для определенных медицинских изделий, например ортопедических имплантатов или сосудистых протезов, механические свойства могут вызывать биологическую реакцию, например перестройку ткани.
Примечание — Форма и геометрические размеры медицинских изделий и их частей могут оказывать влияние на биологические свойства изделий. Это касается, например, отношения поверхности к объему, толщины и формы по отношению к потоку крови. Информация по конкретным изделиям может быть найдена в соответствующих стандартах на данное изделие.
Настоящий стандарт содержит ряд примеров с описанием ФМТ параметров и методов, которые могут быть использованы для получения ФМТ характеристик материалов, используемых для медицинских изделий.
Изготовители медицинских изделий должны выбрать соответствующие параметры и методы, а также обосновать сделанный выбор.
Степень оценки свойств материалов должна отражать природу и длительность клинического применения, а также может представлять интерес для оценки биологической безопасности изделия. ФМТ характеристики должны также отражать тип материала и его физическое состояние, например твердое тело, жидкость, гель, полимер, металл, керамика, композит или материал биологического происхождения. Оценка свойств материалов, как правило, требует тесной кооперации материаловедов, аналитиков и экспертов по оценке риска.
6 Процедура определения свойств материалов
6.1 Общие положения
Выбор аналитических методов диктуется тем. какая информация должна быть получена для оценки. Перед тем. как разрабатывать новые методы, необходимо изучить существующие стандарты, монографии. научные статьи и другие научные источники по соответствующей тематике на предмет уже существующих методов тестирования. Методы, найденные в литературе, должны быть соответствующим образом адаптированы и подтверждены перед использованием. Если существующие методы не подходят, то тогда необходимо провести разработку новых методов.
Аналитические методы должны быть проверены, подтверждены и описаны в разделах 7 и 8. Подтверждение аналитического метода — это процесс, в котором устанавливается пригодность характеристик, полученных данным методом, требованиям соответствующего аналитического применения. Аналитические методы должны быть подтверждены соответствующими утвержденными характеристиками: точность, ошибка измерения, специфичность, предел детектирования, предел количественной оценки, линейность, диапазон, прочность, сопротивляемость и системная пригодность.
Адекватность полученных данных на каждом этапе процедуры оценки свойств материалов должна быть подтверждена на основе анализа рисков. Данная процедура должна касаться каждого материала по мере его появления в конструкции конечного изделия.
Примечание — Поставщик может рекомендовать использование соответствующих аналитических методов. В отсутствие каких-либо начальных данных по свойствам материалов выбор соответствующих аналитических методов может быть сделан на основе анализа литературы.
6.2 Качественная оценка
Описывают материал/изделие и цель его использования. Рекомендуется документированное качественное описание ФМТ характеристик конечного изделия, включая характеристики каждого материала. используемого в изделии (см. 3.2 и раздел 4 ИСО 10993-1) (см. приложение А). Уровень качественных данных должен отражать категорию медицинского изделия в терминах инвазивности и длительности клинического использования, а также природы данного материала.
Качественное описание, по мере возможности, должно включать детали партии или лота, поставщика и спецификацию для каждого материала.
Изготовители медицинского изделия должны иметь качественную и количественную информацию о характеристиках конечного продукта. Такая информация может быть получена от поставщика исходного материала, из литературы или путем дополнительного тестирования. ФМТ характеристики данного материала должны либо находиться в соответствии со стандартами, принятыми для данных материалов. либо быть предоставлены изготовителем. На этой начальной стадии необходимо получить как можно больше информации, чтобы обеспечить понимание возможных опасностей (потенциальных рисков) и
возможных преимуществ от использования данного материала и оценить его пригодность для данного применения. Данная оценка будет в дальнейшем улучшена по мере получения дополнительной информации в процессе разработки продукта.
6.3 Эквивалентность материала
Частьюоценки пригодности материала является сопоставление этих данныхс целью определения эквивалентности данного материала материалу, используемому в изделии с той же длительностью клинического использования, полученного в результате того же процесса изготовления и подвергнутого той же процедуре стерилизации, например, для установления безопасного и эффективного использования материалов в продукте, предназначенном для контакта с кожей. В приложении А содержится дальнейшее руководство, согласно которому можно судить об эквивалентности материала, а в приложении В содержится информация, касающаяся специального случая материала, используемого в виде наночастиц (размер 5 100 нм хотя бы в одном измерении).
6.4 Количественные данные
В случае, если качественной информации о материале не достаточно для определения его полной пригодности, необходимая количественная информация должна быть получена, документирована и подвергнута оценкам на пользу и риск.
6.5 Количественная оценка
Частью оценки биологических свойств медицинских изделий является получение достаточной количественной информации, необходимой для того, чтобы оценить пригодность использования всех материалов по назначению в готовом для применения изделии. Эти количественные характеристики могут быть сопоставлены с соответствующими данными, полученными для материалов и/или готовых для применения медицинских изделий, безопасность и эффективность использования которых для данной цели клинически установлена. Полезно также сопоставить количественную информацию с информацией, полученной для материалов или продуктов, характеристики которых не пригодны для данного использования. Такая полная оценка находится за пределами области применения настоящего стандарта и будет дополняться сведениями, взятыми из многих других частей серии международных стандартов ИСО 10993. а также будет использовать информацию, содержащуюся в ИСО 14971.
7 Характеристические параметры и методы
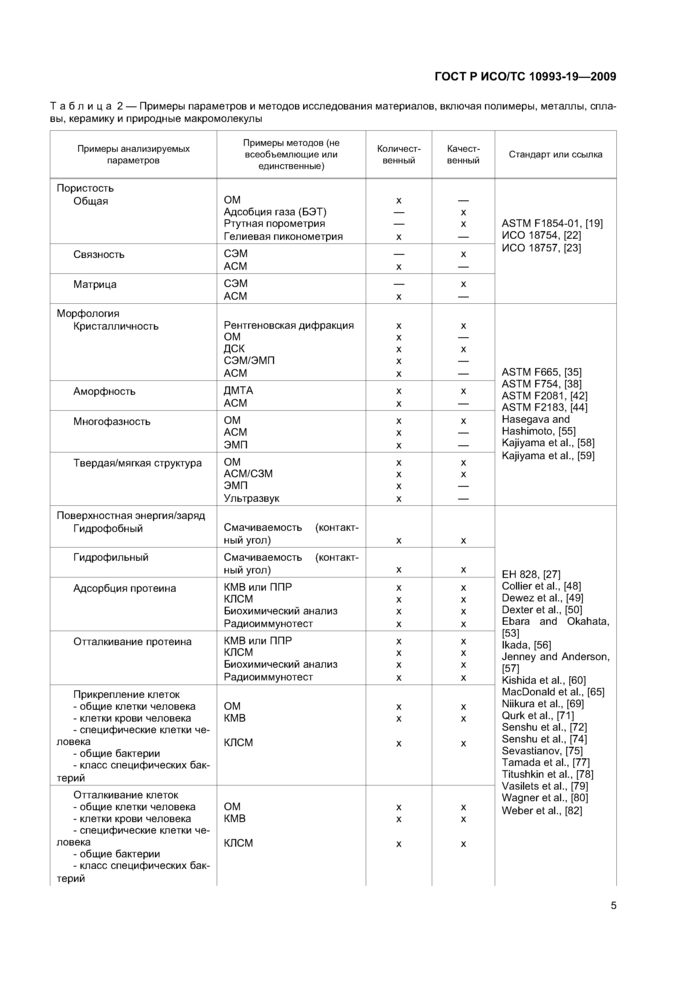
В разделе 6 сформулированы качественные и количественные ФМТ характеристики для использования их при оценке пригодности и риска. В таблице 2 суммируются примеры параметров, необходимых для оценки свойств материалов, и примеры методов, которые могут быть использованы для получения качественной или количественной информации. Соответствующие стандарты и/или ссылки даны для каждого параметра, например для топографии. Не все параметры и связанные с ними методы могут быть применены для материалов всех типов. Характерные параметры следует выбирать соответственно материалу или готовому для применения медицинскому изделию. Вследствие многообразия медицинских изделий установлено, что не все параметры, присущие данному материалу, будут существенны для всех или некоторых применений медицинских изделий. Как отмечается в 6.2. степень оценки свойств материалов, которую необходимо применить, определяется инвазивностью и длительностью клинического использования приданном применении.
Аналитик и специалист в области материаловедения в процессе консультаций с экспертом по оценке риска должны определить, какие параметры существенны при оценке материала или медицинского изделия. Соответствующие данные должны быть получены для всех параметров, являющихся существенными по мнению эксперта по оценке риска.
Примечание — Для природных макромолекул важно, чтобы организм (или его часть), являющийся их источником, а также его происхождение/состояние были бы идентифицированы с самого начала. Серия стандартов ИСО 22442 описывает безопасное использование биотканей животного происхождения и их производных при изготовлении медицинских изделий. EN 455-3 описывает оценку рисков, связанных с остаточным содержанием протеинов в натуральном латексе.
Природные макромолекулы, используемые в медицинских изделиях, включают в себя белки, гликопротеины. полисахариды, керамику и другие соединения. Примерами таких соединений являются: желатин, коллаген, эластин, фибрин, альбумин, альгинат, целлюлоза, гепарин, хитозан, переработанные кости, коралловая и натуральная губка. Все эти материалы могут быть переработаны, очищены и модифицированы до различной степени. Многие из этих материалов описаны в фармакологических монографиях. Характеристики этих материалов содержатся в некоторых стандартах ASTM F04.
4
ГОСТ Р ИСОГГС 10993-19—2009
|
Таблица 2 — Примеры параметров и методов исследования материалов, включая полимеры, металлы, сплавы. керамику и природные макромолекулы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
5 |
|
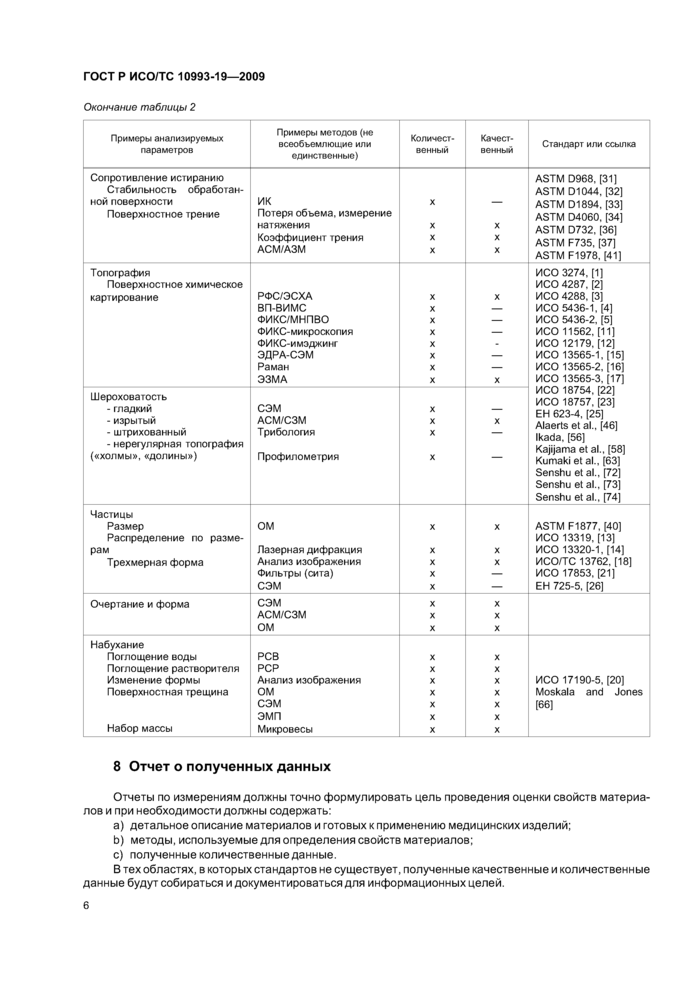
Окончание таблицы 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
8 Отчет о полученных данных
Отчеты по измерениям должны точно формулировать цель проведения оценки свойств материалов и при необходимости должны содержать:
a) детальное описание материалов и готовых к применению медицинских изделий;
b) методы, используемые для определения свойств материалов;
c) полученные количественные данные.
В тех областях, в которых стандартов не существует, полученные качественные и количественные данные будут собираться и документироваться для информационных целей.
6