ГОСТ Р 59326-2021
Молоко и молочное сырье. Определение наличия ветеринарных препаратов и химиотерапевтических лекарственных средств методом иммуноферментного анализа с хемилюминесцентной детекцией с применением технологии биочипов
Купить ГОСТ Р 59326-2021 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на сырое молоко, молочное сырье и устанавливает иммуноферментный метод одновременного определения наличия следующих ветеринарных препаратов и химиотерапевтических лекарственных средств с применением технологии биочипов: - авермектины; - 2-аминобензимидазолы; - амфениколы; - апрамицин; - баквилоприм; - бацитрацин; - бензимидазолы; - бета-лактамы; - вирджиниямицин М1; - галофугинон; - гентамицин; - гигромицин B; - 5-гидрокси-флуниксины; - дапсон; - дексаметазон; - дерквантел; - имидокарб; - канамицин А; - клозантел; - клорсулон; - ласалоцид; - левамизол; - линкомицин; - мелоксикам; - метамизолы; - метилпреднизолоны; - моксидектин; - монензин; - монепантел; - морантел; - неомицины; - нитроксинил; - новобиоцин; - оксиклозанид; - оксфендазолсульфон; - пирлимицин; - полимиксины; - рактопамин; - рифаксимин; - спектиномицин; - спирамицины; - стрептомицины; - сульфагуанидин; - сульфаметазины; - сульфапиридины; - сульфонамиды; - тетрациклины; - тиабендазол; - тилдипирозин; - тилозины; - тобрамицин; - толтразурил; - толфенамовая кислота; - триклабендазол; - триметоприм; - трипиленамин; - фенилбутазоны; - хинолоны; - хлормадинон; - цефалексин; - цефуроксим; - эритромицины. Метод, предусмотренный настоящим стандартом, не является контрольным методом. В качестве контрольного метода применяют метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11
стр. 12
стр. 13
стр. 14
стр. 15
стр. 16
стр. 17
стр. 18
стр. 19
стр. 20

стр. 21
стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27
ГОСТ Р
59326—
2021
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
МОЛОКО И МОЛОЧНОЕ СЫРЬЕ
Определение наличия ветеринарных препаратов и химиотерапевтических лекарственных средств методом иммуноферментного анализа с хемилюминесцентной детекцией с применением технологии биочипов
Издание официальное
СШЩЩ11М|фирМ
2021
Предисловие
1 РАЗРАБОТАН Федеральным государственным автономным научным учреждением «Всероссийский научно-исследовательский институт молочной промышленности» (ФГАНУ «ВНИМИ»)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 470 «Молоко и продукты переработки молока»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 11 февраля 2021 г. No 73-ст
4 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. № 162-ФЗ «О стандартизации в Российской Федерации». Информация об изменениях к настоящему стандарту публикуется в ежегод>юм (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в ин-формационной системе общего пользования — на официалыюм сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (wwyv.gost.ru)
© Стандартинформ. оформление. 2021
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии II
9.1.1.8 С биочипов сливают рабочий буферный раствор, а затем полностью его удаляют, постукивая держателем кассет по безворсовой ткани.
9.1.1.9 В каждую лунку вносят по 0,250 см3 рабочего раствора субстрата, приготовленного по 7.1.3. избегая воздействия солнечных лучей, и оставляют на (120 ± 10) с.
9.1.1.10 По истечении (120 ± 10) с держатель кассет с биочипами помещают в иммунохимичесхий анализатор (5.1.1) и проводят измерение интенсивности люминесценции биочипов согласно инструкции. прилагаемой к анализатору.
9.1.2 Проведение измерений с применением тест-системы N9 2
9.1.2.1 В держатель кассет вставляют необходимое количество кассет с биочипами.
Схема заполнения кассеты с биочипами приведена в приложении Б (пункты Б. 1.1, Б. 1.2).
9.1.2.2 На каждый биочип (лунку) кассеты (5.3.1) наносят по 0.100 см3 аналитического буферного раствора для разведения (5.3.2). обеспечивая равномерное покрытие всей поверхности биочипа.
В лунку 1 добавляют 0,100 см3 контрольного раствора «Аналитический стандарт», приготовленного по 7.1.1.2.
В лунки 2—9 добавляют по 0,100 см3 анализируемой пробы продукта, подготовленной по 7.3.
Растворы в лунках перемешивают аккуратным постукиванием (не менее 10 раз) по ребру держателя кассет с биочипами.
9.1.2.3 Держатель кассет с биочипами помещают в термошейкер и перемешивают/инкубируют при температуре (25 ± 2) °С в течение 30 мин.
9.1.2.4 В каждую лунку вносят по 0,100 см3 раствора ферментного конъюгата (5.3.7) и продолжают перемешивание/инкубирование в термошейкере при температуре (25 ± 2) °С еще в течение 60 мин.
9.1.2.5 Далее проводят процедуры согласно 9.1.1.5—9.1.1.10.
9.2 Проведение измерений с применением автоматического иммунохимического анализатора
9.2.1 В лунку кассеты (5.4.1) вносят 0,500 см3 анализируемой пробы продукта, подготовленной по 7.3.
Схема заполнения кассеты и картриджа с биочипом приведена в приложении Б (пункт Б. 1.3).
9.2.2 Кассету с биочипом и реагентами с внесенной по 9.2.1 анализируемой пробой продукта и картридж с наконечниками для дозаторов (5.4.4) помещают в автоматический анализатор (5.1.2) и проводят измерение интенсивности люминесценции биочипов согласно инструкции, прилагаемой к анализатору.
9.2.3 Периодически один раз в 30 дней автоматический анализатор запрашивает проведение контроля качества с использованием контрольного раствора «Положительный стандарт». В этом случае в лунку кассеты (5.4.1) вместо пробы анализируемого продукта вносят 0,500 см3 контрольного раствора «Положительный стандарт», приготовленного по 7.1.2, и далее проводят процедуры согласно 9.2.2.
10 Обработка результатов измерений
Обработку результатов измерений проводят с применением программного обеспечения, прилагаемого к анализатору.
Результаты анализа отображаются на дисплее иммунохимического анализатора биочипов и сохраняются в памяти прибора.
Если анализируемая проба продукта определена как отрицательная, программное обеспечение отображает значение «n.d.»/«H.O.» (не обнаружено). Это означает, что определяемые вещества в анализируемом продукте отсутствуют или их массовая концентрация менее предела обнаружения.
Если анализируемая проба продукта определена как положительная, программное обеспечение отображает «Positive»/«Обнаружено». Массовая концентрация определяемых веществ в анализируемом продукте более или равна пределу обнаружения.
Примеры вариантов отображения результатов анализа приведены в приложении В.
Дополнительная информация по применению иммунохимического анализатора биочипов для определения ветеринарных препаратов и химиотерапевтических лекарственных средств в пастеризованном молоке, обезжиренном молоке, концентрированном молоке и молочной сыворотке приведена в приложении Г.
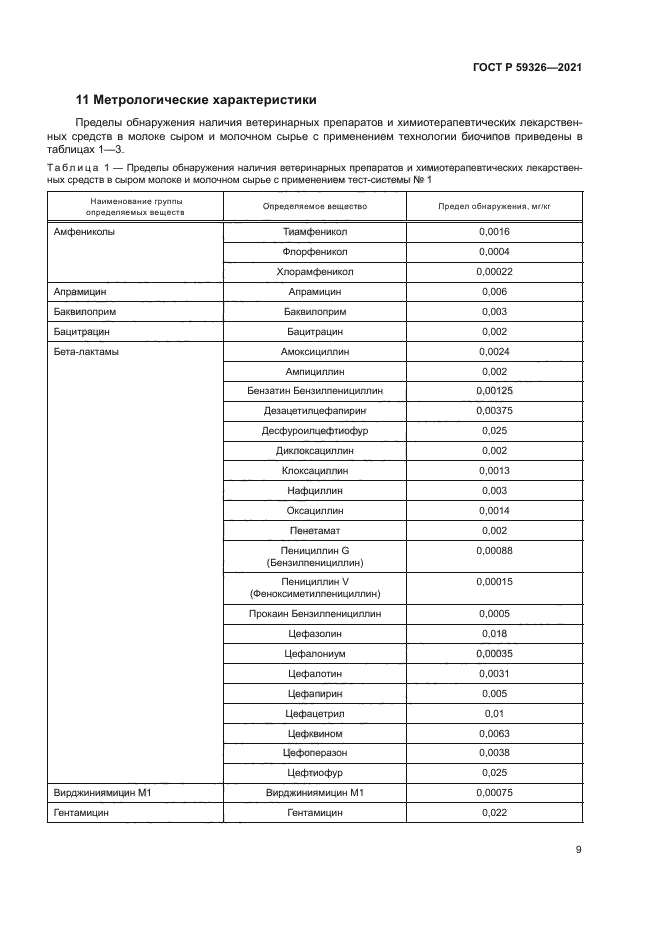
11 Метрологические характеристики
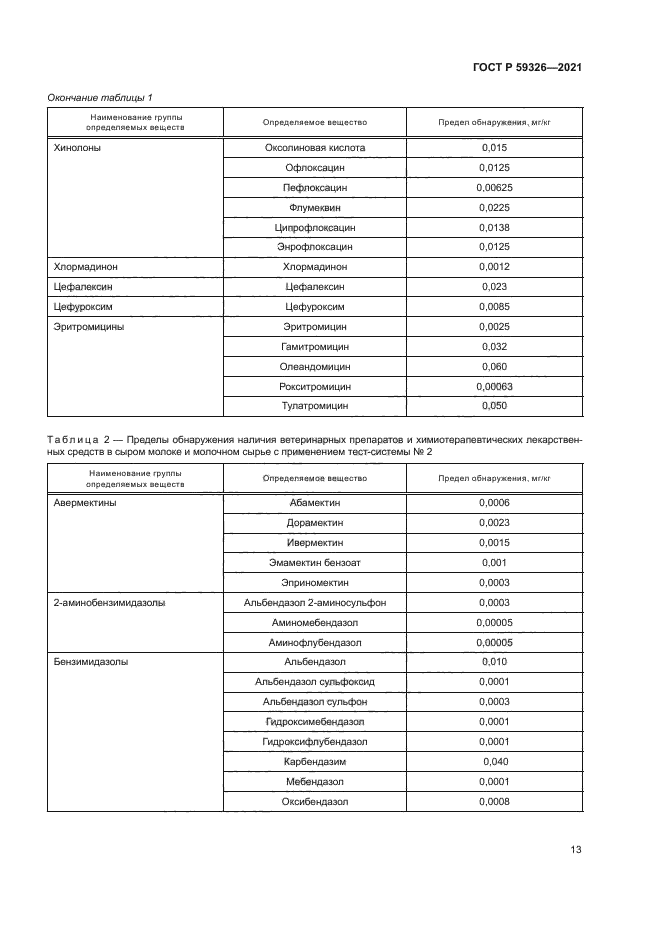
Пределы обнаружения наличия ветеринарных препаратов и химиотерапевтических лекарственных средств в молоке сыром и молочном сырье с применением технологии биочилов приведены в таблицах 1—3.
|
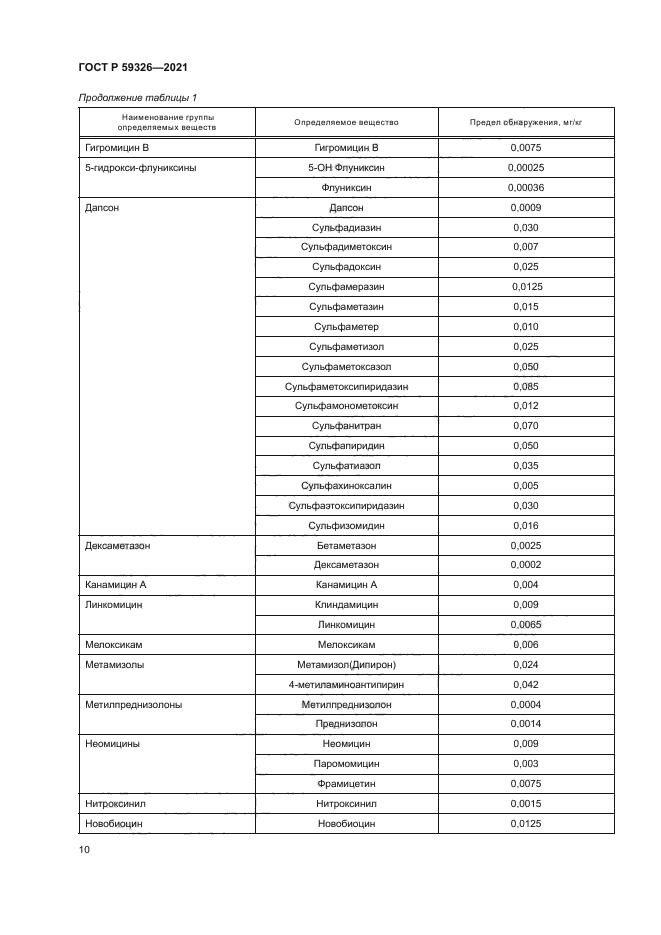
Таблица 1 — Пределы обнаружения наличия ветеринарных препаратов и химиотерапевтических лекарственных средств в сыром молоке и молочном сырье с применением тест-системы № 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
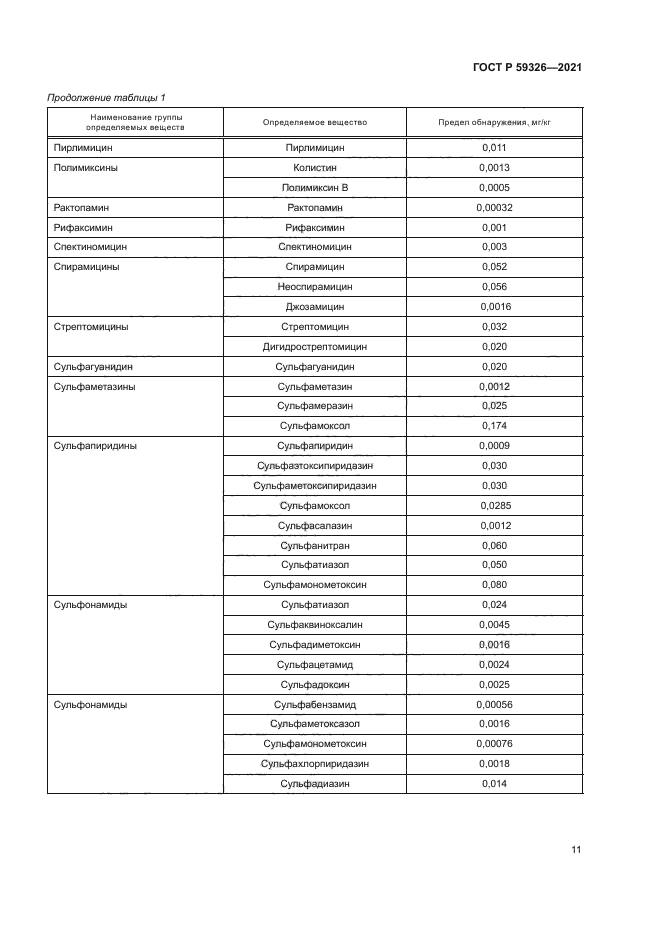
Продолжение таблицы 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Наименование группы определяемых веществ |
Определяемое вещество |
Предел обнаружения, мг/кг |
|
Пирлимицин |
Пирлимицин |
0.011 |
|
Полимиксины |
Колистин |
0.0013 |
|
Полимиксин В |
0.0005 | |
|
Рактопамин |
Рактоламин |
0.00032 |
|
Рифаксимин |
Рифаксимин |
0,001 |
|
Спвктиномицин |
Спвктиномицин |
0,003 |
|
Спирамицины |
Слирамицин |
0.052 |
|
Нвослирамицин |
0,056 | |
|
Джозамицин |
0.0016 | |
|
Стрелтомицины |
Стрептомицин |
0,032 |
|
Дигидрострвптомицин |
0.020 | |
|
Сульфа гуанидин |
Сульфа гуанидин |
0,020 |
|
Сульфамвтазины |
Сульфамвтазин |
0.0012 |
|
Сульфамеразин |
0.025 | |
|
Сульфа моксол |
0.174 | |
|
Сульфалиридины |
Сульфал иридии |
0.0009 |
|
Сульфаэтоксилиридазин |
0,030 | |
|
Сульфамвтоксипиридазин |
0.030 | |
|
Сульфа моксол |
0.0285 | |
|
Сульфасапазин |
0.0012 | |
|
Супьфанитран |
0.060 | |
|
Сульфатиазол |
0,050 | |
|
Сульфамономвтоксин |
0,080 | |
|
Сульфонамиды |
Сульфатиазол |
0,024 |
|
Сульфа квиноксалин |
0.0045 | |
|
Сульфадимвтоксин |
0,0016 | |
|
Сульф ацетамид |
0.0024 | |
|
Сульфадоксин |
0.0025 | |
|
Сульфонамиды |
Сульфабензамид |
0.00056 |
|
Сульфамвтоксазол |
0.0016 | |
|
Сульфамономвтоксин |
0.00076 | |
|
Сульфа хлорпирида зин |
0.0018 | |
|
Сульфадиазин |
0,014 |
|
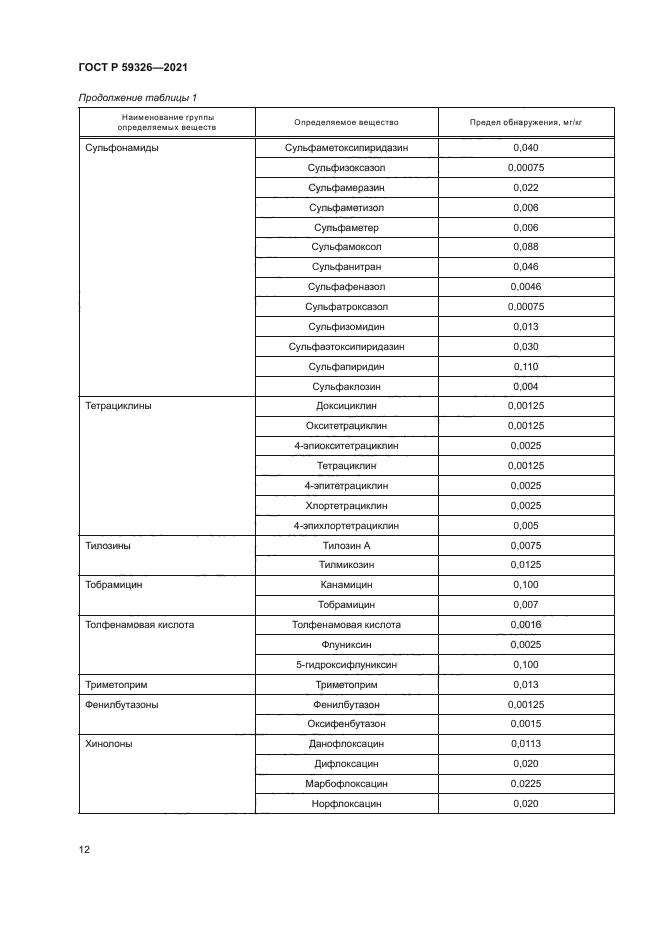
Продолжение таблицы 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Наименование труппы определяемых веществ |
Определяемое вещество |
Предел обнаружения, мг/кт |
|
Хинолоны |
Оксолиновая кислота |
0,015 |
|
Офлоксацин |
0.0125 | |
|
Пефлоксацин |
0.00625 | |
|
Флумеквин |
0.0225 | |
|
Ципрофлоксацин |
0,0138 | |
|
Энрофлоксацин |
0,0125 | |
|
Хлормадинон |
Хлормадинон |
0,0012 |
|
Цефалексин |
Цефалексин |
0.023 |
|
Цефуроксим |
Цефуроксим |
0,0085 |
|
Эритромицины |
Эритромицин |
0,0025 |
|
Гамитромицин |
0.032 | |
|
Олеандомицин |
0,060 | |
|
Рокситромицин |
0,00063 | |
|
Тулатромицин |
0.050 |
|
Таблица 2 — Пределы обнаружения наличия ветеринарных препаратов и химиотерапевтических лекарственных средств в сыром молоке и молочном сырье с применением тест-системы № 2 | ||||||||||||||||||||||||||||||||||||||
|
|
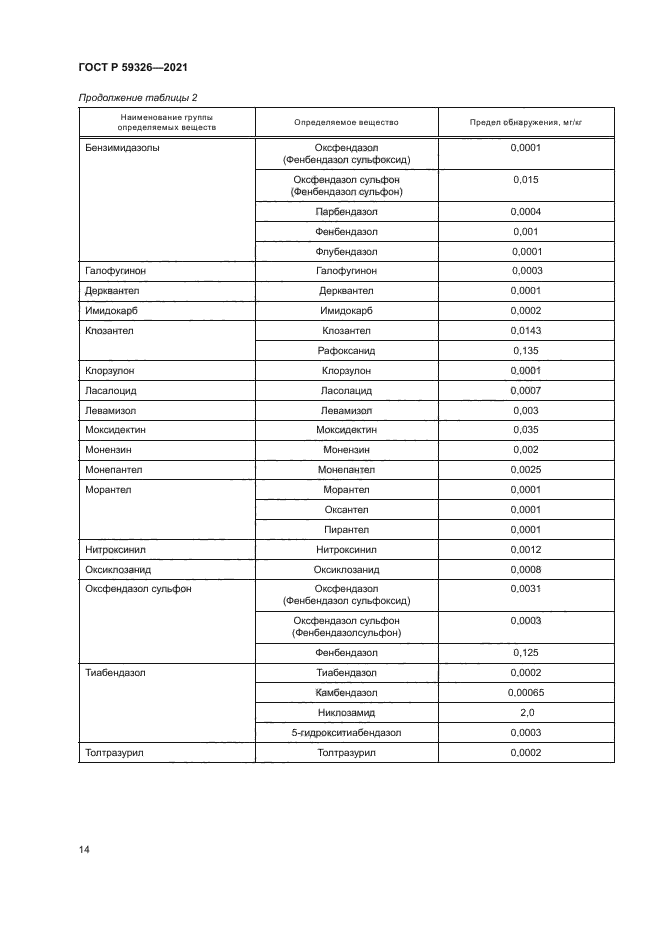
Продолжение таблицы 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Наименование группы определяемых веществ |
Определяемое вещество |
Предел обнаружения, мг/кг |
|
Триклабендаэол |
Триклабендаэол |
0.0015 |
|
Триклабендаэол сульфоксид |
0.0008 | |
|
Триклабендаэол сульфон |
0.0006 | |
|
Кето-триклабендазол |
0.0007 |
|
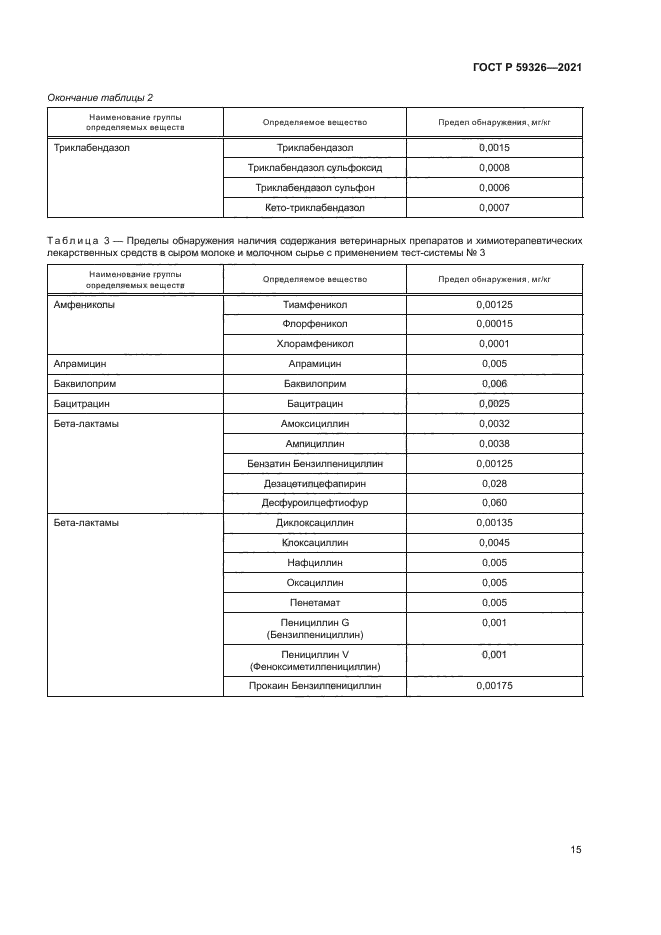
Таблица 3 — Пределы обнаружения наличия содержания ветеринарных препаратов и химиотерапевтических лекарственных средств в сыром молоке и молочном сырье с применением тест-системы № 3 | |||||||||||||||||||||||||||||||||||||||||||||||
|
|
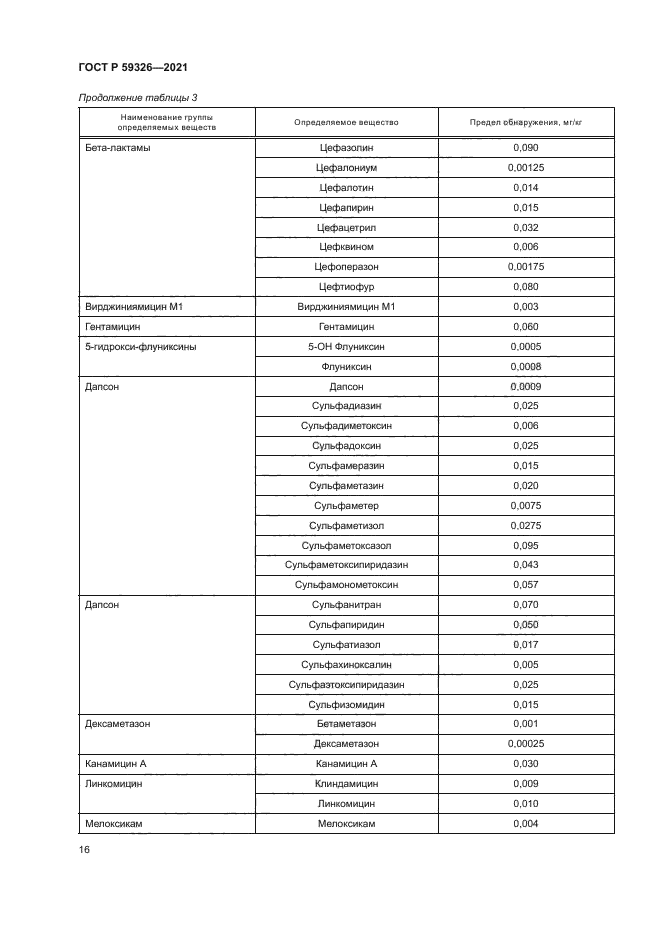
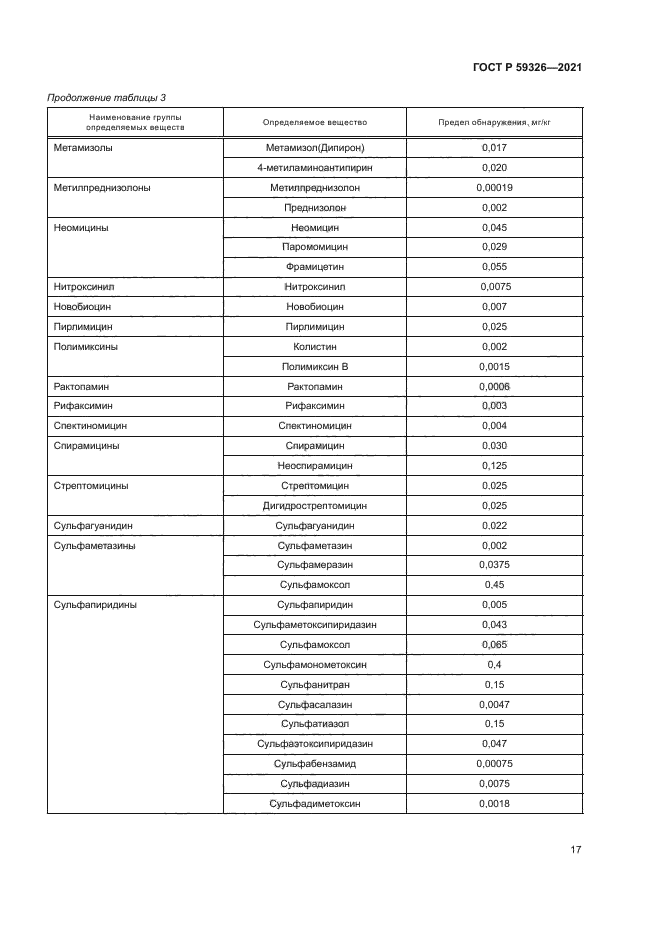
Продолжение таблицы 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Наименование группы определяемых веществ |
Определяемое вещество |
Предел обнаружения, мг/кг |
|
Метамиэолы |
Мвтамизол (Дипирон) |
0,017 |
|
4-метилами ноантипирин |
0,020 | |
|
Метилпредниээлоны |
Метиллреднизолон |
0.00019 |
|
Преднизолон |
0,002 | |
|
Нвомицины |
Неомицин |
0,045 |
|
Паромомицин |
0,029 | |
|
Фрамицетин |
0.055 | |
|
Нитроксинил |
Нитроксинил |
0.0075 |
|
Новобиоцин |
Новобиоцин |
0.007 |
|
Пирлимицин |
Пирлимицин |
0,025 |
|
Полимиксины |
Колистин |
0.002 |
|
Полимиксин В |
0.0015 | |
|
Рактоламин |
Рактопамин |
0,0006 |
|
Рифаксимин |
Рифаксимин |
0.003 |
|
Слектиномицин |
Спектиномицин |
0.004 |
|
Слирамицины |
Спирамицин |
0.030 |
|
Неослирамицин |
0.125 | |
|
Стрелтомицины |
Стрептомицин |
0.025 |
|
Дигидрострептомицин |
0,025 | |
|
Сульфагуанидин |
Сульфагуанидин |
0.022 |
|
Сульфаметазины |
Сульфаметазин |
0,002 |
|
Сульфамеразин |
0.0375 | |
|
Сульфамоксол |
0.45 | |
|
Сульфапяриди.ны |
Сульфапиридин |
0,005 |
|
Сульфаметоксипиридазин |
0,043 | |
|
Сульфамоксол |
0,065 | |
|
Сульфамонометоксин |
0.4 | |
|
Сульфанитран |
0.15 | |
|
Сульфасалазин |
0.0047 | |
|
Сульфатиазол |
0.15 | |
|
Сульфаэтоксипиридазин |
0.047 | |
|
Супьфабензамид |
0.00075 | |
|
Сульфадиазин |
0.0075 | |
|
Сульфадиметохсин |
0.0018 |
Содержание
1 Область применения.................................................................1
2 Нормативные ссылки.................................................................2
3 Термины и определения...................................... 3
4 Сущность метода....................................................................3
5 Средства измерений, вспомогательное оборудование, материалы, посуда и реактивы...........4
6 Отбор проб.........................................................................5
7 Подготовка к проведению измерений....................................................5
8 Условия проведения измерений........................................................7
9 Проведение измерений...............................................................7
10 Обработка результатов измерений.....................................................8
11 Метрологические характеристики......................................................9
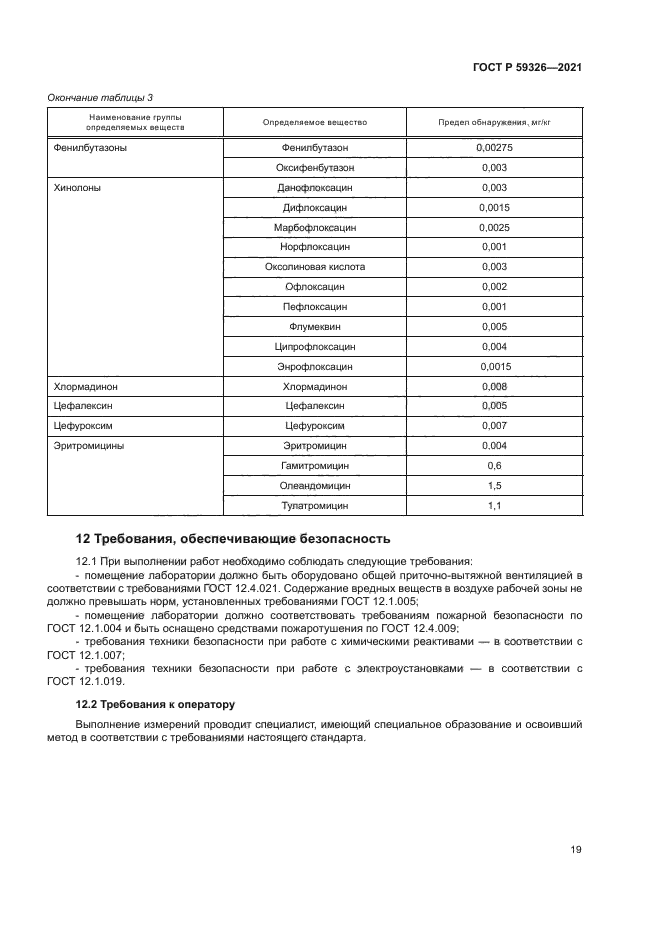
12 Требования, обеспечивающие безопасность............................................19
Приложение А (справочное) Примерный перечень применяемого оборудования и тест-систем____20
Приложение Б (справочное) Схома заполнения кассеты с биочипами.........................21
Приложение В (справочное) Варианты отображения результатов анализа на иммунохимическом
анализаторе биочипов....................................................22
Приложение Г (справочное) Дополнительная информация по применению иммунохимического анализатора биочипов для определения наличия ветеринарных препаратов и химиотерапевтических лекарственных средств в пастеризованном молоке.
обезжиренном молоке, концентрированном молоке и молочной сыворотке........23
Библиография.......................................................................24
|
Продолжение таблицы 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
МОЛОКО И МОЛОЧНОЕ СЫРЬЕ
Опроделонио наличия ветеринарных препаратов и химиотерапевтических лекарственных средств методом иммуноферментного анализа с хемилюминесцентной детекцией с применением технологии биочипов
Milk and milk raw material.
Determination of veterinary drugs and chemotherapeutic drugs by enzyme immunoassay with chemiluminescent detection using biochip technology
Дата введения — 2021—03—15
1 Область применения
Настоящий стандарт распространяется на сырое молоко, молочное сырье* (далее — продукт) и устанавливает иммуноферментный метод одновременного определения наличия следующих ветеринарных препаратов и химиотерапевтических лекарственных средств с применением технологии биочипов:
- авермектины;
- 2-аминобемзимидазолы,
- амфениколы;
- апрамицин;
- баквилоприм;
- бацитрацин:
- бензимидазолы:
- бета-лактамы;
- вирджиниямицин М1;
- галофугинон;
- гентамицин;
- гмгромицин В;
- 5-гидрокси-флуниксины:
- дапсон;
- дексаметазон;
- дерквантел;
- имидокарб:
- канамицин А:
- кпозантел:
- клорсулон;
- ласалоцид;
- левамизол;
- линкомицин;
- мелоксикам;
- метамизолы;
- метиллреднизолоны;
- моксидектин:
* В настоящем стандарте к молочному сырью относят: пастеризованное молоко, обезжиренное молоко, концентрированное молоко и молочную сыворотку.
Издание официальное
- монензин;
- монепантел;
- морантел;
- меомицины:
- нитроксинил;
* новобиоцин;
- оксиклозанид;
- оксфендазолсульфон;
- пирлимицин;
- лолимиксины;
- рактоламин;
* рифаксимин;
- слектииомицим:
- слирамицины;
- стрептомицины;
- сульфагуанидин,
- сульфаметазины;
- сульфапиридины;
- сульфонамиды:
- тетрациклины;
- тиабендазол:
- тилдипирозин;
- тилозины;
- тобрамицин;
- толтразурил;
- толфемамовая кислота;
* триклабендазол;
- триметоприм:
- трипиленамим;
* фенилбутазоны;
- хинолоны:
- хлормадинон;
* цофалвксин;
- цефуроксим;
* эритромицины.
Метод, предусмотренный настоящим стандартом, не является контрольным методом. В качестве контрольного метода применяют метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектором.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ 12.1.004 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.4.009 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 12.1.019 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ 12.4.021 Система стандартов безопасности труда. Системы вентиляционные. Общие требования
ГОСТ 1770 (ИСО 1042—83. ИСО 7788—80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия 2
ГОСТ 4233 Реактивы. Натрий хлористый. Технические условия ГОСТ 6709 Вода дистиллированная. Технические условия
ГОСТ 13928 Молоко и сливки заготовляемые. Правила приемки, методы отбора проб и подготовка их к анализу
ГОСТ 25336 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 26809.1 Молоко и молочная продукция. Правила приемки, методы отбора и подготовки проб к анализу. Часть 1. Молоко, молочные, молочные составные и молокосодержащие продукты
ГОСТ 27752 Часы электронно-механические кварцевые настольные, настенные и часы-будильники. Общие технические условия
ГОСТ Р 52501 (ИСО 3696:1987) Вода для лабораторного анализа. Технические условия ГОСТ OIML R 76-1 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания ГОСТ Р ИСО 707 Молоко и молочные продукты. Руководство по отбору проб
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя «Национальные стандарты» за текущий год. Если заменен ссылочный стандарт, на который дана недатированная ссылка, то рекомендуется использовать действующую версию этого стандарта с учетом всех внесенных в данную версию изменений. Если заменен ссылочный стандарт, на который дана датированная ссылка, го рекомендуется использовать версию этого стандарта с указанным выше годом утверждения (принятия). Если после утверждения настоящего стандарта в ссылочный стандарт, на который дана датированная ссылка, внесено изменение, затрагивающее положение, на которое дана ссылка, то это положение рекомендуется применять без учета данного изменения. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, рекомендуется применять в части, не затрагивающей эту ссыпку.
3 Термины и определения
В настоящем стандарте применены термины по [1]. а также следующие термины с соответствующими определениями:
3.1 иммуноформентный метод: Метод определения низкомолекулярных соединений, макромолекул. вирусов и пр„ в основе которого лежит специфическая реакция «антиген—антитело». Для выявления образовавшегося комплекса в качестве метки для регистрации сигнала применяют специфический для каждой реакции фермент или ферментозависимое вещество.
3.2 тест-систома (тест-набор): Набор (комплект) специально подобранных реагентов (реактивов). оборудования и составных частей, предназначенный для определения одного или нескольких конкретных химиотерапевтических лекарственных средств или групп химиотерапевтических лекарственных средств и ветеринарных препаратов.
4 Сущность метода
Иммунофермеитный метод с хемилюминесцентной детекцией (ИФА-Х) с применением технологии биочипов основан на одновременном измерении анализатором массовой концентрации химиотерапевтических лекарственных средств и ветеринарных препаратов в растворах экстрактов анализируемых проб продукта с помощью прямого твердофазного ИФА-Х.
Метод основан на конкуренции химиотерапевтических лекарственных средств и ветеринарных препаратов к антителам, адсорбированным на дискретных участках биочипа.
В ходе иммуноспецифической реакции образуются комплексы «антитела—лекарственные вещества». Вещества, не связанные с поверхностью биочипа комплексом «антиген—антитело», удаляют на стадии промывания.
После добавления раствора субстрата регистрируют значение интенсивности люминесценции, характеризующее степень взаимодействия антител с антигенами. Измеренное анализатором значение обратно пропорционально массовой концентрации определяемых лекарственных средств и ветеринарных препаратов в растворе.
5 Средства измерений, вспомогательное оборудование, материалы, посуда и реактивы
Примерный перечень оборудования и тест-систем изложен в приложении А.
5.1 Анализатор биочипов иммунохимичоский
5.1.1 Анализатор биснипов иммунохимичосхий полуавтоматический, включающий:
- компьютер с установленным программным обеспечением для управления и обработки результатов измерений;
- блок измерительный, включающий камеру с зарядовой связью для регистрации хемилюминесценции;
- держатель кассет с биочипами;
- термошейкер для перемешивания/инкубации проб;
- сканер штрих-кодов, позволяющий распознавать тест-систему.
5.1.2 Анализатор биочипов иммунохимический автоматический, включающий:
* блок измерительный, включающий камеру с зарядовой связью для регистрации хемилюминесценции, роботизированную систему дозирования и специализированное программное обеспечение:
- сканер штрих-кодов, позволяющий распознавать тест-систему.
5.2 Тест-система No 1 для определения антибиотиков с применением иммунохимичесхого анализатора биочипов полуавтоматического, приведенное в 5.2.1—5.2.7. включающая:
5.2.1 Кассеты с биочипами.
5.2.2 Раствор аналитический буферный для разведения.
5.2.3 Раствор контрольный «Аналитический стандарт» лиофилизированный.
5.2.4 Раствор люминола.
5.2.5 Раствор перекиси водорода.
5.2.6 Концентрат буферного раствора для промывания биочипов.
5.2.7 Раствор ферментного конъюгата.
5.3 Тест-система № 2 для определения кокцидиостатиков и антигельминтных препаратов в молоке с применением иммунохимичесхого анализатора биочипов полуавтоматического, приведенное в 5.3.1—5.3.7, включающая:
5.3.1 Кассеты с биочипами.
5.3.2 Раствор аналитический буферный для разведения.
5.3.3 Раствор контрольный «Аналитический стандарт» лиофилизированный.
5.3.4 Раствор люминола.
5.3.5 Раствор перекиси водорода.
5.3.6 Концентрат буферного раствора для промывания биочипов.
5.3.7 Раствор ферментного конъюгата.
5.4 Тест-система No 3 для определения антибиотиков в молоке с применением иммунохимическо-го анализатора биочипов автоматического, приведенное в 5.4.1— 5.4.4, включающая:
5.4.1 Кассета с биочипом (картридж), содержащая комплекс реагентов, необходимых для проведения иммуноферментного анализа.
5.4.2 Раствор контрольный «Положительный стандарт» лиофилизированный.
5.4.3 Раствор буферный для восстановления.
5.4.4 Картридж с наконечниками для дозаторов.
5.5 Весы неавтоматического действия по ГОСТ OIML R 76-1 с пределом допускаемой абсолютной погрешности не более ±0.01 г.
5.6 Часы 2-го класса точности по ГОСТ 27752.
5.7 Секундомер механический или электронный.
5.8 Вортекс лабораторный.
5.9 Испаритель роторный любого типа или устройство для испарения экстрактов с термостатиру-емым нагревательным модулем, поддерживающим температуру от 25 °С до 100 °С, с системой отдувки растворителей инертным газом.
5.10 Система получения деионизированной воды высокой чистоты.
5.11 Центрифуга лабораторная, обеспечивающая скорость вращения 4000 об/мин.
5.12 Дозаторы пипеточные (пилвт-дозаторы) переменного объема дозирования в диапазоне 0.005—0.05 см3,0.1—1.0 см3. 1.0—5.0 см3 с наконечниками.
5.13 Дозатор пипеточный (пипет-дозатор) переменного объема дозирования в диапазоне 1,0—5.0 см3 со стерильными наконечниками.
5.14 Колбы мерные 1-1000-2 по ГОСТ 1770.
5.15 Цилиндры 1-10 (25. 50)-2 по ГОСТ 1770.
5.16 Виалы из темного стекла с крышкой вместимостью 2 см3.
5.17 Пробирка П-1-15(25)-0,2 или П-2-15(25)-14/23 по ГОСТ 1770 или ПЗ-25(50) по ГОСТ 25336 или пробирки полипропиленовые вместимостью 20-50 см3 с завинчивающимися крышками.
5.18 Пробирки типа Эппендорф вместимостью 0.5—1.5 см3.
5.19 Стаканы В-1-50(150) по ГОСТ 25336.
5.20 Флаконы из темного стекла с крышками вместимостью 10—50 см3 для приготовления рабочего раствора субстрата.
5.21 Промывалка лабораторная.
5.22 Ткань безворсовая.
5.23 Ацетонитрил, содержание основного вещества не менее 98 %.
5.24 н-Гексан. содержание основного вещества не менее 98 %.
5.25 Магний сернокислый безводный, содержание основного вещества не менее 98 %.
5.26 Натрий хлористый по ГОСТ 4233. ч.д.а.
5.27 Вода дистиллированная по ГОСТ 6709.
5.28 Вода деионизированная 2-й степени чистоты по ГОСТ Р 52501.
Допускается применение других средств измерений, испытательного и вспомогательного оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающих необходимую точность измерений, а также реактивов по качеству но ниже вышеуказанных.
6 Отбор проб
Отбор и подготовка проб — по ГОСТ Р ИСО 707. ГОСТ 13928. ГОСТ 26809.1.
Если измерение не может быть проведено сразу после отбора проб продукта, то неконсервированные пробы продукта хранят в холодильнике при температуре (4 ± 2) °С не более 36 ч.
Если измерение не может быть проведено в течение 36 ч. то после отбора проб допускается замораживание проб продукта при температуре (минус 20 ± 2) еС.
Титруемая кислотность анализируемого сырого молока не должна превышать 21.0 °Т.
7 Подготовка к проведению измерений
7.1 Приготовление реактивов и реагентов
7.1.1 Приготовление контрольного раствора «Аналитический стандарт»
7.1.1.1 Приготовление контрольного раствора «Аналитический стандарт» при применении тест-системы No 1 (5.2)
Во флакон с контрольным раствором «Аналитический стандарт» (5.2.3) добавляют 1 см3 деионизированной воды, флакон закрывают пробкой. Содержимое флакона аккуратно перемешивают в течение 20 мин. не допуская образования пены.
Восстановленный контрольный раствор «Аналитический стандарт» стабилен в течение 8 ч при хранении его при температуре от 2 °С до 8 СС.
Восстановленный контрольный раствор «Аналитический стандарт» делят на аликвоты объемом 0,1 см3 в пробирках типа Эппендорф или виалах из темного стекла в течение 1 ч после приготовления и хранят при температуре (минус 20 ± 2) еС но более 1 мес.
После размораживания контрольный раствор «Аналитический стандарт» стабилен в течение 8 ч при хранении его при температуре от 2 °С до 8 °С. Отбирают только необходимое количество материала. Не допускается повторное замораживание восстановленного раствора.
7.1.1.2 Приготовление контрольного раствора «Аналитический стандарт» при применении тест-системы No 2 (5.3)
Во флакон с контрольным раствором «Аналитический стандарт» (5.3.3) добавляют 6 см3 деионизированной воды, флакон закрывают пробкой. Содержимое флакона аккуратно перемешивают в течение 20 мин. не допуская образования пены.
Далее восстановленный контрольный раствор «Аналитический стандарт» готовят по 7.3.2. помещая в центрифужную пробирку вместимостью 30 см3 вместо 5 см3 анализируемого продукта 5 см3 восстановленного контрольного раствора «Аналитический стандарт».
7.1.2 Приготовление контрольного раствора «Положительный стандарт»
Контрольный раствор «Положительный стандарт» используют при применении тест-системы N9 3
(5.4).
Во флакон с контрольным раствором «Положительный стандарт» (5.4.2) добавляют 1 см3 буферного раствора для восстановления (5.4.3) и закрывают крышкой. Содержимое флакона аккуратно перемешивают, не допуская образования пены, и оставляют на 20 мин.
Восстановленный контрольный раствор «Положительный стандарт» делят на аликвоты объемом по 0,3 см3 в виалах из темного стекла в течение 1 ч после приготовления и хранят при температуре (минус 20 ± 2) аС не более 1 мес.
После размораживания контрольный раствор «Положительный стандарт» стабилен в течение 8 ч при хранении его при температуре от 2 5С до 8 ’С. Отбирают только необходимое количество материала. Не допускается повторное замораживание восстановленного раствора.
7.1.3 Приготовление рабочего раствора субстрата при применении тест-системы № 1 (5.2) и тест-системы № 2 (5.3)
Рабочий раствор субстрата готовят, смешивая раствор люминола (5.2.4, 5.3.4) и раствор перекиси водорода (5.2.5. 5.3.5). прилагаемые к тест-системе, в пропорции 1:1 (V/V). На одну кассету с биочипами (девять лунок) необходимо приблизительно 3 см3 рабочего раствора субстрата или 0.250 см3 рабочего раствора субстрата на одну лунку.
Во флакон из темного стекла соответствующей вместимости, используя пипет-доэатор с одноразовыми стерильными наконечниками, помещают необходимые количества растворов люминола (5.2.4. 5.3.4) и перекиси водорода (5.2.5. 5.3.5), при этом раствор люминола добавляют к раствору перекиси водорода, избегая воздействия солнечных лучей.
Полученную смесь аккуратно перемешивают в течение 15 мин.
Рабочий раствор субстрата остается стабильным в течение 4 ч при температуре от 15 °С до 25 °С.
7.1.4 Приготовление рабочего буферного раствора для промывания биочипов при применении тест-системы № 1 (5.2) и тест-системы № 2 (5.3)
В мерную колбу вместимостью 1000 см3 помещают 32 см3 концентрата буферного раствора для промывания биочипов (5.2.6. 5.3.6). добавляют небольшое количество деионизированной воды по ГОСТ Р 52501 и аккуратно перемешивают, объем раствора доводят деионизированной водой до метки.
Срок хранения раствора при температуре от 2 °С до 8 °С — не более 1 мес.
7.2 Подготовка анализатора
Подготовку анализатора проводят в соответствии с прилагаемой к прибору инструкцией.
7.3 Подготовка анализируемой пробы продукта
7.3.1 Подготовка проб продукта при применении тест-системы № 1 и тест-системы № 3
Перед проведением измерения пробы продукта перемешивают, переворачивая не менее трех раз.
Замороженные продукты предварительно размораживают и выдерживают при комнатной температуре в течение 20 мин.
Не допускается проведение измерений проб продукта, если после их размораживания наблюдается выпадение осадка или образование сгустков.
7.3.2 Подготовка проб продукта при применении тест-системы № 2
В центрифужную пробирку вместимостью 30 см3 помещают 5 см3 анализируемого продукта, добавляют 10 см3 ацетонитрила (5.23) и перемешивают на вортексе в течение 60 с. К полученной смеси добавляют (0.05 ± 0.01) г натрия хлористого (5.26). (2.00 ± 0.01) г магния сернокислого безводного (5.25) и тщательно перемешивают во избежание образования комочков. Затем, после получения однородной смеси, добавляют 4 см3 н-Гексана (5.24) и перемешивают на вортексе в течение 60 с.
Полученную смесь центрифугируют при 4000 об/мин в течение 8 мин. Дозатором отбирают 4 см3 нижней фракции, переносят в чистую стеклянную пробирку и сушат в токе азота при температуре (50 ± 2) °С. Полученный сухой остаток растворяют в 0.5 см3 рабочего буферного раствора для промывания. приготовленного по 7.1.4. После этого анализируемая проба продукта подготовлена для проведения измерений.
7.4 Подготовка тест-системы к проведению измерений
7.4.1 Перед применением тест-систему достают из холодильника и выдерживают при комнатной температуре не менее 30 мин. после чего каждый флакон с реагентами, входящий в тест-систему, перемешивают. аккуратно встряхивая его.
После использования флаконы с реагентами сразу убирают в холодильник.
На всех этапах проведения измерений воздействия прямого солнечного света но допускается.
7.4.2 При применении полуавтоматического иммунохимического анализатора биочипов добавление реактивов проводят при помощи пилотирования по направлению к переднему краю биочипа. Для каждого реагента используют отдельный наконечник липет-дозатора. Внесение растворов на биочипы проводят осторожно, не касаясь наконечником пипет-дозатора поверхности биочипа.
8 Условия проведения измерений
При выполнении измерений в лаборатории необходимо соблюдать следующие условия:
температура окружающего воздуха....................от 18 °С до 27 ®С;
относительная влажность воздуха.....................(50 ± 30) %;
атмосферное давление..............................(96 ± 10) кПа.
9 Проведение измерений
9.1 Проведение измерений с применением полуавтоматического иммунохимического анализатора
9.1.1 Проведение измерений с примененном тест-системы № 1
9.1.1.1 В держатель кассет вставляют необходимое количество кассет с биочипами.
Схема заполнения кассеты с биочипами приведена в приложении Б (пункты Б.1.1. Б.1.2).
9.1.1.2 На каждый биочип (лунку) кассеты (5.2.1) наносят по 0.175 см3 аналитического буферного раствора для разведения (5.2.2). обеспечивая равномерное покрытие всей поверхности биочипа.
В лунку 1 добавляют 0.025 см3 контрольного раствора «Аналитический стандарт», приготовленного по 7.1.1.1.
В лунки 2—9 добавляют по 0.025 см3 анализируемой пробы продукта, подготовленной по 7.3.
Растворы в лунках перемешивают аккуратным постукиванием (не менее 10 раз) по ребру держателя кассет с биочипами.
9.1.1.3 Держатель кассет с биочипами помещают в термошейкер и перемешивают/инкубируют при температуре (25 ± 2) °С в течение 30 мин.
9.1.1.4 В каждую лунку вносят по 0.100 см3 раствора ферментного конъюгата (5.2.7) и продолжают перемешивание/инкубирование в термошейкере при температуре (25 ± 2) еС еще в течение 60 мин.
9.1.1.5 Держатель кассет с биочипами достают из термошейкера и сливают реактивы. Биочипы быстро промывают, добавляя в каждую лунку приблизительно по 0.350 см3 рабочего буферного раствора для промывания биочипов, приготовленного по 7.1.4. и выливая его. Процедуру повторяют дважды, при этом необходимо избегать переполнения лунок, чтобы не допустить попадания посторонних примесей из лунки в лунку.
9.1.1.6 После этого в каждую лунку опять вносят по 0.350 см3 рабочего буферного раствора для промывания биочипов, приготовленного по 7.1.4, аккуратно перемешивают, постукивая по всем краям держателя кассет с биочипами в течение 10—15 с, и оставляют в покое на 2 мин. Затем раствор удаляют. Процедуру повторяют четыре раза.
9.1.1.7 После последнего промывания в каждую лунку вносят по 0,350 см3 рабочего буферного раствора для промывания биочипов, приготовленного по 7.1.4. и оставляют до добавления рабочего раствора субстрата в темном месте, но не более чем на 30 мин.