ГОСТ Р 58504-2019
Информатизация здоровья. Идентификация лекарственных средств. Руководство по внедрению элементов данных и структуры ISO 11239 для уникальной идентификации и обмена регистрируемой информацией о дозированных лекарственных формах, единицах представления, путях введения и упаковке
Купить ГОСТ Р 58504-2019 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Описывает элементы данных и структуры для уникальной идентификации и обмена регистрируемой информацией о дозированных лекарственных формах, единицах представления, путях введения и упаковке.
На основании принципов, изложенных в стандарте, гармонизированные нормативные терминологии будут разрабатываться в соответствии с утвержденным процессом ведения, позволяющим пользователям сверяться с терминологиями и находить надлежащие термины для понятий, которые им требуется описать. для облегчения идентификации подходящих терминов будут описаны также условия отображения существующих региональных терминологий на гармонизированные нормативные терминологии. Предусмотренные для терминов коды могут в дальнейшем использоваться в соответствующих полях таких объектов, как PhPID (идентификатор лекарственного препарата), PCID (идентификатор упаковки лекарственного средства), MPID (идентификатор лекарственного средства), чтобы идентифицировать эти понятия.
Стандарт предназначен для использования:
- любой организацией, которая может быть ответственной за разработку и ведение нормативных словарей;
- любыми региональными уполномоченными органами или изготовителями программного обеспечения, предполагающими использовать нормативные словари в своих системах и понять принцип их создания;
- владельцами баз данных, которым требуется сопоставить свои термины с основным перечнем нормативных словарей;
- другими пользователями, желающими понять иерархию нормативных словарей в целях поиска наиболее подходящего термина, описывающего конкретное понятие.
Терминология, подлежащая применению в контексте стандарта и обозначенная в ИСО 11239, находится в разработке. Все коды, термины, определения, используемые в качестве примеров в стандарте, представлены только для иллюстрации и не предназначены для использования в качестве окончательной терминологии.
Идентичен ISO/TS 20440:2016
Оглавление
1 Область применения
2 Организация нормативных терминов
2.1 Общие сведения
2.2 Пара "код и термин" и кодированное понятие
2.3 Управление версиями
3 Терминологии
3.1 Общие сведения
3.2 дозированная лекарственная форма
3.3 Комбинированная лекарственная форма
3.4 Единица представления
3.5 Путь Введения
3.6 Упаковка
4 Отображение территориальных терминов
4.1 Различия в деталях территориальных терминологий
4.2 Организация территориальных терминов в базе данных
Библиография
| Дата введения | 01.05.2020 |
|---|---|
| Добавлен в базу | 01.02.2020 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 29.08.2019 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 574-ст |
|---|---|---|---|
| Разработан | ФГУП СТАНДАРТИНФОРМ | ||
| Издан | Стандартинформ | 2019 г. |
Health informatics. Identification of medicinal products. Implementation guide for ISO 11239 data elements and structures for the unique identification and exchange of regulated information on pharmaceutical dose forms, units of presentation, routes of administration and packaging
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7
стр. 8

стр. 9
стр. 10

стр. 11

стр. 12

стр. 13
стр. 14
стр. 15

стр. 16

стр. 17

стр. 18

стр. 19
стр. 20
стр. 21

стр. 22
стр. 23
стр. 24
стр. 25
стр. 26
стр. 27
стр. 28

стр. 29
стр. 30
|
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ |
ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР58504—
2019/
ISO/TS 20440:2016
ИНФОРМАТИЗАЦИЯ ЗДОРОВЬЯ
Идентификация лекарственных средств. Руководство по внедрению элементов данных и структуры ISO 11239 для уникальной идентификации и обмена регистрируемой информацией о дозированных лекарственных формах, единицах представления, путях введения и упаковке
(ISO/TS 20440:2016, ЮТ)
т
Издание официальное
Москва
Стандартинформ
2019
Предисловие
1 ПОДГОТОВЛЕН Федеральным государственным унитарным предприятием «Российский научно-технический центр информации по стандартизации, метрологии и оценке соответствия» (ФГУП «СТАНДАРТИНФОРМ») на основе собственного перевода на русский язык англоязычной версии документа. указанного в пункте 4
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 468 «Информатизация здоровья»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 29 августа 2019 г. № 574-ст
4 Настоящий стандарт идентичен международному документу ISO/TS 20440:2016 «Информатизация здоровья. Идентификация лекарственных средств. Руководство по внедрению элементов данных и структуры ISO 11239 для уникальной идентификации и обмена регистрируемой информацией о дозированных лекарственных формах, единицах представления, путях введения и упаковке» (ISO/TS 20440:2016 «Health informatics. Identification of medicinal products. Implementation guide for IS011239 data elements and structures for the unique identification and exchange of regulated information on pharmaceutical dose forms, units of presentation, routes of administration and packaging», IDT)
5 ВВЕДЕН ВПЕРВЫЕ
Правила применения настоящего стандарта установлены в статье 26 Федерального закона от 29 июня 2015 г. № 162-ФЗ «О стандартизации в Российской Федерации». Информация об изменениях к настоящему стандарту публикуется в ежегодном (по состоянию на 1 января текущего года) информационном указателе «Национальные стандарты», а официальный текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ближайшем выпуске ежемесячного информационного указателя «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
О ISO, 2016 — Все права сохраняются ©Стандартинформ, оформление. 2019
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
II
|
Таблица 2 — Пример пары «код и термин» дозированной лекарственной формы «Таблетка» в британском английском | ||||||||||||||||||||
| ||||||||||||||||||||
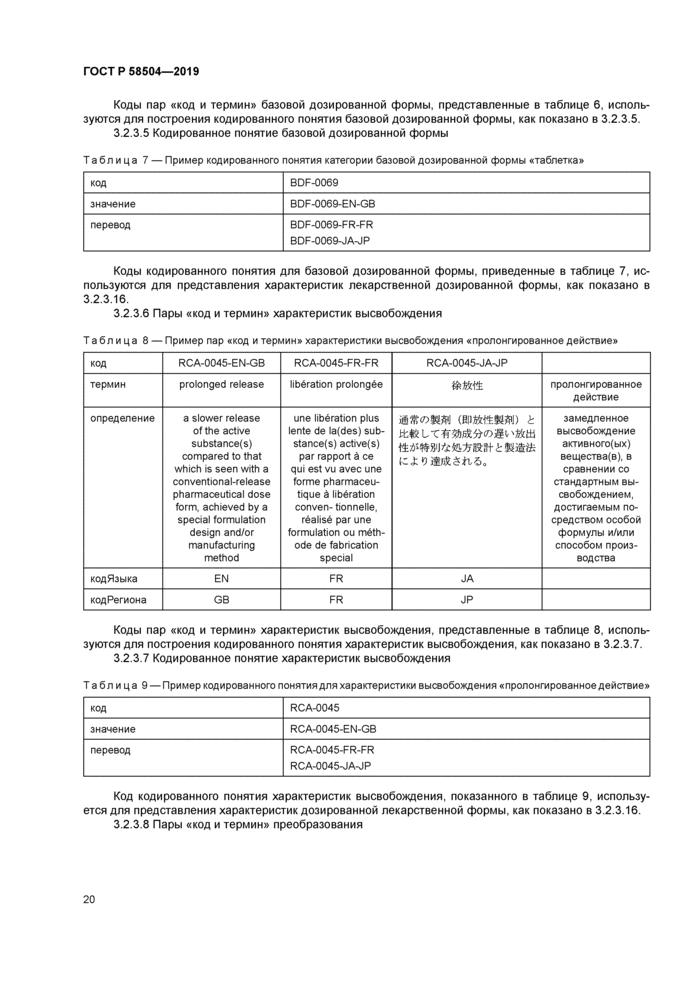
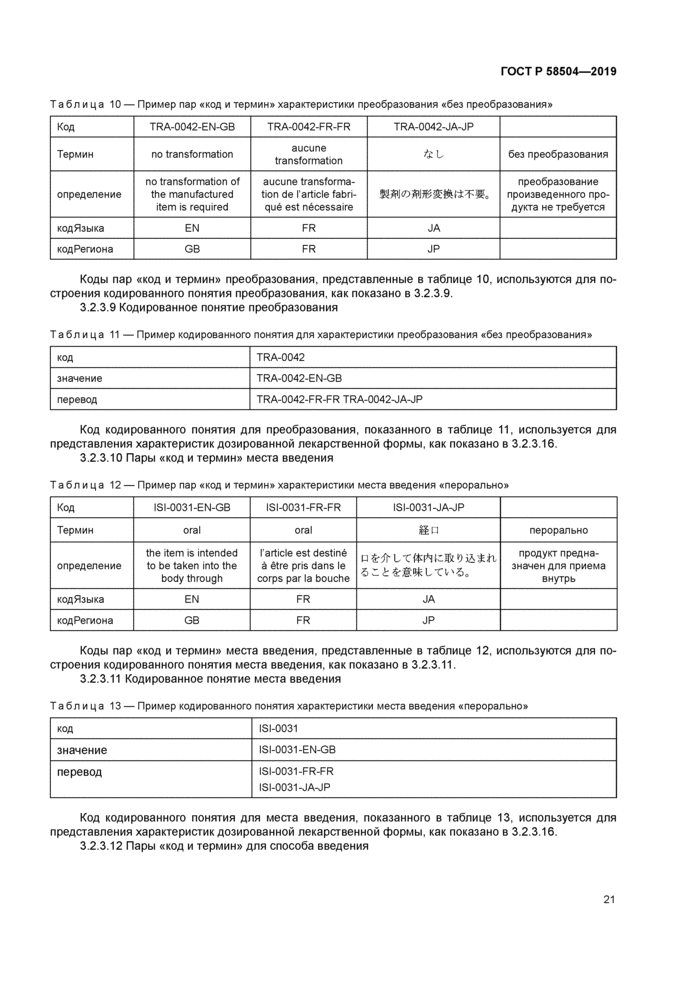
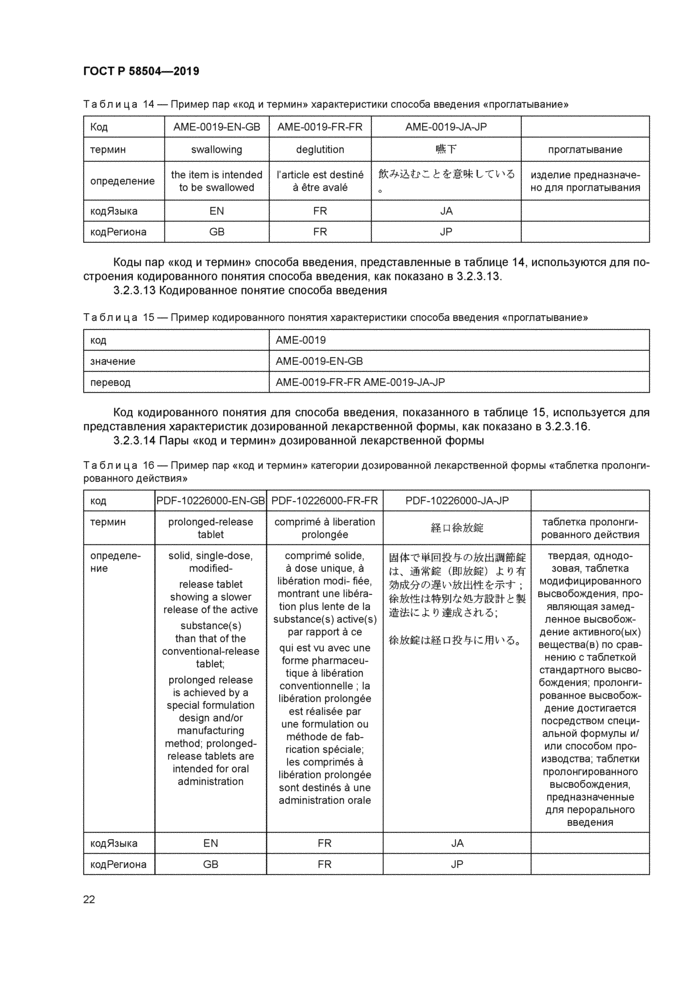
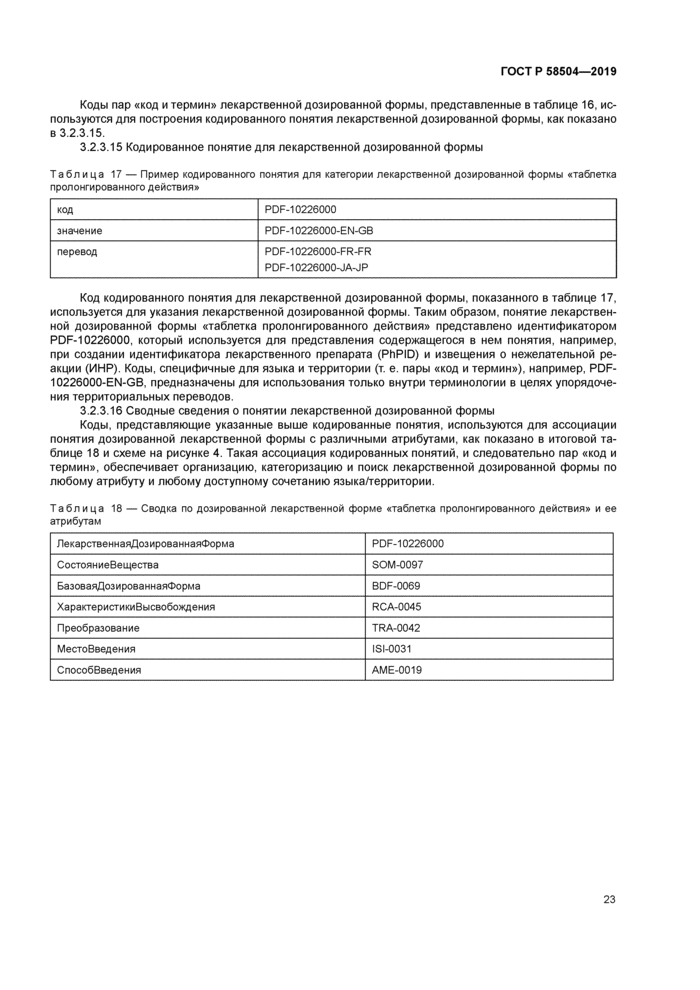
2.2.3 Кодированное понятие
2.2.3.1 Обзор кодированного понятия
Этот класс используется для представления собственно понятия и представляет собой совокупность пар «код и термин», определяющих то же понятие для кахщого сочетания языка/территории. Пары «код и термин» конкретного понятия могут рассматриваться как различные переводы этого понятия. кодированное понятие объединяет эти различные переводы в едином уникальном коде. Для представления кодированного понятия одна из пар «код и термин» выбирается в качестве «значения», а каждая другая пара «код и термин» является «переводом».
Использование кодированного понятия в другой системе позволяет идентифицировать понятие без указания конкретного языка и территории. Пара «код и термин», выбранная в качестве «значения» может использоваться как используемая по умолчанию для представления кодированного понятия, когда требуется текстовое представления термина. В настоящем стандарте по умолчанию для представления пары «код и термин» используется сочетание EN-GB (британский английский язык). Когда запрашивающая система задает сочетание язык/территория, то для представления кодированного понятия может использоваться пара «код и термин», соответствующая этому сочетанию.
Как описано в 2.2.2.1, если требуется новое понятие, должно быть создано новое кодированное понятие и для хранения данных, описывающих понятие, требуется как минимум одна пара «код и термин». Сочетание язык/территория. выбранное для представления «значения», должно создаваться всегда, даже если запрос на описание нового понятия исходит из места, где используется другое сочетание язык/территория. Организация, ответственная за ведение терминологии, должна предоставить инструкции по запросу нового термина или пересмотру уже существующего.
|
2.2.3.2 Кодированное понятие: код | ||||||||||
|
|
2.2.3.3 Кодированное понятие: значение | ||||||||||
|
|
2.2.3.4 Кодированное понятие: перевод | ||||||||||
|
2.2.3.5 Пример кодированного понятия
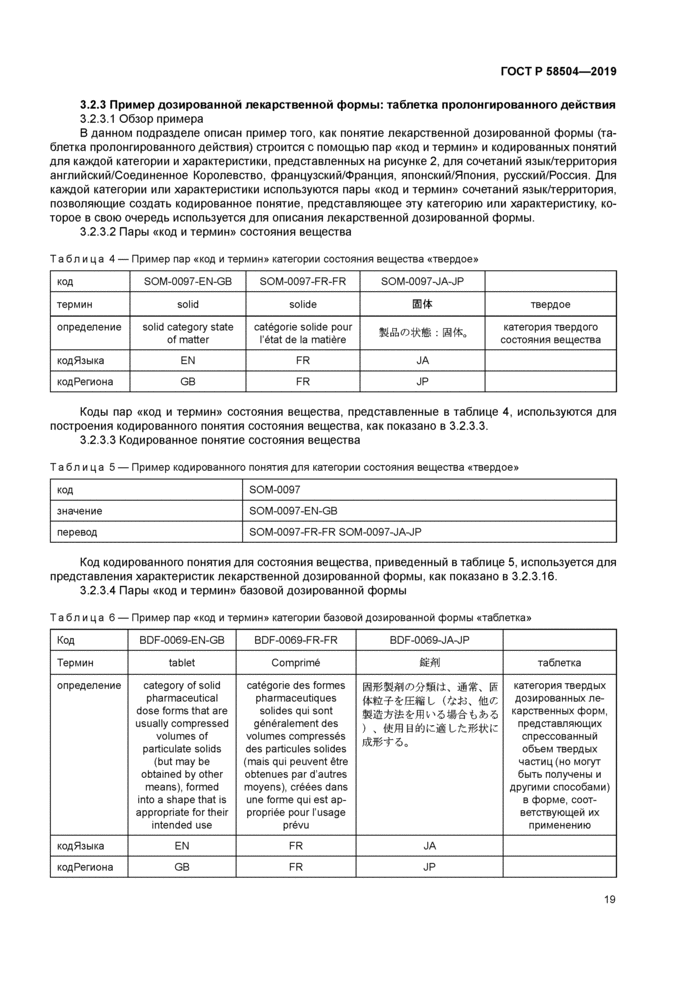
Пример кодированного понятия для понятия «табпетка» представлен в таблице 3. Поскольку рабочим языком настоящего стандарта является британский английский, значением будет пара «код и термин», для которой язык — английский, территория — Соединенное Королевство (как показано в таблице 2). Для упрощения примера с ним связаны только два перевода здесь: пара «код и термин», для которой язык — французский, территория — Франция, а также пара «код и термин», для которой язык — японский, территория — Япония. Как видно из таблицы 3. требуются только идентификаторы пар «код и термин», поскольку каждые представляет всю необходимую информацию по каждому сочетанию язык/территория (пример для английского языка 8 Соединенном Королевстве приведен в таблице 2). Понятие «таблетка» в целом (т е. охватывающее все сочетания язык/территория) имеет свой собственный идентификатор (код PDF-10219000 в данном примере).
|
Таблица 3 — Пример кодированного понятия для дозированной лекарственной формы «таблетка», связывающего пары «код и термин» понятия на английском языке (Соединенное Королевство), французском (Франция), японском (Япония) | ||||||
|
2.3 Управление версиями
2.3.1 Управление версиями термина
Стандарт ИСО/ТР 14872 описывает принципы и процедуры управления версиями и их изменениями.
Пары «код и термин» используются для заполнения терминологической базы данных, и, как таковые. могут рассматриваться в качестве текущего представления конкретных понятий для конкретного сочетания языка/территории. Они содержат информацию, рассматриваемую как наиболее важную и релевантную для пользователя базы данных. Тем не менее, поскольку нормативные словари могут изменяться стечением времени, возникают ситуации, при которых термины, хранящиеся в базе данных, нуждаются в пересмотре, что приводит к необходимости пересмотра пары «код и термин».
Для поддержания прослеживаемости истории пары «код и термин», включая любые ее изменения, камздая пара «код и термин» ассоциирована с версионной информацией. Это делается с помощью использования версий. Каждый раз. когда пара «код и термин» создается или изменяется, создается версия этой пары.
Версия выступает в качестве записи пары «код и термин» в конкретный момент времени. Она содержит элементы пары «код и термин», относящиеся к конкретному моменту времени, а также метку времени, идентификатор оператора, внесшего изменения, и описание внесенного изменения. Также в версии записывается статус термина: любое изменение статуса пары «код и термин» приведет к созданию новой версии этой пары. Определенная информация, например, идентификатор оператора, может не быть общедоступной, но тем не менее регистрируется.
Более подробно данные дополнительные элементы информации управления версиями описываются ниже.
Кодированное понятие может рассматриваться в качестве контейнера всех переводов (т. е. пар «код и термин») заданного понятия: следовательно, оно не требует собственной информации о версии. Добавление нового перевода (т. е. новой пары «код и термин») не влечет таким образом создания новой версии кодированного понятия.
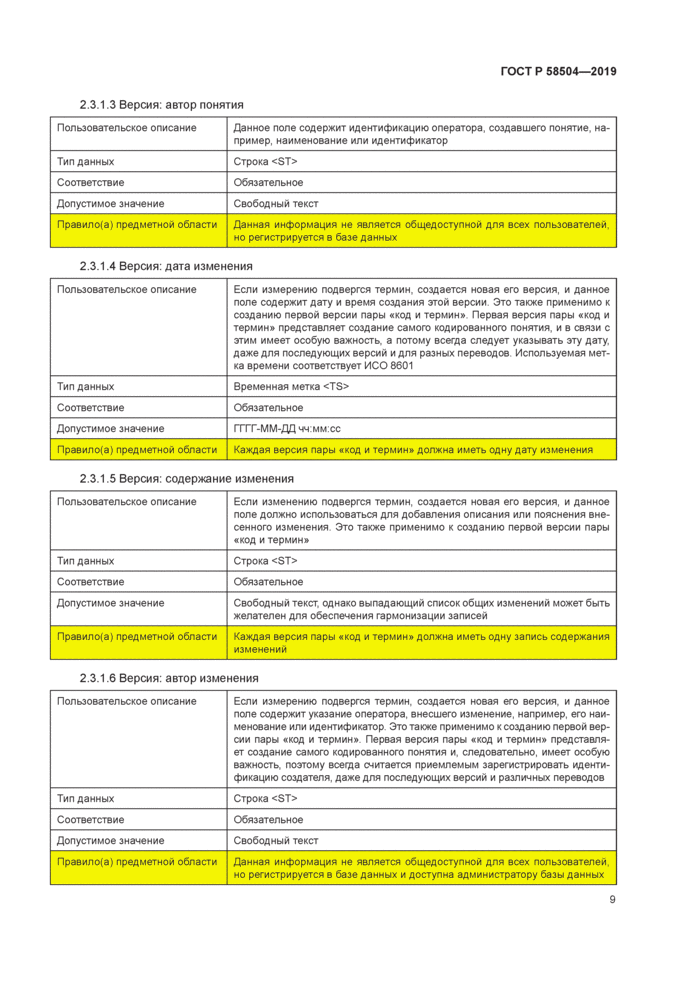
2.3.1.1 Версия: код
|
Пользовательское описание |
Это поле содержит уникальный, машиночитаемый идентификатор для пары «код и термин* подлежащей изменению версии В настоящем стандарте используется следующий формат кода - XXX-12345678-Ll-RR-V где XXX-12345678-LL-RR представляет пару «код и термин»; V представляет номер версии, длина которого не ограничена одной цифрой |
|
Тип данных |
Строка <ST> |
|
Соответствие |
Обязательное |
|
Допустимое значение |
Код генерируется автоматически из пары «код и термин» и номера версии |
|
Правило(а) предметной области |
Каждая версия должна иметь один код |
|
2.3.1.2 Версия: дата создания | ||||||||||
|
|
2.3.1.3 Версия: автор понятия | ||||||||||
|
|
2.3.1.4 Версия: дата изменения | ||||||||||
|
|
2.3.1.5 Версия: содержание изменения | ||||||||||
|
|
2.3.1.6 Версия: автор изменения | ||||||||||
|
|
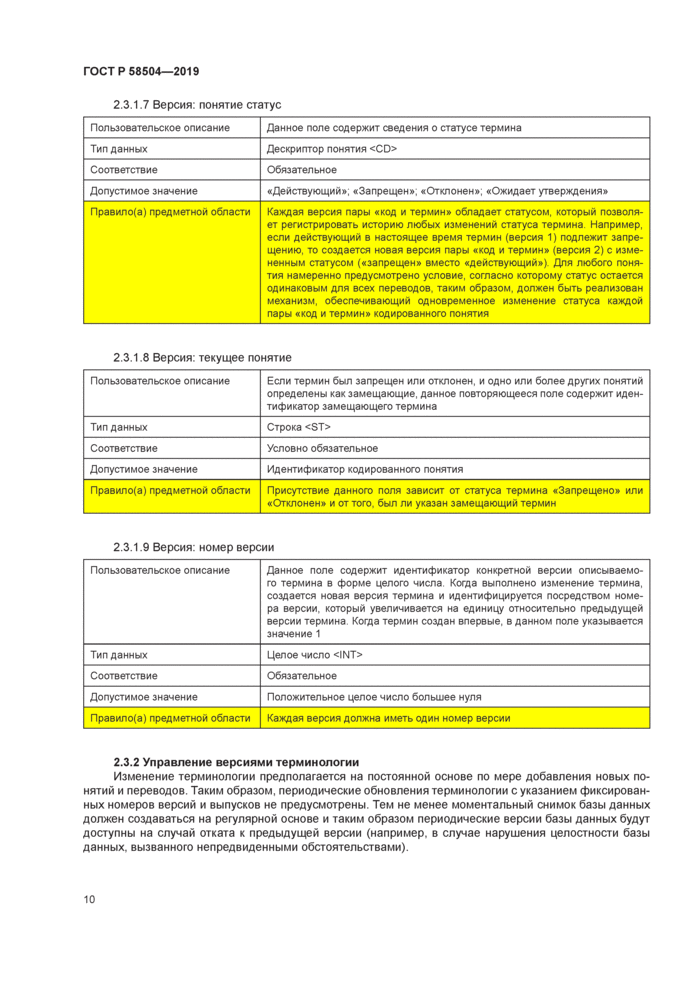
2.3.1.7 Версия: понятие статус | ||||||||||
|
|
2.3.1.8 Версия: текущее понятие | ||||||||||
|
|
2.3.1.9 Версия: номер версии | ||||||||||
|
2.3.2 Управление версиями терминологии
Изменение терминологии предполагается на постоянной основе по мере добавления новых понятий и переводов. Таким образом, периодические обновления терминологии с указанием фиксированных номеров версий и выпусков не предусмотрены. Тем не менее моментальный снимок базы данных должен создаваться на регулярной основе и таким образом периодические версии базы данных будут доступны на случай отката к предыдущей версии (например, в случае нарушения целостности базы данных, вызванного непредвиденными обстоятельствами).
3 Терминологии
3.1 Общие сведения
В целях предоставления информации, необходимой для описания любого отдельного понятия, каждая совокупность терминологий, описываемая в настоящем разделе, использует типы данных, описанные в разделе 2.
Следующие подразделы описывают каждую совокупность терминологий и иллюстрируют их примерами. Все приведенные термины и определения используются только для иллюстрации и не предназначены для отображения точных терминов и определений, составляющих терминологии как таковые.
В разделе 3 каждый элемент описан в отдельном подразделе, состоящем из имени и таблицы, содержащей:
- «Пользовательское описание», описание элемента:
- «Тип данных», описание типа данных;
- «Соответствие», указание, является ли элемент обязательным, необязательным или условно обязательным:
- «Допустимое значение», указывающее возможные значения элемента:
- «Правила предметной области», представляющее техническое руководство для элемента.
3.2 Дозированная лекарственная форма
3.2.1 Обзор дозированной лекарственной формы
Дозированная лекарственная форма является физическим выражением продукта, содержащего активное(ые) и/или вспомогательное(ые) вещество(а). который должен быть применен к пациенту.
Продукт может быть описан на двух различных этапах: этап, на котором он был изготовлен (где он понимается как «произведенный(е) продукт(ы)»), или этап, на котором он был введен пациенту (где он понимается как «лекарственный препарат»). Если произведенный продукт должен подвергнуться какому-либо изменению для преобразования в лекарственный препарат, то дозированная лекарственная форма продукта отличается в зависимости от того, описывает ли она произведенный продукт или лекарственный препарат.
Лекарственное средство таким образом может быть описано двумя «типами» дозированной формы:
- Произведенная дозированная форма (т е. лекарственная дозированная форма произведенного продукта, в том виде, в котором его изготовил производитель):
- Применяемая дозированная форма (т.е. лекарственная дозированная форма лекарственного препарата, готовая к введению пациенту) (см. рисунок 1).
|
Рисунок 1 —Диаграмма, иллюстрирующая для лекарственного средства отношения между произведенным продуктом и произведенной дозированной формой, а также между лекарственным препаратом и применяемой дозированной формой |
Если преобразование не требуется и произведенный продукт совпадает с лекарственным препаратом, произведенная дозированная форма и применяемая дозированная форма идентичны.
Когда описывается лекарственная дозированная форма, специальная ссылка на то. может ли она быть произведенной дозированной формой или применяемой дозированной формой, не дается, тем не менее можно сделать следующий вывод: хотя любая лекарственная дозированная форма может являться произведенной дозированной формой, но только лекарственная дозированная форма, не предполагающая преобразований, может быть применяемой дозированной формой (это свойство может использоваться организацией по ведению терминологии для помощи в определении того, может ли термин относиться только к произведенной дозированной форме, либо к произведенной дозированной форме или применяемой дозированной форме). Цепь использования данных терминов заключается в упрощении используемого языка:
- «Произведенная дозированная форма» = «лекарственная дозированная форма произведенного продукта»;
- «Применяемая лекарственная форма» = «лекарственная дозированная форма лекарственного препарата».
3.2.2 Схема лекарственной дозированной формы
3.2.2.1 Обзор схемы
Лекарственная дозированная форма организована в соответствии с базовой дозированной формой, которая в свою очередь организована в соответствии с состоянием ее вещества. Это простая трехуровневая иерархия, при помощи которой лекарственные дозированные формы подразделяются на категории.
Состояние вещества
Базовая дозированная форма
В дополнение к этой иерархии каждая лекарственная дозированная форма обладает определенным количеством характеристик, которые могут быть использованы для индексирования лекарственных дозированных форм. К данным характеристикам относятся: характеристики высвобождения, преобразование, место введения, способ введения, которые позволяют легче идентифицировать лекарственные дозированные формы и легче разными способами группировать связанные лекарственные дозированные формы (см. рисунок 2).
Лекарственная дозированная форма
| |||||||||||||
|
Рисунок 2 — Принципиальная схема лекарственной дозированной формы, представляющая принципиальную иерархию (сплошные стрелки) и характеристики (пунктирные стрелки) | |||||||||||||
Аналогичная схема представлена на рисунке 3 в форме диаграммы классов на универсальном языке моделирования UML с указанием дополнительной информации об атрибуте «значение» каждого класса (во всех случаях имеет тип «кодированноеПонятие») и отношений между классами. Ассоциации показаны в вилочкообразной нотации, поясняемой в перечне условных обозначений на рисунке.
Состояние Вещества
♦значение: кодироеаниоеПоиятие
Условные обозначения
о
0 ко многим (0...п). необязательно
БазоваяДозированнаяФорма
1 ко многим (1...П), обязательно
♦значение: ЮйкроеанноеПонятие
ЛекарствениаяДоэированнаяФорма
О ♦значение: кодированное Понятие о
|
ХарактеристикиВысвобождеиия | |
|
♦значение: кадироеанмоеПонятие | |
|
Преобразование | |
|
♦значение: «одироеаммое Понятие | |
МестоВведения
крдировзнновПонятие
СпособВведения
кодированнооПонятио
Рисунок 3 — Схема лекарственной дозированной формы с указанием ассоциаций в вилочкообразной нотации
Эти ассоциации отражают следующие условия:
- состояние вещества может ассоциироваться с одной или несколькими (т. е., от 0 до многих, необязательно) базовыми дозированными формами; в то же время возможна ситуация, когда с конкретным состоянием вещества не ассоциирована ни одна базовая дозированная форма, что на практике маловероятно, с учетом значительно ограниченного количества состояний вещества;
- каждая лекарственная дозированная форма должна быть ассоциирована с одним состоянием вещества;
- с базовой дозированной формой могут быть ассоциированы одна или несколько (т. е., от 0 до многих, необязательно) лекарственных дозированных форм; в то же время возможна ситуация, когда с конкретной базовой дозированной формой не ассоциирована ни одна лекарственная дозированная форма, что возможно только в том случае, когда создается новое понятие базовой дозированной формы и в терминологии еще нет ассоциированной с ней лекарственной дозированной формы;
- каждая лекарственная дозированная форма должна быть ассоциирована с одной базовой дозированной формой;
• каждая лекарственная дозированная форма должна быть ассоциирована в отношении один ко многим (т. е.. от 1 до многих) с каждым из следующих свойств: характеристики высвобождения, преобразование. место введения и способ введения: если, к примеру, преобразование не требуется, то для выбора должно быть доступно подходящее пустое значение;
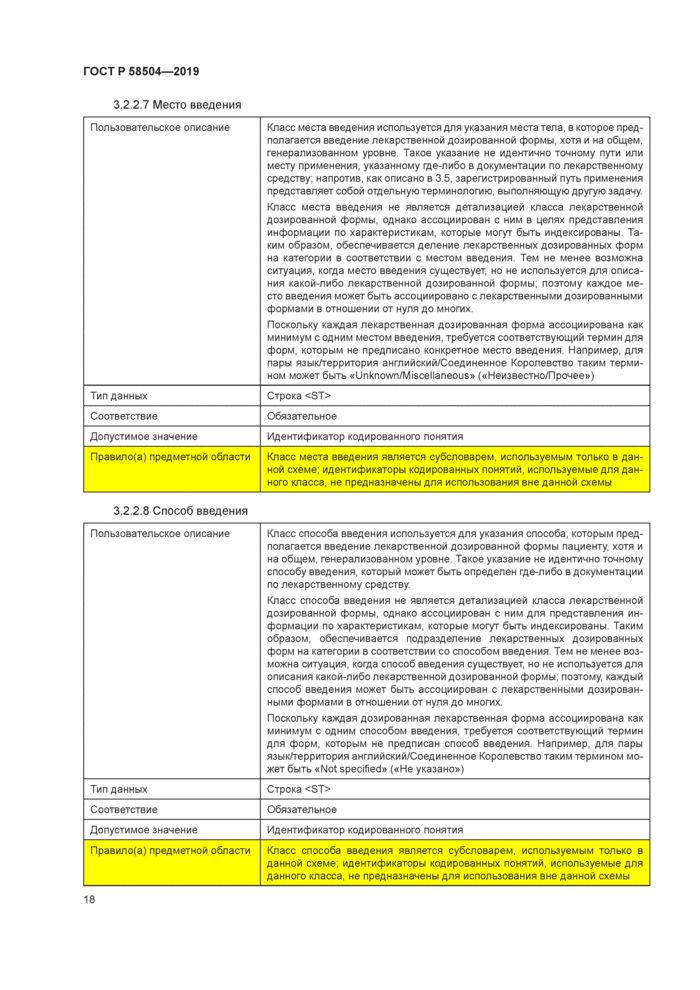
- каждый атрибут (характеристика высвобождения, преобразование, способ введения, место введения) может быть ассоциирован с одной или несколькими (т е., от 0 до многих, необязательно) лекарственными дозированными формами; конкретный атрибут может быть не ассоциирован с дозированной лекарственной формой, например, если он создан впервые до создания какой-либо требующей его лекарственной дозированной формы.
Эти характеристики преимущественно используются для индексирования и не всегда требуют отражения в термине лекарственной дозированной формы, но в некоторых случаях отражаются. Например. раствор, предназначенный для инстилляции в глаза в форме капель может называться «Глазные капли, раствор», термин, в котором будут представлены базовая дозированная форма (раствор), место введения (в глаза, т.е. глазные) и способ введения (инстилляция, т. е. в форме капель). Напротив, раствор, предназначенный для приема перорально путем проглатывания может быть назван «Раствор для приема внутрь», термин, в котором представлены базовая дозированная форма (раствор) и место введения (для приема внутрь), однако способ введения (проглатывание) отсутствует, поскольку это указание представляется необязательным. Эта характеристика все еще используется для описания и индексирования термина, но ее не обязательно указывать как часть термина. В терминах лекарственной дозированной формы будут представлены только те атрибуты, которые будут считаться важными для различения терминов. Информация по основным принципам, управляющим такого рода решениями при создании термина лекарственной дозированной формы (например, правила редактирования) должна быть предоставлена организацией, ведущей терминологию, в форме руководства пользователя.
3.2.2.2 Состояние вещества
|
Пользовательское описание |
Класс состояния вещества является высшим уровнем категории группирования, которая может использоваться для классификации лекарственных дозированных форм, позволяя идентифицировать их в соответствии с тем, являются ли они твердыми, пастообразными, жидкими или газообразными, либо в случаях, когда состояние вещества не определено Например, все твердые дозированные лекарственные формы, например, таблетки, капсулы. гранулы, порошки и т.д., могут классифицироваться совместно в рамках одной категории состояния вещества. Класс состояния вещества является генерализацией класса базовой дозированной формы Каждое состояние вещества может иметь от нуля до многих ассоциированных с ним базовых дозированных форм Причина, по которой состояние вещества может не иметь ассоциированных с ним базовых дозированных форм, заключается в том, что состояние вещества должно быть создано до того, как с ним будет ассоциирована базовая дозированная форма Такая ситуация, как правило, существует только краткое время, поскольку предполагается, что состояние вещества будет определено только при необходимости описания категории предполагаемой новой базовой дозированной формы В силу ограниченности возможных состояний вещества такое возможно только в ходе первоначального заполнения базы данных |
|
Тип данных |
Строка <ST> |
|
Соответствие |
Обязательное |
|
Допустимое значение |
Идентификатор кодированного понятия |
|
Правило(а) предметной области |
Состояние вещества произведенной дозированной формы — состояние вещества произведенного продукта, а не окончательного лекарственного препарата: например, состояние вещества лекарственной дозированной формы «Порошок для приготовления растворов для инъекций» — «твердое», поскольку оно относится к произведенному продукту (порошок), а не к лекарственному препарату (раствор) Класс состояния вещества является субсловарем, используемым только в данной схеме, идентификаторы кодированных понятий, используемые для данного класса, не предназначены для использования вне данной схемы |
|
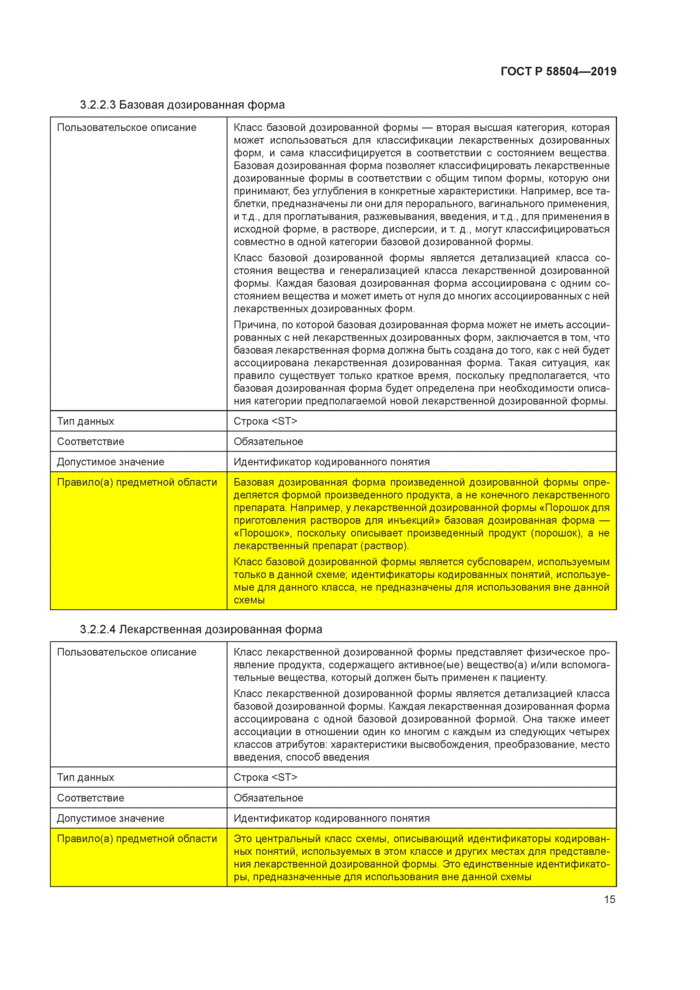
Пользовательское описание |
Класс базовой дозированной формы — вторая высшая категория, которая может использоваться для классификации лекарственных дозированных форм, и сама классифицируется в соответствии с состоянием вещества Базовая дозированная форма позволяет классифицировать лекарственные дозированные формы в соответствии с общим типом формы, которую они принимают, без углубления в конкретные характеристики Например, все таблетки, предназначены ли они для перорального, вагинального применения, и тд., для проглатывания, разжевывания, введения, и тд., для применения в исходной форме, в растворе, дисперсии, и т д . могут классифицироваться совместно в одной категории базовой дозированной формы Класс базовой дозированной формы является детализацией класса состояния вещества и генерализацией класса лекарственной дозированной формы Каждая базовая дозированная форма ассоциирована с одним состоянием вещества и может иметь от нуля до многих ассоциированных с ней лекарственных дозированных форм Причина, по которой базовая дозированная форма может не иметь ассоциированных с ней лекарственных дозированных форм, заключается в том, что базовая лекарственная форма должна быть создана до того, как с ней будет ассоциирована лекарственная дозированная форма Такая ситуация, как правило существует только краткое время, поскольку предполагается, что базовая дозированная форма будет определена при необходимости описания категории предполагаемой новой лекарственной дозированной формы |
|
Тип данных |
Строка <ST> |
|
Соответствие |
Обязательное |
|
Допустимое значение |
Идентификатор кодированного понятия |
|
Правило(а) предметной области |
Базовая дозированная форма произведенной дозированной формы определяется формой произведенного продукта, а не конечного лекарственного препарата Например, у лекарственной дозированной формы «Порошок для приготовления растворов для инъекций» базовая дозированная форма — «Порошок», поскольку описывает произведенный продукт (порошок), а не лекарственный препарат (раствор) Класс базовой дозированной формы является субсловарем, используемым только в данной схеме; идентификаторы кодированных понятий, используемые для данного класса, не предназначены для использования вне данной схемы |
|
3.2.2.4 Лекарственная дозированная форма | ||||||||||
|
Содержание
1 Область применения.................................................................1
2 Организация нормативных терминов....................................................2
2.1 Общие сведения.................................................................2
2.2 Пара «код и термин» и кодированное понятие.........................................2
2.3 Управление версиями.............................................................8
3 Терминологии......................................................................11
3.1 Общие сведения................................................................11
3.2 Дозированная лекарственная форма...............................................11
3.3 Комбинированная лекарственная форма............................................24
3.4 Единица представления..........................................................28
3.5 Путь Введения..................................................................30
3.6 Упаковка.......................................................................32
4 Отображение территориальных терминов...............................................38
4.1 Различия в деталях территориальных терминологий..................................38
4.2 Организация территориальных терминов в базе данных...............................40
Библиография.......................................................................46
|
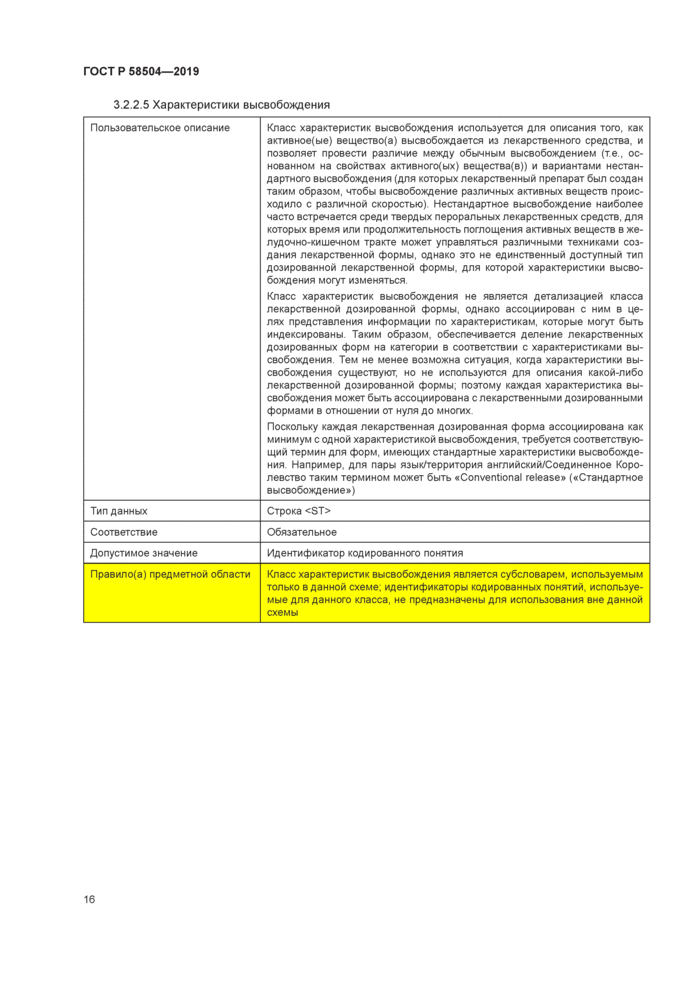
Пользовательское описание |
Класс характеристик высвобождения используется для описания того, как активное(ые) вещество(а) высвобождается из лекарственного средства, и позволяет провести различие между обычным высвобождением (т.е. основанном на свойствах активного{ых) вещества(в)) и вариантами нестандартного высвобождения (для которых лекарственный препарат был создан таким образом, чтобы высвобождение различных активных веществ происходило с различной скоростью) Нестандартное высвобождение наиболее часто встречается среди твердых пероральных лекарственных средств, для которых время или продолжительность поглощения активных веществ в желудочно-кишечном тракте может управляться различными техниками создания лекарственной формы, однако это не единственный доступный тип дозированной лекарственной формы, для которой характеристики высвобождения могут изменяться Класс характеристик высвобождения не является детализацией класса лекарственной дозированной формы, однако ассоциирован с ним в целях представления информации по характеристикам, которые могут быть индексированы Таким образом, обеспечивается деление лекарственных дозированных форм на категории в соответствии с характеристиками высвобождения. Тем не менее возможна ситуация, когда характеристики высвобождения существуют, но не используются для описания какой-либо лекарственной дозированной формы, поэтому каждая характеристика высвобождения может быть ассоциирована с лекарственными дозированными формами в отношении от нуля до многих Поскольку каждая лекарственная дозированная форма ассоциирована как минимум с одной характеристикой высвобождения, требуется соответствующий термин для форм, имеющих стандартные характеристики высвобождения Например, для пары язык/территория английский/Соединенное Королевство таким термином может быть «Conventional release» («Стандартное высвобождение») |
|
Тип данных |
Строка <ST> |
|
Соответствие |
Обязательное |
|
Допустимое значение |
Идентификатор кодированного понятия |
|
Правило(а) предметной области |
Класс характеристик высвобождения является субсловарем, используемым только в данной схеме, идентификаторы кодированных понятий, используемые для данного класса, не предназначены для использования вне данной схемы |
Предисловие к ИСО/ТС 20440
Международная организация по стандартизации (ИСО) — Всемирная федерация национальных органов по стандартизации (комитеты — члены ИСО). Работа по подготовке международных стандартов обычно ведется через технические комитеты ИСО. Каждый комитет — член ИСО. проявляющий интерес к тематике, по которой учрежден технический комитет, имеет право быть представленным в этом комитете. Международные организации, государственные и негосударственные, имеющие связи с ИСО. также принимают участие в работе. ИСО тесно сотрудничает с Международной электротехнической комиссией (МЭК) по всем вопросам стандартизации в области электротехники.
Процедуры, используемые для разработки данного документа, и процедуры, предусмотренные для его дальнейшего ведения, описаны в Директивах ИСО/МЭК, Часть 1. В частности, следует отметить различные критерии утверждения, требуемые для различных типов документов ИСО. Проект данного документа был разработан в соответствии с редакционными правилами Директив ИСО/МЭК. Часть 2: www.iso.org/directives.
Необходимо обратить внимание на возможность того, что ряд элементов данного документа могут быть предметом патентных прав. Международная организация ИСО не должна нести ответственность за идентификацию таких прав, частично или полностью. Сведения о патентных правах, идентифицированных при разработке документа, будут указаны во Введении и/или в перечне полученных ИСО объявлениях о патентном праве: www.iso.org/patents.
Любое торговое название, использованное в данном документе, является информацией, предоставляемой для удобства пользователей, а не свидетельством в пользу того или иного товара или той или иной компании.
Для пояснения значений конкретных терминов и выражений ИСО. относящихся к оценке соответствия. а также информация о соблюдении Международной организацией ИСО принципов ВТО по техническим барьерам в торговле (ТБТ). см. следующий унифицированный локатор ресурса (URL): Foreword — Supplementary information.
За данный документ несет ответственность Технический комитет. ИСО/ТК 215, Информатизация здоровья.
Введение
Терминологии, описываемые в стандарте ЕН/ИС011239:2012 (далее —ИС011239) и в настоящем стандарте, являются необходимыми для соблюдения требований серии стандартов IDMP (Identification of medicinal products — идентификация лекарственных средств) в целом.
На каждой территории традиционно применяются собственная терминология для описания понятий. определенных в ИСО 11239; эти терминологии не согласованы с используемыми в других регионах. Поэтому необходима разработка гармонизированных нормативных терминологий, с помощью которых все регионы могли бы одинаково ссылаться на конкретное понятие. Цель настоящего стандарта — описать способ построения нормативных словарей и продемонстрировать их использование для внедрения ИСО 11239.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ
ИНФОРМАТИЗАЦИЯ ЗДОРОВЬЯ
Идентификация лекарственных средств.
Руководство по внедрению элементов данных и структуры ISO 11239 для уникальной идентификации и обмена регистрируемой информацией о дозированных лекарственных формах, единицах представления, путях введения и упаковке
Health informatics Identification of medicinal products Implementation guide for ISO 11239 data elements and structures for the unique identification and exchange of regulated information on pharmaceutical dose forms, units of presentation, routes of administration and packaging
Дата введения — 2020—05—01
1 Область применения
Настоящий стандарт описывает элементы данных и структуры для уникальной идентификации и обмена регистрируемой информацией о дозированных лекарственных формах, единицах представления. путях введения и упаковке.
На основании принципов, изложенных в настоящем стандарте, гармонизированные нормативные терминологии будут разрабатываться в соответствии с утверхщенным процессом ведения, позволяющим пользователям сверяться с терминологиями и находить надлежащие термины для понятий, которые им требуется описать. Для облегчения идентификации подходящих терминов будут описаны также условия отображения существующих региональных терминологий на гармонизированные нормативные терминологии. Предусмотренные для терминов коды могут в дальнейшем использоваться в соответствующих полях таких объектов, как PhPID (идентификатор лекарственного препарата). PCID (идентификатор упаковки лекарственного средства). MPID (идентификатор лекарственного средства), чтобы идентифицировать эти понятия.
Настоящий стандарт предназначен для использования:
- любой организацией, которая может быть ответственной за разработку и ведение нормативных словарей;
- любыми региональными уполномоченными органами или изготовителями программного обеспечения. предполагающими использовать нормативные словари в своих системах и понять принцип их создания;
- владельцами баз данных, которым требуется сопоставить свои термины с основным перечнем нормативных словарей:
- другими пользователями, желающими понять иерархию нормативных словарей в целях поиска наиболее подходящего термина, описывающего конкретное понятие.
Терминология, подлежащая применению в контексте настоящего стандарта и обозначенная в ИСО 11239, находится в разработке. Все коды, термины, определения, используемые в качестве примеров в настоящем стандарте, представлены только для иллюстрации и не предназначены для использования в качестве окончательной терминологии.
Издание официальное
2 Организация нормативных терминов
2.1 Общие сведения
Настоящий раздел описывает организацию каждого термина, указывая типы данных, используемые для передачи информации, и требования к управлению версиями в целях отслеживания их создания и эволюции. В разделе 3 описываются различные типы терминологий и субсловарей, использующих эти типы данных, а также релевантные отношения между ними.
В разделе 2 для каждого поля выделен отдельный подраздел, состоящий из имени поля и таблицы. содержащей:
- «Пользовательское описание», описание поля;
- «Тип данных», описание типа данных;
- «Соответствие», указание, является ли поле обязательным, не обязательным или условно обязательным;
- «Допустимое значение», указывающее возможные значения поля;
- «Правила предметной области», представляющее техническое руководство для поля.
2.2 Пара «код и термин» и кодированное понятие
2.2.1 Общие положения
Пара код и термин и кодированное понятие являются типами данных, используемыми для представления информации, требуемой для описания каждого термина в каждой терминологии или субсловаре с любым сочетанием язык/территория.
2.2.2 Пара код и термин
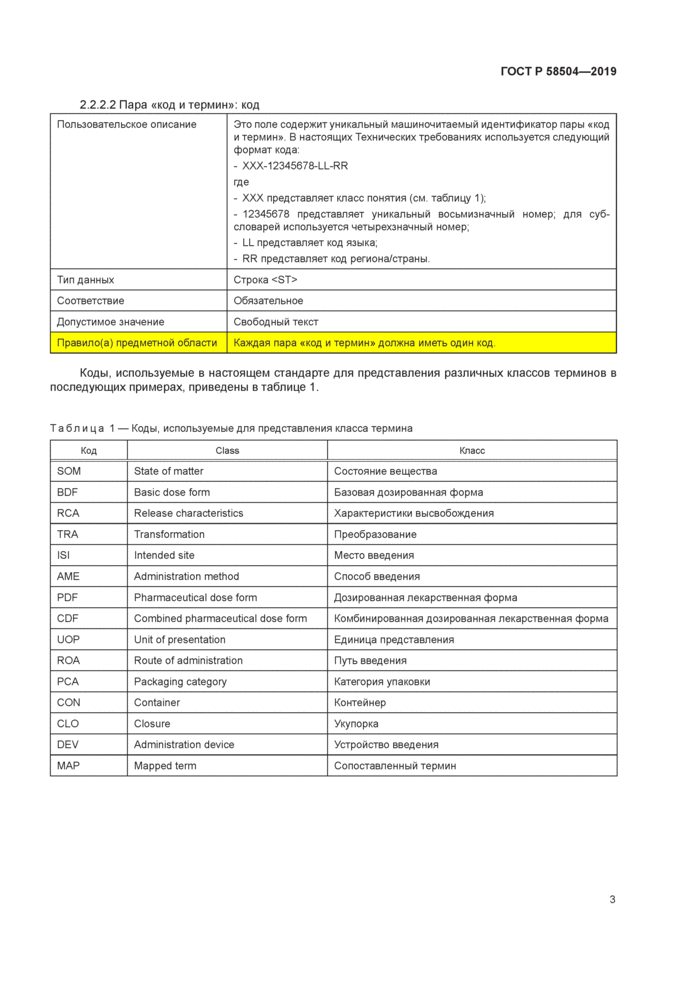
2.2.2.1 Обзор пары код и термин
Это базовый класс каждого термина, используемый для описания и определения термина на конкретном языке и для конкретной территории. Он содержит ключевые атрибуты каждого понятия, в том числе идентификатор, текстовое представление термина (например, собственно нормативный термин), определение, необязательный домен, указывающий, используется ли термин только в ветеринарии. дополнительный текстовый комментарий, а также коды языка и территории.
Каждый нормативный термин или подтермин имеет уникальную пару «код и термин» для каждого сочетания язык/территория. Сочетание языка и территории позволяет указать вариант конкретного языка. используемый на определенной географической территории; например, если написание термина или определения различается в британском и американском английском, такое отличие может быть отображено. Если термины и определения уже существуют в конкретном языке конкретной территории и этот же язык используется на другой территории, решение о том. надо ли создавать отдельные термины и определения для другой территории или следует использовать термины и определения первой территории, оставляется на усмотрение территории.
Если требуется новое понятие, то должны быть созданы новое кодированное понятие и как минимум одна пара «код и термин» необходимая для хранения данных, описывающих понятие. Сочетание язык/территория. выбранное для представления «значения», описывающего понятие, должно всегда создаваться первым, даже если запрос на новый термин исходит из места, где используется другое сочетание язык/территория. Организация, ответственная за ведение терминологии, должна предоставить инструкции по запросу нового термина или пересмотру уже существующего.
|
Пользовательское описание |
Это поле содержит уникальный машиночитаемый идентификатор пары «код и термин» В настоящих Технических требованиях используется следующий формат кода - XXX-12345678-Ll-RR где - XXX представляет класс понятия (см таблицу 1); - 12345678 представляет уникальный восьмизначный номер: для субсловарей используется четырехзначный номер, - LL представляет код языка, - RR представляет код региона/страны |
|
Тип данных |
Строка <ST> |
|
Соответствие |
Обязательное |
|
Допустимое значение |
Свободный текст |
|
Правило(а) предметной области |
Каждая пара «код и термин» должна иметь один код |
Коды, используемые в настоящем стандарте для представления различных классов терминов в последующих примерах, приведены в таблице 1.
|
Таблица 1 — Коды, используемые для представления класса термина | ||||||||||||||||||||||||||||||||||||||||||||||||
|
|
Пользовательское описание |
Это поле содержит текстовое описание термина для пары «код и термин» |
|
Тип данных |
Строка <ST> |
|
Соответствие |
Обязательное |
|
Допустимое значение |
Свободный текст |
|
Правило(а) предметной области |
Каждая пара «код и термин» должна иметь один термин |
|
2.2.2 4 Пара «код и термин»: определение | ||||||||||
|
|
2.2.2.5 Пара «код и термин»: домен | ||||||||||
|
|
Пользовательское описание |
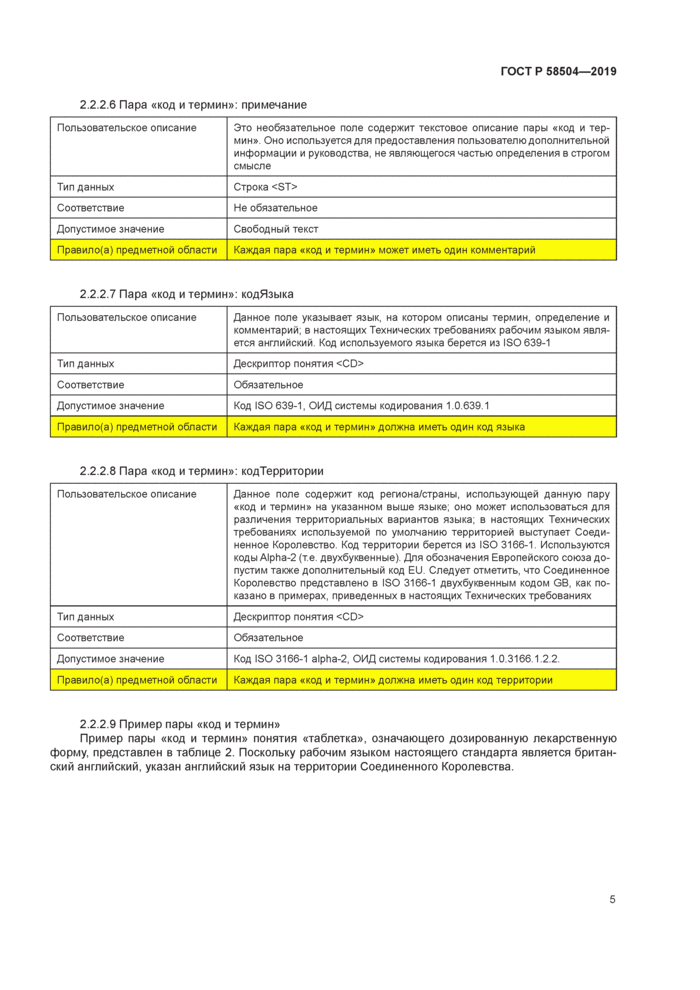
Это необязательное поле содержит текстовое описание пары «код и термин» Оно используется для предоставления пользователю дополнительной информации и руководства, не являющегося частью определения в строгом смысле |
|
Тип данных |
Строка <ST> |
|
Соответствие |
Не обязательное |
|
Допустимое значение |
Свободный текст |
|
Правило(а) предметной области |
Каждая пара «код и термин» может иметь один комментарий |
|
2.2.2 7 Пара «код и термин»: кодЯзыка | ||||||||||
|
|
2.2.2 8 Пара «код и термин»: кодТерритории | ||||||||||
|
2.2.2 9 Пример пары «код и термин»
Пример пары «код и термин» понятия «таблетка», означающего дозированную лекарственную форму, представлен в таблице 2. Поскольку рабочим языком настоящего стандарта является британский английский, указан английский язык на территории Соединенного Королевства.