ГОСТ Р 54655-2011
Мед натуральный. Метод определения антибиотиков
Купить ГОСТ Р 54655-2011 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на натуральный мед и устанавливает метод определения остаточных количеств антибиотиков тетрациклиновой группы и левомицетина (хлорамфеникола), на основе твердофазного иммуноферментного анализа. Пределы обнаружения составляют: - для тетрациклина, ролитетрациклина - 6 мкг/кг; - левомицетина - 0,025 мкг/кг.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Требования безопасности
5 Отбор и подготовка проб ы меда
6 Определение присутствия и массовой доли антибиотиков тетрациклиновой группы
7 Определение присутствия и массовой доли левомицетина (хлорамфеникола, ХАФ)
| Дата введения | 01.01.2013 |
|---|---|
| Добавлен в базу | 01.09.2013 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 13.12.2011 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 804-ст |
|---|---|---|---|
| Разработан | ГНУ НИИ пчеловодства Россельхозакадемии | ||
| Разработан | ООО Аналитический центр Апис | ||
| Издан | Стандартинформ | 2012 г. |
Honey natural. Method for the determination of antibiotics
- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
- ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ Р ИСО 5725-1-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
- ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
- ГОСТ Р 51568-99 Сита лабораторные из металлической проволочной сетки. Технические условия
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
- ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 19881-74 Анализаторы потенциометрические для контроля рН молока и молочных продуктов. Общие технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 3145-84 Часы механические с сигнальным устройством. Общие технические условия
- ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
- ГОСТ 19792-2001 Мед натуральный. Технические условия
- ГОСТ Р 52501-2005 Вода для лабораторного анализа. Технические условия
- ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
- ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7
стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ТЕХНИЧЕСКОМУ РЕГУЛИРОВАНИЮ И МЕТРОЛОГИИ
ГОСТР
54655-
2011
НАЦИОНАЛЬНЫЙ
СТАНДАРТ
РОССИЙСКОЙ
ФЕДЕРАЦИИ
МЕД НАТУРАЛЬНЫЙМетод определения антибиотиков
Издание официальное
Москва
Стандартинформ
2012
Предисловие
Цели и принципы стандартизации в Российской Федерации установлены Федеральным законом от 27 декабря 2002 г. № 184-ФЗ «О техническом регулировании», а правила применения национальных стандартов Российской Федерации — ГОСТ Р 1.0-2004 «Стандартизация Российской Федерации. Основные положения»
Сведения о стандарте
1 РАЗРАБОТАН Государственным научным учреждением Научно-исследовательским институтом пчеловодства Российской академии сельскохозяйственных наук (ГНУ НИИ пчеловодства Россель-хозакадемии) и Обществом с ограниченной ответственностью «Аналитический центр Апис»
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 432 «Пчеловодство»
3 УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Приказом Федерального агентства по техническому регулированию и метрологии от 13 декабря 2011 г. № 804-ст
4 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодно издаваемом информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячно издаваемых информационных указателях «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячно издаваемом информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
© Стандартинформ, 2012
Настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ Р 54655-2011
7.3.1.2 Комплект стандартных водных растворов ХАФ со следующими массовыми концентрациями 0 (нулевой стандарт); 0,025; 0,050; 0,100; 0,250; 0,750 нг/см3 по 1,3 см3 — 6 флаконов.
7.3.1.3 Конъюгат ХАФ с пероксидазой (концентрат) — 0,7 см3.
7.3.1.4 Субстрат/хромогеновый раствор (розового цвета) — 10,0 см3.
7.3.1.5 Стоп-реагент, содержащий 1 Н серную кислоту, — 14,0 см3.
7.3.1.6 Буфер для разбавления конъюгата и растворения образцов — 100,0 см3.
7.3.1.7 Моющий буфер (соли) для приготовления 10 мМ фосфатного буфера (7,4 ед. pH), содержащего 0,05 % твина 20.
Примечание — Набор рассчитан на проведение 48 определений в двух повторностях, включая анализируемые пробы и калибровочные растворы (всего 96 определений на один планшет).
7.3.2 Аналитические характеристики набора1*
7.3.2.1 Чувствительность метода
Предел обнаружения ХАФ в меде — 0,025 мкг/кг.
Предел количественного определения — 0,075 мкг/кг.
Показатель извлекаемости ХАФ из меда — более 80 %.
Перекрестная чувствительность:
-ХАФ —100%;
- ХАФ основной — 12 %;
- тиамфеникол — менее 0,1 %.
7.3.3 Рекомендации по использованию наборов
7.3.3.1 При проведении определений используют реагенты и компоненты, входящие в один и тот же набор. Разбавление или замена реагентов, использование реагентов из набора с другим номером партии могут привести к потере чувствительности или ошибке определения.
7.3.3.2 Необходимо хранить наборы при температуре 2 °С—8 °С в холодильных приборах по ГОСТ 16317. Не допускаются хранение наборов при отрицательной температуре и замораживание реагентов набора.
Для хранения неиспользованных стрипов (лунок) их герметично упаковывают в оригинальный фольгированный пакет вместе с имеющимся осушителем.
7.3.3.3 Необходимо избегать попадания прямых солнечных лучей на флакон с раствором хромогена из-за его светочувствительности.
7.3.3.4 При появлении голубоватого окрашивания розоватого раствора субстрата/хромогена его не применяют, поскольку это признак порчи раствора.
7.3.4 Требования техники безопасности при проведении испытаний
7.3.4.1 Стандартные растворы содержат ХАФ, поэтому требуется особая осторожность.
7.3.4.2 Стоп-реагент содержит в своем составе серную кислоту, поэтому следует избегать контакта стоп-реагента с кожей.
7.4 Проведение определений с применением набора
7.4.1 Отбор и подготовка проб меда — по разделу 5.
7.4.2 Приготовление концентрированного фосфатного моющего буфера
В мерную колбу вместимостью 100 см3 количественно переносят содержимое пакета с буферным составом из набора 7.3.1.7. Для растворения солей используют воду для лабораторного анализа по 6.2.20. Раствор доводят до метки водой и тщательно перемешивают.
Срок хранения концентрированного буферного раствора при комнатной температуре 20 °С—25 °С — 12 недель или при температуре 6 °С—10 °С — не более одного года.
7.4.3 Приготовление рабочего моющего буферного раствора молярной концентрацией 10 ммоль/дм3
Перед анализом в цилиндре смешивают концентрированный фосфатный моющий буфер по 7.4.2 и воду для лабораторного анализа в соотношении 1:9.
Срок хранения рабочего моющего буферного раствора при температуре 2 °С—8 °С — не более 6 недель.
11 Отработка метрологических характеристик метода проводилась с применением наборов «Ридаскрин Хло-рамфеникол». Данная информация приводится для удобства пользователей настоящего стандарта и не содержит требований применять данный набор.
9
7.4.4 Приготовление пробы меда
Взвешивают (2,00 ± 0,002) г меда, подготовленного по разделу 5, в центрифужной пробирке вместимостью 15 см3 по 7.2.4, добавляют 4 см3 воды для лабораторного анализа. Раствор интенсивно перемешивают на шейкере по 6.2.7 до полного растворения меда.
В пробирку добавляют 4 см3этилацетата по 7.2.6, плотно завинчивают крышку и интенсивно встряхивают в течение 10 мин вверх-вниз (или ставят в ультразвуковую ванну).
Пробирку помещают в центрифугу по 6.2.9 для разделения водного и органического слоев. Условия центрифугирования: 10 мин при 3000 д и температуре 20 °С—25 °С.
Дозатором по 6.2.2 отбирают 1 см3 этилацетатного слоя (что соответствует 0,5 г меда) в чистую круглодонную колбу по 7.2.3 (или виалу по 6.2.2). Органический растворитель удаляют с использованием роторного испарителя или высушиванием в токе азота при температуре 60 °С с использованием микроиспарителя по 7.2.1.
Сухой остаток растворяют в 0,5 см3 буфера по 7.3.1.6 (из набора) на шейкере (10 мин) и в ультразвуковой ванне (30 мин).
7.4.5 Приготовление реагентов для анализа
Перед применением набора доводят температуру всех реагентов до комнатной в пределах 20 °С—25 °С, а после использования охлаждают все оставшиеся реагенты до 2 °С—8 °С.
В процессе выполнения анализа нельзя допускать высыхания лунок планшета. На всех стадиях определения следует избегать воздействия прямого солнечного света.
Растворы стандартов ХАФ, субстрата/хромогена, стоп-реагента, входящие в состав набора, поставляются в готовом к употреблению виде. Перед употреблением достаточно вскрыть флакон.
7.4.6 Приготовление раствора конъюгата
Конъюгат ХАФ с ферментом — концентрат. Так как этот раствор ограниченно стабилен, перед анализом разбавляют только требуемое количество.
Флакон с концентратом аккуратно встряхивают, в одноразовую стеклянную виалу вместимостью 1,5 см3 дозатором отбирают конъюгат и буфер по 7.3.1.6 (из набора) в соотношении 1:10. Раствор тщательно перемешивают.
На 4 стрипа по 8 лунок достаточно смешать 0,2 см3 концентрата и 2 см3 буфера по 7.3.1.6.
7.4.7 Подготовка микротитровального планшета
Перед выполнением анализа из планшета необходимо извлечь необходимое количество стрипов. Оставшиеся стрипы следует тщательно упаковать в фольгированный пакет вместе с осушителем, герметично закрыть пакет и поместить на хранение при температуре 2 °С—8 °С.
7.4.8 Порядок проведения анализа
7.4.8.1 В рамку планшета вставляют стрипы (лунки) в количестве, необходимом для выполнения всех запланированных определений (стандартные растворы и образцы) в двух повторностях. Записывают координаты лунок, предназначенных для стандартных растворов и подготовленных исследуемых растворов. Пример формы записи координат лунок представлен на рисунке 2.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Рисунок 2 — Пример формы записи координат лунок (С — стандартные растворы, П — анализируемые пробы) |
7.4.8.2 Одноканальным дозатором по 6.2.2 добавляют по 0,050 см3 стандартных и анализируемых растворов в соответствующие пары лунок.
ГОСТ Р 54655-2011
7.4.8.3 Восьмиканальным дозатором по 6.2.3 на дно каждой лунки добавляют по 0,050 см3 разбавленного раствора конъюгата по 7.4.6. Осторожно перемешивают раствор в лунках вручную легкими круговыми движениями рамки планшета по поверхности стола. Ставят в темное место на инкубацию в течение 1 ч при комнатной температуре 20 °С— 25 °С.
7.4.8.4 Резко переворачивают планшет и выливают жидкость из лунок, выбивают капли жидкости, оставшиеся в лунках, путем энергичного трехкратного постукивания рамки с лунками по столу, покрытому фильтровальной бумагой по 6.2.23. Каждую лунку заполняют 0,250 см3 рабочего раствора моющего буфера по 7.4.3 и вновь удаляют раствор из лунок. Выбивают капли жидкости, как описано выше. Повторяют процедуру промывки лунок моющим буфером еще два раза.
7.4.8.5 Восьмиканальным дозатором добавляют в каждую лунку по 0,100 см3 раствора субстра-та/хромогена. Тщательно перемешивают растворы в лунках вручную. Ставят в темное место на инкубацию в течение 15 мин при температуре 20 °С—25 °С.
7.4.8.6 Восьмиканальным дозатором в каждую лунку добавляют по 0,100 см3 стоп-реагента и тщательно перемешивают растворы в лунках вручную. Планшет помещают в микропланшетный фотометр, измеряют оптическую плотность в каждой лунке при 450 нм. Измерения проводят в течение 30 мин после добавления стоп-реагента.
Примечание — При расчете массовой доли левомицитина в анализируемых пробах учитывают фоновый сигнал с помощью постановки холостого опыта. Для этого в каждой серии анализов ставят контрольную пробу без меда, то есть испаряют чистый этилацетат и затем следуют описанной стандартной процедуре. Измененный фоновый сигнал вычитают на стадии обработки результатов.
7.5 Обработка результатов анализа
Построение градуировочной кривой проводят для каждой серии определений.
7.5.1 Для обработки результатов измерений на компьютере используют программное обеспечение RIDASOFT Win. Окончательный результат выражают в нанограммах на килограмм.
7.5.2 Обработка результатов без использования компьютера
Среднее из двух параллельных значений оптической плотности, измеренной в лунках со стандартными или анализируемыми растворами, делят на среднее значение оптической плотности, измеренной в лунках с нулевым стандартом (С1), результат умножают на 100.
|
Примечание — Если величина оптической плотности, измеренной в лунке с нулевым стандартом, меньше 0,6, то это может быть признаком порчи реагентов. В этом случае заменяют реагенты и повторяют определение. Среднее значение оптической плотности нулевого стандарта |
Относительное поглощение или процент поглощения вычисляют по формуле
(5)
По величинам относительного поглощения, вычисленным для стандартных растворов, и соответствующим известным значениям концентрации ХАФ в нанограммах на килограмм строят градуировочную кривую в полулогарифмической системе координат.
Массовую долю ХАФ в анализируемой пробе меда в нанограммах на килограмм определяют по градуировочной кривой в соответствии с относительным поглощением, измеренным и вычисленным для каждого раствора.
Для определения массовой доли ХАФ в анализируемой пробе меда в микрограммах на килограмм величину концентрации ХАФ, полученную по градуировочной кривой, умножают на 1 (коэффициент разбавления при выполнении анализа в точном соответствии с приведенной методикой) и делят на тысячу (для перевода в микрограммы на килограмм).
Вычисления проводят с записью результата до второго десятичного знака.
Окончательный результат записывают с точностью до первого десятичного знака.
(6)
За окончательный результат определения принимают среднеарифметическое значение результатов двух параллельных определений, если выполняется условие приемлемости
1^хаф, 1 — ^хаф, 2I - г> г ~ 2.8 -аг • 0,01 • Мхдф
11
где Мхдф f и Мхдф 2 — значения результатов параллельных определений остаточных количеств хпо-рамфеникола;
г— предел повторяемости для двух результатов параллельных определений при доверительной вероятности Р = 0,95 (таблица 5); ог— показатель повторяемости (относительное среднеквадратическое отклонение повторяе-_ мости) при доверительной вероятности Р - 0,95;
Мхаф — среднеарифметическое значение результатов двух параллельных определений остаточных количеств хпорамфеникола.
7.6 Точность метода
Статистический анализ результатов испытаний по оценке точности метода проводят в соответствии с требованиями ГОСТ Р ИСО 5725-6. Диапазон измерений массовой доли левомицетина (хло-рамфеникола), для которого рассчитаны метрологические характеристики, составляет 0,075—0,750 мкг/кг.
7.6.1 Повторяемость результатов
Абсолютное расхождение между результатами двух определений МхАф 1 и МхАф 2, которые получены в условиях повторяемости (одна и та же методика, идентичный объект испытания, одна и та же лаборатория, один и тот же оператор, одно и то же оборудование, короткий промежуток времени), не должно превышать предела повторяемости г= 2,8 стг -0,01 • МХАФ. Значения г и ог представлены в таблицах 4 и 5.
|
Таблица 4 — Значения характеристик погрешности и ее составляющих при доверительной вероятности Р = 0,95 | ||||||
|
|
Таблица 5 — Значения пределов повторяемости и воспроизводимости при доверительной вероятности Р = 0,95 | ||||
|
7.6.2 Воспроизводимость результатов _ _
Абсолютное расхождение между результатами двух независимых измерений Мхдф 1 и Л4ХДФ 2, которые получены в условиях воспроизводимости (одна и та же методика, идентичный объект испытания, разные лаборатории, разные операторы, различное оборудование), не должно превышать предела воспроизводимости
1^хаф,1 ^ХАФ.г! — ^ 2,8 'Од '0,01 • Л4ХАФ, (7)
где aR— показатель воспроизводимости (относительное среднеквадратическое отклонение воспроиз-_ водимости) при доверительной вероятности Р = 0,95;
Мхаф — среднеарифметическое значение результатов определений остаточных количеств хлорамфе-никола, полученных в условиях воспроизводимости.
Значения Rhor представлены в таблицах 4 и 5.
7.6.3 При соблюдении всех регламентируемых методикой условий с доверительной вероятностью Р = 0,95 не должны превышать значений, приведенных в таблицах 4 и 5.
7.6.4 Форма представления результата
Результат измерения в документах, предусматривающих его использование, представляют в виде
(.Мср + А), мкг/кг, Р = 0,95, (8)
где Мср — среднеарифметическое значение результатов двух параллельных определений остаточных количеств ХАФ, полученных в условиях повторяемости;
+ А — границы характеристик абсолютной погрешности результатов определения массовой доли ХАФ, мкг/кг;
+ А = +5 /Иср/100, значение относительной погрешности +5 представлено в таблице 4.
13
УДК 638.16:006.354 ОКС 67.180.10 С52 ОКСТУ 9101
Ключевые слова: натуральный мед, твердофазный иммуноферментный анализ (ИФА), антибиотики тетрациклиновой группы, левомицетин (хлорамфеникол), точность метода
Редактор М.Е. Никулина Технический редактор В.Н. Прусакова Корректор Р.А. Ментова Компьютерная верстка В.И. Гоищенко
Сдано в набор 03.09.2012. Подписано в печать 27.09.2012. Формат 60x84V8. Гарнитура Ариал. Уел. печ. л. 1,86.
Уч.-изд. л. 1,55. Тираж 221 экз. Зак. 847.
ФГУП «СТАНДАРТИНФОРМ», 123995 Москва, Гранатный пер., 4. www.gostinfo.ru info@gostinfo.ru Набрано во ФГУП «СТАНДАРТИНФОРМ» на ПЭВМ.
Отпечатано в филиале ФГУП «СТАНДАРТИНФОРМ» — тип. «Московский печатник», 105062 Москва, Лялин пер., 6.
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИМЕД НАТУРАЛЬНЫЙ Метод определения антибиотиков
Natural honey. Method for determination of antibiotics
Дата введения — 2013—01—01
1 Область применения
Настоящий стандарт распространяется на натуральный мед и устанавливает метод определения остаточных количеств антибиотиков тетрацикпиновой группы и левомицетина (хлорамфеникола) (далее — ХАФ) на основе твердофазного иммуноферментного анализа (далее — ИФА).
Пределы обнаружения составляют:
- для тетрациклина, ролитетрациклина — 6 мкг/кг,
- левомицетина — 0,025 мкг/кг.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты:
ГОСТ Р 12.1.019-2009 Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты
ГОСТ Р ИСО 5725-1-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения
ГОСТ Р ИСО 5725-6-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике
ГОСТ Р 51568-99 (ИСО 3310-1—90) Сита лабораторные из металлической проволочной сетки. Технические условия
ГОСТ Р 52501-2005 (ИСО 3696:1987) Вода для лабораторного анализа. Технические условия ГОСТ Р 53228-2008 Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.4.009-83 Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание
ГОСТ 1770-74 (ИСО 1042—83, ИСО 4788—80) Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 3145-84 Часы механические с сигнальным устройством. Общие технические условия
ГОСТ 4233-77 Реактивы. Натрий хлористый. Технические условия
ГОСТ 4328-77 Реактивы. Натрия гидроокись. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
Издание официальное
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
ГОСТ 16317-87 Приборы холодильные электрические бытовые. Общие технические условия
ГОСТ 19792-2001 Мед натуральный. Технические условия
ГОСТ 19881-74 Анализаторы потенциометрические для контроля pH молока и молочных продуктов. Общие технические условия
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодно издаваемому информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по соответствующим ежемесячно издаваемым информационным указателям, опубликованным в текущем году. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены термины по ГОСТ 19792, ГОСТ Р ИСО 5725-1, а также следующие термины с соответствующими определениями:
3.1 антибиотики: Широкий спектр антимикробных ветеринарных препаратов (в т. ч. тетрацикли-ны, левомицетин), используемых для профилактики и лечения инфекционных заболеваний пчел.
3.2 остаточное количество антибиотика в меде: Массовая доля остатка антибиотика в меде, выражают в микрограммах на килограмм.
3.3 иммуноферментный анализ; ИФА (enzyme-linked immunosorbent assay; ELISA): Лабораторный иммунологический метод качественного определения и количественного измерения антигенов и антител.
4 Требования безопасности
4.1 Требования электробезопасности при работе с приборами — по ГОСТ Р 12.1.019.
4.2 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
4.3 При выполнении анализов необходимо соблюдать требования безопасности при работе с химическими реактивами согласно ГОСТ 12.1.007.
5 Отбор и подготовка пробы меда
5.1 Отбор проб — по ГОСТ 19792.
5.2 Закристаллизованный мед размягчают на водяной бане, предназначенной для равномерного обогрева с помощью трубчатых электрических нагревательных элементов мощностью не более 1000 Вт, напряжение сети 220 В, диапазон регулировки температуры от 20 °С до 100 °С или в сушильном шкафу по ГОСТ 14919 при температуре не выше 40 °С и продавливают металлическим или пластмассовым шпателем с длиной рабочей поверхности не менее 20 мм через сито по ГОСТ Р 51568. Крупные механические частицы удаляют вручную.
5.3 Сотовый мед распечатывают, отделяют от сот с помощью металлического сита без нагревания.
6 Определение присутствия и массовой доли антибиотиков тетради клиновой группы6.1 Сущность метода
Базовым принципом для количественного определения антибиотиков тетрациклиновой группы в меде является твердофазный конкурентный ИФА на планшетах из полистирола. Метод основан на конкуренции свободного антибиотика из меда и антибиотика, предварительно адсорбированного на твердой фазе (лунке планшета) в составе белкового конъюгата, за центры связывания специфичных к
ГОСТ Р 54655-2011
тетрациклинам антител во вносимом растворе. После отделения несвязавшихся реагентов количество антител, прореагировавших с иммобилизованным антигеном, определяют с помощью вторичных анти-видовых антител, меченных пероксидазой хрена. Количество связавшегося с антителами конъюгата вторичных антител определяют с помощью субстрат-хромогенной смеси. Количество определяемого антибиотика, содержащегося в анализируемой пробе, обратно пропорционально регистрируемой оптической плотности продукта ферментативной реакции.
6.2 Средства измерений, вспомогательные устройства, посуда, материалы и реактивы
6.2.1 Фотометр микропланшетный вертикального сканирования с фильтрами, соответствующими длине волны 450 нм.
6.2.2 Дозаторы пипеточные автоматические с переменным объемом дозирования 0,010—0,100 см1 2 3; 0,100—1,000 см3 и 1,000—5,000 см3 одноканальные.
6.2.3 Дозаторы пипеточные автоматические восьмиканальные с переменным объемом дозирования 0,050—0,300 см3.
6.2.4 Наконечники для автоматических пипеток вместимостью от 0,300 до 1,000 и до 5,000 см3 однократного применения.
6.2.5 Анализатор потенциометрический с пределом допускаемой основной погрешности измерений + 0,01 ед. pH по ГОСТ 19881.
6.2.6 Весы по ГОСТ Р 53228, с пределами допускаемой абсолютной погрешности однократного взвешивания не более + 0,1 мг и не более + 0,002 г.
6.2.7 Шейкер лабораторный для пробирок.
6.2.8 Часы механические с сигнальным устройством по ГОСТ 3145.
6.2.9 Центрифуга настольная с эффективностью не менее 3000 g или иного типа с теми же характеристиками.
6.2.10 Ультразвуковая ванна с эффективной мощностью ультразвука 60 Вт.
6.2.11 Аппарат универсальный для встряхивания.
6.2.12 Стаканы химические вместимостью 50, 100 см3 по ГОСТ 25336.
6.2.13 Колбы мерные вместимостью 1000 см3 по ГОСТ 1770.
6.2.14 Цилиндры мерные 2-25-1 поГОСТ 1770.
6.2.15 Набор реагентов для количественного определения тетрациклина типа «Ридаскрин Тетрациклин».
6.2.16 Натрий фосфорнокислый 2-замещенный 2-водный, с массовой долей основного вещества не менее 98 %.
6.2.17 Натрий фосфорнокислый 1-замещенный 1-водный, с массовой долей основного вещества не менее 98 %.
6.2.18 Натрий хлористый по ГОСТ 4233.
6.2.19 Натрия гидроокись по ГОСТ 4328.
6.2.20 Вода для лабораторного анализа категории 1 по ГОСТ Р 52501.
6.2.21 Твин 20, имп.
6.2.22 Стеклянные виалы вместимостью 1,5, 80 см3 с завинчивающимися крышками.
6.2.23 Бумага фильтровальная по ГОСТ 12026.
6.2.24 Термостат или другое устройство, позволяющее производить равномерный нагрев до температуры 40 °С.
6.3 Характеристика набора для иммуноферментного определения тетрациклинов
Для иммуноферментного определения тетрациклинов применяют промышленно изготовленные наборы, характеристики которых должны быть не ниже указанных в 6.3.1.
6.3.1 Состав набора1*
6.3.1.1 Планшет микротитровальный на 96 лунок (12 стрипов по 8 лунок), сенсибилизированных препаратом тетрациклина, — 1 шт.
6.3.1.2 Комплект стандартных растворов тетрациклина со следующими массовыми концентрациями 0; 1,5; 4,5; 13,5; 40,5; 121,5 нг/см3 в водном растворе по 1,3 см3 — 6 флаконов.
6.3.1.3 Раствор антител — 6,0 см3.
6.3.1.4 Конъюгат вторичных антител с пироксидазой — 10,0 см3.
6.3.1.5 Субстрат/хромоген, содержащий пероксид карбамида (мочевины) и тетраметилбензи-дин, —10,0 см3.
6.3.1.6 Стоп-реагент, содержащий 1 Н серную кислоту, — 14,0 см3.
6.3.1.7 Буфер 1 для разбавления стандартных растворов тетрациклина и растворов образцов — 50,0 см3.
6.3.1.8 Смесь солей для приготовления 1 дм3 моющего буфера.
Примечание — Набор рассчитан на проведение 48 определений в двух повторностях, включая анализируемые пробы и калибровочные растворы (всего 96 определений на один планшет).
6.3.2 Аналитические характеристики набора
6.3.2.1 Специфичность метода
Метод анализа при использовании набора характеризуется показателем специфичности, составляющим для:
тетрациклина — 100 %; ролитетрацикпина — 100 %; хлортетрацикпина — 42 %; демекпоцикпина — 27 %; окситетрацикпина — 13 %; доксициклина — 8 %.
6.3.2.2 Чувствительность метода Пределы обнаружения:
- тетрациклина, ролитетрацикпина — 6 мкг/кг;
- хлортетрацикпина — 15 мкг/кг;
- демекпоцикпина — 23 мкг/кг;
- окситетрацикпина — 50 мкг/кг;
- доксициклина — 75 мкг/кг.
Показатель извлекаемости тетрациклина из меда — (107 + 11) %.
6.3.3 Рекомендации по использованию наборов
6.3.3.1 При проведении испытаний следует использовать реагенты и компоненты, входящие в один и тот же набор. Разбавление или замена реагентов, использование реагентов из набора с другим номером партии могут привести к потере чувствительности или ошибке определения.
6.3.3.2 Необходимо хранить наборы при температуре 2 °С—8 °С.
Не допускается хранение при отрицательной температуре и замораживание реагентов набора. Для хранения неиспользованных стрипов (лунок) их герметично упаковывают в оригинальный фольги-рованный пакет вместе с имеющимся осушителем.
6.3.3.3 Необходимо избегать попадания прямых солнечных лучей на флакон с раствором хромогена из-за его светочувствительности.
6.3.3.4 Раствор хромогена подкрашен в розовый цвет для удобства использования. В случае окрашивания раствора хромогена в голубой цвет его применение для анализа не допускается, поскольку такое окрашивание раствора хромогена является признаком порчи.
6.3.3.5 Сроки хранения отдельных компонентов набора указаны на упаковке.
6.3.4 Требования техники безопасности при проведении определений
6.3.4.1 Стандартные растворы содержат тетрациклин, поэтому требуется особая осторожность.
6.3.4.2 Стоп-реагент содержит серную кислоту, поэтому следует избегать контакта стоп-реагента с кожей.
6.4 Проведение испытаний с применением набора
6.4.1 Отбор и подготовка проб меда — по разделу 5.
6.4.2 Приготовление раствора натрия гидроокиси молярной концентрации 0,1 моль/дм3
(4,00 + 0,01) г натрия гидроокиси по 6.2.19 взвешивают в стакане вместимостью 100 см3 по 6.2.12, растворяют в 75 см3 воды для лабораторного анализа по 6.2.20, количественно переносят в мерную колбу вместимостью 1000 см3 по 6.2.13, доводят до метки водой и тщательно перемешивают.
6.4.3 Приготовление фосфатного буфера 1 молярной концентрацией 20 ммоль/дм3 для разбавления стандартных растворов тетрациклина и растворов образцов
(0,55 + 0,01) г натрия фосфорнокислого 1-замещенного 1-водного по 6.2.17 взвешивают в стакане вместимостью 50 см3 по 6.2.12, растворяют в 25 см3 воды для лабораторного анализа, количественно 4
ГОСТ Р 54655-2011
переносят в мерную колбу вместимостью 10ОО см3. Аналогично взвешивают и растворяют (2,85 ± 0,01) г натрия фосфорнокислого 2-замещенного 2-водного по 6.2.16 и (9,00 + 0,01) г натрия хлористого по 6.2.18, оба раствора количественно переносят в ту же мерную колбу. В ту же колбу добавляют 800 см3 воды для лабораторного анализа. Раствор тщательно перемешивают. Измеряют значение pH приготовленного раствора, которое должно составлять 7,4 ед. pH. В случае несоответствия значения pH довести его до требуемой величины добавлением в мерную колбу 0,1 Н раствора гидроокиси натрия по 6.4.2. Раствор доводят до метки водой и тщательно перемешивают.
Срок хранения буферного раствора при температуре 6 °С—10 °С — не более одного года.
6.4.4 Приготовление моющего буферного раствора с твином 20
Фосфатный буферный раствор готовят по 6.4.3. Количественно переносят 500 см3 в мерную колбу вместимостью 1000 см3. Дополнительно в мерную колбу добавляют 0,5 см3твина 20 по 6.2.21, доводят водой до метки и тщательно перемешивают.
Срок хранения раствора при температуре 6 °С—10 °С — не более одного года.
6.4.5 Приготовление анализируемой пробы
Взвешивают (1,00 + 0,001) г меда, подготовленного по разделу 5, в стеклянной виале вместимостью 80 см3. Добавляют (49,00 + 0,001) г фосфатного буфера 1 по 6.4.3 и тщательно завинчивают крышку виалы. Виалу помещают в ультразвуковую ванну по 6.2.10 на 5 мин. Затем раствор интенсивно перемешивают на шейкере по 6.2.7 в течение 2 мин. Перед анализом встряхивают пробы вверх-вниз.
6.4.6 Приготовление реагентов для анализа
Перед использованием набора довести температуру всех реагентов до комнатной в пределах 20 °С—25 °С, а после использования охладить все оставшиеся реагенты до температуры 2 °—8 °С в холодильных приборах по ГОСТ 16317.
В процессе выполнения анализа нельзя допускать высыхания лунок планшета. На всех стадиях определения необходимо избегать воздействия прямого солнечного света.
Растворы антител, конъюгата, субстрата/хромогена, стоп-реагента, входящие в состав набора, поставляются в готовом к употреблению виде. Перед употреблением достаточно вскрыть флакон.
6.4.7 Приготовление стандартных растворов
Подготовку стандартных растворов проводят только в одноразовых стеклянных виалах вместимостью 1,5 см3.
Для подготовки к использованию стандартных растворов тетрациклина концентраты стандартных растворов, входящих в состав набора, разбавляют буфером 1 (таблица 1). После разбавления необходимо тщательно перемешать готовые растворы.
После каждой серии определений необходимо готовить свежие стандартные растворы.
Построение градуировочной кривой необходимо проводить для каждой серии определений.
|
Таблица 1 — Приготовление стандартных растворов тетрациклина | ||||||||||||||||||||||||||||
|
6.4.8 Подготовка микротитровального планшета
Перед выполнением анализа из планшета необходимо извлечь необходимое количество стрипов. Оставшиеся стрипы следует тщательно упаковать в фольгированный пакет вместе с осушителем, герметично закрыть пакет и поместить на хранение при температуре 2 °С—8 °С.
6.4.9 Процедура анализа
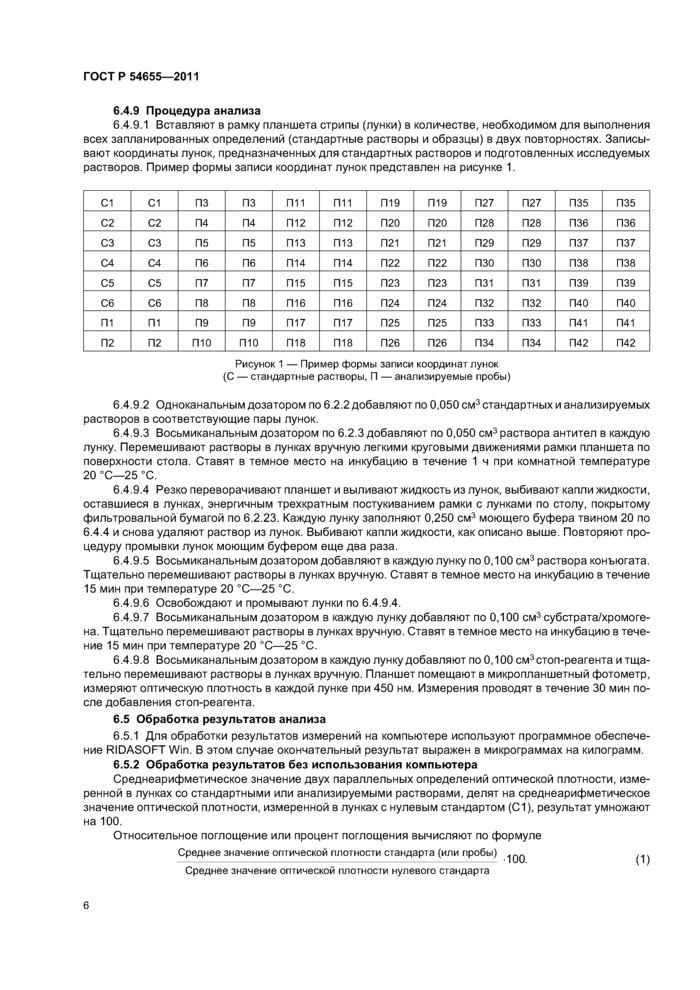
6.4.9.1 Вставляют в рамку планшета стрипы (лунки) в количестве, необходимом для выполнения всех запланированных определений (стандартные растворы и образцы) в двух повторностях. Записывают координаты лунок, предназначенных для стандартных растворов и подготовленных исследуемых растворов. Пример формы записи координат лунок представлен на рисунке 1.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Рисунок 1 — Пример формы записи координат лунок (С — стандартные растворы, П — анализируемые пробы) |
6.4.9.2 Одноканальным дозатором по 6.2.2 добавляют по 0,050 см3 стандартных и анализируемых растворов в соответствующие пары лунок.
6.4.9.3 Восьмиканальным дозатором по 6.2.3 добавляют по 0,050 см3 раствора антител в каждую лунку. Перемешивают растворы в лунках вручную легкими круговыми движениями рамки планшета по поверхности стола. Ставят в темное место на инкубацию в течение 1 ч при комнатной температуре 20 °С—25 °С.
6.4.9.4 Резко переворачивают планшет и выливают жидкость из лунок, выбивают капли жидкости, оставшиеся в лунках, энергичным трехкратным постукиванием рамки с лунками по столу, покрытому фильтровальной бумагой по 6.2.23. Каждую лунку заполняют 0,250 см3 моющего буфера твином 20 по
6.4.4 и снова удаляют раствор из лунок. Выбивают капли жидкости, как описано выше. Повторяют процедуру промывки лунок моющим буфером еще два раза.
6.4.9.5 Восьмиканальным дозатором добавляют в каждую лунку по 0,100 см3 раствора конъюгата. Тщательно перемешивают растворы в лунках вручную. Ставят в темное место на инкубацию в течение 15 мин при температуре 20 °С—25 °С.
6.4.9.6 Освобождают и промывают лунки по 6.4.9.4.
6.4.9.7 Восьмиканальным дозатором в каждую лунку добавляют по 0,100 см3 субстрата/хромоге-на. Тщательно перемешивают растворы в лунках вручную. Ставят в темное место на инкубацию в течение 15 мин при температуре 20 °С—25 °С.
6.4.9.8 Восьмиканальным дозатором в каждую лунку добавляют по 0,100 см3 стоп-реагента и тщательно перемешивают растворы в лунках вручную. Планшет помещают в микропланшетный фотометр, измеряют оптическую плотность в каждой лунке при 450 нм. Измерения проводят в течение 30 мин после добавления стоп-реагента.
6.5 Обработка результатов анализа
6.5.1 Для обработки результатов измерений на компьютере используют программное обеспечение RIDASOFT Win. В этом случае окончательный результат выражен в микрограммах на килограмм.
6.5.2 Обработка результатов без использования компьютера
Среднеарифметическое значение двух параллельных определений оптической плотности, измеренной в лунках со стандартными или анализируемыми растворами, делят на среднеарифметическое значение оптической плотности, измеренной в лунках с нулевым стандартом (С 1), результат умножают на 100.
Относительное поглощение или процент поглощения вычисляют по формуле
Среднее значение оптической плотности нулевого стандарта
Среднее значение оптической плотности стандарта (или пробы) .
6
ГОСТ Р 54655-2011
Примечание — Если величина оптической плотности, измеренной в лунке с нулевым стандартом, меньше 0,6, то это может быть признаком порчи реагентов. В этом случае следует заменить реагенты и повторить определение.
По величинам относительного поглощения, вычисленным для стандартных растворов, и соответствующим известным значениям концентрации тетрациклина в микрограммах на килограмм строят градуировочную кривую в полулогарифмической системе координат.
Концентрацию тетрациклина в растворах анализируемых проб в микрограммах на килограмм определяют по градуировочной кривой в соответствии с относительным поглощением, измеренным и вычисленным для каждого раствора.
Для определения массовой доли тетрациклина в анализируемой пробе в микрограммах на килограмм величину концентрации тетрациклина, полученную по градуировочной кривой, умножают на 50 (коэффициент разбавления при выполнении анализа в точном соответствии с приведенной методикой).
Для определения массовой доли окситетрациклина в анализируемой пробе в микрограммах на килограмм с учетом показателя специфичности величину концентрации тетрациклина, полученную по градуировочной кривой, умножают на 400 (коэффициент разбавления при выполнении анализа в точном соответствии с приведенной методикой).
Вычисления проводят с записью результата до второго десятичного знака.
Окончательный результат записывают с точностью до первого десятичного знака.
За окончательный результат определения принимают среднеарифметическое значение результатов двух параллельных измерений Мт 1 и Мт 2, если выполняется условие приемлемости
2\<г,г=2,8 сг 0,0'\ Мт, (2)
где Мт 1 и Мт 2 — значения результатов параллельных определений остаточных количеств антибиотиков группы тетрациклина; г — предел повторяемости для двух результатов параллельных определений при дове-_ рительной вероятности Р = 0,95 (таблица 3);
Мт—среднеарифметическое значение результатов двух параллельных определений остаточных количеств антибиотиков группы тетрациклина.
6.6 Точность метода
Статистический анализ результатов испытаний по оценке точности метода проводят в соответствии с требованиями ГОСТ Р ИСО 5725-6. Диапазон измерений массовой доли тетрациклина, для которого рассчитаны метрологические характеристики, составляет 7,5—600 мкг/кг.
6.6.1 Повторяемость результатов
Абсолютное расхождение между результатами двух измерений Мт 1 и Мт 2, которые получены в условиях повторяемости (одна и та же методика, идентичный объект испытания, одна и та же лаборатория, один и тот же оператор, одно и тоже оборудование, короткий промежуток времени), не должно превышать предела повторяемости г= 2,8 <тг • 0,01 •Мт. Значения гиог представлены в таблицах 2 и 3.
|
Таблица 2 — Значения характеристик погрешности и ее составляющих при доверительной вероятности Р = 0,95 | ||||||
|
|
Таблица 3 — Значения пределов повторяемости и воспроизводимости при доверительной вероятности Р = 0,95 | ||||
|
6.6.2 Воспроизводимость результатов _ _
Абсолютное расхождение между результатами двух независимых измерений Мт 1 и Мт 2, которые получены в условиях воспроизводимости (одна и та же методика, идентичный объект испытания, разные лаборатории, разные операторы, различное оборудование), не должно превышать предела воспроизводимости
\МТ ^ -Mj2\<R, R = 2,8 •aR- 0,01 •Мт. (3)
Значения R и aR представлены в таблицах 2 и 3.
6.6.3 При соблюдении всех регламентируемых методикой условий с доверительной вероятностью Р = 0,95 не должны превышать значений, приведенных в таблицах 2 и 3.
6.6.4 Форма представления результата
Результат измерения в документах, предусматривающих его использование, представляют в
виде:
(Мср ± А), мкг/кг, Р = 0,95, (4)
где Мср — среднеарифметическое значение результатов двух параллельных определений остаточных количеств антибиотиков группы тетрациклина, полученных в условиях повторяемости;
+Д — границы характеристик абсолютной погрешности результатов измерения массовой доли тетрациклина, мкг/кг;
+Д = +5 МСр/100, значение относительной погрешности +8 представлено в таблице 2.
7 Определение присутствия и массовой доли левомицетина (хлорамфеникола, ХАФ)7.1 Сущность метода
Базовым принципом для количественного определения ХАФ в меде является твердофазный конкурентный ИФА на планшетах из полистирола. Метод основан на конкуренции свободного ХАФ из анализируемой пробы и коньюгата ХАФ за центры связывания специфичных к ХАФ антител, адсорбированных на твердой фазе (лунке планшета). Весь несвязанный ферментный конъюгат удаляется на стадии промывки лунок. Субстрат-хромогеновый раствор добавляют в лунки, связанный ферментный конъюгат взаимодействует с хромогеном, образуются продукты голубого цвета. При добавлении стоп-реагента цвет раствора меняется с голубого на желтый. Количество определяемого ХАФ, содержащегося в исследуемом образце, обратно пропорционально регистрируемой оптической плотности продукта ферментативной реакции, которую измеряют с помощью микропланшетного фотометра при длине волны 450 нм.
7.2 Средства измерений, вспомогательные устройства, посуда, материалы и
реактивы — по 6.2 с дополнением:
7.2.1 Многоканальный микроиспаритель или роторно-пленочный испаритель.
7.2.2 Стеклянные виалы вместимостью 1,5 см3 с завинчивающимися крышками.
7.2.3 Колбы круглодонные для роторного испарителя вместимостью 10 см3 или стеклянные пробирки вместимостью 10 см3 для многоканального микроиспарителя.
7.2.4 Пробирки центрифужные с крышками вместимостью 15 см3 однократного применения.
7.2.5 Набор реагентов для количественного определения хлорамфеникола.
7.2.6 Этилацетат, о. с. ч.
7.3 Характеристика набора для иммуноферментного определения ХАФ
Для иммуноферментного определения ХАФ применяют промышленно изготовленные наборы, характеристики которых не ниже указанных в 7.3.1.
7.3.1 Состав набора1)
7.3.1.1 Планшет микротитровальный на 96 лунок (12 стрипов по 8 лунок), сенсибилизированных антителами против хлорамфеникола, — 1 шт.
Отработка метрологических характеристик метода проводилась с применением наборов «Ридаскрин Хпо-рамфеникол». Данная информация приводится для удобства пользователей настоящего стандарта и не содержит требований применять данный набор.
1
Отработка метрологических характеристик метода проводилась с применением наборов «Ридаскрин Тет
2
рациклин». Данная информация приводится для удобства пользователей настоящего стандарта и не содержит требований применять данный набор.
3
4