ГОСТ ISO 81060-2-2021
Сфигмоманометры (измерители артериального давления) неинвазивные. Часть 2. Клинические испытания моделей с автоматическим типом измерения
Устанавливает требования и методы для клинического испытания медицинского изделия, используемого для периодической неинвазивной автоматической оценки артериального давления с использованием манжеты. Настоящий стандарт применим ко всем сфигмоманометрам, которые воспринимают или отображают пульсации, поток или звуки для оценки, отображения или записи артериального давления. Для этих сфигмоманометров не требуется автоматическая накачка манжеты. Настоящий стандарт распространяется на сфигмоманометры, предназначенные для использования у всех групп пациентов (например, всех возрастов и весовых категорий), и при всех условиях использования (например, амбулаторный мониторинг артериального давления, мониторинг артериального давления с нагрузкой и мониторинг артериального давления в условиях лечения на дому для самоконтроля, а также для использования в медицинской организации
39 страниц
| Дата введения | 01.03.2022 |
|---|---|
| Актуализация | 01.01.2022 |
Этот ГОСТ находится в:
- Раздел Общероссийский классификатор стандартов
- Раздел Здравоохранение
- Раздел Медицинское оборудование
- Раздел Диагностическое оборудование
- Раздел Медицинское оборудование
- Раздел Здравоохранение
Non-invasive sphygmomanometers (measuring devices of arterial pressure). Part 2. Clinical investigation of intermittent automated measurement type
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
стр. 17

стр. 18

стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28

стр. 29

стр. 30
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION. METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ГОСТ
ISO 81060-2— 2021
СФИГМОМАНОМЕТРЫ (ИЗМЕРИТЕЛИ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ) НЕИНВАЗИВНЫЕ
Часть 2
Клинические испытания моделей с автоматическим типом измерения
(ISO 81060-2:2018+Amd.1:2020, Non-invasive sphygmomanometers —
Part 2: Clinical investigation of intermittent automated measurement type, IDT)
Издание официальное
Москва
Российский институт стандартизации 2021
Предисловие
Цели, основные принципы и общие правила проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены».
Сведения о стандарте
1 ПОДГОТОВЛЕН Федеральным государственным бюджетным учреждением «Российский институт стандартизации» (ФГБУ «РСТ») и Обществом с ограниченной ответственностью «Медтехстандарт» (ООО «Медтехстандарт») на основе собственного перевода на русский язык англоязычной версии стандарта. указанного в пункте 5
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 26 августа 2021 г. Мч 142-П)
|
За принятие проголосовали. | ||||||||||||||||||
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 22 октября 2021 г. N® 1258-ст межгосударственный стандарт ГОСТ ISO 81060-2-2021 введен в действие в качестве национального стандарта Российской Федерации с 1 марта 2022 г.
5 Настоящий стандарт идентичен международному стандарту ISO 81060-2:2018 «Сфигмомано-метры неинвазивные. Часть 2. Клинические испытания моделей с автоматическим типом измерения» («Non-invasive sphygmomanometers — Part 2: Clinical investigation of intermittent automated measurement type», IDT), включая изменение Amd.1:2020. Изменение внесено в текст настоящего стандарта и выделено двойной вертикальной линией, расположенной на полях напротив соответствующего текста.
Международный стандарт разработан подкомитетом SC 3 «Вентиляторы легких и сопутствующее оборудование» Технического комитета по стандартизации ISO,ТС 121 «Оборудование для анестезии и искусственной вентиляции легких» Международной организации по стандартизации (ISO) и подкомитетом SC D «Медицинская электроаппаратура» Технического комитета по стандартизации IECTC 62 «Электрооборудование в медицинской практике» Международной электротехнической комиссии (IEC).
Наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для увязки с наименованиями, принятыми в существующем комплексе межгосударственных стандартов.
При применении настоящего стандарта рекомендуется использовать вместо ссылочных международных стандартов соответствующие им межгосударственные стандарты, сведения о которых приведены в дополнительном приложении ДА
6 ВВЕДЕН ВПЕРВЫЕ
1) чувствовал себя комфортно.
Пример — Субъект находится в удобном сидячем положении, ноги не перекрещиваются, ступни на полу;
2) имел опору для спины, локтей и предплечий;
3) имел место измерения давления на уровне правого желудочка сердца.
b) Рекомендуется, чтобы;
1) субъект максимально расслабился, и
2) не разговаривал во время всей ПРОЦЕДУРЫ.
c) МАНЖЕТУ накладывают на кожу руки, около манжеты рука не должна испытывать никаких сдавливаний, например одеждой, проксимальнее МАНЖЕТЫ.
d) До считывания первых ЭТАЛОННЫХ значений должно пройти 5 мин.
Примечание — Дополнительные детали см. в справочном материале [16].
Соответствие устанавливают путем проверки инструкции по эксплуатации и ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.2* Подготовка наблюдателя
a) Наблюдатели должны быть подготовлены к использованию соответствующих методик измерения АРТЕРИАЛЬНОГО ДАВЛЕНИЯ покоя, используя утвержденные клинические протоколы измерения АРТЕРИАЛЬНОГО ДАВЛЕНИЯ. См. [15]. [16] и [25]. в которых содержится дополнительная информация.
b) Наблюдатели должны иметь достаточный опыт измерения АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
c) Данные ЭТАЛОННОГО СФИГМОМАНОМЕТРА, фиксируемые наблюдателями, не должны быть видимы другим наблюдателям.
d) Результаты измерения ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА не должны быть видимы никому из этих наблюдателей.
Пример 1 — Использование третьего наблюдателя для записи показаний ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА.
Пример 2 — Использование электронных средств записи показаний ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА.
e) Наблюдатели должны использовать тон Короткова [пятая фаза или К5] для определения ЭТАЛОННОГО ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ.
f) Если тон Короткова [пятая фаза или К5] не слышим для определения ЭТАЛОННОГО ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ, то субъект должен быть исключен.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.3* ЭТАЛОННЫЕ результаты измерения
a) Два наблюдателя должны проводить одновременное определение значений СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ и ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ на каждом субъекте, используя двойной стетоскоп.
b) Если ИСПЫТУЕМЫЙ СФИГМОМАНОМЕТР не предназначен только для использования при существенно нерегулярном ритме сердца и если любой из наблюдателей определяет существенно нерегулярный ритм сердца, то такое показание должно быть исключено.
Пример — Бигеминия, тригеминия, единичные желудочковые экстрасистолы (VPB). мерцательная аритмия (трепетание предсердий).
Примечание 1 — Хотя оценка АРТЕРИАЛЬНОГО ДАВЛЕНИЯ у ПАЦИЕНТОВ с мерцательной аритмией (трепетанием предсердий) имеет важное клиническое значение, в настоящее время отсутствуют общепринятые руководящие указания по определению АРТЕРИАЛЬНОГО ДАВЛЕНИЯ у таких лиц.
c) Любая пара показаний СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ или ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ, предоставленная наблюдателями, в значении которых есть разница более 4 мм рт. ст. (0,53 кПа), должна быть исключена.
d) Отдельные значения, предоставленные наблюдателями по каждому показанию, должны быть приведены к среднему показателю по формуле (2) для получения значения ЭТАЛОННОГО АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
(2)
ряда парных определений при ЭТАЛОННОМ испытании.
|
где р _ fref |
значение |
|
1* |
казания; |
|
PR£F “ |
значение |
|
>3 |
казания; |
|
PREF |
значение |
|
е) Различия между | |
1) Если какие-либо результаты измерения исключаются, должна быть получена дополнительная пара(ы) для гарантии того, что имеется необходимое количество достоверных пар при ЭТАЛОННОМ измерении.
2) Для каждого субъекта должно быть зафиксировано максимум восемь пар результатов из
мерений.
0 Необходимо использовать ЭТАЛОННЫЙ СФИГМОМАНОМЕТР, соответствующий требованиям ISO 81060-1, за исключением того, что максимальная допустимая погрешность должна быть ± 1 мм рт. ст. (0.13 кПа).
1) Считывание результатов измерений на ЭТАЛОННОМ СФИГМОМАНОМЕТРЕ должно быть максимально точным.
2) При считывании результатов измерений на ЭТАЛОННОМ СФИГМОМАНОМЕТРЕ наблюдателям следует избегать ошибок от параллакса и округлений.
Примечание 2 — Округление оказывает негативное влияние на результаты КЛИНИЧЕСКОГО ИСПЫТАНИЯ.
д) Измерение охвата плеча:
1) Отмечают середину плеча, поставив отметку на задней поверхности руки в точке, расположенной посредине между плечевым и локтевым суставами, когда рука согнута под углом 90 градусов в локте, ладонь обращена вверх.
2) Охват плеча субъекта определяют путем измерения в срединной точке плеча, когда локоть расслаблен, а рука свободно свисает сбоку от туловища.
h)* МАНЖЕТЫ для эталонного СФИГМОМАНОМЕТРА должны иметь:
1) длину, равную 75 % — 100 % охвата плеча:
2) ширину 37 % — 50 % охвата плеча; и
3) конструкцию из 2 частей, содержащую:
i) эластичную внутреннюю камеру; и
ii) неэластичный наружный рукав (оболочку).
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.4 Методы КЛИНИЧЕСКОГО ИСПЫТАНИЯ
5.2.4.1 Метод последовательного определения на одной руке
5.2.4.1.1* Процедура
a) Для исследования можно использовать любую руку
Выполняют следующие действия.
b) Используя ЭТАЛОННЫЙ СФИГМОМАНОМЕТР, наблюдатели определяют значение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ субъекта (см. рисунок 1).
c) Заменяют МАНЖЕТЫ и ожидают не менее 60 с.
d) Определяют АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ субъекта при помощи ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА.
е) Очищают память ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА от предыдущего результата измерения и затем ожидают не менее 60 с.
Примеры — Выключение и включение питания, удаление модуля АРТЕРИАЛЬНОГО ДАВЛЕНИЯ и его повторная установка, а также запуск команды перезагрузки являются методами очистки памяти от предыдущего результата измерения.
1 — двойной стетоскоп: 2 — дисплей ЭТАЛОННОГО СФИГМОМАНОМЕТРА: 3 -- ручной нагнетатель воздуха ЭТАЛОННОГО СФИГМОМАНОМЕТРА. 4 - ИСПЫТУЕМЫЙ СФИГМОМАНОМЕТР
Примечание — Только одна МАНЖЕТА соединена с ИСПЫТУЕМЫМ СФИГМОМАНОМЕТРОМ.
Рисунок 1 — Иллюстрация метода последовательного определения на одной и той же руке
0 При определении точности не используют данные, полученные по пунктам Ь) и d).
g) Наблюдатели определяют АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ субъекта, используя ЭТАЛОННЫЙ СФИГМОМАНОМЕТР
h) Заменяют МАНЖЕТЫ и выжидают не менее 60 с.
i) Определяют АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ субъекта, используя ИСПЫТУЕМЫЙ СФИГМОМАНОМЕТР
j) Заменяют МАНЖЕТЫ и выжидают не менее 60 с.
k) Наблюдатели при помощи ЭТАЛОННОГО СФИГМОМАНОМЕТРА определяют ЭТАЛОННОЕ значение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ субъекта.
l) Заменяют МАНЖЕТЫ и выжидают не менее 60 с.
т) Повторяют действия по пунктам с i) no I) до тех пор. пока не будет выполнено необходимое число достоверных ЭТАЛОННЫХ измерений.
п) Все данные по субъекту должны быть исключены, если:
1) любые два ЭТАЛОННЫХ ЗНАЧЕНИЯ СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ отличаются более. чем на 12 мм pm. cm. (1.60 кПа): или
2) любые два ЭТАЛОННЫХ ЗНАЧЕНИЯ ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ отличаются более, чем на 8 мм pm. cm. (1.07 кПа).
о) Несмотря на требование пункта п). если ЭТАЛОННОЕ АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ отдельного субъекта не отвечает этим критериям в период выполнения испытания, могут использоваться две отвечающие требованиям последовательные пары ЭТАЛОННЫХ измерений и их результатов.
1) В этом случав должны быть привлечены дополнительные субъекты для обеспечения минимального числа измерений.
2) Не более 10% субъектов должны иметь меньше трех достоверных пар ЭТАЛОННЫХ значений и ОПРЕДЕЛЕНИЙ.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.4.1.2 Анализ данных
ИСПЫТУЕМЫЙ СФИГМОМАНОМЕТР должен соответствовать следующим двум критериям.
а) Критерий 1
1) Средняя погрешность определения для л-го количества отдельных парных ОПРЕДЕЛЕНИЙ. полученных ИСПЫТУЕМЫМ СФИГМОМАНОМЕТРОМ и ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ для всех субъектов, рассчитанная отдельно для СИСТОЛИЧЕСКОГО и ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ. должна:
I) в соответствии с формулой (3) иметь среднее значение разницы х . в пределах или равное ±5.0 мм рт. ст. (±0,67 кПа); и
|
SUT |
п
х
п
(3)
|
г-1 | |
|
S о | |
(4)
средняя величина разницы показаний;
разница между /-ми парными значениями АРТЕРИАЛЬНОГО ДАВЛЕНИЯ (ОПРЕДЕЛЕНИЕ ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА — ПОКАЗАНИЕ ЭТАЛОННОГО АРТЕРИАЛЬНОГО ДАВЛЕНИЯ); индекс отдельного элемента: количество ИЗМЕРЕНИЙ:
где х
о
PSUT ~PREF
/
п
II) в соответствии с формулой (4) иметь стандартную величину отклонения sn, не превышающую 8.0 мм рт. ст. (1.07 кПа):
PREf; — ЭТАЛОННОЕ АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ для /-го значения согласно расчету -*». по формуле (5).
Ill) хп и sn должны быть рассчитаны и выражены с точностью, как минимум, до 0.1 мм рт. ст. (0.01 кПа).
2) ПОКАЗАНИЕ ЭТАЛОННОГО АРТЕРИАЛЬНОГО ДАВЛЕНИЯ росе должно быть сред-
КЕг
-•9,
|
1 4 |
(5)
ним значением показаний, полученных наблюдателями с использованием ЭТАЛОННОГО СФИГМОМАНОМЕТРА до и после определения с помощью ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА
где pR_F — значение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ, определенное наблюдателем 1 для /-го п показания;
— значение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ, определенное наблюдателем 2 для /-го '■* показания.
Пример 1 — п - 255 для СФИГМОМАНОМЕТРОВ, предназначенных для взрослых ПАЦИЕНТОВ или подростков (исследование на 85 субъектах).
Пример 2 — л = 255 для СФИГМОМАНОМЕТРОВ, предназначенных для взрослых ПАЦИЕНТОВ или подростков и детей в возрасте от 3 до 12 лет (исследование на 85 субъектах).
Пример 3 — л = 105 для СФИГМОМАНОМЕТРОВ, предназначенных для специального ПРЕДУСМОТРЕННОГО ПРИМЕНЕНИЯ (исследование на 35 субъектах), когда СФИГМОМАНОМЕТР прошел КЛИНИЧЕСКОЕ ИСПЫТАНИЕ в процессе отдельного изучения на 85 субъектах в соответствии с 5.1.1 и 5.2.
Ь) Критерий 2
1) Для СИСТОЛИЧЕСКОГО и ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ для каждого из т субъектов среднеквадратическое отклонение sm усредненных парных ОПРЕДЕЛЕНИЙ для субъекта на ИСПЫТУ-
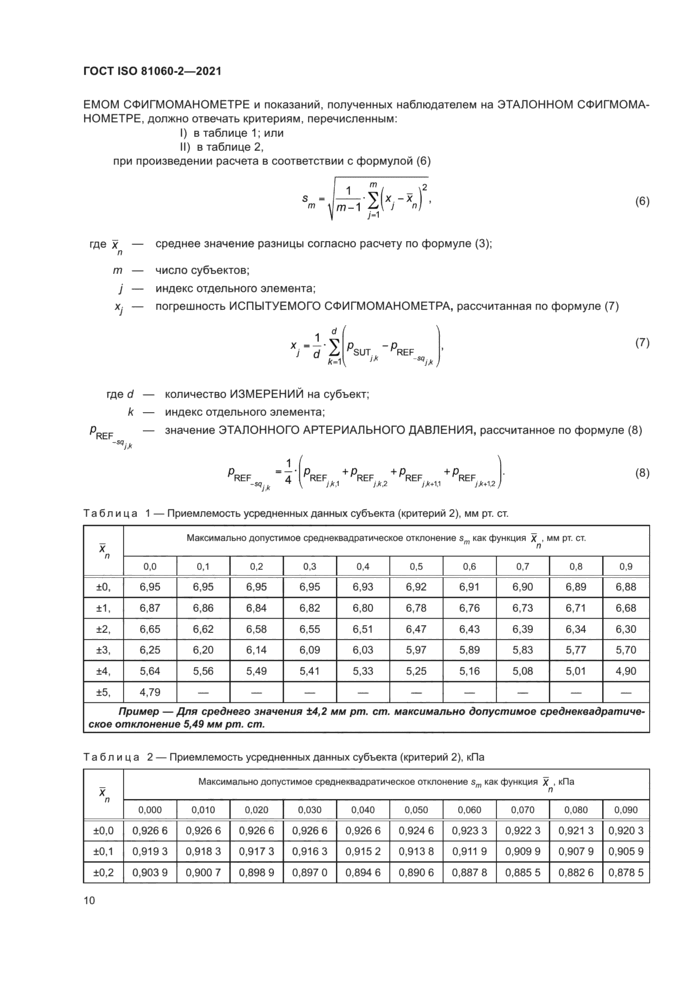
ЕМОМ СФИГМОМАНОМЕТРЕ и показаний, полученных наблюдателем на ЭТАЛОННОМ СФИГМОМА-НОМЕТРЕ, должно отвечать критериям, перечисленным:
I) в таблице 1; или
II) в таблице 2.
при произведении расчета в соответствии с формулой (6)
где х
п
т
j
среднее значение разницы согласно расчету по формуле (3):
число субъектов;
индекс отдельного элемента;
погрешность ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА, рассчитанная по формуле (7)
|
х J |
SUT |
-р,
)*
REF
ГМ|
(7)
где d
к
количество ИЗМЕРЕНИЙ на субъект; индекс отдельного элемента;
значение ЭТАЛОННОГО АРТЕРИАЛЬНОГО ДАВЛЕНИЯ, рассчитанное по формуле (8)
REF
-т • р,
REF
+ Р,
/>1
REF
+ Р,
REF
+ Р,
;Л.\1
REF
,>•12
(8)
|
Таблица 1 — Приемлемость усредненных данных субъекта (критерий 2), мм рт. ст. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Пример —Для среднего значения ±4,2 мм pm. ст. максимально допустимое среднеквадратиче ское отклонение 5.49 мм pm. ст. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Таблица 2 — Приемлемость усредненных данных субъекта (критерий 2). кПа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Окончание таблицы 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Пример — Для среднего значения ±0,520 кПа максимально допустимое среднеквадратическое отклонение 0.759 кПа | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Пример 4 — т = 85 для СФИГМОМАНОМЕТРОВ, предназначенных для взрослых ПАЦИЕНТОВ или подростков (исследование на 85 субъектах).
Пример 5 — т = 85 для СФИГМОМАНОМЕТРОВ. предназначенных для взрослых ПАЦИЕНТОВ или подростков и детей в возрасте от 3 до 12 лет (исследование на 85 субъектах).
Пример 6 — т = 35 для СФИГМОМАНОМЕТРОВ. предназначенных для специального ПРЕДУСМОТРЕННОГО ПРИМЕНЕНИЯ (исследование на 35 субъектах). Когда СФИГМОМАНОМЕТР прошел КЛИНИЧЕСКОЕ ИСПЫТАНИЕ на отдельных 85 субъектах в соответствии с 5.1.1 и 5.2.
Пример 7 — т = 85 для СФИГМОМАНОМЕТРОВ. предназначенных только для специального ПРЕДУСМОТРЕННОГО ПРИМЕНЕНИЯ (исследование на 85 субъектах).
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.4.2* Метод одновременного определения на противоположных руках
5.2.4.2.1 Процедура
a) Исходная сторона при измерении ИСПЫТУЕМЫМ СФИГМОМАНОМЕТРОМ и ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ должна отличаться у разных субъектов.
Выполняют следующие действия:
b) Наблюдатели одновременно определяют значение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ субъекта на противоположных руках при помощи ЭТАЛОННОГО СФИГМОМАНОМЕТРА и ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА (см. рисунок 2).
c) Эти данные не используются при определении точности.
d) Очищают память ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА от значений предыдущего ОПРЕДЕЛЕНИЯ.
Примеры — Выключение и включение питания, удаление и восстановление модуля АРТЕРИАЛЬНОГО ДАВЛЕНИЯ или запуск команды перезагрузки являются методами очистки памяти от предыдущих ОПРЕДЕЛЕНИЙ.
в) Меняют руки для ЭТАЛОННОГО СФИГМОМАНОМЕТРА и ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА.
0 Выжидают не менее 60 с со времени завершения предыдущего ЭТАЛОННОГО ОПРЕДЕЛЕНИЯ или показания.
д) Наблюдатели при помощи ЭТАЛОННОГО СФИГМОМАНОМЕТРА и ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА одновременно определяют АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ субъекта на противоположных руках.
h) Если наблюдатели не выполнили успешно снятие показаний с ЭТАЛОННОГО СФИГМОМАНОМЕТРА и ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА. ожидают не менее 60 с и повторяют всю процедуру на той же руке (то есть без изменения стороны рук).
I) Повторяют действия по пунктам в)—д). пока не будет выполнено шесть парных ОПРЕДЕЛЕНИЙ.
j) Повторяют действия по пунктам b) — i). пока но будет получено необходимое количество достоверных результатов ОПРЕДЕЛЕНИЙ по субъектам.
|
f — двойной стетоскоп: 2 -• дисплей ЭТАЛОННОГО СФИГМОМАНОМЕТРА; 3-■ ручной нагнетатель воздуха ЭТАЛОННОГО СФИГМОМАНОМЕТРА. 4 - ИСПЫТУЕМЫЙ СФИГМОМАНОМЕТР Рисунок 2 — Иллюстрация метода одновременного определения на противоположных руках |
k) Все данные от субъекта должны быть исключены, если:
1) любые два значения ЭТАЛОННОГО СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ на одной и той же руке отличаются более, чем на 12 мм рт. ст. (1.60 кПа);
2) любые два значения ЭТАЛОННОГО ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ на одной и той же руке отличаются более, чем на 8 мм рт. ст. (1,07 кПа);
3) перепад значений ЭТАЛОННОГО СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ превышает 15 мм рт. ст. (2,00 кПа), или
4) перепад значений ЭТАЛОННОГО ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ превышает 10 мм рт. ст. (1,33 кПа).
2PREF_r 2pref_i
M J >-1 >
LD -
(9)
l) Перепад LD вычисляют отдельно для СИСТОЛИЧЕСКОГО И ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ по формуле (9)
где p и PREP L — это ЭТАЛОННОЕ АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ в правой (R) и левой (L)
reF-R' “ I руке соответственно.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.4 2.2* Анализ данных
а) Погрешность ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА х вычисляют методом сложения разницы между значением АРТЕРИАЛЬНОГО ДАВЛЕНИЯ ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА и значением АРТЕРИАЛЬНОГО ДАВЛЕНИЯ ЭТАЛОННОГО СФИГМОМАНОМЕТРА, и перепада LD в соответствии с формулой (10). если значение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА было получено на левой руке, или методом вычитания переда LD в соответствии с формулой (11), если значение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА было получено на правой руке:
х-р -р + LD.
KSUT L ^REF R 1
х - р - р - LD.
^SUT R KREF L
(ID
где pSUT R и pSUT L — АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА на правой (R) руке и левой (L) руке, соответственно.
b) ИСПЫТУЕМЫЙ СФИГМОМАНОМЕТР должен отвечать следующим двум критериям
1) Критерий 1, и
2) Критерий 2.
c) Критерий 1
1) Для СИСТОЛИЧЕСКОГО и ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ средняя разница определения хп для отдельных парных ОПРЕДЕЛЕНИЙ ИСПЫТУЕМЫМ СФИГМОМАНОМЕТРОМ и ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ для всех субъектов должна:
I) по формуле (12) быть в пределах или равна 5.0 мм рт. ст. (±0,67 кПа) со среднеквадратическим отклонением хп\
II) по формуле (13) быть не более 8,0 мм рт. ст. (1,07 кПа) при величине стандартного
отклонения sn:
х
|
1 Л |
(12)
|
п | |
|
$ о | |
(13)
где х(. — погрешность ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА, вычисленная по формулам (10) и
(11);
п — количество ОПРЕДЕЛЕНИЙ;
/' — индекс отдельного элемента.
Пример 1 — п = 510 для СФИГМОМАНОМЕТРОВ. предназначенных для взрослых ПАЦИЕНТОВ или подростков (исследование на 85 субъектах).
Пример 2 — л = 510 для СФИГМОМАНОМЕТРОВ. предназначенных для взрослых ПАЦИЕНТОВ или подростков и детей в возрасте от 3 до 12 лет (исследование на 85 субъектах).
ПримерЗ — л = 210 для СФИГМОМАНОМЕТРОВ. предназначенных (дополнительно) для специального ПРЕДУСМОТРЕННОГО ПРИМЕНЕНИЯ (исследование на 35 субъектах), когда СФИГМОМАНОМЕТР прошел клиническое исследование на 85 субъектах в соответствии с 5.1.1 и 5.2.
d) Критерий 2
1) Для среднего значения СИСТОЛИЧЕСКОГО и ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ для каждого субъекта стандартное отклонение sm усредненного парного ОПРЕДЕЛЕНИЯ для субъекта на ИСПЫТУЕМОМ СФИГМОМАНОМЕТРЕ и ЭТАЛОННОМ СФИГМОМАНОМЕТРЕ, на каждого субъекта, должно отвечать критериям, перечисленным;
I) в таблице 1; или
II) в таблице 2
при вычислении по формуле (14)
где х — среднее значение разницы между всеми субъектами, вычисленное по формуле (12);
п
т — число субъектов;
/ — индекс отдельного элемента;
х( — среднее значение разницы между субъектами, вычисленное по формуле (15)
|
х 1 |
где хк — погрешность ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА для каждого субъекта, вычисленная по формулам (10) и (11);
к — индекс отдельного элемента.
Пример 4 — т = 85 для СФИГМОМАНОМЕТРОВ. предназначенных для взрослых ПАЦИЕНТОВ или подростков (исследование на 85 субъектах).
Пример 5 — т = 85 для СФИГМОМАНОМЕТРОВ. предназначенных для взрослых ПАЦИЕНТОВ или подростков и детей в возрасте от 3 до 12 лет (исследование на 85 субъектах).
Пример в — т = 35 для СФИГМОМАНОМЕТРОВ. предназначенных (дополнительно) для специального ПРЕДУСМОТРЕННОГО ПРИМЕНЕНИЯ (исследование на 35 субъектах), когда СФИГМОМАНОМЕТР прошел КЛИНИЧЕСКОЕ ИСПЫТАНИЕ на отдельных 85 субъектах в соответствии с 5.1.1 и 5.2.
Пример 7 — т = 85 для СФИГМОМАНОМЕТРОВ. предназначенных только для специального ПРЕДУСМОТРЕННОГО ПРИМЕНЕНИЯ (исследование на 85 субъектах).
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.5* Дополнительные требования к СФИГМОМАНОМЕТРАМ, предназначенным для использования в условиях тестов с физической нагрузкой
a) Для СФИГМОМАНОМЕТРОВ. предназначенных для использования в условиях физической нагрузки. должно быть проведено дополнительное КЛИНИЧЕСКОЕ ИСПЫТАНИЕ.
1) Во время этого КЛИНИЧЕСКОГО ИСПЫТАНИЯ субъекты должны подвергаться динамической (аэробной) нагрузке на велоэргометре, чтобы увеличить частоту их сердечных сокращений, как минимум, на 30 % по сравнению с частотой сердечных сокращений состояния покоя.
2) Фиксируют частоту сердечных сокращений в состоянии покоя.
3) Фиксируют частоту сердечных сокращений для каждого ОПРЕДЕЛЕНИЯ.
4) Рука, используемая для снятия ЭТАЛОННЫХ показаний, должна иметь опору.
5) МАНЖЕТА должна находиться на уровне левого желудочка во время снятия ЭТАЛОННОГО показания и ОПРЕДЕЛЕНИЯ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
b) Может быть использован любой из методов КЛИНИЧЕСКОГО ИСПЫТАНИЯ, описанных в 5.2.4.
1) В КЛИНИЧЕСКОМ ИСПЫТАНИИ должно участвовать не менее 35 субъектов.
2) Исследование в условиях физической нагрузки должно быть освобождено от требований 5.1.1, 5.1.3. 5.1.4 и 5.1.5.
3) Не менее 10 % субъектов должны иметь СИСТОЛИЧЕСКОЕ ДАВЛЕНИЕ покоя £140 мм рт. ст. (18.66 кЛа).
4) Нет необходимости оценивать исследования в условиях физической нагрузки с применением критерия 2 в 5.2.4.1.2 или 5.2.4.2.2.
c) Для метода последовательных замеров на той же руке 5.2.4.1 заменяют критерий исключения изменений ЭТАЛОННОГО АРТЕРИАЛЬНОГО ДАВЛЕНИЯ 5.2.4.1.1, п) следующим:
1) Данные по любому субъекту должны быть исключены, если любые два последовательных:
I) показания ЭТАЛОННОГО СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ отличаются более, чем на 8 мм рт. ст. (1.07 кПа): или
II) показания ЭТАЛОННОГО ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ отличаются более, чем на 6 мм рт. ст. (0,80 кПа).
2) Субъект может быть не исключен из процедуры КЛИНИЧЕСКОГО ИСПЫТАНИЯ, а серия ЭТАЛОННЫХ показаний и ОПРЕДЕЛЕНИЙ может быть продолжена.
3) Не обязательно повторять процедуру снятия первоначальных ЭТАЛОННЫХ показаний и ОПРЕДЕЛЕНИЙ в состоянии покоя.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2.6* Дополнительные требования к СФИГМОМАНОМЕТРАМ, предназначенным для использования при амбулаторном наблюдении
а) Для СФИГМОМАНОМЕТРОВ, предназначенных для использования в целях амбулаторного контроля, должно быть проведено дополнительное КЛИНИЧЕСКОЕ ИСПЫТАНИЕ.
1) Во время этого КЛИНИЧЕСКОГО ИСПЫТАНИЯ субъекты должны подвергаться динамической (аэробной) нагрузке на велоэргометре так, чтобы частота их сердечных сокращений увеличилась не менее, чем на 15 % относительно частоты сердечных сокращений состояния покоя.
2) Частота сердечных сокращений состояния покоя должна быть зафиксирована.
3) Частота сердечных сокращений для каждого ОПРЕДЕЛЕНИЯ должна быть зафиксирована.
4) Во время снятия ЭТАЛОННОГО показания и ОПРЕДЕЛЕНИЯ ИСПЫТУЕМОГО СФИГМО-МАНОМЕТРА локоть и предплечье руки должны иметь опору.
5) МАНЖЕТА должна находиться на уровне левого желудочка сердца во время снятия ЭТАЛОННОГО показания и ОПРЕДЕЛЕНИЯ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
b) Любой из методов КЛИНИЧЕСКОГО ИСПЫТАНИЯ, описанный в 5.2.4. может быть применен.
1) КЛИНИЧЕСКОЕ ИСПЫТАНИЕ должно охватывать не менее 35 субъектов.
2) Исследования в рамках амбулаторного наблюдения освобождаются от требований 5.1.1. 5.1.3, 5.1.4 и 5.1.5.
3) Не менее 30 % субъектов должны иметь СИСТОЛИЧЕСКОЕ ДАВЛЕНИЕ >140 мм рт. ст.
(18.66 кПа).
4) Исследования в рамках амбулаторного наблюдения освобождаются от критериев приемлемости 2 5.2.4.1.2 или 5.2 4.2.2.
c) Для метода последовательного замера на той же руке согласно 5.2.4.1 критерий исключения изменений ЭТАЛОННОГО АРТЕРИАЛЬНОГО ДАВЛЕНИЯ 5.2.4.2.1 заменяют на следующее:
1) Данные по субъекту исключаются, если любые два последовательных:
I) показания ЭТАЛОННОГО СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ различаются более, чем на 8 мм рт. ст. (1.07 кПа); или
II) показания ЭТАЛОННОГО ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ различаются более, чем на 6 мм рт. ст. (0.80 кПа).
2) Субъект может быть не исключен из процедуры КЛИНИЧЕСКОГО ИСПЫТАНИЯ, а серия ЭТАЛОННЫХ показаний и ОПРЕДЕЛЕНИЙ может быть продолжена.
3) Не обязательно повторять процедуру снятия первоначальных ЭТАЛОННЫХ показаний и ОПРЕДЕЛЕНИЙ в состоянии покоя.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
6 КЛИНИЧЕСКОЕ ИСПЫТАНИЕ с ЭТАЛОННЫМ ПРИБОРОМ ДЛЯ ИНВАЗИВНОГО МОНИТОРИНГА ДАВЛЕНИЯ КРОВИ
6.1 Требования к субъектам
6.1.1 Количество
a) Любое КЛИНИЧЕСКОЕ ИСПЫТАНИЕ с ЭТАЛОННЫМ ПРИБОРОМ ДЛЯ ИНВАЗИВНОГО МОНИТОРИНГА ДАВЛЕНИЯ КРОВИ должно включать не менее 15 субъектов.
b) Для каждого субъекта должно быть проведено не более 10 достоверных измерений АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
c) При КЛИНИЧЕСКОМ ИСПЫТАНИИ должно быть проведено не менее 150 достоверных измерений АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
6.1.2* Распределение по полу
Измерения должны быть проведены с участием:
a) не менее 30 % субъектов-мужчин, и
b) не менее 30 % субъектов-женщин.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ. 6.1.3* Распределение по оозрастам
6.1.3.1 СФИГМОМАНОМЕТРЫ. предназначенные для использования у взрослых, подростков или
детей
а) Для СФИГМОМАНОМЕТРОВ, предназначенных для взрослых ПАЦИЕНТОВ или ПАЦИЕНТОВ подросткового возраста, возраст ПАЦИЕНТОВ, включенных в исследования, должен быть более 12 лет. Примечание 1 —Всего минимум 15субьектови 150 ОПРЕДЕЛЕНИЙ.
Информация о введении в действие (прекращении действия) настоящего стандарта и uat/e-нений к нему на территории указанных выше государств публикуется в указателях национальных стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных органов по стандартизации.
В случав пересмотра, изменения или отмены настоящего стандарта соответствующая информация будет опубликована на официальном интернет-сайте Межгосударственного совета по стандартизации, метрологии и сертификации в каталоге «Межгосударственные стандарты»
©ISO. 2018 © Оформление. ФГБУ «РСТ», 2021
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
b) Для СФИГМОМАНОМЕТРОВ, дополнительно предназначенных для использования у детей, в КЛИНИЧЕСКОЕ ИСПЫТАНИЕ должны быть дополнительно включены не менее 5 детей в возрасте от 3 до 12 лет.
Примечание 2 — Всего минимум 20 субъектов и 200 ОПРЕДЕЛЕНИЙ.
c) Для СФИГМОМАНОМЕТРОВ, дополнительно предназначенных для использования у детей, должен быть объединен анализ данных {см. 6.2.6) взрослых, подростков и детей.
d) Дети освобождаются от требований к распределению АРТЕРИАЛЬНОГО ДАВЛЕНИЯ по 6.1.5. Соответствие устанавливают путем проверки ЭКСПЛУАТАЦИОННОГО ДОКУМЕНТА и
ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
6.1.3.2 СФИГМОМАНОМЕТР для новорожденных или младенцев
a) СФИГМОМАНОМЕТРЫ, предназначенные для использования у новорожденных, младенцев или детей младше 3 лет. должны быть исследованы на такой выборке ПАЦИЕНТОВ.
b) Для КЛИНИЧЕСКИХ ИСПЫТАНИЙ у новорожденных требуются следующие диапазоны возраста и массы тела:
1) Не менее 3 ПАЦИЕНТОВ должны иметь массу менее 1000 г.
2) Не менее 3 ПАЦИЕНТОВ должны иметь массу от 1000 до 2000 г.
3) Не менее 3 ПАЦИЕНТОВ должны иметь массу более 2000 г.
4) Не менее 3 ПАЦИЕНТОВ должны иметь возраст более 29 дней и менее 1 года.
5) Не менее 3 ПАЦИЕНТОВ должны иметь возраст более 1 года и менее 3 лет.
6) Оставшиеся ПАЦИЕНТЫ могут быть из любой перечисленной выше группы возрастов или массы для того, чтобы достигнуть размера выборки 18 ПАЦИЕНТОВ.
Примечание 1 — Всего минимум 18 ПАЦИЕНТОВ и 180 ОПРЕДЕЛЕНИЙ.
Примечание 2 — ПАЦИЕНТ может одновременно находиться более чем в одной категории.
c) Новорожденные, младенцы и дети возрастом менее 3 лет освобождаются от
1) требований 6.1.5 к распределению АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
2) требований 6.1.2 к распределению по полу, и
3) требований 6.1.4 к распределению по размерам конечностей.
Соответствие устанавливают путем проверки ЭКСПЛУАТАЦИОННОГО ДОКУМЕНТА и ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
6.1.4 Распределение по охвату конечностей
a) охваты конечностей распределяются следующим образом:
1) не менее 20 % испытуемых должны иметь охват конечности, который находится в пределах каждой четверти ПОЛНОГО ДИАПАЗОНА ОХВАТОВ КОНЕЧНОСТЕЙ;
2) не менее 10 % испытуемых должны иметь охват конечности, который находится в пределах наибольшего октиля от ПОЛНОГО ДИАПАЗОНА ОХВАТОВ КОНЕЧНОСТЕЙ; и
3) не менее 10 % испытуемых должны иметь охват конечности, который находится в пределах наименьшего октиля от ПОЛНОГО ДИАПАЗОНА ОХВАТОВ КОНЕЧНОСТЕЙ;
b) кроме того, для СФИГМОМАНОМЕТРА. предназначенного для использования с несколькими размерами МАНЖЕТЫ, каждая манжета должна быть испытана по меньшей мере на Wcuff субъектах согласно формуле (1);
c) ОТЧЕТ О КЛИНИЧЕСКОМ ИСПЫТАНИИ должен содержать установленный диапазон охватов руки каждой МАНЖЕТЫ в сантиметрах (дюймах);
d) ОТЧЕТ О КЛИНИЧЕСКОМ ИСПЫТАНИИ должен содержать графики, показывающие все результаты испытания по охвату руки, где ось У показывает разницу между ИСПЫТУЕМЫМ СФИГМО-МАНОМЕТРОМ и ЭТАЛОННЫМИ ЗНАЧЕНИЯМИ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ, а ось X показывает фактический охват руки испытуемых.
e) На этих графиках также должны быть указаны границы каждой МАНЖЕТЫ с помощью вертикальных линий.
0 Графики должны быть предоставлены для;
1) СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ; и
2) ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
Содержание
1 Область применения..................................................................1
2 Нормативные ссылки..................................................................1
3 Термины и определения................................................................2
4 Общие требования к КЛИНИЧЕСКИМ ИСПЫТАНИЯМ.......................................3
4.1 Методы КЛИНИЧЕСКИХ ИСПЫТАНИЙ.............................................3
4.2 Надлежащая клиническая практика ...............................................3
4.3 Статус предыдущих КЛИНИЧЕСКИХ ИСПЫТАНИЙ...................................3
4.4 Раскрытие сводных данных по КЛИНИЧЕСКИМ ИСПЫТАНИЯМ........................3
5 КЛИНИЧЕСКОЕ ИСПЫТАНИЕ с аускультативным ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ........4
5.1 Требования к субъектам.........................................................4
5.2 Метод КЛИНИЧЕСКОГО ИСПЫТАНИЯ с ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ..........5
6 КЛИНИЧЕСКОЕ ИСПЫТАНИЕ с ЭТАЛОННЫМ ПРИБОРОМ ДЛЯ ИНВАЗИВНОГО
МОНИТОРИНГА ДАВЛЕНИЯ КРОВИ...................................................15
6.1 Требования к субъектам........................................................15
6.2 Методы КЛИНИЧЕСКОГО ИСПЫТАНИЯ с ЭТАЛОННЫМ ПРИБОРОМ
ДЛЯ ИНВАЗИВНОГО МОНИТОРИНГА ДАВЛЕНИЯ КРОВИ...........................17
7* Выборки беременных................................................................21
Приложение А (справочное) Обоснование и руководство.....................................22
Приложение В (справочное) Ссылки на основные принципы..................................29
Приложение С (справочное) Терминология. Алфавитный указатель терминов...................30
Приложение ДА (справочное) Сведения о соответствии ссылочных международных стандартов
межгосударственным стандартам..........................................31
Библиография........................................................................32
Введение
Третье издание (ISO 81060-2:2018) отменяет и заменяет второе издание (ISO 81060-2:2013), которое было технически пересмотрено.
Основные изменения по сравнению с предыдущим изданием следующие:
- метод одновременного определения на одной руке удален:
- добавлен ряд пояснений, а также включены эквивалентные значения в кПа для значений в мм рт. ст.
Измерение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ является важной ПРОЦЕДУРОЙ, которая используется в практической медицине для оценки состояния ПАЦИЕНТА.
АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ выступает в качестве средства контроля скорости введения лекарственных препаратов во время инфузионной терапии, а также средством предупреждения об изменениях состояния ПАЦИЕНТА.
Измерение АРТЕРИАЛЬНОГО ДАВЛЕНИЯ часто является рутинной процедурой во время анестезии. АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ выступает в качестве средства контроля скорости введения лекарственных препаратов во время инфузионной терапии, а также средством предупреждения об изменениях состояния ПАЦИЕНТА.
В настоящем стандарте приняты следующие шрифтовые выделения:
- требования, соответствие которым может быть проверено, и определения — прямой шрифт:
- информационный материал, приведенный вне таблиц (примечания, примеры и справочная информация). а также нормативный текст таблиц — шрифт уменьшенного размера;
- методы испытании — курсив;
- ТЕРМИНЫ. ОПРЕДЕЛЕННЫЕ В РАЗДЕЛЕ 3 ОБЩЕГО СТАНДАРТА И В НАСТОЯЩЕМ СТАНДАРТЕ — ЗАГЛАВНЫЕ БУКВЫ.
В настоящем стандарте союз «или» будет использован как включающее «или», т. е. утверждение будет истинным при любой комбинации условий.
Глагольные формы, используемые в настоящем стандарте, совпадают по форме с описанными в приложении Н Директив ИСО/МЭК (часть 2).
Значение вспомогательных глаголов:
- «должен» — соответствие требованиям или испытаниям обязательно для соответствия настоящему стандарту;
- «следует» — соответствие требованиям или испытаниям рекомендовано, но не обязательно для соответствия настоящему стандарту;
- «может» —описание допустимых путей достижения соответствия требованиям или испытаниям.
Знак звездочки (*) у номера пункта или подпункта раздела, или заголовка таблицы указывает, что
в приложении А приведены соответствующие пояснения.
В приложении В приведена схема соответствия пунктов и подпунктов настоящего стандарта ОСНОВНЫМ ПРИНЦИПАМ ISO 16142-1:2016.
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
СФИГМОМАНОМЕТРЫ (ИЗМЕРИТЕЛИ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ) НЕИНВАЗИВНЫЕ
Часть 2
Клинически© испытания моделей с автоматическим типом измерения
Non-invasive sphygmomanometers (measuring devices of arterial pressure).
Part 2. Clinical investigation of intermittent automated measurement type
Дата введения — 2022—03—01
1 Область применения
Настоящий стандарт устанавливает требования и методы для КЛИНИЧЕСКОГО ИСПЫТАНИЯ ME ИЗДЕЛИЯ, используемого для ПЕРИОДИЧЕСКОЙ неинвазивной автоматической оценки АРТЕРИАЛЬНОГО ДАВЛЕНИЯ с использованием МАНЖЕТЫ.
Настоящий стандарт применим ко всем СФИГМОМАНОМЕТРАМ, которые воспринимают или отображают пульсации, поток или звуки для оценки, отображения или записи АРТЕРИАЛЬНОГО ДАВЛЕНИЯ. Для этих СФИГМОМАНОМЕТРОВ не требуется автоматическая накачка МАНЖЕТЫ.
Настоящий стандарт распространяется на СФИГМОМАНОМЕТРЫ. предназначенные для использования у всех групп ПАЦИЕНТОВ (например, всех возрастов и весовых категорий), и при всех условиях использования (например, амбулаторный мониторинг АРТЕРИАЛЬНОГО ДАВЛЕНИЯ, мониторинг АРТЕРИАЛЬНОГО ДАВЛЕНИЯ с нагрузкой и мониторинг АРТЕРИАЛЬНОГО ДАВЛЕНИЯ в условиях ЛЕЧЕНИЯ НА ДОМУ для самоконтроля, а также для использования в медицинской организации).
Пример — АВТОМАТИЧЕСКИЕ СФИГМОМАНОМЕТРЫ в соответствии с IEC 80601-2-30 подвергаются КЛИНИЧЕСКИМ ИСПЫТАНИЯМ согласно настоящему стандарту.
Настоящий стандарт устанавливает дополнительные требования к ЭКСПЛУАТАЦИОННЫМ ДОКУМЕНТАМ на СФИГМОМАНОМЕТРЫ, прошедшие процедуру КЛИНИЧЕСКОГО ИСПЫТАНИЯ в соответствии с настоящим стандартом.
Настоящий стандарт не применим к КЛИНИЧЕСКИМ ИСПЫТАНИЯМ НЕАВТОМАТИЧЕСКИХ СФИГМОМАНОМЕТРОВ. соответствующих ISO 81060-1. или ПРИБОРОВ ДЛЯ ИНВАЗИВНОГО МОНИТОРИНГА ДАВЛЕНИЯ КРОВИ, соответствующих IEC 60601-2-34.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие стандарты (для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных — последнее издание (включая все изменения)):
Примечание 1 — Способ, при помощи которого указанные ссылочные стандарты приведены в тексте нормативных требований, определяет степень их применения (полностью или частично).
Примечание 2 — Справочные ссылки приведены в разделе «Библиография».
Издание официальное
ISO 14155:2011’*, Clinical investigation of medical devices for human subjects — Good clinical practice (Клинические исследования медицинских изделий для людей. Надлежащая клиническая практика)
ISO 14971:2007. Medical devices — Application of risk management to medical devices21 (Изделия медицинские. Применение менеджмента риска к медицинским изделиям)
ISO 16142-1:2016. Medical devices — Recognized essential pnnciples of safety and performance of medical devices — Part 1: General essential principles and additional specific essential principles for all non-IVD medical devices and guidance on the selection of standards (Изделия медицинские. Важнейшие принципы обеспечения безопасности и эксплуатационных характеристик медицинских изделий. Часть 1. Общие и дополнительные специфические важнейшие принципы для всех медицинских изделий, кроме изделий для диагностики in vitro, и руководство по выбору стандартов)
ISO 81060-1:2007, Non-invasive sphygmomanometers — Part 1: Requirements and test methods for non-automated measurement type (Сфигмоманометры неинвазивные. Часть 1. Требования и методы испытания моделей с неавтоматическим типом измерения)
IEC 60601-1:2005*Amendment 1:2012. Medical electrical equipment — Part 1: General requirements for basic safety and essential performance (Изделия медицинские электрические. Часть 1. Обшие требования безопасности с учетом основных функциональных характеристик)
IEC 60601-1-11:2015, Medical electrical equipment — Part 1-11: General requirements for basic safety and essential performance — Collateral Standard: Requirements for medical electrical equipment and medical electrical systems used in the home healthcare environment (Изделия медицинские электрические. Часть 1-11. Общие требования безопасности с учетом основных функциональных характеристик. Дополнительный стандарт. Требования к медицинским изделиям и системам, используемым для ухода за больными в домашней среде)
IEC 60601-2-34:2011, Medical electrical equipment — Part 2-34: Particular requirements for the basic safety and essential performance of invasive blood pressure monitoring equipment (Изделия медицинские электрические. Часть 2-34. Частные требования безопасности с учетом основных функциональных характеристик к приборам для инвазивного мониторинга кровяного давления)
IEC 80601-2-30:2018. Medical electrical equipment — Part 2-30: Particular requirements for the basic safety and essential performance of automated non-invasive sphygmomanometers (Изделия медицинские электрические. Часть 2-30. Частные требования безопасности с учетом основных функциональных характеристик к автоматическим неинвазивным сфигмоманомстрам)
3 Термины и определения
В настоящем стандарте применены термины по ISO 14155:2011, ISO 14971:2007, ISO 16142-1:2016. ISO 81060-1:2007. IEC 60601-1:2005+AMD1:2012, IEC 60601-1-11:2015, IEC 60601-2-34:2011 и IEC 80601-2-30:2018. а также следующие термины с соответствующими определениями.
Примечание — Для удобства в приложении С приведен алфавитный указатель терминов, используемых в настоящем стандарте.
3.1 периодический (intermittent): Неинвазивный СФИГМОМАНОМЕТР. использующий ПРОЦЕСС оценки АРТЕРИАЛЬНОГО ДАВЛЕНИЯ, обеспечивающий единственный набор значений давления на основании некоторого числа циклов активности сердца.
3.2 эталонный; ЭТ (reference, ref): С установленной точностью, используемый для КЛИНИЧЕСКИХ ИСПЫТАНИЙ других приборов.
3.3 сфигмоманометр (sphygmomanometer): ME ИЗДЕЛИЕ для неинвазивной оценки системного АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
Л Заменен на ISO 14155:2020. Clinical investigation of medical devices for human subjects. Good clinical practice (Клинические исследования медицинских изделий для людей. Надлежащая клиническая практика). Однако для однозначного соблюдения требований настоящего стандарта, выраженного в датированной ссылке, рекомендуется использовать только указанное в этой ссылке издание.
2) Заменен на ISO 14971:2019. Medical devices Application of risk management to medical devices (Изделия медицинские. Применение менеджмента риска к медицинским изделиям). Однако для однозначного соблюдения требований настоящего стандарта, выраженного в датированной ссылке, рекомендуется использовать только указанное в этой ссылке издание.
3.4 испытуемый сфигмоманометр; ИС (sphygmomanometer-under-test, sut): АВТОМАТИЧЕСКИЙ СФИГМОМАНОМЕТР, проходящий КЛИНИЧЕСКОЕ ИСПЫТАНИЕ.
3.5 полный диапазон охватов конечностей (total limb circumference range): диапазон от наименьшего охвата конечности до наибольшего охвата конечности, предназначенный ИЗГОТОВИТЕЛЕМ для использования с АВТОМАТИЧЕСКИМ СФИГМОМАНОМЕТРОМ.
4 Общие требования к КЛИНИЧЕСКИМ ИСПЫТАНИЯМ
4.1 Методы КЛИНИЧЕСКИХ ИСПЫТАНИЙ
a) АВТОМАТИЧЕСКИЕ СФИГМОМАНОМЕТРЫ должны подвергаться КЛИНИЧЕСКИМ ИСПЫТАНИЯМ в соответствии с настоящим стандартом в каждом режиме эксплуатации с применением одного из следующих:
1) неинвазивного (аускультативного) ЭТАЛОННОГО СФИГМОМАНОМЕТРА. применяемого на плече; либо
2) ЭТАЛОННОГО ПРИБОРА ДЛЯ ИНВАЗИВНОГО МОНИТОРИНГА ДАВЛЕНИЯ КРОВИ.
Пример 1 — Режим для взрослых и новорожденных.
Пример 2 — Режим быстрого и медленного стравливания воздуха из МАНЖЕТЫ.
b) КЛИНИЧЕСКОЕ ИСПЫТАНИЕ считается ТИПОВЫМ ИСПЫТАНИЕМ.
c) Для клинического испытания автоматического сфигмоманометра. предназначенного для отображения значений центрального или внутриаортального давления, необходимо пользоваться справочным сайтом инвазивного измерения центрального или внутриаортального давления (см. 6.2.2).
Примечание — Такой автоматический СФИГМОМАНОМЕТР подвергают испытаниям в соответствии с требованиями раздела 6.
Соответствие требованиям настоящего подпункта считается достигнутым, если соблюдены критерии соответствующих проверок и испытаний настоящего стандарта.
4.2 Надлежащая клиническая практика
a) все КЛИНИЧЕСКИЕ ИСПЫТАНИЯ должны соответствовать требованиям ISO 14155:2011;
b) КЛИНИЧЕСКОЕ ИСПЫТАНИЕ ЭТАЛОННЫМ ПРИБОРОМ ДЛЯ ИНВАЗИВНОГО МОНИТОРИНГА ДАВЛЕНИЯ КРОВИ не следует проводить с участием ПАЦИЕНТОВ или добровольцев лишь в целях оценки функциональных характеристик СФИГМОМАНОМЕТРА.
Примечание — Некоторые полномочные органы имеют дополнительные требования:
c) приоритет имеют требования настоящего стандарта, которые в большей степени конкретизированы. чем соответствующие требования ISO 14155:2011.
Соответствие проверяют путем применения требований ISO 14155:2011.
4.3 Статус предыдущих КЛИНИЧЕСКИХ ИСПЫТАНИЙ
Результаты КЛИНИЧЕСКИХ ИСПЫТАНИЙ СФИГМОМАНОМЕТРОВ. успешно прошедших клиническую оценку в соответствии с требованиями предыдущих версий настоящего стандарта, остаются действительными, поэтому для обеспечения соответствия требованиям настоящего стандарта нет необходимости проводить никакие другие КЛИНИЧЕСКИЕ ИСПЫТАНИЯ.
4.4 Раскрытие сводных данных по КЛИНИЧЕСКИМ ИСПЫТАНИЯМ
Техническое описание СФИГМОМАНОМЕТРА должно включать контактную информацию, позволяющую ОТВЕТСТВЕННОЙ ОРГАНИЗАЦИИ получить копию данных по проведенным КЛИНИЧЕСКИМ ИСПЫТАНИЯМ.
5 КЛИНИЧЕСКОЕ ИСПЫТАНИЕ с аускультативным ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ
5.1 Требования к субъектам
5.1.1* Количество
a) КЛИНИЧЕСКОЕ ИСПЫТАНИЕ с аускультативным ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ должно состоять из. как минимум. 85 субъектов.
b) Если не установлено иное требование, то для каждого субъекта должно быть получено не менее трех достоверных значений АРТЕРИАЛЬНОГО ДАВЛЕНИЯ [см. 5.2.4.1.1. о)].
c) Должно быть получено, как минимум, 255 достоверных значений АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.1.2* Распределение по полу
a) Не менее 30 % субъектов должны быть мужчинами.
b) Не менее 30 % субъектов должны быть женщинами.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.1.3* Распределение по возрасту
a) Для СФИГМОМАНОМЕТРОВ, предназначенных для взрослых ПАЦИЕНТОВ или ПАЦИЕНТОВ подросткового возраста, возраст всех субъектов, включенных в КЛИНИЧЕСКОЕ ИСПЫТАНИЕ, должен быть старше 12 лет.
Примечание 1 — Всего минимум 85 субъектов.
b) Для СФИГМОМАНОМЕТРОВ, дополнительно предназначенных для использования у детей, в КЛИНИЧЕСКИЕ ИСПЫТАНИЯ должны быть включены 35 субъектов-детей в возрасте от 3 до 12 лет.
Примечание 2 — Всего минимум 85 субъектов (35 детей в возрасте от 3 до 12 лет, и 50 субъектов старше 12 лет).
c) Если СФИГМОМАНОМЕТР имеет специальный режим для детей, то в этом режиме дети считаются специальной выборкой ПАЦИЕНТОВ (см. 5.1.6). В данном исследовании дети освобождаются от требований 5.1.5 по распределению АРТЕРИАЛЬНОГО ДАВЛЕНИЯ.
d) Детей в возрасте менее 3 лет не следует включать в КЛИНИЧЕСКИЕ ИСПЫТАНИЯ с применением аускультативных ЭТАЛОННЫХ показаний наблюдателями, использующими ЭТАЛОННЫЙ СФИГМОМАНОМЕТР
Соответствие устанавливают путем проверки ЭКСПЛУАТАЦИОННОГО ДОКУМЕНТА и ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.1.4’ Распределение по размерам конечностей
a) Охваты конечностей должны быть распределены следующим образом:
1) не менее 20 % испытуемых должны иметь охват конечности, который находится в пределах каждой четверти ПОЛНОГО ДИАПАЗОНА ОХВАТОВ КОНЕЧНОСТЕЙ;
2) не менее 10 % испытуемых должны иметь охват конечности, который находится в пределах наибольшего октиля от ПОЛНОГО ДИАПАЗОНА ОХВАТОВ КОНЕЧНОСТЕЙ: и
3) не менее 10 % испытуемых должны иметь охват конечности, который находится в пределах наименьшего октиля от ПОЛНОГО ДИАПАЗОНА ОХВАТОВ КОНЕЧНОСТЕЙ.
b) Кроме того, для СФИГМОМАНОМЕТРА. предназначенного для использования с несколькими размерами МАНЖЕТЫ, каждая манжета должна быть испытана по меньшей мере на Ncuff субъектах согласно формуле (1)
N
cuff
Г ^
где
'cuff
'total
2-r total total
общее количество испытуемых в исследовании;
размер диапазона охватов конечностей для индивидуальной манжеты;
размер ПОЛНОГО ДИАПАЗОНА ОХВАТОВ КОНЕЧНОСТЕЙ.
c) ОТЧЕТ О КЛИНИЧЕСКОМ ИСПЫТАНИИ должен содержать установленный диапазон охватов руки каждой МАНЖЕТЫ в сантиметрах (дюймах).
d) ОТЧЕТ О КЛИНИЧЕСКОМ ИСПЫТАНИИ должен содержать графики, показывающие все результаты испытания по охвату руки, где ось У показывает разницу между ИСПЫТУЕМЫМ СФИГМО-МАНОМЕТРОМ и ЭТАЛОННЫМИ ЗНАЧЕНИЯМИ АРТЕРИАЛЬНОГО ДАВЛЕНИЯ, а ось X показывает фактический охват руки испытуемых.
e) На этих графиках также должны быть указаны границы каждой МАНЖЕТЫ с помощью вертикальных линий.
f) Графики должны быть предоставлены для:
1) СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ; и
2) ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ.
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.1.5 Распределение значений давления крови
a) Не менее 5 % показаний должны соответствовать значению СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ S 100 мм рт. ст. (13,33 кПа).
b) Не менее 5 % показаний должны соответствовать значению СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ г 160 мм рт. ст. (21,33 кПа).
c) Не менее 20 % показаний должны соответствовать значению СИСТОЛИЧЕСКОГО ДАВЛЕНИЯ г 140 мм рт. ст. (18,66 кПа).
d) Не менее 5 % показаний должны соответствовать значению ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ S 60 мм рт. ст. (8.0 кЛа).
e) Не менее 5 % показаний должны соответствовать значению ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ г 100 мм рт. ст. (13,33 кПа).
0 Не менее 20 % показаний должны соответствовать значению ДИАСТОЛИЧЕСКОГО ДАВЛЕНИЯ г 85 мм рт. ст. (11,33 кПа).
Соответствие устанавливают путем проверки ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.1.6* Специальные выборки ПАЦИЕНТОВ
a) СФИГМОМАНОМЕТРЫ. предназначенные для использования в специальных выборках ПАЦИЕНТОВ. если существуют ОБЪЕКТИВНЫЕ СВИДЕТЕЛЬСТВА, что точность СФИГМОМАНОМЕТРА может быть проблематичной в этих выборках ПАЦИЕНТОВ, должны подвергаться КЛИНИЧЕСКОМУ ИСПЫТАНИЮ в этих выборках ПАЦИЕНТОВ.
Примечание — В разделе 7 приведен конкретный пример специальной выборки ПАЦИЕНТОВ, к которым применяют особые требования.
b) Если СФИГМОМАНОМЕТРЫ прошли КЛИНИЧЕСКОЕ ИСПЫТАНИЕ в соответствии с требованиями 5.1.1 и 5.2. они должны быть затем КЛИНИЧЕСКИ ИСПЫТАНЫ не менее чем на 35 дополнительных субъектах специальной выборки.
c) Если СФИГМОМАНОМЕТР не прошел успешно КЛИНИЧЕСКОЕ ИСПЫТАНИЕ в соответствии с требованиями 5.1.1 и 5.2, то КЛИНИЧЕСКОЕ ИСПЫТАНИЕ в соответствии с требованиями 5.1.1 и 5.2 должно состоять только из субъектов из специальной выборки.
d) Термины, определяющие специальную выборку ПАЦИЕНТОВ, должны быть четкими и отражать следующие параметры:
1) пол (см. 5.1.2);
2) возраст (см. 5.1.3);
3) охват конечности (см. 5.1.4); и
4) АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ (см. 5.1.5).
e) Краткое определение специальной выборки ПАЦИЕНТОВ приводится в инструкции по эксплуатации.
Соотвепктвие устанавливают путем проверки инструкции по эксплуатации и ОТЧЕТА О КЛИНИЧЕСКИХ ИСПЫТАНИЯХ.
5.2 Метод КЛИНИЧЕСКОГО ИСПЫТАНИЯ с ЭТАЛОННЫМ СФИГМОМАНОМЕТРОМ
5.2.1* Подготовка субъекта
а) Если в инструкции по эксплуатации ИСПЫТУЕМОГО СФИГМОМАНОМЕТРА не указано иное требование, субъект располагают так. чтобы он: