ГОСТ EN 15791-2015
Корма. Определение дезоксиниваленола методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с очисткой на иммуноаффинной колонке
Купить ГОСТ EN 15791-2015 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на метод определения дезоксиниваленола в комбикормах при концентрациях от 150 до 4000 мкг/кг.
Идентичен EN 15791:2009
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Реактивы
5 Оборудование
6 Методика проведения испытания
7 Определение методом ВЭЖХ
8 Обработка результатов
9 Прецизионность
10 Протокол испытаний
Приложение А (справочное) данные по прецизионности
Приложение В (справочное) Хроматограммы
Приложение ДА (справочное) Сведения о соответствии ссылочного европейского стандарта межгосударственному стандарту
Библиография
| Дата введения | 01.07.2017 |
|---|---|
| Добавлен в базу | 01.02.2017 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел Электроэнергия
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
- Раздел 65.120 Корма для животных
- Раздел 65 СЕЛЬСКОЕ ХОЗЯЙСТВО
Организации:
| 27.02.2015 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 75-П |
|---|---|---|---|
| 30.08.2016 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 970-ст |
| Разработан | БелГИСС | ||
| Издан | Стандартинформ | 2016 г. |
Animal feed. Determination of deoxynivalenolby high performance liquid chromatographic (HPLC) method with immunoaffinity column clean-up
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1
стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9
стр. 10
стр. 11
стр. 12

стр. 13

стр. 14

стр. 15
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
ГОСТ
EN 15791— 2015
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
КОРМАОпределение дезоксиниваленола методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с очисткой на иммуноаффинной колонке
(EN 15791:2009 Foodstuffs - Determination of Deoxynivalenol in animal feed -HPLC method with immunoaffinity column clean-up, IDT)
Издание официальное
Москва
Стандартинформ
2016
fOCTEN 15791—2015
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Научно-производственным республиканским унитарным предприятием «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) на основе собственного перевода на русский язык англоязычной версии европейского стандарта, указанного в пункте 5
2 ВНЕСЕН Государственным комитетом по стандартизации Республики Беларусь
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 27 февраля 2015 г. № 75-П)
|
За принятие стандарта проголосовали: | ||||||||||||||||||||||||
|
4 Приказом Федерального агентства по техническому регулированию и метрологии от 30 августа 2016 г. № 970-ст межгосударственный стандарт ГОСТ EN 15791—2015 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2017 г.
5 Настоящий стандарт идентичен европейскому стандарту EN 15791:2009 «Продукция пищевая. Определение дезоксиниваленола в кормах для животных. Метод ВЭЖХ с очисткой на иммуноаф-финной колонке» («Foodstuffs — Determination of Deoxynivalenol in animal feed — HPLC method with immunoaffinity column clean-up». IDT).
Европейский стандарт разработан Техническим комитетом по стандартизации CEN/TC 327 «Корма» Европейского комитета по стандартизации (CEN).
В разделе «Нормативные ссылки» и тексте стандарта ссылки на европейский стандарт актуализированы.
Наименование настоящего стандарта изменено относительно наименования указанного европейского стандарта для приведения в соответствие с ГОСТ 1.5 (подраздел 3.6).
При применении настоящего стандарта рекомендуется использовать вместо ссылочного европейского стандарта соответствующий ему межгосударственный стандарт, сведения о котором приведены в дополнительном приложении ДА
6 ВВЕДЕН ВПЕРВЫЕ
|
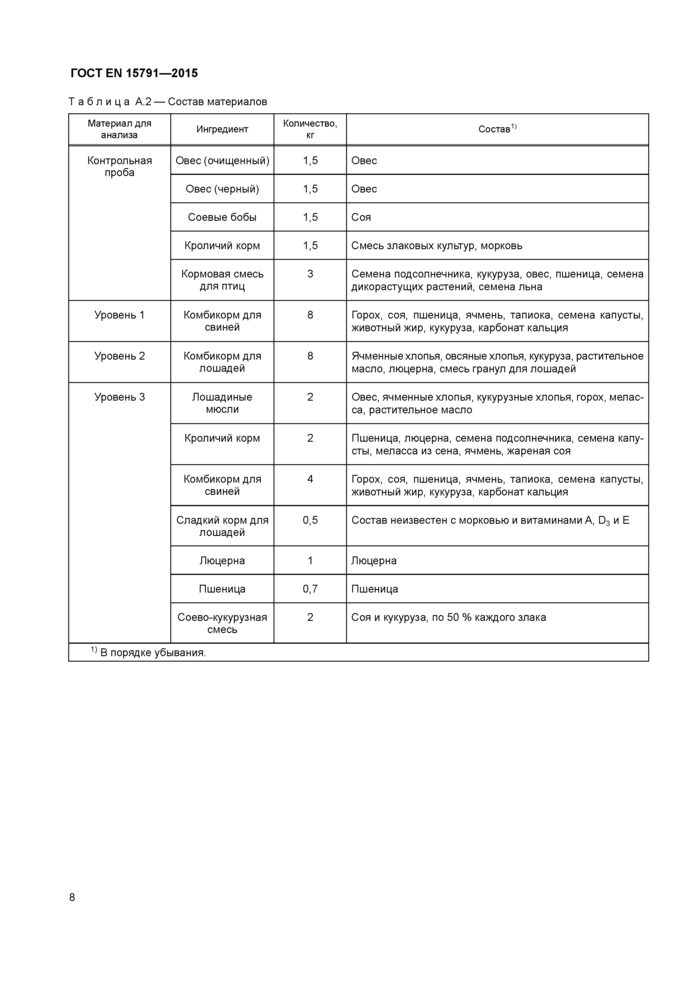
T аблица А2 — Состав материалов | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
8
rOCTEN 15791—2015
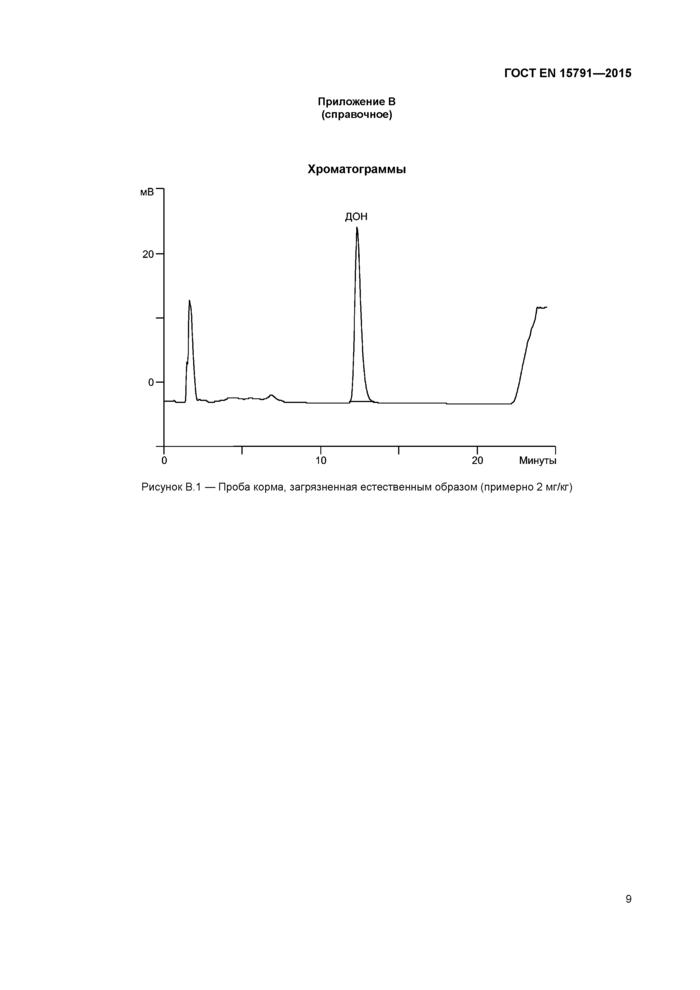
Приложение В (справочное)
|
Хроматограммы |
9
Приложение ДА (справочное)
Сведения о соответствии ссылочного европейского стандарта межгосударственному стандарту
|
Таблица ДА. 1 | |||||||||
| |||||||||
10
rOCTEN 15791—2015
Библиография
(1) Krska, R , et aL, Determination of molar absorptivity coefficients for major type В tnchothecenes and certification of calibrators for deoxymvalenol and nivalenol Anal Bioanal Chem, 2007 388 (5-6): p 1215-1226 (Определение молярных коэффициентов поглощения для основных трихоцетинов типа В и сертификация калибраторов дезоксиниваленола и ниваленола)
(2) ЕС. Commission Regulation (ЕС) No 401/2006 of 23 February 2006 laying down the methods of sampling and analysis for the official control of the levels of mycotoxins in foodstuffs Official Journal of the European Union. 2006 49 (L70): p 12-34
(Регламент Комиссии от 23 февраля 2006 г, устанавливающий методы отбора проб и методы анализа для официального контроля микотоксинов в пищевых продуктах)
(3) Stroka, J.. et al.. Liquid Chromatographic Determination of Deoxymvalenol in Baby Food and Animal Feed Interlaboratory Study J AOAC Int, 2006 89 (4) p 1012-1020
(Определение дезоксиниваленола в пищевых продуктах для детей и кормах для животных методом жидкостной хроматографии Межлабораторное исследование)
(4) AOAC International 1995, AOAC Official Methods Program, р 23-51 (Программа официальных методов АОАС)
11
УДК 636.085:543.544.5:006.35 МКС 65.120 IDT
Ключевые слова: корма, градуировочная кривая, рабочий раствор ДОН. высокоэффективная жидкостная хроматография
Редактор Н Н Мигуиова Технический редактор В Ю Фотиева Корректор М В Бучная Компьютерная верстка А С. Тырюышного
Сдано в набор 02 09 2016 Подписано в печать 07 09 2016 Формат 60 * 84 Vt Гарнитура Ариал Уел. печ л. 1.86 Уч -мзд л. 1.40 Тираж 33 экэ Зак 2111.
Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Издано и отпечатано во ФГУП «СТАНДАРТИНФОРМ». 123995 Москва, Гранатный пер . 4 www gostmfo ni infoQgostinfo ги
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок—в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.ru)
© Стандартинформ. 2016
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен. тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
КОРМА
Определение дезоксиниваленола методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с очисткой на иммуноаффинной колонке
Animal feed
Determination of deoxynivalenolby high performance liquid chromatographic (HPLC) method with immunoaffinity column clean-up
Дата введения — 2017—07—01
1 Область применения
Настоящий стандарт распространяется на метод определения дезоксиниваленола (ДОН) в комбикормах при концентрациях от 150 до 4000 мкг/кг.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на межгосударственные стандарты, которые являются обязательными. Для датированных ссылок применяют только указанное издание. Для недатированных ссылок применяют последнее издание ссылочного стандарта (включая все его изменения).
EN ISO 3696:1995 Water for analytical laboratory use. Specification and test methods (Вода для лабораторного анализа. Технические требования и методы испытаний)
3 Сущность метода
Дезоксиниваленол (ДОН) экстрагируют из продукта, используя воду. Затем водный экстракт очищают на иммуноаффинной колонке, чтобы удалить примеси из пробы. Затем ДОН количественно определяют методом ВЭЖХ с ультрафиолетовым детектором.
4 Реактивы
Для проведения анализа, если не указано иное, используют только реактивы признанной аналитической чистоты и воду не ниже первой степени чистоты no EN ISO 3696. Качество растворителей должно соответствовать требованиям растворителей для ВЭЖХ.
4.1 Ацетонитрил
ПРЕДУПРЕЖДЕНИЕ — Ацетонитрил опасен, поэтому работать с ним необходимо в вытяжном шкафу. Необходимо использовать средства индивидуальной защиты (лабораторный халат, очки, перчатки).
4.2 Дезоксиниваленол (ДОН), чистотой не менее 97 %
ПРЕДУПРЕЖДЕНИЕ — Дезоксиниваленол высокотоксичен. Все время необходимо носить перчатки и очки, а все работы по подготовке пробы и стандартного образца необходимо выполнять в вытяжном шкафу.
4.3 Метанол
ПРЕДУПРЕЖДЕНИЕ — Метанол опасен, поэтому работать с ним необходимо в вытяжном шкафу. Необходимо использовать средства индивидуальной защиты (лабораторный халат, очки, перчатки).
Издание официальное
4.4 Ледяная уксусная кислота
ПРЕДУПРЕЖДЕНИЕ — Ледяная уксусная кислота опасна, поэтому работать с ней необходимо в вытяжном шкафу. Необходимо носить соответствующие средства защиты (лабораторный халат, очки, перчатки).
4.5 Подвижная фаза
Смешивают 15 объемных частей метанола (4.3) с 84.9 объемной части воды и 0.1 объемной части ледяной уксусной кислоты (4.4). Точное количество используемого метанола и необходимость использования уксусной кислоты зависят от выбранной для анализа ВЭЖХ колонки. При необходимости регулируют количество метанола. Дегазируют раствор перед его применением.
4.6 Промывной растворитель
Смешивают 50 объемных частей метанола (4.3) с 50 объемными частями воды.
4.7 Исходный раствор ДОН
Раствор содержит 250 мкг дезоксиниваленола на 1 см3 ацетонитрила.
Раствор можно приготовить следующим образом: добавляют 4.0 мл ацетонитрила (4,1) в 5 мг ДОН (4.2) для получения раствора с концентрацией 1,25 т/см3. Разбавляют 1000 мкл раствора с концентрацией 1.25 мг/ см3 до 5 см3 ацетонитрилом для получения исходного раствора с концентрацией 250 мкг/см3. Разбавляют 200 мкл исходного раствора с концентрацией 250 мкг/см3 в мерной колбе вместимостью 2.0 см3 (5.11) ацетонитрилом, чтобы получить разбавленный исходный раствор с концентрацией 25 мкг/ см3.
Для того чтобы определить точную концентрацию, измеряют значения оптической плотности данного разбавленного исходного раствора с концентрацией 25 мкг/см3 при помощи спектрофотометра (5.15) в диапазоне 200—270 нм в кварцевой кювете с оптической длиной пути 1 см. а в качестве эталона используют ацетонитрил (4.1). Измеряют оптическую плотность при 220 нм. Рассчитывают массовую концентрацию дезоксиниваленола рдон, мкг/см3, по формуле
, А,,,. М 100
Рдон (25 мкг/см3) =-j-j-, (1)
где —оптическая плотность, измеренная при максимальном значении на кривой оптической плотности (220 нм);
М— молярная масса дезоксиниваленола (М = 296,3 г/моль):
к— молярный коэффициент поглощения дезоксиниваленола в ацетонитриле (4.1),
(681.0 ±12.6) м2/моль) ((1]): d— оптическая длина пути кварцевой кюветы, см (1 см).
Рассчитывают точную концентрацию исходного раствора с концентрацией 250 мкг/мл по следующей формуле
Рдон (250 мкг/см3) = рдон (25 мкг/см3 -10). (2)
Исходный раствор хранят в темном месте не более 3 мес при температуре 4 °С — 8 °С или не более 6 мес при температуре ниже минус 18 °С.
Примечание — Приготовление исходного раствора можно выполнять гравиметрически, при этом точно взвешивают стандартный образец ДОН и растворитель, используемый для его растворения
4.8 Раствор для обогащения дезоксиниваленолом
Пипеткой переносят аликвоту исходного раствора ДОН (4.7), эквивалентную 500 мкг ДОН. в мерную колбу вместимостью 5 см3 (5.11). Объем содержимого в колбе доводят до метки ацетонитрилом (4.1). Получают обогащающий раствор с концентрацией 100 мкг/см3.
4.9 Рабочий раствор ДОН
Пипеткой переносят аликвоту разбавленного исходного раствора ДОН (4 7). эквивалентную 50 мкг ДОН. в мерную колбу вместимостью 5 см3 (5.11). Объем содержимого в колбе доводят до метки ацетонитрилом (4.1). Получают рабочий раствор ДОН с концентрацией 10 мкг/см3.
rOCTEN 15791—2015
4.10 Градуировочные растворы ДОН
Градуировочные растворы готовят из рабочего раствора с концентрацией ДОН 10 мкг/см3 (4.9). Добавляют объемы рабочего раствора с концентрацией ДОН 10 мкг/см3 (4.9). приведенные в таблице 1. в мерные колбы вместимостью 10 см3 (5.11). Объем содержимого в колбах доводят до метки подвижной фазой (4.5). Допускаются отклонения, поскольку самый низкий уровень выше предела детектирования, самый высокий уровень не ведет к насыщению сигнала детектора, и существует еще не менее двух уровней, равноудаленных друг от друга.
|
Таблица 1 — Приготовление стандартных растворов | |||||||||||||||||||||
|
4.11 Иммуноаффинные колонки для очистки ДОН
Иммуноаффинная колонка (IA) содержит антитела для дезоксиниваленола. Вместимость колонки должна быть не менее 2500 нг ДОН и обеспечивать степень извлечения не менее 70 % при использовании 25 нг ДОН в 1-2 см3 воды (в зависимости от инструкций изготовителя).
5 Оборудование
Используют стандартное лабораторное оборудование, в том числе перечисленное ниже.
5.1 Аналитические весы с ценой деления d - 0,001 г для взвешивания пробы, с ценой деления d = 0,01 мг для гравиметрического приготовления исходного раствора ДОН (4.7).
5.2 Гомогенизатор/высокоскоростной блендер.
5.3 Лабораторный встряхиватель.
5.4 Вихревой миксер или эквивалентный прибор.
5.5 Измельчитель (разные сита).
5.6 Барабанный смеситель.
5.7 Колбы с резьбовыми крышками вместимостью 250, 500 см3.
5.8 Воронки надлежащего размера.
5.9 Фильтр целлюлозный, с размером поры примерно 30 мкм.
5.10 Фильтр из стеклянного микроволокна без связующих веществ, с размером пор около 2 мкм.
5.11 Мерные колбы вместимостью 2, 5,10 см3.
5.12 Градуированные пипетки вместимостью 1,5 см3.
5.13 Дозаторы пипеточные переменного объема или газонепроницаемые стеклянные шприцы
вместимостью 100.1000 мкл.
5.14 Система ВЭЖХ
5.14.1 Насос бинарный без пульсаций, с расходом, подходящим для аналитической колонки.
5.14.2 Аналитические колонки
Любая колонка, которая обеспечивает достаточное разделение дезоксиниваленола от других интерферирующих компонентов. Примерами являются Phenomenex ODS3-Prodigy (внутренний диаметр 150 х 4.6 мм), размер частиц 5 мкм. размер поры 100 A: Octadecylsilane (ODS), внутренний диаметр 250 х 4.6 мм. размер частиц 3 мкм. размер поры 80 A; Octadecyl (С18) внутренний диаметр 250 * 4.6 мм. размер частиц 5 мкм. размер поры 180 А.
5.14.3 Предколонка (на усмотрение пользователей настоящего стандарта), подходящая для используемой аналитической колонки.
5.14.4 Автодозатор, позволяющий вводить необходимые объемы при достаточной повторяемости.
5.14.5 Ультрафиолетовый детектор, позволяющий измерять при длине волны 220 нм.
5.14.6 Система сбора данных.
fOCTEN 15791—2015
5.15 Ультрафиолетовый спектрофотометр для проверки концентрации исходного раствора ДОН (4.7).
5.16 Емкости соответствующего размера с приспособлением для соединения с иммуноаффинными колонками.
5.17 Стеклянные виалы соответствующего размера для автодозатора (5.14.4). вместимостью не менее 2.0 см3.
5.18 Шприцевой фильтр, полиамид (нейлон), размер пор — 0.45 мкм.
5.19 Испаритель, способный поддерживать температуру 50 °С при постоянном потоке воздуха или азота.
6 Методика проведения испытания
6.1 Подготовка пробы
Важно, чтобы лаборатория получала пробу, которая действительно является представительной и не была повреждена или заменена во время транспортирования или хранения. Пробы отбирают и подготавливают в установленном порядке ([2]). Пробы тонко измельчают и тщательно перемешивают, используя измельчитель (5.5) и барабанный смеситель (5.6) или применяя другой процесс, в отношении которого было доказано, что он обеспечивает полную гомогенизацию до того, как будет отобрана навеска для анализа.
Во всех случаях, если проба заморожена, ей дают полностью разморозиться до отбора навески. Пробу тщательно перемешивают до отбора.
6.2 Экстракция
Взвешивают 25 г подготовленной пробы в колбу с резьбовой крышкой вместимостью 250 или 500 см3 (5.7). Добавляют 200 мл деионизированной воды, завинчивают крышку и встряхивают (5.3) в течение 1 ч.
Готовят воронку (5.8) с фильтром (5.9). Фильтруют экстрагированную пробу в чистую колбу с резьбовой крышкой вместимостью 250 или 500 см3 (5.7).
6.3 Очистка на иммуноаффинной колонке
Присоединяют емкость (5.16) к иммуноаффинной колонке. Добавляют 8 см3 деионизированной воды. Затем переносят 2,0 см-* отфильтрованного экстракта (см. выше; 0.5 мл в случае аналитических результатов более 4000 мкг/кг; см. раздел 8) в емкость (5.16). Дают экстракту самостоятельно полностью протечь через иммуноаффинную колонку со скоростью 1—2 капли в секунду. Когда экстракт полностью протечет через иммуноаффинную колонку, через колонку пропускают 5 см3 деионизированной воды. Удаляют остаточную жидкость, пропуская через колонку азот или воздух в течение примерно 5 с. Выливают все элюаты данного этапа очистки.
Помещают виалу для автодозатора ВЭЖХ (5.17) под колонку и пропускают самотеком 0.5 мл метанола (4.3) через колонку, собирая элюат. После того как последние капли метанола пройдут через колонку, оставляют метанол в колонке примерно на 1 мин. Затем добавляют еще 1.0 мл метанола (4.3) и продолжают собирать элюат. Осторожно пропускают азот или воздух через колонку, чтобы собрать весь остаточный элюат.
Примечание — В качестве альтернативы процедуре очистки на иммуноаффинной колонке, проводимой вручную (6.3). элюирование можно выполнить, используя устройство автоматической подготовки пробы при условии, что обьемы и скорости потока останутся неизменными
6.4 Приготовление аналитического раствора
Помещают виалу с элюатом в испаритель (5.19) и осторожно выпаривают досуха под воздействием азота или воздуха при температуре примерно 50 °С. Сразу после этого охлаждают виалу ВЭЖХ до комнатной температуры и разбавляют остаток 0.50 см3 подвижной фазы (4.5). Хорошо перемешивают при помощи вихревого миксера (5.4) в течение не менее 30 с. чтобы остаток снова полностью растворился. Если аналитический раствор мутный, тогда его фильтруют через шприцевой фильтр (5.18).
6.5 Процедура обогащения
Для того чтобы определить степень извлечения, обогащают материал без дезоксиниваленола обогащающим раствором (4.8). Уровень обогащения должен находиться в пределах диапазона градуировки (желательно средний диапазон). Оставляют обогащенную пробу на 30 мин не менее, чтобы испарился растворитель.
rOCTEN 15791—2015
7 Определение методом ВЭЖХ
7.1 Градуировочная кривая
Градуировочную кривую строят до начала проведения анализов по градуировочным растворам ДОН (4.10) с различными концентрациями. Градуировочную кривую строят до анализа аналитических проб, при этом на ней отражают зависимость концентрации ДОН (нг/см3) (ось х) от пиков в виде площади или высоты (ось у), определяют угол наклона и возможную точку пересечения, используя линейную регрессию, и проверяют график, используя соответствующие средства диагностики.
7.2 Определение дезоксиниваленола в аналитическом растворе
Вводят аликвоты аналитического раствора в хроматограф, применяя те же условия, что и для построения градуировочной кривой.
7.3 Идентификация пика
Идентифицируют пик дезоксиниваленола в аналитическом растворе, сравнив время его удержания со временем удержания ближайшего градуировочного раствора ДОН (4.10), введенного в ходе серии анализов ВЭЖХ. Концентрация дезоксиниваленола в аналитическом растворе должна быть в пределах диапазона градуировки. Если уровень содержания дезоксиниваленола в аналитическом растворе выше концентрации градуировочного раствора ДОН с самым высоким показателем, аналитический раствор разбавляют подвижной фазой, чтобы привести его в соответствие с диапазоном градуировки, и снова проводят анализ. Коэффициент разведения используют во всех проводимых расчетах.
7.4 Рабочие условия ВЭЖХ
При использовании оборудования, перечисленного в 5.14, было установлено, что следующие условия обеспечивают надлежащее разделение:
Инжектированный объем: 100-300 мкл
Длина волны ультрафиолетового детектора: 220 нм
Скорость потока подвижной фазы: 1.0 мл/мин
Время, мин
0-15
15-25
25-35
Канал А, %
100
0
100
Канал В, %
0
100
0
Если насос системы ВЭЖХ подает подвижную фазу (4.5) через канал А и промывной растворитель (4.6) через канал В. тогда порядок подачи следующий:
Примечание — Было доказано, что подвижные фазы, приготовленные с использованием ацетонитрила и воды, также являются подходящими альтернативами и могут быть использованы в случае, если они обеспечивают надлежащее разделение компонентов
8 Обработка результатов
По градуировочной кривой определяют концентрацию дезоксиниваленола в нанограммах на миллилитр в аналитическом растворе, введенном в колонку для ВЭЖХ.
Рассчитывают массовую долю дезоксиниваленола w^, нг/r или мг/кг, с точностью до одного десятичного знака, по следующей формуле
(3)
гДе Сдон — массовая концентрация дезоксиниваленола. определенная посредством градуировки (7.1); V3 — общий объем аналитического раствора, равный 0.5 см3 (6.4);
V2— объем аликвоты экстракта, использованного для очистки, равный 2,0 или 0,5 см3 (6.3);
V, — общий объем растворителя для экстракции, равный 200 см3 (6.2); ms— масса экстрагированной навески, равная 25,0 г (6.2).
5
Формула может быть сокращена, если вставлять в нее указанные значения массы и объема.
^дон = Сдон 2 (при очистке 2 см3 экстракта). (4)
Если по указанной формуле получено значение более 500, проводят новую очистку 0.5 см3 экстракта пробы (см. 6.3). Тогда сокращенная формула выглядит следующим образом:
wflOH = сдон 8 (при очистке 0,5 см3 экстракта). (5)
9 Прецизионность
9.1 Межлабораторное исследование
Подробная информация о межлабораторном исследовании прецизионности метода представлена в [1). Значения, полученные в ходе межлабораторного исследования, могут быть неприменимы к диапазонам концентрации и/или матрицам, отличным от представленных.
9.2 Повторяемость
Абсолютное расхождение между двумя отдельными результатами испытания, которые были получены при применении одного и того же метода на идентичном испытательном материале одним и тем же оператором на одном и том же оборудовании в течение короткого промежутка времени, не должно превышать предел повторяемости г более чем в 5 % случаев.
У = 229 мкг/кг г - 87,5 мкг/кг
г = 97,2 мкг/кг г* 31.9 мкг/кг г - 233,2 мкг/кг г = 232.9 мкг/кг
х = 401 мкг/кг х = 188 мкг/кг х = 505 мкг/кг У = 1 013 мкг/кг
9.3 Воспроизводимость
|
R более чем в 5 % случаев. | |
|
У = 229 мкг/кг |
R= 100,6 мкг/кг |
|
У = 401 мкг/кг |
R = 184.7 мкг/кг |
|
У = 118 мкг/кг |
R = 132,8 мкг/кг |
|
У = 505 мкг/кг |
R = 329,2 мкг/кг |
|
У = 1 013 мкг/кг |
R = 299,0 мкг/кг |
Абсолютное расхождение между двумя отдельными результатами испытания, полученными на идентичном объекте испытаний 8 двух лабораториях, не должно превышать предел воспроизводимости
10 Протокол испытаний
Протокол испытаний должен содержать следующие сведения:
a) всю информацию, необходимую для полной идентификации пробы (вид пробы, место отбора, назначение);
b) ссылку на настоящий стандарт:
c) дату и тип методики отбора пробы (если они известны);
d) дату поступления пробы в лабораторию:
e) дату проведения испытаний.
f) результаты испытаний с указанием единиц выражения результатов испытаний: д) сведения о том, была ли достигнута повторяемость.
h) все особенности, наблюдавшиеся при проведении испытаний:
i) все операции, не оговоренные в методике или рассматриваемые как необязательные, которые могли повлиять на результаты испытаний.
rOCTEN 15791—2015
Приложение А (справочное)
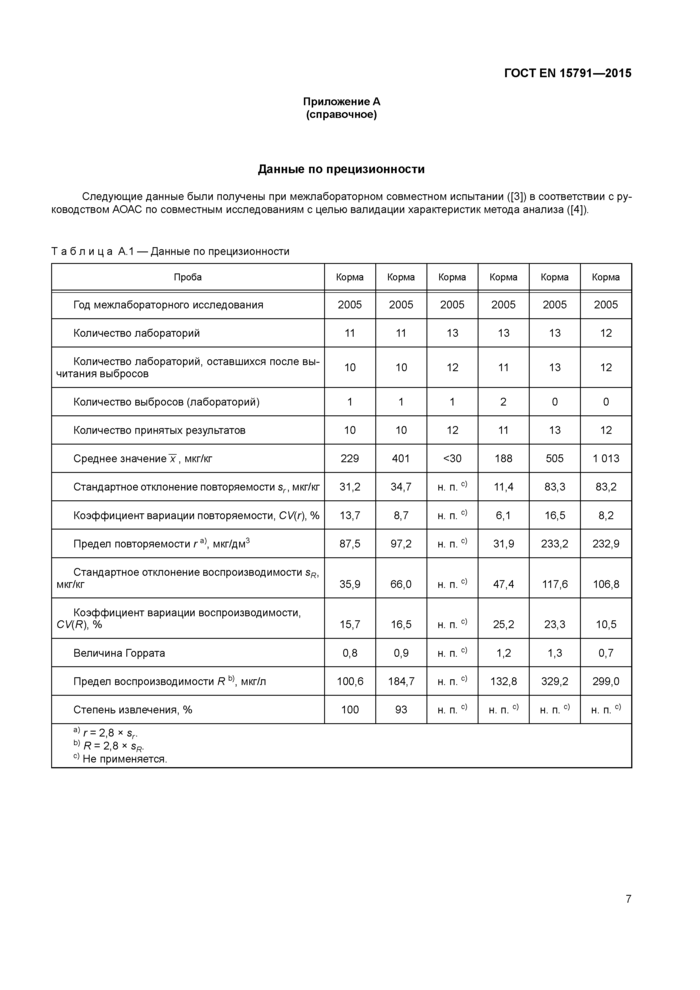
Данные по прецизионности
Следующие данные были получены при межлабораторном совместном испытании ([3]) в соответствии с руководством АОАС по совместным исследованиям с целью валидации характеристик метода анализа ((4)).
|
Таблица А 1 — Данные по прецизионности | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
7