ГОСТ EN 14122-2013
Продукты пищевые. Определение витамина В1 с помощью высокоэффективной жидкостной хроматографии
Купить ГОСТ EN 14122-2013 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает метод определения витамина В1 в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ). Содержание витамина В1 определяется как общее содержание тиамина, включая его фосфорилированные производные
- Заменяет ГОСТ 25999-83 «Продукты переработки плодов и овощей. Методы определения витаминов В1 и В2» в части разделов 3 и 4; ИУС 1-2015
Идентичен EN 14122:2003
Оглавление
1 Область применения
2 Нормативные ссылки
3 Сущность метода
4 Реактивы
5 Аппаратура
6 Проведение анализа
7 Обработка результатов
8 Прецизионность
9 Протокол результатов испытаний
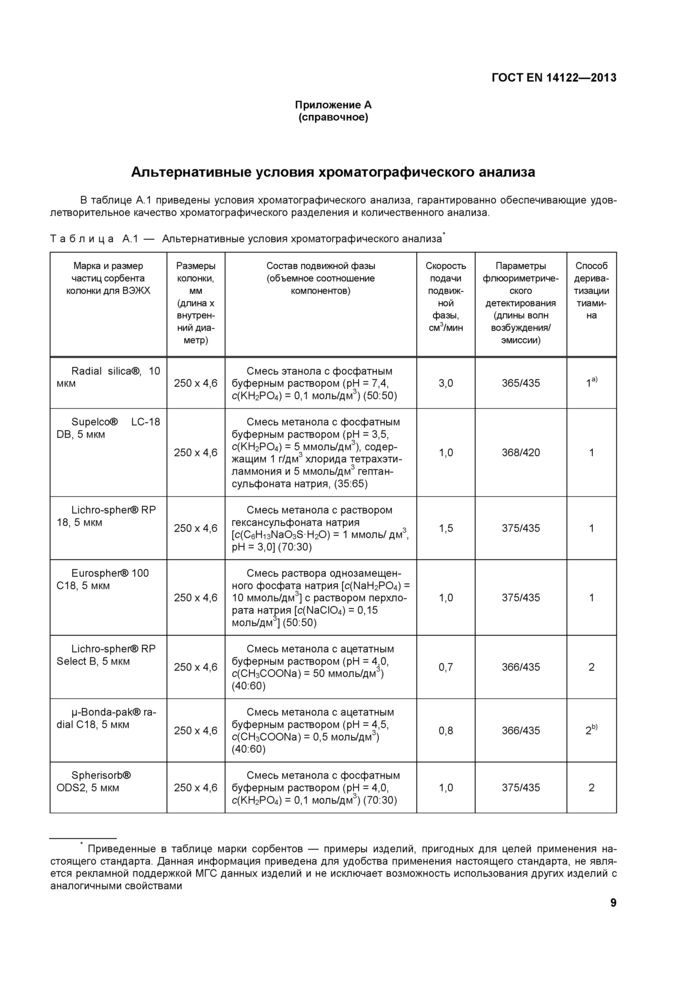
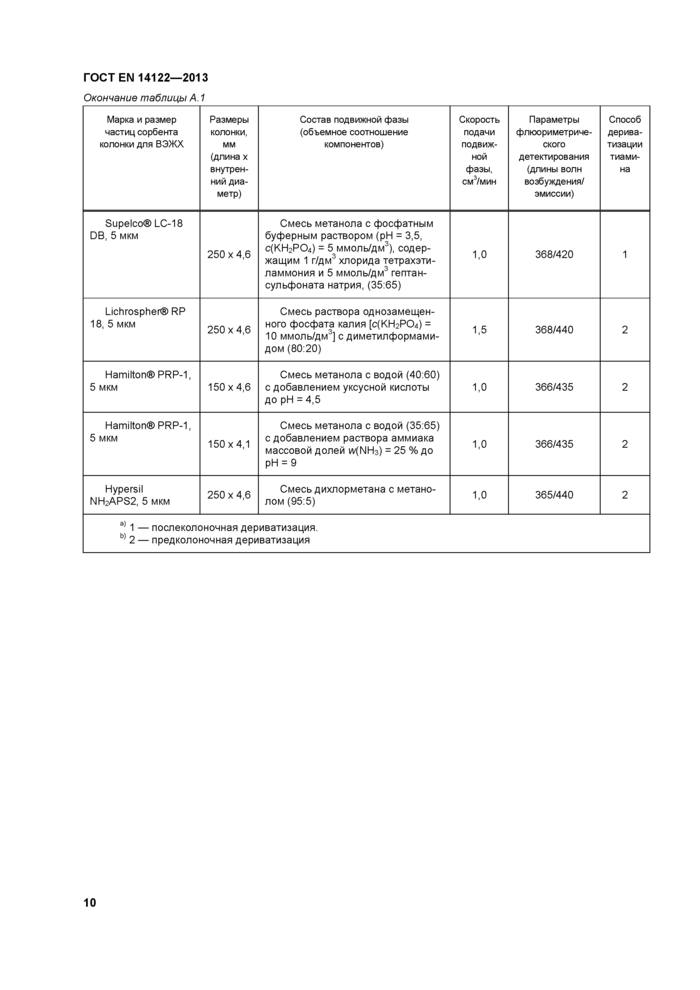
Приложение А (справочное) Альтернативные условия хроматографического анализа
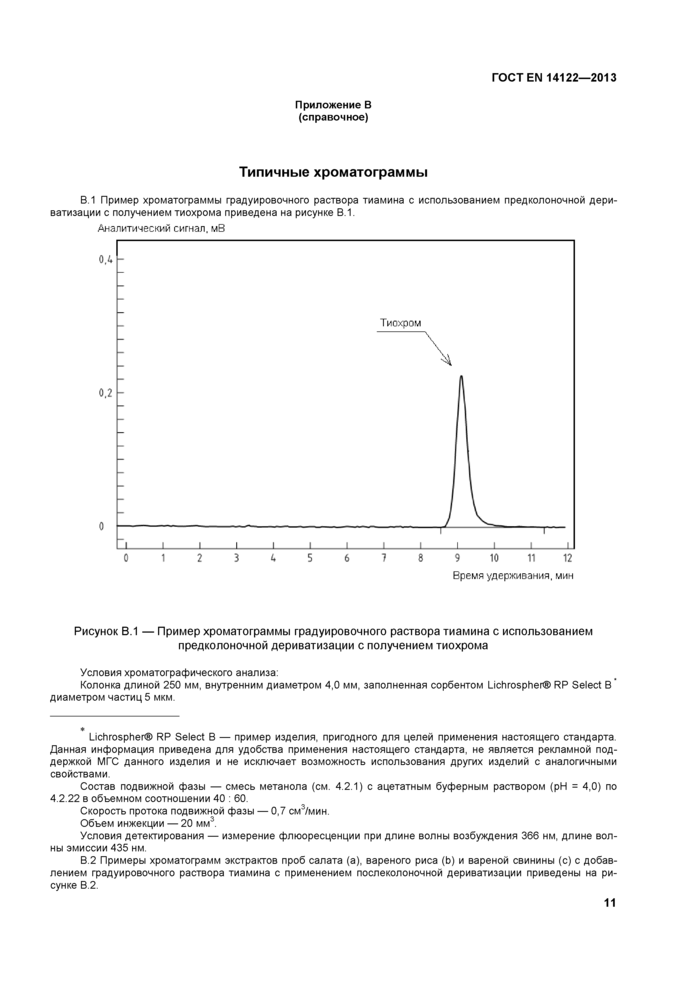
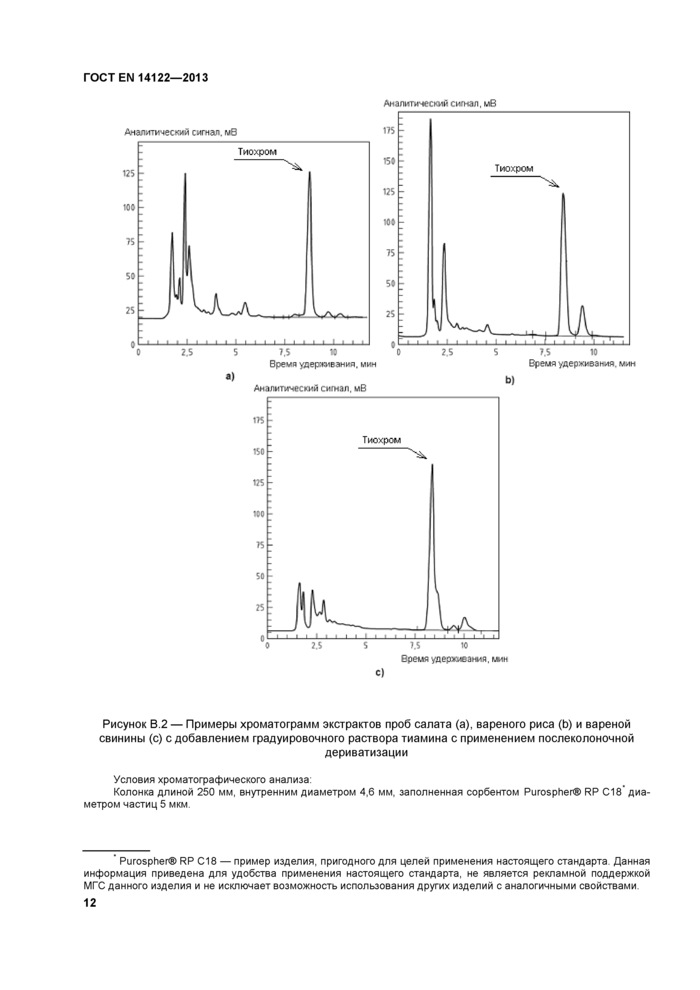
Приложение В (справочное) Типичные хроматограммы
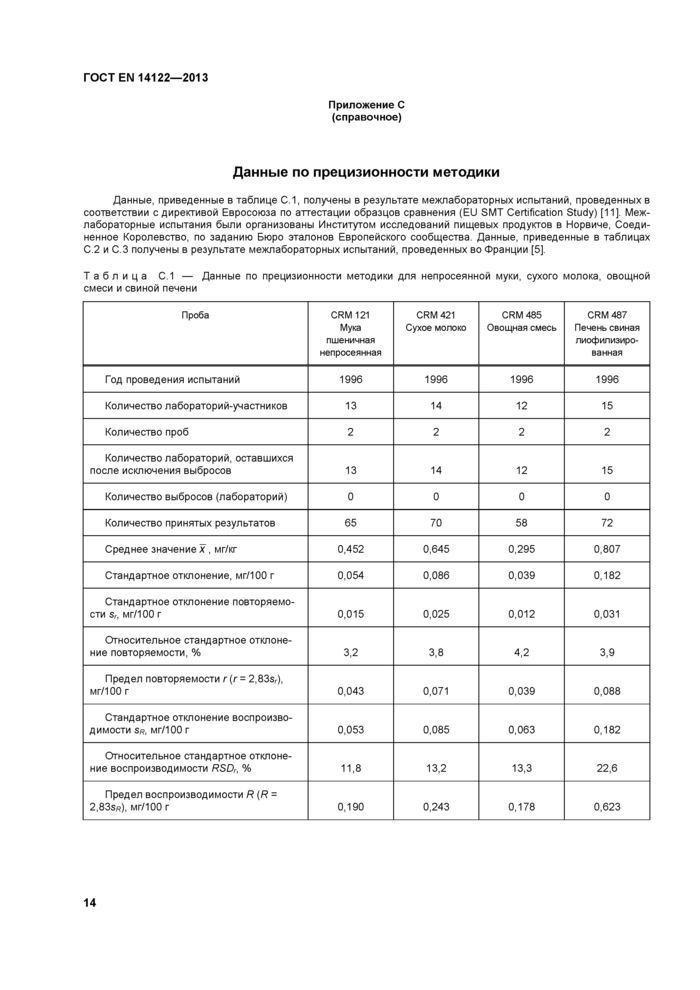
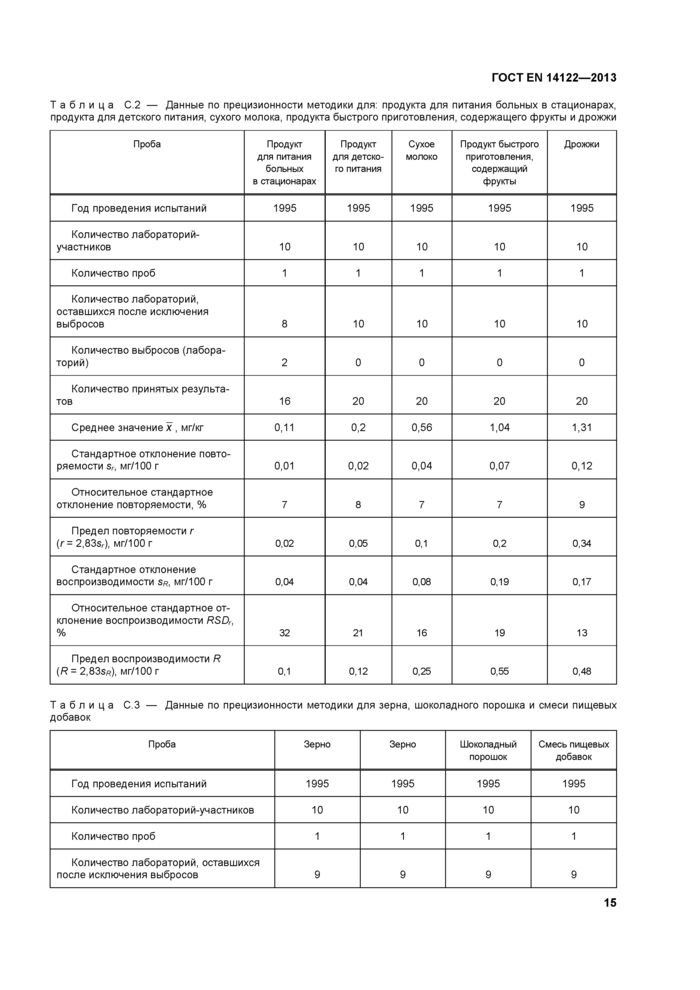
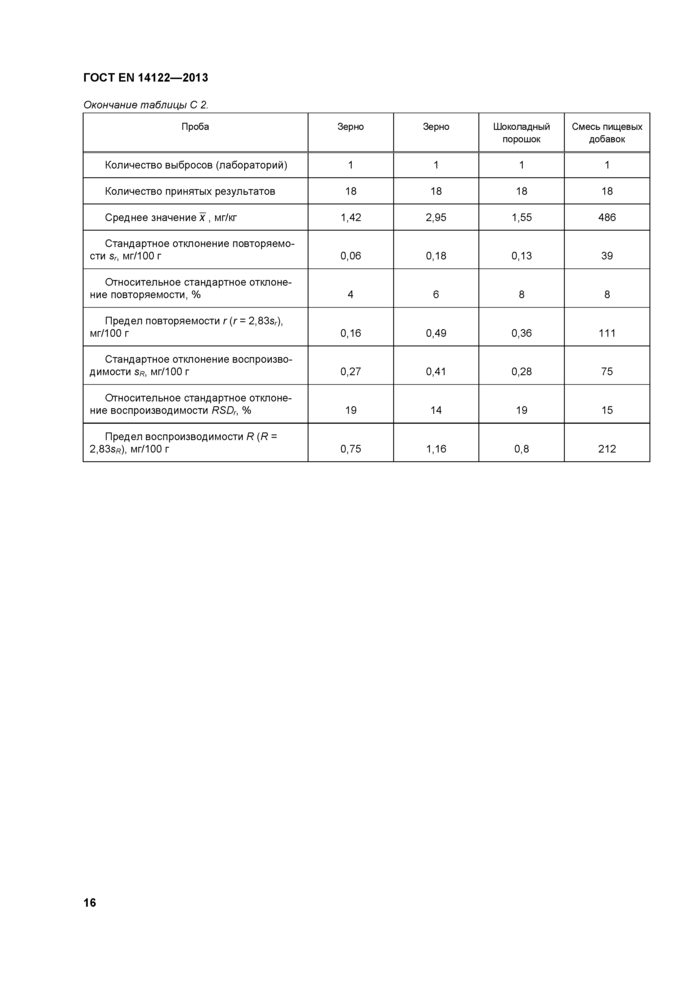
Приложение С (справочное) Данные по прецизионности методики
Приложение ДА (справочное) Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам
Библиография
| Дата введения | 01.07.2015 |
|---|---|
| Добавлен в базу | 21.05.2015 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 05.11.2013 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 61-П |
|---|---|---|---|
| 04.03.2014 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 77-ст |
| Разработан | ГНУ ВНИИКОП Россельхозакадемии | ||
| Издан | Стандартинформ | 2014 г. |
Foodstuffs. Determination of vitamin B1 by HPLC
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13
стр. 14
стр. 15
стр. 16

стр. 17
стр. 18
стр. 19
стр. 20

стр. 21

стр. 22

стр. 23
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
ГОСТ
EN 14122—
2013
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕОпределение витамина Bi с помощью высокоэффективной жидкостной хроматографии
(EN 14122:2003, ЮТ)
Издание официальное
Москва
Стандартинформ
2014
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные. правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН Государственным научным учреждением Всероссийским научно-исследовательским институтом консервной и овощесушильной промышленности Российской академии сельскохозяйственных наук (ГНУ ВНИИКОП Россельхозакадемии)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии (ТК 093)
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 5 ноября 2013 г. № 61 -П)
За принятие проголосовали:
|
Краткое наименование страны по МК (ИСО 3166) 004-97 |
Код страны по МК (ИСО 3166)004-97 |
Сокращенное наименование национального органа по стандартизации |
|
Армения |
AM |
Минэкономики Республики Армения |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Казахстан |
KZ |
Госстандарт Республики Казахстан |
|
Киргизия |
KG |
Кыргызстандарт |
|
Молдова |
MD |
Молдова-Стандарт |
|
Россия |
RU |
Росстандарт |
|
Узбекистан |
UZ |
Узстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 04 марта 2014 г. № 77-ст межгосударственный стандарт ГОСТ EN 14122-2013 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2015 г.
5 Настоящий стандарт идентичен европейскому региональному стандарту EN 14122:2003 Foodstuffs. Detemrination of vitamin B1 by HPLC (Продукты пищевые. Определение витамина В1 с помощью высокоэффективной жидкостной хроматографии).
Европейский региональный стандарт разработан техническим комитетом CEN/TC 275 «Анализ пищевых продуктов. Горизонтальные методы», секретариатом которого считается DIN.
Перевод с немецкого языка (де).
Официальные экземпляры международного стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, имеются в Федеральном агентстве по техническому регулированию и метрологии Российской Федерации.
Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам приведены в дополнительном приложении ДА
Степень соответствия — идентичная (ЮТ)
6 ВЗАМЕН ГОСТ 25999-83 в части разделов 3 и 4
ГОСТ EN 14122—2013
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты». а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
©Стандартинформ. 2014
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен. тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
ГОСТ EN 14122—2013
Содержание
1 Область применения.....................................................................................................................................1
2 Нормативные ссылки....................................................................................................................................1
3 Сущность метода...........................................................................................................................................1
4 Реактивы..........................................................................................................................................................1
5 Аппаратура.....................................................................................................................................................4
6 Проведение анализа.....................................................................................................................................5
7 Обработка результатов.................................................................................................................................7
8 Прецизионность.............................................................................................................................................8
9 Протокол результатов испытаний................................................................................................................8
Приложение А (справочное) Альтернативные условия хроматографического анализа...........................9
Приложение В (справочное) Типичные хроматограммы............................................................................11
Приложение С (справочное) Данные по прецизионности методики..........................................................14
Приложение ДА (справочное) Сведения о соответствии межгосударственных стандартов
ссылочным международным стандартам................................................................................................17
Библиография.................................................................................................................................................18
IV
fOCTEN 14122—2013
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
ПРОДУКТЫ ПИЩЕВЫЕ
Определение витамина Bi с помощью высокоэффективной жидкостной хроматографии
Foodstuffs.
Determination of vitamin В, by HPLC
Дата введения — 2015—07—01
ПРЕДУПРЕЖДЕНИЕ — Применение настоящего стандарта предусматривает использование опасных веществ, процедур и оборудования. В задачи настоящего стандарта не входит решение всех проблем связанных с безопасностью его применения. Ответственность за принятие мер предосторожности и соблюдение правил техники безопасности лежит на пользователе стандарта.
1 Область применения
Настоящий стандарт устанавливает метод определения витамина Bi в пищевых продуктах с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ). Содержание витамина В, определяется как общее содержание тиамина, включая его фосфорилированные производные.
2 Нормативные ссылки
Настоящий стандарт содержит отдельные положения из другого нормативного документа, обозначенного приведенной в данном разделе датированной нормативной ссылкой. Все последующие изменения ссылочного нормативного документа допустимо использовать только после внесения соответствующих изменений в настоящий стандарт.
EN ISO 3696:1995 Water for analytical laboratory use — Specification and test methods (ISO 3696:1987) (Вода для лабораторного анализа. Технические требования и методы испытаний)
3 Сущность метода
Метод основан на экстракции тиамина из пробы путем кислотного гидролиза, последующем ферментативном дефосфорилировании тиамина и его количественном определении с помощью ВЭЖХ с применением предварительной, либо послеколоночной конверсии в тиохром (1) — [6].
4 Реактивы
4.1 Общие положения
Для проведения анализа при отсутствии особо оговоренных условий используют только реактивы гарантированной аналитической чистоты и воду не ниже первой степени чистоты по EN ISO 3696 или бидистиллированную воду.
Издание официальное
4.2 Реактивы и растворы
4.2.1 Метанол для ВЭЖХ чистотой не менее 99.8 %.
4.2.2 Кислота уксусная, раствор молярной концентрации с(СН:,СООН) = 0.02 моль/дм3.
4.2.3 Спирт изобутиловый (изобутанол) чистотой не менее 98 %.
4.2.4 Натрий фосфорнокислый однозамещенный чистотой не менее 99.8 %.
4.2.5 Кислота соляная массовой долей 36 %.
4.2.6 Кислота соляная, раствор молярной концентрации с(НС1) = 0.1 моль/дм3.
4.2.7 Кислота серная, раствор молярной концентрации c(H2S04) = 0.05 моль/дм3.
4.2.8 Натрия гидроокись чистотой не менее 99 %.
4.2.9 Натрия гидроокись, раствор массовой концентрации p(NaOH) = 150 г/дм3.
4.2.10 Натрия гидроокись, раствор массовой концентрации p(NaOH) = 200 г/дм3.
4.2.11 Калия гексацианоферрат (III) чистотой не менее 99 %.
4.2.12 Калия гексацианоферрат (III), раствор массовой концентрации p(K3lFe(CN)e.)) = 10 г/дм3.
4.2.13 Калия гексацианоферрат (III), щелочной раствор массовой концентрации
p(Kj[Fe(CN)6J) = 0,4 г/дм3 для предколоночной дериватизации
Раствор гексацианоферрата (III) калия (см. 4.2.12) объемом 2 см3 разбавляют раствором гидроокиси натрия (см 4.2.9) до объема 50 см3.
Раствор готовят в день проведения испытания.
4.2.14 Калия гексацианоферрат (III), щелочной раствор массовой концентрации
p(Kj[Fe(CN)6J) = 0,5 г/дм3 для послеколоночной дериватизации
Раствор гексацианоферрата (III) калия (см. 4.2.12) объемом 2.5 см разбавляют раствором гидроокиси натрия (см. 4.2.10) до объема 50 см3.
4.2.15 Дефосфорилирующий фермент, пригодный для гидролиза связанного тиамина в пробе.
Примечание — При установлении характеристик прецизионности методики использована така-диастаза .
4.2.16 Натрий уксуснокислый, раствор молярной концентрации c(CH3COONa ЗН:0) = 2.5 моль/дм3.
4.2.17 Натрий уксуснокислый, раствор молярной концентрации c(CH3COONa ЗНгО) = 0.5 моль/дм3.
4.2.18 Подвижные фазы для ВЭЖХ
Варианты подвижных фаз подходящего состава приведены в приложении А. В частности, в качестве подвижных фаз используют смеси метанола с водой, фосфатным или ацетатным буферным раствором при объемной доле метанола от 10 % до 50 %. а также подвижные фазы с добавлением ион-парных реагентов.
4.2.19 Раствор буферный фосфатный (pH = 3.5) молярной концентрации однозамещенного фосфата калия с(КН:Р04) = 9.0 ммоль/дм
4.2.20 Тетраэтиламмония хлорид чистотой не менее 98 %.
4.2.21 Натрия гептансульфонат чистотой не менее 98 %.
4.2.22 Раствор буферный ацетатный (pH = 4) молярной концентрации уксусной кислоты С(СН3СООН) = 50 ммоль/дм3.
4.3 Образцы сравнения
4.3.1 Общие положения
Гидрохлорид тиаминхлорида выпускается многими производителями, при этом его чистота может различаться Это обусловливает необходимость определения концентрации градуировочного раствора тиамина спектрофотометрическим методом по 4 4 4
4.3.2 Тиаминхлорида гидрохлорид (C^H^CIN^OS HCI) чистотой не менее 99 %.
4.3.3 Тиаминмонофосфатхлорид (C12H17CIN.tO.4PS) чистотой не менее 98 %.
4.3.4 Тиаминпирофосфатхлорид (кокарбоксилаза) (C12H19CIN407P2S) чистотой не менее 98 %.
’ Така-диастаза № Т00040 - торговое наименование изделия, выпускаемого Platz and Bauer, Waterbury. CT 06708, США Данная информация приведена для удобства пользования настоящего стандарта и не является рекламной поддержкой МГС данного изделия Допускается использовать аналогичные изделия при условии обеспечения идентичных результатов
fOCTEN 14122—2013
4.4 Основные стандартные растворы
4.4.1 Тиаминхлорида гидрохлорид, раствор массовой концентрации p(C1;Hi7CIN4OS HCI) = 0,1 мг/см1
Образец сравнения гидрохлорида тиаминхлорида (см. 4.3.2) массой, например, около 10 мг, измеренной с высокой точностью, растворяют в заданном объеме, например, 100 см1 подходящего растворителя, например, раствора соляной кислоты (см. 4 2.6).
Срок хранения раствора при температуре 4 °С — четыре недели.
4.4.2 Тиаминмонофосфата хлорид, раствор массовой концентрации pfC^rCIN^PS) = 0,1 мг/см1
Около 10 мг образца сравнения тиаминмонофосфатхлорида (см. 4.3.3), измеренной с высокой точностью, растворяют в 100 см1 подходящего растворителя, например, раствора соляной кислоты (см. 4.2.6).
Срок хранения раствора при температуре минус 20 °С — четыре недели.
4.4.3 Тиаминлирофосфата хлорид, раствор массовой концентрации pfC^H^CI^O/PjS) = 0,1 мг/см1
Около 10 мг образца сравнения тиаминпирофосфатхлорида (см. 4.3 4), измеренной с высокой точностью, растворяют в 100 см1 подходящего растворителя, например, раствора соляной кислоты (см. 4.2.6).
4.4.4 Определение точной концентрации основного раствора гидрохлорида тиаминхлорида
В мерную колбу вместимостью 100 см1 помещают 10 см1 основного раствора гидрохлорида тиаминхлорида (см. 4.4.1), объем содержимого в колбе доводят до метки раствором соляной кислоты (см. 4.2.6). Измеряют оптическую плотность полученного раствора на спектрофотометре (см. 5.2) в кварцевой кювете длиной оптического пути 1 см при длине волны 247 нм. соответствующей максимуму поглощения. В качестве раствора сравнения используют раствор соляной кислоты (см. 4 2.6) Массовую концентрацию гидрохлорида тиаминхлорида в основном стандартном растворе р. мкг/см . рассчитывают по формуле
£2471 о410
Р = ~—^л-. (I)
где £247 — значение оптической плотности при длине волны 247 нм, соответствующей максимуму поглощения;
104 — коэффициент пересчета концентрации измеряемого раствора в микрограммы на кубический сантиметр;
10 — коэффициент, учитывающий кратность разбавления основного стандартного раствора;
421 — коэффициент экстинкции раствора гидрохлорида тиаминхлорида в растворе соляной кислоты молярной концентрации 0,1 моль/дм1 [7], соответствующий условной оптической плотности раствора гидрохлорида тиаминхлорида массовой концентрации 10 г/дм1.
4.5 Градуировочные растворы
4.5.1 Градуировочные растворы гидрохлорида тиаминхлорида массовой концентрации от 1 до 10 мкг/см1
Пипеткой отмеряют от 1 до 10 см основного стандартного раствора тиаминхлорида гидрохлорида (см. 4.4.1) и помещают в мерную колбу вместимостью 100 см1. Объем содержимого в колбе доводят до метки раствором соляной кислоты (см. 4 2.6).
Срок хранения полученного раствора в темном месте при температуре 4 °С — 1 мес.
4.5.2 Градуировочные растворы хлорида тиаминмонофосфата массовой концентрации от 1 до 10 мкг/см1
Пипеткой отмеряют от 1 до 10 см1 основного стандартного раствора хлорида тиаминмонофосфата (см. 4 4.2) и помещают в мерную колбу вместимостью 100 см1. Объем содержимого в колбе доводят до метки раствором соляной кислоты (см. 4.2.6).
Срок хранения полученного раствора в темном месте при температуре 4 °С — 1 мес.
4.5.2 Градуировочные растворы хлорида тиаминпирофосфата массовой концентрации от 1 до 10 мкг/см3
Пипеткой отмеряют от 1 до 10 см3 основного стандартного раствора хлорида тиаминпирофосфата (см. 4.4.3) и помещают в мерную колбу вместимостью 100 см3. Объем содержимого в колбе доводят до метки раствором соляной кислоты (см. 4.2.6).
Срок хранения полученного раствора в темном месте при температуре 4 °С — 1 мес.
5 Аппаратура
5.1 Общие положения
При проведении анализа используют лабораторные приборы, оборудование и стеклянную посуду. в частности, перечисленные ниже.
5.2 Спектрофотометр, пригодный для измерений оптической плотности в ультрафиолетовой области спектра при заданной длине волны.
5.3 Автоклав или нагревательный прибор
Автоклав с контролем температуры и давления или плитка электрическая, или баня водяная с контролем температуры.
5.4 Хроматограф жидкостный
Система для ВЭЖХ. состоящая из насоса, инжектора, флюориметрического детектора, позволяющего проводить измерения при длинах волн возбухщения и эмиссии, указанных в приложении А. например, 366 нм и 420 нм соответственно, и устройства регистрации и обработки аналитического сигнала, например, интегратора.
5.5 Колонка аналитическая для ВЭЖХ
5.5.1 Общие положения
Допускается использовать колонку другого внутреннего диаметра и длины, и заполненную сорбентом другого размера частиц, чем те. что указаны в настоящем стандарте. Условия хроматографического разделения подбирают применительно к используемой колонке для обеспечения сопоставимости результатов анализов. Критерием пригодности анапитической колонки является отделение пика аналита от пиков других компонентов матрицы пробы на уровне базовой линии.
5.5.2 Колонка для ВЭЖХ при анализе с использованием предколоночного окисления тиамина
Колонка длиной от 100 до 250 мм. внутренним диаметром от 4.0 до 4.6 мм. заполненная сорбентом’ размером частиц 5 мкм.
5.5.3 Колонка для ВЭЖХ при анализе с использованием послеколоночного окисления тиамина.
. Колонка длиной от 100 до 250 мм, внутренним диаметром от 4,0 до 4,6 мм. заполненная сорбентом размером частиц 5 мкм.
5.6 Установка для фильтрации
Фильтрование подвижной фазы перед ее использованием и раствора пробы для хроматографического анализа перед инжекцией через мембранный фильтр размером пор. например. 0.45 мкм. продлевает срок службы аналитических колонок.
fOCTEN 14122—2013
5.7 Система для послеколоночной дериватизации
Система, состоящая из насоса для подачи реактива для дериватизации. соединительного элемента для трех капилляров и реактора в виде капилляра длиной 10 м и внутренним диаметром 0.33 мм.
6 Проведение анализа
6.1 Подготовка пробы
Пробу гомогенизируют, продукты твердой консистенции измельчают с помощью подходящей мельницы, после чего перемешивают. Перед измельчением пробу рекомендуется предварительно охладить, чтобы не подвергать ее длительному воздействию высоких температур.
6.2 Приготовление раствора пробы для анализа
6.2.1 Экстракция
От 2 до 10 г анализируемой пробы, измеренной с точностью до 0,001 г. помещают в коническую колбу. Добавляют раствор соляной кислоты (см. 4.2.6) или серной кислоты (см. 4 2.7) объемом от 60 до 200 см3. Значение pH полученной шеей должно быть не более 3.0. Колбу закрывают часовым стеклом и выдерживают в автоклаве при температуре 121 °С в течение 30 мин. либо на водяной бане при температуре 100 °С в течение 60 мин.
Примечание — Согласно результатам исследований, кислотный гидролиз допустимо проводить при различных условиях, в частности, при температуре от 95 °С до 130 °С и продолжительности гидролиза от 15 до 60 мин При этом, чем выше температура, тем меньше времени требуется для проведения гидролиза
6.2.2 Ферментативная обработка
После охлахщения до комнатной температуры к экстракту добавляют раствор ацетата натрия (см. 4.2.16 или 4.2.17) до достижения значения pH. оптимального для действия предполагаемого к использованию фермента. В экстракт вносят необходимое количество дефосфорилирующего фермента (см. 4.2.15). Полученную смесь выдерживают в течение промежутка времени и при температуре. оптимальных для используемого фермента. После охлаждения до комнатной температуры полученный раствор переносят в защищенную от света мерную колбу с помощью дистиллированной воды или другого подходящего растворителя и доводят обьем содержимого в колбе до метки (Уе).
Для каждого ферментного препарата устанавливают оптимальное значение pH и оптимальные температуру и продолжительность инкубации.
Для установления оптимальных условий дефосфорилирования проводят процедуру ферментативной обработки проб с добавлением хлорида тиаминмонофосфата (см. 4 3.3) или хлорида тиамин-пирофосфата (см. 4.3.4), а также проб, аналогичных исследуемой пробе по составу матрицы и являющихся аттестованными образцами сравнения
При использовании для дефосфорилирования така-диастазы возможно привнесение в пробу с ферментным препаратом некоторого количества тиамина, что необходимо учитывать при расчете результата испытания.
Примечания
1 При установлении характеристик прецизионности, приведенных в настоящем стандарте, для проведения дефосфорилирования использована така-диастаза при следующих условиях Значение pH экстракта доводилось до 4.0 добавлением раствора ацетата натрия (см 4 2 16 или 4 2 17), после чего в экстракт вносили така-диастазу из расчета 100 мг препарата на грамм пробы Полученную смесь инкубировали при температуре от 37 °С до 46 °С. продолжительность инкубирования составляла от 16 до 24 ч
2 Скорость дефосфорилирования зависит от используемого ферментного препарата и матрицы пробы По имеющимся данным полное дефосфорилирование может быть достигнуто за более короткое время [8]
6.2.3 Окисление тиамина с образованием тиохрома
6.2.3.1 Предколоночное окисление тиамина
В стеклянный флакон или колбу подходящей вместимости помещают 1 см раствора пробы после ферментативной обработки по 6.2.2. либо градуировочного раствора (см. 4.5.1), либо холостого раствора Добавляют 1 см' щелочного раствора гексацианоферрата (III) калия (см. 4 2.13). содержимое флакона встряхивают в течение 10 с. после чего оставляют в покое на 1 мин. Подготовленный таким образом к хроматографическому анализу раствор пробы, градуировочный раствор или холо-
5
стой раствор анализируют с помощью обращенно-фазовой ВЭЖХ при условиях, указанных в таблице А.1 приложе- ния А.
В качестве альтернативы после окисления тиамина проводят экстракцию тиохрома из раствора порцией изобутанола (см. 4 2.3) объемом 1.5 смэкстракт анализируют с помощью ВЭЖХ.
С целью удаления из раствора пробы веществ, мешающих анализу, и предотвращения порчи аналитической колонки перед проведением анализа с помощью ВЭЖХ рекомендуется нейтрализовать раствор пробы для анализа добавлением фосфорной кислоты или провести его очистку с помощью твердофазной экстракции по (5).
Примечание — Некоторые компоненты пищевых продуктов, например, полифенольные вещества, могут препятствовать окислению тиамина с образованием тиохрома Это явление характерно для продуктов, содержащих какао, а также для некоторых других продуктов Если такая проблема предположительно имеет место. рекомендуется проверить полноту обнаружения аналита путем внесения в экстракт градуировочного раствора тиамина перед проведением процедуры окисления При низкой полноте обнаружения рекомендуется проводить очистку экстракта с помощью катионообменной смолы или выполнять ВЭЖХ-анализ с применением по-слеколоночного окисления тиамина
6.2.3.2 Идентификация аналита при анализе с применением предколоночного окисления тиамина
Проводят хроматографический анализ градуировочных растворов и раствора пробы, подготовленных по 6 2.3.1, при одинаковых объемах инжекции. Пик тиохрома на хроматограмме раствора пробы идентифицируют по совпадению его времени удерживания со временем удерживания пика тиохрома на хроматограмме градуировочного раствора. В качестве альтернативы пик тиохрома на хроматограмме раствора пробы идентифицируют путем ее сопоставления с хроматограммой раствора пробы с добавлением аналитического стандарта.
Ниже приведены условия хроматографического анализа, гарантированно обеспечивающие удовлетворительное качество хроматографического разделения и количественного определения (см. рисунок В.1 приложения В) Альтернативные условия приведены в приложении А. ,
Аналитическая колонка длиной 250 мм, внутренним диаметром 4 мм. заполненная сорбентом диаметром частиц 5 мкм.
Состав подвижной фазы: смесь метанола (см. 4,2.1) с ацетатным буферным раствором (см. 4.2.22).
Скорость протока подвижной фазы — 0.7 см/мин.
Объем инжекции — 20 мм3.
Условия флюориметрического детектирования: длина волны возбуждения 366 нм. длина волны эмиссии 435 нм.
6.2.3.3 Послеколоночное окисление тиамина
При послеколоночном окислении тиамина с образованием тиохрома в качестве дериватизи-рующего реагента используют раствор гексацианоферрата (III) калия (см. 4.2.14). который добавляют в элюат посредством соединительного элемента для трех капилляров при скорости подачи около 0.3 см3/мин.
Примечание — Одним из факторов, влияющих на послеколоночную реакцию, является концентрация гидроксида натрия в реакционной смеси. Чрезмерно высокую или чрезмерно низкую концентрацию гидроксида натрия в дериватизирующем реагенте компенсируют соответственно уменьшением или увеличением скорости его подачи,
6.2.3 4 Идентификация аналита при анализе с применением лослеколоночного окисления тиамина
Проводят хроматографический анализ градуировочных растворов (см. 4.5.1) и раствора пробы (см. 6.2.2) при одинаковых объемах инжекции. Пик тиохрома на хроматограмме раствора пробы идентифицируют по совпадению его времени удерживания со временем удерживания пика тиохрома на хроматограмме градуировочного раствора. В качестве альтернативы пик тиохрома на хроматограмме раствора пробы идентифицируют путем ее сопоставления с хроматограммой раствора пробы с добавлением аналитического стандарта.
* Например. Lichrospher® RP Select В. пригодный для целей применения настоящего стандарта Данная информация приведена для удобства применения настоящего стандарта, не является рекламной поддержкой МГС данного изделия и не исключает возможность использования других изделий с аналогичными свойствами
1
Пригодность для проведения анализа установлена в отношении следующих марок сорбентов на основе силикагеля, доступных для приобретения Lichrosorb® Si-60, Spherosorb® Si, Hypersil® Si и Lichrospher® 100 Diol Пригодность для проведения анализа установлена в отношении следующих марок обращенно-фазовых сорбентов Uuchrospher Si 60 RP Select, Spherisorb® ODS, p-Bondapak® radial Cl8, Supelco® LC-18-DB и Hypersil® ODS Данная информация приведена исключительно для удобства применения настоящего стандарта, не является рекламной поддержкой МГС данных изделий и не исключает возможность использования других изделий с аналогичными свойствами