УПРАВЛЕНИЕ ПО ВНЕДРЕНИЮ НОВЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ И МЕДИЦИНСКОЙ ТЕХНИКИ
ВСЕСОЮЗНЫЙ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ И ИСПЫТАТЕЛЬНЫЙ ИНСТИТУТ МЕДИЦИНСКОЙ ТЕХНИКИ
СБОРНИК РУКОВОДЯЩИХ МЕТОДИЧЕСКИХ МАТЕРИАЛОВ
ПО токсиколого-гигиеническим
ИССЛЕДОВАНИЯМ ПОЛИМЕРНЫХ МАТЕРИАЛОВ И ИЗДЕЛИЙ НА ИХ ОСНОВЕ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ
Москва 1987
Утверждено начальником Управления по внедрению новых лекарственных средств и медицинской техники 3. А. Б а б а я но м от 27 ноября 1985 года
РЕДАКЦИОННАЯ КОЛЛЕГИЯ:
9. А. Бабаян, В. Г. Лаппо, С. Я. Ланина, Т. И. Носкова, В. И. Тимохина.
Научно-методические документы разработаны и внедрены в практику токсиколого-гигиенической оценки материалов и изделий медицинского назначения сотрудниками ВНИИИ медицинской техники Минздрава СССР —
B. Г. Лаппо (зав. отделом токсикологии), В. И. Тимохиной, Н. М. Перовой,
C. Я- Ланиной, В. И. Долгополовым, Н. М. Каминской, Н. Г. Тышковской, Р. И. Каюмовым, Л. А. Самариной, Н. Б. Емельяновой, Т. М. Винокурской, Т. В. Селаври; сотрудниками Института органической химии АН УССР — Г. А. Пхакадзе, Н. А. Галатенко; Киевского медицинского института — В. П. Яценко; сотрудниками Московского медицинского стоматологического института им. Н. А, Семашко — В. П. Марковым, И. Ю. Лебеденко.
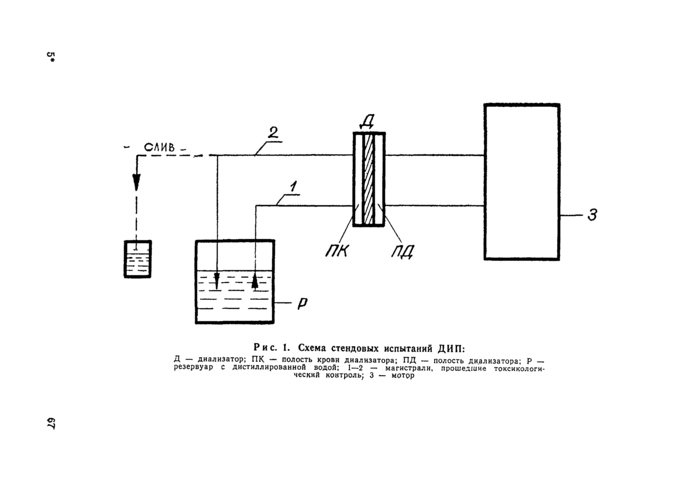
Рис. I. Схема стендовых испытаний ДИП:
Д — диализатор; ПК — полость крови диализатора; ПД — полость диализатора; Р — резервуар с дистиллированной водой; 1—2 — магистрали, прошедшие токсикологический контроль; 3 — мотор
|
|
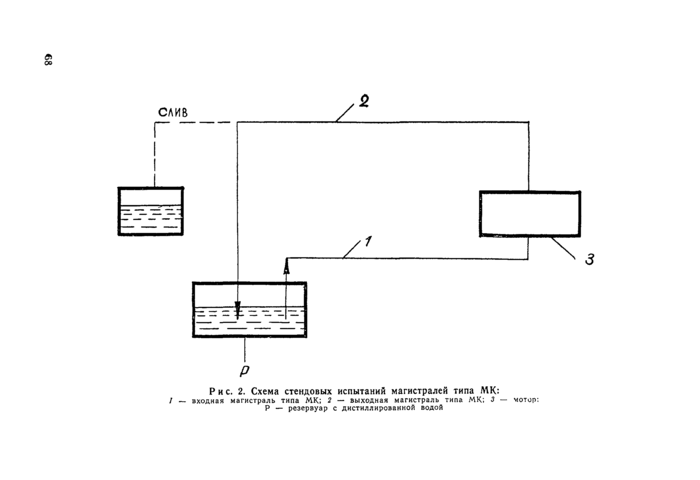
Рис. 2. Схема стендовых испытаний магистралей типа МК:
/ — входная магистраль типа МК: 3 — выходная магистраль типа МК; 3 — мотор: Р — реатрвуар с дистиллирование* водой |
в) свободные концы магистралей (входной и выходной) помещаются в резервуар с 2 л дистиллированной апирогенной во-_ ды, которая с помощью роликового насоса в режиме рециркуляции перемещается через кровопроводящую полость с расходом 200±20 мл/мин в течение 3 часов. Испытаниям подвергается 1 л вытяжки от каждого ДИПа.
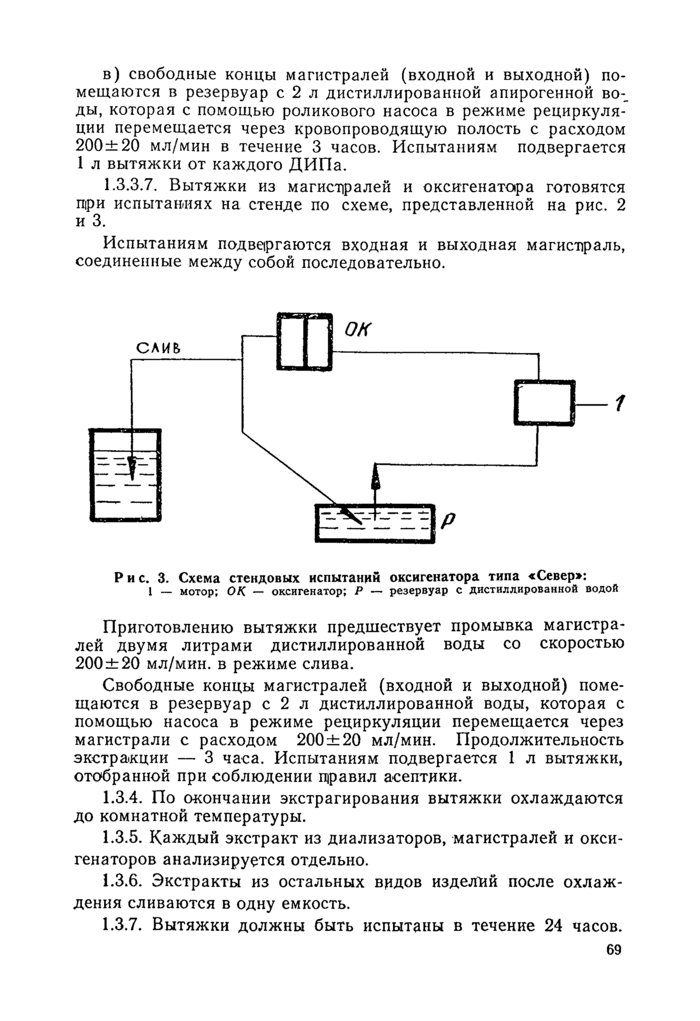
1.3.3.7. Вытяжки из магистралей и оксигенатора готовятся гири испытаниях на стенде по схеме, представленной на рис. 2 и 3.
Испытаниям подвергаются входная и выходная магистраль, соединенные между собой последовательно.
|
|
Рис. 3. Схема стендовых испытаний оксигенатора типа «Север»:
I — мотор; ОК — оксигенатор; Р — резервуар с дистиллированной водой |
Приготовлению вытяжки предшествует промывка магистралей двумя литрами дистиллированной воды со скоростью 200±20 мл/мин. в режиме слива.
Свободные концы магистралей (входной и выходной) помещаются в резервуар с 2 л дистиллированной воды, которая с помощью насоса в режиме рециркуляции перемещается через магистрали с расходом 200±20 мл/мин. Продолжительность экстракции — 3 часа. Испытаниям подвергается 1 л вытяжки, отобранной при соблюдении травил асептики.
1.3.4. По окончании экстрагирования вытяжки охлаждаются до комнатной температуры.
1.3.5. Каждый экстракт из диализаторов, магистралей и оксигенаторов анализируется отдельно.
1.3.6. Экстракты из остальных видов изделий после охлаждения сливаются в одну емкость.
1.3.7. Вытяжки должны быть испытаны в течение 24 часов.
69
Неиспользованная часть вытяжки хранится в холодильнике при температуре 4 ±1°С до оценки результатов испытаний. При необходимости повторных испытаний используют эти же вытяжки. Контрольные растворы хранятся в тех же условиях.
1.4. САНИТАРНО-ХИМИЧЕСКИЕ ИСПЫТАНИЯ ИЗДЕЛИЙ
1.4.1. Санитарно-химическим испытаниям подвергаются:
— диализаторы типа ДИП;
— магистрали кровопроводящие типа МК;
— флаконы для кровезаменителей;
— фильтры крови типа ФК;
— оксигенаторы типа «Север».
1.4.2. Определяемые показатели:
— окисляемость экстракта;
— бромируемость экстракта;
— изменение значения pH экстракта;
— содержание формальдегида (в случае флаконов для кровезаменителей).
1.4.3. Методики определения.
1.4.3.1. Определение окисляемости перманганатным методом.
Реактивы: а) перманганат калия (КМп04)—0,1 Н р-ра;
б) щавелевая кислота (Н2С204)—0,1 Н;
в) серная кислота (H2S04) — уд. вес 1.84.
0,01 Н раствор перманганата калия и 0,01 Н раствор щавелевой кислоты готовят перед употреблением из 0,1 Н раствора.
Для определения окисляемости берут 100 мл вытяжки. В коническую колбу емкостью 300—350 мл наливают 5—50 мл вытяжки, доводят до 100 мл холостым раствором, приливают 5 мл разбавленной 1 :3 серной кислоты, осторожно перемешивают, нагревают 8 минут, не доводя до кипения, и заливают 15 мл 0,01 Н раствора перманганата калия, ставят на плитку (горелку) и замечают 15 минут с момента закипания. Кипячение проводят с обратным холодильником. Затем приливают пипеткой 15 мл 0,01 Н р-р щавелевой кислоты и титруют 0,01 Н р-ром перманганата калия до слабо-розового окрашивания.
у_ (А—В )К • 0,08 • 1000 кол-во мл вытяжки
где А — количество 0,01 Н раствора перманганата калия, пошедшего на титрование избытка щавелевой кислоты в исходной пробе;
В — количество 0,01 Н раствора перманганата калия, пошедшего на титрование избытка щавелевой кислоты в контрольной пробе;
К — коэф. поправки 0,01 Н раствора перманганата калия;
0,08 — количество мг кислорода, эквивалентное 0,01 Н раствору перманганата калия;
X — окисляемость испытуемой вытяжки, выраженная в мг 02/л.
1.4.3.2. Определение бромирующихся веществ.
Реактивы: а) бромид-броматная смесь: 1,67 г бромата калия (КВгОз) и 6,0 г бромида калия (КВг) растворяют в одном литре дистиллированной воды. Перед употреблением раствор разводят в 10 раз.
б) иодит калия (KJ);
в) тиосульфат натрия (Na2S203) —0,1 Н раствор;
г) тиосульфат натрия (i\ra2S203) — 0,005 Н раствор готовят перед определением из 0,1 Н раствора;
д) крахмал растворимый — 0,5% раствор;
е) серная кислота, разведенная 1 : 3.
50 мл вытяжки переносят в коническую колбу емкостью 250—300 мл, снабженную притертой пробкой, и прибавляют 25 мл бромид-броматной смеси. Далее приливают 10 мл разбавленной 1 : 3 серной кислоты, закрывают колбу пробкой, осторожно перемешивают содержимое колбы и оставляют стоять в темноте 30 минут, затем добавляют 1 г иодида калия, снова закрывают колбу пробкой, осторожно перемешивают содержимое колбы и ставят в темноту; через 5 минут титруют выделившийся иод 0,005 Н раствором тиосульфата натрия до слабожелтого цвета. После этого добавляют 0,5 мл 0,5% раствора крахмала и продолжают титровать до обесцвечивания раствора.
Контрольное определение проводят в тех же условиях со 100 мл контрольного раствора.
В другой такой же колбе проводят контрольное определение, для чего вместо исследуемой вытяжки берут 50 мл контрольного раствора и добавляют все реактивы в тех же количествах, в каких они были взяты при исследовании вытяжки.
Результаты определения выражают в количестве прореагировавшего брома (X) в мг В 2/л:
у — (А —В) • К • 1000 • 0.3996 объем вытяжки (мл) ’
где А — объем раствора тиосульфата натрия, израсходованного при проведении контрольного опыта, мл;
В — объем раствора тиосульфата натрия, израсходованного в опыте с вытяжкой, мл;
К — поправочный коэффициент для приведения концентрации раствора тиосульфата натрия точно к 0,005 Н; 0,3996 — количество мг брома, эквивалентное 1 мл 0,005 Н раствора тиосульфата натрия.
1.4.3.3. Определение изменения значения pH вытяжек. Измерение значения pH вытяжек и контроля проводится на рН-мет-ре. Измеренное значение pH вытяжки сравнивается с контро-
71
лем, которым является исходная дистиллированная вода, используемая для приготовления вытяжки.
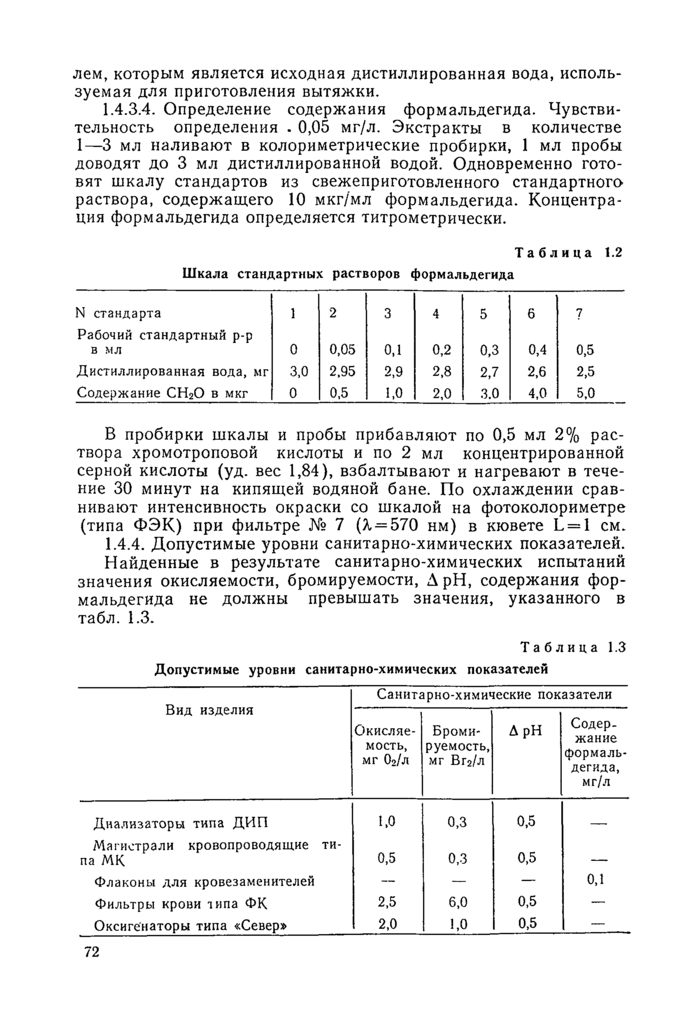
1.4.3.4. Определение содержания формальдегида. Чувствительность определения . 0,05 мг/л. Экстракты в количестве 1—3 мл наливают в колориметрические пробирки, 1 мл пробы доводят до 3 мл дистиллированной водой. Одновременно готовят шкалу стандартов из свежеприготовленного стандартного раствора, содержащего 10 мкг/мл формальдегида. Концентрация формальдегида определяется титрометрически.
|
Таблица 1.2
Шкала стандартных растворов формальдегида |
|
N стандарта |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
Рабочий стандартный р-р в мл |
0 |
0,05 |
0.1 |
0,2 |
0,3 |
0,4 |
0.5 |
|
Дистиллированная вода, мг |
3,0 |
2.95 |
2.9 |
2,8 |
2,7 |
2.6 |
2,5 |
|
Содержание СН20 в мкг |
0 |
0.5 |
1.0 |
2.0 |
3.0 |
4.0 |
5,0 |
|
В пробирки шкалы и пробы прибавляют по 0,5 мл 2% раствора хромотроповой кислоты и по 2 мл концентрированной серной кислоты (уд. вес 1,84), взбалтывают и нагревают в течение 30 минут на кипящей водяной бане. По охлаждении сравнивают интенсивность окраски со шкалой на фотоколориметре (типа ФЭК) при фильтре № 7 (Х = 570 нм) в кювете L = 1 см.
1.4.4. Допустимые уровни санитарно-химических показателей.
Найденные в результате санитарно-химических испытаний значения окисляемости, бромируемости, Д pH, содержания формальдегида не должны превышать значения, указанного в табл. 1.3.
|
Таблица 1.3 Допустимые уровни санитарно-химических показателей |
|
Вид изделия |
Санитарно-химические показатели |
|
Окисляе-мость, мг 02/л |
Броми-руемость, мг Вг2/л |
Д pH |
Содер-
жание
формаль
дегида,
мг/л |
|
Диализаторы типа ДИП |
1,0 |
0,3 |
0,5 |
_ |
|
Магистрали кровопроводящие типа мк |
0,5 |
0,3 |
0,5 |
_ |
|
Флаконы для кровезаменителей |
— |
— |
— |
0,1 |
|
Фильтры крови типа ФК |
2,5 |
6.0 |
0,5 |
— |
|
Оксигенаторы типа «Север* |
2,0 |
1,0 |
0,5 |
_ |
|
|
72 |
ОГЛАВЛЕНИЕ
Часть I. Научно-методические документы по токсиколого-гигиеническим исследованиям новых полимерных, других материалов и изделий на их основе для медицины
1. Общие методические указании к токсиколого-гигиенической оценке
полимерных материалов и изделий на их основе для медицины . 7
2. Методические указания к токсиколого-гигиеническому исследованию полимерных материалов и изделий для эндопротезирования 18
3. Методические указания к токсиколого-гигиеническому исследованию медицинских клеев, предназначенных для соединения мягких и
костной тканей организма 25
4. Методические указания к токсиколого-гигиеническому исследованию
материалов, узлов и аппаратов по замене функций внутренних органов............... 29
5. Методические указания к токсиколого-гигиеническому исследованию
шовных хирургических нитей и перевязочных материалов 34
6. Методические указания к токсиколого-гигиеническому исследованию
полимерных пломбировочных материалов стоматологического назначения ................46
7. Методические указания к токсиколого-гигиеническому исследова
Часть II. Унифицированная методика контроля токсичности серийно выпускаемых полимерных изделий медицинского
нию металлических сплавов для протезирования в ортопедической стоматологии..........58
назначения однократного применения
1.1. Общие положения..............62
1.2. Порядок отбора изделий............63
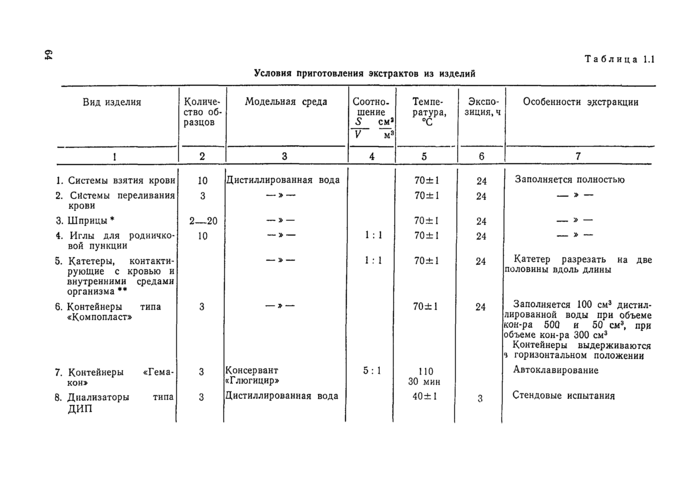
1.3. Условия приготовления экстрактов из изделий......63
1.4. Санитарно-химичсскне испытания изделий.......70
1.5. Гемолитический тест.............73
1.6. Токсикологические испытания па мышах.......73
1.7. Оценка результатов.............74
Часть III. Экспресс-методы определения токсичности полимерных материалов и изделий медицинского назначения
1. Методика определения токсического действия вытяжек из материалов на культуре тканей ...........
2. Методика определения гемолитического действия вытяжек из материалов и изделий «ин витро»..........83
3. Методика определения токсического действия вытяжек из материалов и изделий на изолированном сердце лягушки.....86
4. Методика определения биосовместимости полимерных материалов
и изделий для эндопротезирования по их влиянию на лимфоидную ткань.................88
5. Методика определения токсического действия вытяжек из материалов и изделий на половых клетках крупного рогатого скота 94
Перечень литературы и справочных источников......96
4
ЧАСТЬ II
УНИФИЦИРОВАННАЯ МЕТОДИКА КОНТРОЛЯ ТОКСИЧНОСТИ СЕРИЙНО ВЫПУСКАЕМЫХ ПОЛИМЕРНЫХ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ
61
1. УНИФИЦИРОВАННАЯ МЕТОДИКА КОНТРОЛЯ ТОКСИЧНОСТИ СЕРИЙНО ВЫПУСКАЕМЫХ ПОЛИМЕРНЫХ ИЗДЕЛИЙ МЕДИЦИНСКОГО НАЗНАЧЕНИЯ ОДНОКРАТНОГО ПРИМЕНЕНИЯ
1.1. ОБЩИЕ ПОЛОЖЕНИЯ
1.1.1. Контрольные методики на серийно выпускаемые изделия медицинского назначения разрабатываются головной организацией Минздрава СССР по токсикологическим испытаниям Всесоюзным научно-исследовательским и испытательным институтом медицинской техники, утверждаются Управлением по внедрению новых лекарственных средств и медицинской техники и являются обязательным приложением к техническим условиям на конкретные виды продукции.
1.1.2. Настоящий раздел сборника содержит унифицированную методику для контроля токсичности ряда серийно выпускаемых изделий, разработанную с целью удобства пользования контрольными лабораториями предприятий.
1.1.3. Методика распространяется на следующие серийно выпускаемые полимерные изделия:
— системы инфузионные, трансфузионные, эксфуэйонные (методика контроля утв. 30.3.78 г.);
— шприцы инъекционные (методика контроля утв. 30.3.78 г.):
— иглы для родничковой пункции (методика контроля утв 10.8.79);
— катетеры внутривенные, эпидуральные, пупочные детские желудочные детские, носовые детские, кишечные (методика контроля утв. 21.5.80 г.);
— контейнеры и их комплекты для взятия, транспортировки хранения и переливания крови и ее компонентов типа «Компо пласт» и «Гемакон» (методика контроля утв. 26.6.85 г.);
— диализаторы одноразовые типа ДИП (методика контрол* утв. 29.8.83 г.);
— магистрали кровопроводящие типа МК (методика контро ля утв. 29.8.83);
— флаконы для кровезаменителей (методика контроля утв
29.8.83) ;
— фильтры крови типа ФК (методика контроля утв. 24.5.83)
— оксигенаторы типа «Север» (методика контроля утв
29.8.83) .
62
1.1.4. Контроль токсичности изделий осуществляется заводом-изготовителем.
1.1.5. Испытываются изделия, изготовленные и простерили-зованные согласно действующей НТД, прошедшие этапы маркировки.
1.1.5. Понятие «партия» изделий.
1.1.5.1. Партией радиационно стерилизованных изделий считается такое их количество, которое простерилизовано за сутки.
1.1.5.2. Партией контейнеров типа «Гемакон» считается количество контейнеров, заполненных консервантом крови «Глюги-дир» одной партии и простерилизованных паровым методом за сутки.
1.1.5.3. Партией флаконов считается количество изделий, заполненных одним видом кровезаменителей одной и той же партии.
1.2. ПОРЯДОК ОТБОРА ИЗДЕЛИЙ
1.2.1. Количество отбираемых на испытания образцов для контроля готовой продукции составляет 0,1% от партии, но не менее того количества образцов, которое указано в табл. 1.1. настоящего раздела.
1.2.2. Порядок отбора. Изделия отбираются в равном количестве в начале, середине и в конце изготовления партии. Если изделие стерилизуется паровым методом, то образцы отбираются от разных стерилизаторов.
1.2.3. Периодичность отбора образцов.
1.2.3.1. В период освоения промышленного выпуска изделий, а также в течение первых трех лет серийного выпуска испытаниям подвергается каждая партия изделий.
1.2.3.2. По истечении трех лет серийного выпуска, если изделия трех партий подряд окажутся нетоксичными, то санитарнохимическим и гемолитическим испытаниям (если они предусмотрены методикой) подвергается каждая партия изделий, а собственно токсикологическим — каждая десятая партия.
1.2.3.3. В дальнейшем при стабильной технологии производства и качества выпускаемых изделий, подтвержденных документально, проводятся испытания каждой 25-й партии изделий.
1.2.3.4. При получении отрицательного результата испытаний контролю токсичности подвергается последовательно подряд три партии изделий.
1.2.3.5. При получении положительных результатов по п. 1.2.3.4. контроль осуществляется по пп. 1.2.3.2.,. 1.2.3.3.
1.3. УСЛОВИЯ ПРИГОТОВЛЕНИЯ ЭКСТРАКТОВ ИЗ ИЗДЕЛИЙ
1.3.1. Экстракты из изделий готовятся в соответствии с табл.
63
2
|
Условия приготовления экстрактов из изделий
Таблица 1.1 |
|
Вид изделия |
Количество образцов |
Модельная среда |
Соотио. шение S см» ~7~ м. |
Темпе-
рат^ра, |
Экспозиция. ч |
Особенности экстракции |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
J. Системы взятия крови |
10 |
Дистиллированная вода |
|
70± 1 |
24 |
Заполняется полностью |
|
2. Системы переливания |
3 |
|
|
70± 1 |
24 |
— » — |
|
крови |
|
|
|
|
|
|
|
3. Шприцы * |
2—20 |
|
|
70 ± 1 |
24 |
— > — |
|
4. Иглы для родиичко- |
10 |
|
1:1 |
70± 1 |
24 |
— » — |
|
вой пункции |
|
|
|
|
|
|
|
5. Катетеры, контактирующие с кровью и |
|
— » — |
1:1 |
70± 1 |
24 |
Катетер разрезать на две половины вдоль длины |
|
внутренними средами организма •• |
|
|
|
|
|
|
|
6. Контейнеры типа «Компопласт» |
3 |
— » — |
|
70S: 1 |
24 |
Заполняется 100 см» дистиллированной воды при объеме кои-ра 500 и 50 см*, при объеме кои-ра 300 см» Контейнеры выдерживаются а горизонтальном положении |
|
7. Контейнеры «Гема-кои> |
3 |
Консервант
(Глюгицир» |
5:1 |
ПО 30 мин |
|
Автоклавирование |
|
6. Диализаторы типа |
3 |
Дистиллированная вода |
|
40±1 |
з |
Стендовые испытания |
|
ДИП |
|
|
|
|
|
|
|
|
Й» 1 |
2 |
3 |
4 |
ь |
6 |
7 |
|
5 9. Магистрали кровопро-водящие типа МК
10. Флаконы для кровезаменителей |
3
9 |
— » — |
|
40± 1 |
3 |
Заполняются в условиях производства |
|
11. Фильтры крови типа ФК |
3 |
Дистиллированная вода |
|
70± 1 |
24 |
Каждое изделие заливается 800 см* воды и полностью погружается в воду |
|
12. Оксигенаторы типа «Север» |
3 |
|
|
40*1 |
3 |
Стендовые испытания |
|
|
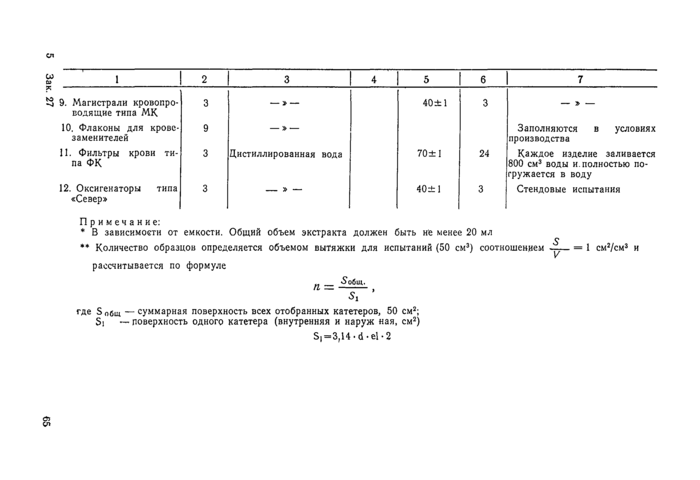
Примечание:
• В зависимо*™ от емкости. Общий объем экстракта должен быть не менее 20 мл ** Количество образцов определяется объемом вытяжки для испытаний (50 см*) соотношением рассчитывается по формуле |
8?
еде Sofia — суммарная поверхность всех отобранных катетеров, 50 см*; Si *— поверхность одного катетера (внутренняя и наруж ная. см*)
S,-3,14 б-el-2
1.3.2. Экстрагентом для всех видов изделий, за исключением контейнеров типа «Гемакон», является дистиллированная вода, полученная с соблюдением правил асептики (Гос. Фармакопея СССР, изд. X, 1968, с. 107). Экстрагентом для контейнеров типа «Гемакон» является консервант «Глюгицир».
1.3.3. Способы экстрагирования.
1.3.3.1. Системы взятия и переливания крови, шприцы» флаконы для кровезаменителей, контейнеры типа «Компопласт» пе-рез испытаниями заливаются дистиллированной водой в соответствии с условиями, указанными в табл. 1.1.
1.3.3.2. Экстракт из контейнеров типа «Гемакон» готовится следующим образом.
В один из стерилизаторов одновременно с изделиями помещается герметичный стеклянный сосуд с консервантом данной партии в количестве не менее 250 мл, который используется в дальнейшем для заполнения пустых емкостей в многокамерных контейнерах, а также для контроля в токсикологическом эксперименте.
Для приготовления экстрактов из многокамерных контейнеров в каждую из незаполненных консервантом дополнительных емкостей, независимо от их числа (для 2-, 3- и 4-камерных контейнеров типа «Гемакон»), заливается через надрез, сделанный на соединяющей емкости трубке, по 50 мл консерванта «Глюгицир», полученного, как указано в предыдущем абзаце. Затем трубка пережимается зажимом ниже надреза (ближе к мешку), после чего контейнеры выдерживаются в горизонтальном положении при комнатной температуре (18—20°С) в течение 24 часов.
1.3.3.3. Для приготовления экстрактов из катетеров, игл для родничковой пункции, фильтров крови типа ФК отобранные изделия помещаются в стеклянные колбы с притертыми пробками, заливаются дистиллированной водой и термостатируются в соответствии с условиями, приведенными в табл. 1.1.
1.3.3.4. Контрольным раствором является дистиллированная вода, на которой готовятся экстракты.
1.3.3.5. Диализаторы типа ДИП, магистрали кровопроводящие типа МК, оксигенаторы типа «Север» испытываются в стендовых условиях.
1.3.3.6. Вытяжки из диализаторов готовятся при испытаниях на стенде по схеме, представленной на рис. 1.
Приготовление вытяжки проводится в следующей последовательности:
а) через полость диализата пропускается дистиллированная вода со скоростью 500±50 мл/мин при вакуумическом давлении не более 7 кПа и температуре 40± 1°С;
б) диализатор промыть 2 л дистиллированной а пирогенной воды со скоростью 200±20 мл/мин в режиме слива через кровопроводящую полость;
66