ГОСТ ISO 5765-2-2016
Молоко сухое, сухие смеси для мороженого и плавленый сыр. Определение содержания лактозы. Часть 2. Ферментативный метод с использованием галактозы в качестве составной части лактозы
Устанавливает ферментативный метод определения содержания лактозы во всех видах сухого молока, в сухих смесях для мороженого в присутствии других углеводов и восстанавливающих веществ, а также в плавленом сыре.
Оглавление
1 Область применения
2 Термины и определения
3 Принцип
4 Реактивы
5 Оборудование
6 Отбор проб
7 Исследования
8 Расчет и выражение результатов
9 Прецизионность
10 Протокол испытаний
Приложение А (обязательное) Правила надлежащей лабораторной практики (НЛП) для проведения ферментативного анализа
Библиография
16 страниц
| Дата введения | 01.05.2017 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Актуализация | 01.01.2021 |
Организации:
| 28.06.2016 | Утвержден | Евразийский совет по стандартизации, метрологии и сертификации | 49 |
|---|---|---|---|
| 14.10.2016 | Утвержден | Госстандарт Республики Беларусь | 79 |
| Разработан | Государственный комитет по стандартизации Республики Беларусь | ||
| Издан | БелГИСС | 2016 г. |
Dried milk, dried ice-mixes and processed cheese. Determination of lactose content. Part 2. Enzymatic method utilizing the galactose moiety of the lactose
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7
стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14

стр. 15

стр. 16
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
МОЛОКО СУХОЕ, СУХИЕ СМЕСИ ДЛЯ МОРОЖЕНОГО И ПЛАВЛЕНЫЙ СЫР
Определение содержания лактозы Часть 2
Ферментативный метод с использованием галактозы в качестве составной части лактозы
МАЛАКО СУХОЕ, СУХ1Я СУМЕС1 ДЛЯ МАРОЖАНАГА I ПЛАУЛЕНЫ СЫР
Вызначэнне змяшчэння лактозы Частка 2
Ферментатыуны метад з выкарыстаннем галактозы у якасщ састауной частю лактозы
(ISO 5765-2:2002, ЮТ) (IDF 79-2:2002, ЮТ)
Издание официальное
Г осстандарт Минск
<£Предисловие
Евразийский совет по стандартизации, метрологии и сертификации (ЕАСС) представляет собой региональное объединение национальных органов по стандартизации государств, входящих в Содружество Независимых Государств. В дальнейшем возможно вступление в ЕАСС национальных органов по стандартизации других государств.
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены».
Сведения о стандарте
1 ВНЕСЕН Государственным комитетом по стандартизации Республики Беларусь
2 ПРИНЯТ Евразийским советом по стандартизации, метрологии и сертификации (протокол № 49 от 28 июня 2016 г.)
|
За принятие стандарта проголосовали: | ||||||||||||||||||||||||
|
3 Настоящий стандарт подготовлен на основе СТБ ISO 5765-2:2012.
4 Настоящий стандарт идентичен международному стандарту ISO 5765-2:2002|IDF 79-2:2002 Dried Milk, dried ice-mixes and processed cheese — Determination of lactose content — Part 2: Enzymatic method utilizing the galactose moiety of the lactose (Молоко сухое, смеси для мороженого сухие и сыр плавленый. Определение содержания лактозы. Часть 2. Ферментативный метод с использованием галактозы в качестве составной части лактозы).
Международный стандарт разработан подкомитетом SC 5 по молоку и молочным продуктам технического комитета по стандартизации ISO/TC 34 по пищевым продуктам и Международной молочной федерацией (IDF) в сотрудничестве с Ассоциацией аналитических сообществ (АОАС International).
Перевод с английского языка (ел).
Официальный экземпляр международного стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, имеется в Национальном фонде ТИПА.
В тексте стандарта ссылки на международные стандарты актуализированы.
Степень соответствия — идентичная (IDT)
5 ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 14 октября 2016 г. № 79 непосредственно в качестве государственного стандарта Республики Беларусь с 1 мая 2017 г.
6 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных (государственных) стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных (государственных) органов по стандартизации.
© Госстандарт, 2016
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
Приложение А (обязательное)Правила надлежащей лабораторной практики (НЛП) для проведения ферментативного анализаА.1 Введение
А.1 Введение
Правила надлежащей лабораторной практики (НЛП) для проведения ферментативного анализа часто менее известны, чем правила относительно других химических анализов.
Рекомендуется обращать большее внимание на эти правила, чтобы получать результаты с удовлетворительной прецизионностью и повторяемостью.
Таким образом, перед началом испытания необходимо внимательно ознакомиться с правилами НЛП, приведенными ниже.
А.2 Реактивы
А.2.1 Используют только ферменты с указанными характеристиками (определенная активность, концентрация, контаминанты ферментной активности, растворители).
А.2.2 Используют только коферменты с указанными характеристиками (степень чистоты, в форме соли или кислоты, контаминанты).
А.2.3 Все реактивы, кроме ферментов и коферментов, должны быть химически чистыми.
А.2.4 Вода, используемая для приготовления растворов ферментов и других реактивов, должна пройти двойное дистиллирование.
А.2.5 Вода для приготовления испытуемых растворов должна пройти двойное дистиллирование или быть деионизированной.
А.2.6 Реактивы и суспензии/растворы ферментов хранят согласно инструкции (обычно при температуре от плюс 2 °С до плюс 8 °С).
А.2.7 Суспензии ферментов не замораживают.
А.2.8 Если истек срок годности реактива, его утилизируют или проверяют эффективность этого реактива, исследуя стандартными растворами с различным количеством анализируемого вещества. Полученные значения поглощения должны быть пропорциональны концентрациям.
А.2.9 Буферные растворы, хранящиеся в холодильнике, необходимо нагреть до комнатной температуры прежде, чем добавить к исследуемой смеси.
А.З Фотометрические и спектрометрические кюветы
А.3.1 Используют стеклянные или пластмассовые кюветы с длиной оптического пути, равной 1 см.
Примечание — Пластмассовые кюветы имеют следующие преимущества перед стеклянными кюветами:
- они дешевые (доступнее);
- можно проводить большее количество испытаний;
- в пределах одной партии пластмассовые кюветы имеют схожие показатели поглощения.
А.З.2 Каждый раз при использовании новой партии кювет перепроверяют длину оптического пути относительно прецизионной кюветы (например, кварцевой кюветы) следующим образом.
Прецизионную кювету и пластмассовые кюветы наполняют водой и измеряют поглощение А1 каждой кюветы относительно воздуха. После промывания кюветы наполняют раствором NADH (приблизительно 0,15 мг/мл) и снова измеряют поглощение А2 относительно воздуха.
Для прецизионной кюветы и для пластмассовых кювет рассчитывают А2- Ау. Значения разницы А2 - Ai у двух типов кювет не должны значительно отличаться. Если значения разницы А2 - А1 превышают 0,5 % от измеренного чистого поглощения для прецизионной кюветы, вычисляют среднюю разницу в процентах, которую затем учитывают при расчете длины оптического пути / (см. 8.1).
А.3.3 Всегда используют только чистые и без царапин кюветы. Оптические боковые поверхности кювет вытирают или чистят только с использованием мягкой ткани.
А.З.4 Не измеряют поглощение кюветы с исследуемой пробой относительно кюветы с контрольной пробой, так как в этом случае не будет получено никакой информации о порядке величины поглощения непосредственно контрольного испытания. Измеряют поглощение как кюветы с исследуемой пробой, так и кюветы с контрольной пробой относительно воздуха и вычисляют разность.
ГОСТ ISO 5765-2-2016
А.3.5 Не измеряют поглощения кюветы с пробой или кюветы с контрольной пробой относительно пустой кюветы (из-за рассеивания света).
А.3.6 Содержимое кювет перемешивают с помощью пластмассовой лопатки или запечатывают кюветы парафином и слегка взбалтывают.
А.3.7 Со стенок кювет удаляют воздушные пузыри при помощи пластмассовой лопатки. Следует избегать царапин оптической боковой поверхности кювет.
А.3.8 Всегда используют один тип кювет для проведения испытаний исследуемой пробы и при контрольных испытаниях.
А.3.9 Кюветы всегда устанавливают в одном и том же положении и в одном направлении в держателе кювет. Для этого одну оптическую боковую поверхность кювет помечают.
А.4 Фотометры и спектрометры
А.4.1 Используют спектрометр (ширина полосы пропускания < 10 нм), оснащенный фильтром помех (ширина полосы пропускания < 10 нм), или фотометр спектральной линии, оснащенный ртутной лампой. Измерения, выполняемые с использованием спектрометра или фильтра-фотометра, должны проводиться при максимуме поглощения NADH или NADPH, т. е. при длине волны 340 нм, а измерения, выполняемые с использованием фотометра спектральной линии, оснащенного ртутной лампой, должны проводиться при длине волны 365 или 334 нм.
Примечание — Коэффициенты молярного поглощения NADH и NADPH, измеренные при длине волны 334, 340 и 365 нм, являются следующими:
- NADH и NADPH при 334 нм (Нд) — 6,18 х 10е см2/моль;
- NADH и NADPH при 340 нм — 6,3 * 10е см2/моль;
- NADPH при 365 нм (Нд) — 3,5 * 10е см2/моль;
- NADH при 365 нм (Нд) — 3,4 * 10е см2/моль.
А.4.2 В диапазоне поглощения, которое не превышает 2,0, должна существовать линейная зависимость между поглощением и концентрацией NADH или NADPH. Проверку проводят следующим образом:
a) 2,00 мл дистиллированной воды с помощью пипетки вносят в кювету. Измеряют поглощение А0 относительно воздуха;
b) 0,10 мл раствора NADH (0,5 мг/мл) с помощью пипетки вносят в кювету и перемешивают. Измеряют поглощение А^.
Вычисляют уменьшенное поглощение АгЬ используя следующую формулу:
Ai=(A_A))x|il, (А.1)
3.5
где Ai — поглощение, полученное в результате измерения на растворе NADH, перечисление Ь);
А0 — поглощение, полученное в результате измерения на воде, перечисление а);
c) процедуру, указанную в перечислении Ь), повторяют 14 раз.
После каждой пары измерений вычисляют пониженное поглощение Агп, используя следующую формулу:
Arn=(An-A0)x^-, (А.2)
3.5
где Ап — поглощение, полученное в результате измерения п\
V — объем содержимого кюветы при измерении п\
d) для каждого измерения строят график зависимости объема раствора NADH, находящегося в кювете, относительно пониженного поглощения. Должна получиться прямая линия, соединяющая полученные точки пересечения.
А.5 Автоматические пипетки и другие дозаторы
А.5.1 Автоматические пипетки и другие дозаторы используют в соответствии с инструкциями изготовителей.
А.5.2 Для каждой пипетки используют соответствующие наконечники.
А.5.3 Периодически (например, ежемесячно) проверяют рабочие характеристики автоматических пипеток и других дозаторов по объему и сходимости следующим образом:
а) взвешивают стеклянный химический стакан с водой и фиксируют начало отсчета времени f;
9
b) при помощи пипетки или дозатора в химический стакан добавляют одну порцию воды и взвешивают точно в момент времени t+ 1 мин после первого взвешивания;
c) процедуру добавления при помощи пипетки или дозатора повторяют 9 раз согласно перечислению Ь);
d) взвешивают химический стакан в моменты времени t + 11 мин, t+ 12 мин, t + 13 мин, t + 14 мин, t + 15 мин без добавления из пипетки или дозатора; по результатам взвешиваний рассчитывают потери при испарении за минуту;
e) вычисляют объем и сходимость пипетки или дозатора с учетом потерь воды в процессе испарения.
А.5.4 На объем некоторых автоматических пипеток может оказать влияние теплопередача от кисти руки в процессе длительного использования.
Это явление проверяют в соответствии с процедурой, указанной в А.5.3, и по возможности не используют такие пипетки.
А.5.5 Непосредственно перед использованием наконечник пипетки промывают несколько раз раствором/суспензией, которые будут использоваться. Для каждого раствора пробы используют новый наконечник пипетки.
А.5.6 Воду, буферный раствор, фермент, кофермент и исследуемый раствор вносят пипеткой (опуская наконечник как можно ниже) в разные углы кюветы.
Примечание — Небольшие количества раствора/суспензии фермента (от 10 до 50 мкл) допускается вносить пипеткой на лопатку, помещенную в кювету, и перемешать лопаткой все содержимое кюветы.
А.5.7 Следует избегать загрязнения.
А.6 Дополнительная информация
А.6.1 Наличие возможных посторонних воздействий и нарушений перепроверяют, определяя поглощения двух растворов с различной концентрацией исследуемого вещества. Полученные значения поглощения должны быть пропорциональны концентрации исследуемого вещества.
А.6.2 Используют стандартный раствор для проверки ферментной реакции. Этот стандартный раствор должен рассматриваться как рабочий стандартный раствор.
Примечание — Эталонные материалы, имеющие сертифицированную степень чистоты, могут быть получены от таких организаций, как Национальный институт стандартов и технологии (бывшее Национальное бюро стандартов) или Бюро стандартов Европейского сообщества (BCR).
А.6.3 При наличии исследуемого раствора проводят испытание на восстановление. Количество добавленного анализируемого вещества должно быть приблизительно таким же, как количество, уже присутствующее в испытуемом растворе.
А.6.4 Для каждой кюветы используют свою пластмассовую лопатку или каждую лопатку используют только один раз.
Примечание — Количеством жидкости, оставшейся на лопатке, можно пренебречь.
10
ГОСТ ISO 5765-2-2016Библиография
[1] ISO 707:2008 Milk and milk products — Guidance on sampling
(Молоко и молочные продукты. Руководство по отбору проб)
[2] ISO 5725-1:1994 Accuracy (trueness and precision) of measurement methods and results —
Part 1: General principles and definitions
(Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Общие принципы и определения)
[3] ISO 5725-2:1994 Accuracy (trueness and precision) of measurement methods and results — Part 2: Basic method for the determination of repeatability and reproducibility of a standard measurement method
(Точность (правильность и прецизионность) методов и результатов измерений. Часть 2. Основной метод определения повторяемости и воспроизводимости стандартного метода измерения)
[4] IDF 135В: 1991 Milk and milk products — Precision characteristics of analytical methods — Outline of collaborative study procedure
(Молоко и молочные продукты. Характеристики точности аналитических методов. Схемы совместной процедуры исследования)
[5] Comite de Nomenclature de I'Union Internationale de Biochimie, Recommandations en matiere de Nomenclatures des Enzymes
(Комитет по номенклатуре ферментов Международного биохимического союза. Рекомендации по веществам номенклатур ферментов. Академическое издание, Нью-Йорк, 1984)
[6] Interlaboratory Collaborative Studies, second series. Bulletin International Dairy Federation, 285, 1993, annex A, annex В and annex C
(Межлабораторные совместные исследования, второй выпуск. Бюллетень Международной федерации производителей молочной продукции, 285, 1993, приложение А, приложение В и приложение С)
11
УДК 637.143.044(083.74)(476) МКС 67.100.10; 67.100.30; 67.100.40 ЮТ
Ключевые слова: определение содержания лактозы, галактоза, молоко сухое, сыр плавленый, сухие смеси для мороженого, ферментативный метод
12
Ответственный за выпуск Н. А. Баранов
Сдано в набор 03.11.2016. Подписано в печать 17.11.2016. Формат бумаги 60x84/8. Бумага офсетная. Гарнитура Arial. Печать ризографическая. Уел. печ. л. 2,09 Уч.-изд. л. 0,92 Тираж2экз. Заказ 2046
Издатель и полиграфическое исполнение:
Научно-производственное республиканское унитарное предприятие «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) Свидетельство о государственной регистрации издателя, изготовителя, распространителя печатных изданий
№ 1/303 от 22.04.2014 ул. Мележа, 3, коми. 406, 220113, Минск.
ГОСТ ISO 5765-2-2016Введение
В настоящем стандарте описан ферментативный метод определения лактозы с использованием галактозы в качестве составной части лактозы. Настоящий стандарт является дополнением к ISO 5765-1, который рассматривает глюкозу как составную часть лактозы.
Выбор между методами, описанными в ISO 5765-1 и ISO 5765-2, зависит от содержания глюкозы или галактозы в исследуемой пробе. Если содержание глюкозы в исследуемой пробе значительно выше, чем содержание лактозы, рекомендуется использовать метод, описанный в настоящем стандарте. Для исследуемой пробы со значительно более высоким содержанием галактозы, чем лактозы, рекомендуется использовать метод, описанный в ISO 5765-1.
Для исследуемой пробы с низким содержанием и глюкозы, и галактозы без предпочтения может использоваться любой метод. Для исследуемой пробы с высоким содержанием и глюкозы, и галактозы для обоих методов точность определения лактозы значительно ниже.
В молоке и молочных продуктах, подвергнутых тепловой обработке, часть лактозы может перейти в лактулозу. Лактулоза не определяется методом, описанным в ISO 5765-1. Однако при использовании метода, описанного в настоящем стандарте, содержание лактулозы будет частично определено как содержание лактозы.
Кроме того, в молоке, подвергнутом интенсивной тепловой обработке (например, стерилизованное молоко), или в молочных продуктах часть лактозы может оказаться связанной с белком в результате реакции Майяра. В таких случаях связанная лактоза не может быть определена ни одним из методов, описанных в ISO 5765-1 и в настоящем стандарте.
Только при строгом соблюдении правил надлежащей лабораторной практики (НЛП) для ферментативного анализа могут быть получены достоверные результаты. Правила НЛП указаны в приложении А.
Ill
_ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ_
МОЛОКО СУХОЕ, СУХИЕ СМЕСИ ДЛЯ МОРОЖЕНОГО И ПЛАВЛЕНЫЙ СЫР Определение содержания лактозы Часть 2
Ферментативный метод с использованием галактозы в качестве составной части лактозы
МАЛАКО СУХОЕ, СУХ1Я СУМECI ДЛЯ МАРОЖАНАГА I ПЛАУЛЕНЫ СЫР Вызначэнне змяшчэння лактозы Частка 2
Ферментатыуны метад з выкарыстаннем галактозы у якасц1 састауной частм лактозы
Dried Milk, dried ice-mixes and processed cheese Determination of lactose content Part 2
Enzymatic method utilizing the galactose moiety of the lactose
Дата введения — 2017-05-01
1 Область применения
Настоящий стандарт устанавливает ферментативный метод определения содержания лактозы во всех видах сухого молока, в сухих смесях для мороженого в присутствии других углеводов и восстанавливающих веществ, а также в плавленом сыре.
2 Термины и определения
В настоящем стандарте применен следующий термин с соответствующим определением:
2.1 содержание лактозы (lactose content): Массовая доля веществ, определенных в соответствии с методом, установленным настоящим стандартом.
Примечание — Содержание лактозы выражают в процентах от массы.
3 Принцип
3.1 Раствор или суспензию рабочей части пробы высвобождают от белка для получения чистого экстракта.
3.2 Очищенный экстракт рабочей части пробы вступает в реакцию со следующими ферментами и биохимическими реактивами:
a) (З-галактозидазой для расщепления лактозы на глюкозу и галактозу;
b) р-галактозидазой дегидрогеназой в присутствии никотинамидадениндинуклеотида (NAD+) с целью катализации окисления галактозы до галактоновой кислоты, при этом NAD+ восстанавливается до NADH.
3.3 Количество НАДФН определяют из величины поглощения исследуемого раствора при длине волны 340 нм.
3.4 Вычисляют содержание лактозы, которое пропорционально количеству NADH, при условии, что в начале анализа сделана поправка на присутствие галактозы в начальной исследуемой пробе.
4 Реактивы
При проведении анализа используют реактивы признанного аналитического качества, если иное не указано. Вода, используемая для приготовления ферментных растворов, должна иметь степень очистки, обеспечиваемую двойной дистилляцией. Вода, используемая для других целей, должна быть дистиллированной или должна иметь эквивалентную степень очистки.
Издание официальное
Необходимо обращать внимание на дату изготовления и срок годности реактивов, указанные изготовителем.
Если используется ферментная суспензия с активностью, отличной от указанной, то объем суспензии, приведенной в схеме определения (7.6.1), должен быть пропорционально увеличен или уменьшен.
Примечание — Реактивы, описанные в 4.4 и в 4.6-4.8 включительно, можно приобрести на рынке в виде наборов для анализа, например тест-набор, изготовленный фирмой Boehringertest kit .
4.1 Раствор гексацианоферрата (II) калия, К4 [Fe(CN)6]
3.6 г гексацианоферрата (II) калия тригидрата растворяют в воде. Доводят объем водой до 100 мл и перемешивают.
4.2 Раствор сульфата цинка, ZnS04
7.2 г гептагидрата сульфата цинка растворяют в воде. Доводят объем водой до 100 мл и перемешивают.
4.3 Раствор гидроокиси натрия, с (NaOH) = 0,1 моль/л
4,0 г гидроокиси натрия растворяют в воде. Доводят объем водой до 1 000 мл и перемешивают.
4.4 Цитратный буферный раствор, pH (6,6 ±0,1)
2,8 г цитрата натрия трехзамещенного двуводного (C6H507Na3-2H20), 0,042 г моногидрата лимонной кислоты (С6Н807 Н20) и 0,625 г сульфата магния гептагидрата (MgS04-7H20) растворяют в 40 мл воды.
Доводят pH раствором серной кислоты (2 моль/л) до (6,6 ±0,1) при температуре 20 °С или раствором гидроокиси натрия (0,1 моль/л). Объем раствора доводят водой до 50 мл и перемешивают.
Раствор можно хранить в холодильнике при температуре от 0 °С до 5 °С в течение 3 мес.
4.5 Фосфатный (КН2Р04) буферный раствор, pH (8,6 ± 0,1)
16.6 г дигидроортофосфата калия растворяют в 80 мл воды. Доводят pH до (8,6 ± 0,1) при температуре 20 °С раствором гидроокиси натрия (1 моль/л). Объем раствора доводят водой до 100 мл и перемешивают.
Раствор можно хранить в холодильнике при температуре от 0 °С до 5 °С в течение 8 нед.
4.6 Буферный раствор 1МАО+/цитрата
25 мг никотинамидадениндинуклеотида (C21H27N7017P2 с содержанием основного вещества около 98 %) растворяют в 5 мл цитратного буферного раствора (4.4).
Раствор можно хранить в течение 3 нед в холодильнике при температуре от 0 °С до 5 °С.
4.7 Суспензия р-галактозидазы (из Escherichia coli), суспензия в растворе сульфата аммония
3,2 моль/л, pH (6,0 ± 0,1)
Активность суспензии р-галактозидазы (ЕС 3.2.1.23) [5] должна быть не менее 60 единиц/мл (субстрат — лактоза при температуре 25 °С). Суспензию можно хранить в холодильнике при температуре от 0 °С до 5 °С в течение 12 мес. Во время использования колба с суспензией должна быть погружена в колотый лед.
Примечание — Установлено, что суспензия р-галактозидазы, которая содержит менее 0,001 % каждой из: p-фруктозидазы, а-галактозидазы, дегидрогеназы глюкозы, а-глюкозидазы и NADH-оксидазы, рассчитанная исходя из удельной активности р-галактозидазы, считается пригодной для использования.
4.8 Суспензия р-галактозидазы дегидрогеназы (из Pseudomonas fluorescens), суспензия в растворе сульфата аммония 3,2 моль/л, pH (6,0 ± 0,1)
Активность суспензии р-галактозидазы дегидрогеназы (ЕС 1.1.1.48) [5] должна быть не менее 8 единиц/мл.
11 Набор для анализа Boehringer test kit является примером коммерчески доступного продукта. Данная информация приводится для удобства пользователей настоящего стандарта и не означает поддержки этого продукта со стороны ISO или IDF.
ГОСТ ISO 5765-2-2016
Суспензию можно хранить в течение 6 мес в холодильнике при температуре от О °С до 5 °С. Во время использования колба с суспензией должна быть погружена в колотый лед.
Примечание — Установлено, что суспензия (3-галактоз ид азы дегидрогеназы, которая содержит менее 0,01 % алкогольдегидрогеназы, менее 0,01 % (3-галактозидазы, менее 0,1 % NADH-оксидазы и ферментов, реагирующих с глюкозой, менее 0,5 % лактат дегидрогеназы, считается пригодной для использования.
4.9 Стандартный раствор лактозы, с (C12H220irH20) = 0,8 мг/мл
Перед использованием моногидрат лактозы высушивают до постоянной массы в термостате при температуре 87 °С.
Растворяют 400 мг сухого моногидрата лактозы в воде. Доводят водой до 500 мл и перемешивают. Раствор можно хранить в холодильнике при температуре от 0 °С до 5 °С в течение 2 дн. Непосредственно перед использованием раствор нагревают до температуры 20 °С.
5 Оборудование
Используют стандартное лабораторное оборудование и дополнительно следующее:
5.1 Аналитические весы, с точностью взвешивания до 1 мг и ценой деления 0,1 мг.
5.2 Стеклянные химические стаканы, номинальной вместимостью 50, 100 и 250 мл.
5.3 Градуированные пипетки, номинальной вместимостью 5 и 10 мл и ценой деления шкалы 0,1 мл.
5.4 Пипетки, номинальной вместимостью 10; 5; 1; 0,2 и 0,05 мл.
5.5 Мерные колбы с одной отметкой, номинальной вместимостью 100 мл.
5.6 Фильтровальная бумага, средней плотности, диаметром 15 см.
5.7 Воронки для фильтрования, диаметром 7 см.
5.8 Спектрометр, позволяющий производить измерения при длине волны 340 нм, оснащенный кюветами с длиной оптического пути 1 см.
5.9 Пластмассовые лопатки, пригодные для перемешивания смеси пробы/фермента в кюветах спектрометра.
5.10 Стеклянные палочки, диаметром 6 мм и длиной 150 мм для смешивания пробы.
5.11 Водяная баня, обеспечивающая поддержание температурного режима от 20 °С до 25 °С, со штативом для размещения кювет спектрометра (5.8) (при необходимости см. 7.6).
Примечание — Выдерживать кюветы на водяной бане необходимо, только если температура в помещении ниже 20 °С.
5.12 Лабораторный блендер, для приготовления суспензий рабочих частей проб плавленого сыра (например, Ultra Turrax 1().
5.13 Термостат, обеспечивающий поддержание температурного режима (87 ± 2) °С.
5.14 Устройство для измельчения или натирания, пригодное для дробления или натирания сыра, легко поддающееся очистке.
6 Отбор проб
Отбор проб не является частью метода, описанного настоящим стандартом. Рекомендуемый метод отбора проб приведен в [1].
Важно, чтобы лаборатория получила пробу, которая является действительно представительной и которая не была повреждена или изменена в процессе транспортирования или хранения.
7 Исследования
7.1 Тест для проверки метода
7.1.1 Следующий тест для проверки восстановления лактозы выполняют в случае, когда имеется хотя бы одно из следующих условий:
а) при использовании новой партии буферного раствора 1\1АО+/цитрата (4.6), новой партии суспензии (З-галактозидазы (4.7) или новой партии суспензии р-галактозидазы дегидрогеназы (4.8);
11 Ultra Turrax — это один из примеров приемлемого, коммерчески доступного продукта. Данная информация приводится для удобства пользователей настоящим стандартом и не означает поддержку этого продукта со стороны ISO или IDF.
3
b) если буферный раствор 1\1АО+/цитрата (4.6), и/или суспензию р-галактозидазы (4.7), и/или суспензию р-галактозидазы дегидрогеназы (4.8) хранили в холодильнике более 2 нед до использования;
c) если был перерыв в проведении анализов;
d) если проведение теста требуют обстоятельства.
7.1.2 При помощи пипетки в две мерные колбы номинальной вместимостью 100 мл (5.5) вносят 5,0 и 10,0 мл стандартного раствора лактозы (4.9). В каждую колбу добавляют по 50 мл воды. Далее действуют согласно 7.5 и 7.6.
7.1.3 Вычисляют содержание моногидрата лактозы в стандартном растворе лактозы (4.9) согласно формуле (3) (см. 8.1), используя следующие значения:
\/3 — объем стандартного раствора лактозы (4.9), \/3 = 500 мл;
V4 — объем использованного стандартного раствора лактозы (7.1.2), V4 = 5 мл и 10 мл соответственно;
V5 — общий объем разведенного стандартного раствора лактозы (7.1.2), V5 = 100 мл.
7.1.4 Принимая во внимание чистоту моногидрата лактозы, восстановление для обоих разведений (7.1.2) должно находиться в диапазоне (100 ± 2) %.
Если восстановление не соответствует указанному диапазону, необходимо проверить реактивы, технику выполнения анализа, точность пипеток и состояние настройки спектрометра. Принимают все необходимые меры для получения соответствующих результатов. Тест для проверки метода повторяют до тех пор, пока не будут получены удовлетворительные результаты.
7.2 Подготовка исследуемой пробы
7.2.1 Сухое молоко и сухие смеси для мороженого
Пробу для исследований помещают в контейнер с герметично закрывающейся крышкой, вместимость которого в два раза больше, чем объем пробы. Контейнер немедленно закрывают. Пробу тщательно перемешивают, многократно встряхивая и переворачивая контейнер.
7.2.2 Плавленый сыр
Удаляют затвердевший, загрязненный или заплесневелый слой сыра, чтобы получить достоверную пробу для исследований в том виде, в котором сыр обычно употребляют в пищу. Пробу для исследований измельчают или растирают при помощи соответствующего приспособления для измельчения или перетирания (5.14). Быстро перемешивают измельченную или растертую массу и, если возможно, проводят повторное измельчение или перетирание. Снова тщательно перемешивают. Если проба для исследований не может быть измельчена или растерта, ее тщательно перемешивают интенсивным встряхиванием и размешиванием.
В случае необходимости хранения до начала проведения анализа пробу для испытаний переносят в контейнер с герметичной крышкой, вместимость которого вдвое превышает объем пробы. Контейнер немедленно закрывают. Принимают все необходимые меры предосторожности для обеспечения надлежащей сохранности пробы для исследований и для предотвращения конденсации влаги на внутренней поверхности контейнера.
После измельчения, перетирания или встряхивания и размешивания или после необходимого хранения полученную пробу для исследований быстро переносят в стеклянный химический стакан номинальной вместимостью 250 мл (5.2). Добавляют такой же объем воды и при помощи лабораторного блендера (5.12) тщательно эмульгируют смесь.
7.3 Исследуемая проба
В химическом стакане номинальной вместимостью 100 мл (5.2) взвешивают 1 г или большее количество (см. ниже) рабочей части пробы (7.2.1) или суспензии рабочей части пробы (7.2.2) с точностью до 1 мг. Рабочую часть пробы при помощи стеклянной палочки (5.10) или лабораторного блендера (5.12) смешивают с 20 мл воды, предварительно нагретой до температуры от 40 °С до 50 °С. Содержимое химического стакана количественно переносят в мерную колбу номинальной вместимостью 100 мл (5.5). Доводят водой примерно до 60 мл и перемешивают.
При определении массы рабочей части пробы учитывают следующие факты:
- рабочая часть пробы должна быть представительной по отношению ко всей исследуемой пробе;
- рекомендуется, чтобы содержание лактозы в кювете спектрометра было в пределах от 5 до 100 мкг;
- значение поглощения А2 раствора в кювете спектрометра для галактозы в рабочей части пробы (см. 8.1) должно находиться в пределах от 0,1 до 0,4;
ГОСТ ISO 5765-2-2016
- если содержание лактозы в пробе меньше 0,2 %, будет необходима рабочая часть пробы массой более чем 1 г. В таком случае объем жира, белка и других веществ, осажденных согласно 7.5.1, может оказывать существенное влияние на объем раствора (см. 1/3 в 8.1).
7.4 Испытание бланка
Испытание бланка проводят дважды. Действуют в соответствии с 7.5 и 7.6, используя все реактивы без внесения рабочей части пробы.
7.5 Удаление белка
7.5.1 В мерную колбу с одной меткой номинальной вместимостью 100 мл с исследуемым раствором или суспензией (7.3) добавляют в следующей последовательности:
- 5,0 мл раствора гексацианоферрата (II) калия (4.1);
- 5,0 мл раствора сульфата цинка (4.2);
- 10,0 мл раствора гидроокиси натрия (4.3).
Все тщательно перемешивают после каждого внесения реактива. Доводят объем водой до метки 100 мл и тщательно перемешивают. Полученной смеси дают отстояться в течение 30 мин.
Содержимое колбы не перемешивают до начала фильтрования.
7.5.2 Отстоявшуюся жидкость фильтруют через фильтровальную бумагу (5.6), первую фракцию фильтрата не используют.
7.6 Определение
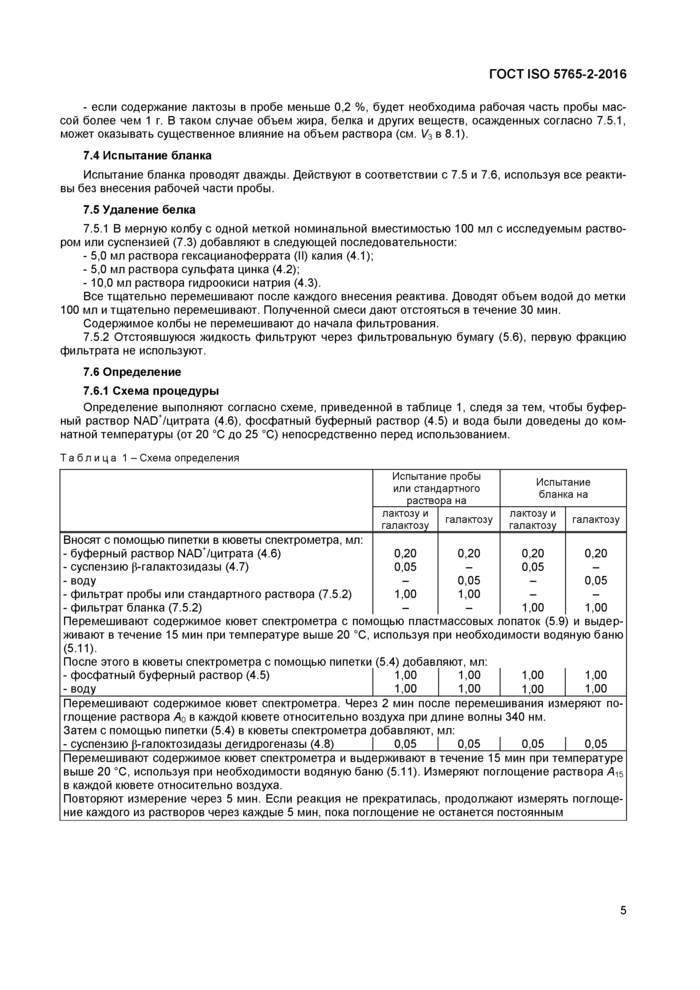
7.6.1 Схема процедуры
Определение выполняют согласно схеме, приведенной в таблице 1, следя за тем, чтобы буферный раствор 1\1АО+/цитрата (4.6), фосфатный буферный раствор (4.5) и вода были доведены до комнатной температуры (от 20 °С до 25 °С) непосредственно перед использованием.
|
Таблица 1- Схема определения | |||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||
|
Перемешивают содержимое кювет спектрометра с помощью пластмассовых лопаток (5.9) и выдерживают в течение 15 мин при температуре выше 20 °С, используя при необходимости водяную баню (5.11). После этого в кюветы спектрометра с помощью пипетки (5.4) добавляют, мл: | ||||||||||
|
Перемешивают содержимое кювет спектрометра. Через 2 мин после перемешивания измеряют поглощение раствора А0 в каждой кювете относительно воздуха при длине волны 340 нм.
Затем с помощью пипетки (5.4) в кюветы спектрометра добавляют, мл:
- суспензию (З-галоктозидазы дегидрогеназы (4.8)_| 0,05 | 0,05 | 0,05 | 0,05
Перемешивают содержимое кювет спектрометра и выдерживают в течение 15 мин при температуре выше 20 °С, используя при необходимости водяную баню (5.11). Измеряют поглощение раствора Я15 в каждой кювете относительно воздуха.
Повторяют измерение через 5 мин. Если реакция не прекратилась, продолжают измерять поглощение каждого из растворов через каждые 5 мин, пока поглощение не останется постоянным
5
7.6.2 Расчет поглощения
7.6.2.1 Если после выдерживания в течение 15 мин не произошло увеличения поглощения, рассчитывают поглощение А для растворов в каждой кювете, по которым ведется расчет (см. 8.1), при помощи следующей формулы:
Д=А-До, О)
где А0 —численное значение поглощения, измеренное до внесения суспензии (З-галоктозидазы дегидрогеназы;
At — численное значение поглощения, измеренное после выдерживания в течение 15 мин.
7.6.2.2 Если после выдерживания в течение 15 мин реакция не прекратилась, рассчитывают поглощение А для растворов в каждой кювете, по которым ведется расчет (см. 8.1), при помощи следующей формулы:
A = (At-A0)--(At -Д_5), (2)
5
где А0 —численное значение поглощения, измеренное до внесения суспензии (З-галоктозидазы дегидрогеназы;
At — численное значение поглощения, измеренное после выдерживания в течение t мин;
At— численное значение поглощения, измеренное после выдерживания в течение t- 5 мин.
7.6.3 Проверка
Если поглощение А превышает 0,500, процедуру повторяют в соответствии 7.6.1 и 7.6.2, разбавив фильтрат (7.5.2) водой.
8 Расчет и выражение результатов
8.1 Расчет
Содержание лактозы WL рассчитывают по формуле
[(Д-Д3)-(А2-Л4)]хМг
WL =■
К х /
хЦхЦхЦх
100
т
(3)
где WL — массовая доля лактозы, %;
— численное значение поглощения (рассчитанное согласно 7.6.2) пробы или стандартного раствора на лактозу и галактозу;
— численное значение поглощения (рассчитанное согласно 7.6.2) пробы или стандартного раствора на галактозу;
— численное значение поглощения (рассчитанное согласно 7.6.2) бланка на лактозу и галактозу;
— численное значение поглощения (рассчитанное согласно 7.6.2) бланка на галактозу;
— относительная молярная масса лактозы:
- для безводной лактозы Мг = 342,30 г/моль;
- для моногидрата лактозы Мг = 360,31 г/моль;
— коэффициент молярного поглощения NADH при длине волны 340 нм (т. е. К = 6,3 х х 106 см^/моль);
— численное значение теоретической длины оптического пути кюветы спектрометра (1 см), см;
— общий объем жидкости в кювете спектрометра согласно (7.6.1) (3,30 мл), мл;
— объем фильтрата (7.5.2) или его разведения (7.6.3), добавленного в кювету спектрометра (1,0 мл), мл;
— объем раствора, приготовленного согласно 7.5.1 (100 мл), мл;
— объем фильтрата (7.5.2), взятого для разбавления (7.6.3) при необходимости, мл;
— объем, до которого был разведен контрольный раствор (7.6.3), при необходимости, мл;
— масса рабочей части пробы (7.3), г.
Если значение А2 - Ал получилось отрицательным, его учитывают.
Примечание — Если масса рабочей части пробы больше 1 г, \/з рассчитывают по формуле
Уз = 100 - Р, (4)
где Р— объем осадка, мл.
Р рассчитывают из приблизительного состава рабочей части пробы при помощи формулы:
Р= 1,1 х (жир, г) + 0,73 х (белок, г) + 0,65 х (крахмал, г) + 0,55 х (нерастворимая зола, г).
WL
А^
А?
Ал
Мг
К
I
У
V2
Уз
Ул
Уъ
т
6
ГОСТ ISO 5765-2-2016
8.2 Выражение результатов
Результаты округляют с точностью до третьего знака после запятой.
9 Прецизионность
9.1 Межлабораторное испытание
Информация о межлабораторном испытании для определения прецизионности метода опубликована (см. [6]).
Значения пределов повторяемости и воспроизводимости, полученные в результате межлабораторного испытания, определяют в соответствии с [3]. Полученные значения не могут быть применены к другим диапазонам концентраций и веществ, кроме приведенных в настоящем стандарте.
Примечание — В [4] содержится конкретное руководство для проведения межлабораторных испытаний по методам анализа молочных продуктов, которое основано на [2] и [3].
9.2 Повторяемость
Абсолютное расхождение между результатами двух независимых испытаний, полученных в результате использования одного и того же метода на идентичном исследуемом материале в одной и той же лаборатории одним и тем же лаборантом, используя одно и то же оборудование, в течение короткого промежутка времени, не должно превышать более чем в 5 % случаев:
- 3 % среднеарифметического значения результатов исследований — для сухого молока и сухих смесей для мороженого;
- 6 % среднеарифметического значения результатов испытаний —для плавленого сыра.
9.3 Воспроизводимость
Абсолютное расхождение между результатами двух независимых испытаний, полученных в результате использования одного метода на идентичной исследуемой пробе в разных лабораториях разными лаборантами на различном оборудовании, не должно превышать более чем в 5 % случаев:
- 6 % среднеарифметического значения результатов исследований — для сухого молока и сухих смесей для мороженого;
-14 % среднеарифметического значения результатов испытаний —для плавленого сыра.
10 Протокол испытаний
Протокол испытаний должен содержать:
a) всю информацию, необходимую для полной идентификации пробы;
b) метод отбора проб, который использовали, если он известен;
c) используемый метод испытания вместе со ссылкой на настоящий стандарт;
d) все подробности проведения испытания, не указанные в настоящем стандарте или указанные как необязательные, вместе со сведениями обо всех случаях, которые могли повлиять на результат (ы) испытания;
e) полученный (ые) результат (ы) испытания или, если была проверена повторяемость, полученный окончательный результат.
7