ГОСТ ISO 22717-2013
Продукция парфюмерно-косметическая. Микробиология. Обнаружение Pseudomonas aeruginosa
Устанавливает общие требования к методу обнаружения и идентификации специфического микроорганизма Pseudomonas aeruginosa в парфюмерно-косметической продукции.
Идентичен ISO 22717:2006
Оглавление
1 Область применения
2 Нормативные ССЫЛКИ
3 Термины и определения
4 Принцип
5 Разбавители и питательные среды
6 Инструменты И стеклянная лабораторная посуда
7 Штаммы микроорганизмов
8 Обращение с парфюмерно-косметической продукцией и лабораторными пробами
9 Методика
10 Выражение результатов
11 Нейтрализация антимикробных свойств продукции
12 Протокол испытания
Приложение А (справочное) Другие бульоны для обогащения
Приложение В (справочное) Нейтрализаторы антимикробной активности консервантов и промывные жидкости
Библиография
Приложение Д.А (справочное) Сведения о соответствии межгосударственного стандарта ссылочному международному стандарту
19 страниц
| Дата введения | 01.01.2014 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Завершение срока действия | 27.07.2018 |
| Актуализация | 01.01.2021 |
Организации:
| 25.03.2013 | Утвержден | Евразийский совет по стандартизации, метрологии и сертификации | 55-П |
|---|---|---|---|
| 29.05.2013 | Утвержден | Госстандарт Республики Беларусь | 27 |
| Разработан | БелГИМ | ||
| Издан | БелГИСС | 2013 г. |
Perfume and cosmetics products. Microbiology. Detection of Pseudomonas aeruginosa
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13

стр. 14
стр. 15

стр. 16
стр. 17

стр. 18

стр. 19
МКС 07.100.99; 71.100.70
|
к ГОСТ ISO 22717-2013 Продукция парфюмерно-косметическая. Микробиология. Обнаружение Pseudomonas aeruginosa | ||||||||||
| ||||||||||
|
(ИУ ТИПА №3-2018) | ||||||||||
государственный стандарт
РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКЦИЯ ПАРФЮМЕРНО-КОСМЕТИЧЕСКАЯ. МИКРОБИОЛОГИЯ
Обнаружение Pseudomonas aeruginosa
ПРАДУКЦЫЯ ПАРФЮМЕРНА-КАСМЕТЫЧНАЯ. М1КРАБ1ЯЛОГ1Я
Выяуленне Pseudomonas aeruginosa
(ISO 22717:2006, IDT)
Издание официальное
Г осстандарт Минск
|
Таблица 1 - Морфологические характеристики Pseudomonas aeruginosa на селективной среде | ||||
|
9.4.2 Идентификация Pseudomonas aeruginosa
9.4.2.1 Общие положения
Проводят дальнейшее подтверждение подозрительных колоний, изолированных на питательном агаре с цетримидом. Наличие Pseudomonas aeruginosa может быть подтверждено различными культуральными и биохимическими тестами.
9.4.2.2 Окраска по Г раму
Следуют процедуре, установленной в ISO 21148. Проверяют наличие грамотрицательных палочек.
9.4.2.3 Оксидазный тест
Следуют процедуре, установленной в ISO 21148.
Проверяют наличие оксидазаположительных колоний.
3.4.2.4 Культивирование на агаризованной Pseudomonas aeruginosa среде для обнаружения пиоцианина
Проводят посев на поверхность агаризованной Pseudomonas aeruginosa среды для обнаружения пиоцианина подозрительных колоний, выращенных на питательном агаре с цетримидом, так, чтобы образовались изолированные колонии. Инкубируют при температуре (32,5 ± 2,5) °С.
Проверяют наличие роста бактерий после 24, 48 и 72 ч. Pseudomonas aeruginosa формирует колонии, окруженные зоной от голубого до зеленого цвета в результате образования пиоцианина или зоной от красного до темно-коричневого цвета в результате образования флуоресцентного пигмента.
10 Выражение результатов
Если при идентификации колоний подтверждено наличие данного вида, результат представляют как: бактерии вида Pseudomonas aeruginosa обнаружены в навеске S пробы.
Если после обогащения роста не наблюдалось и/или если идентификация колоний не подтвердила наличие данного вида, результат представляют как: бактерии вида Pseudomonas aeruginosa не обнаружены в навеске S пробы.
11 Нейтрализация антимикробных свойств продукции
11.1 Общие положения
Описанные ниже процедуры демонстрируют, что микроорганизмы могут расти в условиях проведения анализа.
11.2 Приготовление инокулята
Перед проведением испытания засевают поверхность среды, содержащей соевый и казеиновый гидролизаты (SCDA), или другой подходящей среды (неселективной и не оказывающей нейтрализующее действие) штаммом Pseudomonas aeruginosa. Инкубируют чашки при температуре (32,5 ± 2,5) °С в течение 18 -24 ч.
Стерильной петлей штриховыми движениями снимают с поверхности среды выросшие колонии и ресуспендируют в разбавителе для приготовления калиброванной суспензии с концентрацией клеток 1х10в КОЕ/см3 [(количество клеток можно измерить, используя спектрофотометр, см. ISO 21148:2005 (приложение С)].
Калиброванную суспензию и ее разведения используют в течение 2 ч.
11.3 Валидация метода обнаружения
11.3.1 Процедура
11.3.1.1 В пробирках, содержащих по 9 см3 разбавителя, готовят разведения калиброванной суспензии, чтобы в конечном счете получить концентрацию микроорганизмов, равную 100-500 КОЕ/см3. Для подсчета окончательного количества жизнеспособных микроорганизмов в разведенной калиброванной суспензии вносят 1 см3 суспензии в чашку Петри и заливают 1
15-20 см3 расплавленной агаризованной среды. Температура расплавленной среды поддерживается с помощью водяной бани на уровне не более 48 °С. Дают среде в чашках застыть, а затем инкубируют при температуре (32,5 ± 2,5) °С в течение 20 - 24 ч.
11.3.1.2 Выполняют два параллельных приготовления (две повторности) исходной суспензии пробы в пробирке или колбе, соблюдая выбранные для анализа условия (не менее 1 г или 1 см3 испытуемой продукции и определенный объем бульона для обогащения). Если используют метод мембранной фильтрации, то фильтруют в двух повторностях не менее 1 см3 испытуемой продукции и переносят каждый мембранный фильтр в пробирку или колбу, содержащую бульон для обогащения в условиях, выбранных для теста.
11.3.1.3 Стерильно вносят 0,1 см3 разведенной калиброванной суспензии (11.3.1.1) тест-культуры Pseudomonas aeruginosa в одну пробирку или колбу (валидированный тест). Перемешивают, затем инкубируют обе пробирки или колбы (валидированный тест и контроль неконтаминированной пробы) при температуре (32,5 ± 2,5) °С в течение 20 - 24 ч.
11.3.1.4 Проводят выделение для каждой пробирки или колбы (валидационный тест и контроль неконтаминированной пробы). Используя стерильную петлю, делают высев методом истощающего штриха на поверхность агаризованной среды с цетримидом, разлитой в чашки Петри (диаметр от 85 до 100 мм) в количестве приблизительно 15 - 20 см3. Инкубируют при температуре (32,5 ± 2,5) °С в течение 20 - 24 ч.
11.3.2 Интерпретация результатов валидации
Проверяют, что разведенная калиброванная суспензия бактерий вида Pseudomonas aeruginosa (11.3.1.1) содержит от 100 до 500 КОЕ/см3 микроорганизмов.
Нейтрализация и метод обнаружения являются достоверными, когда ростовые характеристики Pseudomonas aeruginosa наблюдаются у микроорганизмов, выросших на чашке с высевом из обогащения пробы, контаминированной калиброванной суспензией, и отсутствует рост на чашке с высевом из обогащения неконтаминированной пробы.
Когда обнаружен рост на чашке с высевом из обогащения неконтаминированной пробы (естественно контам ин и рован ная продукция), нейтрализация и метод обнаружения являются достоверными, если бактерии вида Pseudomonas aeruginosa выделены на чашке Петри с высевом из обогащения пробы, контаминированной калиброванной суспензией.
Отсутствие роста на чашках Петри с высевом из обогащения пробы, контаминированной калиброванной суспензией, указывает на то, что антимикробная активность все еще не нейтрализована и требуется изменение условий метода путем увеличения объема питательного бульона, при этом количество продукции остается тем же, или путем добавления большего количества инактивирующего вещества в бульон для обогащения, или путем подбора условий, которые позволят выделить Pseudomonas aeruginosa.
Если, несмотря на введение подходящих инактивирующих веществ и значительное увеличение объема бульона, все еще невозможно выделить жизнеспособные культуры, как описано выше, это указывает на малую вероятность контаминации продукции бактериями вида Pseudomonas aeruginosa.
12 Протокол испытания
Протокол испытания должен содержать:
a) всю информацию, необходимую для полной идентификации продукции;
b) используемый метод;
c) полученные результаты;
d) все детали приготовления исходной суспензии;
e) описание метода с указанием использованных нейтрализующих веществ и питательных сред;
f) валидацию метода, даже если испытание было выполнено отдельно;
д) любые моменты, не указанные в настоящем стандарте или рассматриваемые как необязательные, вместе с деталями, которые могут повлиять на полученные результаты. 2
Приложение А
(справочное)
Другие бульоны для обогащения
А1 Среда, содержащая соевый и казеиновый гидролизаты, лецитин и полисорбат80 (SCDLP 80 бульон)
А. 1.1 Состав
- казеиновый пептон - 17,0 г;
- соевый пептон - 3,0 г;
- хлорид натрия - 5,0 г;
- двузамещенный фосфат калия - 2,5 г;
- глюкоза - 2,5 г;
-лецитин -1,0 г;
- полисорбат 80-7,0 г;
- вода -1 000 см3.
А. 1.2 Приготовление
Последовательно растворяют все компоненты (или готовую сухую среду) в кипящей воде до их полного растворения. Разливают среду в подходящую лабораторную посуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин.
После стерилизации и охлаждения pH среды должен быть равен 7,2 ± 0,2 при измерении при комнатной температуре.
А.2 D/Е нейтрализующий бульон (Dey/Engley нейтрализующий бульон) [7]
А. 2.1 Состав
- глюкоза -10,0 г;
- соевый лецитин - 7,0 г;
- пятиводный тиосульфат натрия - 6,0 г;
- полисорбат 80-5,0 г;
- панкреатический гидролизат казеина - 5,0 г;
- гидросульфит натрия - 2,5 г;
- дрожжевой экстракт - 2,5 г;
- тиогликолят натрия -1,0 г;
- краситель бромкрезоловый пурпурный - 0,02 г;
- вода -1 000 см3.
А.2.2 Приготовление
Последовательно растворяют все компоненты (или готовую сухую среду) в кипящей воде до их полного растворения. Разливают среду в подходящую лабораторную посуду. Стерилизуют в автоклаве при 121 °С в течение 15 мин.
После стерилизации и охлаждения pH среды должен быть равен 7,6 ± 0,2 при измерении при комнатной температуре.
А.З Модифицированный Letheen бульон А. 3.1 Состав
- пептический перевар мяса - 20,0 г;
- панкреатический гидролизат казеина - 5,0 г;
- говяжий экстракт - 5,0 г;
- дрожжевой экстракт - 2,0 г;
- лецитин - 0,7 г;
- полисорбат 80 - 5,0 г; 3
-хлорид натрия - 5,0 г;
- бисульфит натрия - 0,1 г;
-вода - 1 ООО см3.
А.3.2 Приготовление
Последовательно растворяют в кипящей воде полисорбат 80 и лецитин до их полного растворения. Растворяют остальные компоненты, помешивая при нагревании. Перемешивают осторожно во избежание пенообразования. Разливают среду в подходящую лабораторную посуду. Стерилизуют в автоклаве при 121 °С в течение 15 мин.
После стерилизации и охлаждения pH среды должен быть равен 7,2 ± 0,2 при измерении при комнатной температуре. 4
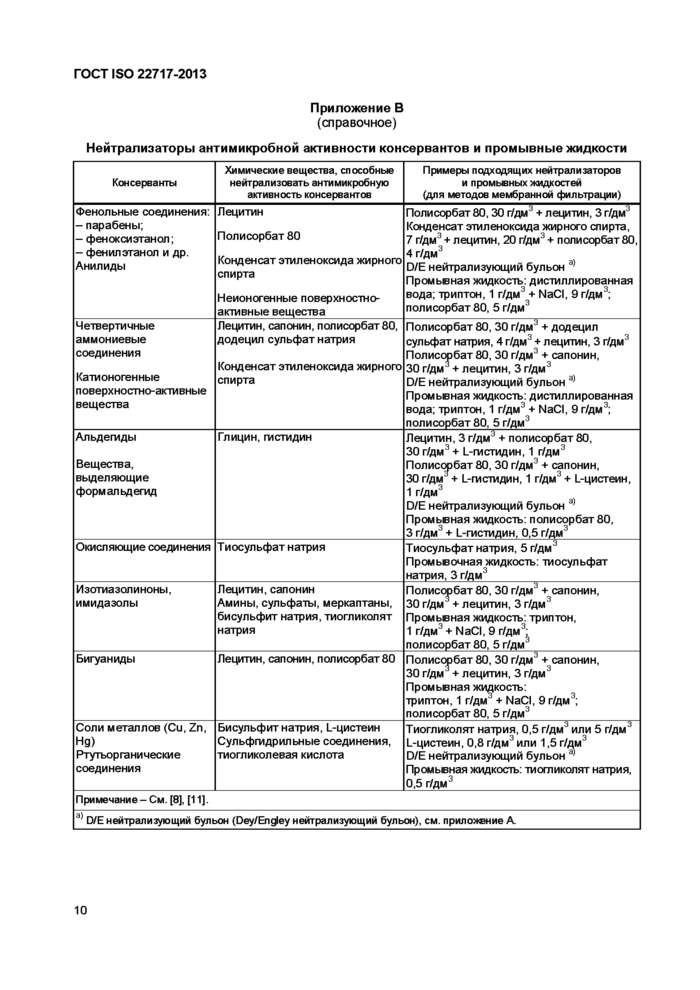
Приложение В
(справочное)
|
Нейтрализаторы антимикробной активности консервантов и промывные жидкости | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
[1]
[2]
[3]
[4]
[5]
[6]
[7]
[8]
Библиография
СО LI РА, Guidelines on Microbial Quality Management, published by the European Cosmetic,
Toiletry and Perfumery Association, 1997
(Руководство по менеджменту качества в микробиологии)
CTFA, Microbiology Guidelines, published by the Cosmetic, Toiletry and Fragrance Association ISBN 1-882621-32-8, 2001 (Руководство по микробиологии)
E P, Microbiological Examination of non-sterile products, 4th edition, published by the European Pharmacopoeia, 2002
(Микробиологическая экспертиза нестерильной продукции)
FDA, Bacteriological Analytical Manual, 8th edition, published by the U.S. Food and Drug Administration, 1995, http ://www. cfsan .fd a. q ov/~ eb am /bam-23. htm I (Руководство по бактериологическому анализу)
JP 14, General Tests - Microbial Limit test, published by the Japanese Pharmacopoeia, 2001 (Общие испытания. Испытания на предельное содержание микроорганизмов)
USP 28, Microbial Limit test (61), published by the U.S. Pharmacopoeia, 2005 [Испытания на предельное содержание микроорганизмов (61)]
Atlas, R.M. FI and book of Microbiological Media, CRC Press, ISBN 0-8493-2944-2,1993 (Справочник по микробиологическим средам)
Singer, S. The Use of Preservative Neutralizers in Diluents and Plating Media, Cosmetics and Toiletries, 102, 55, December 1987
[9]
(Применение нейтрализаторов консервантов в разбавителях и средах для чашек Петри, косметике и туалетных принадлежностях)
ISO 21149:2006 Cosmetics - Microbiology - Enumeration and detection of aerobic meso-philic bacteria
[10]
(Косметика. Микробиология. Подсчет и обнаружение аэробных мезо-филических бактерий)
ISO 18415:2007 Cosmetics - Microbiology - Detection of specified microorganisms (Staphylococcus aureus, Escherichia coli, Pseudomonas aeruginosa, Candida albicans,) and non-specified microorganisms
[11]
(Косметика. Микробиология. Обнаружение специфических и неспецифических микроорганизмов)
EN 1040:2005 Chemical disinfectants and antiseptics - Basic bactericidal activity - Test method and requirements (phase 1)
[Средства дезинфицирующие химические и антисептики. Количественный суспензионный метод испытания для оценки основной бактерицидной активности химических дезинфицирующих и антисептических средств. Метод испытания и требования (фаза 1)]
11
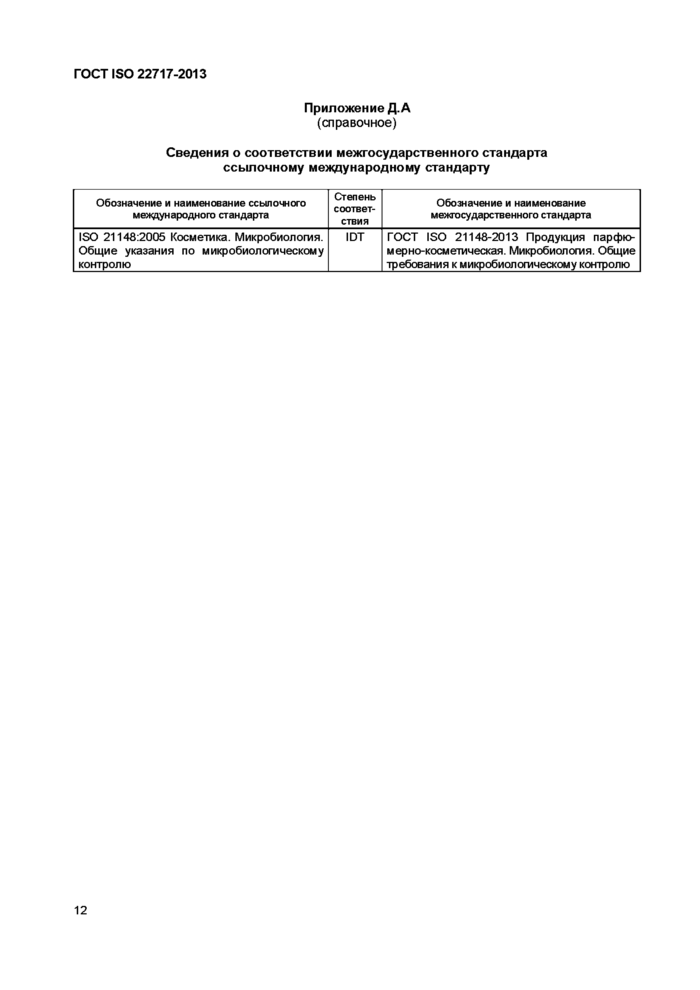
Приложение Д.А
(справочное)
Сведения о соответствии межгосударственного стандарта ссылочному международному стандарту
|
Обозначение и наименование ссылочного меэдународного стандарта |
Степень соответ ствия |
Обозначение и наименование межгосударственного стандарта |
|
ISO 21148:2005 Косметика. Микробиология. Общие указания по микробиологическому контролю |
ют |
ГОСТ ISO 21148-2013 Продукция парфюмерно-косметическая. Микробиология. Общие требования к микробиологическому контролю |
12
УДК 665.57/.58:579.873.62.083.12(083.74)(476) МКС 07.100.99; 71.100.70 ЮТ
Ключевые слова: продукция парфюмерно-косметическая, микробиологические исследования, микроорганизмы, разбавители, питательные среды, штаммы микроорганизмов
13
Ответственный за выпуск Т. В. Варивончик
Сдано в набор 01.07.2013. Подписано в печать 31.07.2013. Формат бумаги 60x84/8. Бумага офсетная. Гарнитура Arial. Печать ризографическая. Уел. печ. л. 2,09. Уч.- изд. л. 0,84. Тираж 7 экз. Заказ 711
Издатель и полиграфическое исполнение: Научно-производственное республиканское унитарное предприятие «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) Л И № 02330/0552843 от 08.04.2009. ул. Мел ежа, 3, комн. 406, 220113, Минск.
Предисловие
Евразийский совет по стандартизации, метрологии и сертификации (ЕАСС) представляет собой региональное объединение национальных органов по стандартизации государств, входящих в Содружество Независимых Государств. В дальнейшем возможно вступление в ЕАСС национальных органов по стандартизации других государств.
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2009 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены»
Сведения о стандарте
1 ПОДГОТОВЛЕН республиканским унитарным предприятием «Белорусский государственный институт метрологии» (БелГИМ)
2 ВНЕСЕН Государственным комитетом по стандартизации Республики Беларусь
3 ПРИНЯТ Евразийским советом по стандартизации, метрологии и сертификации по переписке (протокол № 55-П от 25 марта 2013 г.) 5 6 7
|
За принятие стандарта проголосовали: | |||||||||||||||||||||
|
Содержание
1 Область применения............................................................................................................................1
2 Нормативные ссылки...........................................................................................................................1
3 Термины и определения......................................................................................................................1
4 Принцип.................................................................................................................................................2
5 Разбавители и питательные среды....................................................................................................2
6 Инструменты и стеклянная лабораторная посуда............................................................................4
7 Штаммы микроорганизмов..................................................................................................................4
8 Обращение с парфюмерно-косметической продукцией и лабораторными пробами....................5
9 Методика...............................................................................................................................................5
10 Выражение результатов......................................................................................................................6
11 Нейтрализация антимикробных свойств продукции.........................................................................6
12 Протокол испытания.............................................................................................................................7
Приложение А (справочное) Другие бульоны для обогащения............................................................8
Приложение В (справочное) Нейтрализаторы антимикробной активности консервантов
и промывные жидкости.................................................................................................10
Библиография..........................................................................................................................................11
Приложение Д.А (справочное) Сведения о соответствии межгосударственного стандарта
ссылочному международному стандарту................................................................12
Введение
Микробиологические исследования парфюмерно-косметической продукции должны выполняться согласно соответствующему анализу степени микробиологического риска, для того чтобы обеспечить ее качество и безопасность для потребителей.
Анализ микробиологического риска зависит от таких параметров, как:
- возможное изменение парфюмерно-косметической продукции;
- патогенность микроорганизмов;
-область нанесения парфюмерно-косметической продукции (волосы, кожа, глаза, слизистые оболочки и т. п.);
- тип потребителей (взрослые, дети, включая детей до 3 лет).
Для парфюмерно-косметической и другой аналогичной продукции является важным обнаружение кожных болезнетворных микроорганизмов, таких как Staphylococcus aureus, Pseudomonas aeruginosa и Candida albicans. Обнаружение других видов микроорганизмов также может представлять интерес, поскольку эти микроорганизмы (включая индикаторы фекального загрязнения, например Escherichia coli) указывают на несоблюдение гигиенических требований в процессе производства.
IV
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКЦИЯ ПАРФЮМЕРНО-КОСМЕТИЧЕСКАЯ. МИКРОБИОЛОГИЯ Обнаружение Pseudomonas aeruginosa
ПРАДУКЦЫЯ ПАРФЮМЕРНА-КАСМЕТЫЧНАЯ. М1КРАБ1ЯЛОГ1Я Выяуленне Pseudomonas aeruginosa
Perfume and cosmetic products Microbiology Detection of Pseudomonas aeruginosa
Дата введения 2014-01-01
1 Область применения
Настоящий стандарт устанавливает общие требования к методу обнаружения и идентификации специфического микроорганизма Pseudomonas aeruginosa в парфюмерно-косметической продукции.
Чтобы обеспечить качество и безопасность продукции для потребителя, рекомендуется проводить соответствующий анализ микробиологического риска с целью определения видов парфюмернокосметической продукции, к которой применим настоящий стандарт. К продукции с низкой степенью микробиологического риска относится продукция с низкой водной активностью, продукция на спиртовой основе, продукция с крайними значениями pH и т. д.
Метод, описанный в настоящем стандарте, основан на обнаружении Pseudomonas aeruginosa в неселективной жидкой среде (бульоне для обогащения) с последующим выделением микроорганизмов на селективной агаризованной среде. Можно применять и другие методы в зависимости от требуемого уровня обнаружения.
Примечание - Для обнаружения Pseudomonas aeruginosa субкультуры могут быть пересеяны на неселективные питательные среды с последующей поэтапной идентификацией (например, с помощью идентификационных тестов).
Из-за большого разнообразия парфюмерно-косметической продукции в рассматриваемой области применения отдельные детали данного метода могут быть непригодными для некоторых видов продукции (например, для нерастворимой в воде продукции). Могут применяться другие международные стандарты (например, [10]). Установленный в настоящем стандарте метод испытания можно заменить другими методами (например, автоматизированными) при условии, что продемонстрирована их равнозначность или что альтернативный метод валидирован иным образом.
2 Нормативные ссылки
Для применения настоящего стандарта необходимы следующие ссылочные стандарты. Для датированных ссылок применяют только указанное издание ссылочного стандарта, для недатированных ссылок применяют последнее издание ссылочного стандарта (включая все его изменения).
ISO 21148:2005 Косметика. Микробиология. Общие требования к микробиологическому контролю
EN 12353:2006 Средства дезинфицирующие химические и антисептики. Сохранение микроорганизмов для испытаний, используемых для определения бактерицидной, микобакгерицидной, споро-цидной и фунгицидной активности
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 продукция (product): Часть идентифицированной парфюмерно-косметической продукции, полученная лабораторией для испытания (анализа).
Издание официальное
3.2 проба (sample): Часть продукции не менее 1 г или 1 см3, которая используется при проведении испытаний для приготовления исходной суспензии.
3.3 исходная суспензия (initial suspension): Суспензия (или раствор) пробы в определенном объеме соответствующего бульона для обогащения.
3.4 разведение (я) проб (ы) [ample dilution (s)]: Разведение (я) исходной суспензии.
3.5 специфические микроорганизмы (specified microorganisms): Мезофильные аэробные бактерии или дрожжи, нежелательные в парфюмерно-косметической продукции, которые способны вызывать инфекции на коже человека или в области глаз или являются признаком нарушения гигиенических требований в процессе производства.
3.6 Pseudomonas aeruginosa (Pseudomonas aeruginosa): Подвижные грамотрицательные палочки, имеющие гладкие колонии, окрашенные в коричневый или зеленоватый цвет.
Примечания
1 Основные характеристики для идентификации: рост на селективной агаризованной среде с цетримидом, наличие оксидазы, продуцирование флуоресцентных пигментов, способных к диффузии, и растворимого пигмента феназинового ряда (пиоцианина) на подходящей среде.
2 Бактерии вида Pseudomonas aeruginosa могут быть выделены из разнообразных источников окружающей среды, особенно из воды. Они могут нанести вред различным субстратам. Они также могут вызвать инфекции на коже человека или в области глаз. Этот вид неприемлем в парфюмерно-косметической продукции по причине своей потенциальной болезнетворности, а также из-за способности оказывать воздействие на физико-химические свойства парфюмерно-косметической продукции.
3.7 бульон для обогащения (enrichment broth): Неселективная жидкая питательная среда, содержащая соответствующие нейтрализаторы и/или диспергирующие вещества и валидированная для испытуемой продукции.
4 Принцип
Первым этапом испытания является обогащение в неселективной питательной среде (бульоне) для увеличения числа микроорганизмов без риска подавления селективными ингредиентами, которые присутствуют в селективной/дифференциальной среде.
Второй этап испытания (выделение) выполняется на селективной среде с последующей идентификацией.
Возможное подавление микробного роста пробой должно быть нейтрализовано для обеспечения обнаружения жизнеспособных микроорганизмов [1]. Во всех случаях и независимо от применяемой методики нейтрализация антимикробных свойств должна быть проверена и валидирована [2] - [4].
5 Разбавители и питательные среды
5.1 Общие положения
Общие рекомендации приведены в ISO 21148. Если в настоящем стандарте упоминается вода, то это означает, что применяют дистиллированную или очищенную воду, как установлено в ISO 21148.
Бульон для обогащения используют для диспергирования пробы и увеличения первоначальной микробной популяции. Он может содержать нейтрализаторы, если испытуемая проба обладает антимикробными свойствами. Эффективность нейтрализации должна быть продемонстрирована (см. раздел 11). Информация относительно подходящих нейтрализаторов приведена в приложении В.
Бульон для обогащения пригоден для контроля наличия Pseudomonas aeruginosa согласно настоящему стандарту при условии, что он валидирован в соответствии с разделом 11.
Можно использовать другие разбавители и питательные среды, если была продемонстрирована их пригодность.
5.2 Разбавители для бактериальной суспензии (раствор хлорида натрия с трипгоном)
5.2.1 Общие положения
Разбавитель используют для приготовления бактериальной суспензии, применяемой для процедуры подтверждения метода (см. раздел 11).
5.2.2 Состав
- трип тон, панкреатический гидролизат казеина -1,0 г;
- хлорид натрия - 8,5 г;
- вода -1 ООО см3.
5.2.3 Приготовление
Растворяют компоненты в воде, перемешивая их при нагревании. Разливают в подходящую лабораторную посуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин.
После стерилизации и охлаждения раствора pH должен быть равен 7,0 ± 0,2 при измерении при комнатной температуре.
5.3 Питательные среды5.3.1 Общие положения
Питательные среды могут быть приготовлены, как указано ниже или из готовой сухой питательной среды согласно инструкциям изготовителя. Должны соблюдаться инструкции поставщика среды.
Примечание - Готовые к применению среды можно использовать* если их состав и/или ростовые свойства сопоставимы с данными, приведенными ниже.
5.3.2 Агаризованная среда для подтверждения [агаризованная среда с соевым и казеиновым гидролизатами (SCDA) или триптон-соевый агар (TSA)]5.3.2.1 Состав
- панкреатический гидролизат казеина -15,0 г;
- папаиновый гидролизат соевой муки - 5,0 г;
-хлорид натрия - 5,0 г;
-агар -15,0 г;
-вода - 1 000 см8.
5.3.2.2 Приготовление
Компоненты или готовую сухую среду растворяют в воде, перемешивая при нагревании. Разливают среду в подходящую лабораторную посуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин.
После стерилизации и охлаждения pH среды должен быть равен 7,3 ± 0,2 при измерении при комнатной температуре.
5.3.3 Бульон для обогащения5.3.3.1 Бульон Eugon LT 1005.3.3.1.1 Общие положения
5.3.3.1.1 Общие положения
Данная среда содержит ингредиенты (лецитин и полисорбат 80), которые нейтрализуют ингибирующие вещества, присутствующие в пробе, а также диспергирующий агент окгоксинол 9.
5.3.3.1.2 Состав
- панкреатический гидролизат казеина -15,0 г;
- папаиновый гидролизат соевой муки - 5,0 г;
- L-цистин - 0,7 г;
-хлорид натрия - 4,0 г;
- сульфит натрия - 0,2 г;
- глюкоза - 5,5 г;
- яичный лецитин - 1,0 г;
- полисорбат 80 - 5,0 г;
- окгоксинол 9 - 1,0 г;
-вода - 1 000 см8.
5.3.3.1.3 Приготовление
Последовательно растворяют компоненты (полисорбат, окгоксинол 9 и яичный лецитин) в кипящей воде до их полного растворения. Остальные компоненты растворяют в воде, перемешивая при нагревании. Разливают в подходящую лабораторную посуду. Стерилизуют в автоклаве при температуре 121 °С в течение 15 мин.
После стерилизации и охлаждения pH среды должен быть равен 7,0 ± 0,2 при измерении при комнатной температуре.
5.3.3.2 Другие бульоны для обогащения
Можно использовать и другие подходящие бульоны для обогащения (см. приложение А).
5.3.4 Селективная агаризованная среда для вьщеления Pseudomonas aeruginosa5.3.4.1 Питательный агар с цетримидом5.3.4.1.1 Состав
5.3.4.1.1 Состав
- панкреатический гидролизат желатина - 20,0 г;
- хлорид магния -1,4 г;
- сульфат калия -10,0 г;
- цетримид (бромид цетилтриметиламония) - 0,3 г;
- агар -13,6 г;
- глицерин -10,0 см3;
- вода -1 000 см3.
5.3.4.1.2 Приготовление
Растворяют в воде все твердые компоненты и добавляют глицерин. Нагревают при интенсивном перемешивании и кипятят в течение 1 мин до полного растворения.
Разливают в подходящую лабораторную посуду и стерилизуют при 121 °С в течение 15 мин. После стерилизации и охлаждения pH среды должен бьпъ равен 7,2 ± 0,2 при измерении при комнатной температуре.
5.3.5 Селективная агаризованная среда для подтверждения Pseudomonas aeruginosa5.3.5.1 Агаризованная среда для обнаружения пиоцианина (Pseudomonas agar Р)5.3.5.1.1 Состав
5.3.5.1.1 Состав
- панкреатический гидролизат желатина - 20,0 г;
- хлорид магния -1,4 г;
- сульфат калия -10,0 г;
- агар -15,0 г;
- глицерин -10,0 см3;
- вода -1 000 см3.
5.3.5.1.2 Приготовление
Растворяют в воде все твердые компоненты и добавляют глицерин. Нагревают при интенсивном перемешивании и кипятят в течение 1 мин до полного растворения.
Разливают в подходящую лабораторную посуду и стерилизуют при температуре 121 °С в течение 15 мин.
После стерилизации и охлаждения pH среды должен быть равен 7,2 ± 0,2 при измерении при комнатной температуре.
6 Инструменты и стеклянная лабораторная посуда
Лабораторное оборудование, инструменты и стеклянная посуда должны соответствовать ISO 21148.
7 Штаммы микроорганизмов
Для валидации условий испытаний используют следующие референсные штаммы:
Pseudomonas aeruginosa АТСС 9027 (или эквивалентные штаммы: CIP9 10 82118, или NCIMB 11 8626, или NBRC 12 13275, или КСТС 13 2513, или другой эквивалентный штамм из национальной коллекции).
Культуру следует восстановить согласно процедурам, представленным поставщиком референс-ного штамма.
Штамм разрешается хранить в лаборатории в соответствии с EN 12353.
8 Обращение с парфюмерно-косметической продукцией и лабораторными пробами
При необходимости продукцию, подлежащую испытаниям, хранят при комнатной температуре.
Не следует выдерживать в термостате, охлаждать и замораживать продукцию и пробы ни до, ни после анализа.
Отбор и подготовку проб парфюмерно-косметической продукции для анализа следует проводить в соответствии с ISO 21148. Анализируют пробы согласно ISO 21148 и методике, приведенной в разделе 9.
9 Методика
9.1 Общие положения
Для подготовки пробы, приготовления исходной суспензии и разведений используют стерильные материалы, оборудование и асептические методы. В случае приготовления исходной суспензии в подходящем разбавителе время между окончанием приготовления суспензии и моментом ее внесения в бульон для обогащения не должно превышать 45 мин, если иное не оговорено в соответствующих протоколах или документах.
9.2 Приготовление исходной суспензии в бульоне для обогащения9.2.1 Общие положения
Для обогащения вносят пробу (3.2) хорошо перемешанной испытуемой продукции в количестве не менее 1 г или 1 см3 в бульон для обогащения объемом не менее 9 см3.
Отмечают навеску S, точную массу или точный объем пробы.
Метод необходимо контролировать для гарантии того, что состав (с добавленным в конце приготовления нейтрализатором) и объем бульона удовлетворяют требованиям (см. 11.3).
Примечание - В некоторых случаях (когда это возможно) фильтруют парфюмерно-косметическую продукцию через мембранный фильтр, который затем погружают в бульон для обогащения, что облегчает нейтрализацию антимикробных свойств продукции (см. 11.3).
9.2.2 Водорастворимая продукция
Переносят навеску S пробы продукции в подходящую лабораторную посуду, содержащую соответствующий объем бульона.
9.2.3 Нерастворимая в воде продукция
Переносят навеску S пробы продукции в подходящую лабораторную посуду, содержащую соответствующее количество разбавителя (например, полисорбат 80).
Диспергируют пробу в разбавителе и добавляют соответствующий объем бульона.
9.2.4 Фильтруемая продукция
Используют мембранный фильтр с номинальным размером пор не более 0,45 мкм.
Переносят навеску S пробы продукции на мембранный фильтр в фильтровальном аппарате (см. ISO 21148). Сразу же фильтруют и промывают мембранный фильтр, используя определенные объемы воды и/или разбавителя.
Погружают мембранный фильтр в пробирку или колбу подходящего размера, содержащую соответствующий объем бульона.
9.3 Инкубация инокулированного бульона для обогащения
Инкубируют исходную суспензию, приготовленную в бульоне (см. 9.2), при температуре (32,5 ± 2,5) °С в течение не менее 20 ч, но не более 72 ч.
9.4 Обнаружение и идентификация Pseudomonas aeruginosa9.4.1 Выделение
Стерильной петлей делают пересев аликвоты инкубированного бульона для обогащения на поверхность питательного агара с цетримидом, чтобы получить изолированные колонии.
Переворачивают чашку Петри и инкубируют при температуре (32,5 ± 2,5) °С в течение не менее 24 ч, но не более 48 ч.
Проверяют наличие характерных колоний (см. таблицу 1). 14
1
2
3
4
5
Настоящий стандарт идентичен международному стандарту ISO 22717:2006 Cosmetics -Microbiology - Detection of Pseudomonas aeruginosa (Косметика. Микробиология. Обнаружение Pseudomonas aeruginosa).
Международный стандарт разработан техническим комитетом ISO/TC 217 «Косметика» Международной организации по стандартизации (ISO).
Перевод с английского языка (еп).
Официальные экземпляры международного стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, и международного стандарта, на который даны ссылки, имеются в Национальном фонде ТИПА Республики Беларусь.
В стандарт внесено следующее редакционное изменение: наименование настоящего стандарта изменено относительно наименования указанного международного стандарта для приведения в соответствие ГОСТ 1.5.
В разделе «Нормативные ссылки» и тексте стандарта ссылки на международный и европейский стандарты актуализированы.
Сведения о соответствии межгосударственного стандарта ссылочному международному стандарту приведены в дополнительном приложении Д.А.
Степень соответствия - идентичная (IDT)
6
ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 29 мая 2013 г. № 27 непосредственно в качестве государственного стандарта Республики Беларусь с 1 января 2014 г.
7
ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных (государственных) стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных (государственных) органов по стандартизации.
© Госстандарт, 2013
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
8
9
АТСС - American Type Culture Collection [Американская коллекция типовых культур (микроорганизмов)].
10
r> CIP - Institut Pasteur Collection (Коллекция института Пастера).
11
NCIMB - National Collection of Industrial and Marine Bacteria (Национальная коллекция промышленных и морских бактерий).
12
А> NBRC - National Biological Resource center (Национальный центр биологических исследований).
13
КСТС - Korean Collection for type culture (Корейская коллекция типовых культур).
14