ГОСТ 33483-2015
Продукция парфюмерно-косметическая. Методы определения и оценки клинико-лабораторных показателей безопасности
Купить ГОСТ 33483-2015 — бумажный документ с голограммой и синими печатями. подробнее
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Распространяется на парфюмерно-косметическую продукцию для ухода за кожей лица и тела, губами, вокруг глаз, волосами и ногтями, моющую гигиеническую косметическую продукцию, декоративную косметику, средства гигиены полости рта, косметическую продукцию для бритья, косметическую продукцию для окрашивания, химической завивки, выпрямления волос и другую парфюмерно-косметическую продукцию (продукция), за исключением продукции, имеющей pH более или равно 2,5 или менее или равно 11,5. Стандарт устанавливает методы определения и оценки на волонтерах клинико-лабораторных показателей (возможного раздражающего действия и сенсибилизирующей способности) испытуемой продукции с целью подтверждения ее безопасности для здоровья человека. Стандарт предназначен для специалистов лабораторий учреждений, осуществляющих государственный санитарно-эпидемиологический надзор за безопасностью и безвредностью для человека продукции, а также может быть использован научно-исследовательскими организациями гигиенического профиля, медицинскими учреждениями образования, аккредитованными в установленном порядке.
Оглавление
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Методы испытания продукции
Приложение А (обязательное) Условия, принципы биомедицинской этики и требования безопасности при клинико-лабораторных испытаниях продукции на волонтерах
Приложение Б (обязательное) Алгоритм расчета величины доверительной границы случайной погрешности измерения
Приложение В (справочное) Значения коэффициента t для случайной величины выборки, имеющей распределение Стьюдента с n — 1 степенями свободы
Библиография
| Дата введения | 01.09.2016 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Завершение срока действия | 06.04.2018 |
| Актуализация | 01.01.2021 |
Организации:
| 27.08.2015 | Утвержден | Евразийский совет по стандартизации, метрологии и сертификации | 79-П |
|---|---|---|---|
| 07.10.2015 | Утвержден | Госстандарт Республики Беларусь | 47 |
| Разработан | ГУ Республиканский научно-практический центр гигиены | ||
| Издан | БелГИСС | 2016 г. |
Perfume and cosmetic products. Methods for determination and assessment of clinical and laboratory safety indicators
- ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
- ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
- ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
- ГОСТ 12.1.010-76 Система стандартов безопасности труда. Взрывобезопасность. Общие требования
- ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасность статического электричества. Общие требования
- ГОСТ 12.4.021-75 Система стандартов безопасности труда. Системы вентиляционные. Общие требования
- ГОСТ 10354-82 Пленка полиэтиленовая. Технические условия
- ГОСТ 427-75 Линейки измерительные металлические. Технические условия
- ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
- ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
- ГОСТ 21241-89 Пинцеты медицинские. Общие технические требования и методы испытаний
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 28311-89 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 4919.2-77Реактивы и особо чистые вещества. Методы приготовления буферных растворов. Заменен на ГОСТ 4919.2-2016.- ГОСТ 5556-81 Вата медицинская гигроскопическая. Технические условия
- ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
- ГОСТ 9412-93 Марля медицинская. Общие технические условия
- ГОСТ 8.135-2004 Государственная система обеспечения единства измерений. Стандарт-титры для приготовления буферных растворов - рабочих эталонов рН 2-го и 3-го разрядов. Технические и метрологические характеристики. Методы их определения
- ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
- ГОСТ 31696-2012 Продукция косметическая гигиеническая моющая. Общие технические условия
- ГОСТ 29188.2-2014 Продукция парфюмерно-косметическая. Метод определения водородного показателя pH
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1
стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13

стр. 14

стр. 15

стр. 16
государственный стандарт
РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКЦИЯ ПАРФЮМЕРНО-КОСМЕТИЧЕСКАЯ
Методы определения и оценки клинико-лабораторных показателей безопасности
ПРАДУКЦЫЯ ПАРФУМЕРНА-КАСМЕТЫЧНАЯ
Метады вызначэння i ацэнм юлыка-лабараторных паказчыкау бяспем
Издание официальное
Г осстандарт Минск
GS
Предисловие
Евразийский совет по стандартизации, метрологии и сертификации (ЕАСС) представляет собой региональное объединение национальных органов по стандартизации государств, входящих в Содружество Независимых Государств. В дальнейшем возможно вступление в ЕАСС национальных органов по стандартизации других государств.
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-2015 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Правила разработки, принятия, обновления и отмены».
Сведения о стандарте
1 РАЗРАБОТАН государственным учреждением «Республиканский научно-практический центр гигиены»
2 ВНЕСЕН Госстандартом Республики Беларусь
3 ПРИНЯТ Евразийским советом по стандартизации, метрологии и сертификации по переписке (протокол № 79-П от 27 августа 2015 г.)
|
За принятие стандарта проголосовали: | ||||||||||||||||||
| ||||||||||||||||||
|
4 ВВЕДЕН ВДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 7 октября 2015 г. № 47 непосредственно в качестве государственного стандарта Республики Беларусь с 1 сентября 2016 г. |
5 ВВЕДЕН ВПЕРВЫЕ
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных (государственных) стандартов, издаваемых в этих государствах, а также в сети Интернет на сайтах соответствующих национальных (государственных) органов по стандартизации.
© Госстандарт, 2016
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
Волонтеры обязаны строго выполнять условия информированного соглашения и инструкции персонала.
А4 Требования к условиям безопасного проведения испытаний
Ответственное за клинико-лабораторные испытания лицо должно проинформировать волонтеров о возможном потенциальном риске испытаний, проинструктировать о порядке и соблюдении условий выполнения испытаний, мерах предосторожности и поведении при возможном возникновении негативных проявлений.
Подготовка и проведение испытаний продукции на раздражающее действие и сенсибилизирующую способность должны выполняться в строгом соответствии с методами их проведения.
При проведении испытаний следует соблюдать определенные меры предосторожности, в том числе испытания немедленно прекращают при возникновении у волонтера на эп и кутанные аппликации негативных субъективных клинических (зуд, жжение, болезненность, отечность, слезотечение и т. п.) и/или объективных симптомов воспаления кожи (эритематозная реакция, первичные экссудативные или пролиферативные высыпания), остатки испытуемой продукции с участков эпикутанных аппликаций тотчас удаляют путем смыва под проточной теплой водой с туалетным мылом или тампоном смоченным раствором с объемной долей этилового спирта 20 %.
При возникновении у волонтера негативных последствий испытания персонал испытательной лаборатории должен оказать ему неотложную медицинскую помощь:
- в случае проявления на участках эпикутанных аппликаций выраженных субъективных (выраженные ощущения зуда, жжения, болезненности) и объективных клинических симптомов (выраженная ярко-красная эритема, отек, первичные экссудативные или пролиферативные высыпания) следует после снятия аппликации и удаления остатков испытуемой продукции назначить местное применение мазей (кремов), содержащих глюкортикостероиды (фторокорт, си нал ар, лоринден и т. п.);
-при возникновении выраженных объективных клинических симптомов воспаления кожи, выходящих за границы участков эпикутанных аппликаций, следует назначить пострадавшему волонтеру внутрь антигистаминные препараты (фенкарол, или супрастин, или кларитин ит.п.);
- в случае необходимости (возникновение крапивницы, отека Квинке и других аллергических осложнений) пострадавшего волонтера необходимо сопроводить (направить) в лечебнопрофилактическое учреждение;
-в случае возникновения общих симптомов анафилактического шока (жалобы на чувство жара, слабость, головокружение, тошноту, тяжесть и боли в голове, за грудиной, в животе, затрудненное дыхание, бледность, цианоз губ, заторможенность, холодный пот, одышка, потеря сознания ит.п.) следует немедленно вызвать скорую медицинскую помощь, уложить пострадавшего на твердую поверхность на спину, приподнять ноги, поместить холод на место нанесения испытуемой продукции; ввести внутримышечно в несколько точек (в том числе по возможности выше места аппликации) по 0,2 см3 0,1%-ного адреналина (общая доза до 1 см3), а также внутримышечно 2 см3 2%-ного супрасти-на или 2 см3 0,1%-ного димедрола.
Для оказания неотложной медицинской помощи испытательная лаборатория должна иметь аптечку, укомплектованную в достаточном количестве лекарственными препаратами (антигистаминные, кортикостероидные и т. п.) с соблюдением условий и сроков их хранения.
А5 Ответственность за безопасность испытаний
Ответственность за соблюдение условий и требований безопасного проведения испытаний продукции с привлечением волонтеров возлагается на ответственного исполнителя клиниколабораторных исследований. Контроль за выполнением требований настоящего стандарта осуществляет руководитель испытательной лаборатории (центра). 1
Приложение Б (обязательное)
Алгоритм расчета величины доверительной границы случайной погрешности измерения
Б.1 Величину доверительной границы L случайной погрешности измерения рассчитывают по формуле
L = tSK, (Б.1)
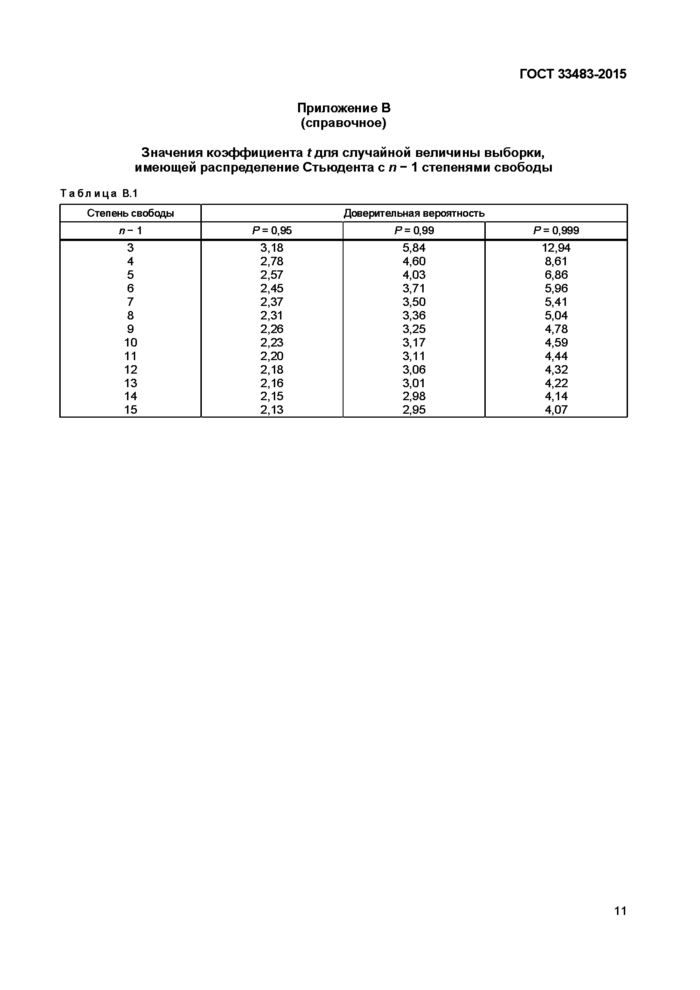
где f — коэффициент Стъюдента, который в зависимости от доверительной вероятности Р и числа результатов наблюдений л (количество волонтеров), находят по таблице В.1 (приложение В); S* — средняя ошибка средней арифметической, рассчитывают по формуле
(Б.2)
где о — среднее квадратичное отклонение результатов измерения; л — число результатов наблюдений.
Б.2 Среднее квадратичное отклонение результатов измерения оценивают по формуле
°"Л/ л-1 ■ (Б-3>
где£(х, -х)^— сумма квадратов отклонений отдельных значений результатов измерения х, от средней арифметической х.
10
Приложение В (справочное)
Значения коэффициента t для случайной величины выборки, имеющей распределение Стьюдента с п - 1 степенями свободы
|
Таблица В.1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
11
Библиография
[1] Хельсинкская декларация Всемирной медицинской ассоциации «Этические принципы проведения медицинских исследований с участием человека в качестве субъекта», принятая на 18-й Генеральной Ассамблее ВМА, Хельсинки, Финляндия, июнь 1964 г. с изменениями
[2] СТБ 1675-2006 Изделия косметические гигиенические моющие. Общие техниче
ские условия
12
УДК 665.5-027.45(083.74)(476) МКС 71.100.70
Ключевые слова: парфюмерно-косметическая продукция, клинико-лабораторные показатели, требования безопасности, методы испытаний, раздражающее действие, сенсибилизирующая способность, волонтеры
13
Ответственный за выпуск Н. А. Баранов
Сдано в набор 06.06.2016. Подписано в печать 20.06.2016. Формат бумаги 60x84/8. Бумага офсетная. Гарнитура Arial. Печать ризографическая. Уел. печ. л. 1,98 Уч.-изд. л. 0,91 Тираж2экз. Заказ 1214
Издатель и полиграфическое исполнение:
Научно-производственное республиканское унитарное предприятие «Белорусский государственный институт стандартизации и сертификации» (БелГИСС) Свидетельство о государственной регистрации издателя, изготовителя, распространителя печатных изданий
№ 1/303 от 22.04.2014 ул. Мел ежа, 3, комн.406, 220113, Минск.
_ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ_
ПРОДУКЦИЯ ПАРФЮМЕРНО-КОСМЕТИЧЕСКАЯ Методы определения и оценки клинико-лабораторных показателей безопасности
ПРАДУКЦЫЯ ПАРФУМЕРНА-КАСМЕТЫЧНАЯ Метады вызначэння i ацэню кгпшка-лабараторных паказчыкау бяспею
Perfume and cosmetic products Methods for determination and assessment of clinical and laboratory safety indicators
Дата введения — 2016-09-01
1 Область применения
Настоящий стандарт распространяется на парфюмерно-косметическую продукцию для ухода за кожей лица и тела, губами, вокруг глаз, волосами и ногтями, моющую гигиеническую косметическую продукцию, декоративную косметику, средства гигиены полости рта, косметическую продукцию для бритья, косметическую продукцию для окрашивания, химической завивки, выпрямления волос и другую парфюмерно-косметическую продукцию (далее— продукция), за исключением продукции, имеющей pH < 2,5 или >11,5.
Стандарт устанавливает методы определения и оценки на волонтерах клинико-лабораторных показателей (возможного раздражающего действия и сенсибилизирующей способности) испытуемой продукции с целью подтверждения ее безопасности для здоровья человека.
Стандарт предназначен для специалистов лабораторий учреждений, осуществляющих государственный санитарно-эпидемиологический надзор за безопасностью и безвредностью для человека продукции, а также может быть использован научно-исследовательскими организациями гигиенического профиля, медицинскими учреждениями образования, аккредитованными в установленном порядке.
2 Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие технические нормативные правовые акты в области технического нормирования и стандартизации (далее — ТИПА):
ГОСТ 8.135-2004 Государственная система обеспечения единства измерений. Стандарт-титры для приготовления буферных растворов— рабочих эталонов pH 2-го и 3-го разрядов. Технические и метрологические характеристики. Методы их определения
ГОСТ 12.1.004-91 Система стандартов безопасности труда. Пожарная безопасность. Общие требования
ГОСТ 12.1.005-88 Система стандартов безопасности труда. Общие санитарно-гигиенические требования к воздуху рабочей зоны
ГОСТ 12.1.007-76 Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности
ГОСТ 12.1.010-76 Система стандартов безопасности труда. Взрывобезопасность. Общие требования
ГОСТ 12.1.018-93 Система стандартов безопасности труда. Пожаровзрывобезопасностъ статического электричества. Общие требования
ГОСТ 12.4.021-75 Система стандартов безопасности труда. Системы вентиляционные. Общие требования
ГОСТ OIML R 76-1—2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания ГОСТ 427-75 Линейки измерительные металлические. Технические условия ГОСТ 4919.2-77 Реактивы и особо чистые вещества. Методы приготовления буферных растворов ГОСТ 5556-81 Вата медицинская гигроскопическая. Общие технические условия ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия ГОСТ 9412-93 Марля медицинская. Общие технические условия ГОСТ 10354-82 Пленка полиэтиленовая. Технические условия
Издание официальное
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
ГОСТ 18300-87 Спирт этиловый ректификованный технический. Технические условия
ГОСТ 21239-2005 Инструменты хирургические. Ножницы. Общие технические требования и методы испытаний
ГОСТ 21241-89 Пинцеты медицинские. Общие технические требования и методы испытаний
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
ГОСТ 28311-89 Дозаторы медицинские лабораторные. Общие технические требования и методы испытаний
ГОСТ 28498-90 Термометры жидкостные стеклянные. Общие технические требования. Методы испытаний
ГОСТ 29188.2-2014 Продукция парфюмерно-косметическая. Метод определения водородного показателя pH
ГОСТ 29227-91 (ИСО 835-1—81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 31696-2012 Продукция косметическая гигиеническая моющая. Общие технические условия
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ТИПА по каталогу, составленному по состоянию на 1 января текущего года, и по соответствующим информационным указателям, опубликованным в текущем году.
Если ссылочные ТИПА заменены (изменены), то при пользовании настоящим стандартом следует руководствоваться заменяющими (измененными) ТИПА. Если ссылочные ТИПА отменены без замены, то положение, в котором дана ссылка на них, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены следующие термины с соответствующими определениями:
3.1 аллерген: Вещество или смесь веществ, способное вызвать при поступлении в организм развитие в нем специфической повышенной чувствительности (сенсибилизации), что при последующем воздействии вещества или смеси веществ с аналогичной характеристикой может приводить к возникновению аллергической реакции.
3.2 волонтер: Совершеннолетнее физическое лицо, информированное о сути и потенциальном риске исследований (испытаний), не имеющее противопоказаний по состоянию здоровья, добровольно изъявившее согласие на участие в испытаниях и подписавшее информированное соглашение (согласие).
3.3 доза: Количество испытуемой продукции, используемое для постановки эпикутанной аппликации.
3.4 информированное соглашение (согласие): Документально оформленное добровольно подписанное согласие лица (волонтера) на участие в испытании продукции после ознакомления с правилами, условиями и особенностями проведения испытания.
3.5 контрольная эпикутанная аппликация: Накожное нанесение (аппликация) растворителя, используемого для подготовки дозы испытуемой продукции.
3.6 клинико-лабораторные исследования (испытания): Исследования (испытания), проводимые в условиях лаборатории с участием человека (волонтера) в качестве субъекта испытания, для оценки показателей безопасности продукции.
3.7 первичная эпикутанная аппликация: Накожное нанесение (первичная аппликация) в установленной дозе испытуемой продукции для выявления и оценки ее раздражающего действия, индукции сенсибилизации.
3.8 провокационная эпикутанная аппликация: Повторное накожное нанесение (вторичная аппликация) в установленной дозе испытуемой продукции для выявления ее сенсибилизирующего действия и оценки сенсибилизирующей способности.
3.9 раздражающее действие: Локализованная неспецифическая воспалительная реакция кожи или слизистой оболочки при контактном воздействии вещества, проявляющаяся субъективными (зуд, жжение, болезненность) и объективными (эритема, отек, высыпания, некроз) симптомами.
3.10 растворитель: Вещество, используемое для разбавления, суспензирования, экстрагирования или растворения испытуемой продукции.
3.11 сенсибилизирующее действие: Способность вещества при поступлении в организм вызвать развитие в нем специфической повышенной чувствительности, опосредованной гиперергиче-скими иммунными механизмами.
3.12 эритематозная реакция: Покраснение (эритема) кожи разной степени выраженности как проявление (симптом) воспалительного процесса в тканях кожных покровов.
4 Методы испытания продукции
4.1 Общие положения
Для продукции, особенностью которой является многократный и (или) длительный контакт с кожей и (или) слизистыми оболочками человека, с целью обеспечения безопасности для потребителя и уточнения экстраполяции результатов, полученных в исследованиях in vitro и in vivo (на лабораторных животных), предусматривают прямую одновременную оценку риска раздражающего и сенсибилизирующего действия на человека постановкой метода закрытой эп и кутанной «лоскутной» (компрессной) пробы или метода открытой эп и кутан ной «капельной» пробы на волонтерах.
4.2 Условия и требования безопасности при проведении клинико-лабораторных испытаний
4.2.1 Общие условия и требования безопасности проведения испытаний
При исследовании продукции на волонтерах необходимо строго выполнять общие условия и требования безопасности, приведенные в А.1 (приложение А).
4.2.2 Требования к персоналу испытательной лаборатории
Для выполнения исследований продукции на волонтерах должны быть соблюдены требования к персоналу испытательной лаборатории, приведенные в А.2 (приложение А).
4.2.3 Ограничительные требования к испытуемой продукции
Не допускается проведение на волонтерах испытаний по определению и оценке сенсибилизирующей способности продукции:
- вызывающей раздражающее действие на кожу в экспериментах на лабораторных животных;
- с pH < 2,5 или >11,5 (на основании результатов измерения pH образцов испытуемой продукции поГОСТ 29188.2).
4.3 Предварительный анализ испытуемой продукции
4.3.1 Общие сведения
Результатом предварительного анализа может быть заключение о нецелесообразности проведения испытаний раздражающего действия и сенсибилизирующей способности продукции на волонтерах.
4.3.2 Данные о продукции
4.3.2.1 Данные об ингредиентном составе продукции
Испытуемая продукция (образец) должна быть идентифицирована и описана (вид, назначение, способ применения, форма). Должен быть полностью определен качественный и количественный ин-гредиентный состав продукции, количественные данные относительно биологической безопасности ингредиентов.
Информация о качественном и количественном содержании ингредиентов в составе продукции должна быть получена от поставщика или изготовителя продукции. Если информация защищена правами на интеллектуальную собственность, то передача и использование такой информации обеспечивается договором о конфиденциальности.
4.3.2.2 Предварительные данные о безопасности продукции
Для уверенности в том, что испытуемая продукция не представляет собой никакого значительного риска для здоровья волонтера, должна быть получена адекватная информация по токсическому профилю испытуемой продукции (острая токсичность, раздражающее действие на кожу и слизистые оболочки, сенсибилизирующая способность ит. п.), полученная при исследованиях in vitro и in vivo (на лабораторных животных).
4.4 Принцип методов
Метод предусматривает прямую оценку риска раздражающего действия испытуемой продукции на волонтере постановкой первичной эп и кутанной аппликации, которая одновременно является сенсибилизирующей, и оценку сенсибилизирующей способности испытуемой продукции постановкой провокационной (вторичной) эп и кутан ной аппликации.
Основными способами оценки является определение индексов раздражающего действия на кожу Icut и сенсибилизирующей способности ls испытуемого образца продукции. 2
4.5 Описание методов
4.5.1 Отбор волонтеров
Настоящий стандарт предназначен для проведения клинико-лабораторных исследований на здоровых волонтерах, которые отбираются квалифицированным специалистом в соответствии с требованиями А.З (приложение А), [1].
4.5.2 Аппаратура, материалы и реактивы
Весы лабораторные по ГОСТ OIMLR76-1, высокого класса точности, с наибольшим пределом взвешивания 200 г.
Дозаторы лабораторные по ГОСТ 28311.
Линейка измерительная металлическая по ГОСТ 427.
Мешалка магнитная.
Ножницы по ГОСТ 21239.
Пинцеты медицинские по ГОСТ 21241.
Термометр жидкостный стеклянный по ГОСТ 28498, с диапазоном измерения температур от 0 °С до 100 °С, с ценой деления 1 °С.
Термостат электрический суховоздушный с автоматическим терморегулятором до 50 °С, позволяющий поддерживать заданную температуру с погрешностью ±1 °С.
Воронка делительная ВД-1-250 ХС по ГОСТ 25336.
Палочка стеклянная.
Пестик 1-2 по ГОСТ 9147.
Пипетки разной вместимости 2 класса точности по ГОСТ 29227.
Стакан Н-2-10 (20) ТХС по ГОСТ 25336.
Ступка 2-3 по ГОСТ 9147.
Вата медицинская гигроскопическая по ГОСТ 5556.
Бумага фильтровальная лабораторная по ГОСТ 12026.
Лейкопластырь медицинский.
Марля медицинская по ГОСТ 9412.
Пленка полиэтиленовая, марка Н по ГОСТ 10354.
Фильтр «синяя лента».
Вода дистиллированная по ГОСТ 6709.
Жидкое мыло по ГОСТ 31696, [2].
Спирт этиловый ректификованный технический по ГОСТ 18300.
Стандарт-титры для приготовления образцовых буферных растворов для рН-метрии по ГОСТ 8.135, допускается приготовление буферных растворов по ГОСТ 4919.2.
Допускается применение аналогичного оборудования и материалов с техническими и метрологическими характеристиками, а также реактивов по качеству не ниже указанных в настоящем стандарте.
4.5.3 Подготовка к испытаниям
4.5.3.1 Приготовление окклюзий
Изготавливают из медицинской марли четырехслойные тампоны размером 1 * 1 см, накладки из полиэтиленовой пленки размером 2 * 2 см, полоски медицинского пластыря размером 3-А * 5-6 см.
4.5.3.2 Приготовление доз испытуемой продукции
Для продукции вязкой консистенции (кремо-, геле-, мазе- и пастообразные, за исключением продукции гигиенической моющей)— непосредственно на марлевый тампон последовательно наносят шпателем испытуемый образец и взвешивают на лабораторных весах, доводя массу навески образца на тампоне до (0,05 ± 0,001) г (разовая аппликационная доза).
Для продукции твердой консистенции — взвешивают на лабораторных весах в стакане 1,00 г испытуемого образца. Кристаллическую, компактную и крупнозернистую продукцию предварительно измельчают до порошкообразного состояния. Готовят исходный раствор, эмульсию или суспензию испытуемого образца с массовой долей вещества 50%, дозируя пипеткой (дозатором) в стакан с навеской испытуемой пробы растворитель в объеме 1,0 см2 с последующим интенсивным перемешиванием с помощью магнитной мешалки.
Для спиртсодержащей продукции — готовят исходный раствор (путем разбавления в соотношении 1:1), дозируя пипеткой (дозатором) в стакан по 1 см2 испытуемого образца и растворителя.
Для гигиенической моющей продукции (шампуни, гели для душа, жидкое мыло и другая аналогичная продукция)— готовят исходный раствор с объемной долей 10 %, дозируя пипеткой (дозатором) в стакан 1 см2 испытуемого образца и 9 см2 растворителя. 3
Для продукции на носителях (косметические салфетки, тканевые косметические маски, косметические маски на нетканой основе, полоски для депиляции и другая аналогичная продукция) — готовят вытяжку в растворитель при соотношении площади образца испытуемой пробы к объему растворителя 1:2, путем вырезания ножницами образца испытуемой пробы размером 2* 2 см (площадь 4 см2), внесения измельченного ножницами образца в стаканчик (10-20 см3), дозирования пипеткой (дозатором) 8 см3 растворителя, инкубации в течение 24 ч в суховоздушном термостате при температуре 37 °С при периодическом (5-6 раз) перемешивании содержимого стаканчика стеклянной палочкой. Водную фазу отделяют фильтрацией в стакан через фильтр «синяя лента» с помощью делительной воронки.
Для продукции (для окрашивания, осветления, мелирования волос, для химической завивки или распрямления волос, сухие косметические маски и другая аналогичная продукция), применение которой согласно аннотации подразумевает смешивание перед применением нескольких компонентов, готовят испытуемые пробы в зависимости от полученной консистенции готовой композиции.
В качестве растворителя используют дистиллированную воду по ГОСТ 6709.
Жидкую продукцию испытывают в нативном виде.
Приготовленные исходные растворы, эмульсии, суспензии, экстракты или нативную жидкую продукцию дозируют пипеткой по 0,05 см3 на марлевые тампоны, размещенные на полиэтиленовых накладках.
4.5.3.3 Формирование группы волонтеров
Группу волонтеров формируют в количестве не менее пяти человек. При испытании продукции, предназначенной для использования мужчинами или женщинами, в группу включают волонтеров соответствующего пола.
4.6 Проведение испытаний методом закрытой эпикутанной «лоскутной» (компрессной) пробы
4.6.1 Постановка первичной эпикутанной аппликации
Первичную эп и кутанную аппликацию выполняют наложением на 24 ч на участок неповрежденной кожи внутренней поверхности предплечья и/или плеча (допускается выполнять аппликации на участках кожи в области спины и живота) волонтера после предварительной обработки кожных участков раствором этилового спирта с объемной долей 60 %, марлевым тампоном с дозой испытуемой пробы под окклюзией (покрытие полиэтиленовой накладкой и фиксация к коже полосками лейкопластыря или бинтованием).
Контрольную эп и кутанную аппликацию выполняют аналогично опытной первичной, дозируя на марлевый тампон 0,05 см3 дистиллированной воды.
Допускается постановка у одного волонтера одновременно нескольких испытуемых образцов при расстоянии между ними не менее 2 см. Участки аппликации отмечают маркером.
Первичную и контрольную аппликации через 24 ч снимают, остатки вещества с участков аппликации кожи смывают струей теплой воды с использованием косметического жидкого мыла или ватным тампоном с растворителем, не влияющим на функциональное состояние кожи (например, раствором с объемной долей этилового спирта 20 % — 60 %), и через 1, 24 и 48 ч регистрируют функциональное состояние кожи на месте аппликации с оценкой выраженности эритематозной реакции.
При возникновении у волонтера в период аппликационной экспозиции негативных субъективных симптомов раздражающего действия (ощущение зуда, жжения, болезненности) даже слабой (переносимой) интенсивности со стороны опытного участка кожи аппликацию немедленно снимают. В этом случае, а также при определении после первичной аппликации на участке кожи эритемы (при отсутствии таковой на контрольном), первичную аппликацию у конкретного волонтера повторяют на другом участке кожи, разбавляя дистиллированной водой испытуемые раствор, эмульсию, суспензию или нативную жидкую продукцию не менее чем в два раза.
В случае появления в процессе экспозиции и после завершения повторной первичной аппликации негативных проявлений в виде субъективных симптомов раздражения и (или) эритематозной реакции кожи только у одного волонтера (с повышенной чувствительностью к данному изделию), он исключается из дальнейших исследований.
При регистрации у двух (и более) волонтеров негативных проявлений дальнейшие испытания не проводят, делают вывод о том, что испытуемая продукция обладает раздражающим действием на кожу (условное обозначение /CiJf = 1 балл).
4.6.2 Постановка провокационной (вторичной) эпикутанной аппликации
При условии отсутствия субъективных симптомов или объективных признаков раздражающего действия испытуемой продукции (lcut = 0 баллов) после первичной аппликации через 24 ч выполняют постановку провокационной (вторичной) эпикутанной аппликации. Ее выполняют аналогично первич-
ной аппликации, накладывая на «чистый» участок неповрежденной кожи рядом с предыдущей аппликацией (на расстоянии не менее 2 см) марлевый тампон с дозой той же испытуемой пробы под окклюзией, а также выполняют повторную контрольную аппликацию с дистиллированной водой (на том же первичном участке кожи). Участки аппликации отмечают маркером.
Возникновение у одного или нескольких волонтеров в период проведения провокационной эпику-танной аппликации субъективных симптомов раздражающего действия (зуд, жжение, болезненность), в том числе на кожных участках первичной аппликации, свидетельствует о развитии повышенной чувствительности. Эпикутанную пробу с испытуемым образцом продукции немедленно прекращают, делают вывод о том, что испытуемая продукция обладает сенсибилизирующей способностью (условное обозначение ls= 1 балл).
Провокационную и контрольную эпикутанные аппликации через 24 ч снимают, остатки вещества с участков аппликации кожи смывают струей теплой воды с использованием косметического жидкого мыла или ватным тампоном, смоченным раствором с объемной долей этилового спирта 20%, и после этого через 1, 24 и 48 ч одновременно на опытных и контрольном кожных участках аппликаций визуально регистрируют характер и выраженность объективных кожных симптомов и учитывают выраженность субъективных симптомов сенсибилизирующего действия.
4.7 Проведение испытаний методом открытой эпикутанной «капельной» пробы
4.7.1 Назначение метода
Открытая эпикутанная «капельная» проба предназначена для определения и оценки на волонтерах раздражающего действия и сенсибилизирующей способности продукции периодического разового применения (продукция для окраски и химической завивки волос, для депиляции и другая аналогичная продукция с возможным раздражающим кожу действием).
4.7.2 Постановка открытой «капельной» эпикутанной пробы
Постановку открытой «капельной» эпикутанной пробы проводят аналогично постановке закрытой эпикутанной «лоскутной» пробы (4.6), за исключением того, что первичную и провокационную (вторичную) аппликации выполняют нанесением на кожные участки пипеткой (дозатором) готовой для применения испытуемой продукции (приготовленной согласно аннотации) в дозе по 0,05 см3 (1-2 капли), которую слегка втирают стеклянной палочкой в участок кожи диаметром 2 см и оставляют до полного высыхания.
Контрольные аппликации выполняют аналогично, нанося на кожные участки по 0,05 см3 дистиллированной воды.
Продолжительность экспозиции аппликаций, составляющую от 15 мин до 24 ч, определяет специалист в зависимости от назначения, способа и условий применения испытуемой продукции и ее потенциальной способности оказать раздражающее действие на кожу.
4.8 Учет, оценка и обработка результатов
4.8.1 Учет и оценка результатов первичной аппликации
Оценку раздражающего действия испытуемой продукции по обоим методам проводят у каждого волонтера по визуальному учету наличия и интенсивности эритематозной реакции кожи на участках первичной и контрольной эпикутанных аппликаций через 1, 24 и 48 ч с оценкой ее выраженности в баллах по шкале в соответствии с таблицей 1.
|
Таблица 1 — Шкала оценки выраженности эритематозной реакции кожи | ||||||||||||
|
4.8.2 Учет и оценка результатов провокационной аппликации
Учет сенсибилизирующего действия испытуемой продукции в обоих методах проводят у каждого волонтера через 24, 48 и 72 ч после завершения провокационной эпикутанной аппликации по наличию и интенсивности субъективных симптомов и объективных проявлений воспалительной реакции кожи на участках провокационной (вторичной) и контрольной эпикутанных аппликаций с оценкой их выраженности в баллах по шкале в соответствии с таблицей 2.
|
Таблица 2 — Шкала оценки сенсибилизирующего действия испытуемой продукции при контакте с кожей человека | ||||||||||
|
4.8.3 Обработка результатов и оценка раздражающего действия на кожу и сенсибилизирующей способности испытуемой продукции
Возможное раздражающее и сенсибилизирующее действие испытуемой продукции при остром воздействии на кожу человека оценивают по индексам раздражающего действия на кожу leut и сенсибилизирующей способности ls испытуемого образца продукции в баллах, которые вычисляют по формуле
= ((Но - Нк)1 + (Но -Щ2+... + (Но - нк)п) In, (1)
где Н — выраженность у волонтера симптомов раздражающего действия (эритематозной ре
акции кожи) или объективных и субъективных симптомов сенсибилизирующего действия в баллах соответственно на участках кожи первичной или провокационной опытной и контрольной эп и кутанных аппликаций;
о — опытнаяаппликация;
к — контрольная аппликация;
1,2,..., п — порядковый номер волонтера;
п — количество волонтеров в группе.
За результат испытаний раздражающего действия или сенсибилизирующей способности испытуемой продукции принимают среднее арифметическое результатов определения разницы выраженности эритематозной реакции кожи на участке первичной аппликации или выраженности объективных и субъективных симптомов сенсибилизирующего действия в баллах на участке кожи провокационной и на соответствующих участках контрольных эпикутанных аппликаций с учетом величины доверительной границы L при уровне вероятности Р= 0,99.
Расчет величины доверительной границы случайной погрешности измерения проводят по алгоритму в соответствии с приложением Б.
Раздражающее действие и сенсибилизирующая способность у испытуемого образца продукции при контакте с кожей отсутствует (условное обозначение соответственно lcut = 0 баллов и /, = 0 баллов), если значение индексов равно нулю или сумма соответствующего индекса с величиной доверительной границы менее одного балла (/Cij!(/S) + L < 1,0).
Испытуемый образец продукции обладает раздражающим действием и (или) сенсибилизирующей способностью и потенциально аллергоопасен (условное обозначение соответственно lCIJ = 1 балл и ls= 1 балл), если сумма значения соответствующего индекса и величины доверительной границы равна или превышает 1,0 балл (lcuils) + L > 1,0).
4.9 Отчет об исследовании (протокол испытания)
Отчет об исследовании должен содержать:
- данные, идентифицирующие продукцию;
- информацию по использованному методу, подготовке образцов испытуемой продукции, особенностям постановки метода при возникновении негативных проявлений;
- индивидуальные результаты учета кожных реакций в экспонируемые периоды на участках первичной, провокационной и контрольных аппликаций;
- описание возможных негативных проявлений и других непрогнозируемых эффектов;
- статистическую обработку результатов;
- заключение о раздражающем действии и сенсибилизирующей способности испытуемой продукции при контакте с кожей человека;
-идентификацию специалистов, проводивших испытание, сроки проведения клиниколабораторных испытаний. 4
Приложение А (обязательное)
Условия, принципы биомедицинской этики и требования безопасности при клинико-лабораторных испытаниях продукции на волонтерах
А.1 Общие условия и требования безопасности проведения испытаний
При выполнении работ персонал испытательной лаборатории должен знать и строго соблюдать на рабочем месте требования:
- пожарной безопасности —по ГОСТ 12.1.004, ГОСТ 12.1.010, ГОСТ 12.1.018;
- правил охраны труда и техники безопасности при работе в испытательной лаборатории— по ГОСТ 12.1.005, ГОСТ 12.1.007, ГОСТ 12.4.021;
-техники безопасности, изложенные в эксплуатационных документах на средства измерений и оборудование, применяемые при проведении испытаний.
При выполнении испытаний в лаборатории должны быть соблюдены следующие условия:
- температура воздуха при выполнении измерений от 18 °С до 27 °С;
- атмосферное давление 84-107 кПа (от 630 до 800 мм рт. ст.);
- относительная влажность воздуха не более 80 % при температуре 25 °С;
- напряжение питающей сети (220 ± 10) В;
- частота переменного тока (50 ± 0,4) Гц.
Помещения для проведения испытаний должны быть оснащены приточно-вытяжной вентиляцией или вытяжным шкафом, подводкой горячей и холодной воды.
А.2 Требования к персоналу испытательной лаборатории
К выполнению клинико-лабораторных испытаний продукции на волонтерах допускаются квалифицированные специалисты, имеющие высшее или среднее специальное медицинское (биологическое) образование, знающие и освоившие выполнение всех операций, предусмотренных методами определения и оценки раздражающего действия и сенсибилизирующей способности испытуемой продукции на волонтерах, знающие потенциальный риск испытаний с возможными негативными проявлениями и осложнениями и владеющие приемами и способами их предупреждения, оказания при необходимости неотложной медицинской помощи.
А.З Требования к отбору волонтеров
К испытаниям привлекаются лица не моложе 18 лет и старше 65 лет, добровольно изъявившие согласие участвовать в них, на основе двухстороннего письменного соглашения ([1]).
Предварительно кандидат в волонтеры должен быть проинформирован персоналом испытательной лаборатории о целях, методах, условиях и порядке проведения, ожидаемых результатах, потенциальном прогнозируемом и непрогнозируемом риске испытания, неудобствах, которые могут быть с ним связаны, о правах волонтера воздержаться от испытания той или иной продукции или аннулировать свое согласие на участие в испытаниях, на защиту от вредного воздействия, на все возможные меры предосторожности и оказание необходимой медицинской помощи, что должно быть отражено в информированном соглашении с волонтером.
К испытаниям в качестве волонтеров не допускаются лица, имеющие следующие противопоказания по состоянию здоровья (поданным медицинской документации, осмотра врача):
-любые нозологические формы заболеваний в острой форме и хронические заболевания в стадии обострения, а также в период реконвалесценции;
- любые хронические заболевания кожи;
- хронические заболевания печени;
-хронические заболевания сердечно-сосудистой системы и бронхолегочного аппарата с выраженной недостаточностью функции;
- органические заболевания центральной нервной системы со стойкими выраженными нарушениями функции, психические заболевания;
- любые аутоиммунные и аллергические заболевания (в том числе в анамнезе);
- непереносимость конкретных наименований средств и препаратов;
- беременные и кормящие женщины.
1
2
3
4