ГОСТ 30417-2018
Масла растительные. Методы определения массовых долей витаминов А и Е
Купить ГОСТ 30417-2018 — бумажный документ с голограммой и синими печатями. подробнее
Цена на этот документ пока неизвестна. Нажмите кнопку "Купить" и сделайте заказ, и мы пришлем вам цену.
Распространяем нормативную документацию с 1999 года. Пробиваем чеки, платим налоги, принимаем к оплате все законные формы платежей без дополнительных процентов. Наши клиенты защищены Законом. ООО "ЦНТИ Нормоконтроль"
Наши цены ниже, чем в других местах, потому что мы работаем напрямую с поставщиками документов.
Способы доставки
- Срочная курьерская доставка (1-3 дня)
- Курьерская доставка (7 дней)
- Самовывоз из московского офиса
- Почта РФ
Устанавливает методы определения массовых долей витаминов А и Е в растительных маслах.
- Заменяет ГОСТ 30417-96 «Масла растительные. Методы определения массовых долей витаминов А и Е» ИУС 1-2019
Оглавление
1 Область применения
2 Нормативные ссылки
3 Условия проведения измерения
4 Отбор проб и подготовка пробы
5 Определение массовой доли витамина А
6 Определение массовой доли витамина Е методом тонкослойной хроматографии
Библиография
| Дата введения | 01.01.2020 |
|---|---|
| Добавлен в базу | 01.02.2020 |
| Актуализация | 01.01.2021 |
Этот ГОСТ находится в:
- Раздел Экология
Организации:
| 30.10.2018 | Утвержден | Межгосударственный Совет по стандартизации, метрологии и сертификации | 113-П |
|---|---|---|---|
| 13.11.2018 | Утвержден | Федеральное агентство по техническому регулированию и метрологии | 982-ст |
| Разработан | ФГБНУ ВНИИЖиров | ||
| Издан | Стандартинформ | 2018 г. |
Vegetable oils. Methods for determination of A and E vitamins content
- ГОСТ 6709-72 Вода дистиллированная. Технические условия
- ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
- ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие технические условия
- ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
- ГОСТ 20015-88 Хлороформ. Технические условия
- ГОСТ 20490-75 Реактивы. Калий марганцовокислый. Технические условия
- ГОСТ 24363-80 Реактивы. Калия гидроокись. Технические условия
- ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры
- ГОСТ 29227-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
- ГОСТ 4147-74 Реактивы. Железо (III) хлорид 6-водный. Технические условия
- ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
- ГОСТ 5815-77 Реактивы. Ангидрид уксусный. Технические условия
- ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
- ГОСТ OIML R 76-1-2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
- ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия
- ГОСТ 32190-2013 Масла растительные. Правила приемки и методы отбора проб
- ГОСТ 4919.1-2016 Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов
- Показать все
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12
стр. 13

стр. 14

стр. 15

стр. 16
МЕЖГОСУДАРСТВЕННЫЙ СОВЕТ ПО СТАНДАРТИЗАЦИИ, МЕТРОЛОГИИ И СЕРТИФИКАЦИИ
(МГС)
INTERSTATE COUNCIL FOR STANDARDIZATION, METROLOGY AND CERTIFICATION
(ISC)
МЕЖГОСУДАРСТВЕННЫЙ
СТАНДАРТ
МАСЛА РАСТИТЕЛЬНЫЕМетоды определения массовых долей витаминов А и Е
ГОСТ
30417—
2018
Издание официальное
Москва
Стандартинформ
2018
ГОСТ
30417—
2018
Издание официальное
|
Москва Стандартинформ 2018 |
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-2015 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2—2015 «Межгосударственная система стандартизации. Стандарты межгосударственные. правила и рекомендации по межгосударственной стандартизации Правила разработки, принятия. обновления и отмены»
Сведения о стандарте
1 РАЗРАБОТАН Федеральным государственным бюджетным научным учрехедением «Всероссийский научно-исследовательский институт жиров» (ВНИИЖиров)
2 ВНЕСЕН Федеральным агентством по техническому регулированию и метрологии
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 30 октября 2018 г. № 113-П)
За принятие проголосовали:
|
Краткое наименование страны no МК (ИСО 3166) 004-97 |
Код страны по МК (ИСО 3166) 004—97 |
Сокращенное наименование национального органа по стандартизации |
|
Армения |
AM |
Минэкономики Республики Армения |
|
Беларусь |
BY |
Госстандарт Республики Беларусь |
|
Киргизия |
KG |
Кыргызстандарт |
|
Россия |
RU |
Госстандарт |
|
Узбекистан |
UZ |
Уэстандарт |
|
Украина |
UA |
Минэкономразвития Украины |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 13 ноября 2018 г № 982-ст межгосударственный стандарт ГОСТ 30417-2018 введен в действие в качестве национального стандарта Российской Федерации с 1 января 2020 г.
5 ВЗАМЕН ГОСТ 30417-96
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе «Национальные стандарты», а текст изменений и поправок — в ежемесячном информационном указателе «Национальные стандарты». В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе «Национальные стандарты». Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет (www.gost.nj)
© Стандартнформ, оформление. 2018
В Российской Федерации настоящий стандарт не может быть полностью или частично воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Федерального агентства по техническому регулированию и метрологии
6.4.1 Выделение неомыляемых веществ
В конической колбе взвешивают (3 ± 0.2) г растительного масла и записывают результат до четвертого десятичного знака. Добавляют (0.2 ± 0.05) г аскорбиновой кислоты и 30 см3 свежеприготовленного спиртового раствора КОН концентрацией с (КОН) = 2 моль/дм3. Смесь нагревают с обратным холодильником на кипящей водяной бане в течение 15 мин. начиная с момента закипания раствора в колбе.
Содержимое колбы охлаждают и количественно переносят в делительную воронку тремя порциями дистиллированной воды общим объемом 100 см3. Неомыляемые вещества экстрагируют этиловым эфиром, тремя порциями по 60 см3. Объединенный эфирный экстракт промывают в делительной воронке дистиллированной водой до нейтральной реакции промывных вод по фенолфталеину. Промытую эфирную вытяжку помещают в сухую колбу, воронку ополаскивают 20 см3 эфира и сливают в ту же колбу. Засыпают от 5 до 10 г безводного сернокислого натрия и оставляют в темном месте на 30 мин. периодически взбалтывая. Затем содержимое колбы фильтруют через бумажный фильтр. Колбу и фильтр промывают этиловым эфиром, тремя порциями по 10 см3. Эфир из объединенного фильтрата отгоняют на водяной бане до объема от 1 до 2 «и3. Остаток из колбы количественно переносят в пробирку. 3—4 раза обмывая колбу порциями эфира по 1 см3. Эфир из пробирки отгоняют под вакуумом при температуре не выше 30 °С до объема от 0.5 до 0.6 см3.
6.4.2 Выделение витамина Е с помощью тонкослойных хроматографических пластинок
На пластинки «Силуфол» пипеткой наносят количественно (дважды обмывая пробирку порциями
эфира по 0.5 см3) весь раствор неомыляемых веществ в виде полосы длиной около 10 см. отстоящей на 2 см от нижнего и боковых краев пластинки. После каждого нанесения полосы дают эфиру улетучиться.
На одном уровне с пробой на расстоянии 1 см от боковых краев пластинки наносят по капле раствор 1 (см. таблицу 2) концентрацией о-токоферола 0.05 мг/см3 в качестве «свидетеля».
Пластинку «Силуфол» помещают в хроматографическую камеру. В качестве подвижной фазы используют смесь этилового эфира и гексана 1:1. Развитие хроматограммы должно проходить в темноте и заканчиваться при подъеме растворителя до верхнего края пластинки. Пластинку вынимают из камеры, подсушивают на воздухе, затем края пластинки, содержащие «свидетель», опрыскивают реактивом Эм-мери-Энгеля, предварительно прикрыв часть пластинки с пробой стеклянной пластинкой. Затем пластинку «Силуфол» помещают в темноту на 3 мин. после чего пятна, содержащие о-токоферол. окрашиваются в розовый цвет. Прочерчивают две линии на 2 мм выше и ниже окрашенных пятен.
Слой силикагеля, заключенный между линиями, соскабливают в бумажный фильтр диаметром 3 см. помещенный в стеклянную воронку, и элюируют токоферолы в градуированную пробирку, промывая силикагель этиловым спиртом 10 раз порциями по 1 см3. Объем элюата доводят этиловым спиртом до 10 см3.
Для определения приблизительной концентрации токоферола отбирают 1 см3 элюата. добавляют 3 см3 этилового спирта, по 1 см3 растворов, а. а-дипиридила (о-фенантролина) и хлорного железа и измеряют оптическую плотность, как указано в 6.3.
Если измеренная оптическая плотность меньше 0.1. то для основного измерения следует увеличить объем элюата и уменьшить объем этилового спирта так. чтобы сумма этих объемов составляла по-прежнему 4 см3 (например, элюата — 1.3 см3, этилового спирта — 2.7 сги3). Если оптическая плотность превышает 0.3, то следует уменьшить объем элюата и соответственно увеличить объем этилового спирта исходя из такого же расчета (например, элюата — 0.8 см3, этилового спирта — 3,2 см3). В полученном таким образом растворе проводят колориметрическую реакцию и измеряют оптическую плотность, как указано в 6.3.
Концентрацию о-токоферола определяют по градуировочному графику.
6.5 Обработка результатов
Массовую долю витамина ЕХ5. мг на 100 г продукта (мг %). вычисляют по формуле
CJ5-10-1W т
ь V2m
где с — концентрация о-токоферола в анализируемом растворе, (мг %)*>;
Внесистемная единица измерения концентрация
6 — общий объем раствора, взятого для колориметрической реакции, см3;
10 — общий объем элюата. см3;
V2 — объем элюата. взятого для колориметрической реакции, см3; т — масса пробы, г.
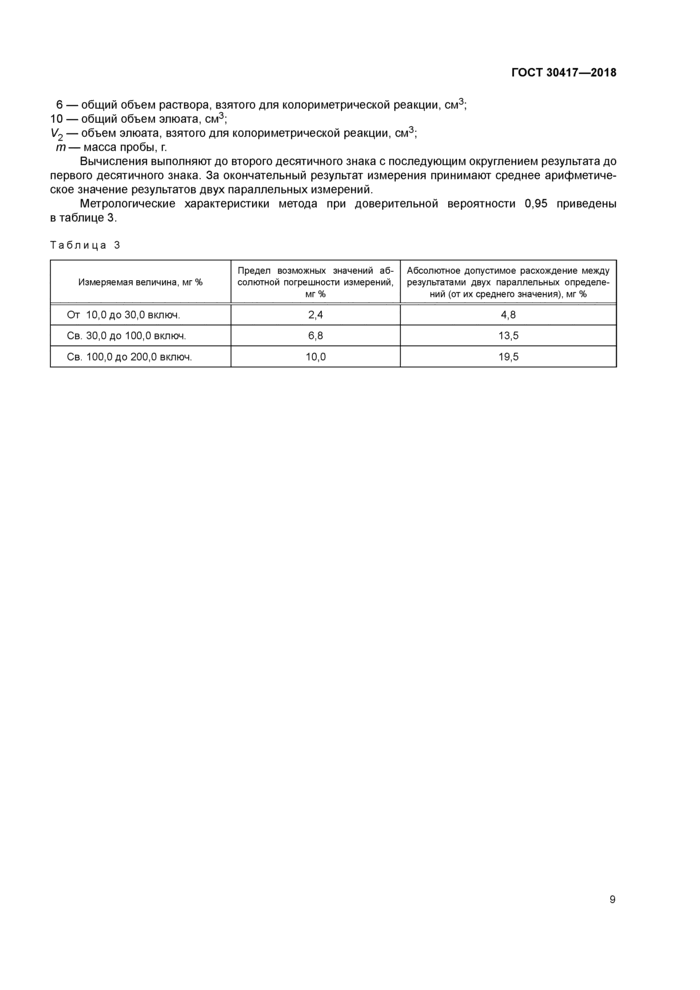
Вычисления выполняют до второго десятичного знака с последующим округлением результата до первого десятичного знака. За окончательный результат измерения принимают среднее арифметическое значение результатов двух параллельных измерений.
Метрологические характеристики метода при доверительной вероятности 0,95 приведены в таблице 3.
|
Таблица 3 | ||||||||||||
|
Библиография
[1] ФС 42-2668-95 Кислота аскорбиновая
[2] Государственная фармакопея, X изд . с 579 Раствор ретинола ацетата в масле
[3] ФС 42-2229—84 Ретинола пальмитат
[4] ФС 42-2495—87 о-Токоферола ацетат
УДК 543.422.7:006 354 МКС 67.200.10
Ключевые слова: масла растительные, витамин А, витамин Е. ретинола ацетат, ретинола пальмитат, токоферола ацетат
Редактор МВ Терехина Технический редактор В Н Прусакова Корректоров Смирнова Компьютерная верстка А Н Золотаревой
Сдано в набор 14 11 2018 Подписано в печать 06 12 2018 Формат 60"84V8. Гарнитура Ариал
Ллпечл. 1.86 Уч.-иад л. 1.68 Подготовлено на основе электронной версии, предоставленной разработчиком стандарта
Создано в единичном исполнении ФГУП «СТАНДАРТИНФОРМ» для комплектования Федерального информационного фонда стандартов. 117418 Москва, Нахимовский пр-т. д. 31. к. 2. www gostinto ш mfo@gostinfo ru
Содержание
1 Область применения.................................................................1
2 Нормативные ссылки.................................................................1
3 Условия проведения измерения........................................................2
4 Отбор проб и подготовка пробы........................................................2
5 Определение массовой доли витамина А................................................2
6 Определение массовой доли витамина Е методом тонкослойной хроматографии...............5
Библиография........................................................................10
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
МАСЛА РАСТИТЕЛЬНЫЕ Методы определения массовых долей витаминов А и Е
Vegetable oils Methods tor determination of A and E vitamins content
Дата введения — 2020—01—01
1 Область применения
Настоящий стандарт устанавливает методы определения массовых долей витаминов А и Е в растительных маслах.
2 Нормативные ссылки
В настоящем стандарте использованы нормативные ссылки на следующие межгосударственные стандарты:
ГОСТ OIML R 76-1—2011 Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия
ГОСТ 4147-74 Реактивы. Железо (III) хлорид 6-водный. Технические условия ГОСТ 4166-76 Реактивы. Натрий сернокислый. Технические условия
ГОСТ 4919.1-2016 Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов
ГОСТ 5815-77 Реактивы. Ангидрид уксусный. Технические условия
ГОСТ 5962-2013 Спирт этиловый ректификованный из пищевого сырья. Технические условия ГОСТ 6709-72 Вода дистиллированная. Технические условия
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 12026-76 Бумага фильтровальная лабораторная. Технические условия
нические условия
ГОСТ 14919-83 Электроплиты, электроплитки и жарочные электрошкафы бытовые. Общие тех
Хлороформ. Технические условия
Реактивы. Калий марганцовокислый. Технические условия Реактивы. Калия гидроокись. Технические условия
Посуда и оборудование лабораторные стеклянные. Типы, основные параметры
и размеры
ГОСТ 29227-91 (ИСО 835-1—81) Посуда лабораторная стеклянная. Пипетки градуированные. Часть 1. Общие требования
ГОСТ 32190-2013 Масла растительные. Правила приемки и методы отбора проб
Примечание — При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования — на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю «Национальные стандарты», который опубликован по состоянию на 1 января текущего года, и по выпускам
Издание официальное
ежемесячного информационного указателя «Национальные стандарты» за текущий год Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку
3 Условия проведения измерения
При подготовке и проведении измерений в помещении лаборатории должны быть соблюдены следующие условия:
- температура окружающей среды...................................от 15 °С до 30 °С;
- относительная влажность воздуха...................................от 20 % до 90 %;
- напряжение питающей сети........................................... (220 ± 15) В;
- частота переменного тока.............................................. (50 ± 2) Гц.
4 Отбор проб и подготовка пробы
Отбор проб — по ГОСТ 32190.
Пробу испытуемого масла тщательно перемешивают.
5 Определение массовой доли витамина А
5.1 Сущность метода
Метод основан на омылении липидов растительного масла, выделении неомыляемых веществ, содержащих витамин А, проведении колориметрической реакции хлороформного раствора неомыляемых веществ с треххлористой сурьмой и измерении оптической плотности полученного раствора при длине волны 620 нм. Определение массовой доли витамина А проводят по градуировочному графику.
5.2 Средства измерений, вспомогательное оборудование, посуда, реактивы и материалы
Средства измерений, вспомогательное оборудование, реактивы и материалы должны соответствовать требованиям нормативных документов, указанных ниже, или требованиям нормативных и технических документов, действующих на территории государства, принявшего стандарт.
Весы неавтоматического действия по ГОСТ OIML R 76-1 с пределами допускаемой абсолютной погрешности ±0,0002 г.
Спектрофотометр, спектроколориметр или фотоколориметр, позволяющий производить измерения при длине волны 620 нм.
Баня водяная.
Электроплитка по ГОСТ 14919 закрытого типа.
Колба К-1-250-29/32 по ГОСТ 25336.
Колба Кн-1-1000-29/32 по ГОСТ 25336.
Колба Кн-2-250-29/32 ТХС по ГОСТ 25336.
Колба 2-100-2 по ГОСТ 1770.
Пробирки П-4-10-14/23 ХС по ГОСТ 25336.
Цилиндры 1 (3)-250-2 по ГОСТ 1770.
Воронка В-25-38 ХС или В-36-50 ХС по ГОСТ 25336.
Воронка ДВ-1-500 по ГОСТ 25336.
Пипетка 2-1-1-1 по ГОСТ 29227.
Пипетка 2-1-1(2)-5(10) по ГОСТ 29227.
Чашка выпарительная 3(4) по ГОСТ 9147.
Бутылка стеклянная любая вместимостью 1 дм3 с корковой пробкой.
Кислота аскорбиновая (1).
Ретинола ацетат (2).
Ретинола пальмитат (3).
Испаритель ротационный или установка, состоящая из колбы К-1-100-29/32 ТС по ГОСТ 25336, холодильника ХПТ-1-400(600)-14/23 по ГОСТ 25336, алонжа АКП-14/23-14/23 ТС по ГОСТ 25336. на-
садки HI-29/32-14/23-14/23 ТС по ГОСТ 25336. колбы К-1-250-14/23 ТС по ГОСТ 25336. насоса водоструйного по ГОСТ 25336.
Бумага фильтровальная Ф по ГОСТ 12026.
Спирт этиловый ректификованный технический по ГОСТ 5962.
Калия гидроокись по ГОСТ 24363, ч„ ч. д. а.
Кальций хлористый плавленый.
Калий марганцовокислый по ГОСТ 20490, ч., ч. д. а.
Натрий сернокислый по ГОСТ 4166, ч., ч. д. а.
Сурьма треххлористая, ч.. ч. д. а.
Ангидрид уксусный по ГОСТ 5815.
Эфир этиловый очищенный или эфир медицинский.
Фенолфталеин, спиртовой раствор с массовой долей индикатора 1 %: готовят по ГОСТ 4919.1.
Вода дистиллированная по ГОСТ 6709.
Хлороформ по ГОСТ 20015.
Допускается применение других средств измерения и оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающих необходимую точность измерения, а также реактивов, имеющих качество не ниже указанных.
5.3 Подготовка к определению
5.3.1 Подготовка растворов и реактивов
5.3.1.1 Приготовление безводного сернокислого натрия Сернокислый натрий нагревают в выпарительной чашке при температуре
(100 ± 5) °С до тех пор. пока не образуется рыхлый порошок.
5.3.1.2 Очистка этилового эфира
В стеклянную бутылку вместимостью 1 дм3 с корковой пробкой взвешивают (5,0 ± 1,0) г марганцовокислого калия и (10,0 ± 1,0) г гидроокиси калия, заливают 1 дм3 этилового эфира и оставляют на 1 сут в темном месте. Затем эфир перегоняют на водяной бане при температуре от 33 °С до 35 °С.
5.3.1.3 Приготовление сухого хлороформа
В стеклянную бутылку вместимостью 1 дм3 помещают от 40 до 50 г прокаленного хлористого кальция. заливают 1 дм3 хлороформа и выдерживают в течение 1 сут. затем перегоняют при температуре от 60 °С до 61 *С и хранят в бутылке из темного стекла с притертой пробкой.
5.3.1.4 Приготовление спиртового раствора гидроокиси калия концентрации с (КОН) = 2 моль/дм3.
(120 ± 5) г гидроокиси калия помещают в колбу и растворяют в 1 дм3 этилового спирта. Спиртовую
щелочь хранят в холодильнике не более 1 мес.
5.3.1.5 Приготовление раствора треххлористой сурьмы (реагент Карр-Прайса) В конической колбе взвешивают (20,0 ± 0.5) г треххлористой сурьмы с записью результата до второго десятичного знака. Добавляют 100 см3 хлороформа и растворяют, нагревая на водяной бане (температура воды не выше 50 °С), периодически встряхивая. Раствор охлаждают до комнатной температуры, добавляют от 2 см3 до 3 см3 уксусного ангидрида, колбу плотно закрывают и оставляют на ночь для отстаивания. Затем верхнюю прозрачную часть раствора осторожно сливают через бумажный фильтр в темную бутылку с притертой пробкой. Раствор годен для работы по истечении 1 сут. Раствор хранят в холодильнике не более 1 мес.
Примечание — Треххлористая сурьма вызывает серьезные ожоги кожи и и слизистых оболочек В случае попадания на кожу или в глаза поврежденный участок необходимо промыть большим количеством воды
5.3.2 Построение градуировочного графика
5.3.2.1 Перед построением градуировочного графика уточняют концентрацию ретинола ацетата или ретинола пальмитата спектрофотометрическим методом в соответствии с (2) или (3).
5.3.2.2 В мерной колбе на 100 см3 взвешивают (0.10 ± 0,01) г масляного раствора витамина А (ретинола пальмитата или ретинола ацетата) с записью результата до четвертого десятичного знака. Растворяют в хлороформе, доводят хлороформом до метки и хорошо перемешивают.
Массовую долю витамина А в растворе X,. ME' в 1 см3, вычисляют по формуле
ME — международная единица (в фармакологии ME обозначает количество вещества).
где с, — концентрация витамина А-ацетата (или А-пальмитата). ME в 1 г масляного раствора; ту — масса масляного раствора, г;
100 — объем хлороформного раствора витамина А. см3.
Если концентрация витамина А-ацетата (или А-пальмитата) в масляном растворе выражена в процентах, то концентрацию витамина А, X, и Х3, ME в 1 см3 хлороформного раствора, вычисляют по формулам:
(для витамина А-ацетата)
(2)
v <h т2 -2907000
Х2"-Тлп-:
(для витамина А-пальмитата)
(3)
v с2т2-1807000 Хз =-100-■
где С2 — концентрация витамина А-ацетата (или А-пальмитата) в масляном растворе, %;
т2— масса масляного раствора, г;
2907000 — биологический эквивалент 1 г витамина А-ацетата с массовой долей 100 %. ME;
1807000 — биологический эквивалент 1 г витамина А-пальмитата с массовой долей 100 %. ME.
5.3.2.3 В пробирках готовят разведением хлороформного раствора витамина А растворы концентрацией витамина А от (5 ± 2) до (40 ± 2) ME в 1 см3 с интервалом 5 ME. Для разведения используют хлороформ.
5.3.2.4 Из каиадой пробирки отбирают пипеткой по 0.4 см3 раствора в кювету толщиной 1 см, помещают кювету в кюветодержатель фотоколориметра или спектрофотометра, добавляют 4 см3 раствора треххлористой сурьмы, приготовленного по 5.3.1.5, и быстро измеряют оптическую плотность раствора при длине волны 620 нм. В качестве контроля используют раствор, состоящий из 0,4 см3 хлороформа и 4 см3 раствора треххлористой сурьмы. Для построения градуировочного графика по оси ординат откладывают полученные значения оптической плотности, а по оси абсцисс соответствующую им концентрацию витамина А, ME в 1 см3.
Примечания
1 Градуировочный график строится для каждого спектрофотометра или фотоколориметра и проверяется при смене партий реактивов и приборов путем измерения оптической плотности стандартных растворов витамина А любых двух разных концентраций Отклонение оптической плотности не должно превышать предела допускаемой погрешности прибора
2 В случае длительного хранения масляного раствора витамина А необходимо один раз в полгода проверять его концентрацию по соответствующему градуировочному графику Отклонение концентрации не должно превышать погрешности метода в данном диапазоне концентраций (см таблицу 1).
5.4 Проведение измерения
(3 ± 1) г растительного масла взвешивают в колбе. Результат записывают до четвертого десятичного знака. Добавляют (0,1 ± 0,01) г аскорбиновой кислоты и 50 см3 спиртового раствора гидроокиси калия концентрации с (КОН) = 2 моль/дм3.
Колбу соединяют с обратным воздушным холодильником и кипятят смесь на водяной бане в течение 30 мин. После этого содержимое колбы охланщают и количественно переносят в делительную воронку, дважды ополаскивая колбу порциями дистиллированной воды по 50 см3. Неомыляемые вещества экстрагируют тремя порциями этилового эфира по 50 см3.
Обьединенный эфирный экстракт переносят в делительную воронку и промывают дистиллированной водой порциями от 50 до 100 см3 до нейтральной реакции по фенолфталеину.
Промытую эфирную вытяжку сливают в сухую колбу, добавляют (10 ± 1) г безводного сернокислого натрия и оставляют на 30 мин в темном месте, периодически взбалтывая. Затем содержимое колбы
фильтруют через бумажный фильтр. Сернокислый натрий в колбе и фильтр промывают этиловым эфиром. Эфир собирают в колбе и отгоняют при температуре не выше 30 °С. Остаток в колбе, представляющий собой неомыляемые вещества, после отгонки растворителя должен быть сухим. Если остаток влажный, то его растворяют в 20 см3 этилового эфира, добавляют (2.0 ± 0.5) г безводного сернокислого натрия и оставляют на 30 мин в темном месте. Затем содержимое колбы фильтруют через бумажный фильтр, тщательно промывая фильтр и сернокислый натрий этиловым эфиром. Эфир отгоняют в вакууме при температуре не выше 30 X. Остаток неомыляемых веществ растворяют в 10 см3 хлороформа.
Колориметрическую реакцию и измерение проводят по 5.3.2.4.
5.5 Обработка результатов
Массовую долю витамина А Х4. ME в 1 г продукта, вычисляют по формуле
Х4=^. W
"Ь
где с3 — концентрация витамина А в хлороформном растворе, определенная по градуировочному графику. ME в см3;
10 — объем раствора неомыляемых веществ в хлороформе, см3; т3 — масса пробы, г
Вычисления проводят до первого десятичного знака с последующим округлением результата до целого числа.
За окончательный результат измерения принимают среднее арифметическое значение результатов двух параллельных измерений.
5.6 Метрологические характеристики
Метрологические характеристики метода при доверительной вероятности 0.95 приведены в таблице 1.
|
Таблица 1 | ||||||||||||
|
Если расхождение между двумя параллельными измерениями превышает значение, указанное в таблице, измерение следует повторить.
6 Определение массовой доли витамина Е методом тонкослойной хроматографии
6.1 Аппаратура, посуда, реактивы, материалы
Средства измерений, вспомогательное оборудование, реактивы и материалы должны соответствовать требованиям нормативных документов, указанных ниже, или требованиям нормативных и технических документов. действующих на территории государства, принявшего стандарт.
Спектрофотометр или фотоколориметр, позволяющий производить измерения при длине волны /. = 520 нм.
Весы неавтоматического действия по ГОСТ OIML R 76-1 с пределами допускаемой абсолютной погрешности ±0.0002 г.
Шкаф сушильный лабораторный.
Баня водяная.
Колба Кн-1-250-29/32 ТС по ГОСТ 25336.
Колба К-1-250-29/32 ТС по ГОСТ 25336.
Воронка В-25-38 ХС или В-56-80 ХС по ГОСТ 25336.
Воронка ВД-1-250 ХС по ГОСТ 25336.
Пробирки П-2-10-14/23 ХС по ГОСТ 1770.
Холодильник воздушный.
Испаритель ротационный или установка, состоящая из колбы К-1-100-29/32 ТС по ГОСТ 25336, холодильника ХПТ-1-400(600)-14/23 по ГОСТ 25336. алонжа АКП-14/23-14/23 ТС по ГОСТ 25336, изгиба И Z 75°2К-29/32-14/23 ТС по ГОСТ 25336, колбы К-1-250-14/23 ТС по ГОСТ 25336. насоса водоструйного по ГОСТ 25336.
Пипетки 2-1-1-0.5; 1-1-1-1 и 2-1-1-5 по ГОСТ 29227.
Цилиндр 1 (3)-25-2 по ГОСТ 1770.
Пластинки «Силуфол» размером 15x15 см или 20x20 см.
Калия гидроокись по ГОСТ 24363, х. ч. или ч. д. а.
Спирт этиловый ректификованный технический по ГОСТ 5962.
Натрий сернокислый по ГОСТ 4166.
Кальций хлористый обезвоженный чистый (3).
Эфир этиловый очищенный или эфир медицинский.
Гексан, х. ч.
Кислота аскорбиновая [1].
Хлороформ по ГОСТ 20015. х. ч.
Калий марганцовокислый по ГОСТ 20490.
Фенолфталеин, спиртовой раствор с массовой долей 1 %; готовят по ГОСТ 4919.1.
Бумага фильтровальная по ГОСТ 12026.
Вода дистиллированная по ГОСТ 6709
Железо (III) хлорид 6-водный (хлорное железо) по ГОСТ 4147, спиртовой раствор с массовой долей 0.25 %.
а. а’-дипиридил или о-фенантролин. спиртовой раствор с массовой долей 0.1 %. а-Токоферола ацетат [4J.
Допускается применение других средств измерений и оборудования, не уступающих вышеуказанным по метрологическим и техническим характеристикам и обеспечивающих необходимую точность измерения, а также реактивы, имеющие качество не ниже указанных.
б. 2 Подготовка к проведению измерения
6.2.1 Подготовка реактивов
6.2.1.1 Приготовление безводного сернокислого натрия по 5.3.1.1.
6.2.1.2 Очистка этилового эфира по 5.3.1.2.
6.2.1.3 Приготовление сухого хлороформа по 5.3.1.3.
Для работы используют только свежеперегнанные растворители.
6.2.1.4 Приготовление реактива Эммери-Энгеля
Реактив Эммери-Энгеля готовят, смешивая равные объемы растворов хлорного железа и а, а'-дипиридила (о-фенантролина).
6.2.2 Подготовка камеры для хроматографирования
Не менее чем за 30 мин до начала хроматографирования в камеру наливают смесь этилового эфира и гексана (1:1) на высоту 0.5 см.
6.3 Построение градуировочного графика
Градуировочный график строят на основании результатов измерения проб с известным содержанием а-токоферола.
а-Токоферол выделяют из препарата — а-токоферола ацетата. Для этого взвешивают в колбе (0.05 ± 0.01) г а-токоферола ацетата и записывают результат до четвертого десятичного знака, проводят омыление и выделяют неомыляемые вещества, как указано в 6.4.1.
Эфир из объединенного фильтрата отгоняют на водяной бане до объема от 1 до 2 см3. Остаток эфира отгоняют под вакуумом при температуре не выше 30 °С. Остаток немедленно растворяют в этиловом спирте.
(5)
Количество а-токоферола в выделенном остатке М, г. рассчитывают по формуле
М = 0.892т,
где 0,892 — содержание о-токоферола в 1 г а-токоферола ацетата; т — масса а-токоферола ацетата, взятая для анализа, г.
Необходимый объем этилового спирта должен быть таким, чтобы концентрация о-токоферола в растворе спирта была 1 мг/см3. (Например, если масса о-токоферола 0.053 г. то объем этилового спирта — 53 см3 и т. д.).
Из полученного раствора готовят серию стандартных растворов в соответствии с таблицей 2.
|
Таблица 2 | ||||||||||||||||||||||||||||
|
Из каждого раствора в пробирку отбирают пипеткой 1 см3, добавляют 3 см3 этилового спирта. 1 см3 раствора а. о'-дипиридила (или о-фенантролина). взбалтывают, добавляют по каплям 1 см3 раствора хлорного железа, снова взбалтывают. Полученный раствор помещают на 3 мин в темное место, после чего наливают в кювету и измеряют его оптическую плотность на спектрофотометре при /. = 520 нм (или фотоэлектроколориметре с зеленым фильтром). В качестве контрольного раствора используют смесь из 4 см3 этилового спирта. 1 см3 раствора, а, о’-дипиридила и 1 см3 раствора хлорного железа, приготовленную в тех же условиях
Градуировочный график строят в координатах: оптическая плотность (Д) — концентрация а-токоферола в анализируемом растворе с2. мг/см3. вычисляемая по формуле
с2 = ^. (6)
6
где с, — концентрация а-токоферола в соответствующем стандартном растворе, мг/см3;
Vy — объем стандартного раствора, взятый для реакции. 1 см3;
6 — объем анализируемого раствора, см3.
Градуировочный график строят для каждого спектрофотометра (фотоколориметра) и проверяют при смене партий реактивов путем измерения оптической плотности стандартных растворов двух разных концентраций.
Примечание — Градуировочный график строится для каждого спектрофотометра или фотоколориметра и проверяется при смене партий реактивов и приборов путем измерения оптической плотности стандартных растворов витамина Е любых двух разных концентраций Отклонение оптической плотности не должно превышать предела допускаемой погрешности прибора
6.4 Проведение измерения
Все этапы измерения следует проводить по возможности быстро, предохраняя пробы от попадания на них прямого солнечного света.