ГОСТ ИСО 21569-2009
Продукты пищевые. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Методы качественного обнаружения на основе анализа нуклеиновых кислот
Содержит описание процедур качественного определения генетически модифицированных организмов (ГМО) и содержащих их продуктов путем анализа нуклеиновых кислот, выделяемых из исследуемого образца. В стандарте приводятся общие требования к специфическому определению и идентификации целевых последовательностей нуклеиновой кислоты (ДНК) и к подтверждению идентичности амплифицированной последовательности ДНК. Стандарт был разработан для матриц пищевых продуктов, однако может быть также применен для анализа других матриц (например, корма для животных, образцы растений из окружающей среды).
Идентичен международному стандарту ISO 21569:2005, IDT
Оглавление
Введение
1 Область применения
2 Нормативные ссылки
3 Термины и определения
4 Принцип метода
5 Реактивы
6 Инструменты и оборудование
7 Процедура анализа
8 Интерпретация результатов
9 Предоставление результатов и контроль качества
10 Протокол испытаний
Приложение А (справочное) Методы, специфичные к целевым таксонам
Приложение В (справочное) Методы скрининга
Приложение С (справочное) Методы, специфичные к генетической конструкции
Приложение D (справочное) Методы, специфичные к трансформационным событиям
Библиография
Приложение Д.А (справочное) Сведения о соответствии межгосударственного стандарта ссылочному международному стандарту
66 страниц
| Дата введения | 30.09.2017 |
|---|---|
| Добавлен в базу | 01.01.2019 |
| Завершение срока действия | 01.06.2020 |
| Актуализация | 01.01.2021 |
Организации:
| 11.11.2009 | Утвержден | Евразийский совет по стандартизации, метрологии и сертификации | 36 |
|---|---|---|---|
| 24.09.2010 | Утвержден | Госстандарт Республики Беларусь | 58 |
| Разработан | БелГИМ |
Foodstuffs. Methods of analysis for the detection of genetically modified organisms and derived products. Qualitative nucleic acid based methods
Чтобы бесплатно скачать этот документ в формате PDF, поддержите наш сайт и нажмите кнопку:

стр. 1

стр. 2

стр. 3

стр. 4

стр. 5

стр. 6

стр. 7

стр. 8

стр. 9

стр. 10

стр. 11

стр. 12

стр. 13
стр. 14

стр. 15

стр. 16

стр. 17
стр. 18
стр. 19

стр. 20

стр. 21

стр. 22

стр. 23

стр. 24

стр. 25

стр. 26

стр. 27

стр. 28
стр. 29

стр. 30
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬ
ПРОДУКТЫ ПИЩЕВЫЕ
Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Методы качественного обнаружения на основе анализа нуклеиновых кислот
ПРАДУКТЫ ХАРЧОВЫЯ
Метады анал1зу для выяулення генетычна мадыф1каваных аргашзмау i вытворных прадуктау. Метады якаснага выяулення на аснове анал1зу нуклешавых мслот
(ISO 21569:2005, ЮТ)
Издание официальное
о>
2
Г осстандарт Минск
Предисловие
Евразийский совет по стандартизации, метрологии и сертификации (ЕАСС) представляет собой региональное объединение национальных органов по стандартизации государств, входящих в Содружество Независимых Государств. В дальнейшем возможно вступление в ЕАСС национальных органов по стандартизации других государств.
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены ГОСТ 1.0-92 «Межгосударственная система стандартизации. Основные положения» и ГОСТ 1.2-97 «Межгосударственная система стандартизации. Стандарты межгосударственные, правила и рекомендации по межгосударственной стандартизации. Порядок разработки, принятия, применения, обновления и отмены».
Сведения о стандарте
1 ПОДГОТОВЛЕН республиканским унитарным предприятием «Белорусский государственный институт метрологии» (БелГИМ) на основе собственного аутентичного перевода стандарта, указанного в пункте 4
2 ВНЕСЕН Государственным комитетом по стандартизации Республики Беларусь
3 ПРИНЯТ Евразийским советом по стандартизации, метрологии и сертификации (протокол № 36 от 11 ноября 2009 г.)
|
За принятие проголосовали: | |||||||||||||||||||||
|
4 Настоящий стандарт идентичен международному стандарту ISO 21569:2005 Foodstuffs - Methods of analysis for the detection of genetically modified organisms and derived products - Qualitative nucleic acid based methods (Продукты пищевые. Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов. Методы качественного обнаружения на основе анализа нуклеиновых кислот).
Международный стандарт разработан CEN/TC 275 «Анализ пищевых продуктов. Горизонтальные методы» Европейского комитета по стандартизации (CEN) совместно с ISO/TC 34 «Пищевые продукты» Международной организации по стандартизации (ISO) в соответствии с Соглашением о техническом сотрудничестве между ISO и CEN (Венским соглашением).
Перевод с английского языка (еп).
Официальные экземпляры международного стандарта, на основе которого подготовлен настоящий межгосударственный стандарт, и международных стандартов, на которые даны ссылки, имеются в Национальном фонде ТИПА.
В разделе «Нормативные ссылки» и тексте стандарта ссылки на международные стандарты актуализированы.
Сведения о соответствии межгосударственного стандарта ссылочному международному стандарту приведены в дополнительном приложении Д.А.
Степень соответствия - идентичная (ЮТ)
5 ВВЕДЕН В ДЕЙСТВИЕ постановлением Госстандарта Республики Беларусь от 24 сентября 2010 г. № 58 непосредственно в качестве государственного стандарта Республики Беларусь с 1 января 2011 г.
6 ВВЕДЕН ВПЕРВЫЕ
ГОСТ ИСО 21569-2009
7.5 Контроли
Из-за существования риска получения ложноположительных и/или ложноотрицательных результатов в каждое исследование ПЦР следует включить соответствующие контроли (см. ISO 24276).
При условии наличия на рынке соответствующих сертифицированных образцов стандартного состава (референсные образцы стандартного состава) их следует использовать в качестве положительных и отрицательных контрольных проб.
7.6 Проведение ПЦР, обнаружение и подтверждение продуктов ПЦР
В приложениях А - D приводится подробное описание конкретных этапов последовательности ПЦР-анализа.
Примечание - Если для обнаружения продуктов ПЦР используется электрофорез в агарозном геле, размер продуктов ПЦР может быть оценен с помощью соответствующих маркеров длины ДНК, которые следует запустить параллельно с исследуемыми ПЦР-продуктами.
В некоторых случаях желательно подтвердить положительный или отрицательный результат для определенной генетической модификации. Такое подтверждение может быть проведено с помощью применения праймеров к альтернативной целевой последовательности; этот способ бывает особенно полезен при подтверждении результатов скрининга.
Положительная идентификация специфической последовательности целевой ДНК может быть подтверждена соответствующим методом (но не определением размера ПЦР-продукта), например:
- путем гибридизации ПЦР-продукга со специфичными зондами, или
- путем проведения рестрикционного анализа ПЦР-продуктов; длина полученных фрагментов должна соответствовать ожидаемой длине целевой последовательности ДНК после рестрикции, или
- путем секвенирования (определения последовательности) ПЦР-продукга, или
-другим эквивалентным методом подтверждения.
Если используемые праймеры подобраны для обнаружения последовательностей, полученных из инфекционных организмов (встречающиеся в природе генетически немодифицированные организмы, например вирусы или бактерии), рекомендуется убедиться в том, что обнаруженная ДНК действительно происходит из ГМО. Такое подтверждение может быть выполнено путем проверки отсутствия другой ДНК, произошедшей из инфекционного организма.
Пример - 35S-npoMomop, полученный из вируса мозаики цветной капусты (CaMV); соответственно, обнаружение этого промотора может быть обусловлено наличием ДНК, произошедшей из ГМО или из CaMV [6]. Проверив наличие другой ДНК из вируса мозаики цветной капусты, можно удостовериться в происхождении Эбб-промотора и последовательности ГМО (если не обнаружена другая последовательность ДНК из CaMV).
8 Интерпретация результатов
8.1 Общие положения
Результат ПЦР может быть:
a) положительным, если обнаружен специфический ПЦР-продукг, а все контрольные пробы дают результаты в соответствии с ISO 24276, таблица 2, или
b) отрицательным, если не обнаружен специфический ПЦР-продукт, а все контрольные пробы дают результаты в соответствии с ISO 24276, таблица 2.
Примечание - Специфичные для трансформационных событий целевые последовательности иногда обнаруживаются вместе с другими специфичными последовательностями трансформационных событий в одном ГМО (например, из-за наложения генов [7]).
Если получен неопределенный (позволяющий проводить двоякую интерпретацию) результат, анализ следует повторить, см. ISO 24276.
8.2 Подтверждение
Подтверждение положительных или отрицательных результатов может быть выполнено в соответствии с 7.6.
5
9 Представление результатов и контроль качества
9.1 Общие положения
Результаты должны быть представлены определенно, т. е. не в виде «±».
Отрицательный результат никогда не следует предоставлять в виде «ГМО отсутствует».
В идеале в протоколе должен быть указан предел обнаружения, определенный по соответствующему исследуемому образцу. Однако это требует определенных материалов, ДНК исключительно высокого качества и/или использования сложного лабораторного оборудования, которое имеется не у всех лабораторий. Такой анализ может стать очень трудоемким и/или дорогостоящим, а следовательно, не может быть применен в обычных лабораторных условиях.
В протоколе следует указать по крайней мере предел обнаружения, определенный для образца стандартного состава, и относительное значение для конкретного материала образца (предпочтительно заданное количество раствора геномной ДНК, например 100 нг 0,01 % ДНК GTS 40-3-2).
9.2 Представление отрицательного результата
В протоколе испытаний должен присутствовать следующий текст:
«Целевая последовательность Y не обнаружена в образце X.
Предел обнаружения метода х % определен по АВС (укажите референсный образец стандартного состава)».
Если невозможно доказать, что количество целевой ДНК, использованное в ПЦР, было достаточным для применения предела обнаружения, в протокол следует добавить следующее предложение:
«Однако количество целевой ДНК, выделенной из образца X, может быть/было недостаточным для применения предела обнаружения в этом образце».
Примечание - Предел обнаружения в образце определяется по количеству ДНК вида, использованному в аналитической реакции (число копий), и соотношению к абсолютному пределу обнаружения целевой генетической модификации (число копий) [7].
9.3 Представление положительного результата
В протоколе испытаний должен присутствовать следующий текст:
«В образце X обнаружена целевая последовательность У».
Можно также указать ГМО, если доступна такая информация.
9.4 Требования к контролю качества
Результаты из обеих анализируемых частей образца должны соответствовать друг другу. Если для одной анализируемой части получен отрицательный результат, а для другой - положительный, то анализ следует повторить (см. ISO 24276), по возможности увеличив количество матрицы нуклеиновой кислоты в реакции, так, чтобы получить соответствующие друг другу результаты для обеих частей. Более того, следует как минимум проверить чистоту матрицы ДНК, включив в анализ контроль ингибирования ПЦР. Возможно, будет полезным использование других контрольных методов, например контроль длины и целостности матрицы нуклеиновой кислоты.
10 Протокол испытаний
Протокол испытаний должен быть оформлен в соответствии с требованиями ISO 24276 и должен содержать по крайней мере следующую дополнительную информацию:
- предел обнаружения и материал образца, использованный для определения предела обнаружения;
- описание специфичности аналитического метода;
- результат, представленный в соответствии с требованиями раздела 9.
ГОСТ ИСО 21569-2009Приложение А
(справочное)
Методы, специфичные к целевым таксонамА.1 Метод, специфичный к целевому таксону, для определения компонентов, полученных из соевых бобовА.1.1 Общие положения
А.1.1 Общие положения
Описана стандартная процедура определения видоспецифичного однокопийного гена, встречающегося в соевых бобах (Glycine max).
Этот метод используется для оценки амплифицируемости ДНК-продуктов, в состав которых входят соевые бобы.
А.1.2 Метрологическая аттестация и критерии выполнения
А.1.2.1 Совместные сличительные испытания
Этот метод был метрологически аттестован в совместных сличительных испытаниях [8], [9], организованных рабочей группой «Разработка методов идентификации пищевой продукции, произведенной с использованием технологий генной инженерии» Немецкого федерального института защиты здоровья потребителей и ветеринарной медицины (BgW) в соответствии со статьей 35 Федерального закона Германии о пищевых продуктах. Для выделения ДНК использовали метод ЦТАБ, описанный в ISO 21571:2005, А.З (однако вес анализируемой части образца составлял 100 мг).
Данные совместных сличительных испытаний приводятся в таблице А.1.
|
Таблица А.1 - Результаты совместных сличительных испытаний | ||||||||||||||||||||||||
|
А.1.2.2 Молекулярная специфичность
А.1.2.2.1 Общие положения
Это приложение удовлетворяет требованиям, изложенным в разделе 7.
Метод был разработан для целевой последовательности, описанной в базе данных GenBank® 3), доступ № К00821 = М30884.
А.1.2.2.2 Теоретическая часть
В качестве целевой последовательности из баз данных генов был выбран ген соевого лектина Le1 [10]'
Поиск по базам данных (NCBI BlastN® , European Molecular Biology Laboratory (EMBL), по состоянию на 28 сентября 2001 г.) не обнаружил сходства последовательностей ДНК с другими сельскохозяйственными растениями. Однако GM03 дал 100%-ное совпадение последовательностей со следующими
3) GenBank и BlastN - это примеры представленных на рынке программных продуктов, которые могут быть использованы для оценки специфичности. Эта информация приводится исключительно для ознакомления пользователей настоящего стандарта и ни при каких условиях не может служить рекомендацией или одобрением этих продуктов организацией ISO. Допускается использование аналогичных программ, если они позволяют получать такие же результаты.
7
пунктами баз данных: АХ033509 (последовательность 17 из патента DE19906169), АХ033507 (последовательность 15 из патента DE19906169) и АХ033501 (последовательность 9 из патента DE19906169), в то время как GM04 совпадало только с доступом № АХ033509 (последовательность 17 из патента DE19906169). Обратите внимание на то, что доступ № М30884- это то же самое, что и доступ К00821, - элемент базы данных GenBank®, первоначально внесенный в базу в 1993 году.
Количество копий целевой последовательности не определяли, однако предполагалось, что это однокопийный ген.
А.1.2.2.3 Экспериментальная часть
При проведении ПЦР с использованием ДНК, выделенной из других сельскохозяйственных растений (бобовых, зерновых и овощных культур), а также из говядины и свинины, не наблюдали амплификацию. Метод ПЦР для соевых бобов показал свою высокую специфичность к ДНК соевых бобов [10], [11].
А.1.2.3 Предел обнаружения
Не был определен абсолютный предел обнаружения, однако с помощью флуорометрического анализа было показано, что метод способен обнаруживать по меньшей мере 0,1 нг ДНК соевых бобов.
А.1.3 Адаптация
Отсутствует конкретная информация.
А.1.4 Принцип
Принцип метода заключается в амплификации фрагмента ДНК из соевых бобов длиной 118 п. н. с использованием ПЦР и разделении с помощью электрофореза в агарозном геле.
А.1.5 Реактивы
Информация по качеству используемых реактивов приводится в ISO 24276.
А.1.5.1 Вода
А.1.5.2 Буфер для ПЦР (без МдС12), 10 * 1.
А. 1.5.3 Раствор МдС12, концентрация МдС12 = 25 ммоль/л.
А. 1.5.4 Раствор dNTP, концентрация dNTP = 2,5 ммоль/л (каждого).
А.1.5.5 Олигонуклеотиды
А.1.5.5.1 Прямой праймер
Ген лектина соевых бобов (позиция базы данных GenBank® № К00821).
Праймер GM03: 5’-дСС СТО ТАС ТСС ACC ССС АТС С-3’.
А.1.5.5.2 Обратный праймер
Ген лектина соевых бобов (позиция базы данных GenBank® № К00821).
Праймер GM04: 5’-gCC CAT СТд САА дСС ТТТ ТТд Тд-3’.
А. 1.5.6 Термостабильная ДНК-полимераза (для ПЦР с «горячим стартом»), 5 IU/мкл.
А. 1.5.7 Зонд для гибридизации (GM)
5’-ggT AgC gTT дСС АдС ТТС д-3’.
А.1.5.8 Солевой буферный раствор с цитратом натрия (SSC) 5 к, pH 7,0
Пятикратный буферный раствор SSC - это раствор, содержащий 0,75 моль/л NaCI и 0,075 моль/л цитрата натрия.
А.1.5.9 Прегибридизационный раствор
Содержит 5 * SSC, 0,1 % (по массе) N-лаурилсаркозина, 0,02 % (по массе) додецил сульфата натрия (SDS) и 1 % блокирующего реактива Blocking Reagent2 или 5 % (по массе) обезжиренного сухого молока [12].
ГОСТ ИСО 21569-2009
А.1.5.10 Раствор для гибридизации
Содержит 10 пмоль зонда для гибридизации в 2,5 мл прегибридизационного раствора (А. 1.5.9). Температура гибридизации - 50 °С. Дополнительная информация по условиям гибридизации приводится в ссылке [12].
А.1.6 Оборудование
А.1.6.1 Амплификатор
А. 1.6.2 Камера для электрофореза, с источником питания.
А.1.7 Процедура анализа
А.1.7.1 Проведение ПЦР
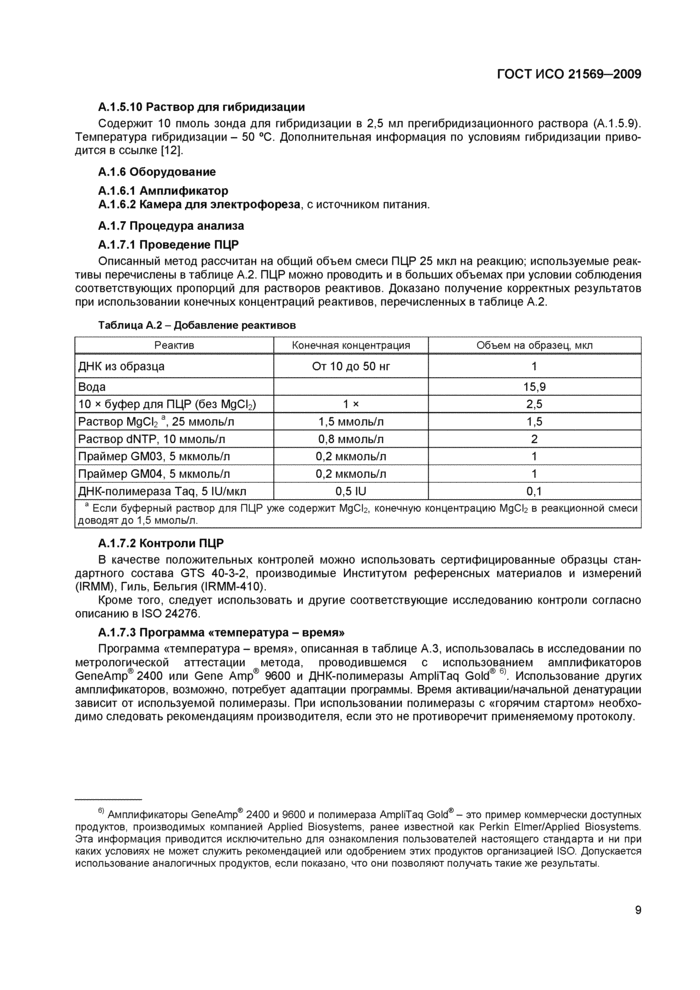
Описанный метод рассчитан на общий объем смеси ПЦР 25 мкл на реакцию; используемые реактивы перечислены в таблице А.2. ПЦР можно проводить и в больших объемах при условии соблюдения соответствующих пропорций для растворов реактивов. Доказано получение корректных результатов при использовании конечных концентраций реактивов, перечисленных в таблице А.2.
|
Таблица А.2 - Добавление реактивов | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
А.1.7.2 Контроля ПЦР
В качестве положительных контролей можно использовать сертифицированные образцы стандартного состава GTS 40-3-2, производимые Институтом референсных материалов и измерений (IRMM), Гиль, Бельгия (IRMM-410).
Кроме того, следует использовать и другие соответствующие исследованию контроли согласно описанию в ISO 24276.
А.1.7.3 Программа «температура - время»
Программа «температура - время», описанная в таблице А.З, использовалась в исследовании по метрологической аттестации метода, проводившемся с использованием амплификаторов GeneAmp®2400 или Gene Amp® 9600 и ДНК-полимеразы AmpliTaq Gold® 3. Использование других амплификаторов, возможно, потребует адаптации программы. Время акгивации/начапьной денатурации зависит от используемой полимеразы. При использовании полимеразы с «горячим стартом» необходимо следовать рекомендациям производителя, если это не противоречит применяемому протоколу.
|
Таблица А.З - Программа «температура - время» | ||||||||||||
|
А.1.8 Специфичность продукта ПЦР
Так как представленный метод может рассматриваться исключительно как контрольный метод для определения качества выделенной ДНК, проверка специфичности основывается только на размере продукта ПЦР.
Если метод используется в целях, отличающихся от упомянутых выше, проверка специфичности продукта амплификации может быть выполнена с помощью гибридизации по Саузерну с использованием олигонуклеотидного зонда GM, меченного дигоксигенином (А.1.5.7-А.1.5.10), или путем секве-нирования (определения последовательности) продукта ПЦР и сравнения результатов с данными базы данных GenBank®, перечисленными в А. 1.5.5.
А.1.9 Общий контроль качества и интерпретация результатов
Предполагается, что целевая последовательность обнаружена, если размер продукта ПЦР соответствует ожидаемой длине целевой последовательности ДНК, определенной путем сравнения с продуктами реакции, полученными из сертифицированных образцов стандартного состава, приготовленных из сои линии GTS 40-3-2 (например, серия стандартов IRMM-410 производства IRMM, Гиль, Бельгия).
Проверка специфичности продукта ПЦР описана в А.1.8.
Обнаружение фрагментов с размером 118 п. н. показывает, что раствор ДНК образца содержит амплифицируемую ДНК, происходящую из соевых бобов, в пределах установленных параметров специфичности, описанных в А. 1.2.2.
Подробная информация об этапах электрофореза приводится в ISO 21571:2005, В.2.
А.2 Метод, специфичный к целевому таксону, для определения многокопийных последовательностей ДНК, обычно присутствующих в хпоропластах растений
А.2.1 Общие положения
Описана стандартная процедура определения многокопийных последовательностей ДНК, обычно присутствующих в хпоропластах растений (интронгенахпоропластов tmL).
Этот метод пригоден для проверки успешности выделения ДНК из образца пищевого продукта, а также для оценки наличия амплифицируемой растительной ДНК. При анализе образцов продуктов, прошедших обработку, применение этого метода зависит от степени деградации ДНК.
Растительная клетка обычно содержит много копий этой последовательности ДНК, а размер целевой последовательности значительно превышает размеры последовательностей ДНК, используемых для обнаружения определенных генетических модификаций. Поэтому этот метод не может использоваться в качестве контроля при количественном определении.
Количество копий в клетке может быть различным у разных видов и тканей растений.
А.2.2 Порядок метрологической аттестации и критерии выполнения
А.2.2.1 Совместное сличительное испытание
Этот метод был метрологически аттестован в совместном сличительном испытании [13], организованном рабочей группой «Разработка методов идентификации пищевой продукции, произведенной с использованием технологий генной инженерии» Немецкого федерального института защиты здоровья потребителей и ветеринарной медицины (BgW) в соответствии со статьей 35 Федерального закона Германии о пищевых продуктах. Для выделения ДНК использовали метод ЦТАБ, описанный в ISO 21571:2005, А.З (однако вес анализируемой части образца составлял 100 мг).
Данные совместных сличительных испытаний приводятся в таблице А.4.
|
Таблица А.4 - Результаты совместных сличительных испытаний | ||||||||||||||||||||
|
А.2.2.2 Молекулярная специфичность
А.2.2.2.1 Общие положения
Это приложение удовлетворяет требованиям, изложенным в разделе 7.
Метод был разработан для целевых последовательностей, описанных в [14], например доступы базы данных GenBank® № Z00044, S54304, XI5901.
А.2.2.2.2 Теоретическая часть
При поиске в базах данных (поиск NCBI BlastN®, база данных EMBL, по состоянию на 28 сентября 2001 г.) не была обнаружена значимая схожесть с последовательностями ДНК нерастительного происхождения.
Были разработаны праймеры, предназначенные для амплификации уникальной последовательности ДНК хлоропластов (интрон, входящий в состав последовательности гена trnL)\ показано отсутствие схожести с нецелевыми последовательностями.
А.2.2.2.3 Экспериментальная часть
При использовании в ПЦР ДНК, выделенной из животных, грибов или бактерий, амплификация не была обнаружена [14].
Была показана амплификация ДНК, выделенной из водорослей, цианобактерий, мхов, птеридо-фитов, покрытосеменных и голосеменных растений [14].
Целевая последовательность была многокопийна и количество копий зависело от вида и типа тканей растений.
А.2.2.3 Предел обнаружения
Не был определен абсолютный предел обнаружения, однако с помощью флуорометрического анализа было показано, что метод способен обнаруживать по меньшей мере 0,1 нг ДНК соевых бобов.
А.2.3 Адаптация
Отсутствует конкретная информация.
А.2.4 Принцип
Принцип метода заключается в амплификации находящегося в гене тРНК хлоропластов фрагмента [14] длиной от 500 до 600 п. н. с использованием ПЦР и разделении с помощью электрофореза в агарозном геле.
А.2.5 Реактивы
Информация по качеству используемых реактивов приводится в ISO 24276.
А.2.5.1 Вода
А.2.5.2 Буфер для ПЦР (без МдС12), 10 *.
А.2.5.3 Раствор МдС12, концентрация МдС12 = 25 ммоль/л.
А.2.5.4 Раствор dNTP, концентрация dNTP = 2,5 ммоль/л (каждого).
А.2.5.5 Олигонуклеотиды
11
А.2.5.5.1 Прямой праймер
Ген тРНКхлоропластов (позиция базы данных GenBank® № Z00044, XI5901).
Праймер с [14]: 5’-CgA ААТ Сдд ТАд АСд СТА Сд-3’.
А.2.5.5.2 Обратный праймер
Ген тРНКхлоропластов (позиция базы данных GenBank® № Z00044, XI5901).
Праймер d [14]: 5’-ggg gAT AgA ggg ACT TgA AC-3’.
A.2.5.6 Термостабильная ДНК-полимераза, 5 IU/мкл.
A.2.6 Оборудование
В соответствии с А.1.6.
А.2.7 Процедура анализа
А.2.7.1 Проведение ПЦР
Описанный метод рассчитан на общий объем смеси ПЦР 25 мкл на реакцию; используемые реактивы перечислены в таблице А.5. ПЦР можно проводить и в больших объемах при условии соблюдения соответствующих пропорций для растворов реактивов. Доказано получение корректных результатов при использовании конечных концентраций реактивов, перечисленных в таблице А.5.
|
Таблица А.5 - Добавление реактивов | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
А.2.7.2 Контроля ПЦР
В качестве положительных контролей можно использовать сертифицированные образцы стандартного состава GTS 40-3-2, производимые Институтом референсных материалов и измерений (IRMM), Гиль, Бельгия (IRMM-410).
Кроме того, следует использовать и другие соответствующие исследованию контроли согласно ISO 24276.
А.2.7.3 Программа «температура - время»
Программа «температура - время», описанная в таблице А.6, использовалась в исследовании по метрологической аттестации метода, проводившемся с использованием амплификаторов GeneAmp®2400 или GeneAmp® 9600 и ДНК-полимеразы AmpliTaq Gold® 4. Использование других амплификаторов, возможно, потребует адаптации программы. Время акгивации/начапьной денатурации зависит от используемой полимеразы. При использовании полимеразы с «горячим стартом» необходимо следовать рекомендациям производителя, если это не противоречит применяемому протоколу.
|
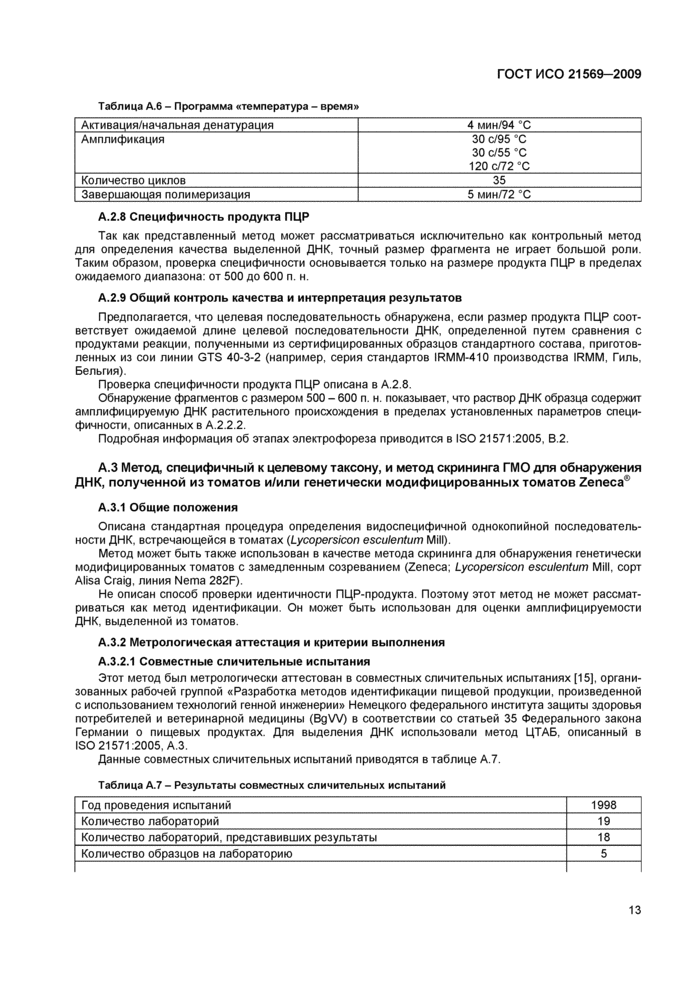
Таблица А.6 - Программа «температура - время» | ||||||||||||
|
А.2.8 Специфичность продукта ПЦР
Так как представленный метод может рассматриваться исключительно как контрольный метод для определения качества выделенной ДНК, точный размер фрагмента не играет большой роли. Таким образом, проверка специфичности основывается только на размере продукта ПЦР в пределах ожидаемого диапазона: от 500 до 600 п. н.
А.2.9 Общий контроль качества и интерпретация результатов
Предполагается, что целевая последовательность обнаружена, если размер продукта ПЦР соответствует ожидаемой длине целевой последовательности ДНК, определенной путем сравнения с продуктами реакции, полученными из сертифицированных образцов стандартного состава, приготовленных из сои линии GTS 40-3-2 (например, серия стандартов IRMM-410 производства IRMM, Гиль, Бельгия).
Проверка специфичности продукта ПЦР описана в А.2.8.
Обнаружение фрагментов с размером 500 - 600 п. н. показывает, что раствор ДНК образца содержит амплифицируемую ДНК растительного происхождения в пределах установленных параметров специфичности, описанных в А.2.2.2.
Подробная информация об этапах электрофореза приводится в ISO 21571:2005, В.2.
А.З Метод, специфичный к целевому таксону, и метод скрининга ГМО для обнаружения ДНК, полученной из томатов и/или генетически модифицированных томатов Zeneca®
А.3.1 Общие положения
Описана стандартная процедура определения видоспецифичной однокопийной последовательности ДНК, встречающейся в томатах (Lycopersicon esculentum Mill).
Метод может быть также использован в качестве метода скрининга для обнаружения генетически модифицированных томатов с замедленным созреванием (Zeneca; Lycopersicon esculentum Mill, сорт Alisa Craig, линия Nema 282F).
He описан способ проверки идентичности ПЦР-продукга. Поэтому этот метод не может рассматриваться как метод идентификации. Он может быть использован для оценки амплифицируемости ДНК, выделенной из томатов.
А.3.2 Метрологическая аттестация и критерии выполнения
А.3.2.1 Совместные сличительные испытания
Этот метод был метрологически аттестован в совместных сличительных испытаниях [15], организованных рабочей группой «Разработка методов идентификации пищевой продукции, произведенной с использованием технологий генной инженерии» Немецкого федерального института защиты здоровья потребителей и ветеринарной медицины (BgW) в соответствии со статьей 35 Федерального закона Германии о пищевых продуктах. Для выделения ДНК использовали метод ЦТАБ, описанный в ISO 21571:2005, А.З.
Данные совместных сличительных испытаний приводятся в таблице А.7.
|
Таблица А.7 - Результаты совместных сличительных испытаний | ||||||||
|
|
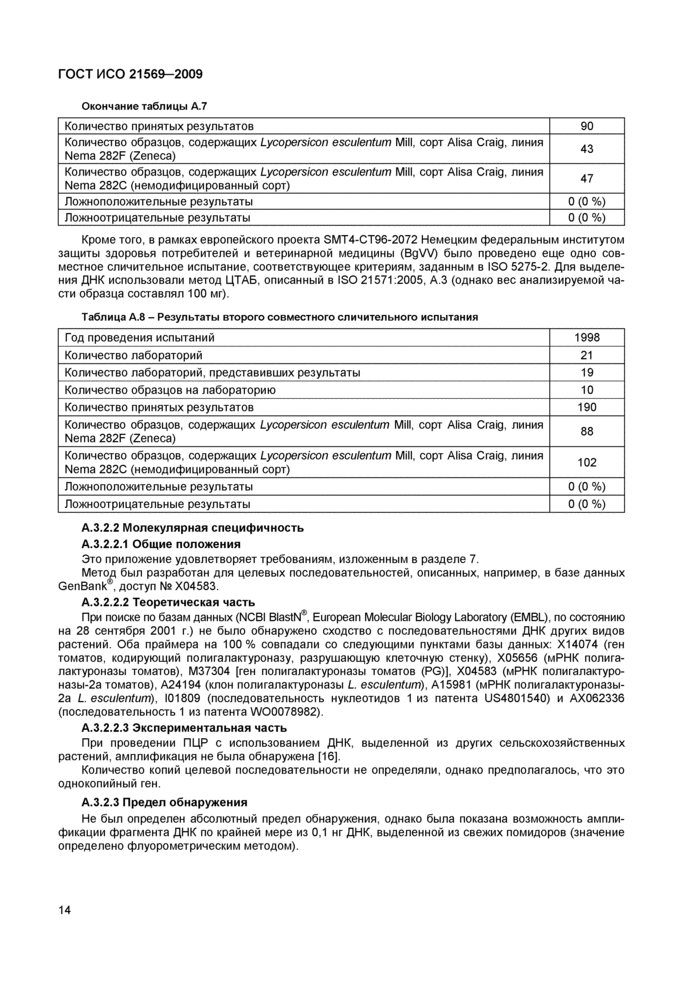
Окончание таблицы А.7 | ||||||||||
|
Кроме того, в рамках европейского проекта SMT4-CT96-2072 Немецким федеральным институтом защиты здоровья потребителей и ветеринарной медицины (BgW) было проведено еще одно совместное сличительное испытание, соответствующее критериям, заданным в ISO 5275-2. Для выделения ДНК использовали метод ЦТАБ, описанный в ISO 21571:2005, А.З (однако вес анализируемой части образца составлял 100 мг).
|
Таблица А.8 - Результаты второго совместного сличительного испытания | ||||||||||||||||||
|
А.3.2.2 Молекулярная специфичность
А.3.2.2.1 Общие положения
Это приложение удовлетворяет требованиям, изложенным в разделе 7.
Метод был разработан для целевых последовательностей, описанных, например, в базе данных GenBank , доступ № Х04583.
А.3.2.2.2 Теоретическая часть
При поиске по базам данных (NCBI BlastN®, European Molecular Biology Laboratory (EMBL), по состоянию на 28 сентября 2001 г.) не было обнаружено сходство с последовательностями ДНК других видов растений. Оба праймера на 100% совпадали со следующими пунктами базы данных: Х14074 (ген томатов, кодирующий полигалакгуроназу, разрушающую клеточную стенку), Х05656 (мРНК полига-лактуроназы томатов), М37304 [ген полигалакгуроназы томатов (PG)], Х04583 (мРНК полигалакгуро-назы-2а томатов), А24194 (клон полигалакгуроназы L esculentum), А15981 (мРНК полигалактуроназы-2а L esculentum), 101809 (последовательность нуклеотидов 1 из патента US4801540) и АХ062336 (последовательность 1 из патента W00078982).
А.3.2.2.3 Экспериментальная часть
При проведении ПЦР с использованием ДНК, выделенной из других сельскохозяйственных растений, амплификация не была обнаружена [16].
Количество копий целевой последовательности не определяли, однако предполагалось, что это однокопийный ген.
А.3.2.3 Предел обнаружения
Не был определен абсолютный предел обнаружения, однако была показана возможность амплификации фрагмента ДНК по крайней мере из 0,1 нг ДНК, выделенной из свежих помидоров (значение определено флуорометрическим методом).
14
ГОСТ ИСО 21569-2009
Информация о введении в действие (прекращении действия) настоящего стандарта и изменений к нему на территории указанных выше государств публикуется в указателях национальных (государственных) стандартов, издаваемых в этих государствах.
© Госстандарт, 2010
Настоящий стандарт не может быть воспроизведен, тиражирован и распространен в качестве официального издания без разрешения Госстандарта Республики Беларусь
ГОСТ ИСО 21569-2009
А.3.3 Адаптация
Анализ образцов, прошедших глубокую переработку, может дать отрицательный результат в связи с возможным отсутствием целевых фрагментов ДНК длиной не менее 383 п. н.
Обнаружение фрагментов длиной 383 п. н. показывает, что раствор ДНК образца содержит ампли-фицируемую ДНК томатов, в то время как обнаружение фрагментов длиной 180 п. н. свидетельствует о том, что раствор ДНК образца содержит амплифицируемую ДНК генетически модифицированных томатов (Zeneca; Lycopersicon esculentum Mill, сорт Alisa Craig, линия Nema 282F).
A.3.4 Принцип
Ген полигалакгуроназы (ген PG) кодирует фермент полигалакгуроназу, связанный с созреванием. Этот метод основан на амплификации эндогенного гена (гена дикого типа) PG [17] с размером фрагмента 383 п. н. В генетически модифицированных томатах Zeneca с этой же парой праймеров будет амплифицироваться второй фрагмент длиной 180 п. н., так как эти томаты трансформировались к ДНК гена PG [18], [19].
А.3.5 Реактивы
Информация по качеству используемых реактивов приводится в ISO 24276.
А.3.5.1 Вода
А.3.5.2 Буфер для ПЦР (без МдС12), 10 х.
А.3.5.3 Раствор МдС12, концентрация МдС12 = 25 ммоль/л.
А.3.5.4 Раствор dNTP, концентрация dNTP = 2,5 ммоль/л (каждого).
А.3.5.5 Олигонуклеотиды
А.3.5.5.1 Прямой праймер
Ген PG (позиция базы данных GenBank® № Х04583).
Праймер PG34L: 5’-ggA ТСС ТТА gAA дСА ТСТ АдТ-3’.
А.3.5.5.2 Обратный праймер
Ген PG (позиция базы данных GenBank® № Х04583).
Праймер PG34R: 5’-СдТ Тдд ТдС АТС ССТ дСА Тдд -3’.
А.3.5.6 Термостабильная ДНК-полимераза (для ПЦР с «горячим стартом»), 5 IU/мкл.
А.3.6 Оборудование
В соответствии с А.1.6.
А.3.7 Процедура анализа
А.3.7.1 Проведение ПЦР
Описанный метод рассчитан на общий объем смеси ПЦР 25 мкл на реакцию; используемые реактивы перечислены в таблице А.9. ПЦР можно проводить и в больших объемах при условии соблюдения соответствующих пропорций для растворов реактивов. Доказано получение корректных результатов при использовании конечных концентраций реактивов, перечисленных в таблице А.9.
|
Таблица А.9 - Добавление реактивов | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
Содержание
Введение.................................................................................................................................................V
1 Область применения............................................................................................................................1
2 Нормативные ссылки...........................................................................................................................1
3 Термины и определения......................................................................................................................1
4 Принцип метода...................................................................................................................................2
5 Реактивы...............................................................................................................................................2
6 Инструменты и оборудование.............................................................................................................3
7 Процедура анализа..............................................................................................................................3
8 Интерпретация результатов................................................................................................................5
9 Предоставление результатов и контроль качества..........................................................................6
10 Протокол испытаний.............................................................................................................................6
Приложение А (справочное) Методы, специфичные к целевым таксонам..........................................7
Приложение В (справочное) Методы скрининга...................................................................................20
Приложение С (справочное) Методы, специфичные к генетической конструкции...........................33
Приложение D (справочное) Методы, специфичные к трансформационным событиям.................51
Библиография..........................................................................................................................................55
Приложение Д.А (справочное) Сведения о соответствии межгосударственного стандарта
ссылочному международному стандарту................................................................60
IV
ГОСТ ИСО 21569-2009Введение
Обнаружение генетически модифицированных источников в ингредиентах пищевых продуктов выполняется посредством описанных далее действий, выполняемых последовательно или одновременно. После отбора пробы из анализируемой порции проводят выделение нуклеиновых кислот. Выделенные нуклеиновые кислоты могут быть дополнительно очищены, одновременно с процессом выделения или после него. Дальнейшими действиями являются определение их концентрации (при необходимости), разведение (при необходимости) и использование в аналитических процедурах (например, в анализе ПЦР). Проведение этих действий подробно описано в настоящем стандарте, а также в группе международных стандартов, объединенных общим заголовком: «Пищевые продукты. Методы анализа для определения генетически модифицированных организмов и содержащих их продуктов»:
- «Отбор проб» (ISO 21568);
- «Методы количественного определения на основе анализа нуклеиновых кислот» (ISO 21570);
- «Выделение нуклеиновых кислот» (ISO 21571).
Дополнительная информация об общих требованиях и определениях, включая описанные выше шаги, приводится в международном стандарте ISO 24276.
Качественное определение целевых последовательностей ДНК выполняется с целью получения ответа «да» или «нет» на вопрос о содержании или отсутствии целевой последовательности ДНК с учетом соответствующих контрольных проб в пределах обнаружения используемого метода анализа и для анализируемой части образца.
Специфичность методов, в соответствии с описаниями в приложениях А - D, варьируется от скрининга (определение типичных последовательностей ДНК, характерных для ГМО) до специфической идентификации генетической конструкции или специфического события генетической трансформации.
V
ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ БЕЛАРУСЬПРОДУКТЫ ПИЩЕВЫЕ Методы анализа для обнаружения генетически модифицированных организмов и производных продуктов.Методы качественного обнаружения на основе анализа нуклеиновых кислотПРАДУКТЫ ХАРЧОВЫЯ Метады анал1зу для выяулення генетычна мадыфшаваных аргашзмау i вытворных прадуктау.Метады якаснага выяулення на аснове анал1зу нукпешавых к1слот
Методы качественного обнаружения на основе анализа нуклеиновых кислотПРАДУКТЫ ХАРЧОВЫЯ Метады анал1зу для выяулення генетычна мадыфшаваных аргашзмау i вытворных прадуктау.Метады якаснага выяулення на аснове анал1зу нукпешавых к1слот
Метады якаснага выяулення на аснове анал1зу нукпешавых к1слот
Foodstuffs
Methods of analysis for the detection of genetically modified organisms
and derived products.
Qualitative nucleic acid based methods
Дата введения 2011-01-011 Область применения
Настоящий стандарт содержит описание процедур качественного определения генетически модифицированных организмов (ГМО) и содержащих их продуктов путем анализа нуклеиновых кислот, выделяемых из исследуемого образца. Основное внимание уделено методам анализа на основе амплификации нуклеиновых кислот с помощью полимеразной цепной реакции (ПЦР).
В настоящем стандарте приводятся общие требования к специфическому определению и идентификации целевых последовательностей нуклеиновой кислоты (ДНК) и к подтверждению идентичности амплифицированной последовательности ДНК.
Руководства, минимальные требования и критерии выполнения, установленные в настоящем стандарте, предназначены для обеспечения получения сопоставимых, точных и воспроизводимых результатов в различных лабораториях.
Настоящий стандарт был разработан для матриц пищевых продуктов, однако может быть также применен для анализа других матриц (например, корма для животных, образцы растений из окружающей среды).
Примеры конкретных методов приводятся в приложениях А - D.
2 Нормативные ссылки
Для применения настоящего стандарта необходимы следующие ссылочные документы. Для датированных ссылок применяют только указанное издание ссылочного документа, для недатированных ссылок применяют последнее издание ссылочного документа.
ISO 21571:2005 Продукты пищевые. Методы анализа для обнаружения генетически модифицированных организмов и их производных. Извлечение нуклеиновой кислоты
ISO 24276:2006 Продукты пищевые. Методы анализа для обнаружения генетически модифицированных организмов и полученных из них продуктов. Общие требования и определения
3 Термины и определения
В настоящем стандарте применяют термины и определения, установленные в ISO 24276.
Издание официальное
4 Принцип метода4.1 Общие положения
Качественный анализ представляет собой специфическое определение целевых последовательностей нуклеиновой кислоты в анализируемых образцах. Каждый метод должен быть специфичен для целевой последовательности.
Результат качественного анализа должен четко показывать наличие или отсутствие исследуемого генетического элемента с учетом соответствующих контролей в пределах обнаружения используемого метода анализа и для анализируемой части образца.
4.2 ПЦР-амплификация
Амплификация целевой последовательности ДНК производится in vitro посредством реакции, катализируемой ДНК-полимеразой, в присутствии олигонуклеотидов-праймеров и дезоксирибонукле-отидтрифосфатов в заданном реакционном буфере [1], [2]. Необходимым условием для проведения амплификации целевой последовательности является отсутствие ингибиторов полимеразы в реакционной смеси. Амплификация ДНК-это циклический процесс, состоящий из следующих этапов:
- денатурация двухнитевой ДНК в однонитевую нуклеиновую кислоту посредством нагрева;
- отжиг (специфическая гибридизация) праймеров к целевой последовательности при соответствующей температуре и
- элонгация праймеров, связанных с обеими одинарными спиралями, ДНК-полимеразой, применимой в ПЦР, при соответствующей температуре.
4.3 Обнаружение и подтверждение продуктов ПЦР
Обнаружение продуктов ПЦР производится с помощью электрофореза в агарозном геле или при необходимости альтернативными доступными методами после изоляции посредством соответствующей процедуры разделения.
Идентификация любой обнаруженной целевой последовательности может быть подтверждена соответствующей методикой (например, с помощью рестрикционного анализа ферментами рестрикции, гибридизации или анализа последовательности ДНК).
В случае использования анализа ПЦР в реальном времени амплификация и детектирование происходят одновременно.
5 Реактивы
Если это не оговаривается особо, растворы реактивов, используемых для анализа, обычно хранят приблизительно при минус 20 °С.
Целесообразно разделить используемые для аналитического метода растворы реактивов на малые порции, это позволит избежать многократного повторения циклов размораживания/замораживания, а также снизить риск перекрестной контаминации.
5.1 Целевая ДНК/Контроль5.2 Вода
5.3 Раствор дезоксирибонуклеотидтрифосфатов (dNTP), содержащий dATP, dCTP, dGTP и dTTP или dUTP.
Примечание- Использование dUTP может отрицательно повлиять на дальнейшее проведение анализа продуктов амплификации ПЦР с помощью рестрикционного анализа.
5.4 Буферный раствор для ПЦР
Буферный раствор для ПЦР обычно поставляется с ДНК-полимеразой. Этот раствор может содержать или не содержать МдС12 в концентрации, указанной производителем. Конечная концентрация МдС12 индивидуальна для каждого метода и, следовательно, приводится в каждом приложении. На рынке также могут быть представлены готовые к использованию реактивы. Для таких реактивов следует соблюдать инструкцию, предоставляемую производителем.
5.5 Термостабильная ДНК-полимеразаГОСТ ИСО 21569-2009
5.6 Прямой праймер5.7 Обратный праймер6 Инструменты и оборудование
6 Инструменты и оборудование
Подробная информация по инструментам и оборудованию приводится в ISO 24276 и приложениях А - D.
7 Процедура анализа7.1 Качество, целостность и амплифицируемость выделенной нуклеиновой кислоты
Раствор нуклеиновой кислоты должен быть достаточно чистым для последующего анализа [3]. Качество и количество выделенной с помощью заданного метода из определенного материала образца нуклеиновой кислоты должны быть повторяемы и воспроизводимы.
Примечание - Качество, целостность и количество образца ДНК влияет на выход ПЦР и, следовательно, на получаемые результаты анализа. Предел обнаружения конкретного метода может, таким образом, зависеть от того, был ли анализируемый материал обработан или очищен, а также от степени деградации (разрушения) ДНК в нем.
Нуклеиновые кислоты, используемые в ПЦР, не должны содержать ингибиторы ПЦР [4]. Необходимо использовать контроли ингибирования ПЦР, описанные в ISO 24276.
7.2 Критерии выполнения анализа
Общие критерии выполнения анализа описаны в ISO 24276.
Значения характеристик выполнения анализа приводятся для каждого метода и указаны в приложениях А - D; при этом следует учитывать размер генома, см. [5].
Для каждой пары праймеров и/или системы следует оптимизировать условия реакции, особенно концентрацию МдС12 и программу работы амплификатора. При использовании какой-либо системы праймеров в первый раз необходимо предварительно доказать, что условия цикла, выбранные для конкретного изучаемого материала образца, позволяют избежать образования нежелательных конкурирующих продуктов реакции, которые в противном случае снизят чувствительность обнаружения в ПЦР.
В оптимальной реакции требуется менее 40 циклов для амплификации 10 и более целевых молекул и получения продукта, который может быть легко обнаружен стандартными методами. По мере увеличения числа циклов возможно накопление неспецифических продуктов реакции. Оптимизированная ПЦР должна позволять получить за 40 циклов из чистого образца стандартного состава, в котором содержатся 100 копий матрицы ДНК, достаточное для обнаружения количество копий продукта ПЦР. Следует строго придерживаться заданных количества циклов, профиля кривой «температура - время» для каждой системы праймеров и реакционной смеси, учитывая используемое оборудование.
В целом следует максимально возможно увеличивать специфичность реакции (например, используя ПЦР с «горячим стартом»). ПЦР с «горячим стартом» рекомендуется как средство снижения побочных реакций (например, амплификация нецелевых последовательностей фоновой ДНК (ошибочная посадка праймеров) или олигомеризация праймеров) и, таким образом, увеличения специфичности метода.
Значения, полученные в ходе метрологической аттестации, могут быть не применимы к диапазонам концентраций анализируемого вещества и материалам образцов, отличающихся от перечисленных в соответствующих приложениях.
7.3 Аспекты подбора параметров ПЦР7.3.1 Общие положения
Так как выполнение каждой индивидуальной ПЦР должно быть сопоставимо с другими специфическими ПЦР, следует учитывать приведенные далее аспекты подбора параметров ПЦР.
7.3.2 Размер ПЦР-продуктов
Размер целевой последовательности следует выбирать таким образом, чтобы он попадал в диапазон молекулярных масс, имеющихся в выделенной из анализируемого образца ДНК.
Пример - Для сильно деградировавшей ДНК из продуктов, прошедших термическую обработку, оптимальный размер ПЦР-продукта должен быть в диапазоне от 60 до 150 пар нуклеотидов (п. н.). Для сырья можно использовать более широкий диапазон, например вполне допустимо значение 250 п. н. 5
Однако, если в результате предварительно проведенных экспериментальных исследований по оценке соответствия наборов праймеров получены ПЦР-продукты различного размера, эти праймеры могут быть использованы для анализа образцов, материал которых был аттестован в таких исследованиях.
7.3.3 Праймеры7.3.3.1 Общие положения
Информация о последовательности праймеров приводится в приложениях А - D.
7.3.3.2 Подбор праймеров
Последовательности праймеров должны по возможности иметь следующие характеристики:
- длина каждого праймера - от 18 до 30 нуклеотидов;
- оптимальная температура отжига - » 60 °С (должна быть установлена экспериментальным путем), т. е. расчетная температура плавления должна быть < 65 °С;
- по возможности соотношение GC : АТ = 50 : 50 или как можно ближе к этому соотношению;
- высокая внутренняя стабильность (не допускается концентрация нуклеотидов G и С в коротких сегментах праймеров);
- минимальная З’-концевая комплементарность для предотвращения образования димеров праймеров;
- минимальная вторичная структура;
- минимальное образование димеров со специфическими зондами для детектирования, разработанными для ПЦР.
Для облегчения подбора праймеров разработаны специализированные программы.
7.3.3.3 Метрологическая аттестация праймеров7.3.3.3.1 Общие положения
Следует подтвердить способность праймеров обнаруживать целевую последовательность.
Аттестацию праймеров следует проводить в два этапа: первый этап заключается в теоретической оценке, а второй - в экспериментальных испытаниях.
7.3.3.3.2 Теоретическая оценка специфичности
Теоретическая оценка специфичности праймеров должна как минимум включать в себя проверку схожести последовательностей (например, с помощью программ FastA, Blast®6) с одной из крупных баз данных последовательностей нуклеиновых кислот (например, EMBL, GenBank® 6). Последовательности гомологичных генов могут быть получены из баз данных последовательностей и проверены на гомологичность для получения оценки шанса обнаружения схожих с целевым таксоном последовательностей или последовательностей других организмов.
7.3.3.3.3 Экспериментальная оценка специфичности
Вне зависимости от использованных критериев подбора праймеров их специфичность обязательно должна быть установлена экспериментальным путем. Такая оценка должна подтвердить способность праймеров различать целевую и нецелевую, но схожую последовательности.
Следует подтвердить, что праймеры, подобранные для обнаружения целевых последовательностей, специфичных к таксону, способны достоверно обнаруживать эти последовательности в достоверном количестве различных членов таксона.
7.4 Описание целей ПЦР
Для качественного обнаружения и идентификации ГМО можно провести различные ПЦР-исследования, зависящие от типа материалов исследуемых образцов и/или от требований к анализу. Эти исследования могут быть направлены на последовательности, специфичные для целевых таксонов, генетических конструкций и трансформационных событий, а также для элементов, пригодных для задач скрининга.
1
10 х означает десятикратный, т. е. буфер для ПЦР, содержащий 1,5 моль/л Трис-НС1, pH 8,3.
2
Blocking Reagent - это пример коммерчески доступного продукта, производимого компанией Boehringer, Mannheim. Эта информация приводится исключительно для ознакомления пользователей настоящего стандарта и ни при каких условиях не может служить рекомендацией или одобрением этих продуктов организацией ISO. Допускается использование аналогичных продуктов, если показано, что они позволяют получать такие же результаты.
3
Амплификаторы GeneAmp® 2400 и 9600 и полимераза AmpliTaq Gold® - это пример коммерчески доступных продуктов, производимых компанией Applied Biosystems, ранее известной как Perkin Elmer/Applied Biosystems. Эта информация приводится исключительно для ознакомления пользователей настоящего стандарта и ни при каких условиях не может служить рекомендацией или одобрением этих продуктов организацией ISO. Допускается использование аналогичных продуктов, если показано, что они позволяют получать такие же результаты.
9
4
Амплификаторы GeneAmp® 2400 и 9600 и полимераза AmpliTaq Gold® - это пример коммерчески доступных продуктов, производимых компанией Applied Biosystems, ранее известной как Perkin Elmer/Applied Biosystems. Эта информация приводится исключительно для ознакомления пользователей настоящего стандарта и ни при каких условиях не может служить рекомендацией или одобрением этих продуктов организацией ISO. Допускается использование аналогичных продуктов, если показано, что они позволяют получать такие же результаты.
5
6
Blast и GenBank - это примеры представленных на рынке программных продуктов, которые могут быть использованы для оценки специфичности. Эта информация приводится исключительно для ознакомления пользователей настоящего стандарта и ни при каких условиях не может служить рекомендацией или одобрением этих продуктов организацией ISO. Допускается использование аналогичных программ, если они позволяют получать такие же результаты.